Global Car T Therapy Treatment Market
Marktgröße in Milliarden USD
CAGR :
% 
 USD
2.44 Billion
USD
6.66 Billion
2024
2032
USD
2.44 Billion
USD
6.66 Billion
2024
2032
| 2025 –2032 | |
| USD 2.44 Billion | |
| USD 6.66 Billion | |
|
|
|
|
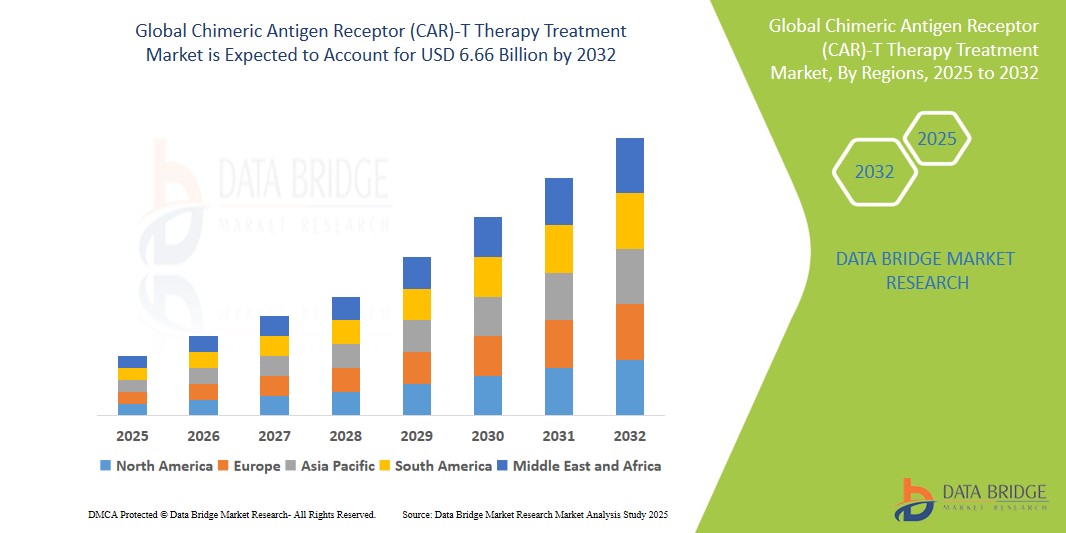
Globale Marktsegmentierung für CAR-T-Zelltherapien nach Zelltypen (Abecma, Breyanzi, Kymriah, Tecartus, Yescarta und andere), Zielantigenen (CD19, CD20, GD2, CD22, CD30, CD33, HER1, HER2, Meso, EGFRVIII und andere) und therapeutischen Anwendungen (akute lymphatische Leukämie, chronische lymphatische Leukämie, Non-Hodgkin-Leukämie, multiples Myelom, Pankreaskrebs, Neuroblastome, Brustkrebs, akute myeloische Leukämie, Leberzellkarzinom, Darmkrebs und andere) – Branchentrends und Prognose bis 2032
Marktgröße für die CAR-T-Zelltherapie
- Der globale Markt für CAR-T-Zelltherapien (Chimeric Antigen Receptor) hatte im Jahr 2023 einen Wert von 2,44 Milliarden US-Dollar und wird voraussichtlich bis 2031 auf 5,97 Milliarden US-Dollar anwachsen, was einer durchschnittlichen jährlichen Wachstumsrate (CAGR) von 15,3 % im Prognosezeitraum entspricht.
- Dieses Wachstum wird durch Faktoren wie die zunehmende Verbreitung von Krebs, Fortschritte in der Immuntherapie und die wachsende Zahl von Zulassungen von CAR-T-Zelltherapien durch die Aufsichtsbehörden angetrieben.
Marktanalyse der CAR-T-Zelltherapie
- Die CAR-T-Zelltherapie ist eine revolutionäre Krebsbehandlung, bei der die T-Zellen eines Patienten so verändert werden, dass sie Krebszellen gezielt angreifen und zerstören. Sie hat sich bei der Behandlung bestimmter Formen von Leukämie, Lymphomen und multiplem Myelom als hochwirksam erwiesen.
- Die Nachfrage nach CAR-T-Zelltherapie steigt aufgrund der zunehmenden Häufigkeit hämatologischer Malignome und vielversprechender Ergebnisse in klinischen Studien.
- Nordamerika wird voraussichtlich den Markt für CAR-T-Zelltherapie dominieren, was auf starke Forschungs- und Entwicklungsaktivitäten, hohe Gesundheitsausgaben und die frühe Einführung fortschrittlicher Therapien zurückzuführen ist.
- Der asiatisch-pazifische Raum dürfte im Prognosezeitraum aufgrund expandierender Biotechnologiebranchen und zunehmender Krebsbelastung die am schnellsten wachsende Region auf dem Markt für CAR-T-Zelltherapie sein.
- Das Segment der akuten lymphatischen Leukämie wird aufgrund der hohen Ansprechrate auf die Behandlung und der laufenden klinischen Entwicklung voraussichtlich mit einem Marktanteil von 30 % den Markt dominieren. Als eine der ersten zugelassenen Indikationen für die CAR-T-Zelltherapie treibt sie das Marktwachstum weiterhin voran.
Berichtsumfang und Marktsegmentierung der CAR-T-Zelltherapie
|
Attribute |
Wichtige Markteinblicke in die CAR-T-Zelltherapie |
|
Abgedeckte Segmente |
|
|
Abgedeckte Länder |
Nordamerika
Europa
Asien-Pazifik
Naher Osten und Afrika
Südamerika
|
|
Wichtige Marktteilnehmer |
|
|
Marktchancen |
|
|
Mehrwertdaten-Infosets |
Zusätzlich zu Erkenntnissen über Marktszenarien wie Marktwert, Wachstumsrate, Segmentierung, geografische Abdeckung und Hauptakteure enthalten die von Data Bridge Market Research erstellten Marktberichte auch Import-Export-Analysen, einen Überblick über die Produktionskapazität, eine Analyse des Produktionsverbrauchs, eine Preistrendanalyse, ein Klimawandelszenario, eine Lieferkettenanalyse, eine Wertschöpfungskettenanalyse, einen Überblick über Rohstoffe/Verbrauchsmaterialien, Kriterien für die Lieferantenauswahl, eine PESTLE-Analyse, eine Porter-Analyse und den regulatorischen Rahmen. |
Markttrends für die CAR-T-Zelltherapie
„CAR-T-Therapien der nächsten Generation und sofort verfügbare (allogene) Lösungen“
- Ein wichtiger Trend im Bereich der CAR-T-Zelltherapie ist das Aufkommen von CAR-T-Therapien der nächsten Generation und die Entwicklung von sofort verfügbaren (allogenen) CAR-T-Lösungen, die darauf abzielen, die Einschränkungen traditioneller autologer CAR-T-Produkte zu überwinden.
- Diese Innovationen zielen darauf ab, die Effizienz der Herstellung zu verbessern, die Behandlungskosten zu senken und einen schnelleren Patientenzugang zu gewährleisten, indem die Notwendigkeit entfällt, patienteneigene T-Zellen zu entnehmen und zu modifizieren.
- Beispielsweise nutzen allogene CAR-T-Zelltherapien, wie sie von Allogene Therapeutics und Precision BioSciences entwickelt werden, Genomeditierungstechnologien, um universelle CAR-T-Zellen von gesunden Spendern zu erzeugen und bieten damit das Potenzial für skalierbare und leicht verfügbare Behandlungen.
- Diese Fortschritte bergen das Potenzial, die Krebsimmuntherapie grundlegend zu verändern, die Zeit bis zum Behandlungsbeginn zu verkürzen, die Zugänglichkeit zu verbessern und die Ausweitung der CAR-T-Zelltherapie auf ein breiteres Indikationsspektrum und größere Patientengruppen zu unterstützen.
Marktdynamik der CAR-T-Zelltherapie
Treiber
„Zunehmende Krebsinzidenz und hohe Wirksamkeit der CAR-T-Zelltherapie bei hämatologischen Malignomen“
- Die weltweit zunehmende Belastung durch Krebs – insbesondere durch hämatologische Malignome wie Leukämie, Lymphome und multiples Myelom – ist ein Schlüsselfaktor für die steigende Nachfrage nach CAR-T-Zelltherapie.
- CAR-T-Zelltherapien bieten eine hohe Wirksamkeit; mehrere von der FDA zugelassene Produkte weisen hohe Remissionsraten bei Patienten auf, die auf konventionelle Behandlungen nicht angesprochen haben.
- Laut der Internationalen Agentur für Krebsforschung (IARC) wurden im Jahr 2022 weltweit etwa 20 Millionen neue Krebsfälle diagnostiziert, wobei Blutkrebs einen erheblichen Anteil dieser Fälle ausmachte. Die zunehmende Verbreitung therapieresistenter Krebsarten verstärkt den Bedarf an fortschrittlichen Therapieoptionen wie der CAR-T-Zelltherapie.
- Durch kontinuierliche Fortschritte im CAR-Design, der Auswahl der Zielantigene und der Therapieverabreichung verbessern sich Wirksamkeit und Sicherheit der CAR-T-Zelltherapie stetig und treiben so das Marktwachstum voran.
Gelegenheit
„Erweiterung der Indikationen auf solide Tumore und frühere Behandlungslinien“
- Eine der vielversprechendsten Möglichkeiten besteht darin, die CAR-T-Zelltherapie über hämatologische Malignome hinaus auf solide Tumore auszuweiten, die den Großteil der weltweiten Krebsfälle ausmachen.
- Innovationen bei der Modulation der Tumormikroumgebung, dual-gerichtete CARs und gepanzerte CAR-T-Zellen ermöglichen es CAR-T-Zellen, besser in solide Tumore einzudringen und dort zu persistieren.
- Darüber hinaus untersuchen Aufsichtsbehörden und Forscher den Einsatz der CAR-T-Zelltherapie in früheren Behandlungsstadien, wodurch sich potenziell die Patienteneignung und die Behandlungsergebnisse verbessern könnten.
- Beispielsweise begannen Forscher des National Cancer Institute (NCI) im März 2024 mit Phase-I-Studien für CAR-T-Zelltherapien zur Behandlung von HER2-positivem Brustkrebs und EGFR-positivem Glioblastom, was einen Wandel hin zur Anwendung bei soliden Tumoren markiert.
- Diese Entwicklungen könnten den kommerziellen Anwendungsbereich von CAR-T-Therapien erheblich erweitern und sie als Erst- oder Zweitlinienoption bei einem breiteren Spektrum von Krebsarten positionieren.
Zurückhaltung/Herausforderung
„Hohe Behandlungskosten und komplexe Herstellungsprozesse“
- Eine der größten Herausforderungen für die breite Anwendung der CAR-T-Zelltherapie sind die hohen Kosten und der komplexe, individualisierte Herstellungsprozess, der die Entnahme, das gentechnische Verfahren und die Wiedereinführung der patienteneigenen T-Zellen umfasst.
- Die Behandlungskosten übersteigen oft Hunderttausende von Dollar pro Patient, was erhebliche finanzielle Hürden für Patienten und Kostenträger darstellt und den Zugang in Ländern mit niedrigem und mittlerem Einkommen einschränkt.
- Eine im Oktober 2024 in Health Affairs veröffentlichte Studie schätzte beispielsweise die durchschnittlichen Gesamtkosten einer CAR-T-Zelltherapie (einschließlich Krankenhausaufenthalt und unterstützender Behandlung) in den USA auf über 500.000 US-Dollar pro Patient, was die Bezahlbarkeit zu einem wichtigen Anliegen für die Gesundheitssysteme macht.
- Folglich können solche Einschränkungen zu Ungleichheiten in der Qualität der Versorgung und beim Zugang zu fortschrittlichen chirurgischen Eingriffen führen und letztendlich das Gesamtwachstum des Marktes behindern.
Marktübersicht für die CAR-T-Zelltherapie
Der Markt ist segmentiert nach Typen, Zielantigen und therapeutischer Anwendung.
|
Segmentierung |
Untersegmentierung |
|
Nach Typen |
|
|
Nach Zielantigen |
|
|
Durch therapeutische Anwendung |
|
Im Jahr 2025 wird das Segment der akuten lymphatischen Leukämie (ALL) voraussichtlich den Markt dominieren und den größten Anteil am Segment der therapeutischen Anwendungen aufweisen.
Es wird erwartet, dass das Segment der akuten lymphatischen Leukämie (ALL) im Jahr 2025 den Markt für CAR-T-Zelltherapien anführen und mit rund 30 % den größten Marktanteil ausmachen wird. Diese Dominanz ist auf die frühe Zulassung und den klinischen Erfolg von CAR-T-Therapien wie Kymriah und Tecartus zur Behandlung von rezidivierter oder refraktärer ALL zurückzuführen. Dank ihrer hohen Ansprechraten und ihres lebensrettenden Potenzials etabliert sich die CAR-T-Therapie zunehmend als Standardbehandlung für Patienten, die auf konventionelle Therapien nicht ansprechen. Die steigende Inzidenz von ALL, insbesondere bei Kindern und Jugendlichen, sowie die kontinuierlichen klinischen Fortschritte werden die führende Position dieses Segments voraussichtlich weiter stärken.
Es wird erwartet, dass das Segment der Zielantigene CD19 den Markt mit dem größten Anteil im Segment der Zielantigene dominieren wird.
Das Segment der CD19-Zielantigene wird im Jahr 2025 voraussichtlich mit einem Marktanteil von 48,6 % den größten Anteil am Markt für CAR-T-Zelltherapien halten. CD19 ist aufgrund seiner hohen Expression bei B-Zell-Malignomen wie akuter lymphatischer Leukämie, Non-Hodgkin-Lymphom und chronischer lymphatischer Leukämie das am häufigsten verwendete Zielantigen. Mehrere von der FDA zugelassene CAR-T-Therapien, darunter Kymriah, Yescarta und Breyanzi, sind CD19-spezifisch und weisen eine signifikante klinische Wirksamkeit auf. Da laufende Studien CD19 in Kombinationstherapien und neuen Indikationen untersuchen, wird erwartet, dass dieses Segment seine dominante Position während des gesamten Prognosezeitraums beibehalten wird.
Regionale Analyse des Marktes für CAR-T-Zelltherapie
„Nordamerika hält den größten Anteil am Markt für CAR-T-Zelltherapien.“
- Nordamerika dominiert den Markt für CAR-T-Zelltherapien. Dies wird durch eine starke klinische Forschungsinfrastruktur, die frühzeitige Einführung innovativer Immuntherapien und einen robusten regulatorischen Rahmen, der die Zulassung fortschrittlicher Zelltherapien erleichtert, begünstigt.
- Die Vereinigten Staaten sind in der Region führend mit einer hohen Konzentration an zugelassenen CAR-T-Therapien, darunter Kymriah, Yescarta und Breyanzi, die in spezialisierten Krebsbehandlungszentren weit verbreitet verfügbar sind.
- Günstige Erstattungspolitiken, steigende Krebsinzidenz und staatlich unterstützte Initiativen zur Förderung der Präzisionsonkologie tragen wesentlich zur Marktexpansion bei.
- Darüber hinaus stärken die Präsenz führender Biotechnologieunternehmen, laufende klinische Studien für neue Indikationen und Investitionen in Produktionsanlagen für Zelltherapien die Führungsrolle der Region im globalen Bereich der CAR-T-Therapie.
„Für den asiatisch-pazifischen Raum wird die höchste durchschnittliche jährliche Wachstumsrate (CAGR) im Markt für CAR-T-Zelltherapien prognostiziert.“
- Die Region Asien-Pazifik dürfte im Markt für CAR-T-Zelltherapie das höchste Wachstum verzeichnen, angetrieben durch den Ausbau der Gesundheitsinfrastruktur, die steigende Krebsprävalenz und wachsende Investitionen in biotechnologische Innovationen.
- Länder wie China, Japan, Südkorea und Indien entwickeln sich aufgrund der zunehmenden Anwendung personalisierter Krebstherapien und der staatlichen Förderung klinischer Forschung und der Entwicklung von Zelltherapien zu Schlüsselmärkten.
- Insbesondere China macht im Bereich der CAR-T-Zelltherapie rasante Fortschritte, mit einer großen Anzahl klinischer Studien und einheimischen Biotechnologieunternehmen, die wettbewerbsfähige Therapien auf den Markt bringen, die auf die Antigene CD19, CD22 und BCMA abzielen.
- Die japanische Zulassungsbehörde hat beschleunigte Zulassungsverfahren für regenerative und fortschrittliche Therapien eingeführt, um den Zugang zu CAR-T-Zelltherapien zu beschleunigen.
- In Indien steigt die Nachfrage nach CAR-T-Zelltherapien, unterstützt durch akademische Kooperationen und Initiativen zur Lokalisierung der Produktion und Senkung der Behandlungskosten. Diese regionale Dynamik dürfte im Prognosezeitraum maßgeblich zum globalen Marktwachstum beitragen.
Marktanteil der CAR-T-Zelltherapie
Die Wettbewerbsanalyse bietet detaillierte Informationen zu jedem einzelnen Wettbewerber. Diese umfassen Unternehmensübersicht, Finanzkennzahlen, Umsatz, Marktpotenzial, Investitionen in Forschung und Entwicklung, neue Marktinitiativen, globale Präsenz, Produktionsstandorte und -anlagen, Produktionskapazitäten, Stärken und Schwächen des Unternehmens, Produkteinführungen, Produktportfolio und Anwendungsdominanz. Die genannten Datenpunkte beziehen sich ausschließlich auf den Fokus der Unternehmen auf den jeweiligen Markt.
Die wichtigsten Marktführer, die auf dem Markt tätig sind, sind:
- Autolus Therapeutics (UK)
- CARsgen Therapeutics Holdings Limited (UK)
- Bristol-Myers Squibb Company (USA)
- Sorrento Therapeutics, Inc. (USA)
- bluebird bio, Inc. (USA)
- Eureka Therapeutics Inc. (USA)
- Avacta Group plc (UK)
- Cibus Inc. (Frankreich)
- Celyad Oncology SA (Belgien)
- Fortress Biotech, Inc. (USA)
- Gilead Sciences, Inc. (USA)
- Novartis AG (Schweiz)
- Alaunos Therapeutics, Inc. (USA)
- Poseida Therapeutics, Inc. (USA)
Neueste Entwicklungen auf dem globalen Markt für CAR-T-Zelltherapie
- Im Dezember 2023 führte Max Healthcare die CAR-T-Zelltherapie erfolgreich in der Region Delhi-NCR ein und markierte damit einen bedeutenden Fortschritt in der Krebsbehandlung. Diese innovative Therapie, die in Zusammenarbeit mit ImmunoACT entwickelt wurde, ist speziell auf die Bekämpfung von Lymphomen und Leukämien ausgerichtet und bietet Patienten mit diesen schweren Erkrankungen neue Hoffnung.
- Im Dezember 2022 ging CARsgen Therapeutics Co., Ltd. eine Partnerschaft mit dem Shanghai Cancer Institute ein, um eine neue Technologie zu entwickeln, die die Antitumorwirkung von T-Zellen deutlich verbessert. Ihr Forschungsteam entdeckte, dass CAR-T-Zellen, die so verändert wurden, dass sie Runx3 überexprimieren, eine anhaltende Antitumoraktivität und eine verbesserte Tumorkontrolle im Vergleich zu herkömmlichen CAR-T-Zelltherapien aufwiesen.
- Im November 2022 gab Caribou Biosciences, Inc. bekannt, dass ihre allogene Anti-CD19-CAR-T-Zelltherapie CB-010 von der US-amerikanischen Arzneimittelbehörde FDA den Status einer regenerativen Therapie für fortgeschrittene Erkrankungen (RMAT) für rezidiviertes oder refraktäres großzelliges B-Zell-Lymphom (LBCL) sowie den Fast-Track-Status für rezidiviertes oder refraktäres B-Zell-Non-Hodgkin-Lymphom erhalten hat.
- Im Juni 2022 präsentierte die Universität Ottawa vielversprechende Ergebnisse der klinischen Studie „Canadian-Led Immunotherapies in Cancer-01“ (CLIC-01). Im Fokus dieser Studie stand eine der ersten in Kanada entwickelten CAR-T-Zelltherapien gegen Krebs. Diese Therapie zeichnet sich durch ein einzigartiges Herstellungsverfahren aus, das zu kostengünstigeren und gerechteren Behandlungsoptionen führen könnte.
- Im November 2021 bewilligte der Verwaltungsrat des California Institute for Regenerative Medicine einen Zuschuss in Höhe von 4,1 Millionen US-Dollar zur Förderung der Weiterentwicklung der innovativen CAR-T-Zell-Therapie, die von Wissenschaftlern der University of California San Diego School of Medicine entwickelt wird. Die Förderung unterstützt deren Bemühungen, diese vielversprechende Krebsbehandlung vom Labor in die klinische Praxis zu überführen.
SKU-
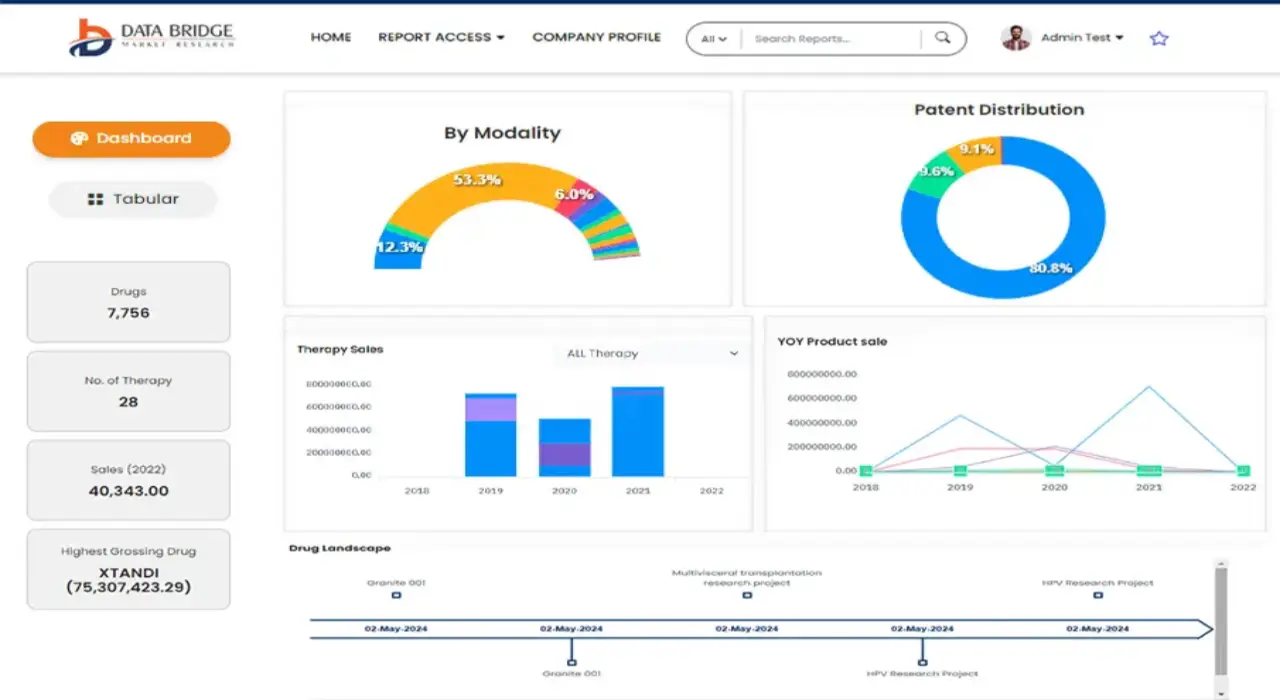
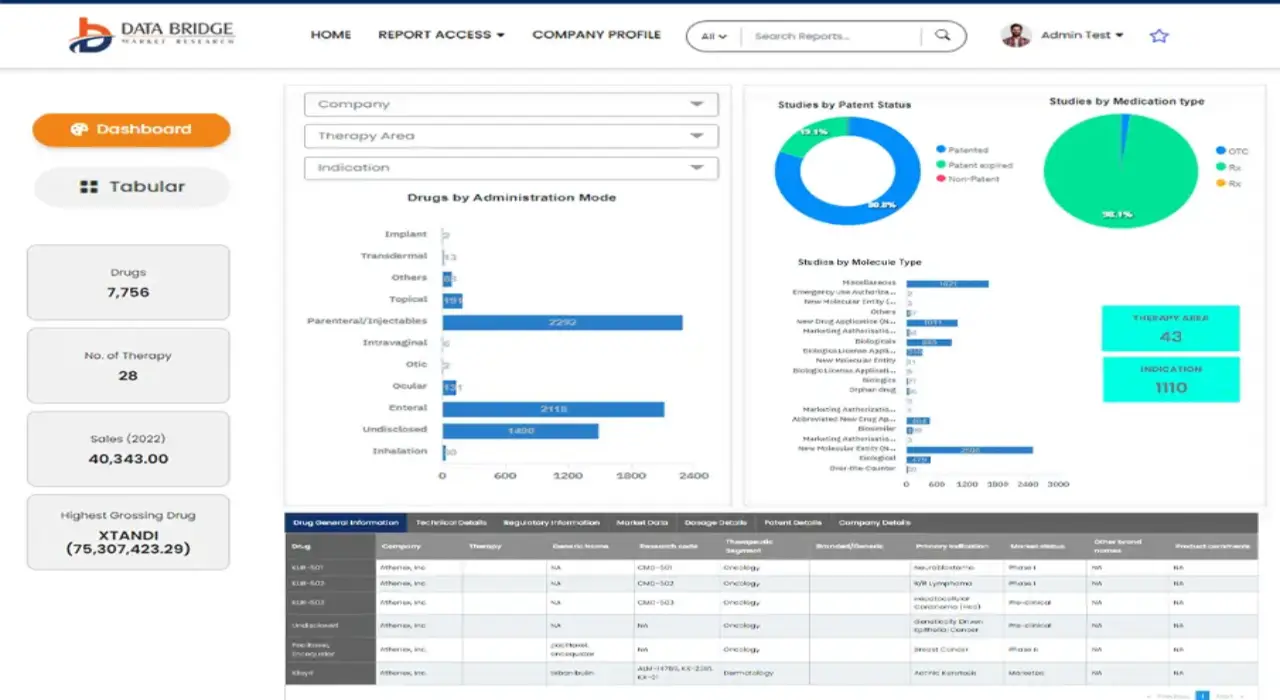
Erhalten Sie Online-Zugriff auf den Bericht zur weltweit ersten Market Intelligence Cloud
- Interaktives Datenanalyse-Dashboard
- Unternehmensanalyse-Dashboard für Chancen mit hohem Wachstumspotenzial
- Zugriff für Research-Analysten für Anpassungen und Abfragen
- Konkurrenzanalyse mit interaktivem Dashboard
- Aktuelle Nachrichten, Updates und Trendanalyse
- Nutzen Sie die Leistungsfähigkeit der Benchmark-Analyse für eine umfassende Konkurrenzverfolgung
Inhaltsverzeichnis
1 EINLEITUNG
1.1 Ziele der Studie
1.2 MARKTDEFINITION
1.3 ÜBERBLICK ÜBER DEN GLOBALEN MARKT FÜR CAR-T-THERAPIE (CHIMERE ANTIGENREZEPTOR)
1.4 WÄHRUNG UND PREISE
1.5 BESCHRÄNKUNG
1.6 ABGEDECKTE MÄRKTE
2 Marktsegmentierung
2.1 WICHTIGSTE ERKENNTNISSE
2.2 Erreichen der globalen Marktgröße für die CAR-T-Therapie
2.2.1 Lieferantenpositionierungsraster
2.2.2 Technologie-Lebenszykluskurve
2.2.3 Datenvalidierungsmodell für Stativ
2.2.4 MARKTÜBERSICHT
2.2.5 Multivariate Modellierung
2.2.6 Analyse von oben nach unten
2.2.7 Herausforderungsmatrix
2.2.8 Anwendungsabdeckungsraster
2.2.9 MESSSTANDARDS
2.2.10 ANALYSE DER ANBIETERANTEILSVERHÄLTNISSE
2.2.11 EPIDEMIOLOGIE
2.2.12 DATENPUNKTE AUS WICHTIGEN PRIMÄRINTERVIEWS
2.2.13 DATENPUNKTE AUS WICHTIGEN SEKUNDÄRDATENBANKEN
2.3 GLOBALER MARKT FÜR CAR-T-THERAPIE: FORSCHUNGSÜBERSICHT
2.4 ANNAHMEN
3 MARKTÜBERSICHT
3.1 FAHRER
3.2 FESSELN
3.3 CHANCEN
3.4 HERAUSFORDERUNGEN
4. ZUSAMMENFASSUNG
5 PREMIUM-EINBLICKE
5.1 PESTEL-ANALYSE
5.2 Porters Fünf-Kräfte-Modell
6 Brancheneinblicke
6.1 Patentanalyse
6.1.1 Patentlandschaft
6.1.2 USPTO-NUMMER
6.1.3 Ablauf des Patents
6.1.4 EPIO-NUMMER
6.1.5 Patentstärke und Qualität
6.1.6 Patentansprüche
6.1.7 Patentzitate
6.1.8 Patentstreitigkeiten und Lizenzierung
6.1.9 Patentakte
6.1.10 Länder, in denen Patente erteilt wurden
6.1.11 TECHNOLOGISCHER HINTERGRUND
6.2 Medikamentenbehandlungsrate in reifen Märkten
6.3 Demografische Trends: Auswirkungen auf alle Inzidenzraten
6.4 Patientenflussdiagramm
6.5 WICHTIGE PREISSTRATEGIEN
6.6 WICHTIGSTE STRATEGIEN ZUR PATIENTENREGISTRIERUNG
6.7 Interviews mit Spezialisten
6.8 Weitere Kollektiv-Momentaufnahmen
7 EPIDEMIOLOGIE
7.1 Häufigkeit aller Fälle nach Geschlecht
7.1.1 PRÄVALENZ DER AKUTE LYMPHOBLASTISCHEN B-ZELL-LEUKÄMIE (ALL)
7.1.2 PRÄVALENZ DES B-ZELL-NON-HODGKIN-LYMPHOMS (NHL)
7.1.3 PRÄVALENZ DES FOLLICULÄREN LYMPHOMS
7.1.4 PRÄVALENZ DES MANTELZELLLYMPHOMS (MCL)
7.1.5 PRÄVALENZ DES MULTIPLEN MYELOMS
7.2 BEHANDLUNGSRATE
7.3 STERBLICHTRETTUNGSRATE
7.4 Behandlungserfolgsraten der Patienten
8 Fusionen und Übernahmen
8.1 LIZENZIERUNG
8.2 Vermarktungsvereinbarungen
9. RECHTLICHER RAHMEN
9.1 Genehmigungsverfahren
9.2 GEOGRAFIEN: EINFACHE BEHÖRDERUNGSPRÜFUNG
9.3 ZULASSUNGSVERFAHREN DER REGULATORISCHEN RICHTLINIEN
9.4 LIZENZIERUNG UND REGISTRIERUNG
9.5 Überwachung nach der Markteinführung
9.6 Richtlinien für gute Herstellungspraxis (GMP)
10 PIPELINE-ANALYSE
10.1 Klinische Studien und Phasenanalyse
10.2 Medikamententherapie-Pipeline
10.3 PHASE III KANDIDATEN
10.4 PHASE-II-KANDIDATEN
10.5 PHASE I KANDIDATEN
10.6 ANDERE (PRÄKLINISCHE UND FORSCHUNGS-)
TABELLE 1 WELTWEITER MARKT FÜR KLINISCHE STUDIEN FÜR XX
Firmenname Therapiegebiet
XX XX
XX XX
XX XX
XX XX
XX XX
XX XX
Quellen: Pressemitteilungen, Geschäftsberichte, SEC-Einreichungen, Investorenpräsentationen, sonstige Regierungsquellen, Analysen auf Basis von Sekundärdaten, Experteninterviews
TABELLE 2 VERTEILUNG DER PRODUKTE UND PROJEKTE NACH PHASE
Phase Anzahl der Projekte
Präklinische/Forschungsprojekte XX
Klinische Entwicklung XX
Phase I XX
Phase II XX
Phase III XX
In den USA eingereicht/genehmigt, aber noch nicht auf dem Markt XX
Insgesamt XX
Quellen: Pressemitteilungen, Geschäftsberichte, SEC-Einreichungen, Investorenpräsentationen, sonstige Regierungsquellen, Analysen auf Basis von Sekundärdaten, Experteninterviews
TABELLE 3 VERTEILUNG DER PROJEKTE NACH THERAPEUTISCHEM BEREICH UND PHASE
Therapeutisches Gebiet Präklinisches/Forschungsprojekt
XX XX
XX XX
XX XX
XX XX
XX XX
Gesamtzahl der Projekte XX
Quellen: Pressemitteilungen, Geschäftsberichte, SEC-Einreichungen, Investorenpräsentationen, sonstige Regierungsquellen, Analysen auf Basis von Sekundärdaten, Experteninterviews
TABELLE 4 VERTEILUNG DER PROJEKTE NACH WISSENSCHAFTLICHEM ANSATZ UND PHASE
Technologie-Präklinisches/Forschungsprojekt
XX XX
XX XX
XX XX
XX XX
XX XX
Gesamtzahl der Projekte XX
Quellen: Pressemitteilungen, Geschäftsberichte, SEC-Einreichungen, Investorenpräsentationen, sonstige Regierungsquellen, Analysen auf Basis von Sekundärdaten, Experteninterviews
ABBILDUNG 1: TOP-UNTERNEHMEN BASIEREND AUF EINEM BLICK AUF F&E FÜR XX
Quellen: Pressemitteilungen, Geschäftsberichte, SEC-Einreichungen, Investorenpräsentationen, sonstige Regierungsquellen, Analysen auf Basis von Sekundärdaten, Experteninterviews
11. Analyse vermarkteter Arzneimittel
11.1 Droge
11.1.1 MARKENNAME
11.1.2 GENERIKANAME
11.2 Therapeutische Indikation
11.3 PHARMAKOLOGISCHE KLASSE DES ARZNEIMITTELS
11.4 Primäre Indikation des Arzneimittels
11.5 Marktstatus
11.6 MEDIKAMENTENART
11.7 ARZNEIMITTELDOSIERUNGSFORM
11.8 VERFÜGBARE DOSIERUNGEN
11.9 Verabreichungsweg von Arzneimitteln
11.1 Dosierungshäufigkeit
11.11 Einblick in die Drogenwelt
11.12 ÜBERBLICK ÜBER DIE ARZNEIMITTELENTWICKLUNGSAKTIVITÄTEN WIE REGULATORISCHE MILSTONE-KRITERIEN, SICHERHEITSDATEN UND WIRKSAMKEITSDATEN, DATEN ZUR MARKTEXKLUSIVITÄT.
11.12.1 Marktprognose
11.12.2 Cross-Wettbewerb
11.12.3 Therapeutisches Portfolio
11.12.4 Aktuelles Entwicklungsszenario
12. Marktzugang
12.1 10-JAHRES-MARKTPROGNOSE
12.2 Aktuelle Aktualisierungen zu klinischen Studien
12.3 Jährlich neu von der FDA zugelassene Arzneimittel
12.4 Arzneimittelhersteller und -geschäfte
12,5 GROSSE DROGENKONSUMGEBUNG
12.6 Aktuelle Behandlungsmethoden
12.7 Auswirkungen der bevorstehenden Therapie
13 F&E-ANALYSE
13.1 VERGLEICHENDE ANALYSE
13.2 Arzneimittelentwicklungslandschaft
13.3 Detaillierte Einblicke in regulatorische Meilensteine
13.4 Therapeutische Beurteilung
13.5 VERMÖGENSBASIERTE KOOPERATIONEN UND PARTNERSCHAFTEN
14 MARKTÜBERSICHT
14.1 FAHRER
14.2 FESSELN
14.3 CHANCEN
14.4 HERAUSFORDERUNGEN
15 GLOBALER MARKT FÜR CAR-T-THERAPIE, NACH ZIELINDIKATION
15.1 ÜBERSICHT
15.2 Akute lymphoblastische Leukämie der B-Zellen (ALL)
15.3 B-Zell-Non-Hodgkin-Lymphom (NHL)
15.4 Follikuläres Lymphom
15.5 Mantelzelllymphom (MCL)
15.6 Multiples Myelom
15.7 ANDERE
16 GLOBAL
16.1 ÜBERSICHT
16.2 AUTOLOGE CAR-T-ZELLEN
16.3 ALLOGENE CAR-T-ZELLEN
17. Weltweiter Markt für CAR-T-Therapien (chimäre Antigenrezeptoren), nach Zielantigen
17.1 ÜBERSICHT
17.2 CD19
17.2.1 TISAGENLECLEUCEL
17.2.1.1. MARKTWERT (Mio. USD)
17.2.1.2. Marktvolumen (Stück)
17.2.1.3. DURCHSCHNITTLICHER VERKAUFSPREIS (USD)
17.2.2 AXIXABTAGENE CILOLEUCEL
17.2.2.1. MARKTWERT (Mio. USD)
17.2.2.2. Marktvolumen (Stück)
17.2.2.3. DURCHSCHNITTLICHER VERKAUFSPREIS (USD)
17.2.3 BREXUCABTAGENE AUTOLLEUCEL
17.2.3.1. MARKTWERT (Mio. USD)
17.2.3.2. Marktvolumen (Stück)
17.2.3.3. DURCHSCHNITTLICHER VERKAUFSPREIS (USD)
17.2.4 LISOCABTAGENE MARALEUCEL
17.2.4.1. MARKTWERT (Mio. USD)
17.2.4.2. Marktvolumen (Stück)
17.2.4.3. DURCHSCHNITTLICHER VERKAUFSPREIS (USD)
17.2.5 ANDERE
17.3 BCMA
17.3.1 IDECABTAGEN VICLEUCEL
17.3.1.1. MARKTWERT (Mio. USD)
17.3.1.2. Marktvolumen (Stück)
17.3.1.3. DURCHSCHNITTLICHER VERKAUFSPREIS (USD)
17.3.2 CILTACABTAGEN AUTOLEUCEL
17.3.2.1. MARKTWERT (Mio. USD)
17.3.2.2. Marktvolumen (Stück)
17.3.2.3. DURCHSCHNITTLICHER VERKAUFSPREIS (USD)
17.3.3 ANDERE
17.4 ANDERE
18 GLOBALER MARKT FÜR CAR-T-THERAPIE, NACH ALTERSGRUPPE
18.1 ÜBERSICHT
18.2 KINDER (0-15)
18.3 ERWACHSENE (16-64)
18.4 SENIOREN (65 JAHRE UND ÄLTER)
19 GLOBALER MARKT FÜR CAR-T-THERAPIE, NACH GESCHLECHT
19.1 ÜBERSICHT
19.2 MÄNNLICH
19.3 WEIBLICH
20 GLOBALER MARKT FÜR CAR-T-THERAPIE (CHIMERE ANTIGENREZEPTOR)-THERAPIE, NACH ENDVERBRAUCHER
20.1 ÜBERSICHT
20.2 KRANKENHAUS
20.2.1 PRIVAT
20.2.2 ÖFFENTLICH
20.3 SPEZIALKLINIKEN
20.4 Forschungsinstitute
20.5 Krebsinstitute
20.6 PHARMAZEUTISCHE UND BIOTECHNOLOGIEUNTERNEHMEN
20.7 ANDERE
21 GLOBALER MARKT FÜR CAR-T-THERAPIE (CHIMERE ANTIGENREZEPTOR)-THERAPIE, NACH VERTRIEBSKANAL
21.1 ÜBERSICHT
21.2 DIREKTVERKAUF
21.3 Einzelhandelsumsätze
21.4 ANDERE
22 GLOBALER MARKT FÜR CAR-T-THERAPIE, UNTERNEHMENSLANDSCHAFT
22.1 UNTERNEHMENSAKTIENANALYSE: WELTWEIT
22.2 AKTIENANALYSE: NORDAMERIKA
22.3 AKTIENANALYSE: EUROPA
22.4 AKTIENANALYSE: ASIEN-PAZIFIK
22.5 Fusionen und Übernahmen
22.6 PRODUKTENTWICKLUNG & ZULASSUNGEN
22.7 ERWEITERUNGEN
22.8 RECHTLICHE ÄNDERUNGEN
22.9 Partnerschaften und andere strategische Entwicklungen
23 GLOBALER MARKT FÜR CAR-T-THERAPIE, NACH GEOGRAFIE
GLOBALER MARKT FÜR CAR-T-THERAPIE (ALLE OBEN ANGEGEBENEN SEGMENTIERUNGEN WERDEN IN DIESEM KAPITEL NACH LÄNDERN DARGESTELLT)
23.1 NORDAMERIKA
23.1.1 US
23.1.2 KANADA
23.1.3 MEXIKO
23.2 EUROPA
23.2.1 DEUTSCHLAND
23.2.2 Vereinigtes Königreich
23.2.3 ITALIEN
23.2.4 FRANKREICH
23.2.5 SPANIEN
23.2.6 RUSSLAND
23.2.7 SCHWEIZ
23.2.8 Türkei
23.2.9 BELGIEN
23.2.10 NIEDERLANDE
23.2.11 DÄNEMARK
23.2.12 SCHWEDEN
23.2.13 POLEN
23.2.14 NORWEGEN
23.2.15 FINNLAND
23.2.16 Übriges Europa
23.3 ASIEN-PAZIFIK
23.3.1 JAPAN
23.3.2 CHINA
23.3.3 SÜDKOREA
23.3.4 INDIEN
23.3.5 SINGAPUR
23.3.6 THAILAND
23.3.7 INDONESIEN
23.3.8 MALAYSIA
23.3.9 PHILIPPINEN
23.3.10 AUSTRALIEN
23.3.11 NEUSEELAND
23.3.12 VIETNAM
23.3.13 TAIWAN
23.3.14 ÜBRIGER ASIEN-PAZIFIK
23.4 SÜDAMERIKA
23.4.1 BRASILIEN
23.4.2 ARGENTINIEN
23.4.3 RESTLICHES SÜDAMERIKA
23.5 MITTLERER OSTEN UND AFRIKA
23.5.1 SÜDAFRIKA
23.5.2 ÄGYPTEN
23.5.3 BAHRAIN
23.5.4 VEREINIGTE ARABISCHE EMIRATE
23.5.5 Kuwait
23.5.6 OMAN
23.5.7 Katar
23.5.8 SAUDI-ARABIEN
23.5.9 Übriger Naher Osten und Afrika
23.6 WICHTIGSTE ERGEBNISSE: NACH WICHTIGEN LÄNDERN
24 GLOBALER MARKT FÜR CAR-T-THERAPIE, SWOT- UND DBMR-ANALYSE
25. WELTWEITER MARKT FÜR CAR-T-THERAPIE, UNTERNEHMENSPROFIL
25.1 Novartis AG
25.1.1 UNTERNEHMENSÜBERSICHT
25.1.2 Umsatzanalyse
25.1.3 GEOGRAFISCHE PRÄSENZ
25.1.4 PRODUKTPORTFOLIO
25.1.5 Aktuelle Entwicklungen
25.2 KITE PHARMA
25.2.1 Unternehmensübersicht
25.2.2 Umsatzanalyse
25.2.3 GEOGRAFISCHE PRÄSENZ
25.2.4 PRODUKTPORTFOLIO
25.2.5 Aktuelle Entwicklungen
25.3 JUNO THERAPTICS
25.3.1 UNTERNEHMENSÜBERSICHT
25.3.2 Umsatzanalyse
25.3.3 GEOGRAFISCHE PRÄSENZ
25.3.4 PRODUKTPORTFOLIO
25.3.5 Aktuelle Entwicklungen
25.4 BRISTOL MYERS SQUIBB
25.4.1 UNTERNEHMENSÜBERSICHT
25.4.2 Umsatzanalyse
25.4.3 GEOGRAFISCHE PRÄSENZ
25.4.4 PRODUKTPORTFOLIO
25.4.5 Aktuelle Entwicklungen
25.5 LEGEND BIOTECH INC
25.5.1 Unternehmensübersicht
25.5.2 Umsatzanalyse
25.5.3 GEOGRAFISCHE PRÄSENZ
25.5.4 PRODUKTPORTFOLIO
25.5.5 Aktuelle Entwicklungen
25.6 AMMGEN, INC
25.6.1 UNTERNEHMENSÜBERSICHT
25.6.2 Umsatzanalyse
25.6.3 GEOGRAFISCHE PRÄSENZ
25.6.4 PRODUKTPORTFOLIO
25.6.5 Aktuelle Entwicklungen
25.7 SORRENTO THERAPUTICS, INC.
25.7.1 Unternehmensübersicht
25.7.2 Umsatzanalyse
25.7.3 GEOGRAFISCHE PRÄSENZ
25.7.4 PRODUKTPORTFOLIO
25.7.5 Aktuelle Entwicklungen
25.8 GILEAD SCIENCE
25.8.1 Unternehmensübersicht
25.8.2 Umsatzanalyse
25.8.3 GEOGRAFISCHE PRÄSENZ
25.8.4 PRODUKTPORTFOLIO
25.8.5 Aktuelle Entwicklungen
25.9 BLUE BIRD BIO, INC.
25.9.1 UNTERNEHMENSÜBERSICHT
25.9.2 Umsatzanalyse
25.9.3 GEOGRAFISCHE PRÄSENZ
25.9.4 PRODUKTPORTFOLIO
25.9.5 Aktuelle Entwicklungen
25.1 IMMUNTHERAPUTICS, INC.
25.10.1 UNTERNEHMENSÜBERSICHT
25.10.2 Umsatzanalyse
25.10.3 GEOGRAFISCHE PRÄSENZ
25.10.4 PRODUKTPORTFOLIO
25.10.5 Aktuelle Entwicklungen
25.11 BELLICUM PARMACEUTICALS, INC.
25.11.1 Unternehmensübersicht
25.11.2 Umsatzanalyse
25.11.3 GEOGRAFISCHE PRÄSENZ
25.11.4 PRODUKTPORTFOLIO
25.11.5 Aktuelle Entwicklungen
25.12 PFIZER, INC.
25.12.1 Unternehmensübersicht
25.12.2 Umsatzanalyse
25.12.3 GEOGRAFISCHE PRÄSENZ
25.12.4 PRODUKTPORTFOLIO
25.12.5 Aktuelle Entwicklungen
25.13 ELI LILLY AND COMPANY
25.13.1 UNTERNEHMENSÜBERSICHT
25.13.2 Umsatzanalyse
25.13.3 GEOGRAFISCHE PRÄSENZ
25.13.4 PRODUKTPORTFOLIO
25.13.5 Aktuelle Entwicklungen
25.14 JW THERAPEUTICS
25.14.1 UNTERNEHMENSÜBERSICHT
25.14.2 Umsatzanalyse
25.14.3 GEOGRAFISCHE PRÄSENZ
25.14.4 PRODUKTPORTFOLIO
25.14.5 Aktuelle Entwicklungen
25.15 FORTRESS BIOTECH, INC.
25.15.1 Unternehmensübersicht
25.15.2 Umsatzanalyse
25.15.3 GEOGRAFISCHE PRÄSENZ
25.15.4 PRODUKTPORTFOLIO
25.15.5 Aktuelle Entwicklungen
25.16 CARTESIAN THERAPEUTICS, INC.
25.16.1 UNTERNEHMENSÜBERSICHT
25.16.2 Umsatzanalyse
25.16.3 GEOGRAFISCHE PRÄSENZ
25.16.4 PRODUKTPORTFOLIO
25.16.5 Aktuelle Entwicklungen
25.17 CASI PHARMAZEUTIKA
25.17.1 Unternehmensübersicht
25.17.2 Umsatzanalyse
25.17.3 GEOGRAFISCHE PRÄSENZ
25.17.4 PRODUKTPORTFOLIO
25.17.5 Aktuelle Entwicklungen
25.18 POSEIDA THERAPEUTICS, INC.
25.18.1 UNTERNEHMENSÜBERSICHT
25.18.2 Umsatzanalyse
25.18.3 GEOGRAFISCHE PRÄSENZ
25.18.4 PRODUKTPORTFOLIO
25.18.5 Aktuelle Entwicklungen
25.19 AUTOLUS THERAPEUTICS
25.19.1 Unternehmensübersicht
25.19.2 Umsatzanalyse
25.19.3 GEOGRAFISCHE PRÄSENZ
25.19.4 PRODUKTPORTFOLIO
25.19.5 Aktuelle Entwicklungen
25.2 EUREKA THERAPEUTICS
25.20.1 UNTERNEHMENSÜBERSICHT
25.20.2 Umsatzanalyse
25.20.3 GEOGRAFISCHE PRÄSENZ
25.20.4 PRODUKTPORTFOLIO
25.20.5 Aktuelle Entwicklungen
25.21 AURORA BIOPHARMA
25.21.1 UNTERNEHMENSÜBERSICHT
25.21.2 Umsatzanalyse
25.21.3 GEOGRAFISCHE PRÄSENZ
25.21.4 PRODUKTPORTFOLIO
25.21.5 Aktuelle Entwicklungen
25.22 IMMUNAKTIV
25.22.1 UNTERNEHMENSÜBERSICHT
25.22.2 Umsatzanalyse
25.22.3 GEOGRAFISCHE PRÄSENZ
25.22.4 PRODUKTPORTFOLIO
25.22.5 Aktuelle Entwicklungen
25,23 FERRING PHARMACEUTICALS A/S
25.23.1 UNTERNEHMENSÜBERSICHT
25.23.2 Umsatzanalyse
25.23.3 GEOGRAFISCHE PRÄSENZ
25.23.4 PRODUKTPORTFOLIO
25.23.5 Aktuelle Entwicklungen
25.24 JANSSEN BIOTECH, INC.
25.24.1 UNTERNEHMENSÜBERSICHT
25.24.2 Umsatzanalyse
25.24.3 GEOGRAFISCHE PRÄSENZ
25.24.4 PRODUKTPORTFOLIO
25.24.5 Aktuelle Entwicklungen
Hinweis: Die aufgeführten Unternehmen sind nicht vollständig und entsprechen den Anforderungen unserer vorherigen Kunden. Wir analysieren über 100 Unternehmen in unserer Studie; daher kann die Liste auf Anfrage geändert oder ersetzt werden.
26 VERWANDTE BERICHTE
27. SCHLUSSFOLGERUNG
28. Fragebogen
29 ÜBER DATA BRIDGE MARKTFORSCHUNG
Forschungsmethodik
Die Datenerfassung und Basisjahresanalyse werden mithilfe von Datenerfassungsmodulen mit großen Stichprobengrößen durchgeführt. Die Phase umfasst das Erhalten von Marktinformationen oder verwandten Daten aus verschiedenen Quellen und Strategien. Sie umfasst die Prüfung und Planung aller aus der Vergangenheit im Voraus erfassten Daten. Sie umfasst auch die Prüfung von Informationsinkonsistenzen, die in verschiedenen Informationsquellen auftreten. Die Marktdaten werden mithilfe von marktstatistischen und kohärenten Modellen analysiert und geschätzt. Darüber hinaus sind Marktanteilsanalyse und Schlüsseltrendanalyse die wichtigsten Erfolgsfaktoren im Marktbericht. Um mehr zu erfahren, fordern Sie bitte einen Analystenanruf an oder geben Sie Ihre Anfrage ein.
Die wichtigste Forschungsmethodik, die vom DBMR-Forschungsteam verwendet wird, ist die Datentriangulation, die Data Mining, die Analyse der Auswirkungen von Datenvariablen auf den Markt und die primäre (Branchenexperten-)Validierung umfasst. Zu den Datenmodellen gehören ein Lieferantenpositionierungsraster, eine Marktzeitlinienanalyse, ein Marktüberblick und -leitfaden, ein Firmenpositionierungsraster, eine Patentanalyse, eine Preisanalyse, eine Firmenmarktanteilsanalyse, Messstandards, eine globale versus eine regionale und Lieferantenanteilsanalyse. Um mehr über die Forschungsmethodik zu erfahren, senden Sie eine Anfrage an unsere Branchenexperten.
Anpassung möglich
Data Bridge Market Research ist ein führendes Unternehmen in der fortgeschrittenen formativen Forschung. Wir sind stolz darauf, unseren bestehenden und neuen Kunden Daten und Analysen zu bieten, die zu ihren Zielen passen. Der Bericht kann angepasst werden, um Preistrendanalysen von Zielmarken, Marktverständnis für zusätzliche Länder (fordern Sie die Länderliste an), Daten zu klinischen Studienergebnissen, Literaturübersicht, Analysen des Marktes für aufgearbeitete Produkte und Produktbasis einzuschließen. Marktanalysen von Zielkonkurrenten können von technologiebasierten Analysen bis hin zu Marktportfoliostrategien analysiert werden. Wir können so viele Wettbewerber hinzufügen, wie Sie Daten in dem von Ihnen gewünschten Format und Datenstil benötigen. Unser Analystenteam kann Ihnen auch Daten in groben Excel-Rohdateien und Pivot-Tabellen (Fact Book) bereitstellen oder Sie bei der Erstellung von Präsentationen aus den im Bericht verfügbaren Datensätzen unterstützen.