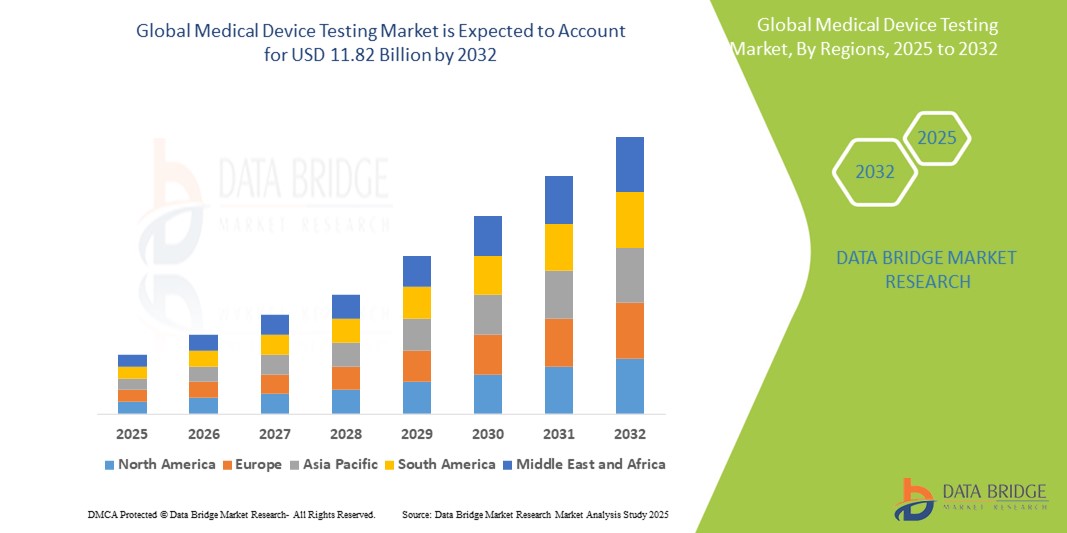
Global Medical Device Testing Market
Marktgröße in Milliarden USD
CAGR :
% 
 USD
5.20 Billion
USD
11.82 Billion
202
2032
USD
5.20 Billion
USD
11.82 Billion
202
2032
| 203 –2032 | |
| USD 5.20 Billion | |
| USD 11.82 Billion | |
|
|
|
|
Globale Marktsegmentierung für Tests medizinischer Geräte nach Servicetyp (Testservices, Inspektionsservices und Zertifizierungsservices), Testtyp (physikalische Tests, chemische/biologische Tests, Cybersicherheitstests, mikrobiologische und Sterilitätstests und andere), Phase (präklinisch und klinisch), Beschaffungstyp (intern und ausgelagert), Geräteklasse (Klasse I, Klasse II und Klasse III), Produkt (aktives Implantat, aktives Medizinprodukt, nicht-aktives Medizinprodukt, In-vitro-Diagnostikprodukt, ophthalmisches Medizinprodukt, orthopädisches und zahnmedizinisches Medizinprodukt, vaskuläres Medizinprodukt und andere) – Branchentrends und Prognose bis 2032
Marktgröße für Tests medizinischer Geräte
- Der globale Markt für Tests medizinischer Geräte wurde im Jahr 2024 auf 5,20 Milliarden US-Dollar geschätzt und dürfte bis 2032 11,82 Milliarden US-Dollar erreichen , was einer jährlichen Wachstumsrate von 10,80 % im Prognosezeitraum entspricht.
- Dieses Wachstum ist auf die steigende Nachfrage nach sichereren und zuverlässigeren Medizinprodukten, den technologischen Fortschritt bei Testmethoden und die weltweit steigende Zahl regulatorischer Anforderungen für die Zulassung von Medizinprodukten zurückzuführen. Darüber hinaus tragen der Anstieg chronischer Krankheiten, die alternde Bevölkerung und der expandierende Gesundheitssektor zum wachsenden Bedarf an umfassenden Tests für Medizinprodukte bei.
Marktanalyse für Tests medizinischer Geräte
- Die Prüfung medizinischer Geräte ist ein entscheidender Teil des Produktentwicklungszyklus. Sie stellt sicher, dass medizinische Geräte den gesetzlichen Standards entsprechen, für die Patienten sicher sind und in verschiedenen Gesundheitsanwendungen, einschließlich Diagnose-, Überwachungs- und Therapiegeräten, die vorgesehene Leistung erbringen.
- Die Nachfrage nach Tests für Medizinprodukte wird vor allem durch die steigende Zahl an Innovationen im Medizinproduktebereich, strenge gesetzliche Anforderungen und wachsende Bedenken hinsichtlich der Patientensicherheit getrieben.
- Nordamerika dominiert den globalen Markt für Medizinproduktetests und wird im Jahr 2024 einen erheblichen Anteil von schätzungsweise 40,2 % haben. Diese Dominanz ist auf die Präsenz großer Medizinproduktehersteller, etablierte regulatorische Rahmenbedingungen und
- Die Region Asien-Pazifik (APAC) verzeichnet das schnellste Wachstum im globalen Markt für Medizinproduktetests. Das Wachstum ist auf die rasch wachsende Gesundheitsinfrastruktur, steigende Gesundheitsausgaben und die steigende Nachfrage nach fortschrittlicher Medizintechnik in Ländern wie China, Indien und Japan zurückzuführen.
- Das Segment der In-vitro-Diagnostik (IVD) wird voraussichtlich den globalen Markt für Medizinproduktetests dominieren und einen Marktanteil von rund 33 % halten. Diese Dominanz ist auf die steigende Nachfrage nach präzisen Diagnoseinstrumenten zurückzuführen, insbesondere als Reaktion auf die zunehmende Belastung durch chronische Krankheiten.
Berichtsumfang und Marktsegmentierung für Medizinproduktetests
|
Eigenschaften |
Wichtige Markteinblicke zum Testen medizinischer Geräte |
|
Abgedeckte Segmente |
|
|
Abgedeckte Länder |
Nordamerika
Europa
Asien-Pazifik
Naher Osten und Afrika
Südamerika
|
|
Wichtige Marktteilnehmer |
|
|
Marktchancen |
|
|
Wertschöpfungsdaten-Infosets |
Zusätzlich zu den Einblicken in Marktszenarien wie Marktwert, Wachstumsrate, Segmentierung, geografische Abdeckung und wichtige Akteure enthalten die von Data Bridge Market Research kuratierten Marktberichte auch Import-Export-Analysen, eine Übersicht über die Produktionskapazität, eine Analyse des Produktionsverbrauchs, eine Preistrendanalyse, ein Szenario des Klimawandels, eine Lieferkettenanalyse, eine Wertschöpfungskettenanalyse, eine Übersicht über Rohstoffe/Verbrauchsmaterialien, Kriterien für die Lieferantenauswahl, eine PESTLE-Analyse, eine Porter-Analyse und regulatorische Rahmenbedingungen. |
Markttrends für Tests medizinischer Geräte
„Integration digitaler Gesundheitslösungen und KI in Gerätetests“
- Ein wichtiger Trend im Markt für Medizinproduktetests ist die zunehmende Integration digitaler Gesundheitslösungen und künstlicher Intelligenz (KI) in die Test- und Validierungsprozesse. Diese Innovationen verbessern die Genauigkeit, Effizienz und Geschwindigkeit der Tests und erhöhen gleichzeitig die Patientensicherheit.
- Die Integration von KI-gestützten Tools und fortschrittlicher Datenanalyse ermöglicht Echtzeitüberwachung, prädiktive Tests und eine schnellere Einhaltung gesetzlicher Vorschriften. Dadurch wird es für Hersteller einfacher, Geräte in verschiedenen Entwicklungsstadien zu testen.
- So führten beispielsweise die Charles River Laboratories im Juli 2023 KI-basierte Testdienste ein, um die Bewertung von Medizinprodukten zu beschleunigen, die Testpräzision zu verbessern und die Einhaltung der sich entwickelnden regulatorischen Standards in den USA zu unterstützen.
- Diese Fortschritte verändern den Testprozess für Medizinprodukte, ermöglichen bessere Entscheidungen, verkürzen die Markteinführungszeit von Geräten und unterstützen Hersteller bei der Einhaltung strenger gesetzlicher Anforderungen.
Marktdynamik für Medizinproduktetests
Treiber
„Steigende Nachfrage nach hochwertigen und konformen Medizinprodukten“
- Die wachsende Nachfrage nach hochwertigen, zuverlässigen und konformen Medizinprodukten treibt den globalen Markt für Medizinproduktetests maßgeblich voran. Da Hersteller von Medizinprodukten strenge regulatorische Standards erfüllen und die Patientensicherheit gewährleisten möchten, steigt der Bedarf an umfassenden Testlösungen für verschiedene Gerätekategorien, darunter Diagnostik-, Überwachungs- und Therapiegeräte.
- Mit der weltweiten Expansion der Gesundheitssysteme, insbesondere in den Schwellenländern, steigt die Nachfrage nach fortschrittlichen medizinischen Technologien und Geräten. Dies veranlasst Hersteller dazu, umfangreiche Testprotokolle einzuführen, um den sich entwickelnden Vorschriften zu entsprechen und den Marktanforderungen gerecht zu werden.
- Hersteller suchen außerdem zunehmend nach spezialisierten, gesetzeskonformen und anpassbaren Testlösungen, um sicherzustellen, dass ihre Produkte sowohl die Sicherheits- als auch die Leistungsstandards im Gesundheitssektor erfüllen.
Zum Beispiel,
- Im März 2024 ging Charles River Laboratories eine Partnerschaft mit einem führenden europäischen Hersteller medizinischer Geräte ein, um fortschrittliche Testdienstleistungen anzubieten und so die Einhaltung gesetzlicher Vorschriften und die Produktzuverlässigkeit für dessen neue Linie implantierbarer Geräte sicherzustellen.
- Aufgrund des wachsenden Bedarfs an zuverlässigen und konformen Medizinprodukten steigt die Nachfrage nach umfassenden Prüfdienstleistungen für Medizinprodukte deutlich an, insbesondere in Regionen mit wachsender Gesundheitsinfrastruktur und regulatorischen Anforderungen.
Gelegenheit
„Integration von KI und Automatisierung bei der Prüfung medizinischer Geräte“
- Die Integration von KI und Automatisierung in die Prüfung medizinischer Geräte bietet eine bedeutende Chance, die Effizienz, Genauigkeit und Geschwindigkeit der Test- und Validierungsprozesse zu steigern. Diese Technologien können wiederkehrende Testverfahren rationalisieren, die Datenanalyse verbessern und sicherstellen, dass die Geräte die gesetzlichen Standards besser erfüllen.
- KI-gestützte Systeme können Testdaten kontinuierlich analysieren, potenzielle Geräteausfälle vorhersagen und den Dokumentationsprozess automatisieren. Dadurch werden menschliche Fehler reduziert und die Konsistenz der Testergebnisse sichergestellt. Diese Automatisierung ermöglicht eine schnellere Markteinführung medizinischer Geräte und gewährleistet gleichzeitig die Einhaltung strenger Vorschriften.
- Die Möglichkeit, KI-basierte prädiktive Analysen in Testsysteme zu integrieren, dürfte die Nachfrage nach fortschrittlicheren und kostengünstigeren Testlösungen für medizinische Geräte branchenübergreifend steigern.
Zum Beispiel,
- Im Januar 2024 ging Medistri SA eine Partnerschaft mit dem auf KI spezialisierten Technologieunternehmen Veeva Systems ein, um eine neue KI-gesteuerte Testplattform für Medizinprodukte einzuführen, die automatisierte Prüfungen der Einhaltung gesetzlicher Vorschriften und eine vorausschauende Qualitätssicherung für kritische Gesundheitsgeräte ermöglicht.
- Die Integration von KI und Automatisierung in die Prüfung medizinischer Geräte dürfte die Testeffizienz deutlich verbessern, die Betriebskosten senken und die Zuverlässigkeit medizinischer Geräte erhöhen, was zu einer breiten Akzeptanz dieser fortschrittlichen Technologien auf dem globalen Markt für die Prüfung medizinischer Geräte führen wird.
Einschränkung/Herausforderung
„Hohe Kosten für Tests und Einhaltung gesetzlicher Vorschriften“
- Die hohen Kosten im Zusammenhang mit der Prüfung medizinischer Geräte und der Einhaltung gesetzlicher Vorschriften stellen eine erhebliche Herausforderung für das Marktwachstum dar, insbesondere für kleine und mittlere Unternehmen (KMU) in Schwellenländern.
- Die Prüfung medizinischer Geräte, insbesondere von hochentwickelten oder risikoreichen Produkten, erfordert erhebliche Investitionen in Spezialausrüstung, qualifizierte Arbeitskräfte und die Einhaltung strenger globaler Vorschriften. Dies kann für Unternehmen mit begrenztem Budget eine erhebliche finanzielle Belastung darstellen, insbesondere bei komplexen Tests wie klinischen Studien oder Langzeit-Leistungsbewertungen.
- Die laufenden Kosten, einschließlich der Prüfung für verschiedene Aufsichtsbehörden (z. B. FDA, CE-Kennzeichnung) sowie die Einhaltung der sich entwickelnden Gesundheitsstandards, können die finanziellen Herausforderungen für Hersteller zusätzlich erhöhen.
Zum Beispiel,
- Im März 2024 hob ein Bericht von Eurofins Scientific hervor, dass kleine Hersteller medizinischer Geräte in Schwellenländern aufgrund der erheblichen Kosten, die mit umfassenden Test- und Zertifizierungsprozessen verbunden sind, vor Herausforderungen bei der Einhaltung internationaler Regulierungsstandards stehen.
- Diese finanziellen Hürden können Unternehmen davon abhalten, in notwendige Testverfahren zu investieren oder neue Testtechnologien einzuführen. Dies führt zu Verzögerungen bei der Produkteinführung oder zu geringeren Markteintrittschancen für kleinere Akteure. Infolgedessen könnten die hohen Kosten für die Prüfung medizinischer Geräte das Marktwachstum langfristig behindern.
Marktumfang für Tests medizinischer Geräte
Der Markt ist nach Servicetyp, Testtyp, Phase, Beschaffungstyp, Geräteklasse und Produkt segmentiert.
|
Segmentierung |
Untersegmentierung |
|
Nach Servicetyp |
|
|
Nach Testtyp |
|
|
Nach Phase |
|
|
Nach Beschaffungstyp |
|
|
Nach Geräteklasse |
|
|
Nach Produkt |
|
Im Jahr 2025 wird das Segment In-vitro-Diagnostik voraussichtlich den Markt für Industriekessel dominieren und im Segment der Brennstoffprodukte den größten Anteil haben.
Das Segment IVD-Tests wird voraussichtlich den globalen Markt für Medizinproduktetests dominieren und einen Marktanteil von rund 33 % halten. Diese Dominanz ist auf die steigende Nachfrage nach präzisen und schnellen Diagnoseinstrumenten zurückzuführen, insbesondere als Reaktion auf die zunehmende Belastung durch chronische Krankheiten und den steigenden Bedarf an nicht-invasiven Testmethoden. IVD-Testlösungen wie Molekulardiagnostik, Point-of-Care-Tests und personalisierte Medizin bieten hohe Genauigkeit, Geschwindigkeit und Komfort und sind daher sowohl für Gesundheitsdienstleister als auch für Patienten die bevorzugte Wahl. Darüber hinaus unterstützen die kontinuierlichen Fortschritte im Bereich der digitalen Gesundheit und Automatisierung die breite Akzeptanz von IVD-Testlösungen in verschiedenen Bereichen des Gesundheitswesens, von Krankenhäusern bis hin zur häuslichen Pflege.
Es wird erwartet, dass die Cybersicherheitstests im Prognosezeitraum den größten Anteil an den Testartensegmenten ausmachen werden
Das Segment Cybersicherheitstests wird voraussichtlich einen signifikanten Marktanteil von rund 35 % im Jahr 2025 halten. Diese Dominanz ist auf die zunehmende Bedeutung des Schutzes medizinischer Geräte vor Cybersicherheitsbedrohungen zurückzuführen, da Gesundheitssysteme durch das Internet der Dinge (IoT) und Cloud-basierte Technologien immer stärker vernetzt werden. Angesichts der zunehmenden Cyberangriffe auf Gesundheitseinrichtungen und medizinische Geräte hat die Gewährleistung der Sicherheit von Geräten wie Herzschrittmachern, Insulinpumpen und Diagnosegeräten höchste Priorität.
Regionale Analyse des Marktes für Medizinproduktetests
„Nordamerika hält den größten Anteil am Markt für Tests medizinischer Geräte“
- Nordamerika dominiert den globalen Markt für Tests medizinischer Geräte und wird im Jahr 2024 etwa 40,2 % des Marktanteils ausmachen.
- Die USA halten im Jahr 2024 einen signifikanten Anteil von etwa 35 % am weltweiten Markt für Medizinproduktetests. Diese Dominanz ist auf die hohe Nachfrage nach fortschrittlichen Medizinprodukten, ein gut etabliertes Gesundheitssystem und kontinuierliche Innovationen bei Medizinproduktetechnologien und Testlösungen zurückzuführen.
- Die Verfügbarkeit etablierter regulatorischer Rahmenbedingungen, wie z. B. FDA-Zulassungsverfahren, und wachsende Investitionen in Forschung und Entwicklung durch führende Hersteller medizinischer Geräte stärken den Markt in Nordamerika weiter
- Darüber hinaus treiben der zunehmende Fokus auf Patientensicherheit, die Einhaltung gesetzlicher Vorschriften und die Einführung modernster Testtechnologien wie KI und Automatisierung die Marktexpansion in der gesamten Region voran.
„ Im asiatisch-pazifischen Raum wird auf dem Markt für Tests medizinischer Geräte voraussichtlich die höchste durchschnittliche jährliche Wachstumsrate verzeichnet .“
- Im asiatisch-pazifischen Raum (APAC) wird das weltweite Wachstum im Markt für Medizinproduktetests voraussichtlich am höchsten ausfallen. Dies ist auf die rasante Entwicklung der Gesundheitsinfrastruktur, die steigende Nachfrage nach Medizinprodukten und die zunehmenden Anforderungen an die Einhaltung gesetzlicher Vorschriften zurückzuführen.
- Länder wie China, Indien und Japan entwickeln sich aufgrund ihrer expandierenden Gesundheitssysteme, der steigenden Nachfrage nach fortschrittlichen Medizintechnologien und der zunehmenden Konzentration auf Patientensicherheit und regulatorische Standards zu Schlüsselmärkten
- China mit seinem großen Gesundheitssektor und hohen Investitionen in die Herstellung medizinischer Geräte treibt die Nachfrage nach Prüfdienstleistungen für medizinische Geräte voran. Das Land konzentriert sich zudem auf die Verbesserung der regulatorischen Standards und die Verbesserung der Qualität der Gesundheitsversorgung, was die Einführung fortschrittlicher Testlösungen weiter vorantreibt.
- Indien, mit seiner aufstrebenden Gesundheitsbranche und der wachsenden Nachfrage nach erschwinglichen und innovativen medizinischen Geräten, erlebt eine schnelle Einführung von Testlösungen für medizinische Geräte, um den steigenden Bedürfnissen der Patienten gerecht zu werden
- Verstärkte staatliche Initiativen und Investitionen des Privatsektors in die Gesundheitsinfrastruktur tragen weiter zum Marktwachstum in der Region bei
Marktanteil bei Tests medizinischer Geräte
Die Wettbewerbslandschaft des Marktes liefert detaillierte Informationen zu den einzelnen Wettbewerbern. Zu den Details gehören Unternehmensübersicht, Unternehmensfinanzen, Umsatz, Marktpotenzial, Investitionen in Forschung und Entwicklung, neue Marktinitiativen, globale Präsenz, Produktionsstandorte und -anlagen, Produktionskapazitäten, Stärken und Schwächen des Unternehmens, Produkteinführung, Produktbreite und -umfang sowie Anwendungsdominanz. Die oben genannten Datenpunkte beziehen sich ausschließlich auf die Marktausrichtung der Unternehmen.
Die wichtigsten Marktführer auf dem Markt sind:
- Intertek Group plc (Großbritannien)
- SGS SA (Schweiz)
- Bureau Veritas (Frankreich)
- TÜV SÜD (Deutschland)
- TÜV Rheinland (Deutschland)
- Tempo (USA)
- Charles River Laboratories (USA)
- Labore für biomedizinische Geräte (USA)
- UL LLC (USA)
- North American Science Associates, LLC (USA)
- Medistri SA (Schweiz)
- WuXi AppTec (China)
- NSF (USA)
- Labcorp (USA)
- Eurofins Scientific (Luxemburg)
- Nelson Laboratories, LLC – Ein Unternehmen von Sotera Health (USA)
- Gateway Analytical (USA)
- ITC ZLIN (Tschechische Republik)
- Element Materials Technology (Großbritannien)
- EndoLab Mechanical Engineering GmbH (Deutschland)
- Hohenstein (Deutschland)
- Medical Engineering Technologies Ltd. (Großbritannien)
- Bioneeds (Indien)
- Cigniti (Indien)
- Arbro Pharmaceuticals Private Limited und Auriga Research Private Limited (Indien)
- Q Laboratories (USA)
- IMR Test Labs (USA)
Neueste Entwicklungen auf dem globalen Markt für Medizingerätetests
- Im Januar 2025 trat die IMQ Group mit der Gründung von Elettra Tech Labs in den indischen Markt ein, einem Joint Venture, das sich auf Prüf- und Inspektionsdienstleistungen für Medizinprodukte sowie elektrische und elektronische Produkte konzentriert. Diese Expansion stärkt die globale Präsenz von IMQ und unterstützt indische Unternehmen bei der Einhaltung strenger Qualitäts- und Sicherheitsstandards und erleichtert gleichzeitig den internationalen Marktzugang. Die Initiative steht im Einklang mit Indiens wachsendem Medizinproduktesektor und nutzt fortschrittliche Prüftechnologien, um Compliance und Innovation zu verbessern.
- Im März 2024 erweiterte Stryker seine Prototypen- und Testanlage in Indien und markierte damit einen wichtigen Meilenstein in seiner Forschungs- und Entwicklungstätigkeit. Die 5.150 Quadratmeter große Anlage vereint modernste Infrastruktur und erweiterte mikrobiologische Kapazitäten und stärkt so Produktsicherheit und Innovation. Die Erweiterung unterstützt strenge Lebenszyklustests von Medizinprodukten und gewährleistet die Einhaltung globaler regulatorischer Standards. Die Anlage verfügt zudem über fortschrittliche Prototyping-Tools, darunter 3D-Kunststoffdruck und Metallbearbeitung, und unterstreicht damit Strykers Engagement für den Fortschritt in der Medizintechnik.
- Im März 2024 startete TidalSense, ein britisches Unternehmen für Beatmungsgeräte, eine Pilotstudie zur Evaluierung seines Geräts N-Tidal, das zur Asthmadiagnose bei Kindern entwickelt wurde. Die Studie wurde in Zusammenarbeit mit der University of Nottingham und dem Nottingham University Hospitals NHS Trust durchgeführt und umfasste 75 Kinder unter fünf Jahren mit Asthma und viraler Keuchatmung. Im Gegensatz zu herkömmlichen Spirometrietests, die komplexe Atemmanöver erfordern, nutzt N-Tidal die Kapnographie, um den CO₂-Gehalt während der normalen Atmung zu messen. Dies macht die Diagnose einfacher und zugänglicher.
- Im Juni 2023 eröffnete TÜV SÜD in New Brighton, Minnesota, ein hochmodernes mikrobiologisches und chemisches Labor und bekräftigte damit sein Engagement für hochwertige Prüfdienstleistungen für Medizinprodukte. Die nach ISO 17025 akkreditierte Einrichtung ist auf biologische und chemische Prüfungen spezialisiert und unterstützt Medizinprodukteunternehmen bei der Beschleunigung ihrer Forschung und Entwicklung. Ausgestattet mit modernster Technologie bietet das Labor Prüfungen in den Bereichen Mikrobiologie, wiederverwendbare Geräte, Chemie, Biokompatibilität und Verpackung an. Diese Erweiterung stärkt das globale Labornetzwerk von TÜV SÜD und gewährleistet Präzision und Konformität für medizinische Innovationen.
- Im Juli 2022 übernahm Eurofins Scientific WESSLING Hungary und stärkte damit seine Kompetenzen in den Bereichen Umwelt-, Lebensmittel- und Biopharma-Produktprüfung in ganz Europa. WESSLING Hungary, ein führendes Labor, erwirtschaftete 2021 einen Umsatz von 15 Millionen Euro und beschäftigte über 300 Mitarbeiter. Dies unterstreicht das Engagement von Eurofins für hochwertige analytische Dienstleistungen.
SKU-
Erhalten Sie Online-Zugriff auf den Bericht zur weltweit ersten Market Intelligence Cloud
- Interaktives Datenanalyse-Dashboard
- Unternehmensanalyse-Dashboard für Chancen mit hohem Wachstumspotenzial
- Zugriff für Research-Analysten für Anpassungen und Abfragen
- Konkurrenzanalyse mit interaktivem Dashboard
- Aktuelle Nachrichten, Updates und Trendanalyse
- Nutzen Sie die Leistungsfähigkeit der Benchmark-Analyse für eine umfassende Konkurrenzverfolgung
Forschungsmethodik
Die Datenerfassung und Basisjahresanalyse werden mithilfe von Datenerfassungsmodulen mit großen Stichprobengrößen durchgeführt. Die Phase umfasst das Erhalten von Marktinformationen oder verwandten Daten aus verschiedenen Quellen und Strategien. Sie umfasst die Prüfung und Planung aller aus der Vergangenheit im Voraus erfassten Daten. Sie umfasst auch die Prüfung von Informationsinkonsistenzen, die in verschiedenen Informationsquellen auftreten. Die Marktdaten werden mithilfe von marktstatistischen und kohärenten Modellen analysiert und geschätzt. Darüber hinaus sind Marktanteilsanalyse und Schlüsseltrendanalyse die wichtigsten Erfolgsfaktoren im Marktbericht. Um mehr zu erfahren, fordern Sie bitte einen Analystenanruf an oder geben Sie Ihre Anfrage ein.
Die wichtigste Forschungsmethodik, die vom DBMR-Forschungsteam verwendet wird, ist die Datentriangulation, die Data Mining, die Analyse der Auswirkungen von Datenvariablen auf den Markt und die primäre (Branchenexperten-)Validierung umfasst. Zu den Datenmodellen gehören ein Lieferantenpositionierungsraster, eine Marktzeitlinienanalyse, ein Marktüberblick und -leitfaden, ein Firmenpositionierungsraster, eine Patentanalyse, eine Preisanalyse, eine Firmenmarktanteilsanalyse, Messstandards, eine globale versus eine regionale und Lieferantenanteilsanalyse. Um mehr über die Forschungsmethodik zu erfahren, senden Sie eine Anfrage an unsere Branchenexperten.
Anpassung möglich
Data Bridge Market Research ist ein führendes Unternehmen in der fortgeschrittenen formativen Forschung. Wir sind stolz darauf, unseren bestehenden und neuen Kunden Daten und Analysen zu bieten, die zu ihren Zielen passen. Der Bericht kann angepasst werden, um Preistrendanalysen von Zielmarken, Marktverständnis für zusätzliche Länder (fordern Sie die Länderliste an), Daten zu klinischen Studienergebnissen, Literaturübersicht, Analysen des Marktes für aufgearbeitete Produkte und Produktbasis einzuschließen. Marktanalysen von Zielkonkurrenten können von technologiebasierten Analysen bis hin zu Marktportfoliostrategien analysiert werden. Wir können so viele Wettbewerber hinzufügen, wie Sie Daten in dem von Ihnen gewünschten Format und Datenstil benötigen. Unser Analystenteam kann Ihnen auch Daten in groben Excel-Rohdateien und Pivot-Tabellen (Fact Book) bereitstellen oder Sie bei der Erstellung von Präsentationen aus den im Bericht verfügbaren Datensätzen unterstützen.