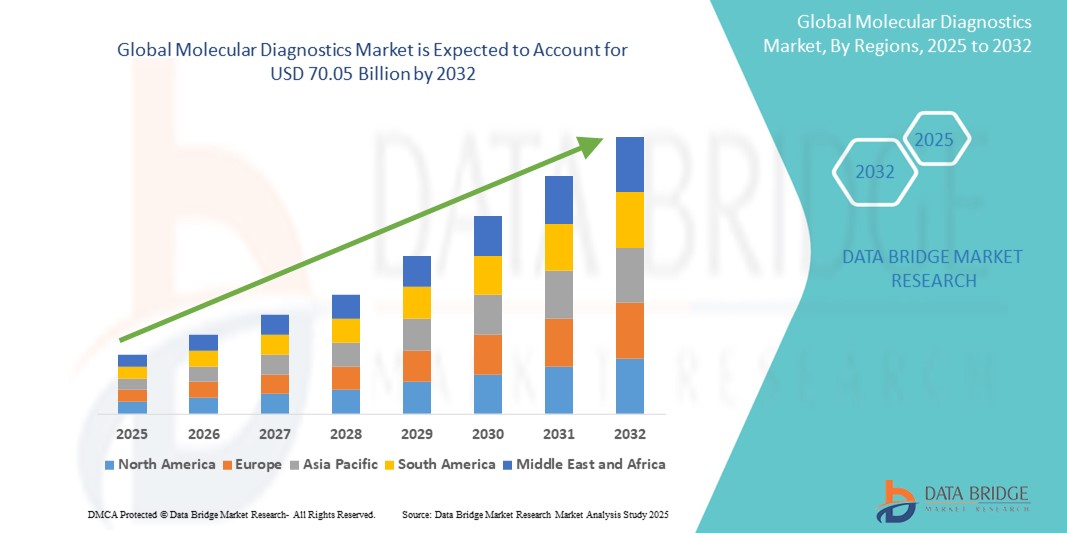
Global Molecular Diagnostics Market
Marktgröße in Milliarden USD
CAGR :
% 
 USD
25.80 Billion
USD
70.05 Billion
2024
2032
USD
25.80 Billion
USD
70.05 Billion
2024
2032
| 2025 –2032 | |
| USD 25.80 Billion | |
| USD 70.05 Billion | |
|
|
|
|
Globale Marktsegmentierung für molekulare Diagnostik nach Produkten (Reagenzien und Kits, Instrumente, Dienstleistungen und Software), Technologie (Massenspektrometrie (MS), Kapillarelektrophorese, Next-Generation-Sequenzierung (NGS), Chips und Microarrays, PCR-basierte Methoden, Zytogenetik, In-situ-Hybridisierung (ISH oder FISH), molekulare Bildgebung und Sonstige), Anwendung (Onkologie, Pharmakogenomik, Mikrobiologie, Pränataldiagnostik, Gewebetypisierung, Blutuntersuchungen, Herz-Kreislauf-Erkrankungen, neurologische Erkrankungen, Infektionskrankheiten und Sonstige), Endnutzer (Krankenhäuser, klinische Labore und akademische Einrichtungen) – Branchentrends und Prognose bis 2032
Marktgröße für molekulare Diagnostik
- Der globale Markt für molekulare Diagnostik wurde im Jahr 2024 auf 25,8 Milliarden US-Dollar geschätzt und wird voraussichtlich bis 2032 auf 70,05 Milliarden US-Dollar anwachsen.
- Im Prognosezeitraum von 2025 bis 2032 wird der Markt voraussichtlich mit einer durchschnittlichen jährlichen Wachstumsrate (CAGR) von 13,30 % wachsen, vor allem getrieben durch die hohe Nutzung von PCR-Tests.
- Dieses Wachstum wird durch Faktoren wie Genauigkeit, Sensibilität und kurze Bearbeitungszeiten angetrieben.
Marktanalyse für molekulare Diagnostik
- Die Molekulardiagnostik ist ein Bereich der medizinischen Testverfahren, der molekularbiologische Techniken wie PCR und NGS nutzt, um Krankheiten zu erkennen und zu überwachen, genetische Prädispositionen zu identifizieren und gezielte Therapien zu steuern. Sie findet breite Anwendung im Gesundheitswesen, in klinischen Laboren und in der Forschung.
- Das Marktwachstum wird durch die zunehmende Verbreitung von Infektionskrankheiten und chronischen Erkrankungen, die steigende Nachfrage nach personalisierter Medizin und die wachsende Akzeptanz fortschrittlicher Diagnosetechnologien wie Echtzeit-PCR und Next-Generation-Sequenzierung angetrieben.
- Der Markt entwickelt sich durch technologische Innovationen in automatisierten Plattformen, die Integration von KI und maschinellem Lernen zur Ergebnisinterpretation sowie die Entwicklung tragbarer, patientennaher Diagnosegeräte weiter, die Geschwindigkeit, Genauigkeit und Zugänglichkeit verbessern.
- Beispielsweise nutzen Unternehmen wie Roche und Thermo Fisher Scientific digitale Technologien und Automatisierung, um schnellere und präzisere molekulardiagnostische Lösungen anzubieten, die auf die Bedürfnisse von Klinik und Labor zugeschnitten sind.
- Der Markt für molekulare Diagnostik dürfte ein anhaltendes Wachstum verzeichnen, unterstützt durch die fortlaufenden Fortschritte in der Genomik, den Ausbau der Gesundheitsinfrastruktur und verstärkte Investitionen in die Früherkennung von Krankheiten und Initiativen zur Präzisionsmedizin.
Berichtsumfang und Marktsegmentierung für molekulare Diagnostik
|
Attribute |
Wichtige Markteinblicke in die molekulare Diagnostik |
|
Abgedeckte Segmente |
|
|
Abgedeckte Länder |
Nordamerika
Europa
Asien-Pazifik
Naher Osten und Afrika
Südamerika
|
|
Wichtige Marktteilnehmer |
|
|
Marktchancen |
|
|
Mehrwertdaten-Infosets |
Zusätzlich zu den Erkenntnissen über Marktszenarien wie Marktwert, Wachstumsrate, Segmentierung, geografische Abdeckung und Hauptakteure enthalten die von Data Bridge Market Research erstellten Marktberichte auch detaillierte Expertenanalysen, Patientenepidemiologie, Pipeline-Analyse, Preisanalyse und regulatorische Rahmenbedingungen. |
Markttrends in der Molekulardiagnostik
„Zunehmende Anwendung von Flüssigbiopsieverfahren“
- Ein auffälliger Trend auf dem globalen Markt für molekulare Diagnostik ist die zunehmende Anwendung von Flüssigbiopsie -Techniken.
- Dieser Trend wird durch die wachsende Nachfrage nach nicht-invasiven Diagnoseverfahren, den Bedarf an Echtzeitüberwachung des Krankheitsverlaufs und den zunehmenden Fokus auf personalisierte Behandlungsstrategien, insbesondere in der Onkologie, vorangetrieben.
- Beispielsweise entwickeln Unternehmen wie Guardant Health und Biocept Technologien für die Flüssigbiopsie, die zirkulierende Tumor-DNA (ctDNA) und andere Biomarker analysieren, um eine frühzeitige Krebserkennung und die Auswahl geeigneter Therapien zu ermöglichen.
- Die anhaltende Verlagerung hin zu minimalinvasiven Verfahren sowie die technologischen Verbesserungen bei der Biomarker-Erkennung und Genomanalyse beschleunigen die Integration der Flüssigbiopsie in die klinische Routinepraxis.
- Da sich Gesundheitssysteme zunehmend auf Präzisionsmedizin, Früherkennung und verbesserte Patientenergebnisse konzentrieren, wird erwartet, dass die Flüssigbiopsie eine transformative Rolle bei der Erweiterung des Zugangs zu zeitnaher, genauer und personalisierter Diagnostik in verschiedenen Krankheitsbereichen spielen wird.
Marktdynamik der molekularen Diagnostik
Treiber
„Zunehmende ältere Bevölkerung“
- Die wachsende Zahl älterer Menschen ist ein wichtiger Wachstumstreiber auf dem globalen Markt für molekulare Diagnostik.
- Dieser demografische Wandel trägt zu einer höheren Inzidenz altersbedingter Erkrankungen wie Krebs, Herz-Kreislauf-Erkrankungen und neurodegenerativen Erkrankungen bei und treibt damit die Nachfrage nach frühzeitigen und präzisen Diagnoselösungen an.
- Da die alternde Bevölkerung häufigere Gesundheitsüberwachung und personalisierte Betreuung benötigt, bietet die molekulare Diagnostik nicht-invasive, schnelle und präzise Testmöglichkeiten, die sich für das Management chronischer Krankheiten und die präventive Gesundheitsversorgung eignen.
- Vorteile wie Früherkennung, gezielte Therapieführung und Echtzeit-Krankheitsverfolgung machen die molekulare Diagnostik zu einem unverzichtbaren Instrument in Strategien zur Altenpflege in allen Gesundheitssystemen.
- Anbieter von Diagnoselösungen reagieren darauf mit der Entwicklung benutzerfreundlicher, minimalinvasiver Plattformen, die auf die Bedürfnisse älterer Patienten zugeschnitten sind, und erweitern den Zugang durch Tests zu Hause und die Integration von Telemedizin.
Zum Beispiel,
- Roche und Abbott entwickeln molekulare Testverfahren zur Früherkennung von Krebs und Infektionskrankheiten weiter und gehen dabei insbesondere auf die diagnostischen Bedürfnisse älterer Menschen ein.
- Thermo Fisher Scientific erweitert seine Genomplattformen, um personalisierte Diagnostik für altersbedingte genetische Risiken zu unterstützen.
- Da die Weltbevölkerung immer älter wird und sich die Prioritäten im Gesundheitswesen hin zu Prävention und personalisierter Versorgung verlagern, wird erwartet, dass die Rolle der molekularen Diagnostik bei der Unterstützung langfristiger Gesundheitsergebnisse für ältere Erwachsene deutlich zunehmen wird.
Gelegenheit
„Steigende Nachfrage nach molekularer Diagnostik in der patientennahen Versorgung“
- Die steigende Nachfrage nach molekularer Diagnostik in patientennahen Sofortdiagnostiksystemen (Point-of-Care, POC) bietet ein erhebliches Potenzial für den Markt für molekulare Diagnostik. Durch die Ermöglichung schneller Tests vor Ort verbessern POC-Diagnostika die Zugänglichkeit, die Geschwindigkeit und die klinische Entscheidungsfindung in Echtzeit.
- Fortschritte bei tragbaren Technologien, benutzerfreundlichen Testformaten und integrierten Systemen von der Probenahme bis zum Ergebnis ermöglichen es Gesundheitsdienstleistern, in Umgebungen wie Kliniken, Notaufnahmen und abgelegenen Orten sofortige diagnostische Erkenntnisse zu liefern.
- Merkmale wie kompaktes Design, minimaler Probenbedarf und automatisierte Arbeitsabläufe werden genutzt, um eine schnellere Diagnose und einen rascheren Behandlungsbeginn zu unterstützen, insbesondere im Bereich der Infektionskrankheiten und der Überwachung chronischer Erkrankungen.
Zum Beispiel,
- Die Plattformen GeneXpert von Cepheid und ID NOW von Abbott werden in dezentralen Gesundheitseinrichtungen häufig für schnelle und genaue molekulare Tests eingesetzt.
- bioMérieux entwickelt kompakte molekulare Systeme, die darauf abzielen, die Diagnostik in Notfallambulanzen und ressourcenarmen Umgebungen zu optimieren .
- Da die globalen Gesundheitssysteme bestrebt sind, die Behandlungsergebnisse für Patienten zu verbessern, diagnostische Verzögerungen zu reduzieren und den Zugang zu qualitativ hochwertiger Versorgung zu erweitern, dürfte die kontinuierliche Weiterentwicklung der patientennahen molekularen Diagnostik neue Möglichkeiten sowohl in entwickelten als auch in aufstrebenden Märkten eröffnen.
Zurückhaltung/Herausforderung
„Zunehmende behördliche Genehmigungen“
- Die zunehmende Anzahl behördlicher Zulassungen und Compliance-Anforderungen stellt eine erhebliche Herausforderung für den Markt der molekularen Diagnostik dar. Zulassungen sind zwar unerlässlich, um Sicherheit und Wirksamkeit zu gewährleisten, doch die Komplexität und Variabilität globaler Zulassungsverfahren können die Produktentwicklung und den Markteintritt verlangsamen.
- Diese Herausforderung ist besonders ausgeprägt für Unternehmen, die innovative Diagnosetechnologien in mehreren Regionen einführen wollen, da sie unterschiedliche Standards, Dokumentationsanforderungen und Genehmigungsfristen berücksichtigen müssen.
- Langwierige Zulassungsverfahren können die Verfügbarkeit wichtiger Diagnoseinstrumente verzögern, die Entwicklungskosten erhöhen und Hürden für kleinere oder neu aufkommende Marktteilnehmer schaffen.
Zum Beispiel,
- Startups sehen sich bei der Beantragung der FDA- oder CE-Kennzeichnung für neuartige molekulare Testverfahren häufig mit langen Bearbeitungszeiten konfrontiert, was die Kommerzialisierungsstrategien behindern kann.
- Ohne optimierte regulatorische Verfahren und internationale Harmonisierung könnte der Markt für molekulare Diagnostik mit Verzögerungen bei der Einführung von Innovationen konfrontiert werden, was den zeitnahen Zugang zu fortschrittlichen Diagnoseverfahren einschränken und sich negativ auf die Patientenversorgung auswirken würde.
Marktumfang der molekularen Diagnostik
Der Markt ist segmentiert nach Produkten, Technologie, Anwendung und Endnutzer.
|
Segmentierung |
Untersegmentierung |
|
Nebenprodukte |
|
|
Durch Technologie |
|
|
Durch Bewerbung |
|
|
Vom Endbenutzer
|
|
Regionale Analyse des Marktes für molekulare Diagnostik
„ Nordamerika ist die dominierende Region auf dem Markt für molekulare Diagnostik .“
- Nordamerika dominiert den Markt für molekulare Diagnostik . Treiber dieser Entwicklung sind die gestiegenen Gesundheitsausgaben, die fortschrittliche medizinische Versorgung und ein etabliertes Gesundheitssystem, das Innovation und Zugänglichkeit fördert.
- Die USA halten einen bedeutenden Marktanteil aufgrund ihrer hohen Gesundheitsausgaben pro Kopf, der Vielzahl an Forschungseinrichtungen und Biotechnologieunternehmen sowie des weit verbreiteten Bewusstseins der Verbraucher für die Bedeutung der Früherkennung von Krankheiten und der personalisierten Medizin.
- Führende Unternehmen in Nordamerika treiben die Innovation mit diagnostischen Plattformen der nächsten Generation voran, indem sie künstliche Intelligenz, Fortschritte in der Molekularbiologie und Cloud-Technologien integrieren. Dies führt zu effizienteren, skalierbaren und präziseren Diagnoselösungen, die die Behandlungsergebnisse für Patienten und die Gesundheitsversorgung verbessern.
- Dank einer starken Infrastruktur, einer alternden Bevölkerung und einer steigenden Verbrauchernachfrage nach präzisionsmedizinischer Versorgung wird Nordamerika voraussichtlich seine Position als größter und fortschrittlichster Markt für molekulare Diagnostik im gesamten Prognosezeitraum von 2025 bis 2032 behaupten.
„ Für den asiatisch-pazifischen Raum wird die höchste Wachstumsrate prognostiziert .“
- Im asiatisch-pazifischen Raum wird voraussichtlich das höchste Wachstum im Markt für molekulare Diagnostik verzeichnet werden , angetrieben durch rasche demografische Veränderungen, eine alternde Bevölkerung und die zunehmende Verbreitung von Krankheiten wie Krebs und Infektionskrankheiten.
- Länder wie China, Indien und Japan führen das regionale Wachstum an, dank ihrer wachsenden Gesundheitsinfrastruktur, staatlicher Initiativen zur Verbesserung des Zugangs zur Gesundheitsversorgung und eines steigenden Bewusstseins für die Früherkennung von Krankheiten.
- Die Region erlebt zudem bedeutende Fortschritte in der Gesundheitstechnologie, darunter Telemedizin, Genomik und mobile Gesundheitsdiagnostik, was die Nachfrage nach fortschrittlichen molekulardiagnostischen Werkzeugen steigert, die in der Lage sind, große Patientenzahlen zu bewältigen und genaue sowie kostengünstige Tests zu ermöglichen.
- Mit der zunehmenden Digitalisierung des Gesundheitswesens, der staatlichen Förderung biotechnologischer Fortschritte und der wachsenden Verbreitung personalisierter Medizin positioniert sich der asiatisch-pazifische Raum als der am schnellsten wachsende regionale Markt für molekulare Diagnostik. Da sich die Gesundheitssysteme stetig weiterentwickeln, wird der asiatisch-pazifische Raum seinen Marktanteil von 2025 bis 2032 weiter ausbauen und sich zu einem wichtigen Zentrum für Innovationen und die Anwendung molekularer Diagnostik entwickeln.
Marktanteil der Molekulardiagnostik
Die Wettbewerbsanalyse bietet detaillierte Informationen zu jedem einzelnen Wettbewerber. Diese umfassen Unternehmensübersicht, Finanzkennzahlen, Umsatz, Marktpotenzial, Investitionen in Forschung und Entwicklung, neue Marktinitiativen, globale Präsenz, Produktionsstandorte und -anlagen, Produktionskapazitäten, Stärken und Schwächen des Unternehmens, Produkteinführungen, Produktportfolio und Anwendungsdominanz. Die genannten Datenpunkte beziehen sich ausschließlich auf den Fokus der Unternehmen auf den jeweiligen Markt.
Die wichtigsten Marktführer, die auf dem Markt tätig sind, sind:
- F. Hoffmann-La Roche AG (Schweiz)
- Hologic, Inc. (USA)
- bioMérieux SA (Frankreich)
- Abbott Laboratories (USA)
- QIAGEN NV (Niederlande)
- Thermo Fisher Scientific Inc. (USA)
- Siemens AG (Deutschland)
- Danaher Corporation (USA)
- Myriad Genetics, Inc. (USA)
- Illumina, Inc. (USA)
- Agilent Technologies, Inc. (USA)
- Becton, Dickinson and Company (BD) (USA)
- DiaSorin SpA (Italien)
- Grifols, SA (Spanien)
- QuidelOrtho Corporation (USA)
- Genetic Signatures Limited (Australien)
- MDxHealth SA (Belgien)
- Exact Sciences Corporation (USA)
- Biocartis Group NV (Belgien)
- TBG Diagnostics Limited (Australien)
- GenMark Diagnostics, Inc. (USA)
- Luminex Corporation (USA)
- HTG Molecular Diagnostics, Inc. (USA)
- Vela Diagnostics (Singapur)
- Amoy Diagnostics Co., Ltd. (China)
- Molbio Diagnostics Pvt. Ltd. (Indien)
- geneOmbio Technologies Pvt. Ltd. (Indien)
Neueste Entwicklungen auf dem globalen Markt für molekulare Diagnostik
- Roche schloss 2021 die Übernahme der TIB Molbiol Group ab. Die TIB Molbiol Group verfügt über rund 45 CE-IVD-zugelassene Tests für die Diagnostik erblicher genetischer Erkrankungen, Infektionskrankheiten, Transplantationsmedizin und hämatologischer Tests.
- Im Jahr 2020 führte Roche Diagnostics India die Cobas 8800 und Cobas 6800 am Nationalen Institut für Cholera und Enterische Erkrankungen in Kolkata ein, um die SARS-CoV-2-Diagnostik zu unterstützen. Die Roche Cobas 6800/8800 Systeme liefern Testergebnisse innerhalb von dreieinhalb Stunden und ermöglichen höhere betriebliche Effizienz, Flexibilität und schnellste Ergebnisse.
SKU-
Erhalten Sie Online-Zugriff auf den Bericht zur weltweit ersten Market Intelligence Cloud
- Interaktives Datenanalyse-Dashboard
- Unternehmensanalyse-Dashboard für Chancen mit hohem Wachstumspotenzial
- Zugriff für Research-Analysten für Anpassungen und Abfragen
- Konkurrenzanalyse mit interaktivem Dashboard
- Aktuelle Nachrichten, Updates und Trendanalyse
- Nutzen Sie die Leistungsfähigkeit der Benchmark-Analyse für eine umfassende Konkurrenzverfolgung
Inhaltsverzeichnis
1 EINLEITUNG
1.1 Ziele der Studie
1.2 MARKTDEFINITION
1.3 ÜBERBLICK ÜBER DEN GLOBALEN MARKT FÜR MOLEKULARE DIAGNOSTIK
1.4 WÄHRUNG UND PREISE
1.5 BESCHRÄNKUNG
1.6 ABGEDECKTE MÄRKTE
2. Marktsegmentierung
2.1 WICHTIGSTE ERKENNTNISSE
2.2 Erreichen der globalen Marktgröße für molekulare Diagnostik
2.2.1 Lieferantenpositionierungsraster
2.2.2 Technologie-Lebenszykluskurve
2.2.3 Datenvalidierungsmodell für Stativ
2.2.4 MARKTÜBERSICHT
2.2.5 Multivariate Modellierung
2.2.6 Analyse von oben nach unten
2.2.7 Herausforderungsmatrix
2.2.8 Anwendungsabdeckungsraster
2.2.9 MESSSTANDARDS
2.2.10 ANALYSE DER ANBIETERANTEILSVERHÄLTNISSE
2.2.11 Daten zum Absatzvolumen
2.2.12 DATENPUNKTE AUS WICHTIGEN PRIMÄRINTERVIEWS
2.2.13 DATENPUNKTE AUS WICHTIGEN SEKUNDÄRDATENBANKEN
2.3 GLOBALER MARKT FÜR MOLEKULARE DIAGNOSTIK: FORSCHUNGSÜBERSICHT
2.4 ANNAHMEN
3 MARKTÜBERSICHT
3.1 FAHRER
3.2 FESSELN
3.3 CHANCEN
3.4 HERAUSFORDERUNGEN
4. ZUSAMMENFASSUNG
5 PREMIUM-EINBLICKE
5.1 PESTEL-ANALYSE
5.2 Porters Fünf-Kräfte-Modell
6 Brancheneinblicke
6.1 Mikro- und makroökonomische Faktoren
6.2 Penetrations- und Wachstumspotenzialanalyse
6.3 WICHTIGSTE PREISSTRATEGIEN
6.4 Interviews mit Spezialisten
6.5 Analyse und Empfehlung
7. Portfolio für geistiges Eigentum (IP)
7.1 PATENTQUALITÄT UND -STÄRKE
7.2 Patentfamilien
7.3 LIZENZIERUNG UND KOOPERATIONEN
7.4 Wettbewerbsumfeld
7.5 IP-STRATEGIE UND -MANAGEMENT
7.6 SONSTIGES
8. KOSTENANALYSE AUFSCHLÜSSELUNG
9 TECHNOLOGIE-ROADMAP
10. Innovationstracker und strategische Analyse
10.1 Analyse wichtiger Transaktionen und strategischer Allianzen
10.1.1 Joint Ventures
10.1.2 Fusionen und Übernahmen
10.1.3 LIZENZIERUNG UND PARTNERSCHAFTEN
10.1.4 TECHNOLOGIE-KOOPERATIONEN
10.1.5 Strategische Desinvestitionen
10.2 ANZAHL DER IN ENTWICKLUNG ENTWICKELTEN PRODUKTE
10.3 Entwicklungsstadium
10.4 ZEITSTRAHL UND MEILENSTEINE
10.5 Innovationsstrategien und -methoden
10.6 Risikobewertung und Risikominderung
10.7 ZUKUNFTSAUSBLICK
11. Einhaltung gesetzlicher Bestimmungen
11.1 Aufsichtsbehörden
11.2 Regulatorische Klassifizierungen
11.2.1 Klasse I
11.2.2 Klasse II
11.2.3 Klasse III
11.3 Einreichungen bei den Aufsichtsbehörden
11.4 Internationale Harmonisierung
11.5 Compliance- und Qualitätsmanagementsysteme
11.6 Regulatorische Herausforderungen und Strategien
12. Erstattungsrahmen
13. Chancenkartenanalyse
14 INSTALLIERTE BASISDATEN
15 WERTKETTENANALYSE
16 GESUNDHEITSWESEN
16.1 Gesundheitsausgaben
16.2 Investitionsausgaben
16.3 Investitionstrends
16.4 Investitionszuweisung
16.5 Finanzierungsquellen
16.6 Branchen-Benchmarks
16,7 BIP-Verhältnis zum Gesamt-BIP
16.8 Struktur des Gesundheitssystems
16.9 Regierungspolitik
16.1 Wirtschaftliche Entwicklung
17. WELTWEITER MARKT FÜR MOLEKULARE DIAGNOSTIK, NACH PRODUKTEN UND DIENSTLEISTUNGEN
17.1 ÜBERSICHT
17.2 PRODUKT
17.2.1 INSTRUMENTE
17.2.1.1. NACH TYP
17.2.1.1.1. VOLLAUTOMATISIERT
17.2.1.1.2. Halbautomatisiert
17.2.1.1.3. HANDBUCH
17.2.1.2. NACH MODALITÄT
17.2.1.2.1. TRAGBAR
17.2.1.2.2. Standalone
17.2.1.2.3. BENCHTOP
17.2.2 Reagenzien und Kits
17.2.2.1. Bausätze
17.2.2.1.1. DNA-EXTRAKTIONS- UND REINIGUNGSKITS
17.2.2.1.1.1 PLASMID MINIPREP- UND MAXIPREP-KITS
17.2.2.1.1.2 PLASMID-REINIGUNGSSETS
17.2.2.1.1.3 PCR-Reinigungskits
17.2.2.1.1.4 Kits zur Reinigung genomischer DNA
17.2.2.1.1.5 ANDERE
17.2.2.1.2. RNAI UND RNA-REAGENZIEN
17.2.2.1.3. Nukleinsäure-Reinigungssets
17.2.2.1.4. Nukleinsäuresynthese-Kits, Puffer und Reagenzien
17.2.2.1.5. HPV-Kits
17.2.2.1.6. TB-Kits
17.2.2.1.7. Entleerungssets
17.2.2.1.8. ANDERE
17.2.2.2. QC-Sätze und -Panels
17.2.2.2.1. BEDIENFELD
17.2.2.2.1.1 MULTIPLEX-VAGINALBEDIENFELD
17.2.2.2.1.2 Bedienfeld für das humane Papillomavirus (HPV)
17.2.2.2.1.3 Bedienfeld für Candida vaginalis/Trichomonas vaginalis (CV/TV)
17.2.2.2.1.4 CT/NG-BEDIENFELD
17.2.2.2.1.5 Kontrollfeld für bakterielle Vaginose (BV)
17.2.2.2.1.6 Zellularitätskontrolle
17.2.2.2.1.7 Atemkontrollfeld
17.2.2.2.1.8 FLU/RSV/SARS-COV-2-KONTROLLFELD
17.2.2.2.1.8.1. NXG-BEDIENFELD
17.2.2.2.1.8.2. KOMPLETTES BEDIENFELD
17.2.2.2.1.8.3. ANDERE
17.2.2.2.1.9 MPN-Panel
17.2.2.2.1.10 AML-Panel
17.2.2.2.1.11 QC-Panel
17.2.2.2.1.12 ALL PANEL
17.2.2.2.1.13 VERIFIZIERUNGSFELD
17.2.2.2.1.14 ANDERE
17.2.2.3. MUTATIONSERKENNUNGSSET
17.2.2.3.1. KRAS-PCR-Kit
17.2.2.3.2. EGFR-Kit
17.2.2.3.3. BRAF-Mutationskit
17.2.2.3.4. AML1-ETO-KIT
17.2.2.3.5. NRAS-Mutationskit
17.2.2.3.6. CALR KIT
17.2.2.3.7. FLT3-Mutationserkennung
17.2.2.3.8. C-KIT MUTATIONSERKENNUNGSKIT
17.2.2.3.9. MGMT-METHYLATIONS-DETEKTIONSKIT
17.2.2.3.10. CBFB-MYH11 KIT
17.2.2.3.11. Genfusions-Nachweisset
17.2.2.3.12. ANDERE KITS UND BAUSATZBAUTEILE
17.2.2.4. ENZYME
17.2.2.4.1. POLYMERASEN
17.2.2.4.2. LIGASEN
17.2.2.4.3. Restriktionsendonukleasen
17.2.2.4.4. RÜCKWÄRTS-TRANSKRIPTASEN
17.2.2.4.5. PHOSPHATASEN
17.2.2.4.6. PROTEASEN UND PROTEINASEN
17.2.2.4.7. DNA-Leitern
17.2.2.4.8. ANDERE ENZYME
17.2.2.5. Puffer
17.2.2.6. GRUNDLAGEN
17.2.2.7. ANDERE
17.3 SOFTWARE UND DIENSTLEISTUNGEN
17.3.1 DIENSTLEISTUNGEN
17.3.1.1. Instrumentenreparaturdienste
17.3.1.1.1. Vor-Ort-Reparaturdienste
17.3.1.1.2. Reparaturdienste außerhalb des Betriebsgeländes
17.3.1.2. Schulungsdienste
17.3.1.2.1. PCR-basierte molekulare Diagnostik
17.3.1.2.2. IMMUNOHISTOCHEMIE (IHC)
17.3.1.2.3. VIRALBELASTUNGSTEST
17.3.1.2.4. Interphasen-Chromosomenprofilierung (ICP)
17.3.1.2.5. ANDERE
17.3.1.3. Compliance-Dienstleistungen
17.3.1.3.1. IQ/OQ- und PM/OQ-Dienstleistungen
17.3.1.3.2. INSTALLATIONSDIENSTLEISTUNGEN
17.3.1.3.3. Validierungsdienste
17.3.1.3.4. SONSTIGE DIENSTLEISTUNGEN
17.3.1.4. SKALIERBARE AUTOMATISIERUNGSDIENSTE
17.3.1.4.1. AUTOMATISIERUNG FÜR DAS HIGH-CONTENT-SCREENING (HCS)
17.3.1.4.2. AUTOMATISIERUNG FÜR HOCHDURCHSATZ-PLATTENBASIERTE ASSAYS
17.3.1.4.3. AUTOMATISIERUNG FÜR DAS HOCHDURCHSATZ-KLON-SCREENING
17.3.1.5. KALIBRIERUNGSDIENSTE
17.3.1.6. Wartungsdienste
17.3.1.7. INSTRUMENTENUMZUGSDIENSTLEISTUNGEN
17.3.1.7.1. Kennzeichenerneuerung
17.3.1.7.2. Vom Hersteller freigegebene Teile
17.3.1.7.3. LEISTUNGSBEWERTUNG DER INSTRUMENTE
17.3.1.7.4. SONSTIGE DIENSTLEISTUNGEN
17.3.1.8. Hardware-Anpassung
17.3.1.9. LEISTUNGSSICHERUNGSDIENSTLEISTUNGEN
17.3.1.10. DESIGN- UND ENTWICKLUNGSDIENSTLEISTUNGEN
17.3.1.11. LÖSUNGEN FÜR DIE LIEFERKETTE
17.3.1.12. KLINISCHE FORSCHUNGSDIENSTE
17.3.1.13. SONSTIGE DIENSTLEISTUNGEN
17.3.2 SOFTWARE
17.3.2.1. NACH TYP
17.3.2.1.1. INTEGRIERT
17.3.2.1.2. STANDALONE
17.3.2.2. DURCH EINSATZ
17.3.2.2.1. WOLKENBASEN
17.3.2.2.2. VOR ORT
17.3.2.2.3. HYBRID
18. WELTWEITER MARKT FÜR MOLEKULARE DIAGNOSTIK, NACH TECHNOLOGIE
18.1 ÜBERSICHT
18.2 Polymerase-Kettenreaktion (PCR)
18.2.1 NACH TYP
18.2.1.1. Echtzeit-PCR
18.2.1.2. Digitale PCR
18.2.1.3. Reverse-Transkriptase-PCR
18.2.1.4. Quantitative Fluoreszenz-PCR
18.2.1.5. Kalt-PCR
18.2.1.6. ANDERE
18.2.2 NACH PRODUKTEN UND DIENSTLEISTUNGEN
18.2.2.1. PRODUKT
18.2.2.2. DIENSTLEISTUNGEN UND SOFTWARE
18.3 ISOTHERMALE NUKLEINSÄURE-AMPLIFIKATIONSTECHNOLOGIE (INAAT)
18.3.1 NACH PRODUKTEN UND DIENSTLEISTUNGEN
18.3.1.1. PRODUKT
18.3.1.2. DIENSTLEISTUNGEN UND SOFTWARE
18.4 Sequenzierung der nächsten Generation (NGS)
18.4.1 NACH PRODUKTEN UND DIENSTLEISTUNGEN
18.4.1.1. PRODUKT
18.4.1.2. DIENSTLEISTUNGEN UND SOFTWARE
18.5 Zytogenetik
18.5.1 NACH PRODUKTEN UND DIENSTLEISTUNGEN
18.5.1.1. PRODUKT
18.5.1.2. DIENSTLEISTUNGEN UND SOFTWARE
18.6 Kapillarelektrophorese
18.6.1 NACH PRODUKTEN UND DIENSTLEISTUNGEN
18.6.1.1. PRODUKT
18.6.1.2. DIENSTLEISTUNGEN UND SOFTWARE
18.7 In-situ-Hybridisierung (ISH oder FISH)
18.7.1 NACH PRODUKTEN UND DIENSTLEISTUNGEN
18.7.1.1. PRODUKT
18.7.1.2. DIENSTLEISTUNGEN UND SOFTWARE
18.8 Molekulare Bildgebung
18.8.1 NACH TYP
18.8.1.1. Optische Bildgebung
18.8.1.2. FDG-PET
18.8.1.3. ANDERE
18.8.2 NACH PRODUKTEN UND DIENSTLEISTUNGEN
18.8.2.1. PRODUKT
18.8.2.2. DIENSTLEISTUNGEN UND SOFTWARE
18.9 MASSENSPEZTROMETRIE (MS)
18.9.1 NACH PRODUKTEN UND DIENSTLEISTUNGEN
18.9.1.1. PRODUKT
18.9.1.2. DIENSTLEISTUNGEN UND SOFTWARE
18.1 CHIPS UND MIKROARRAY
18.10.1 NACH PRODUKTEN UND DIENSTLEISTUNGEN
18.10.1.1. PRODUKT
18.10.1.2. DIENSTLEISTUNGEN UND SOFTWARE
18.11 ANDERE
19. WELTWEITER MARKT FÜR MOLEKULARE DIAGNOSTIK, NACH ANWENDUNG
19.1 ÜBERSICHT
19.2 Onkologische Tests
19.2.1 Onkologie, nach Krebsart
19.2.1.1. BRUSTKREBS
19.2.1.1.1. MARKTWERT (MILLIONEN USD)
19.2.1.1.2. Marktvolumen (Anzahl der Tests)
19.2.1.1.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.2.1.2. Darmkrebs
19.2.1.2.1. MARKTWERT (MILLIONEN USD)
19.2.1.2.2. Marktvolumen (Anzahl der Tests)
19.2.1.2.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.2.1.3. LUNGENKREBS
19.2.1.3.1. MARKTWERT (MILLIONEN USD)
19.2.1.3.2. Marktvolumen (Anzahl der Tests)
19.2.1.3.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.2.1.4. Prostatakrebs
19.2.1.4.1. MARKTWERT (MILLIONEN USD)
19.2.1.4.2. Marktvolumen (Anzahl der Tests)
19.2.1.4.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.2.1.5. ANDERE
19.2.2 Onkologie durch Technologie
19.2.2.1. POLYMERASE-KETTENREAKTION (PCR)
19.2.2.1.1. MARKTWERT (MILLIONEN USD)
19.2.2.1.2. Marktvolumen (Anzahl der Tests)
19.2.2.1.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.2.2.2. ISOTHERMALE NUKLEINSÄURE-AMPLIFIKATIONSTECHNOLOGIE (INAAT)
19.2.2.2.1. MARKTWERT (MILLIONEN USD)
19.2.2.2.2. Marktvolumen (Anzahl der Tests)
19.2.2.2.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.2.2.3. Sequenzierung der nächsten Generation (NGS)
19.2.2.3.1. MARKTWERT (MILLIONEN USD)
19.2.2.3.2. Marktvolumen (Anzahl der Tests)
19.2.2.3.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.2.2.4. Zytogenetik
19.2.2.4.1. MARKTWERT (MILLIONEN USD)
19.2.2.4.2. Marktvolumen (Anzahl der Tests)
19.2.2.4.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.2.2.5. Kapillarelektrophorese
19.2.2.5.1. MARKTWERT (MILLIONEN USD)
19.2.2.5.2. Marktvolumen (Anzahl der Tests)
19.2.2.5.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.2.2.6. In-situ-Hybridisierung (ISH oder FISH)
19.2.2.6.1. MARKTWERT (MILLIONEN USD)
19.2.2.6.2. Marktvolumen (Anzahl der Tests)
19.2.2.6.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.2.2.7. MOLEKULARE BILDGEBUNG
19.2.2.7.1. MARKTWERT (MILLIONEN USD)
19.2.2.7.2. Marktvolumen (Anzahl der Tests)
19.2.2.7.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.2.2.8. MASSENSPEZTROMETRIE (MS)
19.2.2.8.1. MARKTWERT (MILLIONEN USD)
19.2.2.8.2. Marktvolumen (Anzahl der Tests)
19.2.2.8.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.2.2.9. CHIPS UND MIKROARRAY
19.2.2.9.1. MARKTWERT (MILLIONEN USD)
19.2.2.9.2. Marktvolumen (Anzahl der Tests)
19.2.2.9.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.2.2.10. ANDERE
19.3 Pharmakogenomik
19.3.1 Polymerase-Kettenreaktion (PCR)
19.3.1.1. MARKTWERT (MILLIONEN USD)
19.3.1.2. Marktvolumen (Anzahl der Tests)
19.3.1.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.3.2 ISOTHERMALE NUKLEINSÄURE-AMPLIFIKATIONSTECHNOLOGIE (INAAT)
19.3.2.1. MARKTWERT (MILLIONEN USD)
19.3.2.2. Marktvolumen (Anzahl der Tests)
19.3.2.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.3.3 Sequenzierung der nächsten Generation (NGS)
19.3.3.1. MARKTWERT (MILLIONEN USD)
19.3.3.2. Marktvolumen (Anzahl der Tests)
19.3.3.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.3.4 Zytogenetik
19.3.4.1. MARKTWERT (MILLIONEN USD)
19.3.4.2. Marktvolumen (Anzahl der Tests)
19.3.4.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.3.5 Kapillarelektrophorese
19.3.5.1. MARKTWERT (MILLIONEN USD)
19.3.5.2. Marktvolumen (Anzahl der Tests)
19.3.5.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.3.6 In-situ-Hybridisierung (ISH oder FISH)
19.3.6.1. MARKTWERT (MILLIONEN USD)
19.3.6.2. Marktvolumen (Anzahl der Tests)
19.3.6.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.3.7 MOLEKULARE BILDGEBUNG
19.3.7.1. MARKTWERT (MILLIONEN USD)
19.3.7.2. Marktvolumen (Anzahl der Tests)
19.3.7.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.3.8 MASSENSPEZTROMETRIE (MS)
19.3.8.1. MARKTWERT (MILLIONEN USD)
19.3.8.2. Marktvolumen (Anzahl der Tests)
19.3.8.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.3.9 CHIPS UND MIKROARRAY
19.3.9.1. MARKTWERT (MILLIONEN USD)
19.3.9.2. Marktvolumen (Anzahl der Tests)
19.3.9.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.3.10 ANDERE
19.4 Mikrobiologie
19.4.1 POLYMERASE-KETTENREAKTION (PCR)
19.4.1.1. MARKTWERT (MILLIONEN USD)
19.4.1.2. Marktvolumen (Anzahl der Tests)
19.4.1.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.4.2 ISOTHERMALE NUKLEINSÄURE-AMPLIFIKATIONSTECHNOLOGIE (INAAT)
19.4.2.1. MARKTWERT (MILLIONEN USD)
19.4.2.2. Marktvolumen (Anzahl der Tests)
19.4.2.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.4.3 Sequenzierung der nächsten Generation (NGS)
19.4.3.1. MARKTWERT (MILLIONEN USD)
19.4.3.2. Marktvolumen (Anzahl der Tests)
19.4.3.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.4.4 Zytogenetik
19.4.4.1. MARKTWERT (MILLIONEN USD)
19.4.4.2. Marktvolumen (Anzahl der Tests)
19.4.4.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.4.5 Kapillarelektrophorese
19.4.5.1. MARKTWERT (MILLIONEN USD)
19.4.5.2. Marktvolumen (Anzahl der Tests)
19.4.5.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.4.6 In-situ-Hybridisierung (ISH oder FISH)
19.4.6.1. MARKTWERT (MILLIONEN USD)
19.4.6.2. Marktvolumen (Anzahl der Tests)
19.4.6.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.4.7 MOLEKULARE BILDGEBUNG
19.4.7.1. MARKTWERT (MILLIONEN USD)
19.4.7.2. Marktvolumen (Anzahl der Tests)
19.4.7.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.4.8 MASSENSPEZTROMETRIE (MS)
19.4.8.1. MARKTWERT (MILLIONEN USD)
19.4.8.2. Marktvolumen (Anzahl der Tests)
19.4.8.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.4.9 CHIPS UND MIKROARRAY
19.4.9.1. MARKTWERT (MILLIONEN USD)
19.4.9.2. Marktvolumen (Anzahl der Tests)
19.4.9.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.4.10 ANDERE
19.5 PRÄNATALTESTS
19.5.1 Sichelzellanämie
19.5.1.1. MARKTWERT (MILLIONEN USD)
19.5.1.2. Marktvolumen (Anzahl der Tests)
19.5.1.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.5.2 Zystische Fibrose
19.5.2.1. MARKTWERT (MILLIONEN USD)
19.5.2.2. Marktvolumen (Anzahl der Tests)
19.5.2.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.5.3 Tay-Sachs-Krankheit
19.5.3.1. MARKTWERT (MILLIONEN USD)
19.5.3.2. Marktvolumen (Anzahl der Tests)
19.5.3.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.5.4 ANDERE
19.6 Gewebetypisierungstest
19.6.1 POLYMERASE-KETTENREAKTION (PCR)
19.6.1.1. MARKTWERT (MILLIONEN USD)
19.6.1.2. Marktvolumen (Anzahl der Tests)
19.6.1.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.6.2 ISOTHERMALE NUKLEINSÄURE-AMPLIFIKATIONSTECHNOLOGIE (INAAT)
19.6.2.1. MARKTWERT (MILLIONEN USD)
19.6.2.2. Marktvolumen (Anzahl der Tests)
19.6.2.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.6.3 Sequenzierung der nächsten Generation (NGS)
19.6.3.1. MARKTWERT (MILLIONEN USD)
19.6.3.2. Marktvolumen (Anzahl der Tests)
19.6.3.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.6.4 Zytogenetik
19.6.4.1. MARKTWERT (MILLIONEN USD)
19.6.4.2. Marktvolumen (Anzahl der Tests)
19.6.4.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.6.5 Kapillarelektrophorese
19.6.5.1. MARKTWERT (MILLIONEN USD)
19.6.5.2. Marktvolumen (Anzahl der Tests)
19.6.5.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.6.6 In-situ-Hybridisierung (ISH oder FISH)
19.6.6.1. MARKTWERT (MILLIONEN USD)
19.6.6.2. Marktvolumen (Anzahl der Tests)
19.6.6.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.6.7 MOLEKULARE BILDGEBUNG
19.6.7.1. MARKTWERT (MILLIONEN USD)
19.6.7.2. Marktvolumen (Anzahl der Tests)
19.6.7.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.6.8 MASSENSPEZTROMETRIE (MS)
19.6.8.1. MARKTWERT (MILLIONEN USD)
19.6.8.2. Marktvolumen (Anzahl der Tests)
19.6.8.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.6.9 CHIPS UND MIKROARRAY
19.6.9.1. MARKTWERT (MILLIONEN USD)
19.6.9.2. Marktvolumen (Anzahl der Tests)
19.6.9.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.6.10 ANDERE
19.7 Blutuntersuchung
19.7.1 Polymerase-Kettenreaktion (PCR)
19.7.1.1. MARKTWERT (MILLIONEN USD)
19.7.1.2. Marktvolumen (Anzahl der Tests)
19.7.1.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.7.2 ISOTHERMALE NUKLEINSÄURE-AMPLIFIKATIONSTECHNOLOGIE (INAAT)
19.7.2.1. MARKTWERT (MILLIONEN USD)
19.7.2.2. Marktvolumen (Anzahl der Tests)
19.7.2.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.7.3 Sequenzierung der nächsten Generation (NGS)
19.7.3.1. MARKTWERT (MILLIONEN USD)
19.7.3.2. Marktvolumen (Anzahl der Tests)
19.7.3.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.7.4 Zytogenetik
19.7.4.1. MARKTWERT (MILLIONEN USD)
19.7.4.2. Marktvolumen (Anzahl der Tests)
19.7.4.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.7.5 Kapillarelektrophorese
19.7.5.1. MARKTWERT (MILLIONEN USD)
19.7.5.2. Marktvolumen (Anzahl der Tests)
19.7.5.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.7.6 In-situ-Hybridisierung (ISH oder FISH)
19.7.6.1. MARKTWERT (MILLIONEN USD)
19.7.6.2. Marktvolumen (Anzahl der Tests)
19.7.6.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.7.7 MOLEKULARE BILDGEBUNG
19.7.7.1. MARKTWERT (MILLIONEN USD)
19.7.7.2. Marktvolumen (Anzahl der Tests)
19.7.7.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.7.8 MASSENSPEZTROMETRIE (MS)
19.7.8.1. MARKTWERT (MILLIONEN USD)
19.7.8.2. Marktvolumen (Anzahl der Tests)
19.7.8.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.7.9 CHIPS UND MIKROARRAY
19.7.9.1. MARKTWERT (MILLIONEN USD)
19.7.9.2. Marktvolumen (Anzahl der Tests)
19.7.9.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.7.10 ANDERE
19.8 TESTUNG VON HERZ-KREISLAUF-ERKRANKUNGEN
19.8.1 POLYMERASE-KETTENREAKTION (PCR)
19.8.1.1. MARKTWERT (MILLIONEN USD)
19.8.1.2. Marktvolumen (Anzahl der Tests)
19.8.1.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.8.2 ISOTHERMALE NUKLEINSÄURE-AMPLIFIKATIONSTECHNOLOGIE (INAAT)
19.8.2.1. MARKTWERT (MILLIONEN USD)
19.8.2.2. Marktvolumen (Anzahl der Tests)
19.8.2.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.8.3 Sequenzierung der nächsten Generation (NGS)
19.8.3.1. MARKTWERT (MILLIONEN USD)
19.8.3.2. Marktvolumen (Anzahl der Tests)
19.8.3.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.8.4 Zytogenetik
19.8.4.1. MARKTWERT (MILLIONEN USD)
19.8.4.2. Marktvolumen (Anzahl der Tests)
19.8.4.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.8.5 Kapillarelektrophorese
19.8.5.1. MARKTWERT (MILLIONEN USD)
19.8.5.2. Marktvolumen (Anzahl der Tests)
19.8.5.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.8.6 In-situ-Hybridisierung (ISH oder FISH)
19.8.6.1. MARKTWERT (MILLIONEN USD)
19.8.6.2. Marktvolumen (Anzahl der Tests)
19.8.6.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.8.7 MOLEKULARE BILDGEBUNG
19.8.7.1. MARKTWERT (MILLIONEN USD)
19.8.7.2. Marktvolumen (Anzahl der Tests)
19.8.7.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.8.8 MASSENSPEZTROMETRIE (MS)
19.8.8.1. MARKTWERT (MILLIONEN USD)
19.8.8.2. Marktvolumen (Anzahl der Tests)
19.8.8.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.8.9 CHIPS UND MIKROARRAY
19.8.9.1. MARKTWERT (MILLIONEN USD)
19.8.9.2. Marktvolumen (Anzahl der Tests)
19.8.9.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.8.10 ANDERE
19.9 Tests auf neurologische Erkrankungen
19.9.1 Polymerase-Kettenreaktion (PCR)
19.9.1.1. MARKTWERT (MILLIONEN USD)
19.9.1.2. Marktvolumen (Anzahl der Tests)
19.9.1.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.9.2 ISOTHERMALE NUKLEINSÄURE-AMPLIFIKATIONSTECHNOLOGIE (INAAT)
19.9.2.1. MARKTWERT (MILLIONEN USD)
19.9.2.2. Marktvolumen (Anzahl der Tests)
19.9.2.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.9.3 Sequenzierung der nächsten Generation (NGS)
19.9.3.1. MARKTWERT (MILLIONEN USD)
19.9.3.2. Marktvolumen (Anzahl der Tests)
19.9.3.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.9.4 Zytogenetik
19.9.4.1. MARKTWERT (MILLIONEN USD)
19.9.4.2. Marktvolumen (Anzahl der Tests)
19.9.4.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.9.5 Kapillarelektrophorese
19.9.5.1. MARKTWERT (MILLIONEN USD)
19.9.5.2. Marktvolumen (Anzahl der Tests)
19.9.5.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.9.6 In-situ-Hybridisierung (ISH oder FISH)
19.9.6.1. MARKTWERT (MILLIONEN USD)
19.9.6.2. Marktvolumen (Anzahl der Tests)
19.9.6.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.9.7 MOLEKULARE BILDGEBUNG
19.9.7.1. MARKTWERT (MILLIONEN USD)
19.9.7.2. Marktvolumen (Anzahl der Tests)
19.9.7.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.9.8 MASSENSPEZTROMETRIE (MS)
19.9.8.1. MARKTWERT (MILLIONEN USD)
19.9.8.2. Marktvolumen (Anzahl der Tests)
19.9.8.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.9.9 CHIPS UND MICROARRAY
19.9.9.1. MARKTWERT (MILLIONEN USD)
19.9.9.2. Marktvolumen (Anzahl der Tests)
19.9.9.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.9.10 ANDERE
19.1 Tests auf Infektionskrankheiten
19.10.1 NACH TYP
19.10.1.1. COVID-19
19.10.1.1.1. MARKTWERT (MILLIONEN USD)
19.10.1.1.2. Marktvolumen (Anzahl der Tests)
19.10.1.1.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.10.1.2. Hepatitis
19.10.1.2.1. MARKTWERT (MILLIONEN USD)
19.10.1.2.2. Marktvolumen (Anzahl der Tests)
19.10.1.2.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.10.1.3. HIV
19.10.1.3.1. MARKTWERT (MILLIONEN USD)
19.10.1.3.2. Marktvolumen (Anzahl der Tests)
19.10.1.3.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.10.1.4. CT/NG
19.10.1.4.1. MARKTWERT (MILLIONEN USD)
19.10.1.4.2. Marktvolumen (Anzahl der Tests)
19.10.1.4.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.10.1.5. HAI
19.10.1.5.1. MARKTWERT (MILLIONEN USD)
19.10.1.5.2. Marktvolumen (Anzahl der Tests)
19.10.1.5.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.10.1.6. HPV
19.10.1.6.1. MARKTWERT (MILLIONEN USD)
19.10.1.6.2. Marktvolumen (Anzahl der Tests)
19.10.1.6.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.10.1.7. TUBERKULOSE
19.10.1.7.1. MARKTWERT (MILLIONEN USD)
19.10.1.7.2. Marktvolumen (Anzahl der Tests)
19.10.1.7.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.10.1.8. Grippe
19.10.1.8.1. MARKTWERT (MILLIONEN USD)
19.10.1.8.2. Marktvolumen (Anzahl der Tests)
19.10.1.8.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.10.1.9. Vektorübertragene Krankheit
19.10.1.9.1. MALERIE
19.10.1.9.1.1 MARKTWERT (MILLIONEN USD)
19.10.1.9.1.2 Marktvolumen (Anzahl der Tests)
19.10.1.9.1.3 DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.10.1.9.2. DENGUE
19.10.1.9.2.1 MARKTWERT (MILLIONEN USD)
19.10.1.9.2.2 Marktvolumen (Anzahl der Tests)
19.10.1.9.2.3 DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.10.1.9.3. ZIKA-VIRUS
19.10.1.9.3.1 MARKTWERT (MILLIONEN USD)
19.10.1.9.3.2 Marktvolumen (Anzahl der Tests)
19.10.1.9.3.3 DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.10.1.9.4. ANDERE
19.10.2 DURCH TECHNOLOGIE
19.10.2.1. POLYMERASE-KETTENREAKTION (PCR)
19.10.2.1.1. MARKTWERT (MILLIONEN USD)
19.10.2.1.2. Marktvolumen (Anzahl der Tests)
19.10.2.1.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.10.2.2. ISOTHERMALE NUKLEINSÄURE-AMPLIFIKATIONSTECHNOLOGIE (INAAT)
19.10.2.2.1. MARKTWERT (MILLIONEN USD)
19.10.2.2.2. Marktvolumen (Anzahl der Tests)
19.10.2.2.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.10.2.3. Sequenzierung der nächsten Generation (NGS)
19.10.2.3.1. MARKTWERT (MILLIONEN USD)
19.10.2.3.2. Marktvolumen (Anzahl der Tests)
19.10.2.3.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.10.2.4. Zytogenetik
19.10.2.4.1. MARKTWERT (MILLIONEN USD)
19.10.2.4.2. Marktvolumen (Anzahl der Tests)
19.10.2.4.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.10.2.5. Kapillarelektrophorese
19.10.2.5.1. MARKTWERT (MILLIONEN USD)
19.10.2.5.2. Marktvolumen (Anzahl der Tests)
19.10.2.5.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.10.2.6. In-situ-Hybridisierung (ISH oder FISH)
19.10.2.6.1. MARKTWERT (MILLIONEN USD)
19.10.2.6.2. Marktvolumen (Anzahl der Tests)
19.10.2.6.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.10.2.7. MOLEKULARE BILDGEBUNG
19.10.2.7.1. MARKTWERT (MILLIONEN USD)
19.10.2.7.2. Marktvolumen (Anzahl der Tests)
19.10.2.7.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.10.2.8. MASSENSPEZTROMETRIE (MS)
19.10.2.8.1. MARKTWERT (MILLIONEN USD)
19.10.2.8.2. Marktvolumen (Anzahl der Tests)
19.10.2.8.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.10.2.9. CHIPS UND MIKROARRAY
19.10.2.9.1. MARKTWERT (MILLIONEN USD)
19.10.2.9.2. Marktvolumen (Anzahl der Tests)
19.10.2.9.3. DURCHSCHNITTLICHE TESTKOSTEN (USD)
19.10.2.10. ANDERE
19.11 ANDERE
20 GLOBALER MARKT FÜR MOLEKULARE DIAGNOSTIK, NACH TESTSTANDORT
20.1 ÜBERSICHT
20.2 Laborbasiert
20.3 Point-of-Care-Tests
21. WELTWEITER MARKT FÜR MOLEKULARE DIAGNOSTIK, NACH ENDVERBRAUCHER
21.1 ÜBERSICHT
21.2 KRANKENHÄUSER UND KERNLABITALE
21.3 ALTERNATIVE KRANKENHAUSSTANDORTE
21.3.1 KLINIKEN
21.3.2 Referenzlaboratorien
21.3.3 DIAGNOSTISCHE ZENTREN
21.3.4 AKADEMISCHE UND FORSCHUNGSEINRICHTUNGEN
21.3.5 ANDERE
21.4 DEZENTRALE TESTSTANDORTE
21.4.1 DEZENTRALISIERTE KLINISCHE LABORE
21.4.2 APOTHEKEN
21.4.3 Häusliche Pflege
21,5 ANDERE
22. WELTWEITER MARKT FÜR MOLEKULARE DIAGNOSTIK, NACH VERTRIEBSKANAL
22.1 ÜBERSICHT
22.2 Direktausschreibungen
22.3 Einzelhandelsumsätze
22.3.1 ONLINE-VERKÄUFE
22.3.2 OFFLINE-VERKÄUFE
22.4 ANDERE
23. WELTWEITER MARKT FÜR MOLEKULARE DIAGNOSTIK, NACH LÄNDERN
WELTWEITER MARKT FÜR MOLEKULARE DIAGNOSTIK (ALLE OBEN ANGEGEBENEN SEGMENTIERUNGEN WERDEN IN DIESEM KAPITEL NACH LÄNDERN DARGESTELLT)
23.1 NORDAMERIKA
23.1.1 US
23.1.2 KANADA
23.1.3 MEXIKO
23.2 EUROPA
23.2.1 DEUTSCHLAND
23.2.2 FRANKREICH
23.2.3 Vereinigtes Königreich
23.2.4 ITALIEN
23.2.5 SPANIEN
23.2.6 RUSSLAND
23.2.7 Türkei
23.2.8 BELGIEN
23.2.9 NIEDERLANDE
23.2.10 SCHWEIZ
23.2.11 Übriges Europa
23.3 ASIEN-PAZIFIK
23.3.1 JAPAN
23.3.2 CHINA
23.3.3 SÜDKOREA
23.3.4 INDIEN
23.3.5 AUSTRALIEN
23.3.6 SINGAPUR
23.3.7 THAILAND
23.3.8 MALAYSIA
23.3.9 INDONESIEN
23.3.10 PHILIPPINEN
23.3.11 ÜBRIGES ASIEN-PAZIFIK
23.4 SÜDAMERIKA
23.4.1 BRASILIEN
23.4.2 ARGENTINIEN
23.4.3 PERU
23.4.4 CHILE
23.4.5 KOLUMBIEN
23.4.6 VENEZUELA
23.4.7 RESTLICHES SÜDAMERIKA
23.5 MITTLERER OSTEN UND AFRIKA
23.5.1 SÜDAFRIKA
23.5.2 SAUDI-ARABIEN
23.5.3 VAE
23.5.4 ÄGYPTEN
23.5.5 ISRAEL
23.5.6 Übriger Naher Osten und Afrika
23.6 WICHTIGSTE ERGEBNISSE: NACH WICHTIGEN LÄNDERN
24. Globaler Markt für die Behandlung von Atemwegserkrankungen bei Schweinen und Geflügel, Unternehmenslandschaft
24.1 UNTERNEHMENSAKTIENANALYSE: WELTWEIT
24.2 AKTIENANALYSE: NORDAMERIKA
24.3 AKTIENANALYSE: EUROPA
24.4 AKTIENANALYSE: ASIEN-PAZIFIK
24.5 Fusionen und Übernahmen
24.6 PRODUKTENTWICKLUNG & ZULASSUNGEN
24.7 ERWEITERUNGEN
24.8 RECHTLICHE ÄNDERUNGEN
24.9 Partnerschaften und andere strategische Entwicklungen
25 GLOBALER MARKT FÜR MOLEKULARE DIAGNOSTIK, UNTERNEHMENSLANDSCHAFT
25.1 AKTIENANALYSE: ASIEN-PAZIFIK
25.2 Fusionen und Übernahmen
25.3 PRODUKTENTWICKLUNG & ZULASSUNGEN
25.4 ERWEITERUNGEN
25.5 RECHTLICHE ÄNDERUNGEN
25.6 Partnerschaften und andere strategische Entwicklungen
26. Globaler Markt für molekulare Diagnostik: SWOT- und DBMR-Analyse
27. WELTWEITER MARKT FÜR MOLEKULARE DIAGNOSTIK, UNTERNEHMENSPROFIL
27.1 ABBOTT
27.1.1 Unternehmensübersicht
27.1.2 Umsatzanalyse
27.1.3 GEOGRAFISCHE PRÄSENZ
27.1.4 PRODUKTPORTFOLIO
27.1.5 Aktuelle Entwicklungen
27.2 SIEMENS HEALTHCARE PRIVATE LIMITED
27.2.1 Unternehmensübersicht
27.2.2 Umsatzanalyse
27.2.3 GEOGRAFISCHE PRÄSENZ
27.2.4 PRODUKTPORTFOLIO
27.2.5 Aktuelle Entwicklungen
27.3 THERMO FISHER SCIENTIFIC INC.
27.3.1 Unternehmensübersicht
27.3.2 Umsatzanalyse
27.3.3 GEOGRAFISCHE PRÄSENZ
27.3.4 PRODUKTPORTFOLIO
27.3.5 Aktuelle Entwicklungen
27,4 BD
27.4.1 Unternehmensübersicht
27.4.2 Umsatzanalyse
27.4.3 GEOGRAFISCHE PRÄSENZ
27.4.4 PRODUKTPORTFOLIO
27.4.5 Aktuelle Entwicklungen
27.5 BIOMÉRIEUX SA
27.5.1 Unternehmensübersicht
27.5.2 Umsatzanalyse
27.5.3 GEOGRAFISCHE PRÄSENZ
27.5.4 PRODUKTPORTFOLIO
27.5.5 Aktuelle Entwicklungen
27.6 DANAHER CORPORATION
27.6.1 Unternehmensübersicht
27.6.2 Umsatzanalyse
27.6.3 GEOGRAFISCHE PRÄSENZ
27.6.4 PRODUKTPORTFOLIO
27.6.5 Aktuelle Entwicklungen
27.7 HOLOGIC, INC.
27.7.1 Unternehmensübersicht
27.7.2 Umsatzanalyse
27.7.3 GEOGRAFISCHE PRÄSENZ
27.7.4 PRODUKTPORTFOLIO
27.7.5 Aktuelle Entwicklungen
27.8 MYRIAD GENETICS, INC.
27.8.1 Unternehmensübersicht
27.8.2 Umsatzanalyse
27.8.3 GEOGRAFISCHE PRÄSENZ
27.8.4 PRODUKTPORTFOLIO
27.8.5 Aktuelle Entwicklungen
27.9 QIAGEN
27.9.1 UNTERNEHMENSÜBERSICHT
27.9.2 Umsatzanalyse
27.9.3 GEOGRAFISCHE PRÄSENZ
27.9.4 PRODUKTPORTFOLIO
27.9.5 Aktuelle Entwicklungen
27.1 AGILENT TECHNOLOGIES, INC.
27.10.1 UNTERNEHMENSÜBERSICHT
27.10.2 Umsatzanalyse
27.10.3 GEOGRAFISCHE PRÄSENZ
27.10.4 PRODUKTPORTFOLIO
27.10.5 Aktuelle Entwicklungen
27.11 QUIDEL CORPORATION.
27.11.1 UNTERNEHMENSÜBERSICHT
27.11.2 Umsatzanalyse
27.11.3 GEOGRAFISCHE PRÄSENZ
27.11.4 PRODUKTPORTFOLIO
27.11.5 Aktuelle Entwicklungen
27.12 BIO-RAD LABORATORIES, INC.
27.12.1 Unternehmensübersicht
27.12.2 Umsatzanalyse
27.12.3 GEOGRAFISCHE PRÄSENZ
27.12.4 PRODUKTPORTFOLIO
27.12.5 Aktuelle Entwicklungen
27.13 ILLUMINA, INC.
27.13.1 UNTERNEHMENSÜBERSICHT
27.13.2 Umsatzanalyse
27.13.3 GEOGRAFISCHE PRÄSENZ
27.13.4 PRODUKTPORTFOLIO
27.13.5 Aktuelle Entwicklungen
27.14 IMMUCOR (WERFEN, SA)
27.14.1 UNTERNEHMENSÜBERSICHT
27.14.2 Umsatzanalyse
27.14.3 GEOGRAFISCHE PRÄSENZ
27.14.4 PRODUKTPORTFOLIO
27.14.5 Aktuelle Entwicklungen
27.15 DIASORIN SPA
27.15.1 Unternehmensübersicht
27.15.2 Umsatzanalyse
27.15.3 GEOGRAFISCHE PRÄSENZ
27.15.4 PRODUKTPORTFOLIO
27.15.5 Aktuelle Entwicklungen
27.16 SD BIOSENSOR
27.16.1 Unternehmensübersicht
27.16.2 Umsatzanalyse
27.16.3 GEOGRAFISCHE PRÄSENZ
27.16.4 PRODUKTPORTFOLIO
27.16.5 Aktuelle Entwicklungen
27.17 F. HOFFMANN-LA ROCHE LTD
27.17.1 Unternehmensübersicht
27.17.2 Umsatzanalyse
27.17.3 GEOGRAFISCHE PRÄSENZ
27.17.4 PRODUKTPORTFOLIO
27.17.5 Aktuelle Entwicklungen
27.18 GENEPATH DIAGNOSTIK
27.18.1 Unternehmensübersicht
27.18.2 Umsatzanalyse
27.18.3 GEOGRAFISCHE PRÄSENZ
27.18.4 PRODUKTPORTFOLIO
27.18.5 Aktuelle Entwicklungen
27.19 EXACT SCIENCES CORPORATION
27.19.1 Unternehmensübersicht
27.19.2 Umsatzanalyse
27.19.3 GEOGRAFISCHE PRÄSENZ
27.19.4 PRODUKTPORTFOLIO
27.19.5 Aktuelle Entwicklungen
27.2 GUARDANT HEALTH
27.20.1 UNTERNEHMENSÜBERSICHT
27.20.2 Umsatzanalyse
27.20.3 GEOGRAFISCHE PRÄSENZ
27.20.4 PRODUKTPORTFOLIO
27.20.5 Aktuelle Entwicklungen
27.21 REVVITY INC.
27.21.1 UNTERNEHMENSÜBERSICHT
27.21.2 Umsatzanalyse
27.21.3 GEOGRAFISCHE PRÄSENZ
27.21.4 PRODUKTPORTFOLIO
27.21.5 Aktuelle Entwicklungen
27.22 CARIS LIFE SCIENCES.
27.22.1 Unternehmensübersicht
27.22.2 Umsatzanalyse
27.22.3 GEOGRAFISCHE PRÄSENZ
27.22.4 PRODUKTPORTFOLIO
27.22.5 Aktuelle Entwicklungen
27.23 RANDOX LABORATORIES LTD.
27.23.1 UNTERNEHMENSÜBERSICHT
27.23.2 Umsatzanalyse
27.23.3 GEOGRAFISCHE PRÄSENZ
27.23.4 PRODUKTPORTFOLIO
27.23.5 Aktuelle Entwicklungen
27.24 DAAN GENE CO., LTD.
27.24.1 UNTERNEHMENSÜBERSICHT
27.24.2 Umsatzanalyse
27.24.3 GEOGRAFISCHE PRÄSENZ
27.24.4 PRODUKTPORTFOLIO
27.24.5 Aktuelle Entwicklungen
27.25 JIANGSU MACRO & MICRO-TEST MED-TECH CO., LTD.
27.25.1 UNTERNEHMENSÜBERSICHT
27.25.2 Umsatzanalyse
27.25.3 GEOGRAFISCHE PRÄSENZ
27.25.4 PRODUKTPORTFOLIO
27.25.5 Aktuelle Entwicklungen
27.26 GENOBIO PHARMACEUTICAL CO., LTD. (ERA BIOLOGY GROUP)
27.26.1 Unternehmensübersicht
27.26.2 Umsatzanalyse
27.26.3 GEOGRAFISCHE PRÄSENZ
27.26.4 PRODUKTPORTFOLIO
27.26.5 Aktuelle Entwicklungen
27.27 LEPU MEDICAL TECHNOLOGY (BEIJING) CO.,LTD.
27.27.1 Unternehmensübersicht
27.27.2 Umsatzanalyse
27.27.3 GEOGRAFISCHE PRÄSENZ
27.27.4 PRODUKTPORTFOLIO
27.27.5 Aktuelle Entwicklungen
27.28 PROMEGA CORPORATION
27.28.1 Unternehmensübersicht
27.28.2 Umsatzanalyse
27.28.3 GEOGRAFISCHE PRÄSENZ
27.28.4 PRODUKTPORTFOLIO
27.28.5 Aktuelle Entwicklungen
27.29 TRIPLEX INTERNATIONAL BIOSCIENCES CO. LTD.
27.29.1 UNTERNEHMENSÜBERSICHT
27.29.2 Umsatzanalyse
27.29.3 GEOGRAFISCHE PRÄSENZ
27.29.4 PRODUKTPORTFOLIO
27.29.5 Aktuelle Entwicklungen
27.3 MGMED
27.30.1 UNTERNEHMENSÜBERSICHT
27.30.2 Umsatzanalyse
27.30.3 GEOGRAFISCHE PRÄSENZ
27.30.4 PRODUKTPORTFOLIO
27.30.5 Aktuelle Entwicklungen
27.31 MOLBIO DIAGNOSTICS PVT. LTD.
27.31.1 UNTERNEHMENSÜBERSICHT
27.31.2 Umsatzanalyse
27.31.3 GEOGRAFISCHE PRÄSENZ
27.31.4 PRODUKTPORTFOLIO
27.31.5 Aktuelle Entwicklungen
27.32 GENOME DIAGNOSTICS PVT. LTD.
27.32.1 UNTERNEHMENSÜBERSICHT
27.32.2 Umsatzanalyse
27.32.3 GEOGRAFISCHE PRÄSENZ
27.32.4 PRODUKTPORTFOLIO
27.32.5 Aktuelle Entwicklungen
27.33 VELA DIAGNOSTIK
27.33.1 UNTERNEHMENSÜBERSICHT
27.33.2 Umsatzanalyse
27.33.3 GEOGRAFISCHE PRÄSENZ
27.33.4 PRODUKTPORTFOLIO
27.33.5 Aktuelle Entwicklungen
27,34 SHANGHAI CHUANGKUN BIO
27.34.1 UNTERNEHMENSÜBERSICHT
27.34.2 Umsatzanalyse
27.34.3 GEOGRAFISCHE PRÄSENZ
27.34.4 PRODUKTPORTFOLIO
27.34.5 Aktuelle Entwicklungen
27.35 TRANSGEN BIOTECH CO., LTD.
27.35.1 UNTERNEHMENSÜBERSICHT
27.35.2 Umsatzanalyse
27.35.3 GEOGRAFISCHE PRÄSENZ
27.35.4 PRODUKTPORTFOLIO
27.35.5 Aktuelle Entwicklungen
27.36 NANJING VAZYME BIOTECH CO.,LTD.
27.36.1 UNTERNEHMENSÜBERSICHT
27.36.2 Umsatzanalyse
27.36.3 GEOGRAFISCHE PRÄSENZ
27.36.4 PRODUKTPORTFOLIO
27.36.5 Aktuelle Entwicklungen
27.37 WUXI NEST BIOTECHNOLOGY CO.,LTD
27.37.1 UNTERNEHMENSÜBERSICHT
27.37.2 Umsatzanalyse
27.37.3 GEOGRAFISCHE PRÄSENZ
27.37.4 PRODUKTPORTFOLIO
27.37.5 Aktuelle Entwicklungen
27,38 HANGZHOU BIGFISH BIO-TECH CO., LTD.
27.38.1 UNTERNEHMENSÜBERSICHT
27.38.2 Umsatzanalyse
27.38.3 GEOGRAFISCHE PRÄSENZ
27.38.4 PRODUKTPORTFOLIO
27.38.5 Aktuelle Entwicklungen
27.39 MAGGENOME TECHNOLOGIES PVT. LTD.
27.39.1 UNTERNEHMENSÜBERSICHT
27.39.2 Umsatzanalyse
27.39.3 GEOGRAFISCHE PRÄSENZ
27.39.4 PRODUKTPORTFOLIO
27.39.5 Aktuelle Entwicklungen
27.4 YANENG BIOSCIENCE (SHENZHEN) CO., LTD.
27.40.1 UNTERNEHMENSÜBERSICHT
27.40.2 Umsatzanalyse
27.40.3 GEOGRAFISCHE PRÄSENZ
27.40.4 PRODUKTPORTFOLIO
27.40.5 Aktuelle Entwicklungen
27.41 MERIDIAN BIOSCIENCE
27.41.1 UNTERNEHMENSÜBERSICHT
27.41.2 Umsatzanalyse
27.41.3 GEOGRAFISCHE PRÄSENZ
27.41.4 PRODUKTPORTFOLIO
27.41.5 Aktuelle Entwicklungen
28 VERWANDTE BERICHTE
29. SCHLUSSFOLGERUNG
30 FRAGEBOGEN
31 ÜBER DATA BRIDGE MARKTFORSCHUNG
Forschungsmethodik
Die Datenerfassung und Basisjahresanalyse werden mithilfe von Datenerfassungsmodulen mit großen Stichprobengrößen durchgeführt. Die Phase umfasst das Erhalten von Marktinformationen oder verwandten Daten aus verschiedenen Quellen und Strategien. Sie umfasst die Prüfung und Planung aller aus der Vergangenheit im Voraus erfassten Daten. Sie umfasst auch die Prüfung von Informationsinkonsistenzen, die in verschiedenen Informationsquellen auftreten. Die Marktdaten werden mithilfe von marktstatistischen und kohärenten Modellen analysiert und geschätzt. Darüber hinaus sind Marktanteilsanalyse und Schlüsseltrendanalyse die wichtigsten Erfolgsfaktoren im Marktbericht. Um mehr zu erfahren, fordern Sie bitte einen Analystenanruf an oder geben Sie Ihre Anfrage ein.
Die wichtigste Forschungsmethodik, die vom DBMR-Forschungsteam verwendet wird, ist die Datentriangulation, die Data Mining, die Analyse der Auswirkungen von Datenvariablen auf den Markt und die primäre (Branchenexperten-)Validierung umfasst. Zu den Datenmodellen gehören ein Lieferantenpositionierungsraster, eine Marktzeitlinienanalyse, ein Marktüberblick und -leitfaden, ein Firmenpositionierungsraster, eine Patentanalyse, eine Preisanalyse, eine Firmenmarktanteilsanalyse, Messstandards, eine globale versus eine regionale und Lieferantenanteilsanalyse. Um mehr über die Forschungsmethodik zu erfahren, senden Sie eine Anfrage an unsere Branchenexperten.
Anpassung möglich
Data Bridge Market Research ist ein führendes Unternehmen in der fortgeschrittenen formativen Forschung. Wir sind stolz darauf, unseren bestehenden und neuen Kunden Daten und Analysen zu bieten, die zu ihren Zielen passen. Der Bericht kann angepasst werden, um Preistrendanalysen von Zielmarken, Marktverständnis für zusätzliche Länder (fordern Sie die Länderliste an), Daten zu klinischen Studienergebnissen, Literaturübersicht, Analysen des Marktes für aufgearbeitete Produkte und Produktbasis einzuschließen. Marktanalysen von Zielkonkurrenten können von technologiebasierten Analysen bis hin zu Marktportfoliostrategien analysiert werden. Wir können so viele Wettbewerber hinzufügen, wie Sie Daten in dem von Ihnen gewünschten Format und Datenstil benötigen. Unser Analystenteam kann Ihnen auch Daten in groben Excel-Rohdateien und Pivot-Tabellen (Fact Book) bereitstellen oder Sie bei der Erstellung von Präsentationen aus den im Bericht verfügbaren Datensätzen unterstützen.