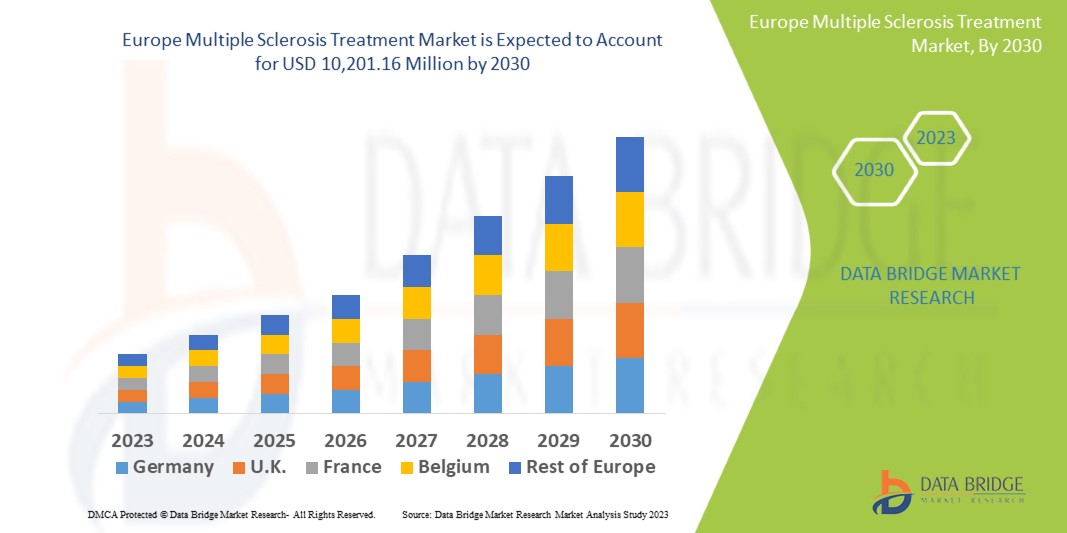
Europe Multiple Sclerosis Treatment Market
Tamaño del mercado en miles de millones de dólares
Tasa de crecimiento anual compuesta (CAGR) :
% 
 USD
6,026.70 Million
USD
10,201.16 Million
2022
2030
USD
6,026.70 Million
USD
10,201.16 Million
2022
2030
| 2023 –2030 | |
| USD 6,026.70 Million | |
| USD 10,201.16 Million | |
|
|
|
|
Mercado europeo de tratamientos para la esclerosis múltiple, tipo de enfermedad (esclerosis múltiple remitente-recurrente (EMRR), esclerosis múltiple secundaria progresiva (EMSP), esclerosis múltiple primaria progresiva (EMPP), esclerosis múltiple remitente-recurrente grave (EMRS)), tratamiento (terapias preventivas, terapias abortivas/tratamiento de exacerbaciones agudas, terapias sintomáticas), tipo de medicamento (de marca, genérico), usuario final (hospitales y clínicas, laboratorios de diagnóstico, otros) – tendencias de la industria y pronóstico hasta 2030.
Análisis y tamaño del mercado europeo de tratamiento de la esclerosis múltiple
La creciente carga que suponen diversas enfermedades infecciosas para el sistema sanitario mundial es una preocupación fundamental, y los países en desarrollo soportan una parte desproporcionada de dicha carga. Según el Instituto de Ciencias Hepáticas y Biliares de la India, alrededor del 3 % de la población mundial está infectada con el virus de la hepatitis C. El aumento global de la incidencia de infecciones por VHC, especialmente tanto en países desarrollados como en desarrollo, es un factor clave que impulsa el crecimiento del mercado de tratamientos para la esclerosis múltiple.
Según un análisis de Data Bridge Market Research, se prevé que el mercado de tratamientos para la esclerosis múltiple alcance los 10.201,16 millones de dólares en 2030, frente a los 6.026,7 millones de dólares en 2022, con una tasa de crecimiento anual compuesta (TCAC) del 6,8 % durante el periodo de previsión de 2022 a 2030. Además de información sobre el mercado (valor, tasa de crecimiento, segmentación, cobertura geográfica y principales actores), los informes de mercado de Data Bridge Market Research incluyen análisis exhaustivos de expertos, epidemiología de pacientes, análisis de proyectos en desarrollo, análisis de precios y marco regulatorio.
Alcance y segmentación del mercado europeo de tratamientos para la esclerosis múltiple
|
Métrica del informe |
Detalles |
|
Período de previsión |
2023 a 2030 |
|
Año base |
2022 |
|
Años históricos |
2021 (Personalizable para el período 2015-2020) |
|
Unidades cuantitativas |
Ingresos en millones de USD, volúmenes en unidades, precios en USD |
|
Segmentos cubiertos |
Tipo de enfermedad (Esclerosis múltiple remitente-recurrente (EMRR), Esclerosis múltiple secundaria progresiva (EMSP), Esclerosis múltiple primaria progresiva (EMPP), Esclerosis múltiple remitente-recurrente grave (EMRG)), Tratamiento (Terapias preventivas, Terapias abortivas/Tratamiento de exacerbaciones agudas, Terapias sintomáticas), Tipo de medicamento (De marca, Genérico), Usuario final (Hospitales, Centros de traumatología, Centros quirúrgicos ambulatorios y Otros) |
|
Países cubiertos |
Alemania, Francia, Reino Unido, Países Bajos, Suiza, Bélgica, Rusia, Italia, España, Turquía, Resto de Europa en Europa |
|
Participantes del mercado cubiertos |
AbbVie Inc. (EE. UU.), Bausch Health Companies Inc. (Canadá), Biora Therapeutics, Inc. (EE. UU.), Boehringer Ingelheim International GmbH (Alemania), Amgen Inc. (EE. UU.), Pfizer Inc. (EE. UU.), F. Hoffmann-La Roche Ltd. (Suiza), Mylan NV (EE. UU.), Novartis AG (Suiza), Bayer AG (Alemania), Bristol Myers Squibb Company (EE. UU.), Biogen (EE. UU.), Teva Pharmaceutical Industries Ltd. (Israel), Takeda Pharmaceutical Company Limited (Japón), Jazz Pharmaceuticals, Inc. (Reino Unido), Abbott (EE. UU.), Bio-Rad Laboratories Inc. (EE. UU.), Mylan NV (EE. UU.) |
|
Oportunidades de mercado |
|
Definición de mercado
La esclerosis múltiple (EM) es una enfermedad crónica, inflamatoria e inmunomediada que puede causar sección axonal, desmielinización y neurodegeneración de las células nerviosas de la médula espinal y el cerebro. Algunas de las terapias más utilizadas incluyen la administración de medicamentos inyectables, orales e intravenosos, antidepresivos , fisioterapia y relajantes musculares.
Dinámica del mercado europeo de tratamientos para la esclerosis múltiple
Conductores
- Mayor concienciación sobre la esclerosis múltiple
Ha habido una creciente concienciación sobre la enfermedad, lo que está contribuyendo al crecimiento del mercado. Por ejemplo, la Fundación de Esclerosis Múltiple y grupos afiliados instauraron el Mes Nacional de Educación y Concienciación sobre la EM, que se celebra en marzo desde 2003, con el fin de crear conciencia sobre la enfermedad. El objetivo principal de este programa es promover la comprensión de la esclerosis múltiple y ayudar a los pacientes a tomar decisiones informadas sobre su tratamiento. Además, la Sociedad Nacional de Esclerosis Múltiple creó y lanzó la campaña «La EM mata la conexión > < La conexión mata la EM» para conectar a las personas que padecen EM, a quienes tratan a pacientes con EM y a quienes realizan actividades para crear un mundo libre de esclerosis múltiple. Por lo tanto, este factor impulsa el crecimiento del mercado.
- Aumento de la incidencia de esclerosis múltiple
En esta región se ha observado un aumento en la incidencia de esclerosis múltiple. Según un estudio de la Sociedad Nacional de Esclerosis Múltiple, la prevalencia estimada de la enfermedad era de aproximadamente 309 casos por cada 100 000 habitantes en 2010, lo que resultó en un total de 727 344 casos de esclerosis múltiple en adultos. Europa se considera una región de alta prevalencia de EM. La Sociedad de Esclerosis Múltiple indicó que alrededor de 110 000 personas padecían esta enfermedad en el Reino Unido en 2018. Asimismo, se ha observado que la EM es más del doble de frecuente en mujeres en esta región. El número de nuevos pacientes diagnosticados cada año también está aumentando, pasando de 5000 pacientes en 2017 a 6700 en 2018. Por lo tanto, esta tasa de incidencia está impulsando la demanda de medicamentos para el tratamiento de la EM.
Oportunidades
- Aumento de las actividades de I+D por parte de las organizaciones
Numerosos fármacos se encuentran en fase de investigación para el tratamiento de la esclerosis múltiple (EM) y muchos están en ensayos clínicos. La FDA estadounidense ha aprobado varios fármacos para el tratamiento de la EM, como fingolimod, interferones , natalizumab, acetato de glatiramero, teriflunomida y dimetilfumarato. Varios genetistas e investigadores estudian el genoma humano para determinar las causas y posibles tratamientos de enfermedades como la distrofia muscular, el Alzheimer, el cáncer y la diabetes. Por ejemplo, han descubierto que algunas personas con un gen específico tienen mayor probabilidad de desarrollar la enfermedad de Alzheimer. Por ello, los investigadores trabajan actualmente en fármacos que modifiquen o reparen ese gen en particular. Asimismo, muchos investigadores han descubierto que algunas personas con esclerosis múltiple poseen un gen que las hace más vulnerables a la enfermedad. Por consiguiente, trabajan constantemente en fármacos que alteren o reparen ese gen.
Limitaciones/Desafíos
- Alto costo de los medicamentos
El costo de los medicamentos para la esclerosis múltiple sigue siendo un desafío constante para el crecimiento del mercado, a pesar de la alta prevalencia de esta enfermedad. El elevado precio de los fármacos dificulta la satisfacción de las necesidades de la población afectada. Los tratamientos modificadores de la enfermedad (TME) son la opción estándar, pero su costo excesivo conlleva una adherencia inadecuada al tratamiento y un mal control de la enfermedad. Según la Sociedad Nacional de Esclerosis Múltiple, el costo de los medicamentos para la EM está aumentando considerablemente. Se prevé que este factor limite el crecimiento del mercado.
Este informe sobre el mercado de tratamientos para la esclerosis múltiple ofrece información detallada sobre los últimos avances, la normativa comercial, el análisis de importaciones y exportaciones, el análisis de producción, la optimización de la cadena de valor, la cuota de mercado, el impacto de los actores del mercado nacionales y locales, el análisis de oportunidades en términos de nuevos nichos de ingresos, los cambios en la normativa, el análisis estratégico del crecimiento del mercado, el tamaño del mercado, el crecimiento de las distintas categorías, los nichos de aplicación y su dominio, las aprobaciones y lanzamientos de productos, la expansión geográfica y las innovaciones tecnológicas. Para obtener más información sobre el mercado de tratamientos para la esclerosis múltiple, contacte con Data Bridge Market Research para solicitar un informe de análisis. Nuestro equipo le ayudará a tomar una decisión informada para impulsar el crecimiento de su negocio.
Últimos desarrollos:
- En 2021, Janssen recibió la aprobación de la FDA estadounidense para Ponvory. Es un modulador selectivo del receptor 1 de esfingosina-1-fosfato (S1P1) de administración oral una vez al día, que se utiliza para tratar a adultos con formas recurrentes de esclerosis múltiple (EM), como el síndrome clínicamente aislado, la enfermedad recurrente-remitente y la enfermedad secundaria progresiva activa.
- En 2020, Novartis anunció la aprobación por parte de la FDA estadounidense de Kesimpta en forma de inyección para uso subcutáneo para el tratamiento de las formas recurrentes de esclerosis múltiple (EMR), que incluyen el síndrome clínicamente aislado, la enfermedad recurrente-remitente y la enfermedad secundaria progresiva activa, en adultos.
Alcance del mercado europeo de tratamientos para la esclerosis múltiple
El mercado de tratamientos para la esclerosis múltiple se segmenta según el tipo de enfermedad, el tratamiento, el tipo de fármaco y el usuario final. El crecimiento en estos segmentos le permitirá analizar los segmentos de menor crecimiento en la industria y proporcionará a los usuarios una valiosa visión general del mercado e información clave para la toma de decisiones estratégicas en la identificación de las principales aplicaciones del mercado.
Tipo de enfermedad
- Esclerosis múltiple remitente-recurrente (EMRR)
- Esclerosis Múltiple Secundaria Progresiva (EMSP)
- Esclerosis Múltiple Primaria Progresiva (EMPP)
- Esclerosis múltiple remitente-recurrente grave (RES)
Tratamiento
- Terapias preventivas
- Terapias abortivas/Tratamiento de las exacerbaciones agudas
- Terapias sintomáticas
Tipo de medicamento
- Marca
- Genérico
Vía administrativa
- Oral
- Parenteral
Usuario final
- Hospitales y clínicas
- Laboratorios de diagnóstico
- Otros
Análisis/Perspectivas regionales sobre el tratamiento de la esclerosis múltiple
Se analiza el mercado de tratamientos para la esclerosis múltiple y se proporcionan datos sobre el tamaño del mercado y las tendencias por tipo de enfermedad, tratamiento, tipo de fármaco y usuario final, como se mencionó anteriormente.
Los países que abarca el informe sobre el mercado del tratamiento de la esclerosis múltiple son Alemania, Francia, Reino Unido, Países Bajos, Suiza, Bélgica, Rusia, Italia, España, Turquía y el resto de Europa.
Se prevé que Alemania lidere el mercado durante el período de pronóstico de 2023 a 2030 debido a la introducción de nuevas opciones de tratamiento para la esclerosis múltiple en la región. El creciente desarrollo de la investigación y el desarrollo de fármacos en la región también impulsa el crecimiento del mercado. La mayor concienciación sobre la esclerosis múltiple y sus tratamientos contribuye a este crecimiento.
La sección del informe dedicada a cada país también proporciona información sobre los factores que influyen en el mercado y los cambios en la normativa nacional que afectan a las tendencias actuales y futuras. Para pronosticar el panorama del mercado en cada país, se utilizan datos como el análisis de la cadena de valor (tanto aguas arriba como aguas abajo), las tendencias tecnológicas, el análisis de las cinco fuerzas de Porter y estudios de caso. Asimismo, se consideran la presencia y disponibilidad de marcas europeas y los retos a los que se enfrentan debido a la competencia (ya sea intensa o escasa) de marcas locales y nacionales, así como el impacto de los aranceles y las rutas comerciales nacionales.
Análisis del panorama competitivo y la cuota de mercado del tratamiento de la esclerosis múltiple en Europa
El análisis competitivo del mercado de tratamientos para la esclerosis múltiple ofrece información detallada por competidor. Esta información incluye: descripción general de la empresa, datos financieros, ingresos generados, potencial de mercado, inversión en investigación y desarrollo, nuevas iniciativas de mercado, presencia en Europa, plantas de producción, capacidad de producción, fortalezas y debilidades, lanzamientos de productos, amplitud y profundidad de la gama de productos y dominio de aplicaciones. Los datos presentados se refieren exclusivamente a la actividad de las empresas en el mercado de tratamientos para la esclerosis múltiple.
Algunos de los principales actores que operan en el mercado del tratamiento de la esclerosis múltiple son:
- AbbVie Inc. (EE. UU.)
- Bausch Health Companies Inc. (Canadá)
- Biora Therapeutics, Inc. (EE. UU.)
- Boehringer Ingelheim International GmbH (Alemania)
- Amgen Inc. (EE. UU.)
- Pfizer Inc (EE. UU.)
- F. Hoffmann-La Roche Ltd (Suiza)
- Mylan NV (EE. UU.)
- Novartis AG (Suiza)
- Bayer AG (Alemania)
- Compañía Bristol Myers Squibb (EE. UU.)
- Biogen (EE. UU.)
- Industrias Farmacéuticas Teva Ltd (Israel)
- Compañía Farmacéutica Takeda Limited (Japón)
- Jazz Pharmaceuticals, Inc. (Reino Unido)
- Abbott (EE. UU.)
- Bio-Rad Laboratories Inc. (EE. UU.)
- Mylan NV (EE. UU.)
SKU-
Obtenga acceso en línea al informe sobre la primera nube de inteligencia de mercado del mundo
- Panel de análisis de datos interactivo
- Panel de análisis de empresas para oportunidades con alto potencial de crecimiento
- Acceso de analista de investigación para personalización y consultas
- Análisis de la competencia con panel interactivo
- Últimas noticias, actualizaciones y análisis de tendencias
- Aproveche el poder del análisis de referencia para un seguimiento integral de la competencia
Tabla de contenido
1 INTRODUCCIÓN
1.1 OBJETIVOS DEL ESTUDIO
1.2 DEFINICIÓN DE MERCADO
1.3 PANORAMA GENERAL DEL MERCADO EUROPEO DE TRATAMIENTO DE LA ESCLEROSIS MÚLTIPLE
1.4 MONEDA Y PRECIOS
1.5 LIMITACIÓN
1.6 MERCADOS CUBIERTOS
2 SEGMENTACIÓN DE MERCADO
2.1 CONCLUSIONES CLAVE
2.2 TAMAÑO DEL MERCADO EUROPEO DE TRATAMIENTO DE LA ESCLEROSIS MÚLTIPLE
2.2.1 CUADRÍCULA DE POSICIONAMIENTO DE PROVEEDORES
2.2.2 CURVA DEL CICLO DE VIDA DE LA TECNOLOGÍA
2.2.3 MODELO DE VALIDACIÓN DE DATOS TRÍPODE
2.2.4 GUÍA DE MERCADO
2.2.5 MODELADO MULTIVARIADO
2.2.6 ANÁLISIS DE ARRIBA A ABAJO
2.2.7 MATRIZ DE DESAFÍOS
2.2.8 CUADRÍCULA DE COBERTURA DE LA APLICACIÓN
2.2.9 NORMAS DE MEDICIÓN
2.2.10 ANÁLISIS DE LA PARTICIPACIÓN DE MERCADO DE LOS PROVEEDORES
2.2.11 MODELO BASADO EN LA EPIDEMIOLOGÍA
2.2.12 DATOS CLAVE DE LAS ENTREVISTAS PRIMARIAS
2.2.13 PUNTOS DE DATOS DE BASES DE DATOS SECUNDARIAS CLAVE
2.3 MERCADO EUROPEO DE TRATAMIENTO DE LA ESCLEROSIS MÚLTIPLE: RESUMEN DE LA INVESTIGACIÓN
2.4 SUPUESTOS
3. PANORAMA DEL MERCADO
3.1 CONDUCTORES
3.2 RESTRICCIONES
3.3 OPORTUNIDADES
3.4 DESAFÍOS
4 RESUMEN EJECUTIVO
5 PERSPECTIVAS PREMIUM
5.1 ANÁLISIS PESTEL
5.2 LAS CINCO FUERZAS DE PORTER
6 EPIDEMIOLOGÍA
6.1 INCIDENCIA DE TODOS POR GÉNERO
6.2 TASA DE TRATAMIENTO
6.3 TASA DE MORTALIDAD
6.4 MODELO DE ADHERENCIA A LA FARMACIA Y CAMBIO DE TERAPIA
6.5 TASAS DE ÉXITO DEL TRATAMIENTO DE PACIENTES
7 PERSPECTIVAS DEL SECTOR
7.1 ANÁLISIS DE PATENTES
7.2 TASA DE TRATAMIENTO FARMACOLÓGICO EN MERCADOS MADUROS
7.3 TENDENCIAS DEMOGRÁFICAS: IMPACTO EN TODAS LAS TASAS DE INCIDENCIA
7.4 DIAGRAMA DE FLUJO DE PACIENTES
7.5 ESTRATEGIAS CLAVE DE PRECIOS
7.6 ESTRATEGIAS CLAVE PARA LA CAPTACIÓN DE PACIENTES
7.7 ENTREVISTAS CON HEMATÓLOGOS
7.8 ENTREVISTAS CON ONCÓLOGOS
7.9 ENTREVISTAS CON ORGANIZACIONES CONTRA EL CÁNCER
7.1 OTRAS INFORMACIONES DE KOL
8 ANÁLISIS DE LA TUBERÍA
8.1 ENSAYOS CLÍNICOS Y ANÁLISIS DE FASE
8.2 DESARROLLO DE FARMACÉUTICA
8.3 CANDIDATOS DE LA FASE III
8.4 CANDIDATOS DE LA FASE II
8.5 CANDIDATOS DE LA FASE I
8.6 OTROS (PRECLÍNICOS Y DE INVESTIGACIÓN)
9 MARCO REGULATORIO
10. MERCADO EUROPEO DE TRATAMIENTO DE LA ESCLEROSIS MÚLTIPLE, POR TIPO
10.1 GENERALIDADES
10.2 ESCLEROSIS MÚLTIPLE REMITENTE-RECURRIENTE (EMRR)
10.3 SÍNDROME CLÍNICAMENTE AISLADO (SCA)
10.4 EM PRIMARIA PROGRESIVA (EMPP)
10.5 EM SECUNDARIA PROGRESIVA (EMSP)
11. MERCADO EUROPEO DE TRATAMIENTOS PARA LA ESCLEROSIS MÚLTIPLE, POR TRATAMIENTO
11.1 GENERALIDADES
11.2 MEDICAMENTOS
11.2.1 FÁRMACOS MODIFICADORES DE LA ENFERMEDAD
11.2.1.1. ANTICUERPO MONOCLONAL
11.2.1.1.1. ANTICUERPOS MONOCLONALES, POR TIPO
11.2.1.1.1.1 OCRELIZUMAB
11.2.1.1.1.2 NATALIZUMAB
11.2.1.1.1.3 DACLIZUMAB
11.2.1.1.1.4 OTROS
11.2.1.1.2. ANTICUERPOS MONOCLONALES, POR TIPO DE FÁRMACO
11.2.1.1.2.1 GENÉRICO
11.2.1.1.2.2 DE MARCA
11.2.1.1.2.2.1. OCREVUS
11.2.1.1.2.2.2. TYSABRI
11.2.1.1.2.2.3. ZENAPAX
11.2.1.2. FÁRMACOS INMUNOMODULADORES
11.2.1.2.1. FÁRMACOS INMUNOMODULADORES, POR FÁRMACO
11.2.1.2.1.1 GLATIRAMER
11.2.1.2.1.2 CLADRIBINA
11.2.1.2.1.3 TERIFLUNOMIDA
11.2.1.2.1.4 FUMARATO DE DIMETIL
11.2.1.2.1.5 OTROS
11.2.1.2.2. FÁRMACOS INMUNOMODULADORES, POR TIPO DE FÁRMACO
11.2.1.2.2.1 GENÉRICO
11.2.1.2.2.2 DE MARCA
11.2.1.2.2.2.1. GLATOPA
11.2.1.2.2.2.2. COPAXONA
11.2.1.2.2.2.3. MAVENCLAD
11.2.1.2.2.2.4. OTROS
11.2.1.3. MODULADORES DEL RECEPTOR DE ESFINGOSINA 1-FOSFATO (S1P)
11.2.1.3.1. MODULADORES DEL RECEPTOR DE ESFINGOSINA 1-FOSFATO (S1P), POR TIPO
11.2.1.3.1.1 PONESIMOD
11.2.1.3.1.2 FINGOLIMOD
11.2.1.3.1.3 SIPONIMOD
11.2.1.3.1.4 OZANIMOD
11.2.1.3.1.5 OTROS
11.2.1.3.2. MODULADORES DEL RECEPTOR DE ESFINGOSINA 1-FOSFATO (S1P), POR TIPO DE FÁRMACO
11.2.1.3.2.1 GENÉRICO
11.2.1.3.2.2 DE MARCA
11.2.1.3.2.2.1. PONVORY
11.2.1.3.2.2.2. ZEPOSIA
11.2.1.3.2.2.3. MAYZENT
11.2.1.3.2.2.4. ZEPOSIA
11.2.1.4. FÁRMACOS ANTICANCERÍGENOS
11.2.1.4.1. FÁRMACOS ANTICANCERÍGENOS, POR TIPO
11.2.1.4.1.1 MITOXANTRONA
11.2.1.4.1.2 CICLOFOSFAMIDA
11.2.1.4.1.3 MELFALANO FLUFENAMIDA
11.2.1.4.1.4 OTROS
11.2.1.4.2. FÁRMACOS ANTICANCERÍGENOS, POR TIPO DE FÁRMACO
11.2.1.4.2.1 GENÉRICO
11.2.1.4.2.2 DE MARCA
11.2.1.4.2.2.1. PEPAXTO
11.2.1.4.2.2.2. CITOXANO
11.2.1.4.2.2.3. NEOSAR
11.2.1.4.2.2.4. OTROS
11.2.1.5. INTERFERÓN
11.2.1.5.1. INTERFERONA, POR TIPO
11.2.1.5.1.1 INTERFERÓN BETA-1B
11.2.1.5.1.2 INTERFERÓN BETA-1A
11.2.1.5.1.3 INTERFERÓN BETA-1A PEGILADO
11.2.1.5.1.4 OTROS
11.2.1.5.2. INTERFERONA, POR TIPO DE FÁRMACO
11.2.1.5.2.1 GENÉRICO
11.2.1.5.2.2 DE MARCA
11.2.1.5.2.2.1. ROFERÓN
11.2.1.5.2.2.2. VIRAFERÓN
11.2.1.5.2.2.3. AVONEX
11.2.1.5.2.2.4. BETASERON
11.2.1.6. INMUNOSUPRESORES
11.2.1.6.1. INMUNOSUPRESORES, POR TIPO
11.2.1.6.1.1 AZATIOPRINA
11.2.1.6.1.2 METOTREXATO
11.2.1.6.1.3 OTROS
11.2.1.6.2. INMUNOSUPRESORES, POR TIPO DE FÁRMACO
11.2.1.6.2.1 AZASAN
11.2.1.6.2.2 IMURAN
11.2.1.6.2.3 REDITREX
11.2.1.6.2.4 TREXALL
11.2.1.6.2.5 XATMEP
11.2.2 TERAPIAS SINTOMÁTICAS
11.2.2.1. RELAJANTES MUSCULARES
11.2.2.1.1. RELAJANTES MUSCULARES, POR TIPO
11.2.2.1.1.1 BACLOFENO
11.2.2.1.1.2 TIZANIDINA
11.2.2.1.1.3 CICLOBENSAPINA
11.2.2.1.1.4 OTROS
11.2.2.1.2. RELAJANTES MUSCULARES, POR TIPO DE FÁRMACO
11.2.2.1.2.1 GENÉRICO
11.2.2.1.2.2 DE MARCA
11.2.2.1.2.2.1. LIORESAL
11.2.2.1.2.2.2. ZANAFLEX
11.2.2.1.2.2.3. FLEXERIL
11.2.2.2. MEDICAMENTOS PARA LA FATIGA
11.2.2.2.1. MEDICAMENTOS PARA LA FATIGA, POR TIPO
11.2.2.2.1.1 AMANTADINA
11.2.2.2.1.2 MODAFINIL
11.2.2.2.1.3 METILFENIDATO
11.2.2.2.1.4 OTROS
11.2.2.2.2. MEDICAMENTOS PARA LA FATIGA, POR TIPO DE FÁRMACO
11.2.2.2.2.1 GENÉRICO
11.2.2.2.2.2 DE MARCA
11.2.2.2.2.2.1. GOCOVRI
11.2.2.2.2.2.2. PROVIGIL
11.2.2.2.2.2.3. RITALINO
11.2.2.3. DOLOR NEUROPÁTICO
11.2.2.3.1. GABAPENTINA
11.2.2.3.2. CARBAMAZEPINA
11.2.2.3.3. AMITRIPTILINA
11.2.2.3.4. OTROS
11.2.2.4. CORTICOSTEROIDES
11.2.2.4.1. PREDNISONA
11.2.2.4.2. METILPREDNISOLONA
11.2.2.4.3. DEXAMETASONA
11.2.2.4.4. PREDNISOLONA
11.2.2.4.5. BETAMETASONA
11.2.2.4.6. OTROS
11.3 FISIOTERAPIA
11.3.1 TERAPIA MANUAL
11.3.2 TRATAMIENTOS ESPECIALIZADOS
11.3.3 TÉCNICAS DE MOVILIZACIÓN CONJUNTA
11.3.4 TERAPIA DE SUSPENSIÓN
11.3.5 TÉCNICAS DE RELAJACIÓN
11.3.6 MÉTODOS DE CORRECCIÓN POSTURAL
11.4 PLASMAFÉRESIS
11.4.1 INTERCAMBIO PLASMÁTICO (PE)
11.4.2 PLASMAFÉRESIS POR FILTRACIÓN DE DOBLE MEMBRANA (DFP)
11.4.3 PLASMAFÉRESIS POR ADSORCIÓN
11.5 OTROS
12. MERCADO MUNDIAL DE ESCLEROSIS MÚLTIPLE, POR TIPO DE FÁRMACO
12.1 GENERALIDADES
12.2 GENÉRICO
12.3 DE MARCA
12.3.1 OCREVUS
12.3.2 TYSABRI
12.3.3 ZENAPAX
12.3.4 GLATOPA
12.3.5 COPAXONA
12.3.6 MAVENCLAD
12.3.7 PONVORY
12.3.8 ZEPOSIA
12.3.9 MAYZENT
12.3.10 ZEPOSIA
12.3.11 PEPAXTO
12.3.12 CITOXANO
12.3.13 NEOSAR
12.3.14 ROFERÓN
12.3.15 VIRAFERÓN
12.3.16 AVONEX
12.3.17 BETASERON
12.3.18 BACLOFENO
12.3.19 TIZANIDINA
12.3.20 CICLOBENSAPRINA
12.3.21 OTROS
13. MERCADO EUROPEO DE TRATAMIENTOS PARA LA ESCLEROSIS MÚLTIPLE, POR VÍA DE ADMINISTRACIÓN
13.1 GENERALIDADES
13.2 ORAL
13.2.1 TABLETA
13.2.2 CÁPSULA
13.2.3 OTROS
13.3 PARENTERAL
13.3.1 INTRAVENOSA
13.3.2 SUBCUTÁNEO
13.3.3 OTROS
13.4 OTROS
14. MERCADO EUROPEO DE TRATAMIENTOS PARA LA ESCLEROSIS MÚLTIPLE, POR TIPO DE PRESCRIPCIÓN
14.1 GENERALIDADES
14.2 SIN MOSTRADOR
14.3 PRESCRIPCIÓN
15. MERCADO EUROPEO DE TRATAMIENTO DE LA ESCLEROSIS MÚLTIPLE, POR GRUPO DE EDAD
15.1 GENERALIDADES
15.2 NIÑOS
15.3 ADULTOS
15.4 GERIÁTRICO
16. MERCADO EUROPEO DE TRATAMIENTO DE LA ESCLEROSIS MÚLTIPLE, POR GÉNERO
16.1 GENERALIDADES
16.2 HOMBRE
16.3 MUJER
17. MERCADO EUROPEO DE TRATAMIENTO DE LA ESCLEROSIS MÚLTIPLE, POR USUARIO FINAL
17.1 GENERALIDADES
17.2 HOSPITALES
17.3 CLÍNICAS ESPECIALIZADAS
17.4 ATENCIÓN DOMICILIARIA
17,5 CENTROS QUIRÚRGICOS AMBULATORIOS
17.6 OTROS
18. MERCADO EUROPEO DE TRATAMIENTO DE LA ESCLEROSIS MÚLTIPLE, POR CANAL DE DISTRIBUCIÓN
18.1 GENERALIDADES
18.2 FARMACIA HOSPITALARIA
18.3 FARMACIA MINORISTA
18.3.1 TIENDAS EN LÍNEA
18.3.2 FARMACIAS
18.4 OTROS
19. MERCADO EUROPEO DE TRATAMIENTO DE LA ESCLEROSIS MÚLTIPLE, POR GEOGRAFÍA
MERCADO EUROPEO DE TRATAMIENTO DE LA ESCLEROSIS MÚLTIPLE (TODA LA SEGMENTACIÓN PROPORCIONADA ANTERIORMENTE SE PRESENTA EN ESTE CAPÍTULO POR PAÍS)
19.1 EUROPA
19.1.1 ALEMANIA
19.1.2 Reino Unido
19.1.3 ITALIA
19.1.4 FRANCIA
19.1.5 ESPAÑA
19.1.6 RUSIA
19.1.7 SUIZA
19.1.8 TURQUÍA
19.1.9 BÉLGICA
19.1.10 PAÍSES BAJOS
19.1.11 DINAMARCA
19.1.12 SUECIA
19.1.13 POLONIA
19.1.14 NORUEGA
19.1.15 FINLAND
19.1.16 RESTO DE EUROPA
20. MERCADO EUROPEO DE TRATAMIENTO DE LA ESCLEROSIS MÚLTIPLE: PANORAMA EMPRESARIAL
20.1 ANÁLISIS DE ACCIONES DE LA EMPRESA: GLOBAL
20.2 ANÁLISIS DE ACCIONES DE LA COMPAÑÍA: NORTEAMÉRICA
20.3 ANÁLISIS DE ACCIONES DE LA EMPRESA: EUROPA
20.4 ANÁLISIS DE ACCIONES DE LA EMPRESA: EUROPA
20.5 FUSIONES Y ADQUISICIONES
20.6 DESARROLLO Y APROBACIÓN DE NUEVOS PRODUCTOS
20.7 EXPANSIONES
20.8 CAMBIOS REGULATORIOS
20.9 ALIANZAS Y OTROS DESARROLLOS ESTRATÉGICOS
21. MERCADO EUROPEO DE TRATAMIENTO DE LA ESCLEROSIS MÚLTIPLE: ANÁLISIS FODA Y DBMR
22. MERCADO EUROPEO DE TRATAMIENTO DE LA ESCLEROSIS MÚLTIPLE, PERFIL DE LA EMPRESA
22.1 BIOGEN
22.1.1 INFORMACIÓN GENERAL DE LA EMPRESA
22.1.2 ANÁLISIS DE INGRESOS
22.1.3 PRESENCIA GEOGRÁFICA
22.1.4 CARTERA DE PRODUCTOS
22.1.5 DESARROLLOS RECIENTES
22.2 TEVA NEUROSCIENCE, INC.
22.2.1 INFORMACIÓN GENERAL DE LA EMPRESA
22.2.2 ANÁLISIS DE INGRESOS
22.2.3 PRESENCIA GEOGRÁFICA
22.2.4 CARTERA DE PRODUCTOS
22.2.5 DESARROLLOS RECIENTES
22.3 VIATRIS INC.
22.3.1 INFORMACIÓN GENERAL DE LA EMPRESA
22.3.2 ANÁLISIS DE INGRESOS
22.3.3 PRESENCIA GEOGRÁFICA
22.3.4 CARTERA DE PRODUCTOS
22.3.5 DESARROLLOS RECIENTES
22.4 NOVARTIS AG
22.4.1 INFORMACIÓN GENERAL DE LA EMPRESA
22.4.2 ANÁLISIS DE INGRESOS
22.4.3 PRESENCIA GEOGRÁFICA
22.4.4 CARTERA DE PRODUCTOS
22.4.5 DESARROLLOS RECIENTES
22.5 MERCK KGAA
22.5.1 INFORMACIÓN GENERAL DE LA EMPRESA
22.5.2 ANÁLISIS DE INGRESOS
22.5.3 PRESENCIA GEOGRÁFICA
22.5.4 CARTERA DE PRODUCTOS
22.5.5 DESARROLLOS RECIENTES
22.6 GLENMARK PHARMACEUTICALS LTD
22.6.1 INFORMACIÓN GENERAL DE LA EMPRESA
22.6.2 ANÁLISIS DE INGRESOS
22.6.3 PRESENCIA GEOGRÁFICA
22.6.4 CARTERA DE PRODUCTOS
22.6.5 DESARROLLOS RECIENTES
22,7 LUPIN
22.7.1 INFORMACIÓN GENERAL DE LA EMPRESA
22.7.2 ANÁLISIS DE INGRESOS
22.7.3 PRESENCIA GEOGRÁFICA
22.7.4 CARTERA DE PRODUCTOS
22.7.5 DESARROLLOS RECIENTES
22.8 CIPLA INC
22.8.1 INFORMACIÓN GENERAL DE LA EMPRESA
22.8.2 ANÁLISIS DE INGRESOS
22.8.3 PRESENCIA GEOGRÁFICA
22.8.4 CARTERA DE PRODUCTOS
22.8.5 DESARROLLOS RECIENTES
22.9 SANOFI
22.9.1 INFORMACIÓN GENERAL DE LA EMPRESA
22.9.2 ANÁLISIS DE INGRESOS
22.9.3 PRESENCIA GEOGRÁFICA
22.9.4 CARTERA DE PRODUCTOS
22.9.5 DESARROLLOS RECIENTES
22.1 BAYER
22.10.1 INFORMACIÓN GENERAL DE LA EMPRESA
22.10.2 ANÁLISIS DE INGRESOS
22.10.3 PRESENCIA GEOGRÁFICA
22.10.4 CARTERA DE PRODUCTOS
22.10.5 DESARROLLOS RECIENTES
22.11 ABBVIE, INC
22.11.1 INFORMACIÓN GENERAL DE LA EMPRESA
22.11.2 ANÁLISIS DE INGRESOS
22.11.3 PRESENCIA GEOGRÁFICA
22.11.4 CARTERA DE PRODUCTOS
22.11.5 DESARROLLOS RECIENTES
22.12 ABBOTT
22.12.1 INFORMACIÓN GENERAL DE LA EMPRESA
22.12.2 ANÁLISIS DE INGRESOS
22.12.3 PRESENCIA GEOGRÁFICA
22.12.4 CARTERA DE PRODUCTOS
22.12.5 DESARROLLOS RECIENTES
22.13 F. HOFFMANN-LA ROCHE LTD
22.13.1 INFORMACIÓN GENERAL DE LA EMPRESA
22.13.2 ANÁLISIS DE INGRESOS
22.13.3 PRESENCIA GEOGRÁFICA
22.13.4 CARTERA DE PRODUCTOS
22.13.5 DESARROLLOS RECIENTES
22.14 BRISTOL MYERS SQUIBB
22.14.1 INFORMACIÓN GENERAL DE LA EMPRESA
22.14.2 ANÁLISIS DE INGRESOS
22.14.3 PRESENCIA GEOGRÁFICA
22.14.4 CARTERA DE PRODUCTOS
22.14.5 DESARROLLOS RECIENTES
22.15 TG THERAPEUTICS, INC
22.15.1 INFORMACIÓN GENERAL DE LA EMPRESA
22.15.2 ANÁLISIS DE INGRESOS
22.15.3 PRESENCIA GEOGRÁFICA
22.15.4 CARTERA DE PRODUCTOS
22.15.5 DESARROLLOS RECIENTES
NOTA: LA LISTA DE EMPRESAS QUE SE MUESTRA NO ES EXHAUSTIVA Y SE AJUSTA A LOS REQUISITOS DE NUESTROS CLIENTES ANTERIORES. EN NUESTRO ESTUDIO ANALIZAMOS MÁS DE 100 EMPRESAS, POR LO QUE LA LISTA PUEDE MODIFICARSE O REEMPLAZARSE SI SE SOLICITA.
23 INFORMES RELACIONADOS
24 CONCLUSIÓN
25 CUESTIONARIO
26 ACERCA DE LA INVESTIGACIÓN DE MERCADO DE DATA BRIDGE
1 INTRODUCCIÓN
1.1 OBJETIVOS DEL ESTUDIO
1.2 DEFINICIÓN DE MERCADO
1.3 PANORAMA GENERAL DEL MERCADO EUROPEO DE TRATAMIENTO DE LA ESCLEROSIS MÚLTIPLE
1.4 MONEDA Y PRECIOS
1.5 LIMITACIÓN
1.6 MERCADOS CUBIERTOS
2 SEGMENTACIÓN DE MERCADO
2.1 CONCLUSIONES CLAVE
2.2 LLEGADA AL MERCADO EUROPEO DE TRATAMIENTO DE LA ESCLEROSIS MÚLTIPLE
2.2.1 CUADRÍCULA DE POSICIONAMIENTO DE PROVEEDORES
2.2.2 CURVA DEL CICLO DE VIDA DE LA TECNOLOGÍA
2.2.3 MODELO DE VALIDACIÓN DE DATOS TRÍPODE
2.2.4 GUÍA DE MERCADO
2.2.5 MODELADO MULTIVARIADO
2.2.6 ANÁLISIS DE ARRIBA A ABAJO
2.2.7 MATRIZ DE DESAFÍOS
2.2.8 CUADRÍCULA DE COBERTURA DE LA APLICACIÓN
2.2.9 NORMAS DE MEDICIÓN
2.2.10 ANÁLISIS DE LA PARTICIPACIÓN DE MERCADO DE LOS PROVEEDORES
2.2.11 DATOS DE VOLUMEN DE VENTAS
2.2.12 DATOS CLAVE DE LAS ENTREVISTAS PRIMARIAS
2.2.13 PUNTOS DE DATOS DE BASES DE DATOS SECUNDARIAS CLAVE
2.3 MERCADO EUROPEO DE TRATAMIENTO DE LA ESCLEROSIS MÚLTIPLE: RESUMEN DE LA INVESTIGACIÓN
2.4 SUPUESTOS
3. PANORAMA DEL MERCADO
3.1 CONDUCTORES
3.2 RESTRICCIONES
3.3 OPORTUNIDADES
3.4 DESAFÍOS
4 RESUMEN EJECUTIVO
5 PERSPECTIVAS PREMIUM
5.1 ANÁLISIS PESTEL
5.2 EL MODELO DE LAS CINCO FUERZAS DE PORTER
5.3 EVOLUCIÓN DEL MERCADO DE TRATAMIENTOS PARA LA EM EN EUROPA EN LOS ÚLTIMOS 10-20 AÑOS
6 PERSPECTIVAS DEL SECTOR
6.1 ANÁLISIS DE PATENTES
6.1.1 PANORAMA DE PATENTES
6.1.2 NÚMERO DE LA USPTO
6.1.3 VENCIMIENTO DE LA PATENTE
6.1.4 NÚMERO DE EPIO
6.1.5 FUERZA Y CALIDAD DE LAS PATENTES
6.1.6 REIVINDICACIONES DE PATENTE
6.1.7 CITAS DE PATENTES
6.1.8 LITIGIOS Y LICENCIAS DE PATENTES
6.1.9 EXPEDIENTE DE PATENTE
6.1.10 PAÍSES CONCEDIDOS A PATENTES
6.1.11 ANTECEDENTES TECNOLÓGICOS
6.2 TASA DE TRATAMIENTO FARMACOLÓGICO EN MERCADOS MADUROS
6.3 TENDENCIAS DEMOGRÁFICAS: IMPACTO EN TODAS LAS TASAS DE INCIDENCIA
6.4 DIAGRAMA DE FLUJO DE PACIENTES
6.5 ESTRATEGIAS CLAVE DE PRECIOS
6.6 ESTRATEGIAS CLAVE DE CAPTACIÓN DE PACIENTES
6.7 ENTREVISTAS CON ESPECIALISTAS
6.8 OTRAS INSTANTÁNEAS DE KOL
7 EPIDEMIOLOGÍA
7.1 INCIDENCIA DE TODOS POR GÉNERO
7.2 TASA DE TRATAMIENTO
7.3 TASA DE MORTALIDAD
7.4 MODELO DE ADHERENCIA A LA FARMACIA Y CAMBIO DE TERAPIA
7,5 TASAS DE ÉXITO DEL TRATAMIENTO DE PACIENTES
8 FUSIONES Y ADQUISICIONES
8.1 LICENCIAS
8.2 ACUERDOS DE COMERCIALIZACIÓN
9 MARCO REGULATORIO
9.1 PROCESO DE APROBACIÓN REGULATORIA
9.2 FACILIDAD DE APROBACIÓN REGULATORIA EN LAS REGIONES GEOGRÁFICAS
9.3 VÍAS DE APROBACIÓN REGULATORIA
9.4 LICENCIAS Y REGISTRO
9.5 VIGILANCIA POSTCOMERCIALIZACIÓN
9.6 DIRECTRICES DE BUENAS PRÁCTICAS DE FABRICACIÓN (BPF)
10 ANÁLISIS DE LA TUBERÍA
10.1 ENSAYOS CLÍNICOS Y ANÁLISIS DE FASE
10.2 DESARROLLO DE FARMACÉUTICA
10.3 CANDIDATOS DE LA FASE III
10.4 CANDIDATOS DE LA FASE II
10.5 CANDIDATOS DE LA FASE I
10.6 OTROS (PRECLÍNICOS Y DE INVESTIGACIÓN)
TABLA 1 MERCADO EUROPEO DE ENSAYOS CLÍNICOS PARA EL TRATAMIENTO DE LA ESCLEROSIS MÚLTIPLE
Nombre de la empresa Área terapéutica
XX XX
XX XX
XX XX
XX XX
XX XX
XX XX
Fuentes: Comunicados de prensa, informes anuales, documentos presentados ante la SEC, presentaciones para inversores, otras fuentes gubernamentales, análisis basado en información secundaria y entrevistas con expertos.
TABLA 2 DISTRIBUCIÓN DE PRODUCTOS Y PROYECTOS POR FASE DEL MERCADO DE TRATAMIENTO DE LA ESCLEROSIS MÚLTIPLE
Número de fase de los proyectos
Proyectos preclínicos/de investigación XX
Desarrollo Clínico XX
Fase I XX
Fase II XX
Fase III XX
Solicitud presentada/aprobada en EE. UU., pero aún no comercializada XX
Total XX
Fuentes: Comunicados de prensa, informes anuales, documentos presentados ante la SEC, presentaciones para inversores, otras fuentes gubernamentales, análisis basado en información secundaria y entrevistas con expertos.
TABLA 3 DISTRIBUCIÓN DE PROYECTOS POR ÁREA TERAPÉUTICA Y FASE MERCADO DE TRATAMIENTO DE LA ESCLEROSIS MÚLTIPLE
Área terapéutica Proyecto preclínico/de investigación
XX XX
XX XX
XX XX
XX XX
XX XX
Total de proyectos XX
Fuentes: Comunicados de prensa, informes anuales, documentos presentados ante la SEC, presentaciones para inversores, otras fuentes gubernamentales, análisis basado en información secundaria y entrevistas con expertos.
TABLA 4 DISTRIBUCIÓN DE PROYECTOS POR ENFOQUE CIENTÍFICO Y FASE MERCADO DE TRATAMIENTO DE LA ESCLEROSIS MÚLTIPLE
Proyecto de investigación/preclínica tecnológica
XX XX
XX XX
XX XX
XX XX
XX XX
Total de proyectos XX
Fuentes: Comunicados de prensa, informes anuales, documentos presentados ante la SEC, presentaciones para inversores, otras fuentes gubernamentales, análisis basado en información secundaria y entrevistas con expertos.
FIGURA 1 PRINCIPALES ENTIDADES SEGÚN EL ANÁLISIS DE I+D PARA EL MERCADO DE TRATAMIENTO DE LA ESCLEROSIS MÚLTIPLE
Fuentes: Comunicados de prensa, informes anuales, documentos presentados ante la SEC, presentaciones para inversores, otras fuentes gubernamentales, análisis basado en información secundaria y entrevistas con expertos.
11 ANÁLISIS DE MEDICAMENTOS COMERCIALIZADOS
11.1 DROGA
11.1.1 NOMBRE DE LA MARCA
11.1.2 NOMBRE GENÉRICO
11.2 INDICACIÓN TERAPÉUTICA
11.3 CLASE FARMACOLÓGICA DEL MEDICAMENTO
11.4 INDICACIÓN PRINCIPAL DEL MEDICAMENTO
11.5 ESTADO DEL MERCADO
11.6 TIPO DE MEDICAMENTO
11.7 FORMULARIO DE DOSIFICACIÓN DE MEDICAMENTOS
11.8 DISPONIBILIDAD DE DOSIS
11.9 VÍA DE ADMINISTRACIÓN DEL MEDICAMENTO
11.1 FRECUENCIA DE DOSIFICACIÓN
11.11 INFORMACIÓN SOBRE FÁRMACOS
11.12 UNA VISIÓN GENERAL DE LAS ACTIVIDADES DE DESARROLLO DE FÁRMACOS, COMO LOS HITOS REGULATORIOS, LOS DATOS DE SEGURIDAD Y EFICACIA, Y LOS DATOS DE EXCLUSIVIDAD DE MERCADO.
11.12.1 PRONÓSTICO DE LAS PERSPECTIVAS DEL MERCADO
11.12.2 COMPETENCIA CRUZADA
11.12.3 CARTERA TERAPÉUTICA
11.12.4 ESCENARIO DE DESARROLLO ACTUAL
12 ACCESO AL MERCADO
12.1 PRONÓSTICO DE MERCADO A 10 AÑOS
12.2 ACTUALIZACIONES RECIENTES DE ENSAYOS CLÍNICOS
12,3 NUEVOS MEDICAMENTOS APROBADOS POR LA FDA ANUALMENTE
12.4 FABRICANTE Y DISTRIBUCIÓN DE DROGAS
12.5 CONSUMO DE MEDICAMENTOS IMPORTANTES
12.6 PRÁCTICAS DE TRATAMIENTO ACTUALES
12.7 IMPACTO DE LA PRÓXIMA TERAPIA
13 ANÁLISIS DE I+D
13.1 ANÁLISIS COMPARATIVO
13.2 PANORAMA DEL DESARROLLO DE FÁRMACOS
13.3 ANÁLISIS DETALLADO DE LOS HITOS REGULATORIOS
13.4 EVALUACIÓN TERAPÉUTICA
13.5 COLABORACIONES Y ASOCIACIONES BASADAS EN ACTIVOS
14. PANORAMA DEL MERCADO
14.1 CONDUCTORES
14.2 RESTRICCIONES
14.3 OPORTUNIDADES
14.4 DESAFÍOS
15. MERCADO EUROPEO DE TRATAMIENTO DE LA ESCLEROSIS MÚLTIPLE, POR TIPO
15.1 GENERALIDADES
15.2 SÍNDROME CLÍNICAMENTE AISLADO (SCA)
15.3 ESCLEROSIS MÚLTIPLE REMITENTE-RECURRIENTE (EMRR)
15.4 ESCLEROSIS MÚLTIPLE PROGRESIVA SECUNDARIA (EMPS)
15.5 ESCLEROSIS MÚLTIPLE PROGRESIVA PRIMARIA (EMPP)
15.6 ESCLEROSIS MÚLTIPLE REMITENTE GRAVE (RES)
16. MERCADO EUROPEO DE TRATAMIENTOS PARA LA ESCLEROSIS MÚLTIPLE, POR TERAPÉUTICA
16.1 GENERALIDADES
16.2 MEDICAMENTOS APROBADOS/COMERCIALIZADOS
16.2.1 TERAPIAS PREVENTIVAS
16.2.1.1. MEDICACIÓN ORAL
16.2.1.1.1. TECFIDERA
16.2.1.1.2. GIleneya
16.2.1.1.3. AUBAGIO
16.2.1.1.4. MAVENCLAD
16.2.1.1.5. MAYZENT
16.2.1.1.6. VENCERIDAD
16.2.1.1.7. OTROS
16.2.1.2. MEDICAMENTO INYECTABLE
16.2.1.2.1. INTERFERÓN BETA-1A
16.2.1.2.1.1 AVONEX
16.2.1.2.1.2 REBIF
16.2.1.2.1.3 OTROS
16.2.1.2.2. ACETATO DE GLATIRAMER
16.2.1.2.2.1 COPAXONA
16.2.1.2.2.2 GLATOPA
16.2.1.2.2.3 OTROS
16.2.1.2.3. INTERFERÓN BETA-1B
16.2.1.2.3.1 BETASERON
16.2.1.2.3.2 EXTAVIA
16.2.1.2.4. PLEGRIDY/PEGINTERFERÓN BETA-1A
16.2.1.2.5. FÁRMACO DE QUIMIOTERAPIA
16.2.1.2.6. ANTICUERPOS MONOCLONALES
16.2.1.3. MEDICAMENTO INFUSIONADO
16.2.1.3.1. TYSABRI
16.2.1.3.2. OCREVUS
16.2.1.3.3. LEMTRADA
16.2.1.3.4. MITOXANTRONA
16.2.1.3.5. NOVANTRONE
16.2.1.3.6. OTROS
16.2.1.4. TRASPLANTE DE CÉLULAS MADRE HEMATOPOYÉTICAS (TCMH)
16.2.2 TERAPIAS ABORTIVAS/TRATAMIENTO DE LAS EXACERBACIONES AGUDAS
16.2.2.1. CORTICOSTEROIDES
16.2.2.1.1. PREDNISONA ORAL
16.2.2.1.2. METILPREDNISOLONA
16.2.2.1.3. DEXAMETASONA
16.2.2.1.4. PREDNISOLONA
16.2.2.1.5. BETAMETASONA
16.2.2.1.6. OTROS
16.2.2.2. BENZODIAZEPINAS
16.2.2.2.1. CLONAZEPAM
16.2.2.2.2. DIAZEPAM
16.2.2.2.3. OTROS
16.2.2.3. INMUNOSUPRESORES
16.2.2.3.1. AZATIOPRINA
16.2.2.3.2. CICLOFOSFAMIDA
16.2.2.3.3. METOTREXATO
16.2.2.3.4. MITOXANTRONA
16.2.2.3.5. OTROS
16.2.2.4. MODULADORES DEL RECEPTOR DE ESFINGOSINA 1-FOSFATO
16.2.2.4.1. SIPONIMOD
16.2.2.4.2. FINGOLIMOD
16.2.2.4.3. OZANIMOD
16.2.2.4.4. OTROS
16.2.2.5. AGONISTAS DE LA DOPAMINA
16.2.2.5.1. OSMOLEX ER
16.2.2.5.2. GOCOVRI
16.2.2.5.3. OTROS
16.2.2.6. BLOQUEADORES NEUROMUSCULARES
16.2.2.6.1. BOTOX
16.2.2.6.2. BOTOX COSMÉTICO
16.2.2.6.3. TOXINA BOTULÍNICA
16.2.2.7. HORMONA ADRENOCORTICOTRÓPICA
16.2.2.8. INMUNOGLOBULINA INTRAVENOSA
16.2.2.9. PLASMAFÉRESIS
16.2.2.10. OTROS
16.2.3 TERAPIAS SINTOMÁTICAS
16.2.3.1. RELAJANTES MUSCULARES
16.2.3.1.1. LIORESAL
16.2.3.1.2. ZANAFLEX
16.2.3.1.3. OTROS
16.2.3.2. MEDICAMENTOS PARA LA FATIGA
16.2.3.2.1. GOCOVRI
16.2.3.2.2. OSMOLEX
16.2.3.2.3. PROVIGIL
16.2.3.2.4. RITALINO
16.2.3.2.5. OTROS
16.2.3.3. ESTIMULANTES
16.2.3.3.1. MODAFINIL
16.2.3.3.2. ARMODAFINIL
16.2.3.3.3. OTROS
16.2.3.4. ANTICONVULSANTES
16.2.3.4.1. GABAPENTINA
16.2.3.4.2. CARBAMAZEPINA
16.2.3.4.3. PREGABALINA
16.2.3.4.4. TOPIRAMATO
16.2.3.4.5. OTROS
16.2.3.5. FÁRMACOS ANTIINFLAMATORIOS NO ESTEROIDEOS
16.2.3.5.1. IBUPROFENO
16.2.3.5.2. NAPROXEN
16.2.3.5.3. DICLOFENACO
16.2.3.5.4. INDOMETACINA
16.2.3.5.5. OTROS
16.2.3.6. ANTIDIARRÉICOS
16.2.3.7. BLOQUEADORES DE LOS CANALES DE POTASIO
16.2.3.8. FISIOTERAPIA
16.2.3.9. LAXANTES
16.2.3.10. OTROS
16.3 DROGAS EN TUBERÍAS
16.3.1 SCM-0101
16.3.2 IMCY-MS-001
16.3.3 TUBERÍA-307
16.3.4 ATA188
16.3.5 WP1303
16.3.6 PARA ALUMAB
16.3.7 OTROS
17. MERCADO EUROPEO DE TRATAMIENTO DE LA ESCLEROSIS MÚLTIPLE, POR TIPO DE FÁRMACO
17.1 GENERALIDADES
17.2 DE MARCA
17.2.1 TECFIDERA
17.2.2 GIleneya
17.2.3 AUBAGIO
17.2.4 AVONEX
17.2.5 TYSABRI
17.2.6 REBIF
17.2.7 COPAXONA
17.2.8 8 BETASERON
17.2.9 AMPYRA/FAMPYRA
17.2.10 OTROS
17.3 GENÉRICOS
18. MERCADO EUROPEO DE TRATAMIENTOS PARA LA ESCLEROSIS MÚLTIPLE, POR VÍA DE ADMINISTRACIÓN
18.1 GENERALIDADES
18.2 ORAL
18.2.1 COMPRIMIDOS
18.2.2 CÁPSULAS
18.2.3 OTROS
18.3 PARENTERAL
18.3.1 INTRAVENOSA
18.3.2 SUBCUTÁNEO
18.3.3 OTROS
18.4 OTROS
19. MERCADO EUROPEO DE TRATAMIENTO DE LA ESCLEROSIS MÚLTIPLE, POR GRUPO DE EDAD
19.1 GENERALIDADES
19.2 PEDIÁTRICO
19.2.1 MASCULINO
19.2.2 MUJER
19.3 ADULT
19.3.1 MASCULINO
19.3.2 MUJER
19.4 GERIÁTRICO
19.4.1 MASCULINO
19.4.2 MUJER
20 MERCADO EUROPEO DE TRATAMIENTO DE LA ESCLEROSIS MÚLTIPLE, POR GÉNERO
20.1 GENERALIDADES
20.2 HOMBRE
20.3 MUJER
21. MERCADO EUROPEO DE TRATAMIENTO DE LA ESCLEROSIS MÚLTIPLE, POR USUARIO FINAL
21.1 GENERALIDADES
21.2 HOSPITALES
21.2.1 PÚBLICO
21.2.1.1. NIVEL 1
21.2.1.2. NIVEL 2
21.2.1.3. NIVEL 3
21.2.2 PRIVADO
21.2.2.1. NIVEL 1
21.2.2.2. NIVEL 2
21.2.2.3. NIVEL 3
21.3 ATENCIÓN DOMICILIARIA
21.4 CENTRO DE ESPECIALIDADES
21.5 INSTITUTOS ACADÉMICOS Y DE INVESTIGACIÓN
21,6 OTROS
22. MERCADO EUROPEO DE TRATAMIENTO DE LA ESCLEROSIS MÚLTIPLE, POR CANAL DE DISTRIBUCIÓN
22.1 GENERALIDADES
22.2 LICITACIONES DIRECTAS
22,3 VENTAS MINORISTAS
22.3.1 EN LÍNEA
22.3.1.1. TIENDAS ELECTRÓNICAS
22.3.1.2. SITIO WEB DE LA EMPRESA
22.3.1.3. OTROS
22.3.2 SIN CONEXIÓN
22.3.2.1. FARMACIA HOSPITALARIA
22.3.2.2. FARMACIA MINORISTA
22.3.2.3. OTROS
22,4 OTROS
23. MERCADO EUROPEO DE TRATAMIENTO DE LA ESCLEROSIS MÚLTIPLE: PANORAMA EMPRESARIAL
23.1 ANÁLISIS DE ACCIONES DE LA EMPRESA: EUROPA
23.2 FUSIONES Y ADQUISICIONES
23.3 DESARROLLO Y APROBACIÓN DE NUEVOS PRODUCTOS
23.4 EXPANSIONES
23.5 CAMBIOS REGULATORIOS
23.6 ALIANZAS Y OTROS DESARROLLOS ESTRATÉGICOS
24. MERCADO EUROPEO DE TRATAMIENTO DE LA ESCLEROSIS MÚLTIPLE: ANÁLISIS FODA Y DBMR
25 MERCADO EUROPEO DE TRATAMIENTO DE LA ESCLEROSIS MÚLTIPLE, POR PAÍS
MERCADO EUROPEO DE TRATAMIENTO DE LA ESCLEROSIS MÚLTIPLE (TODA LA SEGMENTACIÓN PROPORCIONADA ANTERIORMENTE SE PRESENTA EN ESTE CAPÍTULO POR PAÍS)
25.1 EUROPA
25.1.1 ALEMANIA
25.1.2 FRANCIA
25.1.3 Reino Unido
25.1.4 ITALIA
25.1.5 ESPAÑA
25.1.6 RUSIA
25.1.7 TURQUÍA
25.1.8 BÉLGICA
25.1.9 DINAMARCA
25.1.10 PAÍSES BAJOS
25.1.11 SUIZA
25.1.12 SUECIA
25.1.13 POLONIA
25.1.14 NORUEGA
25.1.15 FINLAND
25.1.16 RESTO DE EUROPA
25.2 PRINCIPALES CONCLUSIONES: POR PAÍSES PRINCIPALES
26. MERCADO EUROPEO DE TRATAMIENTO DE LA ESCLEROSIS MÚLTIPLE, PERFIL DE LA EMPRESA
26.1 FABRICANTES COMERCIALIZADOS/APROBADOS
26.1.1 BIOGEN
26.1.1.1. INFORMACIÓN GENERAL DE LA EMPRESA
26.1.1.2. ANÁLISIS DE INGRESOS
26.1.1.3. PRESENCIA GEOGRÁFICA
26.1.1.4. CARTERA DE PRODUCTOS
26.1.1.5. DESARROLLOS RECIENTES
26.1.2 NOVARTIS AG
26.1.2.1. INFORMACIÓN GENERAL DE LA EMPRESA
26.1.2.2. ANÁLISIS DE INGRESOS
26.1.2.3. PRESENCIA GEOGRÁFICA
26.1.2.4. CARTERA DE PRODUCTOS
26.1.2.5. DESARROLLOS RECIENTES
26.1.3 GENZYME CORPORATION (UNA SUBSIDIARIA DE SANOFI)
26.1.3.1. INFORMACIÓN GENERAL DE LA EMPRESA
26.1.3.2. ANÁLISIS DE INGRESOS
26.1.3.3. PRESENCIA GEOGRÁFICA
26.1.3.4. CARTERA DE PRODUCTOS
26.1.3.5. DESARROLLOS RECIENTES
26.1.4 MERCK KGAA
26.1.4.1. INFORMACIÓN GENERAL DE LA EMPRESA
26.1.4.2. ANÁLISIS DE INGRESOS
26.1.4.3. PRESENCIA GEOGRÁFICA
26.1.4.4. CARTERA DE PRODUCTOS
26.1.4.5. DESARROLLOS RECIENTES
26.1.5 TEVA PHARMACEUTICALS USA, INC. (UNA SUBSIDIARIA DE TEVA PHARMACEUTICALS INDUSTRIES LTD.)
26.1.5.1. INFORMACIÓN GENERAL DE LA EMPRESA
26.1.5.2. ANÁLISIS DE INGRESOS
26.1.5.3. PRESENCIA GEOGRÁFICA
26.1.5.4. CARTERA DE PRODUCTOS
26.1.5.5. DESARROLLOS RECIENTES
26.1.6 F. HOFFMANN-LA ROCHE LTD
26.1.6.1. INFORMACIÓN GENERAL DE LA EMPRESA
26.1.6.2. ANÁLISIS DE INGRESOS
26.1.6.3. PRESENCIA GEOGRÁFICA
26.1.6.4. CARTERA DE PRODUCTOS
26.1.6.5. DESARROLLOS RECIENTES
26.1.7 ACORDA THERAPEUTICS, INC
26.1.7.1. INFORMACIÓN GENERAL DE LA EMPRESA
26.1.7.2. ANÁLISIS DE INGRESOS
26.1.7.3. PRESENCIA GEOGRÁFICA
26.1.7.4. CARTERA DE PRODUCTOS
26.1.7.5. DESARROLLOS RECIENTES
26.1.8 AMNEAL PHARMACEUTICALS LLC
26.1.8.1. INFORMACIÓN GENERAL DE LA EMPRESA
26.1.8.2. ANÁLISIS DE INGRESOS
26.1.8.3. PRESENCIA GEOGRÁFICA
26.1.8.4. CARTERA DE PRODUCTOS
26.1.8.5. DESARROLLOS RECIENTES
26.1.9 BAYER AG
26.1.9.1. INFORMACIÓN GENERAL DE LA EMPRESA
26.1.9.2. ANÁLISIS DE INGRESOS
26.1.9.3. PRESENCIA GEOGRÁFICA
26.1.9.4. CARTERA DE PRODUCTOS
26.1.9.5. DESARROLLOS RECIENTES
26.1.10 CELGENE CORPORATION (UNA SUBSIDIARIA DE BRISTOL-MYERS SQUIBB COMPANY)
26.1.10.1. INFORMACIÓN GENERAL DE LA EMPRESA
26.1.10.2. ANÁLISIS DE INGRESOS
26.1.10.3. PRESENCIA GEOGRÁFICA
26.1.10.4. CARTERA DE PRODUCTOS
26.1.10.5. DESARROLLOS RECIENTES
26.1.11 HIKMA PHARMACEUTICALS PLC
26.1.11.1. INFORMACIÓN GENERAL DE LA EMPRESA
26.1.11.2. ANÁLISIS DE INGRESOS
26.1.11.3. PRESENCIA GEOGRÁFICA
26.1.11.4. CARTERA DE PRODUCTOS
26.1.11.5. DESARROLLOS RECIENTES
26.1.12 MALLINCKRODT FARMACÉUTICOS
26.1.12.1. INFORMACIÓN GENERAL DE LA EMPRESA
26.1.12.2. ANÁLISIS DE INGRESOS
26.1.12.3. PRESENCIA GEOGRÁFICA
26.1.12.4. CARTERA DE PRODUCTOS
26.1.12.5. DESARROLLOS RECIENTES
26.1.13 VITARIS INC.
26.1.13.1. INFORMACIÓN GENERAL DE LA EMPRESA
26.1.13.2. ANÁLISIS DE INGRESOS
26.1.13.3. PRESENCIA GEOGRÁFICA
26.1.13.4. CARTERA DE PRODUCTOS
26.1.13.5. DESARROLLOS RECIENTES
26.1.14 PAR PHARMACEUTICAL (UNA SUBSIDIARIA DE ENDO INTERNATIONAL PLC)
26.1.14.1. INFORMACIÓN GENERAL DE LA EMPRESA
26.1.14.2. ANÁLISIS DE INGRESOS
26.1.14.3. PRESENCIA GEOGRÁFICA
26.1.14.4. CARTERA DE PRODUCTOS
26.1.14.5. DESARROLLOS RECIENTES
26.1.15 PFIZER INC.
26.1.15.1. INFORMACIÓN GENERAL DE LA EMPRESA
26.1.15.2. ANÁLISIS DE INGRESOS
26.1.15.3. PRESENCIA GEOGRÁFICA
26.1.15.4. CARTERA DE PRODUCTOS
26.1.15.5. DESARROLLOS RECIENTES
26.1.16 ZYDUS PHARMACEUTICALS, INC. (UNA SUBSIDIARIA DE ZYDUS CADILA)
26.1.16.1. INFORMACIÓN GENERAL DE LA EMPRESA
26.1.16.2. ANÁLISIS DE INGRESOS
26.1.16.3. PRESENCIA GEOGRÁFICA
26.1.16.4. CARTERA DE PRODUCTOS
26.1.16.5. DESARROLLOS RECIENTES
26.1.17 JOHNSON & JOHNSON CONSUMER INC.
26.1.17.1. INFORMACIÓN GENERAL DE LA EMPRESA
26.1.17.2. CARTERA DE PRODUCTOS
26.1.17.3. ANÁLISIS DE INGRESOS
26.1.17.4. PRESENCIA GEOGRÁFICA
26.1.17.5. CARTERA DE PRODUCTOS
26.1.18 PERRIGO COMPANY PLC,
26.1.18.1. INFORMACIÓN GENERAL DE LA EMPRESA
26.1.18.2. CARTERA DE PRODUCTOS
26.1.18.3. ANÁLISIS DE INGRESOS
26.1.18.4. PRESENCIA GEOGRÁFICA
26.1.18.5. CARTERA DE PRODUCTOS
26.1.19 GLENMARK PHARMACEUTICAL INC., EE. UU.
26.1.19.1. INFORMACIÓN GENERAL DE LA EMPRESA
26.1.19.2. ANÁLISIS DE INGRESOS
26.1.19.3. PRESENCIA GEOGRÁFICA
26.1.19.4. CARTERA DE PRODUCTOS
26.1.19.5. DESARROLLOS RECIENTES
26.1.20 GLAXOSMITHKLINE PLC.
26.1.20.1. INFORMACIÓN GENERAL DE LA EMPRESA
26.1.20.2. CARTERA DE PRODUCTOS
26.1.20.3. ANÁLISIS DE INGRESOS
26.1.20.4. PRESENCIA GEOGRÁFICA
26.1.20.5. CARTERA DE PRODUCTOS
26.2 EMPRESAS DE OLEODUCTOS
26.2.1 IMCYSE
26.2.1.1. INFORMACIÓN GENERAL DE LA EMPRESA
26.2.1.2. CARTERA DE PRODUCTOS
26.2.1.3. ANÁLISIS DE INGRESOS
26.2.1.4. PRESENCIA GEOGRÁFICA
26.2.1.5. CARTERA DE PRODUCTOS
26.2.2 WORG PHARMACEUTICALS (ZHEJIANG) CO., LTD.
26.2.2.1. INFORMACIÓN GENERAL DE LA EMPRESA
26.2.2.2. CARTERA DE PRODUCTOS
26.2.2.3. ANÁLISIS DE INGRESOS
26.2.2.4. PRESENCIA GEOGRÁFICA
26.2.2.5. CARTERA DE PRODUCTOS
26.2.3 CIENCIAS DE LA VIDA TIZIANA
26.2.3.1. INFORMACIÓN GENERAL DE LA EMPRESA
26.2.3.2. CARTERA DE PRODUCTOS
26.2.3.3. ANÁLISIS DE INGRESOS
26.2.3.4. PRESENCIA GEOGRÁFICA
26.2.3.5. CARTERA DE PRODUCTOS
27 INFORMES RELACIONADOS
28 CONCLUSIÓN
29 CUESTIONARIO
30 SOBRE LA INVESTIGACIÓN DE MERCADO DE DATA BRIDGE
Metodología de investigación
La recopilación de datos y el análisis del año base se realizan utilizando módulos de recopilación de datos con muestras de gran tamaño. La etapa incluye la obtención de información de mercado o datos relacionados a través de varias fuentes y estrategias. Incluye el examen y la planificación de todos los datos adquiridos del pasado con antelación. Asimismo, abarca el examen de las inconsistencias de información observadas en diferentes fuentes de información. Los datos de mercado se analizan y estiman utilizando modelos estadísticos y coherentes de mercado. Además, el análisis de la participación de mercado y el análisis de tendencias clave son los principales factores de éxito en el informe de mercado. Para obtener más información, solicite una llamada de un analista o envíe su consulta.
La metodología de investigación clave utilizada por el equipo de investigación de DBMR es la triangulación de datos, que implica la extracción de datos, el análisis del impacto de las variables de datos en el mercado y la validación primaria (experto en la industria). Los modelos de datos incluyen cuadrícula de posicionamiento de proveedores, análisis de línea de tiempo de mercado, descripción general y guía del mercado, cuadrícula de posicionamiento de la empresa, análisis de patentes, análisis de precios, análisis de participación de mercado de la empresa, estándares de medición, análisis global versus regional y de participación de proveedores. Para obtener más información sobre la metodología de investigación, envíe una consulta para hablar con nuestros expertos de la industria.
Personalización disponible
Data Bridge Market Research es líder en investigación formativa avanzada. Nos enorgullecemos de brindar servicios a nuestros clientes existentes y nuevos con datos y análisis que coinciden y se adaptan a sus objetivos. El informe se puede personalizar para incluir análisis de tendencias de precios de marcas objetivo, comprensión del mercado de países adicionales (solicite la lista de países), datos de resultados de ensayos clínicos, revisión de literatura, análisis de mercado renovado y base de productos. El análisis de mercado de competidores objetivo se puede analizar desde análisis basados en tecnología hasta estrategias de cartera de mercado. Podemos agregar tantos competidores sobre los que necesite datos en el formato y estilo de datos que esté buscando. Nuestro equipo de analistas también puede proporcionarle datos en archivos de Excel sin procesar, tablas dinámicas (libro de datos) o puede ayudarlo a crear presentaciones a partir de los conjuntos de datos disponibles en el informe.