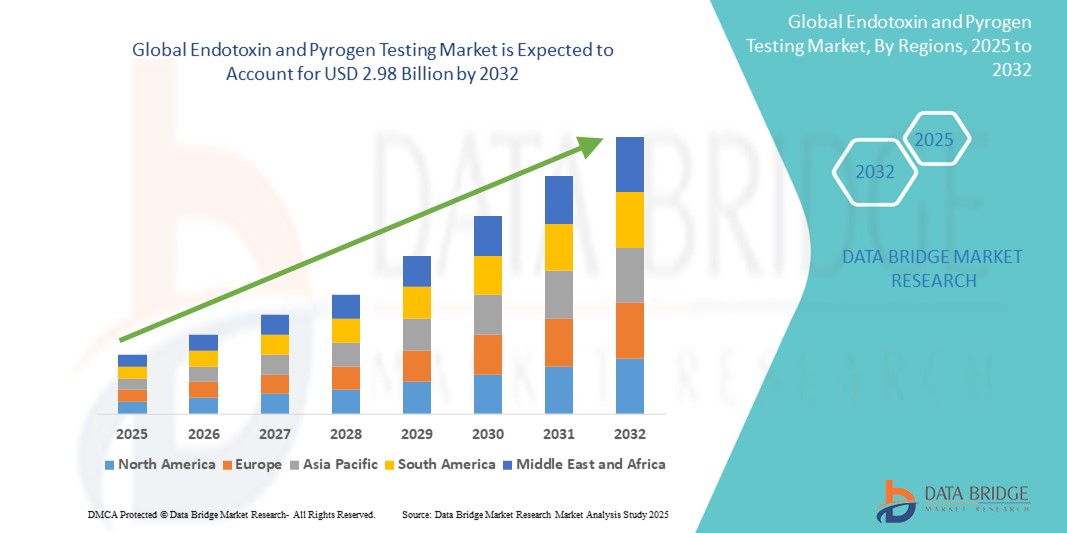
Global Endotoxin And Pyrogen Testing Market
Tamaño del mercado en miles de millones de dólares
Tasa de crecimiento anual compuesta (CAGR) :
% 
 USD
1.27 Billion
USD
2.98 Billion
2024
2032
USD
1.27 Billion
USD
2.98 Billion
2024
2032
| 2025 –2032 | |
| USD 1.27 Billion | |
| USD 2.98 Billion | |
|
|
|
|
Segmentación del mercado global de pruebas de endotoxinas y pirógenos, por producto y servicios (kits y reactivos de detección, instrumentos y sistemas, servicios de pruebas de endotoxinas y pirógenos, y consumibles y accesorios), tipo de prueba (prueba de lisado de amebocitos de Limulus (LAL), pruebas de TAL, prueba de activación de monocitos (MAT), ensayo de C recombinante (RFC), in vitro y prueba de pirógenos de conejo), tipo (prueba de endotoxinas y pirógenos preformada, prueba de proendotoxinas y pirógenos y prueba combinada de endotoxinas y pirógenos), categoría de producto (ingrediente de etiqueta limpia y convencional), forma (polvo y líquido) aplicación (fabricación farmacéutica, fabricación de dispositivos médicos, producción de materias primas y fabricación de envases), método (prueba de endotoxinas y pirógenos de coágulo de gel, prueba cromogénica de endotoxinas y pirógenos y prueba turbidimétrica de endotoxinas y pirógenos), modo de compra (grupo grande, mediano y grande) Grupos pequeños e individuales), producto final (vacunas y/o CGT, productos biológicos, inyectables y otros), usuario final (empresas farmacéuticas, empresas de biotecnología, empresas biomédicas, empresas de dispositivos médicos, organizaciones de investigación por contrato (CRO), organizaciones de fabricación por contrato (CMO) y otras): tendencias de la industria y pronóstico hasta 2032
Tamaño del mercado de pruebas de endotoxinas y pirógenos
- El tamaño del mercado global de pruebas de endotoxinas y pirógenos se valoró en USD 1.27 mil millones en 2024 y se espera que alcance los USD 2.98 mil millones para 2032 , con una CAGR del 11,3% durante el período de pronóstico.
- El crecimiento del mercado está impulsado en gran medida por la creciente adopción y el avance tecnológico en los procesos de control de calidad farmacéutico y bioseguridad, lo que conduce a una mayor digitalización y automatización en la fabricación de productos farmacéuticos, biotecnológicos y de dispositivos médicos.
- Además, la creciente demanda de métodos de detección de endotoxinas y pirógenos precisos, rápidos y que cumplan con la normativa está consolidando las pruebas de endotoxinas y pirógenos como un componente fundamental de los flujos de trabajo modernos de producción de productos farmacéuticos y dispositivos médicos. Estos factores convergentes están acelerando la adopción de soluciones de pruebas de endotoxinas y pirógenos, impulsando así significativamente el crecimiento de la industria.
Análisis del mercado de pruebas de endotoxinas y pirógenos
- Las pruebas de endotoxinas y pirógenos, que ofrecen una garantía crítica de seguridad biológica mediante la detección de endotoxinas y pirógenos bacterianos dañinos en productos farmacéuticos y médicos, son cada vez más vitales en la atención médica moderna, la biofarmacéutica y la fabricación de dispositivos debido a su función para garantizar el cumplimiento normativo y la seguridad del paciente.
- La creciente demanda de pruebas de endotoxinas y pirógenos se ve impulsada principalmente por la expansión de la industria biofarmacéutica, la creciente incidencia de enfermedades crónicas que requieren terapias inyectables y un mayor escrutinio regulatorio en torno al control de la contaminación en medicamentos inyectables, vacunas y dispositivos implantables.
- Norteamérica dominó el mercado de análisis de endotoxinas y pirógenos, con la mayor participación en ingresos, un 40,01 % en 2024. Esto se caracterizó por una rápida adopción regulatoria, una sólida inversión en investigación biotecnológica y la presencia de importantes empresas que ofrecen soluciones de análisis avanzadas. EE. UU. captó el 81 % del mercado regional, impulsado por un aumento en la producción de productos biológicos y la creciente adopción de tecnologías de análisis automatizadas y recombinantes en laboratorios con certificación GMP.
- Se proyecta que Asia-Pacífico será la región de más rápido crecimiento en el mercado de pruebas de endotoxinas y pirógenos durante el período de pronóstico, con una CAGR del 24,02 % entre 2025 y 2032, impulsada por la rápida industrialización, la expansión de la capacidad de fabricación farmacéutica y el creciente apoyo gubernamental a la infraestructura de control de calidad en países como China, India y Japón.
- El segmento de kits de detección y reactivos dominó el mercado de pruebas de endotoxinas y pirógenos con una participación del 46,8 % en 2024, debido a su aplicación generalizada, facilidad de uso y papel crucial en los protocolos de garantía de calidad de rutina en empresas farmacéuticas y biotecnológicas.
Alcance del informe y segmentación del mercado de pruebas de endotoxinas y pirógenos
|
Atributos |
Análisis de endotoxinas y pirógenos: Perspectivas clave del mercado |
|
Segmentos cubiertos |
|
|
Países cubiertos |
América del norte
Europa
Asia-Pacífico
Oriente Medio y África
Sudamerica
|
|
Actores clave del mercado |
|
|
Oportunidades de mercado |
|
|
Conjuntos de información de datos de valor añadido |
Además de los conocimientos sobre escenarios de mercado, como valor de mercado, tasa de crecimiento, segmentación, cobertura geográfica y actores principales, los informes de mercado seleccionados por Data Bridge Market Research también incluyen análisis en profundidad de expertos, análisis de precios, análisis de participación de marca, encuesta de consumidores, análisis demográfico, análisis de la cadena de suministro, análisis de la cadena de valor, descripción general de materias primas/consumibles, criterios de selección de proveedores, análisis PESTLE, análisis de Porter y marco regulatorio. |
Tendencias del mercado de pruebas de endotoxinas y pirógenos
Creciente demanda de precisión, cumplimiento y soluciones de pruebas rápidas
- Una tendencia significativa y en auge en el mercado de pruebas de endotoxinas y pirógenos de Asia-Pacífico es el mayor énfasis en la precisión, la rapidez de entrega y el cumplimiento normativo en la fabricación de productos farmacéuticos y dispositivos médicos. Esta demanda impulsa el desarrollo y la adopción de soluciones de prueba estandarizadas y de alta sensibilidad.
- Por ejemplo, los actores líderes están introduciendo pruebas de endotoxinas basadas en el factor C recombinante (rFC) que eliminan el uso de reactivos derivados de animales, al tiempo que garantizan resultados precisos y consistentes, abordando así las preocupaciones éticas y regulatorias.
- Los avances tecnológicos en sistemas automatizados también permiten a los laboratorios optimizar los procesos de detección de endotoxinas, reducir la intervención manual y mejorar la reproducibilidad. Los lectores de placas automatizados y los kits de detección basados en cartuchos están ganando popularidad gracias a su fácil manejo y sus mínimos márgenes de error.
- La integración de software avanzado con equipos de prueba permite una mejor trazabilidad, monitoreo en tiempo real y una generación más sencilla de informes de datos, todo lo cual es fundamental para el cumplimiento de las BPM. Esto es especialmente relevante para las compañías farmacéuticas que amplían la producción de inyectables estériles, vacunas y productos biológicos.
- Además, la creciente colaboración entre los gobiernos regionales y los fabricantes farmacéuticos para mejorar la infraestructura de atención médica, particularmente después de la COVID-19, ha acelerado la necesidad de protocolos confiables de pruebas de endotoxinas y pirógenos en toda la cadena de suministro.
- Como resultado, los fabricantes se están centrando en producir sistemas de prueba compactos, automatizados y altamente sensibles adaptados a laboratorios de gran volumen, lo que está cambiando las expectativas de eficiencia, cumplimiento y escalabilidad en entornos de control de calidad.
Dinámica del mercado de pruebas de endotoxinas y pirógenos
Conductor
Necesidad creciente debido al aumento de los riesgos de contaminación y las exigencias regulatorias.
- La creciente prevalencia de riesgos de contaminación en la producción farmacéutica, biotecnológica y de dispositivos médicos, junto con marcos regulatorios más estrictos, es un factor importante para la mayor demanda de soluciones de pruebas de endotoxinas y pirógenos.
- Por ejemplo, en abril de 2024, Onity, Inc. (Honeywell International, Inc.) anunció avances en tecnologías de seguridad biofarmacéutica, con el objetivo de integrar sensores de detección en tiempo real en entornos de fabricación aséptica. Se espera que estos avances, realizados por actores clave, impulsen el crecimiento del mercado de pruebas de endotoxinas y pirógenos en la región Asia-Pacífico.
- A medida que las empresas priorizan la seguridad del paciente y el cumplimiento normativo, pruebas como el lisado de amebocitos de Limulus (LAL) y la prueba de activación de monocitos (MAT) se adoptan cada vez más por su capacidad para detectar niveles mínimos de endotoxinas en medicamentos inyectables, vacunas y dispositivos implantables.
- Además, el auge de los productos biológicos y los medicamentos personalizados está impulsando la necesidad de métodos de análisis fiables y de alto rendimiento que se integren a la perfección en los procesos de control de calidad. Las plataformas de análisis automatizadas y los kits rápidos se están convirtiendo en componentes esenciales de las líneas de producción modernas.
- La conveniencia de la automatización, la reducción de errores manuales y la capacidad de gestionar pruebas de gran volumen con precisión son factores clave que impulsan la adopción de estas soluciones en compañías farmacéuticas, organizaciones de fabricación por contrato (CMO) y laboratorios de investigación. La tendencia hacia la descentralización de la fabricación y la expansión de los centros biotecnológicos regionales contribuye aún más al crecimiento del mercado en Asia-Pacífico.
Restricción/Desafío
Preocupaciones sobre los altos costos y la armonización regulatoria
- El alto costo de los sistemas de detección de endotoxinas recombinantes o alternativas, junto con la necesidad de instrumentos especializados, puede ser una barrera para las pequeñas y medianas empresas en las economías emergentes de Asia-Pacífico.
- Por ejemplo, si bien las pruebas tradicionales de LAL con gel-clot son relativamente económicas, los métodos cromogénicos y turbidimétricos cinéticos más avanzados, así como los sistemas basados en MAT, conllevan costos iniciales y requisitos de capacitación significativamente más altos.
- Además, la adopción regulatoria inconsistente en los países de Asia-Pacífico (como los diferentes niveles de aceptación de los métodos rFC o MAT) genera incertidumbre entre los fabricantes que buscan optimizar sus procesos de validación a nivel regional.
- Abordar estos desafíos mediante la optimización de costos, la armonización regulatoria regional y la ampliación de las iniciativas de capacitación es crucial para impulsar la adopción. Las empresas líderes ofrecen cada vez más soluciones integrales de hardware y software, así como soporte técnico, para mitigar estas barreras de entrada e impulsar el crecimiento sostenido del mercado.
Alcance del mercado de pruebas de endotoxinas y pirógenos
El mercado está segmentado en función del producto y los servicios, el tipo de prueba, el tipo, la categoría del producto, la forma, la aplicación, el método, el modo de compra, el producto final y el usuario final.
• Por producto y servicios
En cuanto a productos y servicios, el mercado de pruebas de endotoxinas y pirógenos se segmenta en kits y reactivos de detección, instrumentos y sistemas, servicios de pruebas de endotoxinas y pirógenos, y consumibles y accesorios. El segmento de kits y reactivos de detección dominó el mercado con la mayor participación en los ingresos, con un 46,8 % en 2024, gracias a su alta demanda en las industrias farmacéutica y biotecnológica gracias a su facilidad de uso y fiabilidad en la detección de endotoxinas.
Se espera que el segmento de servicios de pruebas de endotoxinas y pirógenos crezca a la CAGR más alta del 11,2 % entre 2025 y 2032, debido al aumento de la subcontratación por parte de las empresas farmacéuticas y biotecnológicas.
• Por tipo de prueba
Según el tipo de prueba, el mercado de análisis de endotoxinas y pirógenos se segmenta en la prueba de lisado de amebocitos de Limulus (LAL), pruebas TAL, prueba de activación de monocitos (MAT), análisis de factor C recombinante (rFC), pruebas in vitro y pruebas de pirógenos de conejo. El segmento de pruebas LAL obtuvo la mayor cuota de mercado, con un 41,2%, en 2024, gracias a su aceptación regulatoria y alta sensibilidad.
Se proyecta que el segmento de análisis del factor C recombinante (rFC) se expandirá a una CAGR del 12,7 % entre 2025 y 2032, impulsado por la demanda de pruebas sin animales y consideraciones de sostenibilidad.
• Por tipo
Según el tipo, el mercado de pruebas de endotoxinas y pirógenos se segmenta en pruebas preformadas, pruebas de proendotoxinas y pirógenos, y pruebas combinadas. El segmento de pruebas combinadas de endotoxinas y pirógenos representó la mayor cuota de mercado, con un 38,5 %, en 2024, gracias a su capacidad para detectar múltiples contaminantes de forma eficiente.
Se espera que el segmento de pruebas de proendotoxinas y pirógenos crezca a una CAGR del 10,6 % entre 2025 y 2032, impulsado por la demanda de pruebas predictivas en etapa temprana.
• Por categoría de producto
Según la categoría de producto, el mercado de análisis de endotoxinas y pirógenos se segmenta en ingredientes de etiqueta limpia y convencionales. El segmento convencional lideró el mercado con una participación del 58,1 % en 2024, ya que incluye reactivos y sistemas de uso generalizado.
Se proyecta que el segmento de ingredientes de etiqueta limpia crecerá a una CAGR del 9,3 % entre 2025 y 2032, debido a los cambios regulatorios impulsados por la transparencia y las preferencias de los consumidores.
• Por formulario
En cuanto a la forma, el mercado de pruebas de endotoxinas y pirógenos se segmenta en polvo y líquido. El segmento líquido tuvo una participación dominante del 63,9 % en 2024, gracias a su fácil automatización y uso directo.
Se espera que el segmento de polvos crezca a una CAGR del 8,8% entre 2025 y 2032, beneficiándose de una mayor vida útil y transportabilidad.
• Por aplicación
Según su aplicación, el mercado de pruebas de endotoxinas y pirógenos se segmenta en la fabricación de productos farmacéuticos, la fabricación de dispositivos médicos, la producción de materias primas y la fabricación de envases. El segmento de fabricación farmacéutica representó la mayor participación, con un 49,5 %, en 2024, debido a las altas exigencias de esterilidad.
Se proyecta que el segmento de fabricación de dispositivos médicos crecerá a una CAGR del 10,1 % entre 2025 y 2032, debido a las crecientes pruebas regulatorias de implantes y equipos quirúrgicos.
• Por método
Según el método, el mercado de pruebas de endotoxinas y pirógenos se segmenta en pruebas de gel-clot, pruebas cromogénicas y pruebas turbidimétricas. El método de gel-clot dominó el mercado con una participación del 42,7 % en 2024, gracias a su rentabilidad y a la aprobación regulatoria.
Se prevé que el método cromogénico crezca a la CAGR más rápida del 11,4 % entre 2025 y 2032, respaldado por su precisión cuantitativa y compatibilidad con la automatización.
• Por modo de compra
Según el método de compra, el mercado de pruebas de endotoxinas y pirógenos se segmenta en grupos grandes, grupos medianos y pequeños, e individuales. El segmento de grupos grandes obtuvo la mayor cuota de mercado, con un 55,2 %, en 2024, gracias a las adquisiciones a gran escala realizadas por empresas farmacéuticas y CDMO.
Se proyecta que el segmento de grupos medianos y pequeños crecerá a una CAGR del 9,9 % entre 2025 y 2032, con una creciente demanda de las PYME y las instituciones académicas.
• Por producto final
En función del producto final, el mercado de pruebas de endotoxinas y pirógenos se segmenta en vacunas y/o CGT, productos biológicos, inyectables y otros. El segmento de productos biológicos representó la mayor participación, con un 38,9 %, en 2024, impulsado por la creciente demanda de anticuerpos monoclonales y biosimilares.
Se espera que el segmento de vacunas y/o CGT crezca a una CAGR del 12,1% entre 2025 y 2032, debido al aumento de las aprobaciones en terapias avanzadas y el desarrollo de vacunas.
• Por el usuario final
En función del usuario final, el mercado de pruebas de endotoxinas y pirógenos se segmenta en compañías farmacéuticas, biotecnológicas, biomédicas, de dispositivos médicos, CRO, CMO, entre otras. El segmento de compañías farmacéuticas dominó el mercado con una participación del 40,4 % en 2024, gracias a la inversión constante en control de calidad y pruebas de cumplimiento.
Se espera que el segmento de organizaciones de investigación por contrato (CRO) registre la CAGR más rápida del 11,6 % entre 2025 y 2032, impulsada por el aumento de la subcontratación y el crecimiento de las líneas de descubrimiento de fármacos.
Análisis regional del mercado de pruebas de endotoxinas y pirógenos
- América del Norte dominó el mercado mundial de pruebas de endotoxinas y pirógenos con la mayor participación en los ingresos del 40,01 % en 2024, impulsada por una creciente rigurosidad regulatoria, sólidas líneas de producción biofarmacéutica y un uso generalizado de medicamentos inyectables y productos biológicos.
- La región se beneficia de una infraestructura sanitaria avanzada, un alto volumen de ensayos clínicos y una creciente tendencia hacia métodos de prueba recombinantes y sin animales. Empresas líderes de EE. UU. y Canadá están invirtiendo en sistemas automatizados de detección de endotoxinas y soluciones de prueba sostenibles.
- La creciente preferencia por protocolos de control de calidad más rápidos y compatibles fortalece aún más la presencia en el mercado en esta región.
Análisis del mercado estadounidense de pruebas de endotoxinas y pirógenos
El mercado estadounidense de pruebas de endotoxinas y pirógenos representó el 83 % del mercado norteamericano en 2024. El país lidera gracias a la fabricación a gran escala de productos biológicos y vacunas, la fuerte inversión en I+D farmacéutica y la rápida adopción de ensayos de factor C recombinante (rFC) y pruebas de activación de monocitos (MAT). La armonización regulatoria con la iniciativa de la FDA de buscar alternativas a las pruebas en animales está acelerando aún más la expansión del mercado.
Análisis del mercado europeo de pruebas de endotoxinas y pirógenos
Se proyecta que el mercado europeo de pruebas de endotoxinas y pirógenos crezca a una tasa de crecimiento anual compuesta (TCAC) notable durante el período de pronóstico debido a la creciente concienciación sobre la seguridad de los productos, los estrictos requisitos de la farmacopea europea y el aumento de las aprobaciones de productos biológicos. Países como Alemania, el Reino Unido y Francia están priorizando alternativas de prueba sostenibles. El sólido crecimiento de la fabricación por contrato y la externalización de la I+D también está contribuyendo a la demanda del mercado en el desarrollo de fármacos y las pruebas de dispositivos médicos.
Análisis del mercado de pruebas de endotoxinas y pirógenos en el Reino Unido
Se prevé que el mercado británico de pruebas de endotoxinas y pirógenos crezca de forma constante durante el período de pronóstico, gracias a las regulaciones de la MHRA, alineadas con los estándares globales de BPM, un sector biofarmacéutico consolidado y la creciente inversión en infraestructura de investigación clínica. La demanda de métodos rápidos de pruebas de endotoxinas para el aseguramiento de la esterilidad y la producción de fármacos inyectables es un factor clave de crecimiento.
Análisis del mercado alemán de pruebas de endotoxinas y pirógenos
Se prevé un crecimiento significativo del mercado alemán de pruebas de endotoxinas y pirógenos gracias a su sólida base de fabricación farmacéutica, la automatización de los laboratorios de control de calidad y el apoyo a las tecnologías de pruebas recombinantes. El cumplimiento normativo y un fuerte enfoque en la seguridad y la eficiencia de los productos están configurando las tendencias de compras.
Análisis del mercado de pruebas de endotoxinas y pirógenos en Asia-Pacífico
Se prevé que el mercado de pruebas de endotoxinas y pirógenos en Asia-Pacífico crezca a la tasa de crecimiento anual compuesta (TCAC) más alta, del 24,02 % (2025-2032), impulsada por el aumento de las exportaciones farmacéuticas, la creciente demanda de productos biológicos y el apoyo gubernamental a la fabricación local de fármacos en países como China, Japón e India. La rápida expansión de la actividad de ensayos clínicos y un mayor conocimiento de las normas de control de la contaminación están impulsando la adopción de los ensayos MAT y rFC en la región.
Análisis del mercado japonés de pruebas de endotoxinas y pirógenos
El mercado japonés de pruebas de endotoxinas y pirógenos está experimentando una creciente demanda de estas pruebas debido a su alto nivel de innovación en terapias celulares y génicas y a su panorama farmacéutico bien regulado. Los organismos reguladores están fomentando alternativas de prueba sin animales, mientras que el envejecimiento de la población del país está incrementando la necesidad de medicamentos inyectables.
Análisis del mercado de pruebas de endotoxinas y pirógenos en China
El mercado chino de pruebas de endotoxinas y pirógenos capturó la mayor cuota de mercado en Asia-Pacífico en 2024, impulsado por su vasta capacidad de fabricación farmacéutica, el sólido apoyo gubernamental a la producción local de productos biológicos y la creciente adopción de soluciones sostenibles de control de calidad. El auge de empresas nacionales que ofrecen kits y servicios de prueba rentables está impulsando aún más el crecimiento del mercado.
Cuota de mercado de las pruebas de endotoxinas y pirógenos
La industria de pruebas de endotoxinas y pirógenos está liderada principalmente por empresas bien establecidas, entre las que se incluyen:
- Pall Corporation (EE. UU.)
- Thermo Fisher Scientific Inc. (EE. UU.)
- Laboratorios Charles River (EE. UU.)
- Eurofins Scientific (Luxemburgo)
- SGS Société Générale de Surveillance SA (Suiza)
- Lonza (Suiza)
- Merck KGaA (Alemania)
- STERIS (Irlanda)
- Sartorius AG (Alemania)
- BIOMÉRIEUX (Francia)
- Ellab A/S (Dinamarca)
- ASOCIADOS DE CAPE COD, INC. (EE. UU.)
- WuXi AppTec (China)
- Microcoat Biotechnologie GmbH (Alemania)
Últimos avances en el mercado global de pruebas de endotoxinas y pirógenos
- En marzo de 2024, el Grupo Lonza anunció la expansión de sus capacidades de análisis de endotoxinas y pirógenos con el lanzamiento de un nuevo kit de análisis basado en factor C recombinante (rFC). Este desarrollo se alinea con la creciente aceptación regulatoria de los métodos de análisis sin animales y apoya los objetivos de sostenibilidad al reducir la dependencia de la sangre de cangrejo herradura.
- En febrero de 2024, Charles River Laboratories introdujo plataformas mejoradas de Pruebas de Activación de Monocitos (MAT) mediante la integración de la automatización, con el objetivo de mejorar el rendimiento y la reproducibilidad de la detección de pirógenos en productos biológicos y terapias celulares. Esta innovación busca optimizar los flujos de trabajo de las compañías farmacéuticas que cumplen con las estrictas regulaciones globales.
- En enero de 2024, FUJIFILM Wako Chemicals USA Corporation mejoró su cartera de reactivos de lisado de amebocitos de Limulus (LAL) con mayor sensibilidad y menor variabilidad, lo que mejoró la fiabilidad de las pruebas de endotoxinas en medicamentos parenterales y dispositivos médicos. La compañía también anunció nuevas alianzas de distribución para ampliar su alcance en el Sudeste Asiático.
- En diciembre de 2023, Associates of Cape Cod, Inc. (ACC) recibió aprobaciones adicionales de las autoridades reguladoras asiáticas para su ensayo PyroSmart NextGen rFC. Se espera que esta aprobación acelere la adopción de métodos sostenibles y sin animales para el análisis de endotoxinas entre los fabricantes biofarmacéuticos de Japón, China y Corea del Sur.
- En octubre de 2023, Merck KGaA (MilliporeSigma) presentó una nueva solución turbidimétrica de alto rendimiento para el análisis de endotoxinas, diseñada para la producción de vacunas y productos biológicos. Este lanzamiento forma parte de la iniciativa de la compañía para acelerar la liberación de lotes, cumpliendo al mismo tiempo con las normas GMP en constante evolución.
- En septiembre de 2023, Thermo Fisher Scientific reveló el desarrollo de una plataforma integrada de automatización de pruebas LAL en colaboración con CDMO globales. Esta solución combina las pruebas LAL con la captura de datos en tiempo real, con el objetivo de reducir el error humano, mejorar la eficiencia y garantizar la preparación para auditorías en las presentaciones regulatorias.
SKU-
Obtenga acceso en línea al informe sobre la primera nube de inteligencia de mercado del mundo
- Panel de análisis de datos interactivo
- Panel de análisis de empresas para oportunidades con alto potencial de crecimiento
- Acceso de analista de investigación para personalización y consultas
- Análisis de la competencia con panel interactivo
- Últimas noticias, actualizaciones y análisis de tendencias
- Aproveche el poder del análisis de referencia para un seguimiento integral de la competencia
Tabla de contenido
1 INTRODUCCIÓN
1.1 OBJETIVOS DEL ESTUDIO
1.2 DEFINICIÓN DE MERCADO
1.3 DESCRIPCIÓN GENERAL DEL MERCADO MUNDIAL DE PRUEBAS DE ENDOTOXINAS Y PIROGENOS
1.4 MONEDA Y PRECIOS
1.5 LIMITACIÓN
1.6 MERCADOS CUBIERTOS
2 SEGMENTACIÓN DEL MERCADO
2.1 CONCLUSIONES CLAVE
2.2 LLEGADA AL TAMAÑO DEL MERCADO MUNDIAL DE PRUEBAS DE ENDOTOXINAS Y PIROGENOS
2.2.1 CUADRÍCULA DE POSICIONAMIENTO DE PROVEEDORES
2.2.2 CURVA DE LÍNEA DE VIDA DE LA TECNOLOGÍA
2.2.3 MODELO DE VALIDACIÓN DE DATOS DE TRÍPODE
2.2.4 GUÍA DE MERCADO
2.2.5 MODELADO MULTIVARIADO
2.2.6 ANÁLISIS DE ARRIBA A ABAJO
2.2.7 MATRIZ DE DESAFÍO
2.2.8 CUADRÍCULA DE COBERTURA DE LA APLICACIÓN
2.2.9 NORMAS DE MEDICIÓN
2.2.10 ANÁLISIS DE PARTICIPACIÓN DE PROVEEDORES
2.2.11 VOLUMEN DE VENTAS
2.2.12 PUNTOS DE DATOS DE ENTREVISTAS PRIMARIAS CLAVE
2.2.13 PUNTOS DE DATOS DE BASES DE DATOS SECUNDARIAS CLAVE
2.3 MERCADO GLOBAL DE PRUEBAS DE ENDOTOXINAS Y PIROGENOS: RESUMEN DE LA INVESTIGACIÓN
2.4 SUPUESTOS
3 DESCRIPCIÓN GENERAL DEL MERCADO
3.1 CONDUCTORES
3.2 RESTRICCIONES
3.3 OPORTUNIDADES
3.4 DESAFÍOS
4 RESUMEN EJECUTIVO
5 INFORMACIÓN PREMIUM
5.1 ANÁLISIS PESTEL
5.2 MODELO DE LAS CINCO FUERZAS DE PORTER
6 PERSPECTIVAS DE LA INDUSTRIA
6.1 FACTORES MICRO Y MACROECONÓMICOS
6.2 MAPEO DE PERSPECTIVAS DE PENETRACIÓN Y CRECIMIENTO
6.3 ESTRATEGIAS CLAVE DE PRECIOS
6.4 ENTREVISTAS CON ESPECIALISTA
6.5 ANÁLISIS Y RECOMENDACIÓN
7 DESGLOSE DEL ANÁLISIS DE COSTOS
8 HOJA DE RUTA TECNOLÓGICA
9 SEGUIMIENTO DE INNOVACIÓN Y ANÁLISIS ESTRATÉGICO
9.1 ANÁLISIS DE GRANDES ACUERDOS Y ALIANZAS ESTRATÉGICAS
9.1.1 EMPRESAS CONJUNTAS
9.1.2 FUSIONES Y ADQUISICIONES
9.1.3 LICENCIAS Y ASOCIACIONES
9.1.4 COLABORACIONES TECNOLÓGICAS
9.1.5 DESINVERSIONES ESTRATÉGICAS
9.2 NÚMERO DE PRODUCTOS EN DESARROLLO
9.3 ETAPA DE DESARROLLO
9.4 CRONOGRAMAS E HITOS
9.5 ESTRATEGIAS Y METODOLOGÍAS DE INNOVACIÓN
9.6 EVALUACIÓN Y MITIGACIÓN DE RIESGOS
9.7 PERSPECTIVAS FUTURAS
10 CUMPLIMIENTO NORMATIVO
10.1 AUTORIDADES REGULADORAS
10.2 CLASIFICACIONES REGLAMENTARIAS
10.2.1 CLASE I
10.2.2 CLASE II
10.2.3 CLASE III
10.3 PRESENTACIONES REGLAMENTARIAS
10.4 ARMONIZACIÓN INTERNACIONAL
10.5 SISTEMAS DE GESTIÓN DE CALIDAD Y CUMPLIMIENTO
10.6 DESAFÍOS Y ESTRATEGIAS REGULATORIAS
11 MARCO DE REEMBOLSO
12 ANÁLISIS DE LA CADENA DE VALOR
13 ECONOMÍA DE LA SALUD
13.1 GASTO EN SALUD
13.2 GASTOS DE CAPITAL
13.3 TENDENCIAS DE CAPEX
13.4 ASIGNACIÓN DE CAPEX
13.5 FUENTES DE FINANCIAMIENTO
13.6 PUNTOS DE REFERENCIA DE LA INDUSTRIA
13.7 RACIÓN DEL PIB EN EL PIB GENERAL
13.8 ESTRUCTURA DEL SISTEMA DE SALUD
13.9 POLÍTICAS GUBERNAMENTALES
13.1 DESARROLLO ECONÓMICO
14 MERCADO MUNDIAL DE PRUEBAS DE ENDOTOXINAS Y PIROGENOS, POR PRODUCTO Y SERVICIOS
14.1 INFORMACIÓN GENERAL
14.2 KITS DE DETECCIÓN Y REACTIVOS
14.2.1 REACTIVOS DE PRUEBA LAL
14.2.2 DETECCIÓN Y ELIMINACIÓN DE MICOPLASMAS
14.2.3 KIT DE DETECCIÓN DE MICOPLASMA POR PCR
14.2.4 CÓCTEL DE ELIMINACIÓN DE MICOPLASMAS
14.2.5 OTROS
14.3 INSTRUMENTOS Y SISTEMAS
LECTOR DE TUBOS SERIE 14.3.1
14.3.2 LECTOR DE MICROPLACAS
14.3.3 RECUPERACIÓN DE BAJAS ENDOTOXINAS (LER)
14.3.4 ELIMINACIÓN DE ENDOTOXINAS
14.3.5 RECUPERACIÓN DE BAJAS ENDOTOXINAS (LER)
14.3.6 OTROS
14.4 CONSUMIBLES Y ACCESORIOS
14.5 SOFTWARE Y SERVICIOS
14.6 OTROS
15 MERCADO MUNDIAL DE PRUEBAS DE ENDOTOXINAS Y PIROGENOS, POR TIPO DE PRUEBA
15.1 INFORMACIÓN GENERAL
15.2 PRUEBA DE LISADO DE AMEBOCITOS DE LIMULUS (LAL)
15.3 PRUEBA DE ACTIVACIÓN DE MONOCITOS (MAT)
15.4 ENSAYO DE FACTOR C RECOMBINANTE (RFC)
15.5 PRUEBA DE PIROGENOS EN CONEJOS
16 MERCADO MUNDIAL DE PRUEBAS DE ENDOTOXINAS Y PIROGENOS, POR TIPO
16.1 DESCRIPCIÓN GENERAL
16.2 PRUEBAS DE ENDOTOXINAS Y PIROGENOS PREFORMADOS
16.3 PRUEBAS DE PROENDOTOXINAS Y PIROGENOS
16.4 PRUEBAS COMBINADAS DE ENDOTOXINAS Y PIROGENOS
17 MERCADO MUNDIAL DE PRUEBAS DE ENDOTOXINAS Y PIROGENOS, POR FORMA
17.1 INFORMACIÓN GENERAL
17.2 POLVO
17.3 LÍQUIDO
18 MERCADO MUNDIAL DE PRUEBAS DE ENDOTOXINAS Y PIROGENOS, POR CATEGORÍA DE PRODUCTO
18.1 DESCRIPCIÓN GENERAL
18.2 INGREDIENTE ETIQUETADO LIMPIO
18.3 CONVENCIONAL
19 MERCADO MUNDIAL DE PRUEBAS DE ENDOTOXINAS Y PIROGENOS, POR APLICACIÓN
19.1 DESCRIPCIÓN GENERAL
19.2 FABRICACIÓN DE PRODUCTOS FARMACÉUTICOS
19.3 FABRICACIÓN DE DISPOSITIVOS MÉDICOS
19.4 PRODUCCIÓN DE MATERIAS PRIMAS
19.5 FABRICACIÓN DE EMBALAJES
20 MERCADO MUNDIAL DE PRUEBAS DE ENDOTOXINAS Y PIROGENOS, POR MÉTODO
20.1 INFORMACIÓN GENERAL
20.2 PRUEBA DE ENDOTOXINAS Y PIROGENOS CON COÁGULO DE GEL
20.3 PRUEBA DE ENDOTOXINAS Y PIROGENOS CROMOGÉNICOS
20.4 PRUEBA TURBIDIMÉTRICA DE ENDOTOXINAS Y PIROGENOS
21 MERCADO MUNDIAL DE PRUEBAS DE ENDOTOXINAS Y PIROGENOS, POR MODO DE COMPRA
21.1 INFORMACIÓN GENERAL
21.2 GRUPO GRANDE
21.3 GRUPOS MEDIANOS Y PEQUEÑOS
21.4 INDIVIDUAL
22 MERCADO MUNDIAL DE PRUEBAS DE ENDOTOXINAS Y PIROGENOS, POR PRODUCTO FINAL
22.1 INFORMACIÓN GENERAL
22.2 PRODUCTOS BIOLÓGICOS
22.3 VACUNAS Y/O CGT
22.4 INYECTABLES
22.5 OTROS
22.5.1 ENDOSCOPIOS
22.5.2 DISPOSITIVOS BIOMÉDICOS REUTILIZABLES
22.5.3 OTROS
23 MERCADO MUNDIAL DE PRUEBAS DE ENDOTOXINAS Y PIROGENOS, POR USUARIO FINAL
23.1 INFORMACIÓN GENERAL
23.2 COMPAÑÍAS FARMACÉUTICAS
23.3 EMPRESAS DE BIOTECNOLOGÍA
23.4 EMPRESAS BIOMÉDICAS
23.5 EMPRESAS DE DISPOSITIVOS MÉDICOS
23.6 ORGANIZACIÓN DE INVESTIGACIÓN POR CONTRATO (CRO)
23.7 ORGANIZACIÓN DE FABRICACIÓN POR CONTRATO (OCM)
24 MERCADO MUNDIAL DE PRUEBAS DE ENDOTOXINAS Y PIROGENOS, GEOGRAFÍA
24.1 MERCADO MUNDIAL DE PRUEBAS DE ENDOTOXINAS Y PIROGENOS (TODA LA SEGMENTACIÓN PROPORCIONADA ANTERIORMENTE SE REPRESENTA EN ESTE CAPÍTULO POR PAÍS)
24.2 AMÉRICA DEL NORTE
24.2.1 EE. UU.
24.2.2 CANADÁ
24.2.3 MÉXICO
24.3 EUROPA
24.3.1 ALEMANIA
24.3.2 FRANCIA
24.3.3 Reino Unido
24.3.4 ITALIA
24.3.5 ESPAÑA
24.3.6 RUSIA
24.3.7 BÉLGICA
24.3.8 PAÍSES BAJOS
24.3.9 SUIZA
24.3.10 RESTO DE EUROPA
24.4 ASIA-PACÍFICO
24.4.1 JAPÓN
24.4.2 CHINA
24.4.3 COREA DEL SUR
24.4.4 INDIA
24.4.5 AUSTRALIA
24.4.6 SINGAPUR
24.4.7 MALASIA
24.4.8 RESTO DE ASIA-PACÍFICO
24.5 SUDAMÉRICA
24.5.1 BRASIL
24.5.2 ARGENTINA
24.5.3 RESTO DE SUDAMÉRICA
24.6 INFORMACIÓN PRINCIPAL CLAVE: POR PAÍSES PRINCIPALES
25 MERCADO GLOBAL DE PRUEBAS DE ENDOTOXINAS Y PIROGENOS, PANORAMA EMPRESARIAL
25.1 ANÁLISIS DE ACCIONES DE LA EMPRESA: GLOBAL
25.2 ANÁLISIS DE ACCIONES DE LA EMPRESA: AMÉRICA DEL NORTE
25.3 ANÁLISIS DE ACCIONES DE EMPRESAS: EUROPA
25.4 ANÁLISIS DE ACCIONES DE LA EMPRESA: ASIA PACÍFICO
25.5 FUSIONES Y ADQUISICIONES
25.6 DESARROLLO Y APROBACIONES DE NUEVOS PRODUCTOS
25.7 EXPANSIONES
25.8 CAMBIOS REGLAMENTARIOS
25.9 ASOCIACIÓN Y OTROS DESARROLLOS ESTRATÉGICOS
26 MERCADO GLOBAL DE PRUEBAS DE ENDOTOXINAS Y PIRÓGENOS, ANÁLISIS FODA Y DBMR
27 MERCADO GLOBAL DE PRUEBAS DE ENDOTOXINAS Y PIROGENOS, PERFIL DE LA EMPRESA
27.1 PALL EUROPE LIMITED (DANAHER CORPORATION)
27.1.1 DESCRIPCIÓN GENERAL DE LA EMPRESA
27.1.2 ANÁLISIS DE INGRESOS
27.1.3 PRESENCIA GEOGRÁFICA
27.1.4 PORTAFOLIO DE PRODUCTOS
27.1.5 DESARROLLOS RECIENTES
27.2 THERMO FISHER SCIENTIFIC INC.
27.2.1 DESCRIPCIÓN GENERAL DE LA EMPRESA
27.2.2 ANÁLISIS DE INGRESOS
27.2.3 PRESENCIA GEOGRÁFICA
27.2.4 PORTAFOLIO DE PRODUCTOS
27.2.5 DESARROLLOS RECIENTES
27.3 LABORATORIOS CHARLES RIVER
27.3.1 DESCRIPCIÓN GENERAL DE LA EMPRESA
27.3.2 ANÁLISIS DE INGRESOS
27.3.3 PRESENCIA GEOGRÁFICA
27.3.4 PORTAFOLIO DE PRODUCTOS
27.3.5 DESARROLLOS RECIENTES
27.4 EUROFINS CIENTÍFICO
27.4.1 DESCRIPCIÓN GENERAL DE LA EMPRESA
27.4.2 ANÁLISIS DE INGRESOS
27.4.3 PRESENCIA GEOGRÁFICA
27.4.4 PORTAFOLIO DE PRODUCTOS
27.4.5 DESARROLLOS RECIENTES
27.5 SGS SOCIÉTÉ GÉNÉRALE DE SURVEILLANCE SA.
27.5.1 DESCRIPCIÓN GENERAL DE LA EMPRESA
27.5.2 ANÁLISIS DE INGRESOS
27.5.3 PRESENCIA GEOGRÁFICA
27.5.4 PORTAFOLIO DE PRODUCTOS
27.5.5 DESARROLLOS RECIENTES
27.6 PACIFIC BIOLABS
27.6.1 DESCRIPCIÓN GENERAL DE LA EMPRESA
27.6.2 ANÁLISIS DE INGRESOS
27.6.3 PRESENCIA GEOGRÁFICA
27.6.4 PORTAFOLIO DE PRODUCTOS
27.6.5 DESARROLLOS RECIENTES
27.7 LONZA
27.7.1 DESCRIPCIÓN GENERAL DE LA EMPRESA
27.7.2 ANÁLISIS DE INGRESOS
27.7.3 PRESENCIA GEOGRÁFICA
27.7.4 PORTAFOLIO DE PRODUCTOS
27.7.5 DESARROLLOS RECIENTES
27.8 MERCK KGAA
27.8.1 DESCRIPCIÓN GENERAL DE LA EMPRESA
27.8.2 ANÁLISIS DE INGRESOS
27.8.3 PRESENCIA GEOGRÁFICA
27.8.4 PORTAFOLIO DE PRODUCTOS
27.8.5 DESARROLLOS RECIENTES
27.9 STERIS
27.9.1 DESCRIPCIÓN GENERAL DE LA EMPRESA
27.9.2 ANÁLISIS DE INGRESOS
27.9.3 PRESENCIA GEOGRÁFICA
27.9.4 PORTAFOLIO DE PRODUCTOS
27.9.5 DESARROLLOS RECIENTES
27.1 SARTORIUS AG
27.10.1 DESCRIPCIÓN GENERAL DE LA EMPRESA
27.10.2 ANÁLISIS DE INGRESOS
27.10.3 PRESENCIA GEOGRÁFICA
27.10.4 PORTAFOLIO DE PRODUCTOS
27.10.5 DESARROLLOS RECIENTES
27.11 BIOMÉRIEUX
27.11.1 DESCRIPCIÓN GENERAL DE LA EMPRESA
27.11.2 ANÁLISIS DE INGRESOS
27.11.3 PRESENCIA GEOGRÁFICA
27.11.4 PORTAFOLIO DE PRODUCTOS
27.11.5 DESARROLLOS RECIENTES
27.12 FUJIFILM WAKO CORPORACIÓN DE PRODUCTOS QUÍMICOS PUROS
27.12.1 DESCRIPCIÓN GENERAL DE LA EMPRESA
27.12.2 ANÁLISIS DE INGRESOS
27.12.3 PRESENCIA GEOGRÁFICA
27.12.4 PORTAFOLIO DE PRODUCTOS
27.12.5 DESARROLLOS RECIENTES
27.13 ELLAB A/S.
27.13.1 DESCRIPCIÓN GENERAL DE LA EMPRESA
27.13.2 ANÁLISIS DE INGRESOS
27.13.3 PRESENCIA GEOGRÁFICA
27.13.4 PORTAFOLIO DE PRODUCTOS
27.13.5 DESARROLLOS RECIENTES
27.14 ASOCIADOS DE CAPE COD, INC. (CORPORACIÓN SEIKAGAKU)
27.14.1 DESCRIPCIÓN GENERAL DE LA EMPRESA
27.14.2 ANÁLISIS DE INGRESOS
27.14.3 PRESENCIA GEOGRÁFICA
27.14.4 PORTAFOLIO DE PRODUCTOS
27.14.5 DESARROLLOS RECIENTES
27.15 WUXI APPTEC
27.15.1 DESCRIPCIÓN GENERAL DE LA EMPRESA
27.15.2 ANÁLISIS DE INGRESOS
27.15.3 PRESENCIA GEOGRÁFICA
27.15.4 PORTAFOLIO DE PRODUCTOS
27.15.5 ACONTECIMIENTOS RECIENTES
27.16 GENSCRIPT
27.16.1 DESCRIPCIÓN GENERAL DE LA EMPRESA
27.16.2 ANÁLISIS DE INGRESOS
27.16.3 PRESENCIA GEOGRÁFICA
27.16.4 PORTAFOLIO DE PRODUCTOS
27.16.5 DESARROLLOS RECIENTES
27.17 MICROCOAT BIOTECHNOLOGIE GMBH
27.17.1 DESCRIPCIÓN GENERAL DE LA EMPRESA
27.17.2 ANÁLISIS DE INGRESOS
27.17.3 PRESENCIA GEOGRÁFICA
27.17.4 PORTAFOLIO DE PRODUCTOS
27.17.5 ACONTECIMIENTOS RECIENTES
27.18 SANQUIN
27.18.1 DESCRIPCIÓN GENERAL DE LA EMPRESA
27.18.2 ANÁLISIS DE INGRESOS
27.18.3 PRESENCIA GEOGRÁFICA
27.18.4 PORTAFOLIO DE PRODUCTOS
27.18.5 ACONTECIMIENTOS RECIENTES
27.19 SERVICIOS CIENTÍFICOS DE LECTURA LTD.
27.19.1 DESCRIPCIÓN GENERAL DE LA EMPRESA
27.19.2 ANÁLISIS DE INGRESOS
27.19.3 PRESENCIA GEOGRÁFICA
27.19.4 PORTAFOLIO DE PRODUCTOS
27.19.5 ACONTECIMIENTOS RECIENTES
27.2 NANOCOMPÓSITOS
27.20.1 DESCRIPCIÓN GENERAL DE LA EMPRESA
27.20.2 ANÁLISIS DE INGRESOS
27.20.3 PRESENCIA GEOGRÁFICA
27.20.4 PORTAFOLIO DE PRODUCTOS
27.20.5 ACONTECIMIENTOS RECIENTES
27.21 LABORATORIO ZWISLER GMBH
27.21.1 DESCRIPCIÓN GENERAL DE LA EMPRESA
27.21.2 ANÁLISIS DE INGRESOS
27.21.3 PRESENCIA GEOGRÁFICA
27.21.4 PORTAFOLIO DE PRODUCTOS
27.21.5 ACONTECIMIENTOS RECIENTES
27.22 NELSON LABORATORIES, LLC – UNA COMPAÑÍA DE SOTERA HEALTH
27.22.1 DESCRIPCIÓN GENERAL DE LA EMPRESA
27.22.2 ANÁLISIS DE INGRESOS
27.22.3 PRESENCIA GEOGRÁFICA
27.22.4 PORTAFOLIO DE PRODUCTOS
27.22.5 DESARROLLOS RECIENTES
27.23 ASOCIADOS DE CIENCIAS DE AMÉRICA DEL NORTE, LLC
27.23.1 DESCRIPCIÓN GENERAL DE LA EMPRESA
27.23.2 ANÁLISIS DE INGRESOS
27.23.3 PRESENCIA GEOGRÁFICA
27.23.4 PORTAFOLIO DE PRODUCTOS
27.23.5 ACONTECIMIENTOS RECIENTES
27.24 CORPORACIÓN PROMEGA
27.24.1 DESCRIPCIÓN GENERAL DE LA EMPRESA
27.24.2 ANÁLISIS DE INGRESOS
27.24.3 PRESENCIA GEOGRÁFICA
27.24.4 PORTAFOLIO DE PRODUCTOS
27.24.5 DESARROLLOS RECIENTES
27.25 HYCULT BIOTECH INC.
27.25.1 DESCRIPCIÓN GENERAL DE LA EMPRESA
27.25.2 ANÁLISIS DE INGRESOS
27.25.3 PRESENCIA GEOGRÁFICA
27.25.4 PORTAFOLIO DE PRODUCTOS
27.25.5 ACONTECIMIENTOS RECIENTES
27.26 GRUPO ALMAC
27.26.1 DESCRIPCIÓN GENERAL DE LA EMPRESA
27.26.2 ANÁLISIS DE INGRESOS
27.26.3 PRESENCIA GEOGRÁFICA
27.26.4 PORTAFOLIO DE PRODUCTOS
27.26.5 ACONTECIMIENTOS RECIENTES
27.27 MAT BIOTECH
27.27.1 DESCRIPCIÓN GENERAL DE LA EMPRESA
27.27.2 ANÁLISIS DE INGRESOS
27.27.3 PRESENCIA GEOGRÁFICA
27.27.4 PORTAFOLIO DE PRODUCTOS
27.27.5 ACONTECIMIENTOS RECIENTES
27.28 SOLVÍAS
27.28.1 DESCRIPCIÓN GENERAL DE LA EMPRESA
27.28.2 ANÁLISIS DE INGRESOS
27.28.3 PRESENCIA GEOGRÁFICA
27.28.4 PORTAFOLIO DE PRODUCTOS
27.28.5 ACONTECIMIENTOS RECIENTES
27.29 WICKHAM MICRO LIMITADA
27.29.1 DESCRIPCIÓN GENERAL DE LA EMPRESA
27.29.2 ANÁLISIS DE INGRESOS
27.29.3 PRESENCIA GEOGRÁFICA
27.29.4 PORTAFOLIO DE PRODUCTOS
27.29.5 ACONTECIMIENTOS RECIENTES
27.3 BIOLABS CREATIVOS
27.30.1 DESCRIPCIÓN GENERAL DE LA EMPRESA
27.30.2 ANÁLISIS DE INGRESOS
27.30.3 PRESENCIA GEOGRÁFICA
27.30.4 PORTAFOLIO DE PRODUCTOS
27.30.5 ACONTECIMIENTOS RECIENTES
*NOTA: LA LISTA DE EMPRESAS PRESENTADAS NO ES EXHAUSTIVA Y SE ADAPTA A LOS REQUISITOS DE NUESTROS CLIENTES ANTERIORES. NUESTRO ESTUDIO PRESENTA MÁS DE 100 EMPRESAS, POR LO QUE ESTA LISTA PUEDE MODIFICARSE O SUSTITUIRSE A PETICIÓN.
28 INFORMES RELACIONADOS
29 CUESTIONARIO
30 ACERCA DE LA INVESTIGACIÓN DE MERCADO DE DATA BRIDGE
Metodología de investigación
La recopilación de datos y el análisis del año base se realizan utilizando módulos de recopilación de datos con muestras de gran tamaño. La etapa incluye la obtención de información de mercado o datos relacionados a través de varias fuentes y estrategias. Incluye el examen y la planificación de todos los datos adquiridos del pasado con antelación. Asimismo, abarca el examen de las inconsistencias de información observadas en diferentes fuentes de información. Los datos de mercado se analizan y estiman utilizando modelos estadísticos y coherentes de mercado. Además, el análisis de la participación de mercado y el análisis de tendencias clave son los principales factores de éxito en el informe de mercado. Para obtener más información, solicite una llamada de un analista o envíe su consulta.
La metodología de investigación clave utilizada por el equipo de investigación de DBMR es la triangulación de datos, que implica la extracción de datos, el análisis del impacto de las variables de datos en el mercado y la validación primaria (experto en la industria). Los modelos de datos incluyen cuadrícula de posicionamiento de proveedores, análisis de línea de tiempo de mercado, descripción general y guía del mercado, cuadrícula de posicionamiento de la empresa, análisis de patentes, análisis de precios, análisis de participación de mercado de la empresa, estándares de medición, análisis global versus regional y de participación de proveedores. Para obtener más información sobre la metodología de investigación, envíe una consulta para hablar con nuestros expertos de la industria.
Personalización disponible
Data Bridge Market Research es líder en investigación formativa avanzada. Nos enorgullecemos de brindar servicios a nuestros clientes existentes y nuevos con datos y análisis que coinciden y se adaptan a sus objetivos. El informe se puede personalizar para incluir análisis de tendencias de precios de marcas objetivo, comprensión del mercado de países adicionales (solicite la lista de países), datos de resultados de ensayos clínicos, revisión de literatura, análisis de mercado renovado y base de productos. El análisis de mercado de competidores objetivo se puede analizar desde análisis basados en tecnología hasta estrategias de cartera de mercado. Podemos agregar tantos competidores sobre los que necesite datos en el formato y estilo de datos que esté buscando. Nuestro equipo de analistas también puede proporcionarle datos en archivos de Excel sin procesar, tablas dinámicas (libro de datos) o puede ayudarlo a crear presentaciones a partir de los conjuntos de datos disponibles en el informe.