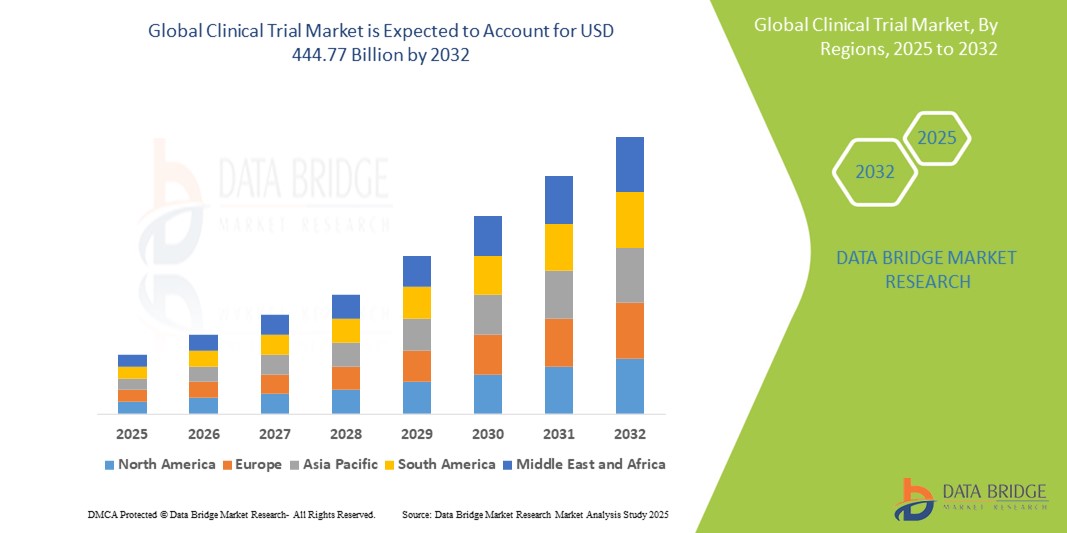
Global Clinical Trials Market
Taille du marché en milliards USD
TCAC :
% 
 USD
297.62 Billion
USD
444.77 Billion
2024
2032
USD
297.62 Billion
USD
444.77 Billion
2024
2032
| 2025 –2032 | |
| USD 297.62 Billion | |
| USD 444.77 Billion | |
|
|
|
|
Segmentation du marché mondial des essais cliniques, par phase (phase I, phase II, phase III et phase IV), indication (auto-immune/inflammation, gestion de la douleur, oncologie, affection du SNC, diabète, obésité, cardiovasculaire et autres), conception (études interventionnelles, études de traitement, études observationnelles et accès élargi), utilisateur final (hôpital, laboratoires et cliniques) - Tendances et prévisions de l'industrie jusqu'en 2032.
Taille du marché des essais cliniques
- Le marché mondial des essais cliniques était évalué à 297,62 millions USD en 2024 et devrait atteindre 444,77 milliards USD d'ici 2032.
- Au cours de la période de prévision de 2025 à 2032, le marché devrait croître à un TCAC de 5,15 %, principalement grâce à la demande croissante de thérapies innovantes, aux progrès des technologies de recherche clinique et à l'augmentation de l'externalisation des essais cliniques.
- Cette croissance est due à des facteurs tels que la complexité croissante des essais cliniques, l’augmentation du nombre d’essais cliniques, l’adoption croissante d’essais décentralisés et le besoin croissant de processus d’essais rentables et plus rapides.
Analyse du marché des essais cliniques
- Un essai clinique est une étude de recherche impliquant des participants humains pour évaluer la sécurité, l'efficacité et les effets secondaires potentiels de nouveaux traitements ou interventions médicaux.
- Le marché mondial des essais cliniques connaît une expansion rapide, porté par l'accent croissant mis sur le développement de nouvelles thérapies et l'amélioration des soins aux patients grâce à de nouveaux traitements et médicaments, en particulier dans des domaines tels que l'oncologie et les maladies rares.
- Par exemple, le développement de thérapies à base de cellules CAR T pour le traitement du cancer a considérablement accéléré les essais cliniques en oncologie.
- Les progrès technologiques, tels que l’utilisation de l’intelligence artificielle et de l’apprentissage automatique pour l’analyse des données, ont considérablement amélioré l’efficacité et la précision des essais cliniques.
- Par exemple, l’utilisation de l’IA dans le recrutement de patients pour les essais cliniques, avec des entreprises telles qu’IBM Watson Health qui mènent des efforts pour rationaliser le processus et assurer une mise en correspondance plus rapide des participants.
- Le nombre d'essais cliniques menés à l'échelle mondiale a augmenté, les essais cliniques sur les vaccins contre la COVID-19 étant un excellent exemple de la capacité du secteur à s'adapter rapidement pour répondre aux besoins urgents de santé publique. La rapidité des essais cliniques des vaccins Pfizer et Moderna contre la COVID-19 illustre la capacité du secteur à accélérer son développement sous pression.
- L'externalisation des essais cliniques auprès d'organismes de recherche sous contrat (ORC) est de plus en plus courante, ce qui permet aux entreprises pharmaceutiques de réduire leurs coûts et d'accéder à une expertise spécialisée. La collaboration entre Novartis et Covance pour des essais cliniques mondiaux en est un exemple concret. Covance a fourni des services spécialisés dans la gestion d'essais internationaux à grande échelle.
- L’intégration des essais décentralisés, qui permettent aux patients de participer depuis chez eux via des plateformes numériques, s’est accélérée, notamment à la suite de la pandémie.
- Par exemple, les essais cliniques du vaccin COVID-19 d'AstraZeneca, qui comprenaient des modèles d'essais décentralisés pour accroître la participation et maintenir les protocoles de sécurité
Portée du rapport et segmentation du marché des essais cliniques
|
Attributs |
Informations clés sur le marché des essais cliniques |
|
Segments couverts |
|
|
Pays couverts |
Amérique du Nord
Europe
Asie-Pacifique
Moyen-Orient et Afrique
Amérique du Sud
|
|
Acteurs clés du marché |
|
|
Opportunités de marché |
|
|
Ensembles d'informations de données à valeur ajoutée |
Outre les informations sur les scénarios de marché tels que la valeur marchande, le taux de croissance, la segmentation, la couverture géographique et les principaux acteurs, les rapports de marché organisés par Data Bridge Market Research incluent également une analyse approfondie des experts, une épidémiologie des patients, une analyse du pipeline, une analyse des prix et un cadre réglementaire. |
Tendances du marché des essais cliniques
« Adoption croissante des essais cliniques décentralisés »
- Les essais cliniques décentralisés permettent aux patients de participer depuis leur domicile ou depuis des établissements de santé locaux, réduisant ainsi le besoin de visites fréquentes vers des sites de recherche centraux, ce qui améliore la commodité pour les participants.
- Par exemple, les essais à distance de Pfizer pendant la pandémie de COVID-19 ont permis aux patients de participer à des études sur les vaccins sans avoir besoin de se rendre sur le site d'essai.
- Ces essais s'appuient sur des technologies telles que la télémédecine, les appareils portables et les plateformes numériques pour surveiller les patients, collecter des données et maintenir la communication, permettant ainsi un suivi en temps réel de la santé des patients.
- Par exemple, Eli Lilly a utilisé des appareils portables pour surveiller les patients à distance dans ses essais cliniques sur les médicaments contre le diabète.
- La pandémie de COVID-19 a accéléré l’adoption d’essais cliniques décentralisés alors que le secteur de la santé s’adaptait pour assurer la continuité
- Par exemple, Moderna a mené des essais à distance pour le développement de son vaccin contre la COVID-19, en utilisant la télésanté et la surveillance à domicile pour suivre les personnes vaccinées tout en maintenant la sécurité et en réduisant les risques d'exposition.
- Les essais décentralisés ont amélioré l’accès des patients, en particulier dans les zones rurales ou mal desservies, en éliminant les obstacles liés aux longs déplacements vers les sites cliniques.
- Par exemple, les essais du vaccin COVID-19 d'AstraZeneca ont utilisé des consultations virtuelles et la livraison à domicile des médicaments, permettant aux patients dans des endroits éloignés de rester impliqués dans l'essai
- Les sociétés pharmaceutiques et les organismes de recherche sous contrat adoptent désormais des modèles hybrides, combinant des essais traditionnels sur site avec des méthodes décentralisées
- Par exemple, Novartis a intégré des éléments décentralisés dans ses essais mondiaux en cours pour les traitements oncologiques, permettant aux patients des régions éloignées de participer tout en adhérant aux protocoles d'essai.
Dynamique du marché des essais cliniques
Conducteur
« Demande croissante de thérapies nouvelles et innovantes »
- La demande croissante de thérapies nouvelles et innovantes, notamment en oncologie, dans les maladies rares et les maladies chroniques, stimule le marché des essais cliniques.
- Par exemple, l’essor des traitements personnalisés contre le cancer, tels que la thérapie par cellules CAR-T, a suscité de nombreux essais pour tester leur efficacité et leur sécurité.
- Les sociétés pharmaceutiques et les instituts de recherche se concentrent sur les traitements ciblés et la médecine de précision, qui nécessitent des essais cliniques robustes
- Par exemple, le développement de thérapies géniques, telles que celles pour l’amyotrophie spinale, qui ont fait l’objet d’essais cliniques approfondis pour garantir leur efficacité.
- Les traitements révolutionnaires tels que les inhibiteurs de points de contrôle immunitaires contre le cancer, y compris des médicaments comme Keytruda et Opdivo, ont accéléré la demande d'essais cliniques pour affiner et étendre leurs applications, de nombreux essais étudiant désormais leur utilisation dans divers types de cancer.
- Le développement rapide des vaccins contre la COVID-19, notamment ceux de Pfizer et de Moderna, a mis en évidence le besoin urgent d'essais cliniques accélérés, montrant comment la recherche clinique peut s'adapter rapidement aux besoins de santé publique et accélérer la fourniture de traitements vitaux.
- La prévalence croissante des maladies chroniques et le vieillissement de la population contribuent à l’augmentation des essais cliniques
- Par exemple, l’incidence mondiale croissante du diabète a conduit à de nombreux essais explorant de nouveaux traitements et technologies pour améliorer les résultats des patients.
Opportunité
« Demande croissante d'essais cliniques dans les marchés émergents »
- La demande d'essais cliniques augmente dans les marchés émergents tels que l'Inde et la Chine, où des populations de patients importantes et diversifiées offrent un recrutement plus rapide et des conditions de test variées
- Par exemple, en Inde, les essais de vaccins et de traitements contre le cancer se sont développés en raison de la disponibilité d’un bassin de patients large et diversifié.
- La prévalence croissante des maladies chroniques et le vieillissement de la population mondiale créent un besoin accru de traitements et multiplient les possibilités d'essais cliniques dans des domaines tels que l'oncologie et le diabète. L'augmentation des cas de diabète a entraîné une multiplication des essais cliniques testant de nouvelles formulations d'insuline et de nouveaux traitements dans des pays comme les États-Unis et l'Europe.
- Les progrès technologiques tels que les plateformes numériques et les essais virtuels, rationalisent le recrutement, la collecte de données et le suivi tout en réduisant les coûts des essais
- Par exemple, des plateformes telles que science 37 ont permis des essais cliniques à distance, permettant aux patients de participer aux essais depuis leur domicile et réduisant ainsi le besoin de déplacement.
- L'assouplissement réglementaire dans des pays comme le Brésil et la Corée du Sud permet d'accélérer l'approbation des essais cliniques et encourage les laboratoires pharmaceutiques internationaux à y mener des recherches. Au Brésil, l'ANVISA, l'organisme de réglementation, a simplifié le processus d'approbation des essais cliniques, faisant de ce pays une destination incontournable pour la recherche clinique en Amérique latine.
- L'accent accru mis sur la médecine personnalisée, conduisant au développement d'essais de précision adaptés à des sous-groupes de patients spécifiques, comme l'essor des thérapies géniques pour les maladies rares
- Par exemple, les essais cliniques pour les traitements de thérapie génique tels que Zolgensma pour l'amyotrophie spinale, qui sont adaptés à des marqueurs génétiques spécifiques chez les enfants affectés
Retenue/Défi
« Complexité de la conduite des essais cliniques »
- Les défis réglementaires découlent des directives différentes selon les pays, ce qui complique le processus d’approbation.
- Par exemple, les récents retards dans les essais de vaccins contre la COVID-19 en raison de réglementations différentes de la FDA américaine et de l'EMA en Europe ont démontré à quel point la conformité internationale peut être complexe.
- Le recrutement et la rétention des patients sont souvent entravés par une sensibilisation et une accessibilité limitées, en particulier dans les régions mal desservies.
- Par exemple, les essais cliniques sur des maladies rares telles que la dystrophie musculaire de Duchenne sont confrontés à des difficultés pour recruter suffisamment de participants éligibles, ce qui retarde la recherche et le développement.
- La gestion des données devient de plus en plus complexe à mesure que les essais génèrent des volumes considérables d'informations. Dans les essais multicentriques, garantir l'exactitude et la cohérence de la collecte de données, comme dans les essais oncologiques, nécessite une technologie de pointe pour prévenir les erreurs, comme l'a démontré l'essai du vaccin AstraZeneca, où des incohérences dans les données ont entraîné de brefs contretemps.
- Les contraintes de coût et de temps demeurent un enjeu majeur dans les essais cliniques, notamment ceux de longue durée ou nécessitant un suivi important des patients. Le coût des essais à grande échelle, comme ceux portant sur les médicaments contre la maladie d'Alzheimer, peut dépasser des millions de dollars, et les retards sont fréquents, comme en témoignent les retards dans l'essai de l'aducanumab.
- Les préoccupations éthiques concernant la sécurité des patients et le consentement éclairé sont cruciales, en particulier lorsque des populations vulnérables sont concernées. Les essais cliniques de thérapies géniques, comme ceux concernant l'amyotrophie spinale, nécessitent une réflexion éthique approfondie afin de garantir que les patients comprennent pleinement les risques, comme l'a montré le processus d'approbation du Zolgensma.
Portée du marché des essais cliniques
Le marché est segmenté en fonction de la phase, de l'indication, de la conception et de l'utilisateur final.
|
Segmentation |
Sous-segmentation |
|
Par phase |
|
|
Par indication |
|
|
Par conception |
|
|
Par utilisateur final |
|
Analyse régionale du marché des essais cliniques
« L'Amérique du Nord est la région dominante sur le marché des essais cliniques »
- L'Amérique du Nord domine le marché des essais cliniques, principalement en raison du solide système de santé américain doté d'une technologie de pointe, offrant une base solide pour les essais cliniques.
- La région abrite de nombreuses sociétés pharmaceutiques et biotechnologiques mondiales, qui stimulent l'innovation et la recherche clinique.
- L’Amérique du Nord bénéficie de processus réglementaires clairs et favorables qui facilitent l’approbation et l’exécution des essais cliniques
- Le financement continu de la recherche clinique, ainsi qu’un bassin de patients large et diversifié, accélèrent la croissance du marché et renforcent la domination de l’Amérique du Nord
« L'Asie-Pacifique devrait enregistrer le taux de croissance le plus élevé »
- La région Asie-Pacifique est le marché qui connaît la croissance la plus rapide en matière d'essais cliniques, stimulé par le besoin de traitements et de médicaments innovants dans un marché de la santé en pleine expansion.
- Destinations attractives pour les essais cliniques, notamment en Chine, en Inde et au Japon, en raison de populations vastes et diversifiées et de coûts inférieurs par rapport aux marchés occidentaux
- L’amélioration des infrastructures de santé et l’augmentation du nombre de sites de recherche clinique contribuent à la croissance rapide de la région
- Un environnement réglementaire plus favorable, favorisant l’exécution efficace des essais cliniques dans la région
- Des investissements continus dans le secteur de la santé et un nombre croissant de professionnels expérimentés positionnent l'Asie-Pacifique comme la région à la croissance la plus rapide en matière d'essais cliniques
Part de marché des essais cliniques
Le paysage concurrentiel du marché fournit des détails par concurrent. Il comprend la présentation de l'entreprise, ses données financières, son chiffre d'affaires, son potentiel de marché, ses investissements en recherche et développement, ses nouvelles initiatives commerciales, sa présence mondiale, ses sites et installations de production, ses capacités de production, ses forces et faiblesses, le lancement de nouveaux produits, leur ampleur et leur portée, ainsi que la domination de ses applications. Les données ci-dessus ne concernent que les activités des entreprises par rapport à leur marché.
Les principaux leaders du marché opérant sur le marché sont :
- Clinipace (États-Unis)
- Laboratory Corporation of America Holdings (LabCorp) (États-Unis)
- Eli Lilly and Company (États-Unis)
- ICON Plc. (Irlande)
- Novo Nordisk A/S (Danemark)
- Parexel International Corporation (États-Unis)
- Pfizer Inc. (États-Unis)
- PPD, Inc. (États-Unis)
- IQVIA (États-Unis)
- Sanofi (France)
- F. Hoffmann-La Roche SA (Suisse)
- Alcami Corporation, Inc. (États-Unis)
- Accell Clinical Research LLC (États-Unis)
- Congenix LLP (Royaume-Uni)
- Labcorp Drug Development (États-Unis)
- Ecron Acunova (Inde)
- Medpace (États-Unis)
- LUMITOS AG (Allemagne)
- ICON plc (Irlande)
- SIRO Clapham Private Limited (Inde)
Derniers développements sur le marché mondial des essais cliniques
- En février 2025, Novotech s'est associé à l'hôpital chrétien Wonju Severance pour promouvoir l'excellence en recherche clinique en Corée du Sud. Cette collaboration vise à renforcer les capacités d'essais cliniques en s'appuyant sur l'infrastructure médicale de pointe et l'expertise de l'hôpital. Ce partenariat se concentrera sur l'amélioration des services de recherche clinique et le développement des opportunités d'essais cliniques en Corée. Ce développement devrait accélérer et accroître l'efficacité des essais cliniques, bénéficiant ainsi aux sociétés pharmaceutiques locales et internationales en offrant un environnement de recherche plus solide et plus fiable. L'impact sur le marché sera significatif, car il positionnera la Corée du Sud comme une destination plus attractive pour les essais cliniques mondiaux, ce qui pourrait accélérer la croissance du marché de la recherche clinique dans la région Asie-Pacifique.
- En janvier 2025, ICON plc a annoncé le développement de sa gamme d'outils basés sur l'IA pour optimiser l'efficacité des essais cliniques. Les nouvelles solutions d'IA de l'entreprise sont conçues pour rationaliser divers aspects des essais cliniques, notamment le recrutement des patients, l'analyse des données et la gestion opérationnelle. Cette avancée permettra d'accélérer les délais des essais, de réduire les coûts et d'améliorer la prise de décision tout au long du processus. Parmi les avantages, on compte une utilisation optimisée des ressources, un meilleur ciblage des patients et une plus grande précision des résultats des essais. L'impact sur le marché sera significatif, car ces outils basés sur l'IA transformeront le paysage des essais cliniques, le rendant plus efficace, plus rentable et plus évolutif pour les laboratoires pharmaceutiques internationaux.
SKU-
Accédez en ligne au rapport sur le premier cloud mondial de veille économique
- Tableau de bord d'analyse de données interactif
- Tableau de bord d'analyse d'entreprise pour les opportunités à fort potentiel de croissance
- Accès d'analyste de recherche pour la personnalisation et les requêtes
- Analyse de la concurrence avec tableau de bord interactif
- Dernières actualités, mises à jour et analyse des tendances
- Exploitez la puissance de l'analyse comparative pour un suivi complet de la concurrence
Méthodologie de recherche
La collecte de données et l'analyse de l'année de base sont effectuées à l'aide de modules de collecte de données avec des échantillons de grande taille. L'étape consiste à obtenir des informations sur le marché ou des données connexes via diverses sources et stratégies. Elle comprend l'examen et la planification à l'avance de toutes les données acquises dans le passé. Elle englobe également l'examen des incohérences d'informations observées dans différentes sources d'informations. Les données de marché sont analysées et estimées à l'aide de modèles statistiques et cohérents de marché. De plus, l'analyse des parts de marché et l'analyse des tendances clés sont les principaux facteurs de succès du rapport de marché. Pour en savoir plus, veuillez demander un appel d'analyste ou déposer votre demande.
La méthodologie de recherche clé utilisée par l'équipe de recherche DBMR est la triangulation des données qui implique l'exploration de données, l'analyse de l'impact des variables de données sur le marché et la validation primaire (expert du secteur). Les modèles de données incluent la grille de positionnement des fournisseurs, l'analyse de la chronologie du marché, l'aperçu et le guide du marché, la grille de positionnement des entreprises, l'analyse des brevets, l'analyse des prix, l'analyse des parts de marché des entreprises, les normes de mesure, l'analyse globale par rapport à l'analyse régionale et des parts des fournisseurs. Pour en savoir plus sur la méthodologie de recherche, envoyez une demande pour parler à nos experts du secteur.
Personnalisation disponible
Data Bridge Market Research est un leader de la recherche formative avancée. Nous sommes fiers de fournir à nos clients existants et nouveaux des données et des analyses qui correspondent à leurs objectifs. Le rapport peut être personnalisé pour inclure une analyse des tendances des prix des marques cibles, une compréhension du marché pour d'autres pays (demandez la liste des pays), des données sur les résultats des essais cliniques, une revue de la littérature, une analyse du marché des produits remis à neuf et de la base de produits. L'analyse du marché des concurrents cibles peut être analysée à partir d'une analyse basée sur la technologie jusqu'à des stratégies de portefeuille de marché. Nous pouvons ajouter autant de concurrents que vous le souhaitez, dans le format et le style de données que vous recherchez. Notre équipe d'analystes peut également vous fournir des données sous forme de fichiers Excel bruts, de tableaux croisés dynamiques (Fact book) ou peut vous aider à créer des présentations à partir des ensembles de données disponibles dans le rapport.