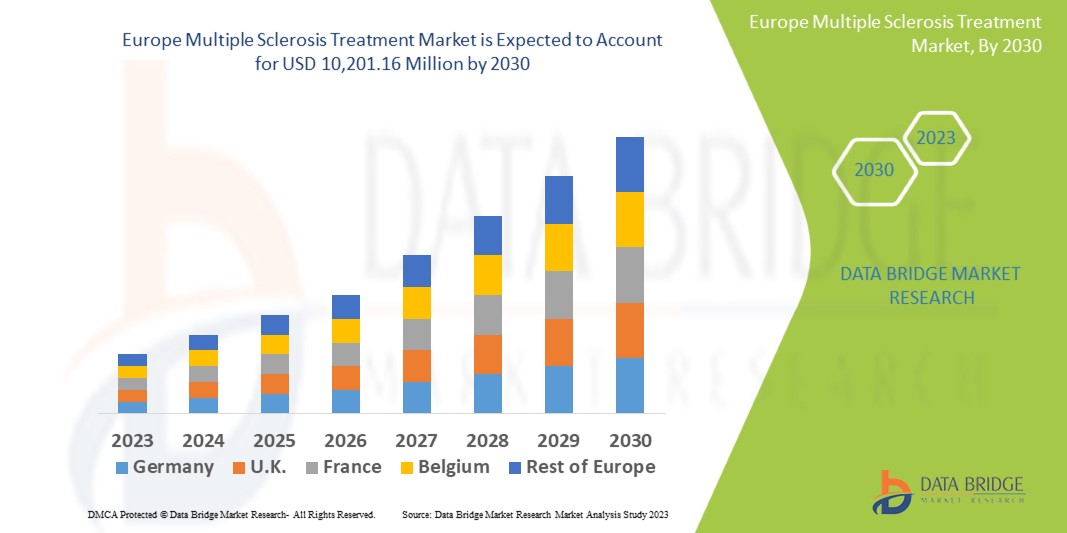
Europe Multiple Sclerosis Treatment Market
Tamanho do mercado em biliões de dólares
CAGR :
% 
 USD
6,026.70 Million
USD
10,201.16 Million
2022
2030
USD
6,026.70 Million
USD
10,201.16 Million
2022
2030
| 2023 –2030 | |
| USD 6,026.70 Million | |
| USD 10,201.16 Million | |
|
|
|
|
Mercado Europeu de Tratamento da Esclerose Múltipla, Tipo de Doença (Esclerose Múltipla Remitente-Recorrente (EMRR), Esclerose Múltipla Secundária Progressiva (EMSP), Esclerose Múltipla Primária Progressiva (EMPP), Esclerose Múltipla Remitente-Recorrente Grave (EMRR)), Tratamento (Terapias Preventivas, Terapias Abortivas/Tratamento de Exacerbações Agudas, Terapias Sintomáticas), Tipo de Medicamento (Marca, Genérico), Usuário Final (Hospitais e Clínicas, Laboratórios de Diagnóstico, Outros) – Tendências e Previsões do Setor até 2030.
Análise e tamanho do mercado europeu de tratamento da esclerose múltipla
O crescente impacto de diversas doenças infecciosas no sistema global de saúde é uma preocupação central, com os países em desenvolvimento arcando com uma parcela desproporcional desse ônus. Segundo o Instituto de Ciências Hepáticas e Biliares da Índia, cerca de 3% da população mundial está infectada com o vírus da hepatite C. O aumento global na incidência de infecções por VHC, especialmente em países desenvolvidos e em desenvolvimento, é um dos principais fatores que impulsionam o crescimento do mercado de tratamento da esclerose múltipla.
A Data Bridge Market Research prevê que o mercado de tratamento da esclerose múltipla deverá atingir US$ 10.201,16 milhões até 2030, o que corresponde a US$ 6.026,7 milhões em 2022, com uma taxa de crescimento anual composta (CAGR) estimada em 6,8% durante o período de previsão de 2022 a 2030. Além das informações sobre cenários de mercado, como valor de mercado, taxa de crescimento, segmentação, abrangência geográfica e principais players, os relatórios de mercado elaborados pela Data Bridge Market Research também incluem análises aprofundadas de especialistas, epidemiologia de pacientes, análise de projetos em desenvolvimento, análise de preços e estrutura regulatória.
Âmbito e segmentação do mercado europeu de tratamento da esclerose múltipla
|
Métrica do relatório |
Detalhes |
|
Período de previsão |
2023 a 2030 |
|
Ano Base |
2022 |
|
Anos históricos |
2021 (Personalizável para 2015 - 2020) |
|
Unidades Quantitativas |
Receita em milhões de dólares, Volume em unidades, Preços em dólares |
|
Segmentos abrangidos |
Tipo de doença (Esclerose Múltipla Remitente-Recorrente (EMRR), Esclerose Múltipla Secundária Progressiva (EMSP), Esclerose Múltipla Primária Progressiva (EMPP), Esclerose Múltipla Remitente-Recorrente Grave (EMRR)), Tratamento (Terapias preventivas, Terapias abortivas/Tratamento de exacerbações agudas, Terapias sintomáticas), Tipo de medicamento (Marca, Genérico), Usuário final (Hospitais, Centros de trauma, Centros cirúrgicos ambulatoriais e outros) |
|
Países abrangidos |
Alemanha, França, Reino Unido, Países Baixos, Suíça, Bélgica, Rússia, Itália, Espanha, Turquia, Resto da Europa na Europa |
|
Participantes do mercado abrangidos |
AbbVie Inc. (EUA), Bausch Health Companies Inc. (Canadá), Biora Therapeutics, Inc (EUA), Boehringer Ingelheim International GmbH (Alemanha), Amgen Inc. (EUA), Pfizer Inc (EUA), F. Hoffmann-La Roche Ltd (Suíça), Mylan NV (EUA), Novartis AG (Suíça), Bayer AG (Alemanha), Bristol Myers Squibb Company (EUA), Biogen (EUA), Teva Pharmaceutical Industries Ltd (Israel), Takeda Pharmaceutical Company Limited (Japão), Jazz Pharmaceuticals, Inc (Reino Unido), Abbott (EUA), Bio-Rad Laboratories Inc. (EUA), Mylan NV (EUA) |
|
Oportunidades de mercado |
|
Definição de mercado
A esclerose múltipla (EM) é uma doença crônica e inflamatória, mediada pelo sistema imunológico, que pode causar secção axonal, desmielinização e neurodegeneração das células nervosas da medula espinhal e do cérebro. Algumas das terapias frequentemente utilizadas incluem a administração de medicamentos injetáveis, orais e por infusão, antidepressivos , fisioterapia e relaxantes musculares.
Dinâmica do mercado europeu de tratamento da esclerose múltipla
Motoristas
- Aumento da conscientização sobre a esclerose múltipla
Tem havido uma crescente conscientização sobre a doença, o que está contribuindo para impulsionar o crescimento do mercado. Por exemplo, a Fundação de Esclerose Múltipla e grupos afiliados iniciaram o Mês Nacional de Educação e Conscientização sobre a Esclerose Múltipla, celebrado em março desde 2003, para conscientizar sobre a doença. O principal objetivo deste programa é promover a compreensão da esclerose múltipla e auxiliar os pacientes a tomarem decisões informadas relacionadas ao seu tratamento. Além disso, a Sociedade Nacional de Esclerose Múltipla criou e lançou a campanha “A Esclerose Múltipla Mata a Conexão > A Conexão Mata a Esclerose Múltipla” para conectar pessoas que sofrem de EM, pessoas que tratam pacientes com EM e pessoas que realizam atividades para criar um mundo livre da esclerose múltipla. Assim, esse fator impulsiona o crescimento do mercado.
- Aumento da incidência de esclerose múltipla
A incidência de esclerose múltipla tem aumentado nesta região. De acordo com um estudo da Sociedade Nacional de Esclerose Múltipla (National Multiple Sclerosis Society), a prevalência estimada da doença era de cerca de 309 casos por 100.000 pessoas em 2010, resultando em um total de 727.344 casos de esclerose múltipla em adultos. A Europa é considerada uma região de alta prevalência de EM. A Sociedade de Esclerose Múltipla afirmou que cerca de 110.000 pessoas sofriam da doença no Reino Unido em 2018. Observa-se também que a incidência de EM é mais que o dobro em mulheres nesta região. O número de novos pacientes diagnosticados a cada ano também está aumentando, passando de 5.000 pacientes em 2017 para 6.700 em 2018. Portanto, essa taxa de incidência está impulsionando a demanda por medicamentos para o tratamento.
Oportunidades
- Aumento das atividades de P&D por parte das organizações
Diversos medicamentos estão em fase de pesquisa para o tratamento da esclerose múltipla (EM) e muitos estão passando por ensaios clínicos. A FDA (Food and Drug Administration) dos EUA aprovou vários medicamentos para o tratamento da EM, como o fingolimode, os interferons , o natalizumabe, o acetato de glatirâmer, a teriflunomida e o fumarato de dimetila. Vários geneticistas, assim como outros pesquisadores, estão estudando o genoma humano em busca de causas e possíveis tratamentos para doenças como distrofia muscular, Alzheimer, câncer e diabetes. Por exemplo, descobriram que algumas pessoas com um gene específico têm maior probabilidade de desenvolver a doença de Alzheimer. Assim, os pesquisadores estão trabalhando em medicamentos que modifiquem ou reparem esse gene em particular. Da mesma forma, muitos pesquisadores descobriram que algumas pessoas que sofrem de esclerose múltipla possuem um determinado gene que as torna mais vulneráveis à doença. Portanto, eles estão constantemente trabalhando em medicamentos que alterem ou reparem esse gene.
Restrições/Desafios
- Alto custo dos medicamentos
O custo dos medicamentos para esclerose múltipla continua sendo um desafio constante para o crescimento do mercado, apesar da alta prevalência da doença. Os preços elevados dos medicamentos dificultam o atendimento às necessidades da população afetada. As terapias modificadoras da doença (TMDs) são a opção padrão de tratamento, mas o custo exorbitante desses medicamentos leva à adesão inadequada e ao manejo incorreto da doença. De acordo com a Sociedade Nacional de Esclerose Múltipla, o custo dos medicamentos para EM está aumentando consideravelmente. Prevê-se que esse fator limite o crescimento do mercado.
Este relatório sobre o mercado de tratamento da esclerose múltipla fornece detalhes sobre os desenvolvimentos recentes, regulamentações comerciais, análise de importação e exportação, análise de produção, otimização da cadeia de valor, participação de mercado, impacto de players de mercado nacionais e locais, análise de oportunidades em termos de novos nichos de receita, mudanças nas regulamentações de mercado, análise estratégica de crescimento de mercado, tamanho do mercado, crescimento de mercado por categoria, nichos de aplicação e dominância, aprovações de produtos, lançamentos de produtos, expansões geográficas e inovações tecnológicas no mercado. Para obter mais informações sobre o mercado de tratamento da esclerose múltipla, entre em contato com a Data Bridge Market Research para uma análise detalhada. Nossa equipe ajudará você a tomar decisões de mercado informadas para alcançar o crescimento desejado.
Desenvolvimentos recentes:
- Em 2021, a Janssen recebeu aprovação da FDA (Food and Drug Administration) dos EUA para o Ponvory. Trata-se de um modulador seletivo do receptor 1 da esfingosina-1-fosfato (S1P1), administrado por via oral uma vez ao dia, utilizado no tratamento de adultos com formas recorrentes de esclerose múltipla (EM), como a síndrome clinicamente isolada, a doença remitente-recorrente e a doença secundária progressiva ativa.
- Em 2020, a Novartis anunciou a aprovação do FDA (Food and Drug Administration) dos EUA para o Kesimpta, na forma de injeção subcutânea, para o tratamento das formas recorrentes de esclerose múltipla (EMR), que incluem a síndrome clinicamente isolada, a doença remitente-recorrente e a doença secundária progressiva ativa, em adultos.
Escopo do mercado europeu de tratamento da esclerose múltipla
O mercado de tratamento da esclerose múltipla é segmentado com base no tipo de doença, tratamento, tipo de medicamento e usuário final. O crescimento entre esses segmentos ajudará você a analisar os segmentos de crescimento mais lento do setor e fornecerá aos usuários uma visão geral valiosa do mercado e informações relevantes para ajudá-los a tomar decisões estratégicas na identificação das principais aplicações de mercado.
Tipo de doença
- Esclerose Múltipla Remitente-Recorrente (EMRR)
- Esclerose Múltipla Secundária Progressiva (EMSP)
- Esclerose Múltipla Primária Progressiva (EMPP)
- Esclerose Múltipla Remitente-Recorrente Grave (RES)
Tratamento
- Terapias Preventivas
- Terapias abortivas/Tratamento de exacerbações agudas
- Terapias Sintomáticas
Tipo de medicamento
- De marca
- Genérico
Via de Administração
- Oral
- Parenteral
Usuário final
- Hospital e Clínicas
- Laboratórios de diagnóstico
- Outros
Análise/Informações Regionais sobre o Tratamento da Esclerose Múltipla
O mercado de tratamento da esclerose múltipla é analisado e são fornecidas informações sobre o tamanho e as tendências do mercado por tipo de doença, tratamento, tipo de medicamento e usuário final, conforme mencionado acima.
Os países abrangidos no relatório de mercado sobre tratamento da esclerose múltipla são Alemanha, França, Reino Unido, Holanda, Suíça, Bélgica, Rússia, Itália, Espanha, Turquia e o restante da Europa.
A Alemanha deverá liderar o mercado no período de previsão de 2023 a 2030 devido à introdução de novas opções de tratamento para esclerose múltipla na região. O crescente investimento em pesquisa e desenvolvimento de medicamentos na região também impulsiona o crescimento do mercado. A maior conscientização da população sobre a esclerose múltipla e seu tratamento contribui para esse crescimento.
A seção do relatório dedicada a cada país também fornece informações sobre os fatores que impactam o mercado local e as mudanças na regulamentação que afetam as tendências atuais e futuras. Dados como análises da cadeia de valor a montante e a jusante, tendências tecnológicas, análise das cinco forças de Porter e estudos de caso são alguns dos indicadores utilizados para prever o cenário de mercado em cada país. Além disso, a presença e a disponibilidade de marcas europeias e os desafios que enfrentam devido à forte ou fraca concorrência de marcas locais e nacionais, bem como o impacto das tarifas e rotas comerciais internas, são considerados na análise das previsões para cada país.
Análise do cenário competitivo e da participação de mercado no tratamento da esclerose múltipla na Europa
O panorama competitivo do mercado de tratamento da esclerose múltipla fornece detalhes sobre cada concorrente. Os detalhes incluem visão geral da empresa, dados financeiros, receita gerada, potencial de mercado, investimento em pesquisa e desenvolvimento, iniciativas em novos mercados, presença na Europa, locais e instalações de produção, capacidades de produção, pontos fortes e fracos da empresa, lançamento de produtos, amplitude e variedade do portfólio de produtos e domínio de aplicações. Os dados acima referem-se apenas ao foco das empresas no mercado de tratamento da esclerose múltipla.
Alguns dos principais participantes que atuam no mercado de tratamento da esclerose múltipla são:
- AbbVie Inc. (EUA)
- Bausch Health Companies Inc. (Canadá)
- Biora Therapeutics, Inc (EUA)
- Boehringer Ingelheim International GmbH (Alemanha)
- Amgen Inc. (EUA)
- Pfizer Inc (EUA)
- F. Hoffmann-La Roche Ltda. (Suíça)
- Mylan NV (EUA)
- Novartis AG (Suíça)
- Bayer AG (Alemanha)
- Empresa Bristol Myers Squibb (EUA)
- Biogen (EUA)
- Teva Pharmaceutical Industries Ltd (Israel)
- Takeda Pharmaceutical Company Limited (Japão)
- Jazz Pharmaceuticals, Inc (Reino Unido)
- Abbott (EUA)
- Bio-Rad Laboratories Inc. (EUA)
- Mylan NV (EUA)
SKU-
Obtenha acesso online ao relatório sobre a primeira nuvem de inteligência de mercado do mundo
- Painel interativo de análise de dados
- Painel de análise da empresa para oportunidades de elevado potencial de crescimento
- Acesso de analista de pesquisa para personalização e customização. consultas
- Análise da concorrência com painel interativo
- Últimas notícias, atualizações e atualizações Análise de tendências
- Aproveite o poder da análise de benchmark para um rastreio abrangente da concorrência
Índice
1 INTRODUÇÃO
1.1 OBJETIVOS DO ESTUDO
1.2 DEFINIÇÃO DE MERCADO
1.3 VISÃO GERAL DO MERCADO EUROPEU DE TRATAMENTO DA ESCLEROSE MÚLTIPLA
1.4 MOEDA E PREÇOS
1.5 LIMITAÇÃO
1.6 MERCADOS ABRANGIDOS
2. SEGMENTAÇÃO DE MERCADO
2.1 PRINCIPAIS CONCLUSÕES
2.2 ATINGINDO O TAMANHO DO MERCADO EUROPEU DE TRATAMENTO DA ESCLEROSE MÚLTIPLA
2.2.1 GRADE DE POSICIONAMENTO DE FORNECEDORES
2.2.2 CURVA DO CICLO DE VIDA DA TECNOLOGIA
2.2.3 MODELO DE VALIDAÇÃO DE DADOS TRIPÉ
2.2.4 GUIA DE MERCADO
2.2.5 MODELAGEM MULTIVARIADA
2.2.6 ANÁLISE DE CIMA PARA BAIXO
2.2.7 MATRIZ DE DESAFIO
2.2.8 GRADE DE COBERTURA DE APLICAÇÕES
2.2.9 NORMAS DE MEDIÇÃO
2.2.10 ANÁLISE DA PARTICIPAÇÃO DE MERCADO DOS FORNECEDORES
2.2.11 MODELO BASEADO EM EPIDEMIOLOGIA
2.2.12 PONTOS DE DADOS DE ENTREVISTAS PRIMÁRIAS PRINCIPAIS
2.2.13 PONTOS DE DADOS DE PRINCIPAIS BASES DE DADOS SECUNDÁRIAS
2.3 MERCADO EUROPEU DE TRATAMENTO DA ESCLEROSE MÚLTIPLA: PANORAMA DA PESQUISA
2.4 PRESSUPOSTOS
3. VISÃO GERAL DO MERCADO
3.1 MOTORISTAS
3.2 RESTRIÇÕES
3.3 OPORTUNIDADES
3.4 DESAFIOS
4 RESUMO EXECUTIVO
5 INFORMAÇÕES PREMIUM
5.1 ANÁLISE PESTEL
5.2 AS CINCO FORÇAS DE PORTER
6 EPIDEMIOLOGIA
6.1 INCIDÊNCIA DE TODOS POR GÊNERO
6.2 TAXA DE TRATAMENTO
6.3 TAXA DE MORTALIDADE
6.4 MODELO DE ADESÃO A MEDICAMENTOS E MUDANÇA DE TERAPIA
6.5 TAXAS DE SUCESSO NO TRATAMENTO DE PACIENTES
7 VISÕES SOBRE O SETOR
7.1 ANÁLISE DE PATENTES
7.2 TAXA DE TRATAMENTO MEDICAMENTOSO POR MERCADOS MADUROS
7.3 TENDÊNCIAS DEMOGRÁFICAS: IMPACTOS EM TODAS AS TAXAS DE INCIDÊNCIA
7.4 DIAGRAMA DE FLUXO DE PACIENTES
7.5 PRINCIPAIS ESTRATÉGIAS DE PRECIFICAÇÃO
7.6 PRINCIPAIS ESTRATÉGIAS DE RECRUTAMENTO DE PACIENTES
7.7 ENTREVISTAS COM HEMATOLOGISTAS
7.8 ENTREVISTAS COM ONCOLOGISTAS
7.9 ENTREVISTAS COM ORGANIZAÇÕES DE COMBATE AO CÂNCER
7.1 OUTRAS FOTOS DE KOLs
8 ANÁLISE DE DUTOS
8.1 ENSAIOS CLÍNICOS E ANÁLISE DE FASE
8.2 PROGRAMA DE TERAPIA MEDICAMENTOSA
8.3 CANDIDATOS DA FASE III
8.4 CANDIDATOS DA FASE II
8.5 CANDIDATOS DA FASE I
8.6 OUTROS (PRÉ-CLÍNICOS E DE PESQUISA)
9. QUADRO REGULATÓRIO
10. MERCADO EUROPEU DE TRATAMENTO DA ESCLEROSE MÚLTIPLA, POR TIPO
10.1 VISÃO GERAL
10.2 ESCLEROSE MÚLTIPLA RECIDIVANTE-REMITENTE (EMRR)
10.3 SÍNDROME CLINICAMENTE ISOLADA (SCI)
10.4 Esclerose Múltipla Primária Progressiva (EMPP)
10.5 Esclerose Múltipla Progressiva Secundária (EMPS)
11 MERCADO EUROPEU DE TRATAMENTO DA ESCLEROSE MÚLTIPLA, POR TRATAMENTO
11.1 VISÃO GERAL
11.2 MEDICAMENTOS
11.2.1 MEDICAMENTOS MODIFICADORES DA DOENÇA
11.2.1.1. ANTICORPO MONOCLONAL
11.2.1.1.1. ANTICORPO MONOCLONAL, POR TIPO
11.2.1.1.1.1 OCRELIZUMAB
11.2.1.1.1.2 NATALIZUMAB
11.2.1.1.1.3 DACLIZUMAB
11.2.1.1.1.4 OUTROS
11.2.1.1.2. ANTICORPO MONOCLONAL, POR TIPO DE MEDICAMENTO
11.2.1.1.2.1 GENÉRICO
11.2.1.1.2.2 MARCA
11.2.1.1.2.2.1. OCREVUS
11.2.1.1.2.2.2. TYSABRI
11.2.1.1.2.2.3. ZENAPAX
11.2.1.2. MEDICAMENTOS IMUNOMODULADORES
11.2.1.2.1. MEDICAMENTOS IMUNOMODULADORES, POR MEDICAMENTO
11.2.1.2.1.1 GLATIRAMER
11.2.1.2.1.2 CLADRIBINA
11.2.1.2.1.3 TERIFLUNOMIDA
11.2.1.2.1.4 FUMARATO DE DIMETILA
11.2.1.2.1.5 OUTROS
11.2.1.2.2. MEDICAMENTOS IMUNOMODULADORES, POR TIPO DE MEDICAMENTO
11.2.1.2.2.1 GENÉRICO
11.2.1.2.2.2 MARCA
11.2.1.2.2.2.1. GLATOPA
11.2.1.2.2.2.2. COPAXONE
11.2.1.2.2.2.3. MAVENCLAD
11.2.1.2.2.2.4. OUTROS
11.2.1.3. MODULADORES DO RECEPTOR DE ESFINGOSINA 1-FOSFATO (S1P)
11.2.1.3.1. MODULADORES DO RECEPTOR DE ESFINGOSINA 1-FOSFATO (S1P), POR TIPO
11.2.1.3.1.1 PONESIMOD
11.2.1.3.1.2 FINGOLIMOD
11.2.1.3.1.3 SIPONIMOD
11.2.1.3.1.4 OZANIMOD
11.2.1.3.1.5 OUTROS
11.2.1.3.2. MODULADORES DO RECEPTOR DE ESFINGOSINA 1-FOSFATO (S1P), POR TIPO DE FÁRMACO
11.2.1.3.2.1 GENÉRICO
11.2.1.3.2.2 MARCA
11.2.1.3.2.2.1. PONVORY
11.2.1.3.2.2.2. ZEPOSIA
11.2.1.3.2.2.3. MAYZENT
11.2.1.3.2.2.4. ZEPOSIA
11.2.1.4. MEDICAMENTOS ANTICÂNCER
11.2.1.4.1. MEDICAMENTOS ANTICANCERÍGENOS, POR TIPO
11.2.1.4.1.1 MITOCANTRONA
11.2.1.4.1.2 CICLOFOSFAMIDA
11.2.1.4.1.3 MELFALAN FLUFENAMIDA
11.2.1.4.1.4 OUTROS
11.2.1.4.2. MEDICAMENTOS ANTICANCERÍGENOS, POR TIPO DE MEDICAMENTO
11.2.1.4.2.1 GENÉRICO
11.2.1.4.2.2 MARCA
11.2.1.4.2.2.1. PEPAXTO
11.2.1.4.2.2.2. CITOXANO
11.2.1.4.2.2.3. NEOSAR
11.2.1.4.2.2.4. OUTROS
11.2.1.5. INTERFERÊNCIA
11.2.1.5.1. INTERFERONA, POR TIPO
11.2.1.5.1.1 INTERFERON BETA-1B
11.2.1.5.1.2 INTERFERON BETA-1A
11.2.1.5.1.3 INTERFERON BETA-1A PEGILARIZADO
11.2.1.5.1.4 OUTROS
11.2.1.5.2. INTERFERONA, POR TIPO DE MEDICAMENTO
11.2.1.5.2.1 GENÉRICO
11.2.1.5.2.2 MARCA
11.2.1.5.2.2.1. ROFERON
11.2.1.5.2.2.2. VIRAFERON
11.2.1.5.2.2.3. AVONEX
11.2.1.5.2.2.4. BETASERON
11.2.1.6. IMUNOSSUPRESSORES
11.2.1.6.1. IMUNOSSUPRESSORES, POR TIPO
11.2.1.6.1.1 AZATIOPRINA
11.2.1.6.1.2 METOTREXATO
11.2.1.6.1.3 OUTROS
11.2.1.6.2. IMUNOSSUPRESSORES, POR TIPO DE MEDICAMENTO
11.2.1.6.2.1 AZASAN
11.2.1.6.2.2 IMURAN
11.2.1.6.2.3 REDITREX
11.2.1.6.2.4 TREXALL
11.2.1.6.2.5 XATMEP
11.2.2 TERAPIAS SINTOMÁTICAS
11.2.2.1. RELAXANTES MUSCULARES
11.2.2.1.1. RELAXANTES MUSCULARES, POR TIPO
11.2.2.1.1.1 BACLOFEN
11.2.2.1.1.2 TIZANIDINA
11.2.2.1.1.3 CICLOBENZAPRINA
11.2.2.1.1.4 OUTROS
11.2.2.1.2. RELAXANTES MUSCULARES, POR TIPO DE MEDICAMENTO
11.2.2.1.2.1 GENÉRICO
11.2.2.1.2.2 MARCA
11.2.2.1.2.2.1. LIORESAL
11.2.2.1.2.2.2. ZANAFLEX
11.2.2.1.2.2.3. FLEXERIL
11.2.2.2. MEDICAMENTOS PARA FADIGA
11.2.2.2.1. MEDICAMENTOS PARA FADIGA, POR TIPO
11.2.2.2.1.1 AMANTADINA
11.2.2.2.1.2 MODAFINIL
11.2.2.2.1.3 METILFENIDATO
11.2.2.2.1.4 OUTROS
11.2.2.2.2. MEDICAMENTOS PARA FADIGA, POR TIPO DE MEDICAMENTO
11.2.2.2.2.1 GENÉRICO
11.2.2.2.2.2 MARCA
11.2.2.2.2.2.1. GOCOVRI
11.2.2.2.2.2.2. PROVIGIL
11.2.2.2.2.2.3. RITALIN
11.2.2.3. DOR NEUROPÁTICA
11.2.2.3.1. GABAPENTINA
11.2.2.3.2. CARBAMAZEPINA
11.2.2.3.3. AMITRIPTILINA
11.2.2.3.4. OUTROS
11.2.2.4. CORTICOSTEROIDES
11.2.2.4.1. PREDNISONA
11.2.2.4.2. METILPREDNISOLONA
11.2.2.4.3. DEXAMETASONA
11.2.2.4.4. PREDNISOLONA
11.2.2.4.5. BETAMETASONA
11.2.2.4.6. OUTROS
11.3 FISIOTERAPIA
11.3.1 TERAPIA MANUAL
11.3.2 TRATAMENTOS ESPECIALIZADOS
11.3.3 TÉCNICAS DE MOBILIZAÇÃO ARTICULAR
11.3.4 TERAPIA DE SUSPENSÃO
11.3.5 TÉCNICAS DE RELAXAMENTO
11.3.6 MÉTODOS DE CORREÇÃO DE POSTURA
11.4 PLASMAFERÉS
11.4.1 TROCA PLASMÁTICA (TP)
11.4.2 PLASMAFERÉS DE FILTRAÇÃO DE DUPLA MEMBRANA (DFP)
11.4.3 PLASMAFERÉS DE ADSORÇÃO
11.5 OUTROS
12. MERCADO GLOBAL DE ESCLEROSE MÚLTIPLA, POR TIPO DE MEDICAMENTO
12.1 VISÃO GERAL
12.2 GENÉRICO
12.3 MARCA
12.3.1 OCREVUS
12.3.2 TYSABRI
12.3.3 ZENAPAX
12.3.4 GLATOPA
12.3.5 COPAXONE
12.3.6 MAVENCLAD
12.3.7 PONVORY
12.3.8 ZEPOSIA
12.3.9 MAYZENT
12.3.10 ZEPOSIA
12.3.11 PEPAXTO
12.3.12 CITOXANO
12.3.13 NEOSAR
12.3.14 ROFERON
12.3.15 VIRAFERON
12.3.16 AVONEX
12.3.17 BETASERON
12.3.18 BACLOFEN
12.3.19 TIZANIDINA
12.3.20 CICLOBENZAPRINA
12.3.21 OUTROS
13 MERCADO EUROPEU DE TRATAMENTO DA ESCLEROSE MÚLTIPLA, POR VIA DE ADMINISTRAÇÃO
13.1 VISÃO GERAL
13.2 ORAL
13.2.1 COMPRIMIDO
13.2.2 CÁPSULA
13.2.3 OUTROS
13.3 PARENTERAL
13.3.1 INTRAVENOSO
13.3.2 SUBCUTÂNEO
13.3.3 OUTROS
13.4 OUTROS
14 MERCADO EUROPEU DE TRATAMENTO DA ESCLEROSE MÚLTIPLA, POR TIPO DE PRESCRIÇÃO
14.1 VISÃO GERAL
14.2 SEM RECEITA MÉDICA
14.3 PRESCRIÇÃO
15. MERCADO EUROPEU DE TRATAMENTO DA ESCLEROSE MÚLTIPLA, POR FAIXA ETÁRIA
15.1 VISÃO GERAL
15.2 CRIANÇAS
15,3 ADULTOS
15.4 GERIÁTRICO
16. MERCADO EUROPEU DE TRATAMENTO DA ESCLEROSE MÚLTIPLA, POR GÊNERO
16.1 VISÃO GERAL
16,2 MASCULINO
16,3 FEMININO
17. MERCADO EUROPEU DE TRATAMENTO DA ESCLEROSE MÚLTIPLA, POR USUÁRIO FINAL
17.1 VISÃO GERAL
17.2 HOSPITAIS
17.3 CLÍNICAS ESPECIALIZADAS
17.4 CUIDADOS DE SAÚDE DOMICILIARES
17,5 CENTROS CIRÚRGICOS AMBULATORIAIS
17.6 OUTROS
18. MERCADO EUROPEU DE TRATAMENTO DA ESCLEROSE MÚLTIPLA, POR CANAL DE DISTRIBUIÇÃO
18.1 VISÃO GERAL
18.2 FARMÁCIA HOSPITALAR
18.3 FARMÁCIA DE VAREJO
18.3.1 LOJAS ONLINE
18.3.2 FARMÁCIAS
18.4 OUTROS
19 MERCADO EUROPEU DE TRATAMENTO DA ESCLEROSE MÚLTIPLA, POR GEOGRAFIA
MERCADO EUROPEU DE TRATAMENTO DA ESCLEROSE MÚLTIPLA (TODA A SEGMENTAÇÃO ACIMA ESTÁ REPRESENTADA NESTE CAPÍTULO POR PAÍS)
19.1 EUROPA
19.1.1 ALEMANHA
19.1.2 Reino Unido
19.1.3 ITÁLIA
19.1.4 FRANÇA
19.1.5 ESPANHA
19.1.6 RÚSSIA
19.1.7 SUÍÇA
19.1.8 TURQUIA
19.1.9 BÉLGICA
19.1.10 PAÍSES BAIXOS
19.1.11 DINAMARCA
19.1.12 SUÉCIA
19.1.13 POLÔNIA
19.1.14 NORUEGA
19.1.15 FINLÂNDIA
19.1.16 RESTO DA EUROPA
20 MERCADO EUROPEU DE TRATAMENTO DA ESCLEROSE MÚLTIPLA, PANORAMA DAS EMPRESAS
20.1 ANÁLISE DAS AÇÕES DA EMPRESA: GLOBAL
20.2 ANÁLISE DAS AÇÕES DA EMPRESA: AMÉRICA DO NORTE
20.3 ANÁLISE DAS AÇÕES DA EMPRESA: EUROPA
20.4 ANÁLISE DAS AÇÕES DA EMPRESA: EUROPA
20.5 FUSÕES E AQUISIÇÕES
20.6 DESENVOLVIMENTO E APROVAÇÕES DE NOVOS PRODUTOS
20.7 EXPANSÕES
20.8 ALTERAÇÕES REGULAMENTARES
20.9 PARCERIAS E OUTROS DESENVOLVIMENTOS ESTRATÉGICOS
21 MERCADO EUROPEU DE TRATAMENTO DA ESCLEROSE MÚLTIPLA, ANÁLISE SWOT E DBMR
22. MERCADO EUROPEU DE TRATAMENTO DA ESCLEROSE MÚLTIPLA, PERFIL DA EMPRESA
22.1 BIOGEN
22.1.1 VISÃO GERAL DA EMPRESA
22.1.2 ANÁLISE DE RECEITAS
22.1.3 PRESENÇA GEOGRÁFICA
22.1.4 PORTFÓLIO DE PRODUTOS
22.1.5 DESENVOLVIMENTOS RECENTES
22.2 TEVA NEUROSCIENCE, INC.
22.2.1 VISÃO GERAL DA EMPRESA
22.2.2 ANÁLISE DE RECEITAS
22.2.3 PRESENÇA GEOGRÁFICA
22.2.4 PORTFÓLIO DE PRODUTOS
22.2.5 DESENVOLVIMENTOS RECENTES
22.3 VIATRIS INC.
22.3.1 VISÃO GERAL DA EMPRESA
22.3.2 ANÁLISE DE RECEITAS
22.3.3 PRESENÇA GEOGRÁFICA
22.3.4 PORTFÓLIO DE PRODUTOS
22.3.5 DESENVOLVIMENTOS RECENTES
22.4 NOVARTIS AG
22.4.1 VISÃO GERAL DA EMPRESA
22.4.2 ANÁLISE DE RECEITAS
22.4.3 PRESENÇA GEOGRÁFICA
22.4.4 PORTFÓLIO DE PRODUTOS
22.4.5 DESENVOLVIMENTOS RECENTES
22,5 MERCK KGAA
22.5.1 VISÃO GERAL DA EMPRESA
22.5.2 ANÁLISE DE RECEITAS
22.5.3 PRESENÇA GEOGRÁFICA
22.5.4 PORTFÓLIO DE PRODUTOS
22.5.5 DESENVOLVIMENTOS RECENTES
22.6 GLENMARK PHARMACEUTICALS LTD
22.6.1 VISÃO GERAL DA EMPRESA
22.6.2 ANÁLISE DE RECEITAS
22.6.3 PRESENÇA GEOGRÁFICA
22.6.4 PORTFÓLIO DE PRODUTOS
22.6.5 DESENVOLVIMENTOS RECENTES
22,7 LUPINO
22.7.1 VISÃO GERAL DA EMPRESA
22.7.2 ANÁLISE DE RECEITAS
22.7.3 PRESENÇA GEOGRÁFICA
22.7.4 PORTFÓLIO DE PRODUTOS
22.7.5 DESENVOLVIMENTOS RECENTES
22.8 CIPLA INC
22.8.1 VISÃO GERAL DA EMPRESA
22.8.2 ANÁLISE DE RECEITAS
22.8.3 PRESENÇA GEOGRÁFICA
22.8.4 PORTFÓLIO DE PRODUTOS
22.8.5 DESENVOLVIMENTOS RECENTES
22,9 SANOFI
22.9.1 VISÃO GERAL DA EMPRESA
22.9.2 ANÁLISE DE RECEITAS
22.9.3 PRESENÇA GEOGRÁFICA
22.9.4 PORTFÓLIO DE PRODUTOS
22.9.5 DESENVOLVIMENTOS RECENTES
22.1 BAYER
22.10.1 VISÃO GERAL DA EMPRESA
22.10.2 ANÁLISE DE RECEITAS
22.10.3 PRESENÇA GEOGRÁFICA
22.10.4 PORTFÓLIO DE PRODUTOS
22.10.5 DESENVOLVIMENTOS RECENTES
22.11 ABBVIE, INC
22.11.1 VISÃO GERAL DA EMPRESA
22.11.2 ANÁLISE DE RECEITAS
22.11.3 PRESENÇA GEOGRÁFICA
22.11.4 PORTFÓLIO DE PRODUTOS
22.11.5 DESENVOLVIMENTOS RECENTES
22.12 ABBOTT
22.12.1 VISÃO GERAL DA EMPRESA
22.12.2 ANÁLISE DE RECEITAS
22.12.3 PRESENÇA GEOGRÁFICA
22.12.4 PORTFÓLIO DE PRODUTOS
22.12.5 DESENVOLVIMENTOS RECENTES
22.13 F. HOFFMANN-LA ROCHE LTD
22.13.1 VISÃO GERAL DA EMPRESA
22.13.2 ANÁLISE DE RECEITAS
22.13.3 PRESENÇA GEOGRÁFICA
22.13.4 PORTFÓLIO DE PRODUTOS
22.13.5 DESENVOLVIMENTOS RECENTES
22.14 BRISTOL MYERS SQUIBB
22.14.1 VISÃO GERAL DA EMPRESA
22.14.2 ANÁLISE DE RECEITAS
22.14.3 PRESENÇA GEOGRÁFICA
22.14.4 PORTFÓLIO DE PRODUTOS
22.14.5 DESENVOLVIMENTOS RECENTES
22.15 TG THERAPEUTICS, INC
22.15.1 VISÃO GERAL DA EMPRESA
22.15.2 ANÁLISE DE RECEITAS
22.15.3 PRESENÇA GEOGRÁFICA
22.15.4 PORTFÓLIO DE PRODUTOS
22.15.5 DESENVOLVIMENTOS RECENTES
NOTA: A LISTA DE EMPRESAS APRESENTADA NÃO É EXAUSTIVA E RESULTA DE ACORDO COM AS SOLICITAÇÕES DE NOSSOS CLIENTES ANTERIORES. AVALIAMOS MAIS DE 100 EMPRESAS EM NOSSO ESTUDO, PORTANTO, A LISTA PODE SER MODIFICADA OU SUBSTITUÍDA MEDIANTE SOLICITAÇÃO.
23 RELATÓRIOS RELACIONADOS
24 CONCLUSÃO
25 QUESTIONÁRIO
26 SOBRE A DATA BRIDGE MARKET RESEARCH
1 INTRODUÇÃO
1.1 OBJETIVOS DO ESTUDO
1.2 DEFINIÇÃO DE MERCADO
1.3 VISÃO GERAL DO MERCADO EUROPEU DE TRATAMENTO DA ESCLEROSE MÚLTIPLA
1.4 MOEDA E PREÇOS
1.5 LIMITAÇÃO
1.6 MERCADOS ABRANGIDOS
2. SEGMENTAÇÃO DE MERCADO
2.1 PRINCIPAIS CONCLUSÕES
2.2 CHEGANDO AO MERCADO EUROPEU DE TRATAMENTO DA ESCLEROSE MÚLTIPLA
2.2.1 GRADE DE POSICIONAMENTO DE FORNECEDORES
2.2.2 CURVA DO CICLO DE VIDA DA TECNOLOGIA
2.2.3 MODELO DE VALIDAÇÃO DE DADOS TRIPÉ
2.2.4 GUIA DE MERCADO
2.2.5 MODELAGEM MULTIVARIADA
2.2.6 ANÁLISE DE CIMA PARA BAIXO
2.2.7 MATRIZ DE DESAFIO
2.2.8 GRADE DE COBERTURA DE APLICAÇÕES
2.2.9 NORMAS DE MEDIÇÃO
2.2.10 ANÁLISE DA PARTICIPAÇÃO DE MERCADO DOS FORNECEDORES
2.2.11 DADOS DE VOLUME DE VENDAS
2.2.12 PONTOS DE DADOS DE ENTREVISTAS PRIMÁRIAS PRINCIPAIS
2.2.13 PONTOS DE DADOS DE PRINCIPAIS BASES DE DADOS SECUNDÁRIAS
2.3 MERCADO EUROPEU DE TRATAMENTO DA ESCLEROSE MÚLTIPLA: PANORAMA DA PESQUISA
2.4 PRESSUPOSTOS
3. VISÃO GERAL DO MERCADO
3.1 MOTORISTAS
3.2 RESTRIÇÕES
3.3 OPORTUNIDADES
3.4 DESAFIOS
4 RESUMO EXECUTIVO
5 INFORMAÇÕES PREMIUM
5.1 ANÁLISE PESTEL
5.2 MODELO DAS CINCO FORÇAS DE PORTER
5.3 EVOLUÇÃO DO MERCADO DE TRATAMENTO DE ESCLEROSE MÚLTIPLA NA EUROPA NOS ÚLTIMOS 10 A 20 ANOS
6 VISÕES SOBRE O SETOR
6.1 ANÁLISE DE PATENTES
6.1.1 PANORAMA DE PATENTES
6.1.2 NÚMERO USPTO
6.1.3 EXPIRAÇÃO DA PATENTE
6.1.4 NÚMERO DO EPISÓDIO
6.1.5 FORÇA E QUALIDADE DA PATENTE
6.1.6 REIVINDICAÇÕES DE PATENTE
6.1.7 CITAÇÕES DE PATENTES
6.1.8 LITÍGIOS E LICENCIAMENTO DE PATENTES
6.1.9 PEDIDO DE PATENTE
6.1.10 PAÍSES COM PATENTE CONCEDIDA
6.1.11 CONTEXTO TECNOLÓGICO
6.2 TAXA DE TRATAMENTO MEDICAMENTOSO POR MERCADOS MADUROS
6.3 TENDÊNCIAS DEMOGRÁFICAS: IMPACTOS EM TODAS AS TAXAS DE INCIDÊNCIA
6.4 DIAGRAMA DE FLUXO DE PACIENTES
6.5 PRINCIPAIS ESTRATÉGIAS DE PRECIFICAÇÃO
6.6 PRINCIPAIS ESTRATÉGIAS DE RECRUTAMENTO DE PACIENTES
6.7 ENTREVISTAS COM ESPECIALISTAS
6.8 OUTRAS FOTOS DE KOL
7 EPIDEMIOLOGIA
7.1 INCIDÊNCIA DE TODOS POR GÊNERO
7.2 TAXA DE TRATAMENTO
7.3 TAXA DE MORTALIDADE
7.4 MODELO DE ADESÃO A MEDICAMENTOS E MUDANÇA DE TERAPIA
7,5 TAXAS DE SUCESSO NO TRATAMENTO DE PACIENTES
8. FUSÕES E AQUISIÇÕES
8.1 LICENCIAMENTO
8.2 ACORDOS DE COMERCIALIZAÇÃO
9. QUADRO REGULATÓRIO
9.1 PROCESSO DE APROVAÇÃO REGULATÓRIA
9.2 FACILIDADE DE APROVAÇÃO REGULATÓRIA DAS REGIÕES GEOGRÁFICAS
9.3 CAMINHOS DE APROVAÇÃO REGULATÓRIA
9.4 LICENCIAMENTO E REGISTRO
9.5 VIGILÂNCIA PÓS-COMERCIALIZAÇÃO
9.6 DIRETRIZES DE BOAS PRÁTICAS DE FABRICAÇÃO (BPF)
10 ANÁLISE DE DUTOS
10.1 ENSAIOS CLÍNICOS E ANÁLISE DE FASE
10.2 PROGRAMA DE TERAPIA MEDICAMENTOSA
10.3 CANDIDATOS DA FASE III
10.4 CANDIDATOS DA FASE II
10.5 CANDIDATOS DA FASE I
10.6 OUTROS (PRÉ-CLÍNICOS E DE PESQUISA)
TABELA 1 MERCADO EUROPEU DE ENSAIOS CLÍNICOS PARA O TRATAMENTO DA ESCLEROSE MÚLTIPLA
Nome da empresa Área terapêutica
XX XX
XX XX
XX XX
XX XX
XX XX
XX XX
Fontes: Comunicados de imprensa, Relatórios anuais, Documentos da SEC, Apresentações para investidores, Outras fontes governamentais, Análises baseadas em informações secundárias, Entrevistas com especialistas
TABELA 2 DISTRIBUIÇÃO DE PRODUTOS E PROJETOS POR FASE NO MERCADO DE TRATAMENTO DA ESCLEROSE MÚLTIPLA
Número de fases dos projetos
Projetos pré-clínicos/de pesquisa XX
Desenvolvimento Clínico XX
Fase I XX
Fase II XX
Fase III XX
Registrado/Aprovado nos EUA, mas ainda não comercializado XX
Total XX
Fontes: Comunicados de imprensa, Relatórios anuais, Documentos da SEC, Apresentações para investidores, Outras fontes governamentais, Análises baseadas em informações secundárias, Entrevistas com especialistas
TABELA 3 DISTRIBUIÇÃO DE PROJETOS POR ÁREA TERAPÊUTICA E FASE DO MERCADO DE TRATAMENTO DA ESCLEROSE MÚLTIPLA
Área terapêutica: Projeto pré-clínico/de pesquisa
XX XX
XX XX
XX XX
XX XX
XX XX
Total de Projetos XX
Fontes: Comunicados de imprensa, Relatórios anuais, Documentos da SEC, Apresentações para investidores, Outras fontes governamentais, Análises baseadas em informações secundárias, Entrevistas com especialistas
TABELA 4 DISTRIBUIÇÃO DE PROJETOS POR ABORDAGEM CIENTÍFICA E FASE DO MERCADO DE TRATAMENTO DA ESCLEROSE MÚLTIPLA
Projeto de pesquisa/pré-clínica tecnológica
XX XX
XX XX
XX XX
XX XX
XX XX
Total de Projetos XX
Fontes: Comunicados de imprensa, Relatórios anuais, Documentos da SEC, Apresentações para investidores, Outras fontes governamentais, Análises baseadas em informações secundárias, Entrevistas com especialistas
FIGURA 1 PRINCIPAIS ENTIDADES COM BASE EM UMA ANÁLISE DE P&D PARA O MERCADO DE TRATAMENTO DE ESCLEROSE MÚLTIPLA
Fontes: Comunicados de imprensa, Relatórios anuais, Documentos da SEC, Apresentações para investidores, Outras fontes governamentais, Análises baseadas em informações secundárias, Entrevistas com especialistas
11 ANÁLISE DE MEDICAMENTOS COMERCIALIZADOS
11.1 DROGA
11.1.1 NOME DA MARCA
11.1.2 NOME GENÉRICO
11.2 INDICAÇÃO TERAPÊUTICA
11.3 CLASSE FARMACOLÓGICA DO MEDICAMENTO
11.4 INDICAÇÃO PRINCIPAL DO MEDICAMENTO
11.5 SITUAÇÃO DO MERCADO
11.6 TIPO DE MEDICAMENTO
11.7 FORMAS DE DOSAGEM DE MEDICAMENTOS
11.8 DISPONIBILIDADE DE DOSAGENS
11.9 VIA DE ADMINISTRAÇÃO DO MEDICAMENTO
11.1 FREQUÊNCIA DE DOSAGEM
11.11 ANÁLISE DE MEDICAMENTOS
11.12 UMA VISÃO GERAL DAS ATIVIDADES DE DESENVOLVIMENTO DE MEDICAMENTOS, TAIS COMO MARCOS REGULATÓRIOS, DADOS DE SEGURANÇA E EFICÁCIA, DADOS DE EXCLUSIVIDADE DE MERCADO.
11.12.1 PREVISÃO DO MERCADO
11.12.2 COMPETIÇÃO DE CROSS
11.12.3 PORTFÓLIO TERAPÊUTICO
11.12.4 CENÁRIO DE DESENVOLVIMENTO ATUAL
12 ACESSO AO MERCADO
12.1 PREVISÃO DE MERCADO PARA 10 ANOS
12.2 ATUALIZAÇÕES RECENTES DE ENSAIOS CLÍNICOS
12,3 NOVOS MEDICAMENTOS APROVADOS ANUALMENTE PELA FDA
12.4 FABRICANTES E NEGÓCIOS DE MEDICAMENTOS
12,5 CONSUMO DE DROGAS PRINCIPAIS
12.6 PRÁTICAS DE TRATAMENTO ATUAIS
12.7 IMPACTO DA TERAPIA FUTURA
13 ANÁLISE DE P&D
13.1 ANÁLISE COMPARATIVA
13.2 PANORAMA DO DESENVOLVIMENTO DE FÁRMACOS
13.3 ANÁLISES DETALHADAS SOBRE MARCOS REGULATÓRIOS
13.4 AVALIAÇÃO TERAPÊUTICA
13.5 Colaborações e parcerias baseadas em ativos
14. VISÃO GERAL DO MERCADO
14.1 MOTORISTAS
14.2 RESTRIÇÕES
14.3 OPORTUNIDADES
14.4 DESAFIOS
15 MERCADO EUROPEU DE TRATAMENTO DA ESCLEROSE MÚLTIPLA, POR TIPO
15.1 VISÃO GERAL
15.2 SÍNDROME CLINICAMENTE ISOLADA (SCI)
15.3 ESCLEROSE MÚLTIPLA RECIDIVANTE-REMITENTE (EMRR)
15.4 ESCLEROSE MÚLTIPLA PROGRESSIVA SECUNDÁRIA (EMPS)
15.5 ESCLEROSE MÚLTIPLA PROGRESSIVA PRIMÁRIA (EMPP)
15.6 ESCLEROSE MÚLTIPLA RECIDIVANTE-REMITÓRIA GRAVE (RES)
16 MERCADO EUROPEU DE TRATAMENTO DA ESCLEROSE MÚLTIPLA, POR TERAPÊUTICAS
16.1 VISÃO GERAL
16.2 MEDICAMENTOS APROVADOS/COMERCIALIZADOS
16.2.1 TERAPIAS PREVENTIVAS
16.2.1.1. MEDICAÇÃO ORAL
16.2.1.1.1. TECFIDERA
16.2.1.1.2. GILENYA
16.2.1.1.3. AUBAGIO
16.2.1.1.4. MAVENCLAD
16.2.1.1.5. MAYZENT
16.2.1.1.6. VUMERIDADE
16.2.1.1.7. OUTROS
16.2.1.2. MEDICAÇÃO INJETÁVEL
16.2.1.2.1. INTERFERON BETA-1A
16.2.1.2.1.1 AVONEX
16.2.1.2.1.2 REBIF
16.2.1.2.1.3 OUTROS
16.2.1.2.2. ACETATO DE GLATIRAMER
16.2.1.2.2.1 COPAXONE
16.2.1.2.2.2 GLATOPA
16.2.1.2.2.3 OUTROS
16.2.1.2.3. INTERFERON BETA-1B
16.2.1.2.3.1 BETASERON
16.2.1.2.3.2 EXTAVIA
16.2.1.2.4. PLEGRIDY/PEGINTERFERON BETA-1A
16.2.1.2.5. MEDICAMENTO DE QUIMIOTERAPIA
16.2.1.2.6. ANTICORPOS MONOCLONAIS
16.2.1.3. MEDICAÇÃO INFUSADA
16.2.1.3.1. TYSABRI
16.2.1.3.2. OCREVUS
16.2.1.3.3. LEMTRADA
16.2.1.3.4. MITOCANTRONA
16.2.1.3.5. NOVENTRONE
16.2.1.3.6. OUTROS
16.2.1.4. TRANSPLANTE DE CÉLULAS-TRONCO HEMATOPOIÉTICAS (TCTH)
16.2.2 TERAPIAS ABORTIVAS/TRATAMENTO DE EXACERBAÇÕES AGUDAS
16.2.2.1. CORTICOSTEROIDES
16.2.2.1.1. PREDNISONA ORAL
16.2.2.1.2. METILPREDNISOLONA
16.2.2.1.3. DEXAMETASONA
16.2.2.1.4. PREDNISOLONA
16.2.2.1.5. BETAMETASONA
16.2.2.1.6. OUTROS
16.2.2.2. BENZODIAZEPÍNICOS
16.2.2.2.1. CLONAZEPAM
16.2.2.2.2. DIAZEPAM
16.2.2.2.3. OUTROS
16.2.2.3. IMUNOSSUPRESSORES
16.2.2.3.1. AZATIOPRINA
16.2.2.3.2. CICLOFOSFAMIDA
16.2.2.3.3. METOTREXATO
16.2.2.3.4. MITOCANTRONA
16.2.2.3.5. OUTROS
16.2.2.4. MODULADORES DO RECEPTOR DE ESFINGOSINA 1-FOSFATO
16.2.2.4.1. SIPONIMOD
16.2.2.4.2. FINGOLIMOD
16.2.2.4.3. OZANIMOD
16.2.2.4.4. OUTROS
16.2.2.5. AGONISTAS DA DOPAMINA
16.2.2.5.1. OSMOLEX ER
16.2.2.5.2. GOCOVRI
16.2.2.5.3. OUTROS
16.2.2.6. BLOQUEADORES NEUROMUSCULARES
16.2.2.6.1. BOTOX
16.2.2.6.2. BOTOX COSMÉTICO
16.2.2.6.3. TOXINA BOTULÍNICA
16.2.2.7. HORMÔNIO ADRENOCORTICOTRÓPICO
16.2.2.8. Imunoglobulina intravenosa
16.2.2.9. PLASMAFERÉS
16.2.2.10. OUTROS
16.2.3 TERAPIAS SINTOMÁTICAS
16.2.3.1. RELAXANTES MUSCULARES
16.2.3.1.1. LIORESAL
16.2.3.1.2. ZANAFLEX
16.2.3.1.3. OUTROS
16.2.3.2. MEDICAMENTOS PARA FADIGA
16.2.3.2.1. GOCOVRI
16.2.3.2.2. OSMOLEX
16.2.3.2.3. PROVIGIL
16.2.3.2.4. RITALIN
16.2.3.2.5. OUTROS
16.2.3.3. ESTIMULANTES
16.2.3.3.1. MODAFINIL
16.2.3.3.2. ARMODAFINIL
16.2.3.3.3. OUTROS
16.2.3.4. ANTICONVULSIVANTES
16.2.3.4.1. GABAPENTINA
16.2.3.4.2. CARBAMAZEPINA
16.2.3.4.3. PREGABALINA
16.2.3.4.4. TOPIRAMATO
16.2.3.4.5. OUTROS
16.2.3.5. ANTI-INFLAMATÓRIOS NÃO ESTEROIDAIS
16.2.3.5.1. IBUPROFENO
16.2.3.5.2. NÁPROXIM
16.2.3.5.3. DICLOFENACO
16.2.3.5.4. INDOMETACINA
16.2.3.5.5. OUTROS
16.2.3.6. ANTIDIARRÉICOS
16.2.3.7. BLOQUEADORES DOS CANAIS DE POTÁSSIO
16.2.3.8. FISIOTERAPIA
16.2.3.9. LAXANTES
16.2.3.10. OUTROS
16.3 MEDICAMENTOS EM DUTO
16.3.1 SCM-0101
16.3.2 IMCY-MS-001
16.3.3 TUBO-307
16.3.4 ATA188
16.3.5 WP1303
16.3.6 FORALUMAB
16.3.7 OUTROS
17. MERCADO EUROPEU DE TRATAMENTO DA ESCLEROSE MÚLTIPLA, POR TIPO DE MEDICAMENTO
17.1 VISÃO GERAL
17.2 MARCA
17.2.1 TECFIDERA
17.2.2 GILENYA
17.2.3 AUBAGIO
17.2.4 AVONEX
17.2.5 TYSABRI
17.2.6 REBIF
17.2.7 COPAXONE
17.2.8 8 BETASERON
17.2.9 AMPYRA/FAMPYRA
17.2.10 OUTROS
17.3 GENÉRICOS
18. MERCADO EUROPEU DE TRATAMENTO DA ESCLEROSE MÚLTIPLA, POR VIA DE ADMINISTRAÇÃO
18.1 VISÃO GERAL
18.2 ORAL
18.2.1 COMPRIMIDOS
18.2.2 CÁPSULAS
18.2.3 OUTROS
18.3 PARENTERAL
18.3.1 INTRAVENOSO
18.3.2 SUBCUTÂNEO
18.3.3 OUTROS
18.4 OUTROS
19. MERCADO EUROPEU DE TRATAMENTO DA ESCLEROSE MÚLTIPLA, POR FAIXA ETÁRIA
19.1 VISÃO GERAL
19.2 PEDIÁTRICO
19.2.1 MASCULINO
19.2.2 FEMININO
19,3 ADULTO
19.3.1 MASCULINO
19.3.2 FEMININO
19.4 GERIÁTRICO
19.4.1 MASCULINO
19.4.2 FEMININO
20 MERCADO EUROPEU DE TRATAMENTO DA ESCLEROSE MÚLTIPLA, POR GÊNERO
20.1 VISÃO GERAL
20,2 MASCULINO
20,3 FEMININO
21. MERCADO EUROPEU DE TRATAMENTO DA ESCLEROSE MÚLTIPLA, POR USUÁRIO FINAL
21.1 VISÃO GERAL
21.2 HOSPITAIS
21.2.1 PÚBLICO
21.2.1.1. NÍVEL 1
21.2.1.2. NÍVEL 2
21.2.1.3. NÍVEL 3
21.2.2 PRIVADO
21.2.2.1. NÍVEL 1
21.2.2.2. NÍVEL 2
21.2.2.3. NÍVEL 3
21.3 CUIDADOS DE SAÚDE DOMICILIARES
21.4 CENTRO DE ESPECIALIDADES
21.5 INSTITUTOS ACADÊMICOS E DE PESQUISA
21.6 OUTROS
22 MERCADO EUROPEU DE TRATAMENTO DA ESCLEROSE MÚLTIPLA, POR CANAL DE DISTRIBUIÇÃO
22.1 VISÃO GERAL
22.2 LICITAÇÕES DIRETAS
22.3 VENDAS NO VAREJO
22.3.1 ONLINE
22.3.1.1. LOJAS ELETRÔNICAS
22.3.1.2. SITE DA EMPRESA
22.3.1.3. OUTROS
22.3.2 OFFLINE
22.3.2.1. FARMÁCIA HOSPITALAR
22.3.2.2. FARMÁCIA DE VAREJO
22.3.2.3. OUTROS
22.4 OUTROS
23 MERCADO EUROPEU DE TRATAMENTO DA ESCLEROSE MÚLTIPLA, PANORAMA DAS EMPRESAS
23.1 ANÁLISE DAS AÇÕES DA EMPRESA: EUROPA
23.2 FUSÕES E AQUISIÇÕES
23.3 DESENVOLVIMENTO E APROVAÇÕES DE NOVOS PRODUTOS
23.4 EXPANSÕES
23.5 ALTERAÇÕES REGULAMENTARES
23.6 PARCERIAS E OUTROS DESENVOLVIMENTOS ESTRATÉGICOS
24 MERCADO EUROPEU DE TRATAMENTO DA ESCLEROSE MÚLTIPLA, ANÁLISE SWOT E DBMR
25 MERCADO EUROPEU DE TRATAMENTO DA ESCLEROSE MÚLTIPLA, POR PAÍS
MERCADO EUROPEU DE TRATAMENTO DA ESCLEROSE MÚLTIPLA (TODA A SEGMENTAÇÃO ACIMA ESTÁ REPRESENTADA NESTE CAPÍTULO POR PAÍS)
25.1 EUROPA
25.1.1 ALEMANHA
25.1.2 FRANÇA
25.1.3 Reino Unido
25.1.4 ITÁLIA
25.1.5 ESPANHA
25.1.6 RÚSSIA
25.1.7 TURQUIA
25.1.8 BÉLGICA
25.1.9 DINAMARCA
25.1.10 PAÍSES BAIXOS
25.1.11 SUÍÇA
25.1.12 SUÉCIA
25.1.13 POLÔNIA
25.1.14 NORUEGA
25.1.15 FINLÂNDIA
25.1.16 RESTO DA EUROPA
25.2 PRINCIPAIS CONCLUSÕES: POR PRINCIPAIS PAÍSES
26. MERCADO EUROPEU DE TRATAMENTO DA ESCLEROSE MÚLTIPLA, PERFIL DA EMPRESA
26.1 FABRICANTES COMERCIALIZADOS/APROVADOS
26.1.1 BIOGEN
26.1.1.1. VISÃO GERAL DA EMPRESA
26.1.1.2. ANÁLISE DE RECEITAS
26.1.1.3. PRESENÇA GEOGRÁFICA
26.1.1.4. PORTFÓLIO DE PRODUTOS
26.1.1.5. DESENVOLVIMENTOS RECENTES
26.1.2 NOVARTIS AG
26.1.2.1. VISÃO GERAL DA EMPRESA
26.1.2.2. ANÁLISE DE RECEITAS
26.1.2.3. PRESENÇA GEOGRÁFICA
26.1.2.4. PORTFÓLIO DE PRODUTOS
26.1.2.5. DESENVOLVIMENTOS RECENTES
26.1.3 GENZYME CORPORATION (UMA SUBSIDIÁRIA DA SANOFI)
26.1.3.1. VISÃO GERAL DA EMPRESA
26.1.3.2. ANÁLISE DE RECEITAS
26.1.3.3. PRESENÇA GEOGRÁFICA
26.1.3.4. PORTFÓLIO DE PRODUTOS
26.1.3.5. DESENVOLVIMENTOS RECENTES
26.1.4 MERCK KGAA
26.1.4.1. VISÃO GERAL DA EMPRESA
26.1.4.2. ANÁLISE DE RECEITAS
26.1.4.3. PRESENÇA GEOGRÁFICA
26.1.4.4. PORTFÓLIO DE PRODUTOS
26.1.4.5. DESENVOLVIMENTOS RECENTES
26.1.5 TEVA PHARMACEUTICALS USA, INC. (UMA SUBSIDIÁRIA DA TEVA PHARMACEUTICALS INDUSTRIES LTD.)
26.1.5.1. VISÃO GERAL DA EMPRESA
26.1.5.2. ANÁLISE DE RECEITAS
26.1.5.3. PRESENÇA GEOGRÁFICA
26.1.5.4. PORTFÓLIO DE PRODUTOS
26.1.5.5. DESENVOLVIMENTOS RECENTES
26.1.6 F. HOFFMANN-LA ROCHE LTD
26.1.6.1. VISÃO GERAL DA EMPRESA
26.1.6.2. ANÁLISE DE RECEITAS
26.1.6.3. PRESENÇA GEOGRÁFICA
26.1.6.4. PORTFÓLIO DE PRODUTOS
26.1.6.5. DESENVOLVIMENTOS RECENTES
26.1.7 ACORDA THERAPEUTICS, INC
26.1.7.1. VISÃO GERAL DA EMPRESA
26.1.7.2. ANÁLISE DE RECEITAS
26.1.7.3. PRESENÇA GEOGRÁFICA
26.1.7.4. PORTFÓLIO DE PRODUTOS
26.1.7.5. DESENVOLVIMENTOS RECENTES
26.1.8 AMNEAL PHARMACEUTICALS LLC
26.1.8.1. VISÃO GERAL DA EMPRESA
26.1.8.2. ANÁLISE DE RECEITAS
26.1.8.3. PRESENÇA GEOGRÁFICA
26.1.8.4. PORTFÓLIO DE PRODUTOS
26.1.8.5. DESENVOLVIMENTOS RECENTES
26.1.9 BAYER AG
26.1.9.1. VISÃO GERAL DA EMPRESA
26.1.9.2. ANÁLISE DE RECEITAS
26.1.9.3. PRESENÇA GEOGRÁFICA
26.1.9.4. PORTFÓLIO DE PRODUTOS
26.1.9.5. DESENVOLVIMENTOS RECENTES
26.1.10 CELGENE CORPORATION (UMA SUBSIDIÁRIA DA BRISTOL-MYERS SQUIBB COMPANY)
26.1.10.1. VISÃO GERAL DA EMPRESA
26.1.10.2. ANÁLISE DE RECEITAS
26.1.10.3. PRESENÇA GEOGRÁFICA
26.1.10.4. PORTFÓLIO DE PRODUTOS
26.1.10.5. DESENVOLVIMENTOS RECENTES
26.1.11 HIKMA PHARMACEUTICALS PLC
26.1.11.1. VISÃO GERAL DA EMPRESA
26.1.11.2. ANÁLISE DE RECEITAS
26.1.11.3. PRESENÇA GEOGRÁFICA
26.1.11.4. PORTFÓLIO DE PRODUTOS
26.1.11.5. DESENVOLVIMENTOS RECENTES
26.1.12 MALLINCKRODT FARMACÊUTICOS
26.1.12.1. VISÃO GERAL DA EMPRESA
26.1.12.2. ANÁLISE DE RECEITAS
26.1.12.3. PRESENÇA GEOGRÁFICA
26.1.12.4. PORTFÓLIO DE PRODUTOS
26.1.12.5. DESENVOLVIMENTOS RECENTES
26.1.13 VITARIS INC.
26.1.13.1. VISÃO GERAL DA EMPRESA
26.1.13.2. ANÁLISE DE RECEITAS
26.1.13.3. PRESENÇA GEOGRÁFICA
26.1.13.4. PORTFÓLIO DE PRODUTOS
26.1.13.5. DESENVOLVIMENTOS RECENTES
26.1.14 PAR PHARMACEUTICAL (UMA SUBSIDIÁRIA DA ENDO INTERNATIONAL PLC)
26.1.14.1. VISÃO GERAL DA EMPRESA
26.1.14.2. ANÁLISE DE RECEITAS
26.1.14.3. PRESENÇA GEOGRÁFICA
26.1.14.4. PORTFÓLIO DE PRODUTOS
26.1.14.5. DESENVOLVIMENTOS RECENTES
26.1.15 PFIZER INC.
26.1.15.1. VISÃO GERAL DA EMPRESA
26.1.15.2. ANÁLISE DE RECEITAS
26.1.15.3. PRESENÇA GEOGRÁFICA
26.1.15.4. PORTFÓLIO DE PRODUTOS
26.1.15.5. DESENVOLVIMENTOS RECENTES
26.1.16 ZYDUS PHARMACEUTICALS, INC. (UMA SUBSIDIÁRIA DA ZYDUS CADILA)
26.1.16.1. VISÃO GERAL DA EMPRESA
26.1.16.2. ANÁLISE DE RECEITAS
26.1.16.3. PRESENÇA GEOGRÁFICA
26.1.16.4. PORTFÓLIO DE PRODUTOS
26.1.16.5. DESENVOLVIMENTOS RECENTES
26.1.17 JOHNSON & JOHNSON CONSUMER INC.
26.1.17.1. VISÃO GERAL DA EMPRESA
26.1.17.2. PORTFÓLIO DE PRODUTOS
26.1.17.3. ANÁLISE DE RECEITAS
26.1.17.4. PRESENÇA GEOGRÁFICA
26.1.17.5. PORTFÓLIO DE PRODUTOS
26.1.18 PERRIGO COMPANY PLC,
26.1.18.1. VISÃO GERAL DA EMPRESA
26.1.18.2. PORTFÓLIO DE PRODUTOS
26.1.18.3. ANÁLISE DE RECEITAS
26.1.18.4. PRESENÇA GEOGRÁFICA
26.1.18.5. PORTFÓLIO DE PRODUTOS
26.1.19 GLENMARK PHARMACEUTICAL INC., EUA
26.1.19.1. VISÃO GERAL DA EMPRESA
26.1.19.2. ANÁLISE DE RECEITAS
26.1.19.3. PRESENÇA GEOGRÁFICA
26.1.19.4. PORTFÓLIO DE PRODUTOS
26.1.19.5. DESENVOLVIMENTOS RECENTES
26.1.20 GLAXOSMITHKLINE PLC.
26.1.20.1. VISÃO GERAL DA EMPRESA
26.1.20.2. PORTFÓLIO DE PRODUTOS
26.1.20.3. ANÁLISE DE RECEITAS
26.1.20.4. PRESENÇA GEOGRÁFICA
26.1.20.5. PORTFÓLIO DE PRODUTOS
26.2 EMPRESAS DE DUTOS
26.2.1 IMCYSE
26.2.1.1. VISÃO GERAL DA EMPRESA
26.2.1.2. PORTFÓLIO DE PRODUTOS
26.2.1.3. ANÁLISE DE RECEITAS
26.2.1.4. PRESENÇA GEOGRÁFICA
26.2.1.5. PORTFÓLIO DE PRODUTOS
26.2.2 WORG PHARMACEUTICALS (ZHEJIANG) CO., LTD.
26.2.2.1. VISÃO GERAL DA EMPRESA
26.2.2.2. PORTFÓLIO DE PRODUTOS
26.2.2.3. ANÁLISE DE RECEITAS
26.2.2.4. PRESENÇA GEOGRÁFICA
26.2.2.5. PORTFÓLIO DE PRODUTOS
26.2.3 CIÊNCIAS DA VIDA TIZIANA
26.2.3.1. VISÃO GERAL DA EMPRESA
26.2.3.2. PORTFÓLIO DE PRODUTOS
26.2.3.3. ANÁLISE DE RECEITAS
26.2.3.4. PRESENÇA GEOGRÁFICA
26.2.3.5. PORTFÓLIO DE PRODUTOS
27 RELATÓRIOS RELACIONADOS
28 CONCLUSÃO
29 QUESTIONÁRIO
30 SOBRE A DATA BRIDGE MARKET RESEARCH
Metodologia de Investigação
A recolha de dados e a análise do ano base são feitas através de módulos de recolha de dados com amostras grandes. A etapa inclui a obtenção de informações de mercado ou dados relacionados através de diversas fontes e estratégias. Inclui examinar e planear antecipadamente todos os dados adquiridos no passado. Da mesma forma, envolve o exame de inconsistências de informação observadas em diferentes fontes de informação. Os dados de mercado são analisados e estimados utilizando modelos estatísticos e coerentes de mercado. Além disso, a análise da quota de mercado e a análise das principais tendências são os principais fatores de sucesso no relatório de mercado. Para saber mais, solicite uma chamada de analista ou abra a sua consulta.
A principal metodologia de investigação utilizada pela equipa de investigação do DBMR é a triangulação de dados que envolve a mineração de dados, a análise do impacto das variáveis de dados no mercado e a validação primária (especialista do setor). Os modelos de dados incluem grelha de posicionamento de fornecedores, análise da linha de tempo do mercado, visão geral e guia de mercado, grelha de posicionamento da empresa, análise de patentes, análise de preços, análise da quota de mercado da empresa, normas de medição, análise global versus regional e de participação dos fornecedores. Para saber mais sobre a metodologia de investigação, faça uma consulta para falar com os nossos especialistas do setor.
Personalização disponível
A Data Bridge Market Research é líder em investigação formativa avançada. Orgulhamo-nos de servir os nossos clientes novos e existentes com dados e análises que correspondem e atendem aos seus objetivos. O relatório pode ser personalizado para incluir análise de tendências de preços de marcas-alvo, compreensão do mercado para países adicionais (solicite a lista de países), dados de resultados de ensaios clínicos, revisão de literatura, mercado remodelado e análise de base de produtos . A análise de mercado dos concorrentes-alvo pode ser analisada desde análises baseadas em tecnologia até estratégias de carteira de mercado. Podemos adicionar quantos concorrentes necessitar de dados no formato e estilo de dados que procura. A nossa equipa de analistas também pode fornecer dados em tabelas dinâmicas de ficheiros Excel em bruto (livro de factos) ou pode ajudá-lo a criar apresentações a partir dos conjuntos de dados disponíveis no relatório.