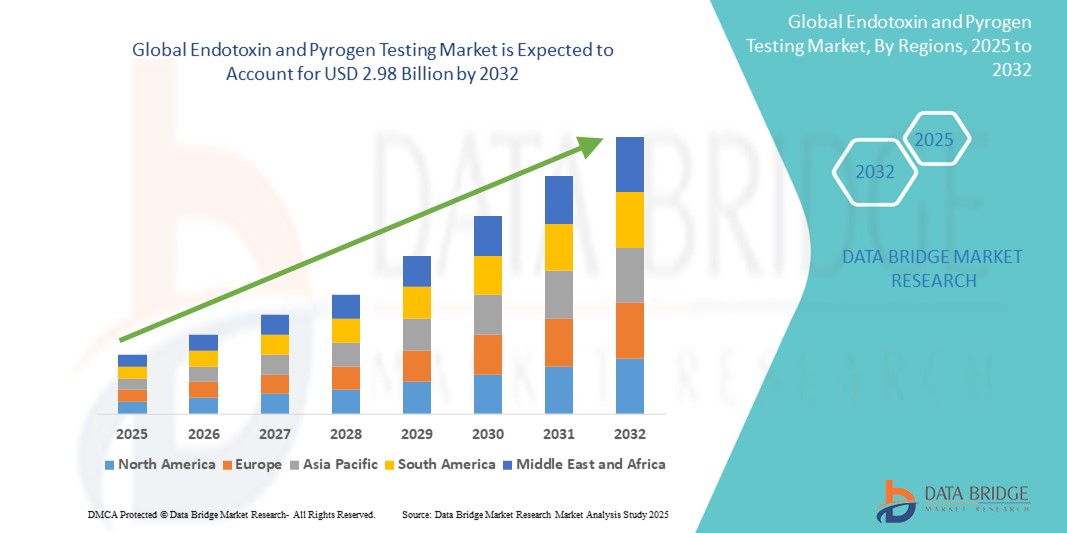
Global Endotoxin And Pyrogen Testing Market
Tamanho do mercado em biliões de dólares
CAGR :
% 
 USD
1.27 Billion
USD
2.98 Billion
2024
2032
USD
1.27 Billion
USD
2.98 Billion
2024
2032
| 2025 –2032 | |
| USD 1.27 Billion | |
| USD 2.98 Billion | |
|
|
|
|
Segmentação do mercado global de testes de endotoxina e pirogênio, por produto e serviços (kits de detecção e reagentes, instrumentos e sistemas, serviços de teste de endotoxina e pirogênio e consumíveis e acessórios), tipo de teste (teste de lisado de amebócitos Limulus (LAL), testes TAL, teste de ativação de monócitos (MAT), ensaio de C recombinante (RFC), in vitro e teste de pirogênio em coelho), tipo (teste de endotoxina e pirogênio pré-formado, teste de proendotoxina e pirogênio e teste combinado de endotoxina e pirogênio), categoria de produto (ingrediente com rótulo limpo e convencional), forma (pó e líquido), aplicação (fabricação farmacêutica, fabricação de dispositivos médicos, produção de matérias-primas e fabricação de embalagens), método (teste de endotoxina e pirogênio de coágulo em gel, teste de endotoxina e pirogênio cromogênico e teste de endotoxina e pirogênio turbidimétrico), modo de compra (Grupo grande, grupo médio e pequeno e individual), produto final (vacinas e/ou CGT, produtos biológicos, injetáveis e outros), usuário final (empresas farmacêuticas, empresas de biotecnologia, empresas biomédicas, empresas de dispositivos médicos, organização de pesquisa contratada (CRO), organização de fabricação contratada (CMO) e outras) - Tendências e previsões do setor até 2032
Tamanho do mercado de testes de endotoxinas e pirogênios
- O tamanho do mercado global de testes de endotoxinas e pirogênios foi avaliado em US$ 1,27 bilhão em 2024 e deve atingir US$ 2,98 bilhões até 2032 , com um CAGR de 11,3% durante o período previsto.
- O crescimento do mercado é amplamente impulsionado pela crescente adoção e avanço tecnológico nos processos de controle de qualidade farmacêutica e biossegurança, levando a uma maior digitalização e automação na fabricação de produtos farmacêuticos, biotecnológicos e dispositivos médicos.
- Além disso, a crescente demanda por métodos precisos, rápidos e em conformidade com as normas de detecção de endotoxinas e pirogênios está consolidando os Testes de Endotoxinas e Pirogênios como um componente essencial dos fluxos de trabalho modernos de produção de dispositivos médicos e farmacêuticos. Esses fatores convergentes estão acelerando a adoção de soluções de Testes de Endotoxinas e Pirogênios, impulsionando significativamente o crescimento do setor.
Análise de Mercado de Testes de Endotoxinas e Pirogênios
- Os testes de endotoxinas e pirogênios, que oferecem garantia crítica de segurança biológica por meio da detecção de endotoxinas bacterianas e pirogênios prejudiciais em produtos farmacêuticos e médicos, são cada vez mais vitais na fabricação moderna de dispositivos, biofarmacêuticos e de assistência médica devido ao seu papel em garantir a conformidade regulatória e a segurança do paciente.
- A crescente demanda por testes de endotoxinas e pirogênios é alimentada principalmente pela expansão da indústria biofarmacêutica, pela crescente incidência de doenças crônicas que exigem terapias injetáveis e pelo maior escrutínio regulatório em torno do controle de contaminação em medicamentos injetáveis, vacinas e dispositivos implantáveis.
- A América do Norte dominou o mercado de testes de endotoxinas e pirogênios, com a maior participação na receita, de 40,01% em 2024, caracterizada pela adoção regulatória antecipada, forte investimento em pesquisa biotecnológica e pela presença de grandes players que oferecem soluções avançadas de testes. Os EUA conquistaram 81% do mercado regional, impulsionados por um aumento na produção de produtos biológicos e pela crescente adoção de tecnologias de testes automatizados e recombinantes em laboratórios certificados pelas Boas Práticas de Fabricação (BPF).
- A Ásia-Pacífico deverá ser a região de crescimento mais rápido no mercado de testes de endotoxinas e pirogênios durante o período previsto, com um CAGR de 24,02% de 2025 a 2032, impulsionado pela rápida industrialização, expansão da capacidade de fabricação farmacêutica e crescente apoio governamental à infraestrutura de controle de qualidade em países como China, Índia e Japão.
- O segmento de kits de detecção e reagentes dominou o mercado de testes de endotoxinas e pirogênios com uma participação de 46,8% em 2024, devido à sua ampla aplicação, facilidade de uso e papel crucial nos protocolos de garantia de qualidade de rotina em empresas farmacêuticas e de biotecnologia.
Escopo do Relatório e Segmentação do Mercado de Testes de Endotoxina e Pirogênio
|
Atributos |
Principais insights de mercado sobre testes de endotoxinas e pirogênios |
|
Segmentos abrangidos |
|
|
Países abrangidos |
América do Norte
Europa
Ásia-Pacífico
Oriente Médio e África
Ámérica do Sul
|
|
Principais participantes do mercado |
|
|
Oportunidades de mercado |
|
|
Conjuntos de informações de dados de valor agregado |
Além dos insights sobre cenários de mercado, como valor de mercado, taxa de crescimento, segmentação, cobertura geográfica e principais participantes, os relatórios de mercado selecionados pela Data Bridge Market Research também incluem análises aprofundadas de especialistas, análises de preços, análises de participação de marca, pesquisas com consumidores, análises demográficas, análises da cadeia de suprimentos, análises da cadeia de valor, visão geral de matérias-primas/consumíveis, critérios de seleção de fornecedores, análise PESTLE, análise de Porter e estrutura regulatória. |
Tendências de mercado de testes de endotoxinas e pirogênios
“ Crescente demanda por precisão, conformidade e soluções de testes rápidos ”
- Uma tendência significativa e crescente no mercado de testes de endotoxinas e pirogênios da Ásia-Pacífico é a ênfase crescente em precisão, rapidez de processamento e conformidade regulatória na fabricação de produtos farmacêuticos e dispositivos médicos. Essa demanda está impulsionando o desenvolvimento e a adoção de soluções de teste altamente sensíveis e padronizadas.
- Por exemplo, os principais intervenientes estão a introduzir testes de endotoxina baseados no fator C recombinante (rFC) que eliminam a utilização de reagentes derivados de animais, garantindo ao mesmo tempo resultados precisos e consistentes, abordando preocupações éticas e regulamentares.
- Os avanços tecnológicos em sistemas automatizados também estão permitindo que os laboratórios otimizem os processos de detecção de endotoxinas, reduzam a intervenção manual e melhorem a reprodutibilidade. Leitores de placas automatizados e kits de detecção baseados em cartuchos estão ganhando popularidade por sua operação fácil de usar e margens de erro mínimas.
- A integração de software avançado com equipamentos de teste permite melhor rastreabilidade, monitoramento em tempo real e relatórios de dados mais fáceis, fatores cruciais para a conformidade com as BPF. Isso é especialmente relevante para empresas farmacêuticas que estão expandindo a produção de injetáveis estéreis, vacinas e produtos biológicos.
- Além disso, a crescente colaboração entre governos regionais e fabricantes de produtos farmacêuticos para melhorar a infraestrutura de saúde — especialmente após a COVID-19 — acelerou a necessidade de protocolos confiáveis de testes de endotoxinas e pirogênios em toda a cadeia de suprimentos.
- Como resultado, os fabricantes estão se concentrando na produção de sistemas de teste compactos, automatizados e altamente sensíveis, adaptados para laboratórios de alto volume, o que está reformulando as expectativas de eficiência, conformidade e escalabilidade em ambientes de controle de qualidade.
Dinâmica do mercado de testes de endotoxinas e pirogênios
Motorista
“Necessidade crescente devido aos crescentes riscos de contaminação e rigor regulatório”
- A crescente prevalência de riscos de contaminação na produção farmacêutica, biotecnológica e de dispositivos médicos, juntamente com estruturas regulatórias mais rigorosas, é um fator significativo para o aumento da demanda por soluções de testes de endotoxinas e pirogênios.
- Por exemplo, em abril de 2024, a Onity, Inc. (Honeywell International, Inc.) anunciou avanços em tecnologias de segurança biofarmacêutica, com o objetivo de integrar sensores de detecção em tempo real em ambientes de fabricação assépticos. Espera-se que tais desenvolvimentos por parte de players importantes impulsionem o crescimento do mercado de testes de endotoxinas e pirogênios na região da Ásia-Pacífico.
- À medida que as empresas priorizam a segurança do paciente e a conformidade regulatória, testes como o Lisado de Amebócitos de Limulus (LAL) e o Teste de Ativação de Monócitos (MAT) estão sendo cada vez mais adotados por sua capacidade de detectar níveis mínimos de endotoxina em medicamentos injetáveis, vacinas e dispositivos implantáveis.
- Além disso, o crescimento dos produtos biológicos e dos medicamentos personalizados está alimentando a necessidade de métodos de teste confiáveis e de alto rendimento que possam se integrar perfeitamente aos processos de garantia de qualidade. Plataformas de teste automatizadas e kits rápidos estão se tornando componentes essenciais das linhas de produção modernas.
- A conveniência da automação, a redução de erros manuais e a capacidade de lidar com testes de alto volume com precisão são fatores importantes que impulsionam a adoção dessas soluções por empresas farmacêuticas, organizações de fabricação sob contrato (CMOs) e laboratórios de pesquisa. A tendência de descentralização da produção e expansão de polos regionais de biotecnologia contribui ainda mais para o crescimento do mercado na região da Ásia-Pacífico.
Restrição/Desafio
“ Preocupações com os altos custos e a harmonização regulatória ”
- O alto custo dos sistemas de detecção de endotoxinas recombinantes ou alternativas, juntamente com a necessidade de instrumentos especializados, pode ser uma barreira para pequenas e médias empresas em economias emergentes na região da Ásia-Pacífico.
- Por exemplo, embora os testes LAL tradicionais de gel-clot sejam relativamente económicos, os métodos cromogénicos cinéticos e turbidimétricos mais avançados, bem como os sistemas baseados em MAT, apresentam custos iniciais e requisitos de formação significativamente mais elevados.
- Além disso, a adoção regulatória inconsistente entre os países da Ásia-Pacífico — como os diferentes níveis de aceitação dos métodos rFC ou MAT — cria incerteza entre os fabricantes que buscam otimizar seus processos de validação regionalmente.
- Enfrentar esses desafios por meio da otimização de custos, harmonização regulatória regional e iniciativas de treinamento expandidas é crucial para impulsionar a adoção. Os principais players estão cada vez mais oferecendo soluções de hardware e software combinadas e suporte técnico para mitigar essas barreiras de entrada e impulsionar o crescimento sustentado do mercado.
Escopo de mercado de testes de endotoxinas e pirogênios
O mercado é segmentado com base em produto e serviços, tipo de teste, tipo, categoria de produto, forma, aplicação, método, modo de compra, produto final e usuário final.
• Por Produto e Serviços
Com base em produtos e serviços, o mercado de testes de endotoxinas e pirogênios é segmentado em kits e reagentes de detecção, instrumentos e sistemas, serviços de testes de endotoxinas e pirogênios e consumíveis e acessórios. O segmento de kits e reagentes de detecção dominou o mercado, com a maior participação na receita, de 46,8% em 2024, impulsionado pela alta demanda nas indústrias farmacêutica e de biotecnologia devido à facilidade de uso e ao desempenho confiável na detecção de endotoxinas.
Espera-se que o segmento de serviços de testes de endotoxinas e pirogênios cresça na maior CAGR de 11,2% entre 2025 e 2032, devido ao aumento da terceirização por empresas farmacêuticas e de biotecnologia.
• Por tipo de teste
Com base no tipo de teste, o mercado de testes de endotoxinas e pirogênios é segmentado em Teste de Lisado de Amebócitos Limulus (LAL), Testes TAL, Teste de Ativação de Monócitos (MAT), Ensaio de Fator C Recombinante (rFC), Teste In Vitro e Teste de Pirogênio em Coelhos. O segmento de Teste LAL detinha a maior participação de mercado, 41,2%, em 2024, devido à sua aceitação regulatória e alta sensibilidade.
O segmento de Ensaio de Fator C Recombinante (rFC) deverá expandir a um CAGR de 12,7% de 2025 a 2032, impulsionado pela demanda por testes sem animais e por considerações de sustentabilidade.
• Por tipo
Com base no tipo, o mercado de testes de endotoxinas e pirogênios é segmentado em testes pré-formados de endotoxinas e pirogênios, testes de proendotoxinas e pirogênios e testes combinados de endotoxinas e pirogênios. O segmento de testes combinados de endotoxinas e pirogênios representou a maior fatia de mercado, 38,5%, em 2024, devido à sua capacidade de detectar múltiplos contaminantes com eficiência.
Espera-se que o segmento de testes de proendotoxinas e pirogênios cresça a um CAGR de 10,6% de 2025 a 2032, impulsionado pela demanda por testes preditivos em estágio inicial.
• Por categoria de produto
Com base na categoria de produto, o mercado de testes de endotoxinas e pirogênios é segmentado em ingredientes com rótulo limpo e convencionais. O segmento convencional liderou o mercado com 58,1% de participação em 2024, pois inclui reagentes e sistemas amplamente utilizados.
O segmento de ingredientes com rótulo limpo deverá crescer a uma CAGR de 9,3% entre 2025 e 2032, devido a mudanças regulatórias impulsionadas pela transparência e às preferências dos consumidores.
• Por Formulário
Com base na forma, o mercado de testes de endotoxinas e pirogênios é segmentado em pó e líquido. O segmento líquido detinha a participação dominante de 63,9% em 2024, devido à facilidade de automação e ao uso direto.
Espera-se que o segmento de pó cresça a um CAGR de 8,8% de 2025 a 2032, beneficiando-se de maior prazo de validade e transportabilidade.
• Por aplicação
Com base na aplicação, o mercado de testes de endotoxinas e pirogênios é segmentado em fabricação farmacêutica, fabricação de dispositivos médicos, produção de matérias-primas e fabricação de embalagens. O segmento de fabricação farmacêutica representou a maior fatia, 49,5%, em 2024, devido aos altos requisitos de conformidade com a esterilidade.
O segmento de fabricação de dispositivos médicos deverá crescer a um CAGR de 10,1% de 2025 a 2032, devido ao aumento dos testes regulatórios de implantes e equipamentos cirúrgicos.
• Por Método
Com base no método, o mercado de testes de endotoxinas e pirogênios é segmentado em teste de endotoxinas e pirogênios de gel coagulado, teste de endotoxinas e pirogênios cromogênicos e teste de endotoxinas e pirogênios turbidimétricos. O método de gel coagulado dominou o mercado com 42,7% de participação em 2024, devido à sua relação custo-benefício e aprovação regulatória.
Espera-se que o método cromogênico cresça na taxa composta de crescimento anual (CAGR) mais rápida, de 11,4%, entre 2025 e 2032, apoiada por sua precisão quantitativa e compatibilidade com automação.
• Por Modo de Compra
Com base no modo de compra, o mercado de testes de endotoxinas e pirogênios é segmentado em grupos grandes, grupos médios e pequenos, e individuais. O segmento de grupos grandes detinha a maior participação de mercado, 55,2%, em 2024, devido à aquisição em larga escala por empresas farmacêuticas e CDMOs.
O segmento de grupos médios e pequenos deverá crescer a uma CAGR de 9,9% entre 2025 e 2032, com demanda crescente de PMEs e instituições acadêmicas.
• Por produto final
Com base no produto final, o mercado de testes de endotoxinas e pirogênios é segmentado em vacinas e/ou CGT, produtos biológicos, injetáveis e outros. O segmento de produtos biológicos representou a maior fatia, 38,9%, em 2024, impulsionado pela crescente demanda por anticorpos monoclonais e biossimilares.
Espera-se que o segmento de vacinas e/ou CGT cresça a um CAGR de 12,1% de 2025 a 2032, devido ao aumento de aprovações em terapias avançadas e desenvolvimento de vacinas.
• Por Usuário Final
Com base no usuário final, o mercado de testes de endotoxinas e pirogênios é segmentado em empresas farmacêuticas, empresas de biotecnologia, empresas biomédicas, empresas de dispositivos médicos, CROs, CMOs e outras. O segmento de empresas farmacêuticas dominou o mercado com uma participação de 40,4% em 2024, devido ao investimento consistente em controle de qualidade e testes de conformidade.
Espera-se que o segmento de organizações de pesquisa contratadas (CROs) registre o CAGR mais rápido de 11,6% entre 2025 e 2032, impulsionado pelo aumento da terceirização e pelo crescimento dos pipelines de descoberta de medicamentos.
Análise regional do mercado de testes de endotoxinas e pirogênios
- A América do Norte dominou o mercado global de testes de endotoxinas e pirogênios com a maior participação na receita de 40,01% em 2024, impulsionada pelo aumento do rigor regulatório, fortes pipelines de produção biofarmacêutica e uso generalizado de medicamentos injetáveis e biológicos
- A região se beneficia de infraestrutura avançada de saúde, alto volume de ensaios clínicos e uma crescente mudança para métodos de testes recombinantes e sem uso de animais. Empresas líderes nos EUA e Canadá estão investindo em sistemas automatizados de detecção de endotoxinas e soluções de testes sustentáveis.
- A crescente preferência por protocolos de controle de qualidade mais rápidos e compatíveis fortalece ainda mais a presença de mercado nesta região
Visão do mercado de testes de endotoxinas e pirogênios nos EUA
O mercado de testes de endotoxinas e pirogênios dos EUA representou 83% da participação de mercado norte-americana em 2024. O país lidera devido à sua fabricação em larga escala de produtos biológicos e vacinas, ao forte investimento em P&D farmacêutico e à rápida adoção de ensaios de fator C recombinante (rFC) e Testes de Ativação de Monócitos (MAT). O alinhamento regulatório com a iniciativa da FDA por alternativas aos testes em animais está acelerando ainda mais a expansão do mercado.
Visão geral do mercado de testes de endotoxinas e pirogênios na Europa
O mercado europeu de testes de endotoxinas e pirogênios deverá crescer a um CAGR notável durante o período previsto, devido à crescente conscientização sobre a segurança dos produtos, aos rigorosos requisitos farmacopeicos da UE e ao aumento das aprovações de produtos biológicos. Países como Alemanha, Reino Unido e França estão enfatizando alternativas sustentáveis de testes. O forte crescimento da fabricação sob contrato e da terceirização de P&D também está contribuindo para a demanda do mercado em desenvolvimento de medicamentos e testes de dispositivos médicos.
Visão geral do mercado de testes de endotoxinas e pirogênios no Reino Unido
Espera-se que o mercado de testes de endotoxinas e pirogênios do Reino Unido cresça de forma constante ao longo do período previsto, apoiado pelas regulamentações da MHRA alinhadas aos padrões globais de Boas Práticas de Fabricação (BPF), por um setor biofarmacêutico maduro e por crescentes investimentos em infraestrutura de pesquisa clínica. A demanda por métodos rápidos de teste de endotoxinas para garantia de esterilidade e produção de medicamentos injetáveis é um importante impulsionador do crescimento.
Visão do mercado de testes de endotoxinas e pirogênios na Alemanha
Espera-se que o mercado alemão de testes de endotoxinas e pirogênios apresente um crescimento significativo devido à sua robusta base de fabricação farmacêutica, à automação em laboratórios de CQ e ao suporte a tecnologias de testes recombinantes. A adesão regulatória e o forte foco na segurança e eficiência dos produtos estão moldando as tendências de compras.
Visão do mercado de testes de endotoxinas e pirogênios na Ásia-Pacífico
O mercado de testes de endotoxinas e pirogênios na Ásia-Pacífico deverá crescer a uma taxa composta de crescimento anual (CAGR) de 24,02% (2025-2032), impulsionado pelo crescimento das exportações farmacêuticas, pela crescente demanda por produtos biológicos e pelo apoio governamental à fabricação localizada de medicamentos em países como China, Japão e Índia. A rápida expansão da atividade de ensaios clínicos e a maior conscientização sobre os padrões de controle de contaminação estão promovendo a adoção de ensaios de MAT e rFC na região.
Visão do mercado de testes de endotoxinas e pirogênios no Japão
O mercado japonês de testes de endotoxinas e pirogênios está testemunhando um aumento na demanda por esses testes devido à alta inovação em terapias celulares e genéticas e ao seu cenário farmacêutico bem regulamentado. Órgãos reguladores estão incentivando alternativas de testes que não envolvam animais, enquanto o envelhecimento da população do país aumenta a necessidade de medicamentos injetáveis.
Visão do mercado de testes de endotoxinas e pirogênios na China
O mercado chinês de testes de endotoxinas e pirogênios conquistou a maior fatia de mercado na região da Ásia-Pacífico em 2024, impulsionado por sua vasta capacidade de fabricação farmacêutica, forte apoio governamental à produção local de produtos biológicos e crescente adoção de soluções sustentáveis de controle de qualidade. A ascensão de empresas nacionais que oferecem kits e serviços de teste com boa relação custo-benefício está impulsionando ainda mais o crescimento do mercado.
Participação no mercado de testes de endotoxinas e pirogênios
O setor de testes de endotoxinas e pirogênios é liderado principalmente por empresas bem estabelecidas, incluindo:
- Pall Corporation (EUA)
- Thermo Fisher Scientific Inc. (EUA)
- Laboratórios Charles River (EUA)
- Eurofins Scientific (Luxemburgo)
- SGS Société Générale de Surveillance SA (Suíça)
- Lonza (Suíça)
- Merck KGaA (Alemanha)
- STERIS (Irlanda)
- Sartorius AG (Alemanha)
- BIOMÉRIEUX (França)
- Ellab A/S (Dinamarca)
- ASSOCIATES OF CAPE COD, INC. (EUA)
- WuXi AppTec (China)
- Microcoat Biotechnologie GmbH (Alemanha)
Últimos desenvolvimentos no mercado global de testes de endotoxinas e pirogênios
- Em março de 2024, o Lonza Group anunciou a expansão de suas capacidades de teste de endotoxinas e pirogênios com o lançamento de um novo kit de ensaio baseado em fator C recombinante (rFC). Este desenvolvimento está alinhado com a crescente aceitação regulatória de métodos de teste sem animais e apoia as metas de sustentabilidade, reduzindo a dependência de sangue de caranguejo-ferradura.
- Em fevereiro de 2024, a Charles River Laboratories introduziu plataformas aprimoradas de Teste de Ativação de Monócitos (MAT) por meio da integração de automação, com o objetivo de melhorar o rendimento e a reprodutibilidade da detecção de pirogênios em produtos biológicos e terapias celulares. A inovação visa otimizar os fluxos de trabalho para empresas farmacêuticas em conformidade com as rigorosas regulamentações globais.
- Em janeiro de 2024, a FUJIFILM Wako Chemicals USA Corporation atualizou seu portfólio de reagentes de Lisado de Amebócitos Limulus (LAL) com maior sensibilidade e menor variabilidade, aumentando a confiabilidade dos testes de endotoxina em medicamentos parenterais e dispositivos médicos. A empresa também anunciou novas parcerias de distribuição para expandir seu alcance no Sudeste Asiático.
- Em dezembro de 2023, a Associates of Cape Cod, Inc. (ACC) recebeu aprovações adicionais das autoridades regulatórias asiáticas para seu ensaio PyroSmart NextGen rFC. Espera-se que a aprovação acelere a adoção de métodos sustentáveis e livres de animais para testes de endotoxinas em fabricantes de biofármacos no Japão, China e Coreia do Sul.
- Em outubro de 2023, a Merck KGaA (MilliporeSigma) lançou uma nova solução de teste turbidimétrico de endotoxina de alto rendimento, projetada para a produção de vacinas e produtos biológicos. O lançamento faz parte da iniciativa da empresa para oferecer suporte a testes de liberação de lote mais rápidos, ao mesmo tempo em que atende aos padrões de BPF em evolução.
- Em setembro de 2023, a Thermo Fisher Scientific revelou o desenvolvimento de uma plataforma integrada de automação de testes de LAL em colaboração com CDMOs globais. Esta solução combina testes de LAL com captura de dados em tempo real, visando reduzir erros humanos, melhorar a eficiência e garantir a prontidão para auditoria em submissões regulatórias.
SKU-
Obtenha acesso online ao relatório sobre a primeira nuvem de inteligência de mercado do mundo
- Painel interativo de análise de dados
- Painel de análise da empresa para oportunidades de elevado potencial de crescimento
- Acesso de analista de pesquisa para personalização e customização. consultas
- Análise da concorrência com painel interativo
- Últimas notícias, atualizações e atualizações Análise de tendências
- Aproveite o poder da análise de benchmark para um rastreio abrangente da concorrência
Índice
1 INTRODUÇÃO
1.1 OBJETIVOS DO ESTUDO
1.2 DEFINIÇÃO DE MERCADO
1.3 VISÃO GERAL DO MERCADO GLOBAL DE TESTES DE ENDOTOXINAS E PIRÓGENOS
1.4 MOEDA E PREÇOS
1.5 LIMITAÇÃO
1.6 MERCADOS COBERTOS
2 SEGMENTAÇÃO DE MERCADO
2.1 PRINCIPAIS CONCLUSÕES
2.2 CHEGANDO AO TAMANHO DO MERCADO GLOBAL DE TESTES DE ENDOTOXINAS E PIRÓGENOS
2.2.1 GRADE DE POSICIONAMENTO DE FORNECEDORES
2.2.2 CURVA DA LINHA DE VIDA DA TECNOLOGIA
2.2.3 MODELO DE VALIDAÇÃO DE DADOS DE TRIPÉ
2.2.4 GUIA DE MERCADO
2.2.5 MODELAGEM MULTIVARIADA
2.2.6 ANÁLISE DE CIMA PARA BAIXO
2.2.7 MATRIZ DE DESAFIOS
2.2.8 GRADE DE COBERTURA DA APLICAÇÃO
2.2.9 PADRÕES DE MEDIÇÃO
2.2.10 ANÁLISE DA PARTICIPAÇÃO DO FORNECEDOR
2.2.11 VOLUME DE VENDAS
2.2.12 PONTOS DE DADOS DAS ENTREVISTAS PRIMÁRIAS PRINCIPAIS
2.2.13 PONTOS DE DADOS DE BASES DE DADOS SECUNDÁRIAS PRINCIPAIS
2.3 MERCADO GLOBAL DE TESTES DE ENDOTOXINAS E PIRÓGENOS: RESUMO DA PESQUISA
2.4 PREMISSAS
3 VISÃO GERAL DO MERCADO
3.1 MOTORISTAS
3.2 RESTRIÇÕES
3.3 OPORTUNIDADES
3.4 DESAFIOS
4 RESUMO EXECUTIVO
5 INSIGHTS PREMIUM
5.1 ANÁLISE PESTEL
5.2 MODELO DAS CINCO FORÇAS DE PORTER
6 VISÕES DO SETOR
6.1 FATORES MICRO E MACRO ECONÔMICOS
6.2 MAPEAMENTO DE PENETRAÇÃO E PERSPECTIVAS DE CRESCIMENTO
6.3 PRINCIPAIS ESTRATÉGIAS DE PREÇOS
6.4 ENTREVISTAS COM ESPECIALISTAS
6.5 ANÁLISE E RECOMENDAÇÃO
7 ANÁLISE DE CUSTOS DETALHADA
8 ROTEIRO DE TECNOLOGIA
9 RASTREADOR DE INOVAÇÃO E ANÁLISE ESTRATÉGICA
9.1 ANÁLISE DE GRANDES NEGÓCIOS E ALIANÇAS ESTRATÉGICAS
9.1.1 JOINT VENTURES
9.1.2 FUSÕES E AQUISIÇÕES
9.1.3 LICENCIAMENTO E PARCERIA
9.1.4 COLABORAÇÕES DE TECNOLOGIA
9.1.5 DESINVESTIMENTOS ESTRATÉGICOS
9.2 NÚMERO DE PRODUTOS EM DESENVOLVIMENTO
9.3 ESTÁGIO DE DESENVOLVIMENTO
9.4 CRONOGRAMAS E MARCOS
9.5 ESTRATÉGIAS E METODOLOGIAS DE INOVAÇÃO
9.6 AVALIAÇÃO E MITIGAÇÃO DE RISCOS
9.7 PERSPECTIVAS FUTURAS
10 CONFORMIDADE REGULAMENTAR
10.1 AUTORIDADES REGULADORAS
10.2 CLASSIFICAÇÕES REGULAMENTARES
10.2.1 CLASSE I
10.2.2 CLASSE II
10.2.3 CLASSE III
10.3 SUBMISSÕES REGULAMENTARES
10.4 HARMONIZAÇÃO INTERNACIONAL
10.5 SISTEMAS DE GESTÃO DA CONFORMIDADE E DA QUALIDADE
10.6 DESAFIOS E ESTRATÉGIAS REGULAMENTARES
11 ESTRUTURA DE REEMBOLSO
12 ANÁLISE DA CADEIA DE VALOR
13 ECONOMIA DA SAÚDE
13.1 DESPESAS COM SAÚDE
13.2 DESPESAS DE CAPITAL
13.3 TENDÊNCIAS DE CAPEX
13.4 ALOCAÇÃO DE CAPEX
13.5 FONTES DE FINANCIAMENTO
13.6 REFERÊNCIAS DO SETOR
13,7% DO PIB NO PIB TOTAL
13.8 ESTRUTURA DO SISTEMA DE SAÚDE
13.9 POLÍTICAS GOVERNAMENTAIS
13.1 DESENVOLVIMENTO ECONÔMICO
14 MERCADO GLOBAL DE TESTES DE ENDOTOXINAS E PIRÓGENOS, POR PRODUTO E SERVIÇOS
14.1 VISÃO GERAL
14.2 KITS DE DETECÇÃO E REAGENTES
14.2.1 REAGENTES DE TESTE LAL
14.2.2 DETECÇÃO E REMOÇÃO DE MICOPLASMA
14.2.3 KIT DE DETECÇÃO DE MICOPLASMA POR PCR
14.2.4 COQUETEL DE ELIMINAÇÃO DE MICOPLASMA
14.2.5 OUTROS
14.3 INSTRUMENTOS E SISTEMAS
LEITOR DE TUBOS SÉRIE 14.3.1
14.3.2 LEITOR DE MICROPLACAS
14.3.3 BAIXA RECUPERAÇÃO DE ENDOTOXINAS (BRE)
14.3.4 REMOÇÃO DE ENDOTOXINAS
14.3.5 BAIXA RECUPERAÇÃO DE ENDOTOXINAS (BRE)
14.3.6 OUTROS
14.4 CONSUMÍVEIS E ACESSÓRIOS
14.5 SOFTWARE E SERVIÇOS
14.6 OUTROS
15 MERCADO GLOBAL DE TESTES DE ENDOTOXINAS E PIRÓGENOS, POR TIPO DE TESTE
15.1 VISÃO GERAL
15.2 TESTE DE LISADO DE AMEEBÓCITOS DE LIMULUS (LAL)
15.3 TESTE DE ATIVAÇÃO DE MONÓCITOS (MAT)
15.4 ENSAIO DO FATOR C RECOMBINANTE (RFC)
15.5 TESTE DE PIRÓGENO EM COELHOS
16 MERCADO GLOBAL DE TESTES DE ENDOTOXINAS E PIRÓGENOS, POR TIPO
16.1 VISÃO GERAL
16.2 TESTES DE ENDOTOXINAS E PIRÓGENOS PRÉ-FORMADOS
16.3 TESTES DE PROENDOTOXINA E PIRÓGENOS
16.4 TESTE COMBINADO DE ENDOTOXINA E PIRÓGENO
17 MERCADO GLOBAL DE TESTES DE ENDOTOXINAS E PIRÓGENOS, POR FORMULÁRIO
17.1 VISÃO GERAL
17.2 PÓ
17.3 LÍQUIDO
18 MERCADO GLOBAL DE TESTES DE ENDOTOXINAS E PIRÓGENOS, POR CATEGORIA DE PRODUTO
18.1 VISÃO GERAL
18.2 INGREDIENTE COM RÓTULO LIMPO
18.3 CONVENCIONAL
19 MERCADO GLOBAL DE TESTES DE ENDOTOXINAS E PIRÓGENOS, POR APLICAÇÃO
19.1 VISÃO GERAL
19.2 FABRICAÇÃO DE PRODUTOS FARMACÊUTICOS
19.3 FABRICAÇÃO DE DISPOSITIVOS MÉDICOS
19.4 PRODUÇÃO DE MATÉRIAS-PRIMAS
19.5 FABRICAÇÃO DE EMBALAGENS
20 MERCADO GLOBAL DE TESTES DE ENDOTOXINAS E PIRÓGENOS, POR MÉTODO
20.1 VISÃO GERAL
20.2 TESTE DE ENDOTOXINA E PIRÓGENO EM GEL CLOT
20.3 TESTE DE ENDOTOXINA CROMOGÊNICA E PIRÓGENO
20.4 TESTE DE ENDOTOXINA TURBIDIMÉTRICA E PIRÓGENO
21 MERCADO GLOBAL DE TESTES DE ENDOTOXINAS E PIRÓGENOS, POR MODO DE COMPRA
21.1 VISÃO GERAL
21.2 GRUPO GRANDE
21.3 GRUPO MÉDIO E PEQUENO
21.4 INDIVIDUAL
22 MERCADO GLOBAL DE TESTES DE ENDOTOXINAS E PIRÓGENOS, POR PRODUTO FINAL
22.1 VISÃO GERAL
22.2 BIOLÓGICOS
22.3 VACINAS E/OU CGT
22.4 INJETÁVEIS
22,5 OUTROS
22.5.1 ENDOSCÓPIOS
22.5.2 DISPOSITIVOS BIOMÉDICOS REUTILIZÁVEIS
22.5.3 OUTROS
23 MERCADO GLOBAL DE TESTES DE ENDOTOXINAS E PIRÓGENOS, POR USUÁRIO FINAL
23.1 VISÃO GERAL
23.2 EMPRESAS FARMACÊUTICAS
23.3 EMPRESAS DE BIOTECNOLOGIA
23.4 EMPRESAS BIOMÉDICAS
23.5 EMPRESAS DE DISPOSITIVOS MÉDICOS
23.6 ORGANIZAÇÃO DE PESQUISA CONTRATADA (ORG)
23.7 ORGANIZAÇÃO DE FABRICAÇÃO CONTRATADA (CMO)
24 MERCADO GLOBAL DE TESTES DE ENDOTOXINAS E PIRÓGENOS, GEOGRAFIA
24.1 MERCADO GLOBAL DE TESTES DE ENDOTOXINAS E PIRÓGENOS (TODA A SEGMENTAÇÃO FORNECIDA ACIMA É REPRESENTADA NESTE CAPÍTULO POR PAÍS)
24.2 AMÉRICA DO NORTE
24.2.1 EUA
24.2.2 CANADÁ
24.2.3 MÉXICO
24.3 EUROPA
24.3.1 ALEMANHA
24.3.2 FRANÇA
24.3.3 Reino Unido
24.3.4 ITÁLIA
24.3.5 ESPANHA
24.3.6 RÚSSIA
24.3.7 BÉLGICA
24.3.8 HOLANDA
24.3.9 SUÍÇA
24.3.10 RESTO DA EUROPA
24.4 ÁSIA-PACÍFICO
24.4.1 JAPÃO
24.4.2 CHINA
24.4.3 COREIA DO SUL
24.4.4 ÍNDIA
24.4.5 AUSTRÁLIA
24.4.6 SINGAPURA
24.4.7 MALÁSIA
24.4.8 RESTO DA ÁSIA-PACÍFICO
24,5 AMÉRICA DO SUL
24.5.1 BRASIL
24.5.2 ARGENTINA
24.5.3 RESTO DA AMÉRICA DO SUL
24.6 PRINCIPAIS INSIGHTS: POR PAÍSES PRINCIPAIS
25 MERCADO GLOBAL DE TESTES DE ENDOTOXINAS E PIRÓGENOS, CENÁRIO DA EMPRESA
25.1 ANÁLISE DE AÇÕES DA EMPRESA: GLOBAL
25.2 ANÁLISE DE AÇÕES DA EMPRESA: AMÉRICA DO NORTE
25.3 ANÁLISE DE AÇÕES DA EMPRESA: EUROPA
25.4 ANÁLISE DE AÇÕES DA EMPRESA: ÁSIA-PACÍFICO
25.5 FUSÕES E AQUISIÇÕES
25.6 DESENVOLVIMENTO E APROVAÇÕES DE NOVOS PRODUTOS
25.7 EXPANSÕES
25.8 ALTERAÇÕES REGULAMENTARES
25.9 PARCERIA E OUTROS DESENVOLVIMENTOS ESTRATÉGICOS
26 ANÁLISE GLOBAL DE MERCADO DE TESTES DE ENDOTOXINAS E PIRÓGENOS, SWOT E DBMR
27 MERCADO GLOBAL DE TESTES DE ENDOTOXINAS E PIRÓGENOS, PERFIL DA EMPRESA
27.1 PALL EUROPE LIMITED (DANAHER CORPORATION)
27.1.1 VISÃO GERAL DA EMPRESA
27.1.2 ANÁLISE DE RECEITA
27.1.3 PRESENÇA GEOGRÁFICA
27.1.4 PORTFÓLIO DE PRODUTOS
27.1.5 DESENVOLVIMENTOS RECENTES
27.2 THERMO FISHER SCIENTIFIC INC.
27.2.1 VISÃO GERAL DA EMPRESA
27.2.2 ANÁLISE DE RECEITA
27.2.3 PRESENÇA GEOGRÁFICA
27.2.4 PORTFÓLIO DE PRODUTOS
27.2.5 DESENVOLVIMENTOS RECENTES
27.3 LABORATÓRIOS CHARLES RIVER
27.3.1 VISÃO GERAL DA EMPRESA
27.3.2 ANÁLISE DE RECEITA
27.3.3 PRESENÇA GEOGRÁFICA
27.3.4 PORTFÓLIO DE PRODUTOS
27.3.5 DESENVOLVIMENTOS RECENTES
27.4 EUROFINS CIENTÍFICO
27.4.1 VISÃO GERAL DA EMPRESA
27.4.2 ANÁLISE DE RECEITA
27.4.3 PRESENÇA GEOGRÁFICA
27.4.4 PORTFÓLIO DE PRODUTOS
27.4.5 DESENVOLVIMENTOS RECENTES
27.5 SGS SOCIÉTÉ GÉNÉRALE DE SURVEILLANCE SA.
27.5.1 VISÃO GERAL DA EMPRESA
27.5.2 ANÁLISE DE RECEITA
27.5.3 PRESENÇA GEOGRÁFICA
27.5.4 PORTFÓLIO DE PRODUTOS
27.5.5 DESENVOLVIMENTOS RECENTES
27.6 PACIFIC BIOLABS
27.6.1 VISÃO GERAL DA EMPRESA
27.6.2 ANÁLISE DE RECEITA
27.6.3 PRESENÇA GEOGRÁFICA
27.6.4 PORTFÓLIO DE PRODUTOS
27.6.5 DESENVOLVIMENTOS RECENTES
27,7 LONZA
27.7.1 VISÃO GERAL DA EMPRESA
27.7.2 ANÁLISE DE RECEITA
27.7.3 PRESENÇA GEOGRÁFICA
27.7.4 PORTFÓLIO DE PRODUTOS
27.7.5 DESENVOLVIMENTOS RECENTES
27,8 MERCK KGAA
27.8.1 VISÃO GERAL DA EMPRESA
27.8.2 ANÁLISE DE RECEITA
27.8.3 PRESENÇA GEOGRÁFICA
27.8.4 PORTFÓLIO DE PRODUTOS
27.8.5 DESENVOLVIMENTOS RECENTES
27.9 STERIS
27.9.1 VISÃO GERAL DA EMPRESA
27.9.2 ANÁLISE DE RECEITA
27.9.3 PRESENÇA GEOGRÁFICA
27.9.4 PORTFÓLIO DE PRODUTOS
27.9.5 DESENVOLVIMENTOS RECENTES
27.1 SARTORIUS AG
27.10.1 VISÃO GERAL DA EMPRESA
27.10.2 ANÁLISE DE RECEITA
27.10.3 PRESENÇA GEOGRÁFICA
27.10.4 PORTFÓLIO DE PRODUTOS
27.10.5 DESENVOLVIMENTOS RECENTES
27.11 BIOMÉRIES
27.11.1 VISÃO GERAL DA EMPRESA
27.11.2 ANÁLISE DE RECEITA
27.11.3 PRESENÇA GEOGRÁFICA
27.11.4 PORTFÓLIO DE PRODUTOS
27.11.5 DESENVOLVIMENTOS RECENTES
27.12 FUJIFILM WAKO PURE CHEMICAL CORPORATION
27.12.1 VISÃO GERAL DA EMPRESA
27.12.2 ANÁLISE DE RECEITA
27.12.3 PRESENÇA GEOGRÁFICA
27.12.4 PORTFÓLIO DE PRODUTOS
27.12.5 DESENVOLVIMENTOS RECENTES
27.13 ELLAB A/S.
27.13.1 VISÃO GERAL DA EMPRESA
27.13.2 ANÁLISE DE RECEITA
27.13.3 PRESENÇA GEOGRÁFICA
27.13.4 PORTFÓLIO DE PRODUTOS
27.13.5 DESENVOLVIMENTOS RECENTES
27.14 ASSOCIADOS DE CAPE COD, INC (SEIKAGAKU CORPORATION)
27.14.1 VISÃO GERAL DA EMPRESA
27.14.2 ANÁLISE DE RECEITA
27.14.3 PRESENÇA GEOGRÁFICA
27.14.4 PORTFÓLIO DE PRODUTOS
27.14.5 DESENVOLVIMENTOS RECENTES
27.15 WUXI APPTEC
27.15.1 VISÃO GERAL DA EMPRESA
27.15.2 ANÁLISE DE RECEITA
27.15.3 PRESENÇA GEOGRÁFICA
27.15.4 PORTFÓLIO DE PRODUTOS
27.15.5 DESENVOLVIMENTOS RECENTES
27.16 GENSCRIPT
27.16.1 VISÃO GERAL DA EMPRESA
27.16.2 ANÁLISE DE RECEITA
27.16.3 PRESENÇA GEOGRÁFICA
27.16.4 PORTFÓLIO DE PRODUTOS
27.16.5 DESENVOLVIMENTOS RECENTES
27.17 MICROCOAT BIOTECHNOLOGIE GMBH
27.17.1 VISÃO GERAL DA EMPRESA
27.17.2 ANÁLISE DE RECEITA
27.17.3 PRESENÇA GEOGRÁFICA
27.17.4 PORTFÓLIO DE PRODUTOS
27.17.5 DESENVOLVIMENTOS RECENTES
27.18 SANQUIN
27.18.1 VISÃO GERAL DA EMPRESA
27.18.2 ANÁLISE DE RECEITA
27.18.3 PRESENÇA GEOGRÁFICA
27.18.4 PORTFÓLIO DE PRODUTOS
27.18.5 DESENVOLVIMENTOS RECENTES
27.19 LEITURA SERVIÇOS CIENTÍFICOS LTDA
27.19.1 VISÃO GERAL DA EMPRESA
27.19.2 ANÁLISE DE RECEITA
27.19.3 PRESENÇA GEOGRÁFICA
27.19.4 PORTFÓLIO DE PRODUTOS
27.19.5 DESENVOLVIMENTOS RECENTES
27.2 NANOCOMPOSIX
27.20.1 VISÃO GERAL DA EMPRESA
27.20.2 ANÁLISE DE RECEITA
27.20.3 PRESENÇA GEOGRÁFICA
27.20.4 PORTFÓLIO DE PRODUTOS
27.20.5 DESENVOLVIMENTOS RECENTES
27.21 ZWISLER LABORATORIUM GMBH
27.21.1 VISÃO GERAL DA EMPRESA
27.21.2 ANÁLISE DE RECEITA
27.21.3 PRESENÇA GEOGRÁFICA
27.21.4 PORTFÓLIO DE PRODUTOS
27.21.5 DESENVOLVIMENTOS RECENTES
27.22 NELSON LABORATORIES, LLC – UMA EMPRESA DE SAÚDE SOTERA
27.22.1 VISÃO GERAL DA EMPRESA
27.22.2 ANÁLISE DE RECEITA
27.22.3 PRESENÇA GEOGRÁFICA
27.22.4 PORTFÓLIO DE PRODUTOS
27.22.5 DESENVOLVIMENTOS RECENTES
27.23 NORTH AMERICAN SCIENCE ASSOCIATES, LLC
27.23.1 VISÃO GERAL DA EMPRESA
27.23.2 ANÁLISE DE RECEITA
27.23.3 PRESENÇA GEOGRÁFICA
27.23.4 PORTFÓLIO DE PRODUTOS
27.23.5 DESENVOLVIMENTOS RECENTES
27.24 PROMEGA CORPORATION
27.24.1 VISÃO GERAL DA EMPRESA
27.24.2 ANÁLISE DE RECEITA
27.24.3 PRESENÇA GEOGRÁFICA
27.24.4 PORTFÓLIO DE PRODUTOS
27.24.5 DESENVOLVIMENTOS RECENTES
27.25 HYCULT BIOTECH INC.
27.25.1 VISÃO GERAL DA EMPRESA
27.25.2 ANÁLISE DE RECEITA
27.25.3 PRESENÇA GEOGRÁFICA
27.25.4 PORTFÓLIO DE PRODUTOS
27.25.5 DESENVOLVIMENTOS RECENTES
27.26 GRUPO ALMAC
27.26.1 VISÃO GERAL DA EMPRESA
27.26.2 ANÁLISE DE RECEITA
27.26.3 PRESENÇA GEOGRÁFICA
27.26.4 PORTFÓLIO DE PRODUTOS
27.26.5 DESENVOLVIMENTOS RECENTES
27.27 MAT BIOTECNOLOGIA
27.27.1 VISÃO GERAL DA EMPRESA
27.27.2 ANÁLISE DE RECEITA
27.27.3 PRESENÇA GEOGRÁFICA
27.27.4 PORTFÓLIO DE PRODUTOS
27.27.5 DESENVOLVIMENTOS RECENTES
27.28 SOLVIAS
27.28.1 VISÃO GERAL DA EMPRESA
27.28.2 ANÁLISE DE RECEITA
27.28.3 PRESENÇA GEOGRÁFICA
27.28.4 PORTFÓLIO DE PRODUTOS
27.28.5 DESENVOLVIMENTOS RECENTES
27.29 WICKHAM MICRO LIMITADA
27.29.1 VISÃO GERAL DA EMPRESA
27.29.2 ANÁLISE DE RECEITA
27.29.3 PRESENÇA GEOGRÁFICA
27.29.4 PORTFÓLIO DE PRODUTOS
27.29.5 DESENVOLVIMENTOS RECENTES
27.3 BIOLABS CRIATIVOS
27.30.1 VISÃO GERAL DA EMPRESA
27.30.2 ANÁLISE DE RECEITA
27.30.3 PRESENÇA GEOGRÁFICA
27.30.4 PORTFÓLIO DE PRODUTOS
27.30.5 DESENVOLVIMENTOS RECENTES
*OBSERVAÇÃO: A LISTA DE EMPRESAS APRESENTADA NÃO É EXAUSTIVA E ESTÁ DE ACORDO COM AS NECESSIDADES DE NOSSOS CLIENTES ANTERIORES. APRESENTAMOS O PERFIL DE MAIS DE 100 EMPRESAS EM NOSSO ESTUDO E, PORTANTO, A LISTA DE EMPRESAS PODE SER MODIFICADA OU SUBSTITUÍDA SOB SOLICITAÇÃO.
28 RELATÓRIOS RELACIONADOS
29 QUESTIONÁRIO
30 SOBRE PESQUISA DE MERCADO DE PONTES DE DADOS
Metodologia de Investigação
A recolha de dados e a análise do ano base são feitas através de módulos de recolha de dados com amostras grandes. A etapa inclui a obtenção de informações de mercado ou dados relacionados através de diversas fontes e estratégias. Inclui examinar e planear antecipadamente todos os dados adquiridos no passado. Da mesma forma, envolve o exame de inconsistências de informação observadas em diferentes fontes de informação. Os dados de mercado são analisados e estimados utilizando modelos estatísticos e coerentes de mercado. Além disso, a análise da quota de mercado e a análise das principais tendências são os principais fatores de sucesso no relatório de mercado. Para saber mais, solicite uma chamada de analista ou abra a sua consulta.
A principal metodologia de investigação utilizada pela equipa de investigação do DBMR é a triangulação de dados que envolve a mineração de dados, a análise do impacto das variáveis de dados no mercado e a validação primária (especialista do setor). Os modelos de dados incluem grelha de posicionamento de fornecedores, análise da linha de tempo do mercado, visão geral e guia de mercado, grelha de posicionamento da empresa, análise de patentes, análise de preços, análise da quota de mercado da empresa, normas de medição, análise global versus regional e de participação dos fornecedores. Para saber mais sobre a metodologia de investigação, faça uma consulta para falar com os nossos especialistas do setor.
Personalização disponível
A Data Bridge Market Research é líder em investigação formativa avançada. Orgulhamo-nos de servir os nossos clientes novos e existentes com dados e análises que correspondem e atendem aos seus objetivos. O relatório pode ser personalizado para incluir análise de tendências de preços de marcas-alvo, compreensão do mercado para países adicionais (solicite a lista de países), dados de resultados de ensaios clínicos, revisão de literatura, mercado remodelado e análise de base de produtos . A análise de mercado dos concorrentes-alvo pode ser analisada desde análises baseadas em tecnologia até estratégias de carteira de mercado. Podemos adicionar quantos concorrentes necessitar de dados no formato e estilo de dados que procura. A nossa equipa de analistas também pode fornecer dados em tabelas dinâmicas de ficheiros Excel em bruto (livro de factos) ou pode ajudá-lo a criar apresentações a partir dos conjuntos de dados disponíveis no relatório.