Europe Diagnostic Tests Market
市场规模(十亿美元)
CAGR :
% 
 USD
160,573.05 Million
USD
324,678.67 Million
2022
2030
USD
160,573.05 Million
USD
324,678.67 Million
2022
2030
| 2023 –2030 | |
| USD 160,573.05 Million | |
| USD 324,678.67 Million | |
|
|
|
|
歐洲診斷測試市場,按類型(葡萄糖測試、傳染病測試、細胞學測試、CBC 測試、血液培養測試、梅毒測試、尿素測試、C 反應蛋白測試、抗原測試、HBA1C 測試、妊娠測試、血脂測試、電解質測試、肝功能測試、糞便幽門螺旋桿菌測試、鈣測試、交叉配血檢測、甲狀腺測試、糞便計數、肝功能檢查、微門螺旋桿菌測試單位測試和其他測試)、解決方案(服務和產品)、技術(基於免疫測定、基於 PCR、下一代基因測序、基於光譜、基於色譜、微流體、基質技術等)、測試模式(基於處方的測試和 OTC測試)、方法(分子診斷儀器、體外診斷儀器和即時檢驗儀器)、樣本類型(尿液、唾液、血液、頭髮、汗水等)、應用(心臟病學、腫瘤學、神經病學、骨科、胃腸病學、婦科、牙科等)、檢測類型(生物化學、血液學、微生物學、組織病理學等)、年齡(兒科、成人和老年科)、最終用戶(醫院、診斷中心、研究實驗室和研究所、研究機構、家庭護理、血庫、專科診所、門診手術中心等)、分銷渠道(直接投標、零售和在線銷售)——行業趨勢和2030 年預測。
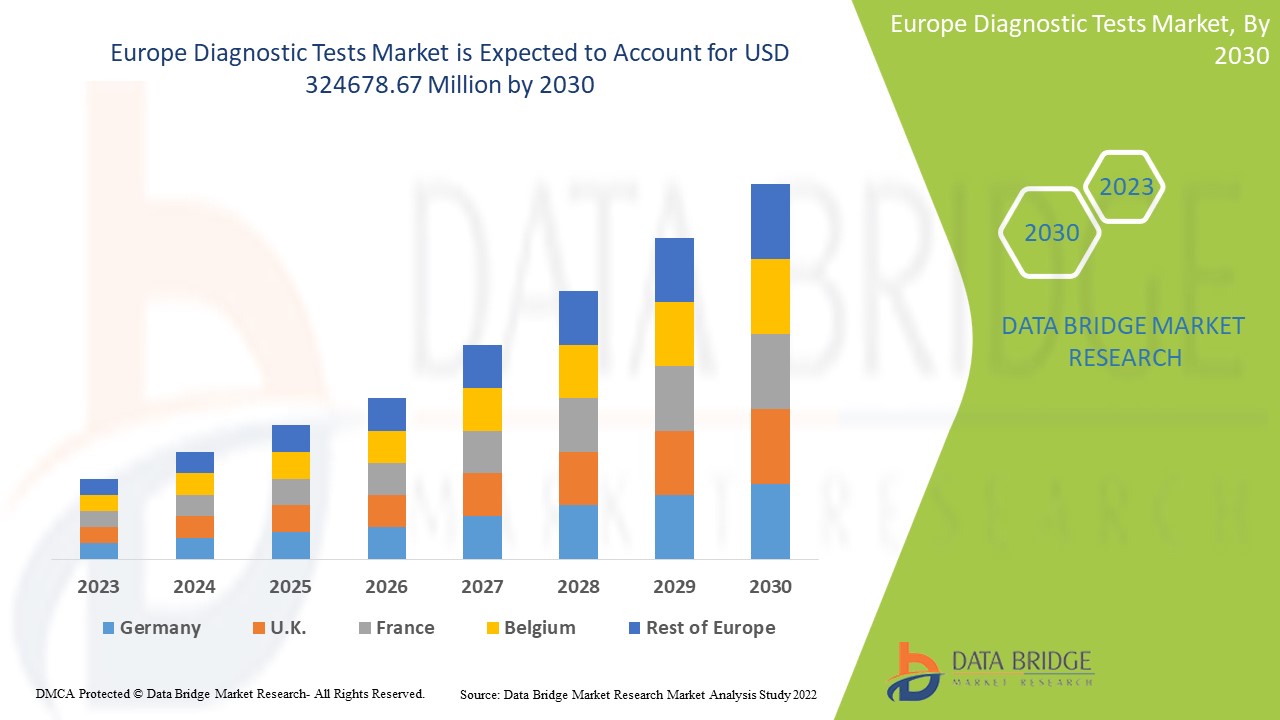
歐洲診斷測試市場分析與規模
根據世界衛生組織 (WHO) 的數據,到 2021 年 4 月,慢性病每年將導致約 4,100 萬人死亡,佔所有死亡人數的 71%。因此,診斷檢測已被證明有助於慢性病的管理,以及疾病的預防、檢測和診斷。透過識別個別風險因素和早期預警指標,臨床診斷能夠實現早期預防和介入。因此,隨著慢性病盛行率的上升,預計整體市場將會成長。
Data Bridge Market Research 分析稱,2022 年診斷測試市場規模為 1605.7305 億美元,預計到 2030 年將達到 3246.7867 億美元,在 2023 年至 2030 年的預測期內複合年增長率為 9.2%。除了對市場價值、成長率、細分、地理覆蓋範圍和主要參與者等市場情景的洞察外,Data Bridge Market Research 整理的市場報告還包括深度專家分析、患者流行病學、管道分析、定價分析和監管框架。
歐洲診斷測試市場範圍和細分
|
報告指標 |
細節 |
|
預測期 |
2023年至2030年 |
|
基準年 |
2022 |
|
歷史歲月 |
2021(可自訂為 2015 - 2020 年) |
|
定量單位 |
收入(百萬美元)、銷售(單位)、定價(美元) |
|
涵蓋的領域 |
類型(葡萄糖檢測、傳染病檢測、細胞學檢測、全血球計數檢測、血液培養檢測、梅毒檢測、尿素檢測、C反應蛋白檢測、抗原檢測、糖化血紅素1C檢測、懷孕檢測、血脂檢測、電解質檢測、肝功能檢測、糞便幽門螺旋桿菌檢測、鈣檢測、交錯叉配血檢測、甲狀腺功能檢測、糞便顯微鏡檢查、尿液顯微鏡檢查、單位包裝紅血球計數檢測、血沉檢測和其他檢測)、解決方案(服務和產品)、技術(基於免疫測定、基於PCR、下一代基因測序、基於光譜、基於色譜、微流體、基質技術和其他)、檢測模式(基於處方的檢測和OTC檢測)、方法(分子診斷儀器、體外診斷儀器和即時檢測儀器)、樣本類型(尿液、唾液、血液、頭髮、汗液和其他)、應用(心臟病學、腫瘤學、神經病學、骨科、胃腸病學、婦科、牙科等)、檢測類型(生物化學、血液學、微生物學、組織病理學等)、年齡(兒科、成人和老年科)、最終用戶(醫院、診斷中心、研究實驗室和研究所、研究所、家庭護理、血庫、專科診所、門診手術中心等)、分銷渠道(直接投標、零售和線上銷售) |
|
覆蓋國家 |
德國、法國、英國、荷蘭、瑞士、比利時、俄羅斯、義大利、西班牙、土耳其、歐洲其他地區 |
|
涵蓋的市場參與者 |
F-Hoffman La-Roche Ltd.(瑞士)、ABBOTT(美國)、Danaher(美國)、BD(美國)、Thermo Fisher Scientific Inc.(美國)、ACON Laboratories Inc.(美國)、Hemosure, Inc.(美國)、MicroGen Diagnostics(美國)、QIAGEN(德國)、Grinoscyk(Apbiotic)、ApbioGEN(韓國)(西班牙)、Yaknos(韓國), GIAGEN(德國)) Systems, Inc.(美國)、Nanoentek(韓國)、DiaSorin SpA(義大利)、Bio-Rad Laboratories, Inc.(美國)、BIOMEDOMICS INC(美國)、EKF Diagnostics Holdings plc(英國)、Siemens Healthcare GmbH(德國)、PerkinElmer Laboratories, Inc.(美國)、Quidel Corporation(美國)、Illumina, Inc.(美國)、Lamdagen Corporation (美國)、LifeSign LLC.(美國)、Medixbiochemica(芬蘭)、Nova Biomedical(美國)、Ortho Clinical Diagnostics(美國)、三諾生物感測有限公司(美國)、SSTRECK. |
|
市場機會 |
|
市場定義
診斷測試是用於輔助檢測或診斷疾病的醫療程序。這些測試在疾病控制、監測和預防中發揮重要作用。它們有助於加強病患照護、保障消費者安全並減少醫療支出。診斷測試用於查明病因。作為體檢的一部分進行的診斷測試可用於識別疾病或確定症狀的病因。當用於其他目的時,診斷測試可用於識別特定的優勢和劣勢。
歐洲診斷測試市場動態
驅動程式
- 傳染病和慢性病發病率不斷上升
傳染病和慢性病給全球人口帶來巨大壓力。白喉、伊波拉、流感、肝炎、愛滋病毒/愛滋病、人類乳突病毒 (HPV)、結核病等傳染病均由微生物引起,而登革熱、寨卡病毒、新冠肺炎 (COVID-19) 和豬流感等突發疫情則推動了全球對臨床診斷檢測的需求。此外,癌症、糖尿病、心血管疾病、肥胖等慢性疾病也推高了對臨床診斷的需求。
- 臨床診斷測試的興起
識別和描述微生物最準確的技術是臨床診斷測試。實用的測試需要快速、精確,並且能夠確定感染的嚴重程度。透過更快、更準確的測試來識別微生物的菌株及其藥物敏感性,可以減少找到合適抗生素所需的時間。根據世界衛生組織 (WHO) 的報告,結核病 (TB) 是十大死因之一。這可能會對市場擴張產生重大影響。生活水平提高導致癌症發病率上升,這在很大程度上可以歸因於更先進診斷技術的可及性和可用性。由於臨床癌症診斷設備在這些程序中被廣泛使用,預測期內對診斷測試的需求將會上升。
機會
- 對先進診斷解決方案的需求不斷增長
臨床診斷用於管理患者的健康。它有助於更早發現疾病並有助於控制病情進展。此外,它還可以幫助感染者避免長期後果,並提高大眾對臨床診斷重要性的認識。醫療保健支出的增加和健康意識的提高促進了市場的成長。隨著人們越來越擔心感染患者傳播疾病的可能性,預計在預測期內,臨床診斷試劑盒的需求將會增加。診斷測試可以透過服務、設備和耗材進行。這項特點幾乎肯定會提高患者的舒適度,從而有利於市場發展。
限制/挑戰
- 診斷測試的可負擔性
預計報銷削減、預算限制以及嚴格的監管政策帶來的定價壓力將阻礙市場成長。此外,在2023-2030年的預測期內,診斷檢測市場預計將面臨挑戰,包括缺乏與權威中心實驗室方法的一致性,以及專業機構對即時檢測(POC)設備的採用不足。
本診斷測試市場報告詳細介紹了最新發展動態、貿易法規、進出口分析、生產分析、價值鏈優化、市場份額、國內和本地市場參與者的影響,並分析了新興收入來源、市場法規變化、戰略市場增長分析、市場規模、品類市場增長、應用領域和市場主導地位、產品審批、產品發布、地域擴張以及市場技術創新等方面的機遇。如需了解更多關於診斷測試市場的信息,請聯繫 Data Bridge 市場研究部門以獲取分析師簡報,我們的團隊將協助您做出明智的市場決策,實現市場成長。
COVID-19 對診斷測試市場的影響
COVID-19疫情對診斷檢測市場產生了負面影響,因為實驗室檢測數量增加,導致需求成長更快,以跟上疑似病例的成長。根據《大西洋月刊》集團(Atlantic Monthly Group)的數據,全球COVID-19檢測數量從2020年9月的760,441次大幅增加到2020年10月的964,792次。因此,由於患者人數增加和政府資金投入,檢測數量不斷增加,預計將推動COVID-19檢測試劑盒的需求,並推動整個市場的指數級增長。
最新動態
- 2020年,西門子醫療有限公司正式宣布推出RAPIDPoint 500e血氣分析儀,不僅豐富了公司的產品組合,也應用於新冠疫情防治工作,有助於提升公司產品線的收入。
- 2020年,西門子醫療有限公司與瑪利亞豪斯醫院集團宣布了一項為期十年的合作。這項合作將使西門子在診斷領域長期受益,並有助於改善公司的財務狀況。
歐洲診斷測試市場範圍
診斷測試市場根據類型、解決方案、技術、測試模式、方法、樣本類型、應用程式、測試類型、年齡、最終用戶和分銷管道進行細分。這些細分市場的成長將幫助您分析行業中成長緩慢的細分市場,並為用戶提供有價值的市場概覽和市場洞察,幫助他們做出策略決策,確定核心市場應用。
類型
- 血糖測試
- 傳染病檢測
- 細胞學檢查
- 全血球計數測試
- 血液培養測試
- 梅毒檢測
- 尿素測試
- C反應蛋白測試
- 抗原檢測
- HBA1C 測試
- 妊娠測試
- 血脂檢測
- 電解質測試
- 肝功能檢查
- 糞便幽門螺旋桿菌檢測
- 鈣檢測、交叉配血檢測
- 甲狀腺功能檢查
- 糞便顯微鏡檢查
- 尿液顯微鏡檢查
- 單位濃縮紅血球檢測
- 血沉測試及其他測試
解決方案
- 服務
- 產品
科技
- 基於免疫測定
- 基於PCR
- 下一代基因定序
- 基於光譜的
- 基於色譜法
- 微流體
- 基板技術
- 其他的
測試模式
- 基於處方的測試
- OTC測試
方法
- 分子診斷儀器
- 體外診斷儀器
- 即時檢驗儀器
樣品類型
- 尿
- 唾液
- 血
- 頭髮
- 汗
- 其他的
應用
- 心臟病學
- 腫瘤學
- 神經病學
- 骨科
- 胃腸病學
- 婦科
- 牙科
- 其他的
測試類型
- 生物化學
- 血液學
- 微生物學
- 組織病理學
- 其他的
年齡
- 兒科
- 成人
- 老年
最終用戶
- 醫院
- 診斷中心
- 研究實驗室和研究所
- 研究所
- 居家護理
- 血庫
- 專科診所
- 門診手術中心
- 其他的
分銷管道
- 直接招標
- 零售銷售
- 網上銷售
歐洲診斷測試市場區域分析/洞察
對診斷測試市場進行分析,並按國家、類型、解決方案、技術、測試模式、方法、樣本類型、應用、測試類型、年齡、最終用戶和分銷管道提供市場規模洞察和趨勢,如上所述。
診斷測試市場報告涵蓋的國家有德國、法國、英國、荷蘭、瑞士、比利時、俄羅斯、義大利、西班牙、土耳其和歐洲其他地區。
德國在歐洲診斷測試市場佔據主導地位,政府採取的戰略舉措包括收購和重點細分產品發布,這些舉措有助於擴大其影響力,也有助於擴大和增強公司的產品組合,最終將為該國帶來更多收入。
報告的國家部分還提供了各個市場的影響因素以及國內市場監管變化,這些變化會影響市場的當前和未來趨勢。下游和上游價值鏈分析、技術趨勢、波特五力模型分析以及案例研究等數據點是預測各國市場狀況的一些指標。此外,在對國家/地區數據進行預測分析時,還考慮了全球品牌的存在和可用性,以及它們因本土和國內品牌的激烈競爭或稀缺而面臨的挑戰,國內關稅和貿易路線的影響。
競爭格局和診斷測試市場份額分析
診斷測試市場競爭格局提供了按競爭對手劃分的詳細資訊。詳細資訊包括公司概況、公司財務狀況、收入、市場潛力、研發投入、新市場計劃、全球佈局、生產基地和設施、生產能力、公司優勢和劣勢、產品發布、產品寬度和廣度以及應用主導地位。以上提供的數據僅與公司在診斷測試市場的重點相關。
診斷測試市場的一些主要參與者包括:
- F-霍夫曼羅氏有限公司(瑞士)
- 雅培(美國)
- 丹納赫(美國)
- BD(美國)
- 賽默飛世爾科技公司(美國)
- ACON Laboratories Inc.(美國)
- Hemosure, Inc.(美國)
- MicroGen Diagnostics(美國)
- QIAGEN(德國)
- Grifols, SA(西班牙)
- BODITECH MED INC.(韓國)
- Chembio Diagnostic Systems, Inc.(美國)
- Nanoentek(韓國)
- DiaSorin SpA(義大利)
- Bio-Rad Laboratories, Inc.(美國)
- BIOMEDOMICS INC(美國)
- EKF Diagnostics Holdings plc(英國)
- 西門子醫療有限公司(德國)
- 珀金埃爾默公司(美國)
- 生物梅里埃(法國)
- ARKRAY USA, Inc.(美國)
- Biohit Oyj(芬蘭)
- Germaine Laboratories, Inc.(美國)
- Quidel Corporation(美國)
- Illumina公司(美國)
- Lamdagen公司(美國)
- LifeSign LLC.(美國)
- Medixbiochemica(芬蘭)
- Nova Biomedical(美國)
- Ortho Clinical Diagnostics(美國)
- 三諾生物感測有限公司(美國)
- STRECK(美國)
- Sysmex株式會社(日本)
SKU-
目录
1 引言
1.1 研究目標
1.2 市場定義
1.3 歐洲診斷測試市場概述
1.4 貨幣和定價
1.5 限制
1.6 覆蓋市場
2 市場區隔
2.1 關鍵要點
2.2 了解歐洲診斷測試市場規模
2.2.1 供應商定位網格
2.2.2 技術生命線曲線
2.2.3 三腳架資料驗證模型
2.2.4 市場引導
2.2.5 多變量建模
2.2.6 自上而下的分析
2.2.7 挑戰矩陣
2.2.8 應用覆蓋網格
2.2.9 測量標準
2.2.10 供應商份額分析
2.2.11 銷售量數據
2.2.12 來自關鍵主要訪談的資料點
2.2.13 來自關鍵二級資料庫的資料點
2.3 歐洲診斷測試市場:研究快照
2.4 假設
3 市場概覽
3.1 驅動程式
3.2 限制
3.3 機遇
3.4 挑戰
4 執行摘要
5 項優質見解
5.1 佩爾斯特分析
5.2 波特五力模型
6 行業洞察
6.1 微觀和宏觀經濟因素
6.2 滲透和成長前景圖
6.3 主要定價策略
6.4 專家訪談
6.5 分析與建議
7 智慧財產權 (IP) 組合
7.1 專利品質和強度
7.2 專利家族
7.3 許可與合作
7.4 競爭格局
7.5 智慧財產權策略與管理
7.6 其他
8 成本分析細目
9 技術路線圖
10 創新追蹤與策略分析
10.1 重大交易與策略聯盟分析
10.1.1 合資企業
10.1.2 合併與收購
10.1.3 許可和合作
10.1.4 技術合作
10.1.5 戰略性撤資
10.2 正在開發的產品數量
10.3 發展階段
10.4 時間表和里程碑
10.5 創新策略和方法
10.6 風險評估與緩解
10.7 未來展望
11 監理合規性
11.1 監管機構
11.2 監理分類
11.2.1 I 類
11.2.2 II 類
11.2.3 III 類
11.3 監管提交
11.4 國際協調
11.5 合規與品質管理體系
11.6 監管挑戰與策略
12 報銷框架
13 機會圖分析
14 安裝基礎數據
15 價值鏈分析
16 醫療經濟
16.1 醫療保健支出
16.2 資本支出
16.3 資本支出趨勢
16.4 資本支出分配
16.5 資金來源
16.6 行業基準
16.7 GDP佔GDP的比重
16.8 醫療保健系統結構
16.9 政府政策
16.1 經濟發展
17 歐洲診斷測試市場(按類型)
17.1 概述
17.2 例行試驗
17.2.1 葡萄糖測試
17.2.2 傳染病檢測
17.2.3 CBC 測試
17.2.4 血液培養測試
17.2.5 梅毒檢測
17.2.6 尿素測試
17.2.7 C反應蛋白檢測
17.2.8 抗原檢測
17.2.9 HBA1C 測試
17.2.10 妊娠測試
17.2.11 血脂檢測
17.2.12 電解質測試
17.2.13 肝功能檢查
17.2.14 糞便幽門螺旋桿菌檢測
17.2.15 鈣測試
17.2.16 交叉配血試驗
17.2.17 甲狀腺功能檢查
17.2.18 糞便顯微鏡檢查
17.2.19 尿液顯微鏡檢查
17.2.20 單元包裝紅血球測試
17.2.21 ESR 測試
17.2.22 其他
17.3 專門測試
17.3.1 分子診斷檢測
17.3.2 免疫學測試
17.3.3 基因檢測
17.3.4 毒理學試驗
17.3.5 其他
18 歐洲診斷測試市場(按組件)
18.1 概述
18.2 產品
18.2.1 儀器
18.2.1.1. 按類型
18.2.1.1.1. 體外診斷儀器
18.2.1.1.1.1 免疫分析儀器
18.2.1.1.1.1.1. 依類型
A. ELISA 讀數儀
B. CLIA 分析儀
C. 其他
18.2.1.1.1.1.2. 按模式
A. 自動化
B.半自動化
C. 手冊
18.2.1.1.1.1.3. 按方式
A. 桌上型
B. 落地式
C. 模組化
18.2.1.1.1.2 臨床化學儀器
18.2.1.1.1.2.1. 依類型
A. 分光光度計
B. 電解質分析儀
C. 血液氣體分析儀
D. 凝血分析儀
E. 微孔板讀數儀
18.2.1.1.1.2.2. 按模式
A. 自動化
B.半自動化
C. 手冊
18.2.1.1.1.2.3. 按方式
A. 桌上型
B. 落地式
C. 模組化
18.2.1.1.1.3 血液學儀器
18.2.1.1.1.3.1. 按模式
A. 自動化
B.半自動化
C. 手冊
18.2.1.1.1.3.2. 按方式
A. 桌上型
B. 落地式
C. 模組化
18.2.1.1.1.4 分子診斷儀器
18.2.1.1.1.4.1. 按模式
A. PCR 儀器
B. NGS儀器
C. 微陣列儀器
D. 等溫擴增儀器
E. 核酸萃取儀器
F. 雜交儀器
18.2.1.1.1.4.2. 按模式
A. 自動化
B.半自動化
C. 手冊
18.2.1.1.1.4.3. 按方式
A. 桌上型
B. 落地式
C. 模組化
18.2.1.1.1.5 其他
18.2.1.1.2. 即時檢驗儀器
18.2.1.1.2.1 血糖監測設備
18.2.1.1.2.2 快速診斷測試設備
18.2.1.1.2.3 心臟標記設備
18.2.1.1.2.4 傳染病檢測設備
18.2.1.1.2.5 尿液分析設備
18.2.1.2. 其他
18.2.2 試劑盒和試劑
18.2.2.1. 妊娠檢測試劑盒
18.2.2.1.1. 條帶
18.2.2.1.2. 磁帶
18.2.2.1.3. 中游
18.2.2.1.4. 推入卡
18.2.2.1.5. 其他
18.2.2.2. 尿液分析檢測試劑盒
18.2.2.2.1. 盒式磁帶測試
18.2.2.2.2. 條帶測試
18.2.2.3. 血糖監測套件
18.2.2.3.1. 條帶
18.2.2.3.2. 墨水匣
18.2.2.4. 心臟分析
18.2.2.4.1. 肌鈣蛋白
18.2.2.4.2. 法國國家鈉肽
18.2.2.4.3. 肌紅蛋白
18.2.2.4.4. 其他
18.2.2.5. 傳染病檢測試劑盒
18.2.2.5.1. 肝炎
18.2.2.5.2. 流感
18.2.2.5.3. 愛滋病毒/愛滋病
18.2.2.5.4. 結核病
18.2.2.5.5. 醫院內感染
18.2.2.5.6. 新冠肺炎
18.2.2.5.7. 其他
18.2.2.6. 藥物檢測試劑盒
18.2.2.6.1. 大麻
18.2.2.6.2. 苯丙胺
18.2.2.6.3. 巴比妥類藥物
18.2.2.6.4. 抗憂鬱藥
18.2.2.6.5. PCP
18.2.2.6.6. 美沙酮
18.2.2.6.7. 其他
18.2.2.7. 其他
18.2.3 消耗品
18.2.3.1. 針頭和注射器
18.2.3.2. 血液採集設備
18.2.3.3. 媒體文化
18.2.3.3.1. 肉湯
18.2.3.3.2. 瓊脂
18.2.3.3.3. 其他
18.2.3.4. 污漬
18.2.3.4.1. 革蘭氏染色
18.2.3.4.2. 分枝桿菌染色
18.2.3.4.3. 真菌污漬
18.2.3.4.4. 其他
18.2.3.5. 對照品和校準品
18.2.3.6. 盤子
18.2.3.7. 其他
18.3 服務
19 歐洲診斷測試市場(按技術)
19.1 概述
19.2 基於PCR的
19.2.1 實時 PCR
19.2.2 嵌套 PCR
19.2.3 多重PCR
19.2.4 定量 PCR
19.2.5 其他
19.3 基於免疫測定的
19.3.1 側流免疫分析
19.3.1.1. 夾心試驗
19.3.1.2. 競爭性測定
19.3.2 紙基免疫測定
19.3.3 其他
19.4 基於色譜的
19.4.1 液相層析-質譜法
19.4.2 氣相層析質譜法
19.4.3 液相層析-串聯質譜法
19.5 基於光譜的
19.5.1 質譜法
19.5.2 拉曼光譜
19.5.3 光譜學
19.5.4 其他
19.6 微流體學
19.6.1 螢光素酶免疫沉澱系統(LIPS)
19.6.2 紙基微流體
19.7 下一代基因定序
19.7.1 全基因組定序
19.7.2 標靶重測序
19.7.3 全外顯子定序
19.7.4 RNA測序
19.7.5 其他
19.8 其他
20 歐洲診斷測試市場(依測試模式)
20.1 概述
20.2 基於處方的檢測
20.3 OTC測試
21 歐洲診斷測試市場(按應用)
21.1 概述
21.2 心臟病學
21.3 腫瘤學
21.4 神經病學
21.5 骨科
21.6 胃腸病學
21.7 婦科
21.8 牙科
21.9 其他
22 歐洲診斷測試市場(按樣本類型)
22.1 血液
22.2 尿液
22.3 唾液
22.4 呼吸道檢體
22.5 凳子
22.6 活檢
22.7 其他
23 歐洲診斷測試市場(依測試站點劃分)
23.1 概述
23.2 在家測試
23.3 基於實驗室的測試
24 歐洲診斷測試市場(依測試類型)
24.1 概述
24.2 生物化學
24.3 血液學
24.4 微生物學
24.5 組織病理學
24.6 其他
25 歐洲診斷測試市場(按年齡劃分)
25.1 概述
25.2 兒科
25.3 成人
25.4 老年人
26 歐洲診斷測試市場(按最終用戶)
26.1 概述
26.2 醫院
26.2.1 公共
26.2.2 私人
26.3 診斷中心
26.4 學術實驗室與研究所
26.5 研究機構
26.6 家庭護理
26.7 血庫
26.8 專科診所
26.9 門診手術中心(ASCS)
26.1 其他
27 歐洲診斷測試市場(按分銷管道)
27.1 概述
27.2 直接投標
27.3 零售額
27.3.1 在線
27.3.2 離線
27.4 其他
28 歐洲診斷測試市場、公司格局
28.1 公司份額分析:歐洲
28.2 合併與收購
28.3 新產品開發與審批
28.4 擴展
28.5 監管變化
28.6 夥伴關係和其他策略發展
29 歐洲診斷測試市場、SWOT 和 DBMR 分析
30 歐洲診斷測試市場(按國家/地區)
歐洲診斷測試市場(本章中所有細分均按國家/地區劃分)
30.1 歐洲
30.1.1 德國
30.1.2 法國
30.1.3 英國
30.1.4 匈牙利
30.1.5 立陶宛
30.1.6 奧地利
30.1.7 愛爾蘭
30.1.8 挪威
30.1.9 波蘭
10.1.30 義大利
11.1.30 西班牙
12.1.30 俄羅斯
13.1.30 土耳其
14.1.30 荷蘭
2015年1月30日 瑞士
2016年1月30日 歐洲其他地區
30.2 主要主要見解:依主要國家
31 歐洲診斷測試市場,公司簡介
31.1 雅培
31.1.1 公司概況
31.1.2 收入分析
31.1.3 地理分佈
31.1.4 產品組合
31.1.5 近期發展
31.2 BIO-RAD實驗室公司
31.2.1 公司概況
31.2.2 收入分析
31.2.3 地理存在
31.2.4 產品組合
31.2.5 近期發展
31.3 丹納赫
31.3.1 公司概況
31.3.2 收入分析
31.3.3 地理存在
31.3.4 產品組合
31.3.5 近期發展
31.4 BD
31.4.1 公司概況
31.4.2 收入分析
31.4.3 地理存在
31.4.4 產品組合
31.4.5 最近的發展
31.5 F.霍夫曼-拉羅氏有限公司
31.5.1 公司概況
31.5.2 收入分析
31.5.3 地理存在
31.5.4 產品組合
31.5.5 近期發展
31.6 EKF診斷
31.6.1 公司概況
31.6.2 收入分析
31.6.3 地理存在
31.6.4 產品組合
31.6.5 最近的發展
31.7 西門子醫療
31.7.1 公司概況
31.7.2 收入分析
31.7.3 地理存在
31.7.4 產品組合
31.7.5 近期發展
31.8 賽默飛世爾科技公司
31.8.1 公司概況
31.8.2 收入分析
31.8.3 地理存在
31.8.4 產品組合
31.8.5 最近的發展
31.9 ACON 實驗室公司
31.9.1 公司概況
31.9.2 收入分析
31.9.3 地理存在
31.9.4 產品組合
31.9.5 近期發展
31.1 生醫公司
31.10.1 公司概況
31.10.2 收入分析
31.10.3 地理存在
31.10.4 產品組合
31.10.5 近期發展
31.11 QUIDELORTHO 公司。
31.11.1 公司概況
31.11.2 收入分析
31.11.3 地理存在
31.11.4 產品組合
31.11.5 近期發展
31.12 愛科來公司
31.12.1 公司概況
31.12.2 收入分析
31.12.3 地理存在
31.12.4 產品組合
31.12.5 近期發展
31.13 斯特雷克
31.13.1 公司概況
31.13.2 收入分析
31.13.3 地理存在
31.13.4 產品組合
31.13.5 近期發展
31.14 珀金‧埃爾默
31.14.1 公司概況
31.14.2 收入分析
31.14.3 地理存在
31.14.4 產品組合
31.14.5 近期發展
31.15 DIASORIN SPA
31.15.1 公司概況
31.15.2 收入分析
31.15.3 地理存在
31.15.4 產品組合
31.15.5 近期發展
31.16 百歐希醫療保健有限公司
31.16.1 公司概況
31.16.2 收入分析
31.16.3 地理存在
31.16.4 產品組合
31.16.5 近期發展
31.17 MICROGEN公司
31.17.1 公司概況
31.17.2 收入分析
31.17.3 地理存在
31.17.4 產品組合
31.17.5 近期發展
31.18 愛爾蘭三一生物技術公司
31.18.1 公司概況
31.18.2 收入分析
31.18.3 地理存在
31.18.4 產品組合
31.18.5 近期發展
31.19 SYSMEX歐洲
31.19.1 公司概況
31.19.2 收入分析
31.19.3 地理存在
31.19.4 產品組合
31.19.5 近期發展
31.2 凱傑
31.20.1 公司概況
31.20.2 收入分析
31.20.3 地理存在
31.20.4 產品組合
31.20.5 近期發展
31.21 生物梅里埃公司
31.21.1 公司概況
31.21.2 收入分析
31.21.3 地理存在
31.21.4 產品組合
31.21.5 近期發展
31.22 CHEMBIO 診斷公司
31.22.1 公司概況
31.22.2 收入分析
31.22.3 地理存在
31.22.4 產品組合
31.22.5 近期發展
31.23 PTS診斷
31.23.1 公司概況
31.23.2 收入分析
31.23.3 地理存在
31.23.4 產品組合
31.23.5 近期動態
31.24 安捷倫科技公司
31.24.1 公司概況
31.24.2 收入分析
31.24.3 地理存在
31.24.4 產品組合
31.24.5 近期動態
31.25 伊萊米納公司
31.25.1 公司概況
31.25.2 收入分析
31.25.3 地理存在
31.25.4 產品組合
31.25.5 近期動態
31.26 精確科學公司
31.26.1 公司概況
31.26.2 收入分析
31.26.3 地理存在
31.26.4 產品組合
31.26.5 近期動態
31.27 麥瑞德遺傳學公司
31.27.1 公司概況
31.27.2 收入分析
31.27.3 地理存在
31.27.4 產品組合
31.27.5 近期動態
31.28 QUEST DIAGNOSTICS INCORPORATED。
31.28.1 公司概況
31.28.2 收入分析
31.28.3 地理存在
31.28.4 產品組合
31.28.5 近期發展
31.29 美國實驗室公司控股。
31.29.1 公司概況
31.29.2 收入分析
31.29.3 地理存在
31.29.4 產品組合
31.29.5 近期發展
31.3 PHC控股公司
31.30.1 公司概況
31.30.2 收入分析
31.30.3 地理存在
31.30.4 產品組合
31.30.5 近期發展
32份相關報告
33 結論
34 問卷
35 關於數據橋市場研究
研究方法
数据收集和基准年分析是使用具有大样本量的数据收集模块完成的。该阶段包括通过各种来源和策略获取市场信息或相关数据。它包括提前检查和规划从过去获得的所有数据。它同样包括检查不同信息源中出现的信息不一致。使用市场统计和连贯模型分析和估计市场数据。此外,市场份额分析和关键趋势分析是市场报告中的主要成功因素。要了解更多信息,请请求分析师致电或下拉您的询问。
DBMR 研究团队使用的关键研究方法是数据三角测量,其中包括数据挖掘、数据变量对市场影响的分析和主要(行业专家)验证。数据模型包括供应商定位网格、市场时间线分析、市场概览和指南、公司定位网格、专利分析、定价分析、公司市场份额分析、测量标准、全球与区域和供应商份额分析。要了解有关研究方法的更多信息,请向我们的行业专家咨询。
可定制
Data Bridge Market Research 是高级形成性研究领域的领导者。我们为向现有和新客户提供符合其目标的数据和分析而感到自豪。报告可定制,包括目标品牌的价格趋势分析、了解其他国家的市场(索取国家列表)、临床试验结果数据、文献综述、翻新市场和产品基础分析。目标竞争对手的市场分析可以从基于技术的分析到市场组合策略进行分析。我们可以按照您所需的格式和数据样式添加您需要的任意数量的竞争对手数据。我们的分析师团队还可以为您提供原始 Excel 文件数据透视表(事实手册)中的数据,或者可以帮助您根据报告中的数据集创建演示文稿。












