Canada And Us Point Of Care Testing Market
Tamaño del mercado en miles de millones de dólares
Tasa de crecimiento anual compuesta (CAGR) :
% 
 USD
15.25 Billion
USD
31.72 Billion
2024
2032
USD
15.25 Billion
USD
31.72 Billion
2024
2032
| 2025 –2032 | |
| USD 15.25 Billion | |
| USD 31.72 Billion | |
|
|
|
|
Segmentación del mercado de pruebas en el punto de atención de Canadá y EE. UU., por producto/enfermedad (enfermedades de transmisión sexual [ETS], hepatitis, infecciones respiratorias, infecciones gastrointestinales, infecciones del torrente sanguíneo [BSI], infecciones por levaduras de la sangre y otras), método/tecnología (pruebas de amplificación de ácidos nucleicos [NAAT], amplificación isotérmica mediada por bucle [LAMP], microfluídica/laboratorio en un chip y otras), tipo de panel (ensayo simple, ensayo dúplex, ensayo tríplex, ensayo múltiple [prueba sindrómica]), lugar de prueba (pruebas en el punto de atención en laboratorio [POCT], pruebas en el punto de atención en el hogar [POCCT]), usuario final (hospitales, clínicas, laboratorios, atención domiciliaria, centros de cirugía ambulatoria, centros de atención para personas mayores y otros), canal de distribución (licitación directa, ventas minoristas, ventas en línea y otros) - Industria Tendencias y pronósticos hasta 2032
Tamaño del mercado de pruebas en el punto de atención de Canadá y EE. UU.
- El mercado de pruebas en el punto de atención de Canadá y Estados Unidos se valoró en USD 15.250 millones en 2024 y se espera que alcance los USD 31.720 millones en 2032.
- Durante el período de pronóstico de 2025 a 2032, es probable que el mercado crezca a una CAGR del 9,6 %, impulsado principalmente por la creciente prevalencia de enfermedades crónicas e infecciosas.
- Este crecimiento está impulsado por factores como la creciente demanda de diagnóstico rápido en entornos de urgencias y ambulatorios.
Análisis del mercado de pruebas en el punto de atención de Canadá y Estados Unidos
- El mercado de pruebas en el punto de atención en Canadá y Estados Unidos está impulsado por la creciente prevalencia de enfermedades crónicas como la diabetes y las enfermedades cardiovasculares, junto con la creciente carga de enfermedades infecciosas que exigen soluciones de diagnóstico rápidas y precisas. La pandemia de COVID-19 aceleró significativamente la adopción de pruebas moleculares y rápidas en el punto de atención, mientras que la demanda continua de paneles para infecciones respiratorias, gastrointestinales, de transmisión sexual y del torrente sanguíneo continúa expandiendo el mercado. La creciente preferencia por la atención médica descentralizada y domiciliaria, respaldada por la amplia disponibilidad de kits de autodiagnóstico y diagnósticos en farmacias minoristas, impulsa aún más el crecimiento.
- Los avances tecnológicos en ensayos moleculares, microfluídica y dispositivos POCT conectados a teléfonos inteligentes están mejorando la precisión y la accesibilidad de las pruebas, mientras que los sistemas de salud adoptan estas soluciones para reducir costos y optimizar los tiempos de respuesta de los pacientes. Además, las políticas gubernamentales favorables, las aprobaciones regulatorias y los marcos de reembolso en Canadá y Estados Unidos están fomentando una mayor adopción de POCT en entornos clínicos, minoristas y de atención domiciliaria.
- Los profesionales sanitarios y los responsables políticos, tanto en Canadá como en Estados Unidos, reconocen cada vez más el valor de la prueba POCT para abordar la creciente carga de enfermedades, especialmente en centros de salud comunitarios, centros de atención de urgencias y regiones remotas donde el acceso a laboratorios centralizados es limitado. Esta creciente demanda impulsa la inversión pública y privada en plataformas de diagnóstico avanzadas que facilitan la toma rápida de decisiones clínicas.
- La pandemia de COVID-19 impulsó la adopción generalizada de soluciones descentralizadas de pruebas, acelerando la implementación de tecnologías POCT en hospitales, farmacias y otros centros de salud de Norteamérica. A medida que los sistemas de salud siguen priorizando la accesibilidad, la detección temprana y la atención centrada en el valor, se prevé que la necesidad de diagnósticos eficientes y cercanos al paciente siga siendo un factor clave de crecimiento en el mercado.
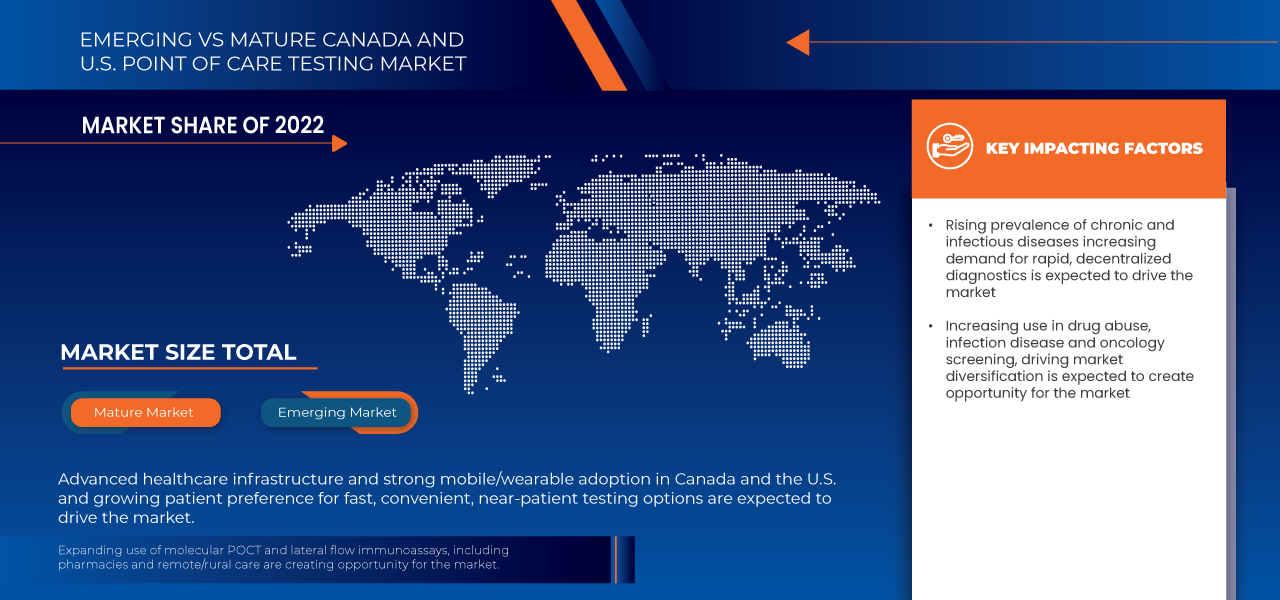
- Se espera que EE. UU. domine el mercado de pruebas en el punto de atención de Canadá y EE. UU. con una participación de mercado del 88,56 % debido a la presencia de una infraestructura de atención médica avanzada, una alta adopción de tecnologías de diagnóstico rápido, un fuerte apoyo gubernamental y una gran población de pacientes que impulsa la demanda de soluciones de pruebas eficientes y precisas.
Alcance del informe y segmentación del mercado de pruebas en el punto de atención de Canadá y EE. UU.
|
Atributos |
Análisis clave del mercado de pruebas en el punto de atención de Canadá y EE. UU. |
|
Segmentos cubiertos |
|
|
Países cubiertos |
|
|
Actores clave del mercado |
|
|
Oportunidades de mercado |
|
|
Conjuntos de información de datos de valor añadido |
Además de los conocimientos sobre escenarios de mercado, como el valor de mercado, la tasa de crecimiento, la segmentación, la cobertura geográfica y los principales actores, los informes de mercado seleccionados por Data Bridge Market Research también incluyen un análisis profundo de expertos, epidemiología de pacientes, análisis de la cartera de productos, análisis de precios y marco regulatorio. |
Tendencias del mercado de pruebas en el punto de atención de Canadá y EE. UU.
La creciente prevalencia de enfermedades crónicas e infecciosas incrementa la demanda de diagnósticos rápidos y descentralizados
- La creciente prevalencia de enfermedades crónicas e infecciosas en Canadá y Estados Unidos está creando una necesidad urgente de soluciones de diagnóstico rápidas y descentralizadas que permitan la detección oportuna y el manejo eficaz de las enfermedades.
- Los proveedores de atención médica y los formuladores de políticas tanto en Canadá como en los EE. UU. reconocen cada vez más el valor del POCT para abordar la creciente carga de enfermedades, especialmente en centros de salud comunitarios, entornos de atención de urgencia y regiones remotas donde el acceso a laboratorios centralizados es limitado.
- Por ejemplo, en mayo de 2025, Renyun (Hunan) Busbar Co., Ltd. recibió recientemente a un valioso cliente en su sede, lo que marcó otro hito en el compromiso de la empresa de forjar alianzas sólidas y duraderas. La visita incluyó una visita guiada a las modernas instalaciones de fabricación de Renyun, donde el cliente observó procesos de producción avanzados, rigurosas pruebas de calidad y diseños de productos innovadores.
- En los centros de datos, donde la disponibilidad es fundamental, se están integrando las pruebas de punto de atención en Canadá y EE. UU. para ofrecer un suministro de energía optimizado y reconfigurable, lo que permite a los operadores escalar la infraestructura sin tiempos de inactividad prolongados. Su tecnología plug-and-play ha sido valorada por permitir conexiones rápidas de alimentación a rack y soportar cambios dinámicos de carga, necesidades que se han vuelto comunes tanto en escenarios de hiperescala como de computación en el borde.
- Los programas de desarrollo energético del Banco Mundial destacan aún más la vinculación de la electrificación con el crecimiento industrial sostenible en las economías emergentes. En las zonas industriales inteligentes y los corredores de infraestructura impulsados por el gobierno, las pruebas en el punto de atención de Canadá y Estados Unidos se están considerando como parte de las estrategias de distribución de baja tensión, especialmente donde se requiere velocidad, flexibilidad y seguridad a largo plazo.
Dinámica del mercado de pruebas en el punto de atención de Canadá y EE. UU.
Conductor
Infraestructura de atención médica avanzada y sólida adopción de dispositivos móviles y portátiles en Canadá y Estados Unidos
- Una de las tendencias clave que impulsa el mercado de pruebas en el punto de atención de Canadá y Estados Unidos son los flujos de trabajo de diagnóstico rápido, el intercambio de datos en tiempo real y la toma de decisiones clínicas optimizada, que en conjunto mejoran los resultados de los pacientes.
- Junto con esta infraestructura, la fuerte adopción por parte de los consumidores de tecnologías sanitarias móviles y portátiles en Canadá y Estados Unidos está impulsando la demanda de dispositivos POCT conectados y fáciles de usar.
- Por ejemplo, en agosto de 2025, Canada Health Infoway lanzó la Beca para Estudiantes Clínicos de Atención Conectada, que ofrece hasta 3000 USD por estudiante para apoyar a los estudiantes clínicos que cursan programas de educación en salud digital en instituciones postsecundarias canadienses acreditadas.
- Esta iniciativa, parte del Centro de Innovación Clínica en Salud Digital (CIDH), busca impulsar la interoperabilidad y la atención conectada, dotando a los estudiantes de conocimientos en áreas como la historia clínica electrónica, la inteligencia artificial aplicada a la atención médica y el análisis de datos sanitarios. La beca se alinea con la Hoja de Ruta de Interoperabilidad Pancanadiense Compartida de Infoway y apoya el desarrollo de capacidades de diagnóstico descentralizadas y soluciones de salud digital.
- Los wearables y las aplicaciones móviles de salud permiten a los pacientes monitorear su salud de forma continua, creando un entorno rico en datos que las soluciones POCT pueden aprovechar para brindar diagnósticos oportunos y personalizados.
- La convergencia de estas tecnologías facilita la monitorización remota de pacientes, el manejo de enfermedades crónicas y la atención preventiva, reduciendo las visitas hospitalarias y aliviando la carga de los sistemas de salud. A medida que la adopción de dispositivos móviles y wearables continúa creciendo, impulsará cada vez más la expansión y aceptación de la POCT como un componente clave de la atención médica moderna.
Oportunidad
El aumento del uso en el análisis de drogas, enfermedades infecciosas y oncología impulsa la diversificación del mercado.
- El panorama de la atención médica en Canadá y Estados Unidos está experimentando una transformación significativa, impulsada por la creciente adopción de las pruebas en el punto de atención (POCT). Este cambio es particularmente evidente en la diversificación de sus aplicaciones, que van más allá del diagnóstico tradicional hacia nuevas áreas de alto crecimiento.
- La expansión de la POCT a campos como el abuso de drogas, las enfermedades infecciosas y el cribado oncológico está creando un nuevo paradigma para la atención oportuna y accesible al paciente. Esta evolución está impulsada por la demanda de resultados más rápidos, lo que puede conducir a decisiones terapéuticas más rápidas y a mejores resultados para los pacientes.
- Por ejemplo, en agosto de 2025, según la Agencia de Medicamentos de Canadá y Estados Unidos, el inicio de la pandemia de COVID-19 impulsó una adopción sustancial de POCT, lo que generó una mayor conciencia de cómo se pueden aplicar estas pruebas en diferentes aspectos de la medicina, con ejemplos que incluyen pruebas de diagnóstico rápido del VIH y pruebas basadas en biomarcadores para lesiones cerebrales traumáticas leves.
- La capacidad de realizar estas pruebas fuera de un laboratorio centralizado, como en clínicas, farmacias e incluso en ubicaciones remotas, es un factor clave de esta tendencia. A medida que la tecnología se vuelve más sofisticada y fácil de usar, la gama de afecciones que se pueden detectar en el punto de atención continúa creciendo, lo que ofrece nuevas oportunidades tanto para los profesionales de la salud como para los pacientes. Esta diversificación no solo aborda los desafíos de larga data en el acceso a la atención médica, sino que también promete optimizar los flujos de trabajo clínicos y reducir la carga sobre la infraestructura de laboratorio tradicional.
- El panorama de las pruebas POCT en EE. UU. está adoptando cada vez más diversas aplicaciones de cribado, desde paneles de drogas de abuso hasta la detección de enfermedades infecciosas y biomarcadores oncológicos, lo que amplía su impacto en todos los ámbitos de la salud. Por ejemplo, las pruebas domiciliarias de enfermedades infecciosas, como los kits de antígenos del SARS-CoV-2, han demostrado un ahorro sustancial de aproximadamente 12,5 millones de dólares en 60 días, lo que pone de relieve la demanda de pruebas descentralizadas. Simultáneamente, los avances en el diagnóstico oncológico, como los análisis de sangre mejorados con aprendizaje automático capaces de detectar el cáncer de ovario en fase temprana con una precisión cercana al 92 %, auguran una expansión similar en el cribado del cáncer mediante pruebas POCT.
Restricción/Desafío
Costos elevados de dispositivos y reactivos POCT avanzados
- La adopción de dispositivos avanzados de pruebas en el punto de atención (POCT) en Canadá y Estados Unidos suele verse obstaculizada por los elevados costos que conllevan. Estas tecnologías suelen contar con componentes sofisticados y requerir reactivos especializados, lo que conlleva mayores gastos de fabricación y adquisición.
- Los gastos recurrentes relacionados con consumibles, mantenimiento y calibración de dispositivos incrementan aún más la carga financiera general. En muchos casos, las organizaciones sanitarias deben evaluar cuidadosamente la relación coste-beneficio antes de invertir en sistemas POCT avanzados, lo que puede provocar un retraso en la adopción o un uso selectivo de estas tecnologías.
- Por ejemplo, en junio de 2025, un estudio publicado en Applied Sciences exploró la integración de las pruebas en el punto de atención (POCT) para el manejo del cáncer y enfermedades crónicas en entornos laborales. El estudio destacó que la variabilidad en el rendimiento y la calidad entre los diferentes dispositivos POCT de diversos fabricantes plantea importantes desafíos para los esfuerzos de estandarización.
- Esta inconsistencia complica el establecimiento de protocolos de prueba uniformes y medidas de garantía de calidad, lo que dificulta su adopción clínica y su integración en las prácticas sanitarias habituales. La falta de dispositivos y procedimientos estandarizados puede generar discrepancias en los resultados de las pruebas, lo que afecta a la atención al paciente y dificulta la implementación generalizada de soluciones POCT.
- Abordar esta limitación de costos será crucial para el crecimiento del mercado. Podría requerir innovaciones para reducir los costos de producción, economías de escala y posible apoyo financiero del gobierno o del sector privado para mejorar la asequibilidad y la accesibilidad en diversos entornos de atención médica.
- Los altos costos asociados con los dispositivos y reactivos POCT avanzados siguen siendo un obstáculo importante para su adopción generalizada en Canadá y Estados Unidos. Superar este desafío financiero mediante estrategias de reducción de costos, mayor eficiencia productiva y mecanismos de financiación de apoyo será esencial para que estas tecnologías sean más accesibles en diversos entornos sanitarios e impulsar el crecimiento del mercado.
Alcance del mercado de pruebas en el punto de atención de Canadá y EE. UU.
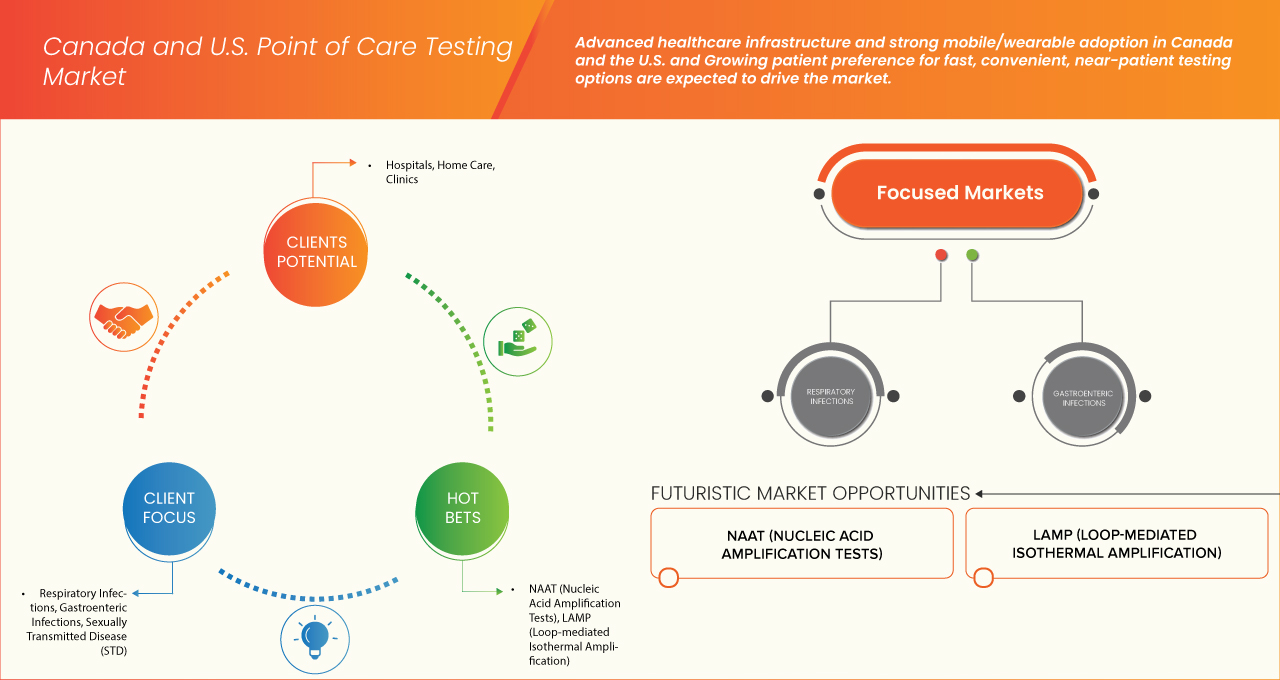
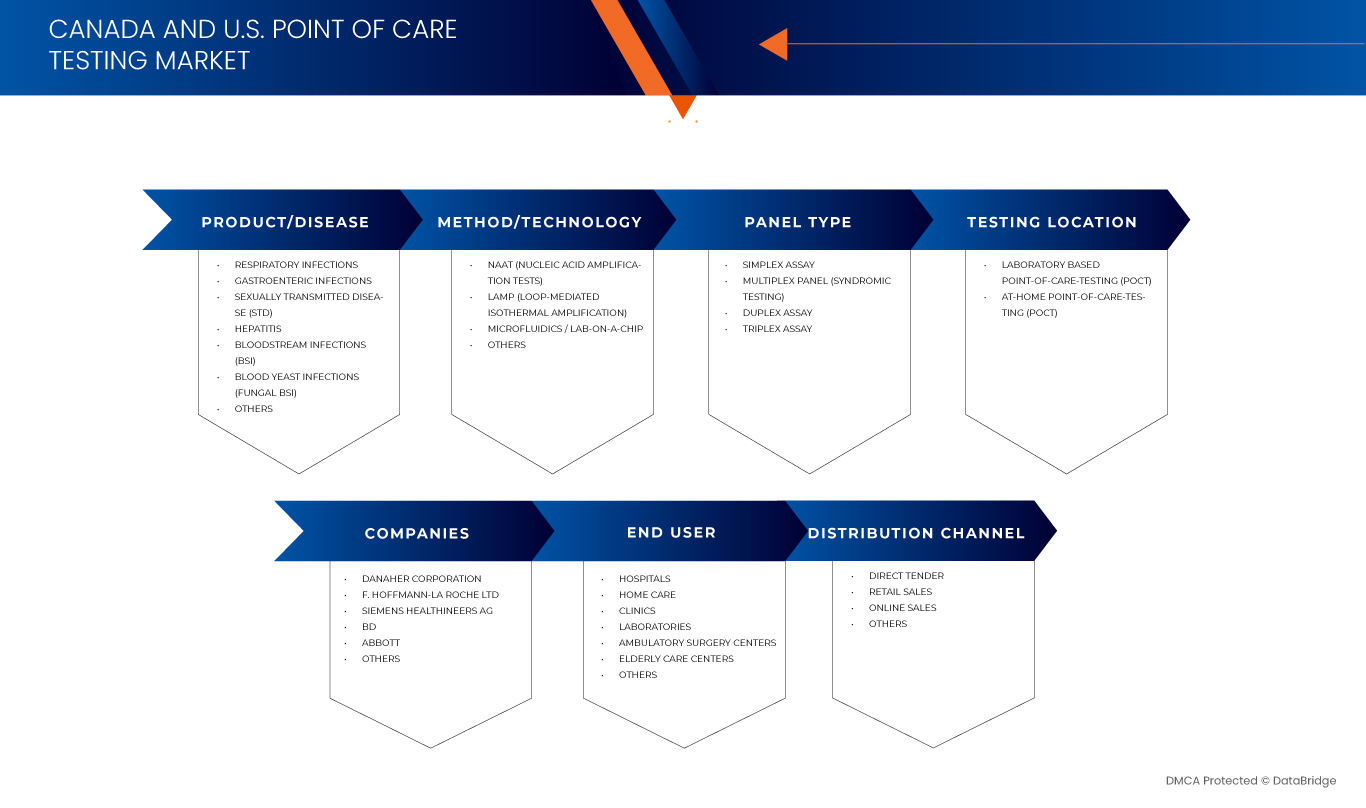
El mercado de pruebas en el punto de atención de Canadá y Estados Unidos está segmentado en seis segmentos según el producto/enfermedad, el método/tecnología, el tipo de panel, la ubicación de la prueba, el usuario final y el canal de distribución.
- Por producto/enfermedad
En función del producto o la enfermedad, el mercado de pruebas en el punto de atención en Canadá y EE. UU. se segmenta en infecciones respiratorias, infecciones gastrointestinales, enfermedades de transmisión sexual (ETS), hepatitis, infecciones del torrente sanguíneo (ITS), infecciones por hongos en la sangre (ITS) y otras. En 2025, se prevé que el segmento de infecciones respiratorias domine el mercado con una cuota de mercado del 48,15 % y el 34,50 % en EE. UU. y Canadá, respectivamente, debido a su alta prevalencia, rápida transmisión y la necesidad clínica de un diagnóstico oportuno. La pandemia de COVID-19 demostró la importancia crucial de las pruebas moleculares descentralizadas y rápidas, lo que aceleró significativamente la inversión en plataformas de diagnóstico en el punto de atención.
Se prevé que el segmento de enfermedades de transmisión sexual (ETS) gane impulso con una CAGR del 10,1 % en los EE. UU. y del 9,4 % en Canadá durante el período de pronóstico de 2025 a 2032, impulsado por la creciente prevalencia de ETS, la creciente demanda de pruebas rápidas y confidenciales, las innovaciones continuas de productos y la creciente adopción de soluciones de diagnóstico en el punto de atención en el hogar y en la clínica.
- Por método/tecnología
En función del método y la tecnología, el mercado de pruebas en el punto de atención de Canadá y EE. UU. se segmenta en NAAT (Pruebas de Amplificación de Ácidos Nucleicos), LAMP (Amplificación Isotermal Mediada por Asa), microfluídica/laboratorio en un chip, entre otros. En 2025, se espera que el segmento NAAT (Pruebas de Amplificación de Ácidos Nucleicos) domine el mercado con una cuota de mercado del 55,27 % y el 55,58 % en EE. UU. y Canadá, respectivamente, debido a que las pruebas rápidas basadas en PCR se han vuelto esenciales para el cribado a gran escala y la toma de decisiones clínicas rápidas. Más allá de la COVID-19, las NAAT se utilizan cada vez más para detectar patógenos respiratorios, infecciones de transmisión sexual (ITS), infecciones gastrointestinales e infecciones del torrente sanguíneo, lo que permite un diagnóstico más rápido en comparación con las pruebas PCR de laboratorio convencionales.
Se prevé que el segmento LAMP (amplificación isotérmica mediada por bucle) gane impulso con una CAGR del 10,2 % en los EE. UU. y del 9,5 % en Canadá durante el período de pronóstico de 2025 a 2032, impulsado por su alta sensibilidad y capacidades de detección rápida, la creciente adopción en el diagnóstico de enfermedades infecciosas, las innovaciones continuas de productos y la creciente demanda de soluciones de pruebas moleculares rentables en entornos clínicos y de atención domiciliaria.
- Por tipo de panel
Según el tipo de panel, el mercado de pruebas en el punto de atención de Canadá y EE. UU. se segmenta en ensayos simplex, paneles multiplex (pruebas sindrómicas), ensayos dúplex y ensayos tríplex. En 2025, se proyecta que el segmento de ensayos simplex domine el mercado con una participación del 52,50 % y el 52,38 % en EE. UU. y Canadá, respectivamente, gracias a su rentabilidad, facilidad de uso y amplia adopción en aplicaciones de diagnóstico rutinario. Estos ensayos están diseñados para detectar un solo analito o patógeno por prueba, lo que los hace especialmente adecuados para necesidades de alto volumen, como la monitorización de la glucemia, las pruebas de embarazo y fertilidad, el cribado de enfermedades infecciosas (como las pruebas rápidas de antígenos del VIH y la COVID-19) y los marcadores cardíacos.
Se prevé que el segmento de paneles multiplex (pruebas sindrómicas) gane impulso con una CAGR del 10,1 % en los EE. UU. y del 9,3 % en Canadá durante el período de pronóstico de 2025 a 2032, impulsado por la creciente demanda de soluciones de diagnóstico rápidas e integrales, innovaciones continuas de productos, creciente adopción en entornos clínicos y cercanos al paciente, y la necesidad de una detección precisa de múltiples patógenos en una sola prueba.
- Por ubicación de prueba
Según la ubicación de las pruebas, el mercado de pruebas en el punto de atención de Canadá y EE. UU. se segmenta en pruebas en el punto de atención (POCT) en laboratorio y pruebas en el punto de atención (POCT) en el hogar. En 2025, se prevé que el segmento de pruebas en el punto de atención (POCT) en laboratorio domine el mercado con una cuota de mercado del 60,13 % y el 59,87 % en EE. UU. y Canadá, respectivamente, gracias a su mayor precisión, fiabilidad e integración en los flujos de trabajo hospitalarios y clínicos, en comparación con las pruebas en el hogar. Estas pruebas se realizan habitualmente en centros sanitarios como hospitales, laboratorios de diagnóstico y centros de urgencias, donde profesionales cualificados pueden garantizar la correcta manipulación de las muestras, el control de calidad y la interpretación de los resultados.
Se prevé que el segmento de pruebas de diagnóstico en el hogar (POCT) gane impulso con una CAGR del 9,9 % en EE. UU. y del 9,2 % en Canadá durante el período de pronóstico de 2025 a 2032, impulsado por la creciente adopción de kits de autoevaluación, las crecientes innovaciones de productos, una mayor disponibilidad a través de canales en línea y minoristas, y la creciente preferencia de los pacientes por soluciones de diagnóstico convenientes y rápidas.
- Por el usuario final
En función del usuario final, el mercado de pruebas en el punto de atención de Canadá y EE. UU. se segmenta en hospitales, atención domiciliaria, clínicas, laboratorios, centros de cirugía ambulatoria, centros de atención a personas mayores y otros. En 2025, se espera que el segmento de hospitales tenga la mayor participación, con un 42,86 % y un 43,28 % en EE. UU. y Canadá, respectivamente, debido al alto volumen de pacientes, la infraestructura avanzada y la sólida integración de diagnósticos rápidos en los flujos de trabajo clínicos. Las pruebas en el punto de atención (POCT) se adoptan ampliamente en entornos hospitalarios para atención de urgencias, unidades de cuidados intensivos, quirófanos y monitorización de pacientes hospitalizados, donde la obtención de resultados oportunos es fundamental para las decisiones de tratamiento. Los hospitales también utilizan una amplia gama de aplicaciones POCT, como la monitorización de la glucemia, las pruebas de marcadores cardíacos, las pruebas de coagulación y el diagnóstico de enfermedades infecciosas, en particular los paneles sindrómicos para infecciones respiratorias y del torrente sanguíneo.
Se prevé que el segmento de atención domiciliaria gane impulso con una CAGR del 10,1 % en los EE. UU., mientras que se espera que el segmento hospitalario crezca a una CAGR del 9,6 % en Canadá durante el período de pronóstico de 2025 a 2032, impulsado por la creciente demanda de diagnósticos rápidos, la creciente disponibilidad de dispositivos POCT innovadores, la preferencia de los pacientes por la monitorización en el hogar y la creciente necesidad de una toma de decisiones más rápida en entornos clínicos.
- Por canal de distribución
Según el canal de distribución, el mercado de pruebas en el punto de atención de Canadá y Estados Unidos se segmenta en licitación directa, venta minorista, venta en línea y otros. En 2025, se prevé que el segmento de licitación directa domine el mercado con una cuota de mercado del 44,13 % y el 43,74 % en Estados Unidos y Canadá, respectivamente, debido a que este es el principal método de adquisición para instituciones sanitarias de gran escala, como hospitales, laboratorios de diagnóstico y centros sanitarios financiados por el gobierno. Mediante licitaciones directas, se establecen acuerdos de compra a granel entre proveedores de servicios sanitarios y fabricantes o distribuidores autorizados, lo que garantiza menores costes unitarios, un suministro estable y una disponibilidad estandarizada de productos.
Se prevé que el segmento de ventas en línea en el mercado POCT gane tracción con una CAGR del 10,3 % en los EE. UU. y del 9,6 % en Canadá durante el período de pronóstico de 2025 a 2032, impulsado por la creciente adopción de plataformas de salud digital, la creciente disponibilidad de dispositivos de diagnóstico a través de canales de comercio electrónico, la creciente preferencia de los pacientes por las pruebas en el hogar y la conveniencia de los modelos de entrega directa al consumidor.
Los principales líderes del mercado que operan en el mercado son:
- Corporación Danaher (EE. UU.)
- F. Hoffmann-La Roche Ltd (Suiza)
- Siemens Healthineers AG (Alemania)
- BD (Becton, Dickinson and Company) (EE. UU.)
- Laboratorios Abbott (EE. UU.)
- Cardinal Health (EE. UU.)
- Agilent Technologies, Inc. (EE. UU.)
- Medline Industries, LP (EE. UU.)
- Trinity Biotech (Irlanda)
- OraSure Technologies Inc (EE. UU.)
- Bio-Rad Laboratories, Inc. (EE. UU.)
- BIOMÉRIEUX (Francia)
- QIAGEN (Alemania)
- Thermo Fisher Scientific Inc. (EE. UU.)
- QuidelOrtho Corporation (EE. UU.)
- Trimedic Inc (Canadá)
- Abaxis, Inc. (EE. UU.)
- Corporación Sysmex (Japón)
- NIPRO (Japón)
- Diagnóstico SEKISUI (EE. UU.)
- SANNER (Alemania)
- Diagnóstico PTS (EE. UU.)
- The Stevens Company Limited (Canadá)
- QuantuMDx Group Ltd. (Reino Unido)
- EKF Diagnostics Holdings plc (Reino Unido)
- Diagnóstico creativo (EE. UU.)
- Hipro Biotechnology Co., Ltd. (China)
- Especialidades Hospitalarias Canadienses Limitada (Canadá)
- Radiometer Medical ApS (Dinamarca)
- Meridian Bioscience, Inc. (EE. UU.)
- Henry Schein, Inc. (EE. UU.)
- Nova Biomedical (EE. UU.)
- binx health, inc. (EE. UU.)
- Sanguina (EE. UU.)
Últimos avances en el mercado de pruebas en el punto de atención de Canadá y Estados Unidos
- En febrero de 2025, Thermo Fisher Scientific adquirió el negocio de Purificación y Filtración de Solventum por 4.100 millones de dólares, reforzando así sus capacidades de bioprocesamiento. Esta adquisición amplía la cartera de tecnologías de filtración y purificación de Thermo Fisher, que utilizan técnicas avanzadas de análisis de superficies para optimizar las interacciones de materiales en aplicaciones tanto biológicas como industriales.
- En julio de 2025, OraSure, a través de su filial DNA Genotek, lanzó el tubo de extracción de sangre HEMAcollect PROTEIN, un nuevo dispositivo para la investigación proteómica. Se trata de un tubo de vacío con un líquido estabilizador patentado, diseñado para preservar y estabilizar las proteínas plasmáticas en sangre completa hasta siete días a temperatura ambiente. Esto elimina la necesidad de procesamiento inmediato o envío en cadena de frío, lo que hace que la extracción y el transporte de muestras sean más eficientes y rentables. Impulsado por la tecnología ProteoPrecision, minimiza la hemólisis y la activación plaquetaria, garantizando que la muestra obtenida refleje con precisión el estado in vivo del organismo, lo que genera datos de investigación de mayor calidad para aplicaciones en oncología, neurología y cardiología.
- En julio de 2025, según la revista Time, el sistema MAI DxO de Microsoft demostró una precisión diagnóstica significativamente mayor que la de los médicos humanos (alrededor del 85 % frente al 20 %) y redujo los costos de las pruebas a los pacientes en un 20 %.
- En agosto de 2025, según Reuters, un equipo con sede en EE. UU. desarrolló una prueba de sangre habilitada con IA que detecta el cáncer de ovario en etapa temprana con más del 90% de precisión, abriendo nuevas vías para el diagnóstico POC en oncología.
- En agosto de 2025, según un informe del Centro Colaborador Nacional para Enfermedades Infecciosas, el POCT puede proporcionar pruebas accesibles para personas que enfrentan barreras a los servicios convencionales, mejorando el acceso en áreas remotas o con recursos limitados.
SKU-
Obtenga acceso en línea al informe sobre la primera nube de inteligencia de mercado del mundo
- Panel de análisis de datos interactivo
- Panel de análisis de empresas para oportunidades con alto potencial de crecimiento
- Acceso de analista de investigación para personalización y consultas
- Análisis de la competencia con panel interactivo
- Últimas noticias, actualizaciones y análisis de tendencias
- Aproveche el poder del análisis de referencia para un seguimiento integral de la competencia
Tabla de contenido
1 INTRODUCCIÓN
1.1 OBJETIVOS DEL ESTUDIO
1.2 DEFINICIÓN DE MERCADO
1.3 RESUMEN
1.4 MONEDA Y PRECIOS
1.5 LIMITACIONES
1.6 MERCADOS CUBIERTOS
2 SEGMENTACIÓN DEL MERCADO
2.1 MERCADOS CUBIERTOS
2.2 ÁMBITO GEOGRÁFICO
2,3 AÑOS CONSIDERADOS PARA EL ESTUDIO
2.4 MODELO DE VALIDACIÓN DE DATOS TRÍPODE DBMR
2.5 MODELADO MULTIVARIADO
2.6 ENTREVISTAS PRINCIPALES CON LÍDERES DE OPINIÓN CLAVE
2.7 CUADRÍCULA DE POSICIÓN DE MERCADO DBMR
2.8 ANÁLISIS DE LA PARTICIPACIÓN DE LOS PROVEEDORES
2.9 CUADRÍCULA DE COBERTURA DEL USUARIO FINAL DEL MERCADO
2.1 FUENTES SECUNDARIAS
2.11 SUPUESTOS
3 RESUMEN EJECUTIVO
4 INFORMACIÓN PREMIUM
4.1 LAS CINCO FUERZAS DE PORTER
4.2 ANÁLISIS PESTEL
4.2.1 FACTORES POLÍTICOS
4.2.2 FACTORES ECONÓMICOS
4.2.3 FACTORES SOCIALES
4.2.4 FACTORES TECNOLÓGICOS
4.2.5 FACTORES AMBIENTALES
4.2.6 FACTORES LEGALES
4.3 ANÁLISIS DE I+D
4.3.1 ANÁLISIS COMPARATIVO
4.3.2 PANORAMA DEL DESARROLLO DE MEDICAMENTOS
4.3.3 INFORMACIÓN PROFUNDA SOBRE LOS HITOS REGULATORIOS
4.3.4 EVALUACIÓN TERAPÉUTICA
4.3.5 COLABORACIONES Y ASOCIACIONES BASADAS EN ACTIVOS
4.4 ANÁLISIS DEL IMPACTO DE LAS TARIFAS DE ATENCIÓN MÉDICA
4.4.1 DESCRIPCIÓN GENERAL
4.4.2 ESTRUCTURAS TARIFARIAS
4.4.2.1 ESTRUCTURAS ARANCELARIAS GLOBALES VS. REGIONALES
4.4.3 ARANCELES FARMACÉUTICOS Y BARRERAS COMERCIALES
4.4.3.1 DERECHOS DE IMPORTACIÓN DE MEDICAMENTOS CON RECETA VS. GENÉRICOS
4.4.3.2 IMPACTO EN LA ASEQUIBILIDAD Y EL ACCESO A LOS MEDICAMENTOS
4.4.3.3 ACUERDOS COMERCIALES CLAVE QUE AFECTAN A LOS ARANCELES
4.4.4 IMPACTO DE LAS TARIFAS EN LOS PROVEEDORES Y PACIENTES
4.4.4.1 CARGA COSTUMBRES SOBRE HOSPITALES Y CENTROS DE SALUD
4.4.4.2 EFECTO EN LA ASEQUIBILIDAD DEL PACIENTE Y LA COBERTURA DEL SEGURO
4.4.4.3 TARIFAS Y TURISMO MÉDICO
4.4.5 ACUERDOS COMERCIALES Y ARANCELES DE ATENCIÓN SANITARIA
4.4.5.1 REGLAMENTOS DE LA OMC
4.4.5.2 IMPACTO DE LAS GUERRAS COMERCIALES EN LA CADENA DE SUMINISTRO DE ATENCIÓN MÉDICA
4.4.5.3 EL PAPEL DE LOS TRATADOS DE LIBRE COMERCIO (TLC) EN LA REDUCCIÓN DE ARANCELES
4.4.6 IMPACTO DE LAS TARIFAS EN LOS COSTOS Y LA ACCESIBILIDAD DE LA ATENCIÓN SANITARIA
4.4.7 IMPORTANCIA DE LAS TARIFAS EN EL SECTOR DE LA SALUD
4.5 ANÁLISIS DE PATENTES-
4.6 ANÁLISIS DE MEDICAMENTOS COMERCIALIZADOS
4.6.1 PRONÓSTICO DEL MERCADO A 10 AÑOS
4.6.2 DROGAS
4.6.3 MEDICAMENTOS DE MARCA
4.6.4 MEDICAMENTOS GENÉRICOS
4.6.5 INDICACIÓN TERAPÉUTICA
4.6.6 CLASE FARMACOLÓGICA DEL MEDICAMENTO
4.6.7 INDICACIÓN PRINCIPAL DEL MEDICAMENTO
4.6.8 ESTADO DEL MERCADO
4.6.9 TIPO DE MEDICACIÓN
4.6.10 FORMA FARMACÉUTICA DEL MEDICAMENTO
4.6.11 DISPONIBILIDAD DE DOSIS
4.6.12 TIPO DE EMBALAJE
4.6.13 VÍA DE ADMINISTRACIÓN DEL MEDICAMENTO
4.6.14 FRECUENCIA DE DOSIFICACIÓN
4.6.15 INFORMACIÓN SOBRE MEDICAMENTOS
4.6.16 UNA VISIÓN GENERAL DE LAS ACTIVIDADES DE DESARROLLO DE MEDICAMENTOS
4.6.17 HITO REGULATORIO, DATOS DE SEGURIDAD Y DATOS DE EFICACIA
4.6.18 DATOS DE EXCLUSIVIDAD DE MERCADO
4.6.19 PRONÓSTICO DE PERSPECTIVAS DEL MERCADO
4.6.20 COMPETICIÓN CRUZADA
4.6.21 PORTAFOLIO TERAPÉUTICO
4.6.22 ESCENARIO DE DESARROLLO ACTUAL
4.7 ACCESO AL MERCADO
4.7.1 PRONÓSTICO DEL MERCADO A 10 AÑOS
4.7.2 ACTUALIZACIONES RECIENTES DE ENSAYOS CLÍNICOS
4.7.3 NUEVOS MEDICAMENTOS ANUALES APROBADOS POR LA FDA
4.7.4 FABRICANTE DE MEDICAMENTOS Y NEGOCIOS
4.7.5 CONSUMO DE MEDICAMENTOS PRINCIPALES
4.7.6 PRÁCTICAS DE TRATAMIENTO ACTUALES
4.7.7 IMPACTO DE LA PRÓXIMA TERAPIA
4.8 EPIDEMOLOGÍA
4.8.1 INCIDENCIA POR GÉNERO: CONDICIONES RELEVANTES PARA EL PUNTO DE VISTA
4.8.2 TASA DE TRATAMIENTO: IMPACTO EN EL POCT
4.8.3 TASA DE MORTALIDAD: LA NECESIDAD DE UN DIAGNÓSTICO TEMPRANO
4.8.4 ADHERENCIA A LOS MEDICAMENTOS Y CAMBIO DE TERAPIA: EL PAPEL DEL POCT EN LA GESTIÓN
4.8.5 TASAS DE ÉXITO DEL TRATAMIENTO DEL PACIENTE: LA VENTAJA DEL POCT
4.9 ECOSISTEMA DE LA CADENA DE SUMINISTRO
4.9.1 EMPRESAS DESTACADAS
4.9.2 COMPONENTES CLAVE DEL ECOSISTEMA:
4.9.3 PEQUEÑAS Y MEDIANAS EMPRESAS (INNOVADORAS)
4.9.4 USUARIOS FINALES
4.1 SEGUIMIENTO DE INNOVACIÓN Y ANÁLISIS ESTRATÉGICO
4.10.1 ANÁLISIS DE GRANDES ACUERDOS Y ALIANZAS ESTRATÉGICAS
4.10.1.1 EMPRESAS CONJUNTAS
4.10.1.2 FUSIONES Y ADQUISICIONES
4.10.1.3 LICENCIAS Y ASOCIACIONES
4.10.1.4 COLABORACIONES TECNOLÓGICAS
4.10.1.5 DESINVERSIONES ESTRATÉGICAS
4.10.2 NÚMERO DE PRODUCTOS EN DESARROLLO
4.10.3 ETAPA DE DESARROLLO
4.10.4 CRONOGRAMAS E HITOS
4.10.5 ESTRATEGIAS Y METODOLOGÍAS DE INNOVACIÓN
4.10.6 EVALUACIÓN Y MITIGACIÓN DE RIESGOS
4.10.7 PERSPECTIVAS FUTURAS
4.11 ANÁLISIS DE CADUCIDAD – MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE CANADÁ Y EE. UU.
4.11.1 ENSAYOS CLÍNICOS Y ANÁLISIS DE FASE
4.11.2 LÍNEA DE TECNOLOGÍA
4.11.3 CANDIDATOS DE LA FASE III
4.11.4 CANDIDATOS DE LA FASE II
4.11.5 CANDIDATOS DE LA FASE I
4.11.6 OTROS (PRECLÍNICOS Y DE INVESTIGACIÓN)
4.11.7 CONCLUSIÓN
5 COBERTURA REGLAMENTARIA
6 PANORAMA GENERAL DEL MERCADO
6.1 CONDUCTORES
6.1.1 AUMENTO DE LA PREVALENCIA DE ENFERMEDADES CRÓNICAS E INFECCIOSAS CRECIENTE DEMANDA DE DIAGNÓSTICOS RÁPIDOS Y DESCENTRALIZADOS
6.1.2 INFRAESTRUCTURA AVANZADA DE ATENCIÓN MÉDICA Y FUERTE ADOPCIÓN DE DISPOSITIVOS MÓVILES Y VESTIBLES EN CANADÁ Y ESTADOS UNIDOS
6.1.3 CRECIENTE PREFERENCIA DE LOS PACIENTES POR OPCIONES DE PRUEBAS RÁPIDAS, CÓMODAS Y CERCA DEL PACIENTE
6.1.4 AUMENTAR LAS INICIATIVAS Y LA FINANCIACIÓN GUBERNAMENTALES PARA APOYAR LA SALUD DIGITAL Y EL DIAGNÓSTICO DESCENTRALIZADO
6.2 RESTRICCIONES
6.2.1 COSTOS ALTOS DE LOS DISPOSITIVOS Y REACTIVOS POCT AVANZADOS
6.2.2 VARIABILIDAD EN EL RENDIMIENTO Y LA CALIDAD DE LOS DISPOSITIVOS ENTRE MARCAS, LO QUE COMPLICA LA ESTANDARIZACIÓN Y LA ADOPCIÓN CLÍNICA
6.3 OPORTUNIDADES
6.3.1 AUMENTO DEL USO EN LA DETECCIÓN DEL ABUSO DE DROGAS, ENFERMEDADES INFECCIOSAS Y ONCOLOGÍA, LO QUE IMPULSA LA DIVERSIFICACIÓN DEL MERCADO
6.3.2 AMPLIACIÓN DEL USO DE PUNTOS MOLECULARES Y DE INMUNOENSAYOS DE FLUJO LATERAL, INCLUYENDO FARMACIAS Y ATENCIÓN REMOTA/RURAL
6.3.3 INTEGRACIÓN DE INTELIGENCIA ARTIFICIAL Y APRENDIZAJE AUTOMÁTICO PARA MEJORAR LA PRECISIÓN DIAGNÓSTICA Y EL APOYO A LA TOMA DE DECISIONES CLÍNICAS
6.4 DESAFÍOS
6.4.1 MANTENER LA PRECISIÓN, LA CONFIABILIDAD Y EL CUMPLIMIENTO DE LA NORMATIVA EN ENTORNOS DE PRUEBAS DESCENTRALIZADOS
6.4.2 ABORDAR LOS RIESGOS DE PRIVACIDAD DE DATOS Y CIBERSEGURIDAD A MEDIDA QUE MÁS DISPOSITIVOS PUNTO DE VISTA SE CONECTAN A LAS REDES DE SALUD
7 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE CANADÁ Y EE. UU., POR PRODUCTO/ENFERMEDAD
7.1 DESCRIPCIÓN GENERAL
7.2 INFECCIÓN RESPIRATORIA
7.2.1 SARS-COV-2
7.2.2 GRIPE A/B
7.2.3 VIRUS RESPIRATORIO SINCICIAL (VSR)
7.2.4 BORDETELLA PERTUSSIS
7.2.5 OTROS
7.3 INFECCIONES GASTROENTÉRICAS
7.3.1 CLOSTRIDIOIDES DIFÍCIL
7.3.2 NOROVIRUS
7.3.3 ROTAVIRUS
7.3.4 SALMONELLA, SHIGELLA, CAMPYLOBACTER, E. COLI (STEC)
7.3.5 GIARDIA
7.4 ENFERMEDADES DE TRANSMISIÓN SEXUAL (ETS)
7.5 HEPATITIS
7.6 INFECCIONES DEL TORRENTE SANGUÍNEO (BSI)
7.7 INFECCIONES POR LEVADURAS EN LA SANGRE (BSI POR HONGOS)
7.8 OTROS
8. MERCADO DE PRUEBAS DE ATENCIÓN MÉDICA EN CANADÁ Y EE. UU., POR MÉTODO/TECNOLOGÍA
8.1 DESCRIPCIÓN GENERAL
8.2 NAAT (PRUEBAS DE AMPLIFICACIÓN DE ÁCIDOS NUCLEICOS)
8.3 LÁMPARA (Amplificación isotérmica mediada por bucle)
8.4 MICROFLUÍDICOS / LABORATORIO EN UN CHIP
8.5 OTROS
9 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE CANADÁ Y EE. UU., POR TIPO DE PANEL
9.1 DESCRIPCIÓN GENERAL
9.2 ENSAYO SIMPLEX
9.3 PANEL MULTIPLEX (PRUEBAS SINDRÓMICAS)
9.4 ENSAYO DÚPLEX
9.5 ENSAYO TRIPLEX
10 MERCADO DE PRUEBAS EN PUNTOS DE ATENCIÓN DE CANADÁ Y EE. UU., POR UBICACIÓN DE PRUEBAS
10.1 DESCRIPCIÓN GENERAL
10.2 PRUEBAS DE PUNTO DE ATENCIÓN (POCT) BASADAS EN LABORATORIO
10.3 PRUEBAS DE PUNTO DE ATENCIÓN EN EL HOGAR (POCT)
11 MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE CANADÁ Y EE. UU., POR USUARIO FINAL
11.1 DESCRIPCIÓN GENERAL
11.2 HOSPITALES
11.3 CUIDADO DOMICILIARIO
11.4 CLÍNICAS
11.5 LABORATORIOS
11.6 CENTROS DE CIRUGÍA AMBULATORIA
11.7 CENTROS DE CUIDADO DE PERSONAS MAYORES
11.8 OTROS
12 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE CANADÁ Y EE. UU., POR CANAL DE DISTRIBUCIÓN
12.1 DESCRIPCIÓN GENERAL
12.2 LICITACIÓN DIRECTA
12.3 VENTAS AL POR MENOR
12.4 VENTAS EN LÍNEA
12.5 OTROS
13 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE CANADÁ Y EE. UU.: PANORAMA DE LA EMPRESA
13.1 ANÁLISIS DE ACCIONES DE LA EMPRESA: EE. UU.
13.2 ANÁLISIS DE ACCIONES DE LA EMPRESA: CANADÁ
14 ANÁLISIS FODA
15 PERFIL DE LA EMPRESA
15.1 CORPORACIÓN DANAHER.
15.1.1 INSTANTÁNEA DE LA EMPRESA
15.1.2 ANÁLISIS DE INGRESOS
15.1.3 PORTAFOLIO DE PRODUCTOS
15.1.4 DESARROLLO RECIENTE
15.2 F. HOFFMANN-LA ROCHE LTD
15.2.1 INSTANTÁNEA DE LA EMPRESA
15.2.2 INFORMACIÓN FINANCIERA RECIENTE
15.2.3 PORTAFOLIO DE PRODUCTOS
15.2.4 DESARROLLOS RECIENTES
15.3 SIEMENS HEALTHINEERS AG
15.3.1 INSTANTÁNEA DE LA EMPRESA
15.3.2 INFORMACIÓN FINANCIERA RECIENTE
15.3.3 PORTAFOLIO DE PRODUCTOS
15.3.4 DESARROLLOS RECIENTES
15,4 BD
15.4.1 INSTANTÁNEA DE LA EMPRESA
15.4.2 INFORMACIÓN FINANCIERA RECIENTE
15.4.3 PORTAFOLIO DE PRODUCTOS
15.4.4 DESARROLLOS RECIENTES
15.5 ABBOTT
15.5.1 INSTANTÁNEA DE LA EMPRESA
15.5.2 ANÁLISIS DE INGRESOS
15.5.3 PORTAFOLIO DE PRODUCTOS
15.5.4 DESARROLLO RECIENTE
15.6 AGILENT TECHNOLOGIES INC.
15.6.1 INSTANTÁNEA DE LA EMPRESA
15.6.2 INFORMACIÓN FINANCIERA RECIENTE
15.6.3 PORTAFOLIO DE PRODUCTOS
15.6.4 DESARROLLOS RECIENTES
15.7 ABAXIS, INC.
15.7.1 INSTANTÁNEA DE LA EMPRESA
15.7.2 PORTAFOLIO DE PRODUCTOS
15.7.3 DESARROLLO RECIENTE
15.8 BINX SALUD, INC.
15.8.1 INSTANTÁNEA DE LA EMPRESA
15.8.2 PORTAFOLIO DE PRODUCTOS
15.8.3 DESARROLLO RECIENTE
15.9 BIOMERIEUX
15.9.1 INSTANTÁNEA DE LA EMPRESA
15.9.2 INFORMACIÓN FINANCIERA RECIENTE
15.9.3 PORTAFOLIO DE PRODUCTOS
15.9.4 DESARROLLO RECIENTE
15.1 LABORATORIOS BIO-RAD, INC.
15.10.1 INSTANTÁNEA DE LA EMPRESA
15.10.2 ANÁLISIS DE INGRESOS
15.10.3 PORTAFOLIO DE PRODUCTOS
15.10.4 DESARROLLO RECIENTE
15.11 DIAGNÓSTICOS CREATIVOS
15.11.1 INSTANTÁNEA DE LA EMPRESA
15.11.2 PORTAFOLIO DE PRODUCTOS
15.11.3 DESARROLLO RECIENTE
15.12 SALUD CARDENAL
15.12.1 INSTANTÁNEA DE LA EMPRESA
15.12.2 ANÁLISIS DE INGRESOS
15.12.3 PORTAFOLIO DE PRODUCTOS
15.12.4 DESARROLLO RECIENTE
15.13 ESPECIALIDADES HOSPITALARIAS CANADIENSES LIMITADAS
15.13.1 INSTANTÁNEA DE LA EMPRESA
15.13.2 PORTAFOLIO DE PRODUCTOS
15.13.3 DESARROLLO RECIENTE
15.14 EKF DIAGNÓSTICO HOLDINGS PLC.
15.14.1 INSTANTÁNEA DE LA EMPRESA
15.14.2 ANÁLISIS DE INGRESOS
15.14.3 PORTAFOLIO DE PRODUCTOS
15.14.4 DESARROLLO RECIENTE
15.15 HENRY SCHEIN, INC.
15.15.1 INSTANTÁNEA DE LA EMPRESA
15.15.2 ANÁLISIS DE INGRESOS
15.15.3 PORTAFOLIO DE PRODUCTOS
15.15.4 DESARROLLO RECIENTE
15.16 HIPRO BIOTECNOLOGÍA CO.,LTD.
15.16.1 INSTANTÁNEA DE LA EMPRESA
15.16.2 PORTAFOLIO DE PRODUCTOS
15.16.3 DESARROLLOS RECIENTES
15.17 MEDLINE INDUSTRIES, LP
15.17.1 INSTANTÁNEA DE LA EMPRESA
15.17.2 PORTAFOLIO DE PRODUCTOS
15.17.3 DESARROLLO RECIENTE
15.18 MERIDIAN BIOSCIENCE, INC
15.18.1 INSTANTÁNEA DE LA EMPRESA
15.18.2 PORTAFOLIO DE PRODUCTOS
15.18.3 DESARROLLO RECIENTE
15.19 NIPRO
15.19.1 INSTANTÁNEA DE LA EMPRESA
15.19.2 INFORMACIÓN FINANCIERA RECIENTE
15.19.3 PORTAFOLIO DE PRODUCTOS
15.19.4 ACONTECIMIENTOS RECIENTES
15.2 NOVA BIOMÉDICA
15.20.1 INSTANTÁNEA DE LA EMPRESA
15.20.2 PORTAFOLIO DE PRODUCTOS
15.20.3 DESARROLLO RECIENTE
15.21 ORASURE TECHNOLOGIES INC
15.21.1 INSTANTÁNEA DE LA EMPRESA
15.21.2 ANÁLISIS DE INGRESOS
15.21.3 PORTAFOLIO DE PRODUCTOS
15.21.4 DESARROLLO RECIENTE
15.22 PTS DIAGNÓSTICO
15.22.1 INSTANTÁNEA DE LA EMPRESA
15.22.2 PORTAFOLIO DE PRODUCTOS
15.22.3 DESARROLLO RECIENTE
15.23 QIAGEN
15.23.1 INSTANTÁNEA DE LA EMPRESA
15.23.2 ANÁLISIS DE INGRESOS
15.23.3 PORTAFOLIO DE PRODUCTOS
15.23.4 DESARROLLO RECIENTE
15.24 GRUPO QUANTUMDX LTD.
15.24.1 INSTANTÁNEA DE LA EMPRESA
15.24.2 PORTAFOLIO DE PRODUCTOS
15.24.3 DESARROLLO RECIENTE
15.25 CORPORACIÓN QUIDELORTHO.
15.25.1 INSTANTÁNEA DE LA EMPRESA
15.25.2 ANÁLISIS DE INGRESOS
15.25.3 PORTAFOLIO DE PRODUCTOS
15.25.4 ACONTECIMIENTOS RECIENTES
15.26 RADIÓMETRO MÉDICO APS
15.26.1 INSTANTÁNEA DE LA EMPRESA
15.26.2 PORTAFOLIO DE PRODUCTOS
15.26.3 ACTUALIZACIONES RECIENTES
15.27 SANNER
15.27.1 INSTANTÁNEA DE LA EMPRESA
15.27.2 PORTAFOLIO DE PRODUCTOS
15.27.3 DESARROLLO RECIENTE
15.28 DIAGNÓSTICO SEKISUI
15.28.1 INSTANTÁNEA DE LA EMPRESA
15.28.2 PORTAFOLIO DE PRODUCTOS
15.28.3 DESARROLLO RECIENTE
15.29 CORPORACIÓN SYSMEX
15.29.1 INSTANTÁNEA DE LA EMPRESA
15.29.2 ANÁLISIS DE INGRESOS
15.29.3 PORTAFOLIO DE PRODUCTOS
15.29.4 DESARROLLO RECIENTE
15.3 SANGRE
15.30.1 INSTANTÁNEA DE LA EMPRESA
15.30.2 PORTAFOLIO DE PRODUCTOS
15.30.3 ACONTECIMIENTOS RECIENTES
15.31 LA COMPAÑÍA STEVENS LIMITADA
15.31.1 INSTANTÁNEA DE LA EMPRESA
15.31.2 PORTAFOLIO DE PRODUCTOS
15.31.3 DESARROLLO RECIENTE
15.32 THERMO FISHER SCIENTIFIC INC.
15.32.1 INSTANTÁNEA DE LA EMPRESA
15.32.2 ANÁLISIS DE INGRESOS
15.32.3 PORTAFOLIO DE PRODUCTOS
15.32.4 DESARROLLO RECIENTE
15.33 TRIMEDIC INC
15.33.1 INSTANTÁNEA DE LA EMPRESA
15.33.2 PORTAFOLIO DE PRODUCTOS
15.33.3 DESARROLLO RECIENTE
15.34 BIOTECNOLOGÍA TRINITY
15.34.1 INSTANTÁNEA DE LA EMPRESA
15.34.2 ANÁLISIS DE INGRESOS
15.34.3 PORTAFOLIO DE PRODUCTOS
15.34.4 DESARROLLO RECIENTE
16 CUESTIONARIO
Lista de Tablas
TABLA 1 DISTRIBUCIÓN POR FASES
CUADRO 2 COBERTURA REGULATORIA
TABLA 3 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE EE. UU., POR PRODUCTO/ENFERMEDAD, 2018-2032 (MILES DE USD)
TABLA 4 MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE CANADÁ, POR PRODUCTO/ENFERMEDAD, 2018-2032 (MILES DE USD)
TABLA 5 INFECCIONES RESPIRATORIAS EN EL MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE EE. UU., POR TIPO, 2018-2032 (MILES DE USD)
TABLA 6 INFECCIONES RESPIRATORIAS EN EL MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE CANADÁ, POR TIPO, 2018-2032 (MILES DE USD)
TABLA 7 INFECCIONES GASTROENTÉRICAS EN EL MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE EE. UU., POR TIPO, 2018-2032 (MILES DE USD)
TABLA 8 INFECCIONES GASTROENTÉRICAS EN EL MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE CANADÁ, POR TIPO, 2018-2032 (MILES DE USD)
TABLA 9 MERCADO DE PRUEBAS DE ENFERMEDADES DE TRANSMISIÓN SEXUAL (ETS) EN EL PUNTO DE ATENCIÓN DE EE. UU., POR TIPO, 2018-2032 (MILES DE USD)
TABLA 10 MERCADO DE PRUEBAS DE ENFERMEDADES DE TRANSMISIÓN SEXUAL (ETS) EN EL PUNTO DE ATENCIÓN DE CANADÁ, POR TIPO, 2018-2032 (MILES DE USD)
TABLA 11 MERCADO DE PRUEBAS DE HEPATITIS EN EL PUNTO DE ATENCIÓN DE EE. UU., POR TIPO, 2018-2032 (MILES DE USD)
TABLA 12 MERCADO DE PRUEBAS DE HEPATITIS EN EL PUNTO DE ATENCIÓN DE CANADÁ, POR TIPO, 2018-2032 (MILES DE USD)
TABLA 13 INFECCIONES DEL TORRENTE SANGUÍNEO (BSI) EN EL MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE EE. UU., POR TIPO, 2018-2032 (MILES DE USD)
TABLA 14 INFECCIONES DEL TORRENTE SANGUÍNEO (BSI) EN EL MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE CANADÁ, POR TIPO, 2018-2032 (MILES DE USD)
TABLA 15 INFECCIONES POR LEVADURAS EN LA SANGRE (BSI POR HONGOS) EN EL MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN, POR TIPO, 2018-2032 (MILES DE USD)
TABLA 16 INFECCIONES POR LEVADURAS SANGUÍNEAS (BSI HÚNGICAS) EN EL MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE CANADÁ, POR TIPO, 2018-2032 (MILES DE USD)
TABLA 17 OTROS MERCADOS DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE EE. UU., POR TIPO, 2018-2032 (MILES DE USD)
TABLA 18 OTROS MERCADOS DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE CANADÁ, POR TIPO, 2018-2032 (MILES DE USD)
TABLA 19 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE EE. UU., POR MÉTODO/TECNOLOGÍA, 2018-2032 (MILES DE USD)
TABLA 20 MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE CANADÁ, POR MÉTODO/TECNOLOGÍA, 2018-2032 (MILES DE USD)
TABLA 21 NAAT (Pruebas de amplificación de ácidos nucleicos) de EE. UU. en el mercado de pruebas de punto de atención, por tipo, 2018-2032 (miles de USD)
TABLA 22 NAAT DE CANADÁ (PRUEBAS DE AMPLIFICACIÓN DE ÁCIDOS NUCLEICOS) EN EL MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN, POR TIPO, 2018-2032 (MILES DE USD)
TABLA 23 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE EE. UU., POR TIPO DE PANEL, 2018-2032 (MILES DE USD)
TABLA 24 MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE CANADÁ, POR TIPO DE PANEL, 2018-2032 (MILES DE USD)
TABLA 25 PANEL MULTIPLEX DE EE. UU. (PRUEBAS SINDRÓMICAS) EN EL MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN, POR TIPO, 2018-2032 (MILES DE USD)
TABLA 26 PANEL MULTIPLEX DE CANADÁ (PRUEBAS SINDRÓMICAS) EN EL MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN, POR TIPO, 2018-2032 (MILES DE USD)
TABLA 27 MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE EE. UU., POR UBICACIÓN DE PRUEBAS, 2018-2032 (MILES DE USD)
TABLA 28 MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE CANADÁ, POR UBICACIÓN DE LAS PRUEBAS, 2018-2032 (MILES DE USD)
TABLA 29 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE EE. UU., POR USUARIO FINAL, 2018-2032 (MILES DE USD)
TABLA 30 MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE CANADÁ, POR USUARIO FINAL, 2018-2032 (MILES DE USD)
TABLA 31 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE EE. UU., POR CANAL DE DISTRIBUCIÓN, 2018-2032 (MILES DE USD)
TABLA 32 MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE CANADÁ, POR CANAL DE DISTRIBUCIÓN, 2018-2032 (MILES DE USD)
Lista de figuras
FIGURA 1 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE CANADÁ Y EE. UU.: SEGMENTACIÓN
FIGURA 2 ÁMBITO GEOGRÁFICO
FIGURA 3 MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE CANADÁ Y EE. UU.: TRIANGULACIÓN DE DATOS
FIGURA 4 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE CANADÁ Y EE. UU.: ANÁLISIS DROC
FIGURA 5 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE EE. UU.: ANÁLISIS DE MERCADO POR PAÍS
FIGURA 6 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE CANADÁ: ANÁLISIS DE MERCADO POR PAÍS
FIGURA 7 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN EN CANADÁ Y EE. UU.: ANÁLISIS DE INVESTIGACIÓN DE EMPRESAS
FIGURA 8 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE CANADÁ Y EE. UU.: MODELADO MULTIVARIADO
FIGURA 9 MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE EE. UU.: DATOS DEMOGRÁFICOS DE LAS ENTREVISTAS
FIGURA 10 MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE CANADÁ: DATOS DEMOGRÁFICOS DE LAS ENTREVISTAS
FIGURA 11 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE CANADÁ Y EE. UU.: CUADRÍCULA DE POSICIÓN DE MERCADO DE DBMR
FIGURA 12 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE EE. UU.: ANÁLISIS DE LA PARTICIPACIÓN DE LOS PROVEEDORES
FIGURA 13 MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE CANADÁ: ANÁLISIS DE LA PARTICIPACIÓN DE LOS PROVEEDORES
FIGURA 14 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE EE. UU.: CUADRÍCULA DE COBERTURA DEL USUARIO FINAL
FIGURA 15 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE CANADÁ: CUADRÍCULA DE COBERTURA DEL USUARIO FINAL
FIGURA 16 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE CANADÁ Y EE. UU.: SEGMENTACIÓN
FIGURA 17 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE CANADÁ: RESUMEN EJECUTIVO
FIGURA 18 MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE EE. UU.: RESUMEN EJECUTIVO
FIGURA 19 SIETE SEGMENTOS COMPRENDEN EL MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE EE. UU., POR PRODUCTO/ENFERMEDAD (2024)
FIGURA 20 SIETE SEGMENTOS COMPRENDEN EL MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE CANADÁ, POR PRODUCTO/ENFERMEDAD (2024)
FIGURA 21 DECISIONES ESTRATÉGICAS
FIGURA 22 AUMENTO DE LA PREVALENCIA DE ENFERMEDADES CRÓNICAS E INFECCIOSAS LA AUMENTO DE LA DEMANDA DE DIAGNÓSTICOS RÁPIDOS Y DESCENTRALIZADOS ESTÁ IMPULSANDO EL CRECIMIENTO DEL MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE CANADÁ DE 2025 A 2032
FIGURA 23 LA CRECIENTE PREFERENCIA DE LOS PACIENTES POR OPCIONES DE PRUEBAS RÁPIDAS, CONVENIENTES Y CERCA DEL PACIENTE ESTÁ IMPULSANDO EL CRECIMIENTO DEL MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE EE. UU. DE 2025 A 2032
FIGURA 24 SE ESPERA QUE EL SEGMENTO DE INFECCIONES RESPIRATORIAS REPRESENTE LA MAYOR PARTICIPACIÓN DEL MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE CANADÁ EN 2025 Y 2032
FIGURA 25 SE ESPERA QUE EL SEGMENTO DE INFECCIONES RESPIRATORIAS REPRESENTE LA MAYOR PARTICIPACIÓN DEL MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE EE. UU. EN 2025 Y 2032
FIGURA 26 ANÁLISIS PESTEL
FIGURA 27 SOLICITUDES DE PATENTES EN VARIAS JURISDICCIONES CLAVE:
FIGURA 28 EE.UU.: SOLICITANTES CLAVE V/S NÚMERO DE PATENTES.
FIGURA 29 CANADÁ: SOLICITANTES CLAVE V/S NÚMERO DE PATENTES
FIGURA 30 EE. UU.: CÓDIGOS IPC V/S NÚMERO DE PATENTES
FIGURA 31 CANADÁ: CÓDIGOS IPC V/S NÚMERO DE PATENTES.
FIGURA 32 EE. UU.: AÑO V/S NÚMERO DE PATENTE PUBLICADA
FIGURA 33 CANADÁ: AÑO V/S NÚMERO DE PATENTE PUBLICADA
FIGURA 34 ANÁLISIS DROC
FIGURA 35 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE EE. UU.: POR PRODUCTO/ENFERMEDAD, 2024
FIGURA 36 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE EE. UU.: POR PRODUCTO/ENFERMEDAD, 2025 A 2032 (MILES DE USD)
FIGURA 37 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE EE. UU.: POR PRODUCTO/ENFERMEDAD, CAGR (2025-2032)
FIGURA 38 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE EE. UU.: POR PRODUCTO/ENFERMEDAD, CURVA DE LÍNEA DE VIDA
FIGURA 39 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE CANADÁ: POR PRODUCTO/ENFERMEDAD, 2024
FIGURA 40 MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE CANADÁ: POR PRODUCTO/ENFERMEDAD, 2025 A 2032 (MILES DE USD)
FIGURA 41 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE CANADÁ: POR PRODUCTO/ENFERMEDAD, CAGR (2025-2032)
FIGURA 42 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE CANADÁ: POR PRODUCTO/ENFERMEDAD, CURVA DE LÍNEA DE VIDA
FIGURA 43 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE EE. UU.: POR MÉTODO/TECNOLOGÍA, 2024
FIGURA 44 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE EE. UU.: POR MÉTODO/TECNOLOGÍA, 2025 A 2032 (MILES DE USD)
FIGURA 45 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE EE. UU.: POR MÉTODO/TECNOLOGÍA, CAGR (2025-2032)
FIGURA 46 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE EE. UU.: POR MÉTODO/TECNOLOGÍA, CURVA DE LÍNEA DE VIDA
FIGURA 47 MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE CANADÁ: POR MÉTODO/TECNOLOGÍA, 2024
FIGURA 48 MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE CANADÁ: POR MÉTODO/TECNOLOGÍA, 2025 A 2032 (MILES DE USD)
FIGURA 49 MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE CANADÁ: POR MÉTODO/TECNOLOGÍA, CAGR (2025-2032)
FIGURA 50 MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE CANADÁ: POR MÉTODO/TECNOLOGÍA, CURVA DE LÍNEA DE VIDA
FIGURA 51 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE EE. UU.: POR TIPO DE PANEL, 2024
FIGURA 52 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE EE. UU.: POR TIPO DE PANEL, 2025 A 2032 (MILES DE USD)
FIGURA 53 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE EE. UU.: POR TIPO DE PANEL, CAGR (2025-2032)
FIGURA 54 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE EE. UU.: POR TIPO DE PANEL, CURVA LIFELINE
FIGURA 55 MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE CANADÁ: POR TIPO DE PANEL, 2024
FIGURA 56 MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE CANADÁ: POR TIPO DE PANEL, 2025 A 2032 (MILES DE USD)
FIGURA 57 MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE CANADÁ: POR TIPO DE PANEL, CAGR (2025-2032)
FIGURA 58 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE CANADÁ: POR TIPO DE PANEL, CURVA LIFELINE
FIGURA 59 MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE EE. UU.: POR UBICACIÓN DE PRUEBAS, 2024
FIGURA 60 MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE EE. UU.: POR UBICACIÓN DE PRUEBAS, 2025 A 2032 (MILES DE USD)
FIGURA 61 MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE EE. UU.: POR UBICACIÓN DE PRUEBA, CAGR (2025-2032)
FIGURA 62 MERCADO DE PRUEBAS EN PUNTOS DE ATENCIÓN DE EE. UU.: POR UBICACIÓN DE PRUEBA, CURVA DE LÍNEA DE VIDA
FIGURA 63 MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE CANADÁ: POR UBICACIÓN DE PRUEBAS, 2024
FIGURA 64 MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE CANADÁ: POR UBICACIÓN DE PRUEBAS, 2025 A 2032 (MILES DE USD)
FIGURA 65 MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE CANADÁ: POR UBICACIÓN DE PRUEBA, CAGR (2025-2032)
FIGURA 66 MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE CANADÁ: POR UBICACIÓN DE PRUEBA, CURVA DE LÍNEA DE VIDA
FIGURA 67 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE EE. UU.: POR USUARIO FINAL, 2024
FIGURA 68 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE EE. UU.: POR USUARIO FINAL, 2025 A 2032 (MILES DE USD)
FIGURA 69 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE EE. UU.: POR USUARIO FINAL, CAGR (2025-2032)
FIGURA 70 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE EE. UU.: POR USUARIO FINAL, CURVA LIFELINE
FIGURA 71 MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE CANADÁ: POR USUARIO FINAL, 2024
FIGURA 72 MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE CANADÁ: POR USUARIO FINAL, 2025 A 2032 (MILES DE USD)
FIGURA 73 MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE CANADÁ: POR USUARIO FINAL, CAGR (2025-2032)
FIGURA 74 MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE CANADÁ: POR USUARIO FINAL, CURVA LIFELINE
FIGURA 75 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE EE. UU.: POR CANAL DE DISTRIBUCIÓN, 2024
FIGURA 76 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE EE. UU.: POR CANAL DE DISTRIBUCIÓN, 2025 A 2032 (MILES DE USD)
FIGURA 77 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE EE. UU.: POR CANAL DE DISTRIBUCIÓN, CAGR (2025-2032)
FIGURA 78 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE EE. UU.: POR CANAL DE DISTRIBUCIÓN, CURVA LIFELINE
FIGURA 79 MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE CANADÁ: POR CANAL DE DISTRIBUCIÓN, 2024
FIGURA 80 MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE CANADÁ: POR CANAL DE DISTRIBUCIÓN, 2025 A 2032 (MILES DE USD)
FIGURA 81 MERCADO DE PRUEBAS EN EL PUNTO DE ATENCIÓN DE CANADÁ: POR CANAL DE DISTRIBUCIÓN, CAGR (2025-2032)
FIGURA 82 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE CANADÁ: POR CANAL DE DISTRIBUCIÓN, CURVA LIFELINE
FIGURA 83 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE EE. UU.: PARTICIPACIÓN DE LA EMPRESA 2024 (%)
FIGURA 84 MERCADO DE PRUEBAS DE PUNTO DE ATENCIÓN DE CANADÁ: PARTICIPACIÓN DE LA EMPRESA 2024 (%)
Metodología de investigación
La recopilación de datos y el análisis del año base se realizan utilizando módulos de recopilación de datos con muestras de gran tamaño. La etapa incluye la obtención de información de mercado o datos relacionados a través de varias fuentes y estrategias. Incluye el examen y la planificación de todos los datos adquiridos del pasado con antelación. Asimismo, abarca el examen de las inconsistencias de información observadas en diferentes fuentes de información. Los datos de mercado se analizan y estiman utilizando modelos estadísticos y coherentes de mercado. Además, el análisis de la participación de mercado y el análisis de tendencias clave son los principales factores de éxito en el informe de mercado. Para obtener más información, solicite una llamada de un analista o envíe su consulta.
La metodología de investigación clave utilizada por el equipo de investigación de DBMR es la triangulación de datos, que implica la extracción de datos, el análisis del impacto de las variables de datos en el mercado y la validación primaria (experto en la industria). Los modelos de datos incluyen cuadrícula de posicionamiento de proveedores, análisis de línea de tiempo de mercado, descripción general y guía del mercado, cuadrícula de posicionamiento de la empresa, análisis de patentes, análisis de precios, análisis de participación de mercado de la empresa, estándares de medición, análisis global versus regional y de participación de proveedores. Para obtener más información sobre la metodología de investigación, envíe una consulta para hablar con nuestros expertos de la industria.
Personalización disponible
Data Bridge Market Research es líder en investigación formativa avanzada. Nos enorgullecemos de brindar servicios a nuestros clientes existentes y nuevos con datos y análisis que coinciden y se adaptan a sus objetivos. El informe se puede personalizar para incluir análisis de tendencias de precios de marcas objetivo, comprensión del mercado de países adicionales (solicite la lista de países), datos de resultados de ensayos clínicos, revisión de literatura, análisis de mercado renovado y base de productos. El análisis de mercado de competidores objetivo se puede analizar desde análisis basados en tecnología hasta estrategias de cartera de mercado. Podemos agregar tantos competidores sobre los que necesite datos en el formato y estilo de datos que esté buscando. Nuestro equipo de analistas también puede proporcionarle datos en archivos de Excel sin procesar, tablas dinámicas (libro de datos) o puede ayudarlo a crear presentaciones a partir de los conjuntos de datos disponibles en el informe.