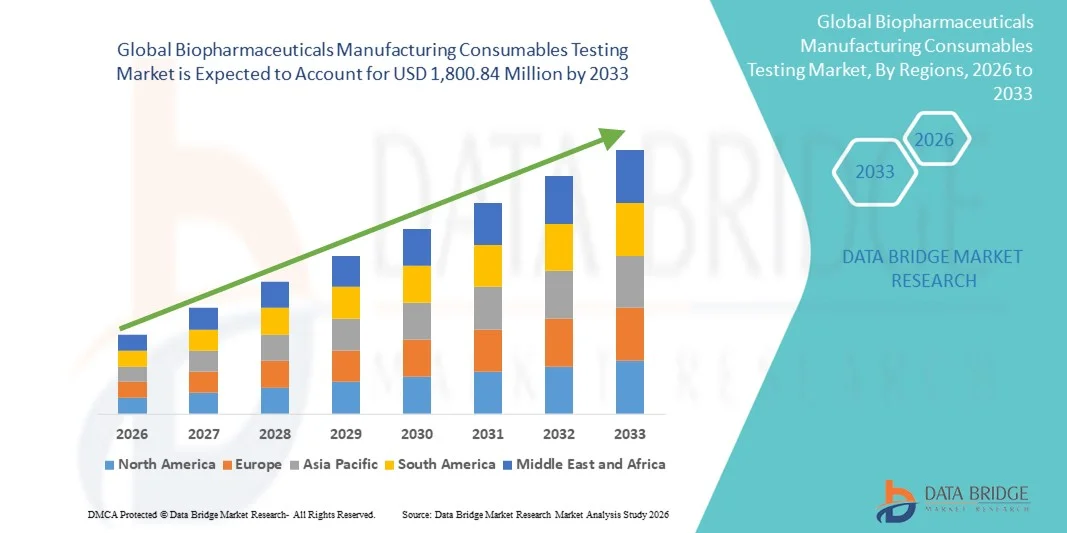
Global Biopharmaceuticals Manufacturing Consumables Testing Market
Tamaño del mercado en miles de millones de dólares
Tasa de crecimiento anual compuesta (CAGR) :
% 
 USD
714.47 Million
USD
1,800.84 Million
2025
2033
USD
714.47 Million
USD
1,800.84 Million
2025
2033
| 2026 –2033 | |
| USD 714.47 Million | |
| USD 1,800.84 Million | |
|
|
|
|
Segmentación del mercado global de pruebas de consumibles para la fabricación de productos biofarmacéuticos, por servicio (pruebas de laboratorio, pruebas personalizadas/pruebas patentadas del cliente, pruebas de laboratorio compendiales y multicomendiales), tipo de materia prima (excipientes de formulación, ingredientes farmacéuticos activos [API] y métodos compendiales [USP/EP/JP], apoyo al programa de calificación de proveedores basado en el apoyo del programa de calificación de proveedores): tendencias de la industria y pronóstico hasta 2033.
Tamaño del mercado de pruebas de consumibles para la fabricación de productos biofarmacéuticos
- El tamaño del mercado global de pruebas de consumibles para la fabricación de productos biofarmacéuticos se valoró en USD 714,47 millones en 2025 y se espera que alcance los USD 1.800,84 millones para 2033 , con una CAGR del 12,25 % durante el período de pronóstico.
- El crecimiento del mercado está impulsado principalmente por el aumento de la producción biofarmacéutica, los estrictos requisitos de cumplimiento normativo y la necesidad crítica de pruebas de consumibles de alta calidad para garantizar la seguridad, la eficacia y la confiabilidad del producto.
- Además, las crecientes inversiones en productos biológicos, medicamentos personalizados y organizaciones de fabricación por contrato (CMO) están expandiendo la demanda de soluciones avanzadas de prueba de consumibles, acelerando así la adopción de medidas de control de calidad sólidas e impulsando el crecimiento del mercado.
Análisis del mercado de pruebas de consumibles para la fabricación de productos biofarmacéuticos
- Las pruebas de consumibles para la fabricación de productos biofarmacéuticos, incluidas las pruebas de laboratorio, las pruebas personalizadas y las pruebas de laboratorio compendiales y multicomendiales, se están convirtiendo en un componente esencial de la producción de productos biológicos, lo que garantiza la seguridad del producto, el cumplimiento y la confiabilidad del proceso en instalaciones de fabricación tanto a pequeña como a gran escala.
- La creciente demanda de productos biofarmacéuticos, junto con los estrictos requisitos regulatorios de agencias como la FDA y la EMA, está impulsando la adopción de servicios avanzados de prueba de consumibles para minimizar los riesgos de contaminación y garantizar la consistencia de lote a lote.
- América del Norte dominó el mercado de pruebas de consumibles para la fabricación de productos biofarmacéuticos con la mayor participación en los ingresos del 39,4 % en 2025, respaldada por una industria biofarmacéutica madura, importantes inversiones en I+D y una sólida presencia de proveedores de servicios clave, particularmente en los EE. UU., donde la innovación en pruebas de laboratorio y programas de calificación de proveedores está avanzando rápidamente.
- Se espera que Asia-Pacífico sea la región de más rápido crecimiento en el mercado durante el período de pronóstico debido a la expansión de las organizaciones de fabricación por contrato (CMO), el aumento de la producción de productos biológicos y el creciente enfoque regulatorio en la calidad y la seguridad en mercados emergentes como China e India.
- El segmento de pruebas de laboratorio dominó el mercado con una participación del 42,6 % en 2025, impulsado por su papel fundamental en la verificación de la calidad de los excipientes de formulación, los ingredientes farmacéuticos activos (API) y el apoyo del programa de calificación de proveedores basado en métodos compendiales (USP/EP/JP), lo que garantiza el cumplimiento y la seguridad del producto en la fabricación biofarmacéutica moderna.
Alcance del informe y segmentación del mercado de pruebas de consumibles para la fabricación de productos biofarmacéuticos
|
Atributos |
Fabricación de productos biofarmacéuticos Consumibles Pruebas Información clave del mercado |
|
Segmentos cubiertos |
|
|
Países cubiertos |
Norteamérica
Europa
Asia-Pacífico
Oriente Medio y África
Sudamérica
|
|
Actores clave del mercado |
|
|
Oportunidades de mercado |
|
|
Conjuntos de información de datos de valor añadido |
Además de los conocimientos sobre escenarios de mercado como el valor de mercado, la tasa de crecimiento, la segmentación, la cobertura geográfica y los principales actores, los informes de mercado seleccionados por Data Bridge Market Research también incluyen un análisis profundo de expertos, epidemiología de pacientes, análisis de canalización, análisis de precios y marco regulatorio. |
Tendencias del mercado de pruebas de consumibles para la fabricación de productos biofarmacéuticos
Cambio hacia servicios avanzados de análisis y pruebas personalizadas
- Una tendencia significativa y en aceleración en el mercado global de pruebas de consumibles para la fabricación de productos biofarmacéuticos es la creciente adopción de métodos analíticos avanzados y servicios de pruebas personalizados para garantizar una mayor precisión, reproducibilidad y cumplimiento de los estándares regulatorios en evolución.
- Por ejemplo, empresas como SGS Life Sciences ofrecen soluciones de prueba personalizadas para sistemas de un solo uso, unidades de filtración y materias primas para satisfacer los requisitos específicos de los clientes, garantizando la integridad del proceso y la seguridad del producto.
- La integración de plataformas de pruebas de alto rendimiento con análisis automatizados permite una detección más rápida de impurezas, contaminación o desviaciones en los ingredientes farmacéuticos activos (API) y los excipientes de formulación, lo que reduce los retrasos en la producción y respalda la calidad constante de los lotes.
- Estos enfoques de prueba avanzados facilitan el control de calidad centralizado, lo que permite a los fabricantes monitorear múltiples consumibles y atributos de materia prima a través de un único flujo de trabajo, optimizando así la eficiencia de la producción y el cumplimiento normativo.
- Esta tendencia hacia soluciones de prueba más precisas, escalables y personalizadas está redefiniendo las expectativas de los fabricantes en cuanto a garantía de calidad y cumplimiento normativo. En consecuencia, proveedores de servicios como Eurofins están ampliando sus plataformas de pruebas asistidas por IA para optimizar el análisis predictivo del rendimiento de las materias primas y los programas de calificación de proveedores.
- La demanda de servicios de pruebas de laboratorio sofisticados y personalizados está creciendo rápidamente tanto en las organizaciones de fabricación por contrato (CMO) como en la producción biofarmacéutica interna, a medida que las empresas priorizan cada vez más la confiabilidad del proceso, el cumplimiento normativo y la seguridad del producto.
Dinámica del mercado de pruebas de consumibles para la fabricación de productos biofarmacéuticos
Impulsor
Aumento de la producción biofarmacéutica y la supervisión regulatoria
- La creciente demanda mundial de productos biofarmacéuticos, junto con los estrictos requisitos regulatorios de agencias como la FDA y la EMA, es un impulsor importante para la adopción de servicios de análisis de consumibles
- Por ejemplo, en marzo de 2025, Charles River Laboratories amplió sus capacidades de prueba para excipientes de formulación y API, apuntando al cumplimiento de los estándares USP, EP y JP para apoyar a los fabricantes de productos biológicos.
- A medida que los fabricantes buscan minimizar los riesgos de contaminación y garantizar una calidad constante del producto, las pruebas de consumibles brindan una validación y un monitoreo críticos de las materias primas y los componentes de un solo uso.
- Además, el uso creciente de organizaciones de fabricación por contrato (CMO) y flujos de trabajo complejos de producción de productos biológicos requieren servicios de pruebas confiables y escalables para mantener la consistencia de lote a lote y el cumplimiento normativo.
- El creciente énfasis en la producción de productos biológicos de alta calidad, junto con una mayor subcontratación de servicios de prueba, está haciendo que las pruebas de laboratorio y personalizadas sean una parte integral de los procesos de fabricación biofarmacéutica modernos.
- Los avances tecnológicos en las metodologías de prueba, como la detección microbiana rápida y los ensayos de alta sensibilidad, están permitiendo una validación más rápida e impulsando la adopción en instalaciones de fabricación a gran escala.
Restricción/Desafío
Altos costos y requisito de equipo especializado
- Los altos costos operativos asociados con las pruebas de consumibles avanzados y la necesidad de equipos analíticos especializados plantean un desafío significativo para la expansión del mercado.
- Por ejemplo, la implementación de pruebas de laboratorio multicompendiales para API y excipientes requiere inversión en instrumentos de alta precisión, personal calificado y calibración y mantenimiento continuos.
- Los fabricantes más pequeños o los CMO en mercados emergentes pueden enfrentar barreras para la adopción debido a los importantes costos iniciales y recurrentes involucrados, lo que limita la penetración del mercado en regiones sensibles a los costos.
- Además, el estricto cumplimiento de múltiples estándares regulatorios, como USP, EP y JP, exige capacitación y validación continuas, lo que puede incrementar aún más la complejidad operativa y los gastos. Abordar estos desafíos mediante soluciones de prueba escalables, modelos de intercambio de tecnología y alianzas estratégicas será crucial para expandir el alcance del mercado, manteniendo al mismo tiempo la calidad y el cumplimiento normativo.
- La disponibilidad limitada de personal capacitado con experiencia en técnicas de pruebas especializadas puede ralentizar la adopción del servicio, en particular en regiones emergentes con una creciente actividad de fabricación biofarmacéutica.
- La volatilidad en el suministro de materia prima y la variabilidad en la calidad pueden introducir complejidades y costos de prueba adicionales, lo que dificulta la prestación constante del servicio y la eficiencia operativa.
Alcance del mercado de pruebas de consumibles para la fabricación de productos biofarmacéuticos
El mercado está segmentado según el tipo de servicio y materia prima.
- Por servicio
En función del servicio, el mercado se segmenta en pruebas de laboratorio, pruebas personalizadas/pruebas patentadas por el cliente y pruebas de laboratorio compendiales y multicomendiales. El segmento de pruebas de laboratorio dominó el mercado con la mayor participación en los ingresos del 42.6% en 2025, impulsado por su papel fundamental para garantizar la calidad, la seguridad y el cumplimiento de los consumibles biofarmacéuticos. Las pruebas de laboratorio de rutina validan los excipientes de la formulación, los ingredientes farmacéuticos activos (API) y los sistemas de un solo uso para cumplir con los estrictos requisitos reglamentarios. Proporcionan a los fabricantes datos fiables para mantener la consistencia entre lotes y prevenir la contaminación. El segmento se beneficia de una alta adopción entre las organizaciones de fabricación por contrato (CMO) y las instalaciones biofarmacéuticas a gran escala que priorizan los procesos sólidos de control de calidad. Además, las pruebas de laboratorio ofrecen soluciones escalables, lo que permite a las instalaciones manejar grandes volúmenes de muestras con procedimientos estandarizados. Su adopción generalizada se ve impulsada aún más por mandatos regulatorios como los requisitos de cumplimiento de la USP, EP y JP, lo que las convierte en una piedra angular de la producción biofarmacéutica moderna
Se prevé que el segmento de pruebas personalizadas/pruebas patentadas por el cliente experimente el mayor crecimiento entre 2026 y 2033, impulsado por la creciente demanda de soluciones de prueba especializadas y específicas para cada cliente. Fabricantes y directores de marketing (CMO) buscan servicios de pruebas a medida para formulaciones únicas, excipientes patentados y productos biológicos emergentes. Las pruebas personalizadas garantizan un cumplimiento preciso de las especificaciones del cliente y las expectativas regulatorias, a la vez que facilitan la innovación en el desarrollo biofarmacéutico. La creciente complejidad de la producción de productos biológicos, junto con la tendencia a la externalización de las pruebas, está impulsando la adopción de estos servicios. Los proveedores que ofrecen soluciones de pruebas personalizadas flexibles, rápidas y escalables están ganando terreno. Además, los avances tecnológicos en instrumentación analítica permiten realizar pruebas personalizadas más precisas y eficientes, lo que impulsa aún más el crecimiento del mercado en este segmento.
- Por tipo de materia prima
Según el tipo de materia prima, el mercado se segmenta en excipientes de formulación, ingredientes farmacéuticos activos (API) y métodos compendiales (USP/EP/JP) con el apoyo de programas de calificación de proveedores. El segmento de pruebas de API dominó el mercado en 2025 debido a la importancia crucial de verificar la pureza, potencia y estabilidad de los ingredientes farmacéuticos activos antes de su uso en la fabricación de productos biológicos. Las pruebas precisas de API previenen la contaminación, garantizan la eficacia terapéutica y respaldan el cumplimiento normativo. El segmento se beneficia de una alta adopción en todas las etapas del desarrollo de fármacos, desde la fase preclínica hasta la producción comercial. Los fabricantes priorizan las pruebas de API para mitigar los riesgos en la producción de productos biológicos y mantener los estándares de calidad en múltiples lotes. La presencia de estrictos marcos regulatorios a nivel mundial refuerza aún más el dominio de este segmento. Los métodos analíticos avanzados y las plataformas automatizadas mejoran la eficiencia y la confiabilidad de las pruebas de API, lo que contribuye a su continuo liderazgo en el mercado.
Se prevé que el segmento de apoyo a programas de calificación de proveedores basados en métodos compendiales experimente el mayor crecimiento entre 2026 y 2033, impulsado por la creciente necesidad de protocolos de prueba estandarizados para calificar a los proveedores de materias primas. Los programas basados en las directrices USP, EP y JP ayudan a los fabricantes a garantizar que todos los materiales cumplan con los estándares globales de calidad. El crecimiento de la fabricación por contrato y las cadenas de suministro internacionales está impulsando la demanda de dichos programas para mantener el cumplimiento normativo y reducir los riesgos en la cadena de suministro. Además, las autoridades reguladoras están priorizando la calificación de proveedores como parte del cumplimiento de las BPM, lo que impulsa su adopción. Las empresas que ofrecen soluciones integradas de calificación y prueba de proveedores, incluyendo apoyo multicomendario, están captando nuevas oportunidades de mercado. Las herramientas avanzadas de gestión de datos y generación de informes mejoran aún más la eficiencia y el atractivo de este segmento en crecimiento.
Análisis regional del mercado de pruebas de consumibles para la fabricación de productos biofarmacéuticos
- América del Norte dominó el mercado de pruebas de consumibles para la fabricación de productos biofarmacéuticos con la mayor participación en los ingresos del 39,4 % en 2025, respaldada por una industria biofarmacéutica madura, importantes inversiones en I+D y una sólida presencia de proveedores de servicios clave.
- Los fabricantes y CMO de la región priorizan las pruebas rigurosas de excipientes de formulación, API y sistemas de un solo uso para garantizar la seguridad, la calidad y el cumplimiento de los estándares globales del producto.
- Esta adopción generalizada está respaldada además por altas inversiones en I+D, infraestructura analítica avanzada y la presencia de proveedores de servicios de prueba líderes, lo que establece a América del Norte como el centro principal de servicios de prueba de consumibles confiables y de alta calidad.
Análisis del mercado de pruebas de consumibles para la fabricación de productos biofarmacéuticos en EE. UU.
El mercado estadounidense de pruebas de consumibles para la fabricación de productos biofarmacéuticos captó la mayor participación en los ingresos, con un 82%, en 2025 en Norteamérica, impulsado por la consolidada industria biofarmacéutica del país y la sólida supervisión regulatoria de la FDA. Los fabricantes priorizan cada vez más las pruebas de alta calidad de excipientes de formulación, API y sistemas de un solo uso para garantizar la seguridad, el cumplimiento normativo y la fiabilidad del proceso. La creciente adopción de organizaciones de fabricación por contrato (CMO) y flujos de trabajo avanzados para la producción de productos biológicos impulsa aún más el crecimiento del mercado. Además, la integración de tecnologías de pruebas automatizadas y de alto rendimiento está mejorando la eficiencia y la precisión, lo que respalda las operaciones a gran escala. Las sólidas inversiones en I+D, la disponibilidad de mano de obra cualificada y la presencia de proveedores líderes de servicios de pruebas consolidan a EE. UU. como un centro clave para las pruebas de consumibles.
Análisis del mercado europeo de pruebas de consumibles para la fabricación de productos biofarmacéuticos
Se proyecta que el mercado europeo de pruebas de consumibles para la fabricación de productos biofarmacéuticos se expandirá a una tasa de crecimiento anual compuesta (TCAC) sustancial durante el período de pronóstico, impulsado principalmente por los estrictos requisitos regulatorios de la EMA y la creciente demanda de producción de productos biológicos de alta calidad. La creciente urbanización y la expansión de las CMO en países como Alemania, Francia y Suiza están impulsando la adopción de servicios de pruebas avanzados. Los fabricantes europeos también se están enfocando en garantizar el cumplimiento de las normas farmacopeicas USP, EP y JP, mejorando así la confiabilidad de los procesos de producción. La región está experimentando un crecimiento significativo en las instalaciones de productos biológicos, tanto a pequeña como a gran escala, con la incorporación de servicios de pruebas en nuevos proyectos y expansiones. Además, las iniciativas gubernamentales que apoyan la innovación farmacéutica y el control de calidad impulsan aún más el desarrollo del mercado.
Análisis del mercado de pruebas de consumibles para la fabricación de productos biofarmacéuticos en el Reino Unido
Se prevé que el mercado británico de pruebas de consumibles para la fabricación de productos biofarmacéuticos crezca a una tasa de crecimiento anual compuesta (TCAC) notable durante el período de pronóstico, impulsado por la creciente demanda de productos biológicos de alta calidad y el riguroso cumplimiento normativo. La creciente concienciación sobre la seguridad, la calidad y la eficacia está animando a fabricantes y CMO a adoptar servicios avanzados de pruebas de laboratorio y personalizadas. Se espera que el sólido ecosistema de investigación farmacéutica del Reino Unido, combinado con sólidos servicios de pruebas por contrato, siga impulsando el crecimiento del mercado. Además, la expansión de la producción de productos biológicos y la creciente complejidad de las formulaciones requieren soluciones sofisticadas para las pruebas de consumibles a fin de garantizar la consistencia de la calidad y el cumplimiento normativo de los productos.
Análisis del mercado alemán de pruebas de consumibles para la fabricación de productos biofarmacéuticos
Se espera que el mercado alemán de pruebas de consumibles para la fabricación de productos biofarmacéuticos se expanda a una tasa de crecimiento anual compuesta (TCAC) considerable durante el período de pronóstico, impulsado por el fuerte enfoque del país en la innovación, los altos estándares de fabricación y el cumplimiento normativo. La sólida infraestructura farmacéutica y biotecnológica alemana promueve la adopción de servicios de pruebas de laboratorio, personalizadas y farmacopeicas, especialmente en la producción de productos biológicos a gran escala. La integración de los flujos de trabajo de las pruebas con sistemas automatizados de control de calidad es cada vez más frecuente, lo que mejora la eficiencia y la precisión. Los fabricantes y las empresas de marketing locales también priorizan la sostenibilidad ambiental y la optimización de procesos, lo que impulsa la adopción de métodos de prueba avanzados.
Análisis del mercado de pruebas de consumibles para la fabricación de productos biofarmacéuticos en Asia-Pacífico
Se prevé que el mercado de pruebas de consumibles para la fabricación de productos biofarmacéuticos en Asia-Pacífico crezca a la tasa de crecimiento anual compuesta (TCAC) más alta, del 23 %, durante el período de pronóstico de 2026 a 2033, impulsado por el aumento de la producción de productos biológicos, la expansión de las CMO y el creciente enfoque regulatorio en países como China, Japón e India. La creciente capacidad de fabricación farmacéutica de la región, sumada a las iniciativas gubernamentales que promueven el cumplimiento normativo y el control de calidad, está impulsando la adopción de servicios de pruebas. Además, la disponibilidad de soluciones de prueba rentables y de proveedores de servicios locales facilita el acceso a las pruebas de consumibles en los mercados emergentes. Los avances tecnológicos y la creciente demanda de productos biológicos de alta calidad contribuyen aún más a la expansión del mercado.
Análisis del mercado japonés de pruebas de consumibles para la fabricación de productos biofarmacéuticos
El mercado japonés de pruebas de consumibles para la fabricación de productos biofarmacéuticos está cobrando impulso gracias al avanzado ecosistema de investigación farmacéutica del país, la creciente producción de productos biológicos y un estricto marco regulatorio. Los fabricantes están adoptando servicios de pruebas de laboratorio y personalizadas de alta precisión para garantizar el cumplimiento normativo y la fiabilidad de sus productos. La integración de los flujos de trabajo de las pruebas con análisis automatizados y programas de calificación de proveedores está mejorando la eficiencia operativa. La demanda de pruebas rigurosas también se ve impulsada por el enfoque de Japón en la calidad, la seguridad y la estandarización de procesos, tanto en instalaciones propias como en las operadas por la CMO. Además, la adopción de productos biológicos innovadores y formulaciones complejas impulsa el crecimiento de los servicios de pruebas especializados.
Análisis del mercado de pruebas de consumibles para la fabricación de productos biofarmacéuticos en India
El mercado indio de pruebas de consumibles para la fabricación de productos biofarmacéuticos representó la mayor participación en los ingresos de Asia Pacífico en 2025, gracias a la expansión del sector farmacéutico del país, la rápida producción de productos biológicos y la creciente conciencia regulatoria. India se está consolidando como un centro clave para las CMO y los servicios de pruebas por contrato, brindando soporte tanto a clientes nacionales como internacionales. El impulso hacia el cumplimiento de los estándares globales de calidad, la creciente inversión en infraestructura analítica y la disponibilidad de soluciones de prueba rentables están impulsando su adopción. Además, la creciente demanda de productos biológicos de alta calidad y medicamentos personalizados está impulsando la necesidad de servicios de pruebas de laboratorio, personalizadas y compendiales en India.
Cuota de mercado de pruebas de consumibles para la fabricación de productos biofarmacéuticos
La industria de pruebas de consumibles para la fabricación de productos biofarmacéuticos está liderada principalmente por empresas bien establecidas, entre las que se incluyen:
- Alcami Corporation (EE. UU.)
- Merck KGaA (Alemania)
- Eurofins Scientific (Luxemburgo)
- Agilent Technologies, Inc. (EE. UU.)
- Laboratorios Charles River (EE. UU.)
- Catalent, Inc (EE. UU.)
- Element Materials Technology (Reino Unido)
- Pace Analytical Services, LLC (EE. UU.)
- Nelson Laboratories, LLC (EE. UU.)
- BioSpectra, Inc. (EE. UU.)
- Avomeen Analytical Services (EE. UU.)
- MabPlex International Ltd. (Reino Unido)
- SGS SA (Suiza)
- Lonza (Suiza)
- TOXIKON (EE. UU.)
- Boston Scientific Corporation (EE. UU.)
- STERIS (EE. UU.)
- Laboratorio Farmacéutico (Reino Unido)
- Albany Molecular Research Inc. (EE. UU.)
- Triclinic Labs, Inc. (EE. UU.)
¿Cuáles son los desarrollos recientes en el mercado global de pruebas de consumibles para la fabricación de productos biofarmacéuticos?
- En septiembre de 2024, Eurofins Scientific amplió su red de pruebas de productos biofarmacéuticos en EE. UU. mediante la adquisición de Infinity Laboratories, Inc. (ocho laboratorios en EE. UU.), ampliando su red de pruebas de microbiología, química y paquetes para consumibles biofarmacéuticos y fortaleciendo así la capacidad para servicios de pruebas de consumibles.
- En abril de 2024, Charles River Laboratories anunció el lanzamiento de métodos de prueba alternativos para reducir la dependencia de las pruebas con animales en sus servicios de pruebas biofarmacéuticas y de consumibles, lo que refleja un cambio hacia flujos de trabajo de pruebas de consumibles más avanzados y éticos.
- En febrero de 2024, Eurofins anunció un nuevo "Enfoque de plataforma" para pruebas rápidas de materias primas GMP (química/bioquímica/microbiología/virales) que cubren componentes de alto riesgo en su laboratorio de materias primas de Lancaster, PA, lo que significa ofertas mejoradas para pruebas de materias primas y consumibles para la fabricación de productos biológicos.
- En enero de 2024, Rapid Micro Biosystems presentó su 10-K, destacando la disponibilidad de sus consumibles automatizados que respaldan los flujos de trabajo de control de calidad de microbiología para productos biológicos/consumibles, lo que ilustra una mayor innovación en las herramientas de prueba de consumibles.
- En marzo de 2022, Intertek Group plc anunció la adquisición de SASTech LLC para expandir sus servicios de pruebas farmacéuticas y biofarmacéuticas, reforzando la capacidad para las pruebas de consumibles en la cadena de suministro biofarmacéutica.
SKU-
Obtenga acceso en línea al informe sobre la primera nube de inteligencia de mercado del mundo
- Panel de análisis de datos interactivo
- Panel de análisis de empresas para oportunidades con alto potencial de crecimiento
- Acceso de analista de investigación para personalización y consultas
- Análisis de la competencia con panel interactivo
- Últimas noticias, actualizaciones y análisis de tendencias
- Aproveche el poder del análisis de referencia para un seguimiento integral de la competencia
Metodología de investigación
La recopilación de datos y el análisis del año base se realizan utilizando módulos de recopilación de datos con muestras de gran tamaño. La etapa incluye la obtención de información de mercado o datos relacionados a través de varias fuentes y estrategias. Incluye el examen y la planificación de todos los datos adquiridos del pasado con antelación. Asimismo, abarca el examen de las inconsistencias de información observadas en diferentes fuentes de información. Los datos de mercado se analizan y estiman utilizando modelos estadísticos y coherentes de mercado. Además, el análisis de la participación de mercado y el análisis de tendencias clave son los principales factores de éxito en el informe de mercado. Para obtener más información, solicite una llamada de un analista o envíe su consulta.
La metodología de investigación clave utilizada por el equipo de investigación de DBMR es la triangulación de datos, que implica la extracción de datos, el análisis del impacto de las variables de datos en el mercado y la validación primaria (experto en la industria). Los modelos de datos incluyen cuadrícula de posicionamiento de proveedores, análisis de línea de tiempo de mercado, descripción general y guía del mercado, cuadrícula de posicionamiento de la empresa, análisis de patentes, análisis de precios, análisis de participación de mercado de la empresa, estándares de medición, análisis global versus regional y de participación de proveedores. Para obtener más información sobre la metodología de investigación, envíe una consulta para hablar con nuestros expertos de la industria.
Personalización disponible
Data Bridge Market Research es líder en investigación formativa avanzada. Nos enorgullecemos de brindar servicios a nuestros clientes existentes y nuevos con datos y análisis que coinciden y se adaptan a sus objetivos. El informe se puede personalizar para incluir análisis de tendencias de precios de marcas objetivo, comprensión del mercado de países adicionales (solicite la lista de países), datos de resultados de ensayos clínicos, revisión de literatura, análisis de mercado renovado y base de productos. El análisis de mercado de competidores objetivo se puede analizar desde análisis basados en tecnología hasta estrategias de cartera de mercado. Podemos agregar tantos competidores sobre los que necesite datos en el formato y estilo de datos que esté buscando. Nuestro equipo de analistas también puede proporcionarle datos en archivos de Excel sin procesar, tablas dinámicas (libro de datos) o puede ayudarlo a crear presentaciones a partir de los conjuntos de datos disponibles en el informe.