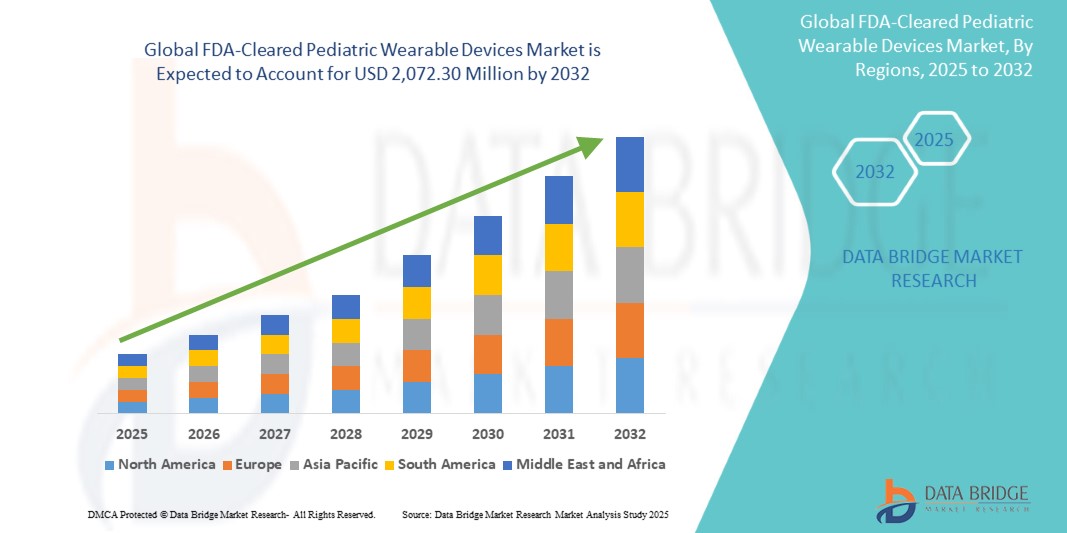
Global Fda Cleared Pediatric Wearable Devices Market
Tamaño del mercado en miles de millones de dólares
Tasa de crecimiento anual compuesta (CAGR) :
% 
 USD
495.00 Million
USD
2,072.30 Million
2024
2032
USD
495.00 Million
USD
2,072.30 Million
2024
2032
| 2025 –2032 | |
| USD 495.00 Million | |
| USD 2,072.30 Million | |
|
|
|
|
Aplicación de dispositivos portátiles de la FDA, por tipo de dispositivo (eximetros del cuerpo, monitores cardíacos / dispositivos ECG, monitores respiratorios, monitores multivital, control de glucosa y monitores del sueño), uso clínico ( monitorización del paciente, monitorización de glóbulos, control de temperaturas, etc.)
FDA-Cleared Pediatric Devices Wearable Tamaño del mercado
- El tamaño del mercado de los dispositivos pediátricos limpiados por la FDA mundial se valoró enUSD 495.00 million in 2024y se espera que alcanceUSD 2,072.30 million by 2032, aCAGR of 19.60%durante el período previsto
- El crecimiento del mercado se ve alimentado en gran medida por el aumento de las aprobaciones reglamentarias de los desgastes centrados en la pediátrica, junto con los avances en tecnologías sensoriales que permiten un seguimiento preciso de los signos vitales, el sueño y las funciones respiratorias en los niños
- Además, el aumento de la demanda tanto de cuidadores como de proveedores de atención médica para soluciones de monitoreo seguras, fiables y en tiempo real está posicionando los wearables pediátricos limpiados por la FDA como una herramienta esencial en la atención médica pediátrica. Estos factores convergentes están acelerando la adopción en entornos clínicos y de atención a domicilio, lo que aumenta significativamente el crecimiento de la industria
FDA-Cleared Pediatric Devices Wearable Análisis de mercado
- Los dispositivos portátiles, diseñados para proporcionar monitorización en tiempo real de signos vitales, el sueño, la salud respiratoria y otras condiciones pediátricas, se están volviendo cada vez más vitales tanto en los entornos clínicos como en el hogar debido a su capacidad de proporcionar datos precisos, continuos y una integración perfecta con plataformas de salud digital
- La creciente demanda de productos pediátricos se ve alimentada principalmente por el aumento de las autorizaciones regulatorias de la FDA, los avances tecnológicos en sensores y conectividad, y el aumento de la conciencia entre los padres y proveedores de atención médica sobre la importancia de la vigilancia proactiva de la salud pediátrica
- América del Norte dominaba el mercado de dispositivos pediátricos con la mayor cuota de ingresos de alrededor del 39% en 2024, caracterizada por marcos regulatorios favorables, una fuerte adopción de soluciones de salud digital, y la presencia de jugadores pioneros, con Estados Unidos experimentando una subida sustancial en entornos hospitalarios y de atención a domicilio impulsados por innovaciones en monitoreo infantil y gestión remota de pacientes
- Se espera que Asia-Pacífico sea la región de mayor crecimiento en el mercado de dispositivos pediátricos portátiles durante el período previsto debido al aumento del gasto sanitario, el aumento de las tasas de natalidad y la adopción creciente de tecnologías de vigilancia de la salud infantil
- Los dispositivos de óxido de pulso dominaron el mercado de dispositivos portátiles pediátricos en 2024 con una proporción estimada del 40% del mercado, impulsado por su papel crítico en la vigilancia de la saturación de oxígeno y la frecuencia cardíaca en los neonatos y bebés, junto con la ampliación de las autorizaciones de la FDA que soportan tanto los casos de uso de recetas como de venta libre.
Report Scope and FDA-Cleared Pediatric Wearable Devices Market Segmentation
| Atributos | Dispositivos Pediátricos de liberación de la FDA |
| Segmentos cubiertos |
|
| Países cubiertos | América del Norte
Europa
Asia y el Pacífico
Oriente Medio y África
América del Sur
|
| Principales jugadores del mercado |
|
| Oportunidades de mercado |
|
| Valor añadido Data Infosets | Además de las ideas sobre escenarios de mercado como el valor de mercado, la tasa de crecimiento, la segmentación, la cobertura geográfica y los principales actores, los informes de mercado comisariados por el Data Bridge Market Research también incluyen análisis profundos de expertos, análisis de precios, análisis de acciones de la marca, análisis de la demografía, análisis de la cadena de suministro, análisis de la cadena de valor, visión general de materias primas/consumibles, criterios de selección de proveedores, análisis de PESTLE Analysis, análisis de PESTLE, análisis, análisis de Porter, análisis de Porter y marco regulador. |
FDA-Cleared Pediatric Devices Wearable tendencias mercado
Rising Adoption of Real Pediatric Health Monitoring
- Una tendencia significativa y aceleradora en el mercado mundial de dispositivos pediátricos utilizables es la creciente integración de tecnologías limpias por la FDA con plataformas de salud digitales y aplicaciones conectadas, mejorando el monitoreo pediátrico en tiempo real y el compromiso de cuidadores
- Por ejemplo, el Owlet Dream Sock recibió la autorización FDA De Novo, permitiendo a los padres monitorear los niveles de oxígeno infantil y la frecuencia cardíaca mediante una aplicación móvil conectada, estableciendo confianza en soluciones accesibles al consumidor y validadas médicamente
- Láminas pediátricas limpias de la FDA ahora cuentan con avanzadosensorespara SpO2, ECG y monitoreo respiratorio continuo, permitiendo la detección proactiva de anomalías y el envío de alertas inteligentes a cuidadores y médicos en tiempo real
- La integración perfecta de estos dispositivos con plataformas de telesalud permite a los proveedores de atención médica monitorear a distancia a los pacientes pediátricos, permitiendo la supervisión centralizada y reduciendo la necesidad de visitas hospitalarias frecuentes
- Esta tendencia hacia la validación clínica de los wearables integrados digitalmente está fundamentalmente remodelando la entrega de cuidados pediátricos. En consecuencia, empresas como Masimo están desarrollando dispositivos pediátricos depurados por la FDA como Stork, diseñados tanto para uso doméstico como clínico con capacidades de monitoreo conectadas
- La demanda de productos pediátricos que combinan la limpieza de la FDA, la precisión clínica y la comodidad de cuidador está creciendo rápidamente en los entornos hospitalarios y de atención en el hogar, ya que las familias y los proveedores priorizan cada vez más la seguridad infantil y la gestión proactiva de la salud
Dinámica del mercado de dispositivos portátiles liberados por la FDA
Conductor
creciente demanda de soluciones de monitoreo pediátrica seguras y fiables
- La creciente prevalencia de los riesgos de salud neonatal e infantil, junto con una mayor conciencia entre los cuidadores, es un factor importante para la adopción cada vez mayor de los productos pediátricos de la FDA
- Por ejemplo, en junio de 2023, Owlet, Inc. anunció la autorización de la FDA para su dispositivo BabySat, lo que permitió el uso de recetas para monitorear la saturación de oxígeno en bebés, marcando un avance en la ampliación de la vigilancia de grado clínico al entorno doméstico
- A medida que los padres y los médicos buscan datos de salud continuos y fiables para los niños, los wearables de la FDA proporcionan características avanzadas tales como monitoreo en tiempo real, seguimiento de datos históricos y alertas de cuidadores, ofreciendo una alternativa convincente a los métodos de monitoreo intermitente tradicionales
- Además, el creciente ecosistema de salud digital y la integración con los servicios de telemedicina están haciendo que los wearables pediátricos sean una parte integral de modelos de atención proactiva, ofreciendo conexiones perfectas entre cuidadores, niños y proveedores de atención médica.
- La comodidad de la vigilancia en el hogar, la dependencia hospitalaria reducida y la capacidad de compartir datos en tiempo real con los médicos son factores clave para impulsar la adopción tanto en el hogar como en el hospital. La tendencia hacia programas remotos de monitoreo de pacientes y vías regulatorias de apoyo contribuye aún más al crecimiento del mercado
Restraint/Challenge
Problemas de sensibilidad de la piel y Cumplimiento Regulatorio Hurdles
- Las preocupaciones acerca de la irritación potencial de la piel del uso prolongado del dispositivo, especialmente en los neonatos y los lactantes, plantean un reto significativo para la penetración más amplia del mercado de los productos pediátricos
- Por ejemplo, los exámenes clínicos han puesto de relieve que el uso continuo de parches de monitoreo basados en adhesivos en los niños puede dar lugar a molestias cutáneas o reacciones alérgicas, creando vacilación entre los padres y cuidadores en relación con la adopción diaria
- Hacer frente a estas preocupaciones mediante el uso de materiales hipoalergénicos, la ergonomía de dispositivos mejorados y pruebas de seguridad regulares es crucial para crear confianza. Empresas como Masimo enfatizan su diseño pediátrico y características centradas en la comodidad en su marketing para tranquilizar a los cuidadores
- Además, los altos estándares regulatorios para dispositivos pediátricos y largos plazos de aprobación de la FDA pueden retrasar la comercialización, creando barreras para los innovadores más pequeños en el espacio. Si bien las aprobaciones se están acelerando, el cumplimiento sigue siendo complejo y intensivo en recursos
- El costo relativamente mayor de los productos pediátricos de la FDA en comparación con los monitores de consumo básicos también puede dificultar la adopción entre las familias sensibles a los precios, en particular en las regiones en desarrollo. Aunque se espera que los precios declinen, la prima percibida para los dispositivos de grado clínico sigue siendo un factor limitante
- La superación de estos desafíos mediante un mejor diseño específico de pediátrica, una vía reglamentaria más rápida y el desarrollo de opciones más asequibles será vital para el crecimiento sostenido del mercado
FDA-Cleared Pediatric Devices Wearable Market Scope
El mercado está segmentado por tipo de dispositivo, uso clínico, tecnología y aplicación.
- Por tipo de dispositivo
Sobre la base del tipo de dispositivo, el mercado de dispositivos pediátricos depurados por la FDA se segmenta en óxidos de pulso, monitores cardíacos/gastables ECG, monitores respiratorios, monitores multivital, monitores de monitoreo de glucosa y rastreadores de sueño. El segmento del óxido de pulso dominaba el mercado en 2024 con la mayor cuota de ingresos del mercado del 40%, impulsada por su papel crítico en el monitoreo de la salud neonatal e infantil. Los óxidos de pulso se utilizan ampliamente para rastrear la saturación de oxígeno y la frecuencia cardíaca, parámetros vitales para detectar problemas respiratorios y problemas cardíacos congénitos en las poblaciones pediátricas. Su dominio está reforzado aún más por múltiples autorizaciones de la FDA de dispositivos centrados en lactantes como Owlet BabySat y Masimo Stork, que han ganado una fuerte adopción tanto en los entornos clínicos como en el hogar. El segmento se beneficia de su naturaleza no invasiva, diseño compacto y confianza de cuidador, lo que lo convierte en el tipo pediátrico más adoptado. A medida que más hospitales y usuarios de cuidado doméstico integran el monitoreo de oxígeno en protocolos de atención pediátrica, los óxidos de pulso siguen liderando la categoría de tipo dispositivo.
Se prevé que el segmento de monitores multivital será testigo de la tasa de crecimiento más rápida de 2025 a 2032, alimentada por avances en la fusión de sensores utilizables y la creciente demanda de soluciones integradas de vigilancia. Estos dispositivos combinan múltiples parámetros, como SpO2, frecuencia cardíaca, frecuencia respiratoria y temperatura, en un solo uso, proporcionando información completa sobre la salud de un niño. Su capacidad para reducir la necesidad de múltiples dispositivos mejora la comodidad del cuidador y mejora la adopción en entornos clínicos, especialmente para programas remotos de monitoreo de pacientes. El impulso creciente para la salud conectada y la necesidad de una recopilación continua de datos pediátricos en tiempo real están acelerando la adopción. Además, se espera que las aprobaciones de la FDA en curso de plataformas pediátricas multivitales amplíen la aceptación clínica y el soporte de reembolso, lo que hace que este sea el tipo de dispositivo de mayor crecimiento.
- Por uso clínico
Sobre la base del uso clínico, el mercado de dispositivos pediátricos depurados por la FDA se segmenta en monitorización cardiaca, monitoreo respiratorio, monitoreo de glucosa, monitoreo de temperatura y monitoreo adjunto de SIDS. El segmento de monitoreo respiratorio dominó el mercado en 2024, impulsado por la alta prevalencia de complicaciones respiratorias neonatales y la necesidad de monitorización continua para detectar apnea y otras condiciones. Los wearables respiratorios pediátricos desempeñan un papel crítico tanto en la configuración de NICU como en el monitoreo en casa, ofreciendo alertas en tiempo real a los cuidadores y los clínicos. Los dispositivos que rastrean los patrones respiratorios y los niveles de oxígeno son especialmente vitales para los bebés prematuros, donde la intervención temprana puede ser salvavidas. Las soluciones limpias de la FDA, como las diseñadas para la vigilancia respiratoria infantil, han consolidado el papel principal de este segmento. Su dominio también está respaldado por una fuerte validación clínica y una adopción generalizada en unidades hospitalarias de atención neonatal en todo el mundo.
Se prevé que el segmento de vigilancia de la glucosa crezca a la velocidad más rápida durante el período de pronóstico, alimentado por la creciente incidencia de la diabetes pediátrica y el aumento de las aprobaciones de la FDA de dispositivos de monitoreo continuo de la glucosa (CGM) para niños. Las MC proporcionan lecturas de glucosa en tiempo real, alertas de hipoglucemia o hiperglicemia, e integración con sistemas de parto de insulina, haciéndolos indispensables para la gestión de la diabetes pediátrica. Los padres y los médicos están adoptando cada vez más CGMs para reducir las pruebas del dedo y mejorar la calidad de vida de los niños con diabetes tipo 1. La limpieza de dispositivos con indicaciones específicas de la FDA está impulsando la confianza y la adopción. Con un fuerte apoyo de los beneficiarios y una expansión de las directrices clínicas que apoyan el uso de CGM en los niños, este segmento se establece para crecer a un ritmo más rápido.
- By Technology
Sobre la base de la tecnología, el mercado de dispositivos pediátricos limpiados por la FDA se segmenta en óptica (PPG), eléctrica (ECG), acelerómetros y bioimpedancia. El segmento óptico (PPG) dominó el mercado en 2024, debido en gran medida a su uso en la oxidación del pulso y el monitoreo de la frecuencia cardíaca para los neonatos y bebés. Los dispositivos basados en PPG son centrales para la mayoría de los productos pediátricos de la FDA, ofreciendo mediciones no invasivas y continuas de saturación de oxígeno y frecuencia cardíaca. La tecnología es bien establecida, confiable y ampliamente confiada tanto por los cuidadores como por los clínicos, lo que lo convierte en la opción preferida para el monitoreo pediátrico crítico. Su dominio está respaldado por su integración en los principales dispositivos aprobados por la FDA y su papel como base para muchas soluciones de monitoreo de hogares conectadas. A medida que los sensores PPG se vuelven más pequeños y precisos, siguen impulsando la mayor parte de la adopción pediátrica usable.
Se prevé que el segmento de bioimpedancia registrará el crecimiento más rápido de 2025 a 2032, impulsado por sus aplicaciones en expansión para vigilar la hidratación, el esfuerzo respiratorio y la calidad del sueño en las poblaciones pediátricas. La tecnología de impacto biológico ofrece información sobre múltiples funciones fisiológicas que van más allá de lo que proporcionan los sensores tradicionales de PPG y ECG. El aumento de la investigación se centra en la salud pediátrica del sueño y la vigilancia respiratoria está creando oportunidades para los desgastes basados en bioimpresión. Las vías de la FDA están acomodando cada vez más dispositivos multiparamétricos, abriendo la puerta para aprobaciones regulatorias más amplias. A medida que estos dispositivos pasan de las herramientas de investigación a la integración del uso clínico y de consumo, se espera que los productos de bio-imedancia vean la absorción rápida en el segmento pediátrico.
- By Application
Sobre la base de la aplicación, el mercado de dispositivos pediátricos depurados por la FDA se segmenta en hospitales, cuidadores/cuidores y clínicas ambulatorias/pacientes. El segmento hospitalario dominó el mercado en 2024, con el apoyo de la alta demanda de monitoreo continuo en unidades de cuidados intensivos neonatales (NICU) y pediátricos. Los hospitales dependen de los wearables limpiados por la FDA para garantizar la precisión, el cumplimiento y la integración con sistemas de monitoreo más amplios. El dominio del segmento se debe a la necesidad crítica de soluciones fiables de vigilancia pediátrica en atención aguda, donde las intervenciones oportunas pueden afectar significativamente los resultados de la salud. Los hospitales también sirven como primeros adoptantes de dispositivos avanzados de limpieza de la FDA, estableciendo el estándar para la validación clínica y la confianza. Con fuertes estructuras de reembolso y pruebas clínicas, los hospitales mantienen la mayor cuota de ingresos en esta categoría.
Se espera que el segmento de cuidadores y cuidadores crezcan a la velocidad más rápida durante el período de previsión, alimentado por el aumento de las aprobaciones de la FDA para los productos pediátricos de venta libre (OTC) y la creciente preferencia de cuidador para el monitoreo en casa. Dispositivos como Owlet Dream Sock y Masimo Stork destacan el cambio hacia el empoderamiento de los padres con soluciones de monitoreo confiables y limpias por la FDA fuera del entorno hospitalario. El crecimiento de este segmento se apoya además en el aumento de la conciencia sobre los riesgos para la salud pediátrica, la adopción más elevada de la telesalud y la conveniencia de la vigilancia continua en el hogar. A medida que los sistemas de salud fomentan la vigilancia remota de los pacientes para reducir la carga hospitalaria, se prevé que el segmento de atención en el hogar sea la categoría de aplicación más rápida.
FDA-Cleared Pediatric Devices Wearable Market Regional Analysis
- América del Norte dominaba el mercado de dispositivos pediátricos limpias por la FDA con la mayor cuota de ingresos de alrededor del 39% en 2024, caracterizado por marcos regulatorios favorables, fuerte adopción de soluciones de salud digital, y la presencia de jugadores pioneros
- Los cuidadores y proveedores de atención médica de la región valoran altamente la precisión, seguridad y las ideas en tiempo real ofrecidas por los wearables pediátricos depurados por la FDA, junto con su integración perfecta en las plataformas de telesalubridad y monitoreo remoto de pacientes
- Esta adopción generalizada es apoyada además por una infraestructura de salud avanzada, una alta conciencia de la vigilancia de la salud pediátrica y programas de reembolso favorables, estableciendo los wearables pediátricos purificados por la FDA como solución de confianza tanto en los entornos clínicos como en el hogar
US FDA-Cleared Pediatric Devices Wearable Market Insight
El mercado de dispositivos pediátricos limpiados por la FDA capturó la mayor cuota de ingresos del 79% en 2024 dentro de América del Norte, alimentada por fuerte apoyo regulatorio de la FDA y la creciente demanda parental de herramientas de monitoreo seguras y validadas clínicamente. Los cuidadores priorizan cada vez más el monitoreo continuo de signos vitales, el sueño y las condiciones crónicas a través de dispositivos despejados por la FDA que aseguran la fiabilidad sobre los desgastes de calidad del consumidor. La tendencia a la integración de la telesalud, junto con el soporte de seguro para el monitoreo remoto de pacientes (RPM), está acelerando la adopción. Además, una fuerte colaboración entre los fabricantes de dispositivos y los principales hospitales infantiles está ampliando aún más la huella del mercado.
EuropaDispositivos portátiles liberados por la FDAMarket Insight
Se proyecta que el mercado de dispositivos pediátricos limpiados por la FDA en Europa se expanda en un CAGR sustancial durante todo el período previsto, impulsado principalmente por el aumento de la digitalización de la salud, los estrictos estándares de seguridad de los dispositivos médicos y el aumento de las inversiones en monitoreo remoto pediátrico. El aumento de la conciencia entre los padres acerca de los riesgos repentinos de salud infantil y la importancia de la detección temprana es impulsar la adopción. La región está presenciando una amplia captación de dispositivos despejados por la FDA no sólo en los hospitales sino también en los hogares, con políticas de reembolso en algunos países que apoyan un acceso más amplio. Los wearables pediátricos se integran cada vez más en programas de gestión de enfermedades crónicas, fortaleciendo aún más el crecimiento del mercado.
U.K.Dispositivos portátiles liberados por la FDAMarket Insight
Se prevé que el mercado de dispositivos pediátricos depurados por la FDA crezca en un CAGR notable durante el período de previsión, impulsado por la adopción de soluciones de salud digital dentro del NHS y el creciente énfasis en el monitoreo del bienestar infantil. Las preocupaciones relativas a las condiciones respiratorias y cardíacas pediátricas son hospitales y padres que fomentan la adopción de dispositivos clínicos aprobados. La rápida adopción de sistemas de salud conectados por el Reino Unido y su fuerte alineación normativa con las normas médicas internacionales apoyan aún más el crecimiento. Se espera que la ampliación de los servicios de telesalud y la tendencia a la vigilancia del hogar sigan siendo los aceleradores clave del crecimiento.
AlemaniaDispositivos portátiles liberados por la FDAMarket Insight
Se espera que el mercado de dispositivos pediátricos limpiados por la FDA se expanda en un CAGR considerable durante el período de previsión, alimentado por una fuerte demanda de sistemas de monitoreo tecnológicamente avanzados y clínicamente fiables. El énfasis del país en la innovación sanitaria y la integración digital de la salud está impulsando la adopción tanto en hospitales como en entornos de atención a domicilio. Los padres y proveedores alemanes valoran la seguridad, privacidad y precisión de los productos pediátricos de la FDA, alineados con los altos estándares de la nación para la tecnología médica. La expansión de los programas de RPM pediátrica y las colaboraciones entre hospitales y fabricantes de dispositivos están fomentando aún más el crecimiento.
Asia y el PacíficoDispositivos portátiles liberados por la FDAMarket Insight
El mercado de dispositivos pediátricos limpiados por la FDA en Asia-Pacífico está preparado para crecer en la CAGR más rápida del 23,5% durante el período de previsión de 2025 a 2032, impulsado por la digitalización rápida de la salud, el aumento de la conciencia de la vigilancia de la salud pediátrica y un aumento de las condiciones crónicas pediátricas en países como China, Japón e India. Las iniciativas de salud inteligente respaldadas por el Gobierno y la mejora del acceso a la atención médica están impulsando la adopción de dispositivos. El papel de la región como centro de fabricación para usos médicos también permite la asequibilidad y la accesibilidad, lo que lleva a los consumidores urbanos premium y a las poblaciones emergentes de clase media.
JapónDispositivos portátiles liberados por la FDAMarket Insight
El mercado de dispositivos pediátricos limpiados por la FDA Japón está ganando impulso debido a la fuerte cultura del país de innovación médica, sistemas hospitalarios avanzados y la alta adopción de tecnologías conectadas. Los padres japoneses están adoptando cada vez más dispositivos validados clínicamente para monitorear la apnea del sueño, la angustia respiratoria y la salud cardíaca en los niños. La integración de los wearables pediátricos con las plataformas hospitalarias y de atención a domicilio basadas en IoT está acelerando la adopción. Además, la población de cuidadores envejecidos de Japón está impulsando la necesidad de soluciones de monitoreo convenientes y automatizadas, fortaleciendo el papel de los cansables pediátricos tanto en el hogar como en el ambiente clínico.
IndiaDispositivos portátiles liberados por la FDAMarket Insight
El mercado de dispositivos pediátricos limpiados por la FDA en la India representó la mayor cuota de ingresos del mercado en Asia-Pacífico en 2024, atribuida a la rápida urbanización, el aumento de las tasas de natalidad y la fuerte demanda de soluciones de vigilancia de la salud infantil entre la clase media en expansión. El impulso del gobierno para la salud digital y el crecimiento de los hospitales pediátricos privados están impulsando la adopción de los wearables de la FDA. La asequibilidad y la producción localizada de dispositivos de monitoreo fomentan aún más la captación, especialmente en centros urbanos. Se espera que la concienciación sobre los riesgos repentinos de salud infantil, junto con la aceptación cada vez mayor de las tecnologías sanitarias basadas en el hogar, impulse la expansión del mercado a largo plazo.
FDA-Cleared Pediatric Devices Wearable Market Share
La industria de dispositivos pediátricos limpia de la FDA está dirigida principalmente por empresas bien establecidas, incluyendo:
- Sibel Health, Inc. (U.S.)
- Laboratorios de Strados (U.S.)
- BioIntelliSense, Inc. (U.S.)
- Masimo (Estados Unidos)
- Aevice Health Pte Ltd (Singapur)
- Empatica Inc. (U.S.)
- CardiacSense Ltd (Israel)
- Owlet (U.S.)
- Medtronic (Irlanda)
- Fitbit LLC (Estados Unidos)
- AMIT International Group FZE. (Suiza)
- SAMSUNG. (Corea del Sur)
- Abbott (U.S.)
- Dexcom, Inc. (U.S.)
- Koninklijke Philips N.V. (Países Bajos)
- NIHON KOHDEN CORPORATION (Japón)
- ResMed Inc. (U.S.)
- AliveCor, Inc. (U.S.)
- Withings (Francia)
¿Cuáles son los desarrollos recientes en el mercado mundial de dispositivos portátiles liberados por la FDA?
- En junio de 2025, la FDA aprobó la Banda Sonu por SoundHealth como el primer tratamiento sin medicamentos para la congestión nasal moderada a severa en niños mayores de 12 años, ampliando la indicación pediátrica para el dispositivo
- En mayo de 2025, el estetoscopio portátil inteligente AeviceMD de AeviceMD recibió autorización de la FDA estadounidense para su uso en pacientes pediátricos mayores de 3 años, lo que lo convierte en una herramienta respiratoria doméstica de vigilancia continua para niños
- En noviembre de 2024, Theranica recibió una indicación de edad ampliada de la FDA para su dispositivo portátil Nerivio REN, permitiendo un tratamiento agudo de migraña en niños mayores de 8 años. Esto lo convirtió en la primera terapia de neuromodulación limpia de la FDA, sin medicamentos específicamente indicado para la migraña pediátrica
- En julio de 2024, Strados Labs completó con éxito un estudio de validación pediátrica de asma de su tecnología RESP Biosensor en el Hospital Infantil Ann & Robert H. Lurie de Chicago para detectar sibilancias en niños, un paso para asegurar la limpieza de la FDA específica para el dispositivo
- En febrero de 2024, Sibel Health anunció su plataforma de monitoreo utilizable ANNE One recibió su 4a FDA 510(k) de limpieza, extendiendo mediciones continuas de ECG ambulatorio, SpO2, temperatura y presión arterial no invasiva a adolescentes de 12 años y más para entornos hospitalarios y domésticos
SKU-
Obtenga acceso en línea al informe sobre la primera nube de inteligencia de mercado del mundo
- Panel de análisis de datos interactivo
- Panel de análisis de empresas para oportunidades con alto potencial de crecimiento
- Acceso de analista de investigación para personalización y consultas
- Análisis de la competencia con panel interactivo
- Últimas noticias, actualizaciones y análisis de tendencias
- Aproveche el poder del análisis de referencia para un seguimiento integral de la competencia
Metodología de investigación
La recopilación de datos y el análisis del año base se realizan utilizando módulos de recopilación de datos con muestras de gran tamaño. La etapa incluye la obtención de información de mercado o datos relacionados a través de varias fuentes y estrategias. Incluye el examen y la planificación de todos los datos adquiridos del pasado con antelación. Asimismo, abarca el examen de las inconsistencias de información observadas en diferentes fuentes de información. Los datos de mercado se analizan y estiman utilizando modelos estadísticos y coherentes de mercado. Además, el análisis de la participación de mercado y el análisis de tendencias clave son los principales factores de éxito en el informe de mercado. Para obtener más información, solicite una llamada de un analista o envíe su consulta.
La metodología de investigación clave utilizada por el equipo de investigación de DBMR es la triangulación de datos, que implica la extracción de datos, el análisis del impacto de las variables de datos en el mercado y la validación primaria (experto en la industria). Los modelos de datos incluyen cuadrícula de posicionamiento de proveedores, análisis de línea de tiempo de mercado, descripción general y guía del mercado, cuadrícula de posicionamiento de la empresa, análisis de patentes, análisis de precios, análisis de participación de mercado de la empresa, estándares de medición, análisis global versus regional y de participación de proveedores. Para obtener más información sobre la metodología de investigación, envíe una consulta para hablar con nuestros expertos de la industria.
Personalización disponible
Data Bridge Market Research es líder en investigación formativa avanzada. Nos enorgullecemos de brindar servicios a nuestros clientes existentes y nuevos con datos y análisis que coinciden y se adaptan a sus objetivos. El informe se puede personalizar para incluir análisis de tendencias de precios de marcas objetivo, comprensión del mercado de países adicionales (solicite la lista de países), datos de resultados de ensayos clínicos, revisión de literatura, análisis de mercado renovado y base de productos. El análisis de mercado de competidores objetivo se puede analizar desde análisis basados en tecnología hasta estrategias de cartera de mercado. Podemos agregar tantos competidores sobre los que necesite datos en el formato y estilo de datos que esté buscando. Nuestro equipo de analistas también puede proporcionarle datos en archivos de Excel sin procesar, tablas dinámicas (libro de datos) o puede ayudarlo a crear presentaciones a partir de los conjuntos de datos disponibles en el informe.