Global Medical Device Clinical Investigation Advisory Solutions Market
Tamaño del mercado en miles de millones de dólares
Tasa de crecimiento anual compuesta (CAGR) :
% 
 USD
186.21 Million
USD
446.13 Million
2025
2033
USD
186.21 Million
USD
446.13 Million
2025
2033
| 2026 –2033 | |
| USD 186.21 Million | |
| USD 446.13 Million | |
|
|
|
|
Segmentación del mercado global de soluciones de asesoramiento para la investigación clínica de dispositivos médicos, por tipo de servicio (asesoramiento regulatorio y gestión de ensayos clínicos), usuario final (empresas de dispositivos médicos y organizaciones de investigación por contrato [CRO]): tendencias de la industria y pronóstico hasta 2033.
Tamaño del mercado de soluciones de asesoramiento para la investigación clínica de dispositivos médicos
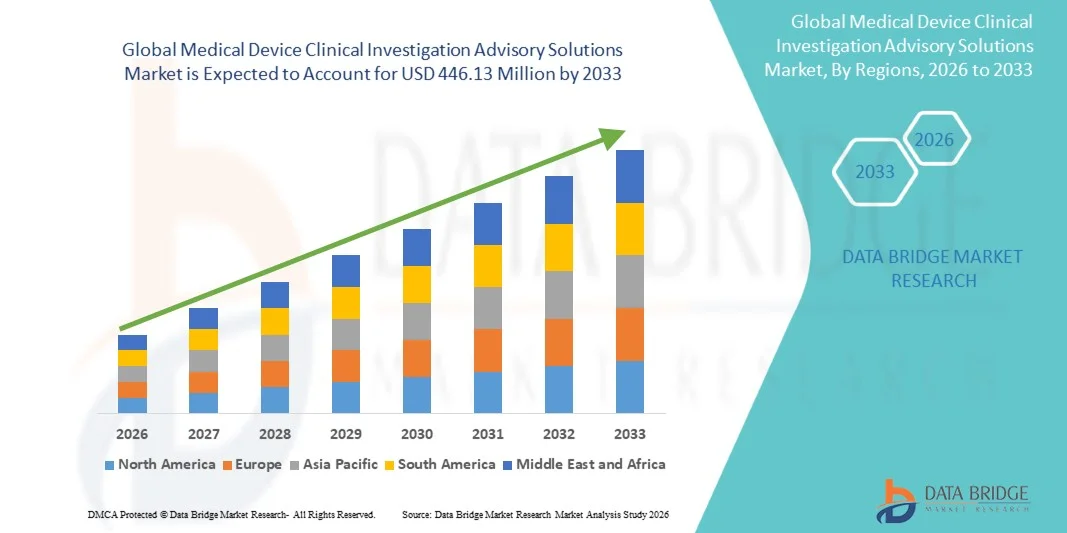
- El tamaño del mercado global de soluciones de asesoramiento en investigación clínica de dispositivos médicos se valoró en USD 186,21 millones en 2025 y se espera que alcance los USD 446,13 millones para 2033 , con una CAGR del 11,54 % durante el período de pronóstico.
- El crecimiento del mercado se ve impulsado en gran medida por la creciente complejidad de los marcos regulatorios en la industria de dispositivos médicos, junto con la creciente adopción de la subcontratación de servicios de asesoramiento en investigación clínica para garantizar aprobaciones de productos más rápidas y cumplimiento en los mercados globales.
- Además, la creciente demanda de orientación para ensayos clínicos rentable y dirigida por expertos está impulsando a los fabricantes de dispositivos médicos a recurrir a soluciones de asesoramiento especializadas, lo que impulsa significativamente el crecimiento de la industria.
Análisis del mercado de soluciones de asesoramiento para la investigación clínica de dispositivos médicos
- Las soluciones de asesoramiento para la investigación clínica de dispositivos médicos, que ofrecen orientación experta y apoyo regulatorio para ensayos clínicos, son cada vez más vitales para que los fabricantes de dispositivos médicos aceleren las aprobaciones de productos, garanticen el cumplimiento y optimicen las operaciones clínicas en los mercados globales.
- La creciente demanda de estas soluciones de asesoramiento se ve impulsada principalmente por la creciente complejidad de los marcos regulatorios, la necesidad de un tiempo de comercialización más rápido y la creciente adopción de la subcontratación por parte de las empresas de dispositivos médicos que buscan un apoyo de ensayos especializado y rentable.
- América del Norte dominó el mercado de soluciones de asesoramiento en investigación clínica de dispositivos médicos con la mayor participación en los ingresos del 39,2 % en 2025, caracterizada por una fuerte presencia de empresas clave de dispositivos médicos, una infraestructura de investigación clínica madura y estrictos requisitos regulatorios.
- Se espera que Asia-Pacífico sea la región de más rápido crecimiento en el mercado durante el período de pronóstico debido al rápido crecimiento de la industria de dispositivos médicos, el aumento de las actividades de ensayos clínicos y una mayor subcontratación de servicios regulatorios y de asesoría.
- El segmento de Asesoría Regulatoria dominó la mayor participación de ingresos del mercado con un 58,4 % en 2025, impulsado por la creciente complejidad de las regulaciones de dispositivos médicos en regiones como América del Norte, Europa y Asia-Pacífico.
Alcance del informe y segmentación del mercado de soluciones de asesoramiento para la investigación clínica de dispositivos médicos
|
Atributos |
Soluciones de asesoramiento para la investigación clínica de dispositivos médicos: información clave del mercado |
|
Segmentos cubiertos |
|
|
Países cubiertos |
América del norte
Europa
Asia-Pacífico
Oriente Medio y África
Sudamerica
|
|
Actores clave del mercado |
|
|
Oportunidades de mercado |
|
|
Conjuntos de información de datos de valor añadido |
Además de los conocimientos sobre escenarios de mercado, como el valor de mercado, la tasa de crecimiento, la segmentación, la cobertura geográfica y los principales actores, los informes de mercado seleccionados por Data Bridge Market Research también incluyen un análisis en profundidad de expertos, epidemiología de pacientes, análisis de la cartera de productos, análisis de precios y marco regulatorio. |
Tendencias del mercado de soluciones de asesoramiento para la investigación clínica de dispositivos médicos
“ Aumento de la adopción de servicios de asesoramiento en investigación clínica avanzada ”
- Una tendencia notable en el mercado global de soluciones de asesoramiento para la investigación clínica de dispositivos médicos es la creciente adopción de servicios de asesoramiento especializados para respaldar ensayos clínicos, presentaciones regulatorias y vigilancia posterior a la comercialización de dispositivos médicos.
- Las empresas invierten cada vez más en soluciones que ayudan a agilizar el diseño de estudios clínicos, el desarrollo de protocolos y el cumplimiento normativo para reducir el tiempo de comercialización y mitigar los riesgos.
- Por ejemplo, en 2024, varios fabricantes de dispositivos médicos en América del Norte se asociaron con proveedores de soluciones de asesoramiento para optimizar sus estrategias de ensayos clínicos y garantizar aprobaciones regulatorias más rápidas.
- También existe una creciente demanda de soluciones integradas que combinen experiencia científica, regulatoria y operativa para ayudar a los fabricantes a realizar investigaciones clínicas de alta calidad y que cumplan con las normas de manera eficiente.
- Esta tendencia refleja la creciente complejidad de los marcos regulatorios y la necesidad de orientación experta durante todo el ciclo de vida del producto, lo que impulsa la adopción de servicios de asesoramiento en investigación clínica a nivel mundial.
Dinámica del mercado de soluciones de asesoramiento para la investigación clínica de dispositivos médicos
Conductor
Creciente necesidad de cumplimiento normativo y gestión eficiente de ensayos clínicos
- Los crecientes requisitos regulatorios para los dispositivos médicos, incluidos los estrictos estándares de seguridad y eficacia, son un impulsor principal para la adopción de soluciones de asesoramiento.
- Los fabricantes buscan apoyo de expertos para abordar regulaciones complejas, preparar presentaciones y garantizar el cumplimiento con organismos como la FDA, la EMA y otras autoridades regionales.
- Por ejemplo, a principios de 2025, una empresa europea de dispositivos médicos contrató servicios de asesoramiento para facilitar el cumplimiento de las nuevas regulaciones MDR de la UE, reduciendo el riesgo de retrasos en la aprobación.
- Además, la necesidad de optimizar la eficiencia de los ensayos clínicos, reducir los costos operativos y acortar los ciclos de desarrollo de productos está impulsando la demanda de estas soluciones.
- La creciente conciencia sobre la seguridad del paciente, la calidad de la evidencia clínica y la gestión de riesgos está alentando aún más a los fabricantes a confiar en servicios de asesoramiento profesional para fortalecer los diseños y resultados de los estudios.
Restricción/Desafío
“ Altos costos y disponibilidad limitada de conocimientos especializados ”
- El costo relativamente alto de contratar servicios de asesoramiento en investigación clínica de dispositivos médicos puede ser una barrera para los fabricantes pequeños y medianos, en particular en los mercados emergentes.
- Las soluciones de asesoramiento avanzadas a menudo requieren contratos o honorarios a largo plazo, lo que puede resultar prohibitivo para organizaciones con presupuestos limitados.
- Por ejemplo, varias empresas emergentes en Asia retrasaron la contratación de servicios de asesoría en 2023 debido a restricciones presupuestarias, lo que afectó el ritmo de sus investigaciones clínicas.
- La disponibilidad limitada de asesores calificados y experimentados en ciertas regiones también restringe la penetración en el mercado y puede provocar retrasos en los proyectos.
- Abordar estos desafíos mediante modelos de servicio rentables, expansión regional de empresas de asesoría y opciones de consultoría remota será clave para el crecimiento sostenido del mercado.
Alcance del mercado de soluciones de asesoramiento para la investigación clínica de dispositivos médicos
El mercado está segmentado según el tipo de servicio y los usuarios finales.
• Por tipo de servicio
Según el tipo de servicio, el mercado de Soluciones de Asesoramiento en Investigación Clínica de Dispositivos Médicos se segmenta en Asesoramiento Regulatorio y Gestión de Ensayos Clínicos. El segmento de Asesoramiento Regulatorio dominó la mayor cuota de mercado en ingresos, con un 58,4%, en 2025, impulsado por la creciente complejidad de las regulaciones de dispositivos médicos en regiones como Norteamérica, Europa y Asia-Pacífico. Las empresas de dispositivos médicos dependen en gran medida de los servicios de asesoramiento regulatorio para gestionar las aprobaciones previas a la comercialización, el cumplimiento normativo posterior a la comercialización y los procesos de presentación. El creciente énfasis en la seguridad del paciente y los estándares de calidad de los productos impulsa la demanda. Los consultores regulatorios brindan orientación sobre gestión de riesgos, etiquetado y documentación, lo que garantiza un acceso más rápido al mercado. Los estrictos requisitos de cumplimiento de organismos como la FDA, la EMA y la PMDA aumentan la dependencia de estos servicios. Los avances tecnológicos en las presentaciones electrónicas y el seguimiento regulatorio digital aumentan aún más la eficiencia. El segmento se beneficia de contratos a largo plazo con fabricantes de dispositivos médicos de primer nivel. El creciente volumen de lanzamiento de dispositivos innovadores e instrumentos de diagnóstico de alto valor impulsa una demanda constante. Los servicios de asesoramiento regulatorio reducen los riesgos legales y operativos para los fabricantes. El creciente enfoque en la armonización global de normas refuerza el dominio del segmento. La externalización de la experiencia regulatoria permite a las empresas optimizar costos y acelerar el tiempo de comercialización. Estos factores, en conjunto, convierten la asesoría regulatoria en el segmento de servicio más importante.
Se espera que el segmento de Gestión de Ensayos Clínicos experimente la tasa de crecimiento anual compuesta (TCAC) más rápida, del 11,3 %, entre 2026 y 2033, impulsada por el creciente número de ensayos clínicos y estudios poscomercialización de dispositivos médicos nuevos e innovadores. La creciente adopción de plataformas digitales de gestión de ensayos garantiza una planificación, un reclutamiento de pacientes, una monitorización y una elaboración de informes optimizados. La externalización de la gestión de ensayos clínicos a proveedores especializados reduce la carga operativa de las empresas de dispositivos. La creciente complejidad de los ensayos multicéntricos y la necesidad de captura de datos en tiempo real impulsan el crecimiento. Las autoridades reguladoras están priorizando la integridad de los datos, la preparación para auditorías y la monitorización basada en riesgos, lo que aumenta la demanda. La expansión de las líneas de I+D de dispositivos médicos en los mercados emergentes impulsa la adopción. Las CRO ofrecen cada vez más soluciones integrales de gestión de ensayos para una mayor eficiencia. La analítica avanzada y la monitorización basada en IA en la gestión de ensayos mejoran la precisión y reducen los plazos. La demanda de soluciones rentables durante el desarrollo de dispositivos impulsa la adopción. La integración con historiales clínicos electrónicos y dispositivos portátiles acelera la eficiencia de los ensayos clínicos. La creciente tendencia de los ensayos centrados en el paciente mejora la adopción. Estos factores en conjunto hacen que la gestión de ensayos clínicos sea el segmento de servicio de más rápido crecimiento.
• Por los usuarios finales
En función de los usuarios finales, el mercado de Soluciones de Asesoramiento para la Investigación Clínica de Dispositivos Médicos se segmenta en Empresas de Dispositivos Médicos y Organizaciones de Investigación por Contrato (CRO). El segmento de Empresas de Dispositivos Médicos representó la mayor cuota de mercado en ingresos, con un 64,7 %, en 2025, impulsado por el creciente número de lanzamientos de dispositivos médicos a nivel mundial y la necesidad de cumplir con las estrictas normas regulatorias. Las empresas dependen en gran medida de servicios de asesoría externos para acelerar la entrada al mercado y mantener el cumplimiento normativo. La creciente complejidad de las clasificaciones de productos, las pruebas de seguridad y la vigilancia poscomercialización impulsa la demanda. Los fabricantes de dispositivos, grandes y medianos, externalizan la experiencia regulatoria y clínica para optimizar costes y garantizar la rapidez de comercialización. La rápida innovación en dispositivos de diagnóstico, quirúrgicos e implantables aumenta la dependencia de las soluciones de asesoría. Las empresas requieren apoyo continuo para los cambios de etiquetado, la notificación de eventos adversos y la preparación de auditorías. Las iniciativas de armonización global, como la ISO 13485 y la MDR, impulsan su adopción. Las alianzas con CRO y firmas de asesoría mejoran la eficiencia operativa. Se minimizan los retrasos regulatorios, lo que reduce el riesgo comercial. Los contratos de alto valor y las alianzas de asesoría a largo plazo refuerzan el dominio del segmento. Las empresas de Norteamérica y Europa lideran la adopción, pero los mercados emergentes contribuyen cada vez más. Estos factores, en conjunto, convierten a las empresas de dispositivos médicos en el segmento dominante de usuarios finales.
Se espera que el segmento de Organizaciones de Investigación por Contrato (CRO) experimente la tasa de crecimiento anual compuesta (TCAC) más rápida, del 10,2 %, entre 2026 y 2033, impulsada por la creciente tendencia a la externalización de ensayos clínicos y servicios de apoyo regulatorio. Las CRO buscan cada vez más soluciones de asesoramiento para ampliar su oferta de servicios y mejorar la eficiencia operativa. El aumento de los ensayos clínicos multicéntricos y globales exige una gestión eficiente de los ensayos y asesoramiento sobre el cumplimiento normativo. La creciente colaboración entre los fabricantes de dispositivos y las CRO impulsa el crecimiento. Los avances tecnológicos, como la monitorización basada en IA y las plataformas de ensayos digitales, impulsan la adopción. Las CRO buscan reducir los plazos y los costes operativos, a la vez que garantizan la calidad de los datos y el cumplimiento normativo. La expansión de los servicios a los mercados emergentes impulsa la adopción. La fuerte demanda de experiencia especializada en categorías de dispositivos de alto riesgo acelera el crecimiento. Las CRO recurren a los servicios de asesoramiento para garantizar el éxito de las presentaciones regulatorias y mitigar los riesgos. Las crecientes inversiones en infraestructura sanitaria y los lanzamientos de dispositivos innovadores amplían aún más el potencial del mercado. La adopción de modelos de ensayos virtuales e híbridos promueve la confianza en las soluciones de asesoramiento. Estos factores, en conjunto, convierten a las CRO en el segmento de usuarios finales de más rápido crecimiento.
Análisis regional del mercado de soluciones de asesoramiento para la investigación clínica de dispositivos médicos
- América del Norte dominó el mercado de soluciones de asesoramiento para investigación clínica de dispositivos médicos con la mayor participación en los ingresos del 39,2 % en 2025.
- Impulsado por un ecosistema de atención médica maduro, una alta concentración de empresas de dispositivos médicos y marcos regulatorios sólidos que respaldan la investigación clínica.
- La región se beneficia de infraestructuras avanzadas de ensayos clínicos, profesionales de investigación altamente capacitados y sistemas de cumplimiento normativo bien establecidos, que fomentan la subcontratación de servicios de asesoramiento para el desarrollo de dispositivos médicos, la validación clínica y las presentaciones reglamentarias.
Perspectivas del mercado de soluciones de asesoramiento para la investigación clínica de dispositivos médicos en EE. UU.
El mercado estadounidense de soluciones de asesoría para la investigación clínica de dispositivos médicos captó la mayor parte de los ingresos de Norteamérica en 2025, impulsado por la alta adopción de servicios de asesoría clínica externalizados y la creciente necesidad de experiencia regulatoria en la aprobación de dispositivos médicos. Las empresas recurren cada vez más a firmas de asesoría especializadas para diseñar estudios clínicos, desarrollar estrategias regulatorias y gestionar eficientemente las solicitudes. Esto es especialmente importante para los dispositivos nuevos que requieren aprobación previa a la comercialización o el cumplimiento de las regulaciones de la FDA. La sólida infraestructura de investigación del país, junto con un enfoque en la innovación y la agilización de las aprobaciones de dispositivos, continúa impulsando el crecimiento del mercado.
Análisis del mercado de soluciones de asesoramiento para la investigación clínica de dispositivos médicos en Europa
Se prevé que el mercado europeo de soluciones de asesoramiento para la investigación clínica de dispositivos médicos se expanda a una tasa de crecimiento anual compuesta (TCAC) sustancial durante el período de pronóstico, impulsado por regulaciones estrictas como el Reglamento de Dispositivos Médicos (MDR) de la UE, la creciente adopción de dispositivos médicos innovadores y el crecimiento de las iniciativas de investigación clínica. Las empresas externalizan cada vez más servicios de asesoramiento clínico para gestionar los complejos requisitos de cumplimiento normativo, gestionar ensayos multicéntricos y agilizar la tramitación de solicitudes regulatorias.
Análisis del mercado de soluciones de asesoramiento para la investigación clínica de dispositivos médicos en el Reino Unido
Se prevé un crecimiento constante del mercado británico de soluciones de asesoramiento para la investigación clínica de dispositivos médicos, respaldado por un ecosistema sanitario consolidado, una sólida infraestructura de investigación clínica e iniciativas gubernamentales que promueven la innovación en dispositivos médicos. El entorno regulatorio del país fomenta la externalización de la gestión de ensayos clínicos, la estrategia regulatoria y el cumplimiento de las normas MDR del Reino Unido y las internacionales. El auge de los dispositivos médicos mínimamente invasivos y tecnológicamente avanzados también ha incrementado la demanda de asesoramiento experto en validación clínica y estrategias de entrada al mercado.
Análisis del mercado de soluciones de asesoramiento para la investigación clínica de dispositivos médicos en Alemania
El mercado alemán de soluciones de asesoramiento para la investigación clínica de dispositivos médicos contribuye de forma clave al crecimiento del mercado europeo, impulsado por su consolidada infraestructura sanitaria, la alta adopción de tecnologías médicas y un fuerte énfasis en la investigación y el desarrollo. Los fabricantes alemanes de dispositivos médicos recurren cada vez más a soluciones de asesoramiento para la investigación clínica para cumplir con la normativa MDR, diseñar ensayos clínicos eficaces y obtener una aprobación más rápida para dispositivos innovadores. El enfoque del país en la medicina de precisión, las tecnologías de salud digital y los diagnósticos de vanguardia impulsa aún más la demanda de servicios de asesoramiento externalizados.
Análisis del mercado de soluciones de asesoramiento para la investigación clínica de dispositivos médicos en Asia-Pacífico
Se prevé que el mercado de soluciones de asesoría para la investigación clínica de dispositivos médicos en Asia-Pacífico sea la región de mayor crecimiento durante el período de pronóstico debido a la rápida expansión de la industria de dispositivos médicos, la creciente externalización de servicios de asesoría clínica y el aumento de los requisitos regulatorios. El crecimiento de la infraestructura sanitaria, la expansión de la fabricación de dispositivos médicos y el acceso rentable a servicios de asesoría son factores clave para el crecimiento. Países como China, India y Japón están experimentando una mayor demanda de servicios de asesoría clínica para garantizar el cumplimiento normativo y la aprobación del mercado de dispositivos innovadores.
Análisis del mercado de soluciones de asesoramiento para la investigación clínica de dispositivos médicos en Japón
El crecimiento del mercado japonés de soluciones de asesoría para la investigación clínica de dispositivos médicos se ve impulsado por su avanzado sector sanitario, el envejecimiento de la población y la fuerte demanda de dispositivos médicos innovadores. Las empresas de asesoría clínica apoyan a los fabricantes de dispositivos con la presentación de solicitudes regulatorias, el diseño de ensayos clínicos y el cumplimiento de las normas locales, lo que permite una validación clínica eficiente y un acceso más rápido al mercado.
Análisis del mercado de soluciones de asesoramiento para la investigación clínica de dispositivos médicos en China
El mercado chino de soluciones de asesoría para la investigación clínica de dispositivos médicos registró la mayor participación en ingresos de la región Asia-Pacífico en 2025, impulsado por una industria nacional de dispositivos médicos en rápida expansión, iniciativas gubernamentales que promueven el cumplimiento normativo y la colaboración con firmas de asesoría globales. Este entorno ha facilitado ciclos de aprobación más cortos y mejorado el acceso al mercado de dispositivos médicos, impulsando aún más la demanda de soluciones de asesoría para la investigación clínica.
Cuota de mercado de soluciones de asesoramiento para la investigación clínica de dispositivos médicos
La industria de soluciones de asesoramiento en investigación clínica de dispositivos médicos está liderada principalmente por empresas bien establecidas, entre las que se incluyen:
- Medpace (EE. UU.)
- ICON plc (Irlanda)
- PPD Inc. (EE. UU.)
- Parexel International (EE. UU.)
- Laboratorios Charles River (EE. UU.)
- Covance Inc. (EE. UU.)
- Servicios de ensayos clínicos de Medtronic (EE. UU.)
- Syneos Health (EE. UU.)
- Eurofins Scientific (Luxemburgo)
- Desarrollo de productos farmacéuticos (PPD) (EE. UU.)
- Wuxi AppTec (China)
- SGS Life Sciences (Suiza)
- Desarrollo de fármacos de Labcorp (EE. UU.)
- Parexel International Corp (EE. UU.)
- CRF Health (Reino Unido)
- PRA Health Sciences (EE. UU.)
- Accenture Life Sciences (Irlanda)
- Covance (EE. UU.)
- Clinipace (EE. UU.)
Últimos avances en el mercado global de soluciones de asesoramiento para la investigación clínica de dispositivos médicos
- En enero de 2025, Tigermed amplió su asociación estratégica con Medidata para acelerar los ensayos clínicos de dispositivos médicos utilizando la plataforma digital de Medidata, automatizando la captura de datos y agilizando las operaciones de CRO en estudios clínicos globales, mejorando la eficiencia de la gestión de ensayos.
- En enero de 2025, NAMSA adquirió las operaciones de pruebas de dispositivos médicos de WuXi AppTec en EE. UU., ampliando su cartera de soluciones de investigación y pruebas clínicas para brindar servicios de asesoramiento preclínico y clínico más completos para los fabricantes de dispositivos que buscan aprobaciones regulatorias y preparación para el mercado.
- En enero de 2025, Canyon Labs completó la adquisición del negocio de servicios de laboratorio y consultoría de iuvo BioScience, fortaleciendo sus servicios de soporte de CRO como pruebas de biocompatibilidad y pruebas analíticas, que son componentes esenciales de las soluciones de asesoramiento en todo el ciclo de vida del dispositivo médico.
- En febrero de 2025, Arterex adquirió Phoenix, una empresa de diseño y desarrollo de dispositivos médicos con sede en Italia, lo que permitió un mejor soporte integral para el desarrollo clínico y servicios de asesoramiento para pruebas de dispositivos y cumplimiento normativo en los mercados europeos.
- En febrero de 2025, Arterex también adquirió Adroit, ampliando sus capacidades globales de investigación por contrato y fabricación, facilitando así el desarrollo clínico optimizado y los servicios de asesoramiento regulatorio para las empresas de dispositivos.
- En marzo de 2025, InTandem Capital anunció una inversión estratégica en Clinilabs, lo que indica un creciente interés de los inversores en CRO especializadas que prestan servicios de investigación de dispositivos médicos, lo que contribuye indirectamente a los servicios de asesoramiento sobre estrategia de investigación y regulatoria.
- En marzo de 2025, ICON plc amplió sus servicios de subcontratación regulatoria en la región Asia-Pacífico, centrándose en una consulta regulatoria más rápida y específica para la región y en el apoyo a pruebas clínicas para clientes de dispositivos médicos en mercados como China e India.
SKU-
Obtenga acceso en línea al informe sobre la primera nube de inteligencia de mercado del mundo
- Panel de análisis de datos interactivo
- Panel de análisis de empresas para oportunidades con alto potencial de crecimiento
- Acceso de analista de investigación para personalización y consultas
- Análisis de la competencia con panel interactivo
- Últimas noticias, actualizaciones y análisis de tendencias
- Aproveche el poder del análisis de referencia para un seguimiento integral de la competencia
Metodología de investigación
La recopilación de datos y el análisis del año base se realizan utilizando módulos de recopilación de datos con muestras de gran tamaño. La etapa incluye la obtención de información de mercado o datos relacionados a través de varias fuentes y estrategias. Incluye el examen y la planificación de todos los datos adquiridos del pasado con antelación. Asimismo, abarca el examen de las inconsistencias de información observadas en diferentes fuentes de información. Los datos de mercado se analizan y estiman utilizando modelos estadísticos y coherentes de mercado. Además, el análisis de la participación de mercado y el análisis de tendencias clave son los principales factores de éxito en el informe de mercado. Para obtener más información, solicite una llamada de un analista o envíe su consulta.
La metodología de investigación clave utilizada por el equipo de investigación de DBMR es la triangulación de datos, que implica la extracción de datos, el análisis del impacto de las variables de datos en el mercado y la validación primaria (experto en la industria). Los modelos de datos incluyen cuadrícula de posicionamiento de proveedores, análisis de línea de tiempo de mercado, descripción general y guía del mercado, cuadrícula de posicionamiento de la empresa, análisis de patentes, análisis de precios, análisis de participación de mercado de la empresa, estándares de medición, análisis global versus regional y de participación de proveedores. Para obtener más información sobre la metodología de investigación, envíe una consulta para hablar con nuestros expertos de la industria.
Personalización disponible
Data Bridge Market Research es líder en investigación formativa avanzada. Nos enorgullecemos de brindar servicios a nuestros clientes existentes y nuevos con datos y análisis que coinciden y se adaptan a sus objetivos. El informe se puede personalizar para incluir análisis de tendencias de precios de marcas objetivo, comprensión del mercado de países adicionales (solicite la lista de países), datos de resultados de ensayos clínicos, revisión de literatura, análisis de mercado renovado y base de productos. El análisis de mercado de competidores objetivo se puede analizar desde análisis basados en tecnología hasta estrategias de cartera de mercado. Podemos agregar tantos competidores sobre los que necesite datos en el formato y estilo de datos que esté buscando. Nuestro equipo de analistas también puede proporcionarle datos en archivos de Excel sin procesar, tablas dinámicas (libro de datos) o puede ayudarlo a crear presentaciones a partir de los conjuntos de datos disponibles en el informe.