North America Medical Device Testing Market, By Service Type (Testing Services, Inspection Service and Certification Services), Testing Type (Physical Testing, Chemical/Biological Testing, Cybersecurity Testing, Microbiology and Sterility Testing, and Others), Phase (Preclinical and Clinical), Sourcing Type (In-House and Outsourced), Device Class (Class I, Class II and Class III), Product (Active Implant Medical Device, Active Medical Device, Non-active Medical Device, In vitro Diagnostics Medical Device, Opthalmic Medical Device, Orthopedic and Dental Medical Device, Vascular Medical Device, and Others) - Industry Trends and Forecast to 2030.
North America Medical Device Testing Market Analysis and Insights
Medical devices are crucial since they directly impact human lives. Medical device manufacturers follow testing, verification, and validation best practices to ensure the quality and reliability of medical equipment to provide safe and effective healthcare services to patients. There is a high-level overview of implementing medical device testing strategies. Multiple regulatory bodies and compliances govern medical devices. On the other hand, end users expect exceptional performance, effectiveness, and safety from the device that they use. This compels medical device manufacturers to create and deploy testing strategies that work across the development cycle - from concept and design to production.
The rising need for the verification and validation of medical devices globally has enhanced the growth of the market. Some of the major market players are highly focusing on various service launches and service approvals during this crucial period. In addition, the increasing demand for in-vitro tests is also contributing to the rising demand for medical device testing. The North America medical device testing market is growing in the forecast year due to a rise in market players and the availability of advanced services.
However, the barriers to the local development of medical devices and the high cost of medical devices might hamper the growth of the North America medical device testing market in the forecast period.
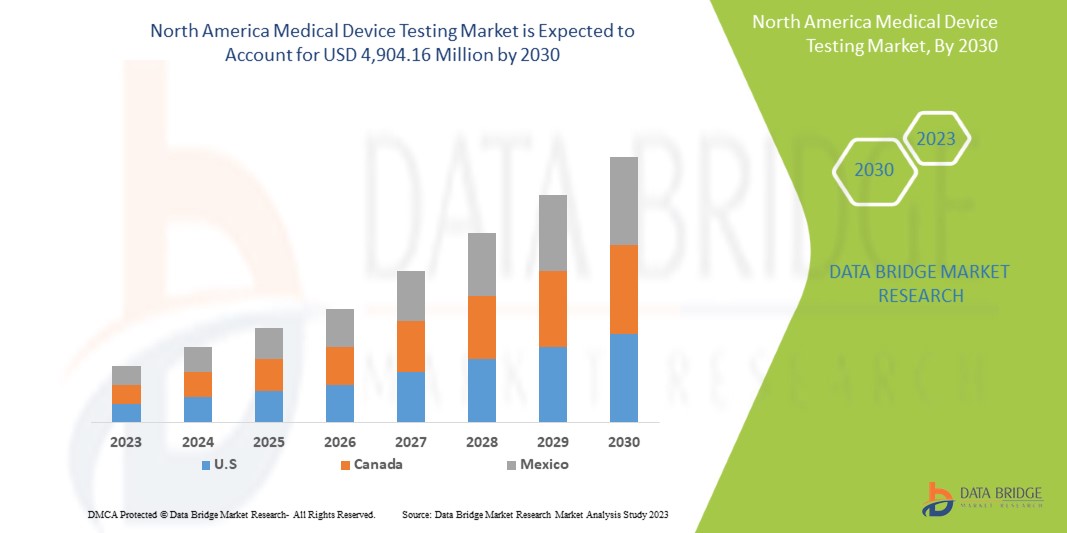
Data Bridge Market Research analyzes that the North America medical device testing market is expected to reach the value of USD 4,904.16 million by 2030, at a CAGR of 12.0% during the forecast period.
|
Report Metric |
Details |
|
Forecast Period |
2023 to 2030 |
|
Base Year |
2022 |
|
Historic Years |
2021 (Customisable to 2015-2020) |
|
Quantitative Units |
Revenue in USD Million |
|
Segments Covered |
Tipo de servicio (servicios de prueba, servicio de inspección y servicios de certificación), tipo de prueba (prueba física, prueba química/biológica, prueba de ciberseguridad, prueba de microbiología y prueba de esterilidad , y otras), fase (preclínica y clínica), tipo de abastecimiento (interno y subcontratado), clase de dispositivo (clase I, clase II y clase III), producto (dispositivo médico de implante activo, dispositivo médico activo, dispositivo médico no activo, dispositivo médico de diagnóstico in vitro, dispositivo médico oftálmico, dispositivo médico ortopédico y dental, dispositivo médico vascular y otros) |
|
Países cubiertos |
Estados Unidos, Canadá y México |
|
Actores del mercado cubiertos |
Intertek Group plc, SGS SA, Bureau Veritas, TUV SUD, TUV Rheinland, Pace, Charles River Laboratories, Biomedical Device Labs, UL LLC, North American Science Associates, LLC, WuXi AppTec, NSF, Laboratory Corporation of America Holdings, Eurofins Scientific, NELSON LABORATORIES, LLC- A SOTERA HEALTH COMPANY, Gateway Analytical, Element Materials Technology, Hohenstein, Cigniti, Q Laboratories e IMR Test Labs, entre otros. |
Definición de mercado
Las pruebas de dispositivos médicos son el proceso de demostrar que el dispositivo funciona de manera confiable y segura durante su uso. En el desarrollo de nuevos productos, se aplican pruebas exhaustivas de validación del diseño. Esto incluye pruebas de rendimiento, toxicidad, análisis químico y, a veces, factores humanos o incluso pruebas clínicas. Las pruebas de control de calidad continuas suelen ser más limitadas. Por lo general, incluyen controles dimensionales, algunas pruebas funcionales y verificación del empaque. En el mercado hay disponibles varios tipos de servicios de pruebas médicas, como servicios de inspección, servicios de certificación y otros.
Dinámica del mercado de pruebas de dispositivos médicos en América del Norte
En esta sección se aborda la comprensión de los factores impulsores, las ventajas, las oportunidades, las limitaciones y los desafíos del mercado. Todo esto se analiza en detalle a continuación:
Conductores
- Necesidad creciente de verificación y validación de dispositivos médicos
La prueba de dispositivos médicos es el proceso de demostrar que el dispositivo realizará diagnósticos y tratamientos de manera confiable y segura. La demanda de dispositivos médicos aumenta constantemente debido a la alta prevalencia de diversas enfermedades en varias regiones del mundo.
Los métodos de verificación y validación están muy extendidos y se utilizan ampliamente en el sector sanitario. En general, la verificación es la fase de desarrollo de un producto si cumple con los requisitos especificados, mientras que la validación comprueba si se ha cumplido el uso previsto y, por tanto, se cumplen las especificaciones de usabilidad. Los tipos más comunes de verificación y validación para dispositivos médicos son la verificación y validación de diseño, de proceso y de software.
Los dispositivos médicos también son cada vez más pequeños y complejos en cuanto a diseño, ya que se utilizan plásticos de ingeniería avanzada. Esto hace que el proceso de validación y verificación (V&V) sea aún más importante. Los resultados son una mejor repetibilidad, menos errores, menos reelaboración y rediseño, un tiempo de comercialización más rápido, una mayor competitividad y menores costos de producción. Además, se prevé que el aumento de los estándares y las regulaciones sobre los servicios de validación y verificación de dispositivos médicos impulse el crecimiento del mercado de pruebas de dispositivos médicos.
- Demanda creciente de pruebas in vitro
Los diagnósticos in vitro (IVD) son pruebas que se realizan en muestras, como sangre o tejido, extraídas del cuerpo humano. Los diagnósticos in vitro pueden detectar enfermedades u otras afecciones y pueden utilizarse para controlar la salud general de una persona y ayudar a curar, tratar o prevenir enfermedades.
Las pruebas in vitro se utilizan para detectar diversas enfermedades, como infecciones por VIH, malaria y hepatitis, entre otras. La prevalencia de estas enfermedades está aumentando rápidamente en todo el mundo, lo que genera una mayor demanda de pruebas in vitro y de diversos dispositivos médicos. Como los dispositivos médicos se han vuelto ampliamente disponibles para diversas enfermedades debido a la rápida fabricación de las empresas de pruebas médicas, es un factor importante que impulsa el crecimiento del mercado.
Oportunidades
- Aumento del gasto sanitario
El gasto en atención sanitaria ha aumentado en todo el mundo a medida que aumenta el ingreso disponible en varios países. Además, para satisfacer las necesidades de la población, los organismos gubernamentales y las organizaciones de atención sanitaria están tomando la iniciativa de acelerar el gasto en atención sanitaria. El aumento del gasto en atención sanitaria ayuda simultáneamente a los centros de atención sanitaria a mejorar sus instalaciones de tratamiento para diversos trastornos en los países.
El aumento del gasto en atención sanitaria también es beneficioso para el crecimiento económico y del sector sanitario, y es fructífero, sobre todo, porque afecta significativamente al desarrollo de productos médicos mejores y más avanzados. Por lo tanto, el aumento del gasto en atención sanitaria es una oportunidad mayor para el crecimiento del mercado de pruebas de dispositivos médicos de América del Norte.
- Desarrollo de IA e IoT en diversos dispositivos médicos
La inteligencia artificial (IA) es una tecnología poderosa y en constante evolución que tiene el potencial de mejorar las capacidades en una multitud de industrias. Los dispositivos médicos con inteligencia artificial prometen revolucionar la industria de la salud, ayudando a los profesionales médicos a diagnosticar y tratar a sus pacientes de manera más precisa y eficaz y a mejorar su atención general. Junto con sus beneficios, la inteligencia artificial de los dispositivos médicos también enfrenta desafíos, incluida la necesidad de una regulación para mantenerse al día con el avance tecnológico.
Por lo tanto, el mercado de pruebas de dispositivos médicos de América del Norte está siendo testigo de una serie de avances en la combinación de medicamentos y dispositivos, la medicina personalizada y una mayor adaptación de varios dispositivos médicos portátiles y ponibles. La implementación de avances tecnológicos como la IoT y la inteligencia artificial en varios dispositivos es un parámetro de crecimiento clave para el mercado global de servicios de pruebas de dispositivos médicos, lo que crea una gran oportunidad.
Desafíos / Restricciones
- Alta competencia en la industria de tecnología médica
Muchas empresas globales se enfrentan a una competencia significativa de muchas empresas, desde grandes empresas de fabricación de dispositivos médicos con múltiples líneas de productos. Algunos actores tienen más recursos financieros y de marketing que otros. La competencia común en el cuidado de la salud involucra varios elementos como precio, calidad, conveniencia y marca. La competencia también puede basarse en nuevas tecnologías e innovación. En general, la competencia reduce las ineficiencias que de otro modo generarían altos costos de producción, que finalmente se trasladan a los consumidores por los altos costos de la atención médica y la prestación. Los productos en el mercado se comercializan en función de las especificaciones del producto, la consistencia del producto, el suministro y el precio. Sin embargo, los consumidores se benefician de la competencia que ofrece recompensas por las actualizaciones continuas del producto y facilita un mayor grado de eficiencia del servicio entre los participantes de la industria. La capacidad de la empresa para competir en el mercado también se ve afectada por los cambios en las preferencias y requisitos de los consumidores, como la creciente demanda de dispositivos médicos más ecológicos que se puedan desechar fácilmente sin dañar el medio ambiente y los productos incorporados con capacidades digitales. Esto muestra una alta competencia en el mercado, lo que es un desafío importante para el mercado.
- Barreras al desarrollo local de dispositivos médicos
Si bien la promoción de normas y el control de los dispositivos médicos es esencial, las regulaciones excesivas, particularmente en el contexto nacional, también pueden actuar como una barrera para la innovación local de esos dispositivos.
Puede obstaculizar la innovación nacional al someter las nuevas tecnologías a un procedimiento de concesión de licencias largo y costoso, lo que aumenta el costo y el tiempo que deben emplear los fabricantes locales, además del costo de fabricación del equipo médico. Algunos productos, que tienen un valor significativo para los países de bajos ingresos, pueden ser retirados del mercado debido a los riesgos percibidos asociados a su uso.
Diversos factores, como los procedimientos de licencia, el costo del equipo médico y varias otras regulaciones para la producción de dispositivos médicos que enfrentan los fabricantes de desarrollo local, todas estas causas pueden obstaculizar el crecimiento del mercado de pruebas de dispositivos médicos.
Acontecimientos recientes
- En abril de 2021, TÜV SÜD anunció que se había presentado en Medtec LIVE para demostrar su capacidad de ser un proveedor integral de pruebas de dispositivos médicos. Los servicios de la empresa abarcan pruebas de seguridad eléctrica y funcional, ciberseguridad y software, compatibilidad electromagnética y biocompatibilidad. Los expertos de TÜV SÜD participaron en el programa de la feria y congreso en línea con varias charlas, un hack en vivo y un discurso de presentación.
- En junio de 2020, Intertek anunció la ampliación de sus servicios de equipos de protección personal para incluir pruebas de precertificación de respiradores N95 según los requisitos establecidos por el Instituto Nacional de Seguridad y Salud Ocupacional (NIOSH). Los nuevos servicios son el resultado de la acreditación exitosa de los Protocolos de prueba estándar de NIOSH, de acuerdo con la norma ISO 17025. Con estos nuevos servicios, Intertek amplía sus soluciones y recursos para apoyar a los clientes y a la comunidad global durante la pandemia de COVID-19.
Alcance del mercado de pruebas de dispositivos médicos de América del Norte
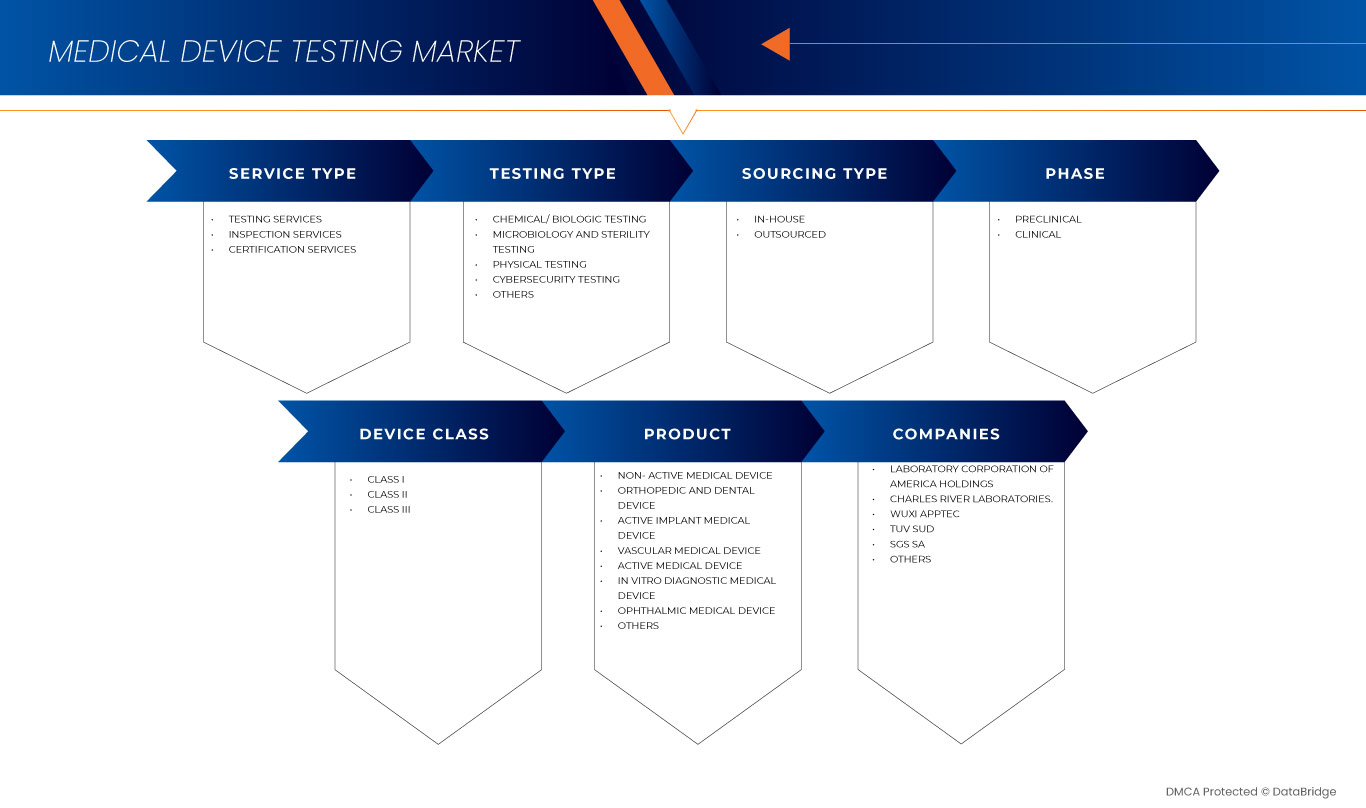
El mercado de pruebas de dispositivos médicos de América del Norte está segmentado en tipo de servicio, tipo de prueba, fase, tipo de abastecimiento, clase de dispositivo y producto. El crecimiento entre segmentos le ayuda a analizar nichos de crecimiento y estrategias para abordar el mercado y determinar sus áreas de aplicación principales y la diferencia en sus mercados objetivo.
Tipo de servicio
- Servicios de prueba
- Servicios de inspección
- Servicios de Certificación
Según el tipo de servicio, el mercado de pruebas de dispositivos médicos de América del Norte se segmenta en servicios de pruebas, servicios de inspección y servicios de certificación.
Tipo de prueba
- Pruebas físicas
- Pruebas químicas y biológicas
- Pruebas de ciberseguridad
- Microbiología y pruebas de esterilidad
- Otros
Según el tipo de prueba, el mercado de pruebas de dispositivos médicos de América del Norte está segmentado en pruebas físicas, pruebas químicas/biológicas, pruebas de ciberseguridad, pruebas de microbiología y esterilidad, y otras.
Fase
- Preclínico
- Clínico
Sobre la base de la fase, el mercado de pruebas de dispositivos médicos de América del Norte se segmenta en preclínico y clínico.
Tipo de abastecimiento
- En casa
- Subcontratado
Sobre la base del tipo de abastecimiento, el mercado de pruebas de dispositivos médicos de América del Norte se segmenta en pruebas internas y subcontratadas.
Clase de dispositivo
- Clase I
- Clase II
- Clase III
Sobre la base de la clase de dispositivo, el mercado de pruebas de dispositivos médicos de América del Norte está segmentado en clase I, clase II y clase III.
Producto
- Dispositivo médico de implante activo
- Dispositivo médico activo
- Dispositivo médico no activo
- Dispositivo médico de diagnóstico in vitro
- Dispositivo médico oftálmico
- Dispositivo médico ortopédico y dental
- Dispositivo médico vascular
- Otros
Sobre la base del producto, el mercado de pruebas de dispositivos médicos de América del Norte está segmentado en dispositivo médico de implante activo, dispositivo médico activo, dispositivo médico no activo, dispositivo médico de diagnóstico in vitro, dispositivo médico oftálmico, dispositivo médico ortopédico y dental, dispositivo médico vascular y otros.
Análisis y perspectivas regionales del mercado de pruebas de dispositivos médicos de América del Norte
El mercado de pruebas de dispositivos médicos de América del Norte está segmentado en tipo de servicio, tipo de prueba, fase, tipo de abastecimiento, clase de dispositivo y producto.
Los países cubiertos en este informe de mercado son Estados Unidos, Canadá y México.
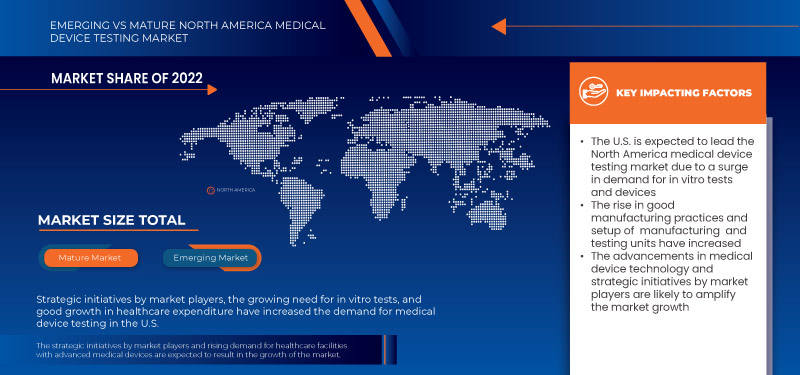
Se espera que Estados Unidos domine el mercado debido a la alta prevalencia de pruebas de dispositivos médicos en la región y al aumento del gasto en atención médica.
La sección de países del informe también proporciona factores individuales que impactan en el mercado y cambios en la regulación en el mercado a nivel nacional que afectan las tendencias actuales y futuras del mercado. Los puntos de datos como nuevas ventas, ventas de reemplazo, demografía del país, leyes regulatorias y aranceles de importación y exportación son algunos de los principales indicadores utilizados para pronosticar el escenario del mercado para países individuales. Además, se consideran la presencia y disponibilidad de marcas europeas y sus desafíos enfrentados debido a la competencia grande o escasa de las marcas locales y nacionales, y el impacto de los canales de venta al proporcionar un análisis de pronóstico de los datos del país.
Análisis del panorama competitivo y de la cuota de mercado de pruebas de dispositivos médicos en América del Norte
El panorama competitivo del mercado de pruebas de dispositivos médicos de América del Norte proporciona detalles por competidor. Los detalles incluidos son una descripción general de la empresa, las finanzas de la empresa, los ingresos generados, el potencial de mercado, la inversión en I+D, las nuevas iniciativas de mercado, los sitios e instalaciones de producción, las fortalezas y debilidades de la empresa, el lanzamiento de productos, las líneas de prueba de productos, las aprobaciones de productos, las patentes, la amplitud y amplitud de los productos, el dominio de las aplicaciones y la curva de la línea de vida de la tecnología. Los puntos de datos anteriores proporcionados solo están relacionados con el enfoque de la empresa en el mercado de pruebas de dispositivos médicos de América del Norte.
Algunos de los principales actores que operan en el mercado de pruebas de dispositivos médicos de América del Norte son Intertek Group plc, SGS SA, Bureau Veritas, TUV SUD, TUV Rheinland, Pace, Charles River Laboratories, Biomedical Device Labs, UL LLC, North American Science Associates, LLC, WuXi AppTec, NSF, Laboratory Corporation of America Holdings, Eurofins Scientific, NELSON LABORATORIES, LLC- A SOTERA HEALTH COMPANY, Gateway Analytical, Element Materials Technology, Hohenstein, Cigniti, Q Laboratories e IMR Test Labs, entre otros.
SKU-
Obtenga acceso en línea al informe sobre la primera nube de inteligencia de mercado del mundo
- Panel de análisis de datos interactivo
- Panel de análisis de empresas para oportunidades con alto potencial de crecimiento
- Acceso de analista de investigación para personalización y consultas
- Análisis de la competencia con panel interactivo
- Últimas noticias, actualizaciones y análisis de tendencias
- Aproveche el poder del análisis de referencia para un seguimiento integral de la competencia
Metodología de investigación
La recopilación de datos y el análisis del año base se realizan utilizando módulos de recopilación de datos con muestras de gran tamaño. La etapa incluye la obtención de información de mercado o datos relacionados a través de varias fuentes y estrategias. Incluye el examen y la planificación de todos los datos adquiridos del pasado con antelación. Asimismo, abarca el examen de las inconsistencias de información observadas en diferentes fuentes de información. Los datos de mercado se analizan y estiman utilizando modelos estadísticos y coherentes de mercado. Además, el análisis de la participación de mercado y el análisis de tendencias clave son los principales factores de éxito en el informe de mercado. Para obtener más información, solicite una llamada de un analista o envíe su consulta.
La metodología de investigación clave utilizada por el equipo de investigación de DBMR es la triangulación de datos, que implica la extracción de datos, el análisis del impacto de las variables de datos en el mercado y la validación primaria (experto en la industria). Los modelos de datos incluyen cuadrícula de posicionamiento de proveedores, análisis de línea de tiempo de mercado, descripción general y guía del mercado, cuadrícula de posicionamiento de la empresa, análisis de patentes, análisis de precios, análisis de participación de mercado de la empresa, estándares de medición, análisis global versus regional y de participación de proveedores. Para obtener más información sobre la metodología de investigación, envíe una consulta para hablar con nuestros expertos de la industria.
Personalización disponible
Data Bridge Market Research es líder en investigación formativa avanzada. Nos enorgullecemos de brindar servicios a nuestros clientes existentes y nuevos con datos y análisis que coinciden y se adaptan a sus objetivos. El informe se puede personalizar para incluir análisis de tendencias de precios de marcas objetivo, comprensión del mercado de países adicionales (solicite la lista de países), datos de resultados de ensayos clínicos, revisión de literatura, análisis de mercado renovado y base de productos. El análisis de mercado de competidores objetivo se puede analizar desde análisis basados en tecnología hasta estrategias de cartera de mercado. Podemos agregar tantos competidores sobre los que necesite datos en el formato y estilo de datos que esté buscando. Nuestro equipo de analistas también puede proporcionarle datos en archivos de Excel sin procesar, tablas dinámicas (libro de datos) o puede ayudarlo a crear presentaciones a partir de los conjuntos de datos disponibles en el informe.