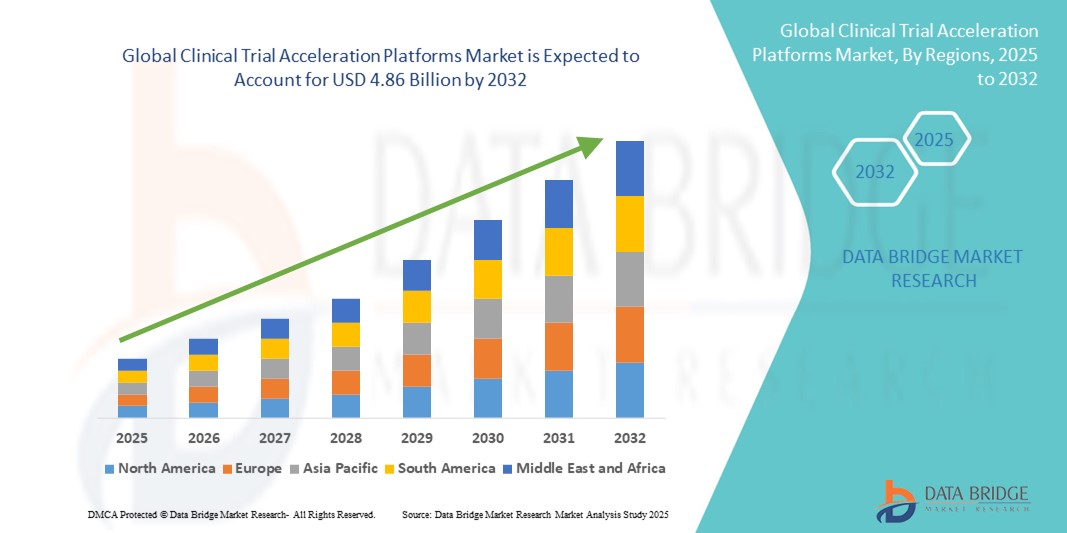
Global Clinical Trial Acceleration Platforms Market
Taille du marché en milliards USD
TCAC :
% 
 USD
1.48 Billion
USD
4.86 Billion
2024
2032
USD
1.48 Billion
USD
4.86 Billion
2024
2032
| 2025 –2032 | |
| USD 1.48 Billion | |
| USD 4.86 Billion | |
|
|
|
|
Segmentation du marché mondial des plateformes d'accélération des essais cliniques, par type (saisie électronique des données (EDC), systèmes de gestion des essais cliniques (CTMS), plateformes eCOA/ePRO, solutions de sécurité et de pharmacovigilance, plateformes de surveillance basée sur les risques et autres), protocole de communication (cloud, sur site, hybride, intégration API et autres), accès et interface utilisateur (web, application mobile, application de bureau, tableau de bord/portail d'analyse et autres), application (entreprises pharmaceutiques, entreprises de biotechnologie , organismes de recherche sous contrat (CRO), établissements universitaires et de recherche, organismes gouvernementaux et réglementaires et autres) - Tendances du secteur et prévisions jusqu'en 2032
Taille du marché des plateformes d'accélération des essais cliniques
- Le marché mondial des plateformes d'accélération des essais cliniques était évalué à 1,48 milliard de dollars américains en 2024 et devrait atteindre 4,86 milliards de dollars américains d'ici 2032 , avec un TCAC de 15,99 % au cours de la période de prévision.
- La croissance du marché est largement alimentée par l'adoption croissante des technologies de santé numérique , notamment la saisie électronique des données (EDC), les résultats rapportés par les patients (ePRO), la télémédecine et les dispositifs portables, qui rationalisent la collecte de données, l'engagement des patients et la gestion des essais cliniques, tant à domicile qu'en milieu clinique.
- De plus, la demande croissante de solutions sécurisées, conviviales et intégrées permettant la surveillance en temps réel, l'automatisation des flux de travail et la gestion à distance des patients stimule l'adoption des plateformes d'accélération des essais cliniques, améliorant ainsi considérablement l'efficacité, réduisant les délais et contribuant à la croissance globale du secteur.
Analyse du marché des plateformes d'accélération des essais cliniques
- Les plateformes d'accélération des essais cliniques sont des composantes de plus en plus essentielles de la recherche clinique moderne, permettant une gestion simplifiée des essais, un suivi des patients en temps réel et une meilleure intégration des données entre les hôpitaux, les centres de recherche et les sites cliniques.
- La demande croissante de plateformes d'accélération des essais cliniques est principalement alimentée par l'adoption généralisée des technologies de santé numérique, le besoin croissant d'un développement plus rapide des médicaments et l'importance accrue accordée aux essais centrés sur le patient et au respect des réglementations.
- L'Amérique du Nord a dominé le marché des plateformes d'accélération des essais cliniques avec la plus grande part de revenus (46,6 %) en 2024, grâce à une infrastructure de santé avancée, une forte présence de grandes entreprises pharmaceutiques et une adoption précoce des solutions d'essais numériques. Les États-Unis ont connu une croissance substantielle des installations de plateformes, stimulée par les innovations des fournisseurs de technologies établis et des jeunes entreprises émergentes.
- La région Asie-Pacifique devrait connaître la croissance la plus rapide sur le marché des plateformes d'accélération des essais cliniques au cours de la période de prévision, en raison de l'urbanisation croissante, de l'augmentation des investissements dans les soins de santé, de l'expansion des infrastructures de recherche clinique et de l'adoption grandissante des solutions de gestion des essais basées sur le cloud et l'IA.
- Le segment des plateformes cloud a dominé le marché des plateformes d'accélération des essais cliniques avec une part de marché de 46,2 % en 2024, grâce à son évolutivité, sa flexibilité et ses coûts initiaux minimes.
Portée du rapport et segmentation du marché des plateformes d'accélération des essais cliniques
|
Attributs |
Plateformes d'accélération des essais cliniques : principaux enseignements du marché |
|
Segments couverts |
|
|
Pays couverts |
Amérique du Nord
Europe
Asie-Pacifique
Moyen-Orient et Afrique
Amérique du Sud
|
|
Acteurs clés du marché |
|
|
Opportunités de marché |
|
|
Ensembles d'informations de données à valeur ajoutée |
En plus des informations sur les scénarios de marché tels que la valeur du marché, le taux de croissance, la segmentation, la couverture géographique et les principaux acteurs, les rapports de marché élaborés par Data Bridge Market Research comprennent également une analyse approfondie par des experts, une analyse des prix, une analyse des parts de marché des marques, une enquête auprès des consommateurs, une analyse démographique, une analyse de la chaîne d'approvisionnement, une analyse de la chaîne de valeur, un aperçu des matières premières/consommables, les critères de sélection des fournisseurs, une analyse PESTLE, une analyse de Porter et le cadre réglementaire. |
Tendances du marché des plateformes d'accélération des essais cliniques
Amélioration de l'efficacité grâce à l'intégration numérique
- A significant and accelerating trend in the global clinical trial acceleration platforms market is the increasing integration of digital technologies, including cloud-based systems, real-time patient monitoring, and advanced analytics. These platforms are enhancing the efficiency and accuracy of clinical trials, enabling faster and more reliable data collection and management
- For instance, leading platforms now allow centralized management of trial data, seamless coordination between multiple research sites, and automated reporting features, streamlining the overall trial process and reducing administrative burdens
- Integration with electronic health records (EHRs) and patient registries allows Clinical Trial Acceleration Platforms to provide researchers with comprehensive datasets, supporting better patient selection, monitoring, and outcome analysis. This enhances decision-making and ensures compliance with regulatory standards
- Cloud-based solutions further facilitate remote access for clinical researchers and sponsors, allowing secure data sharing, collaboration across geographies, and efficient trial oversight without the need for extensive on-site visits
- The trend towards more connected and interoperable platforms is reshaping expectations for clinical trial management, encouraging stakeholders to adopt systems that combine operational efficiency, real-time analytics, and compliance monitoring
- The demand for Clinical Trial Acceleration Platforms that offer integrated, scalable, and user-friendly solutions is growing rapidly across pharmaceutical, biotechnology, and research organizations, as these platforms help accelerate drug development while maintaining high standards of data integrity and regulatory compliance
Clinical Trial Acceleration Platforms Market Dynamics
Driver
Growing Need Due to Rising Demand for Efficient Clinical Trials
- The increasing complexity of clinical trials, coupled with the growing need for faster drug development, is a significant driver for the heightened adoption of clinical trial acceleration platforms.
- For instance, in April 2024, Medidata Solutions announced the launch of an enhanced platform for decentralized clinical trials, designed to streamline patient enrollment, remote monitoring, and real-time data collection. Such innovations by key companies are expected to accelerate the growth of the Clinical Trial Acceleration Platforms market during the forecast period
- As pharmaceutical and biotechnology companies strive to reduce timelines and costs associated with drug development, these platforms provide advanced features such as automated data integration, analytics dashboards, and patient management tools, offering substantial operational improvements over traditional trial management methods
- Furthermore, the increasing adoption of digital health technologies, electronic health records, and wearable devices is enhancing the effectiveness of clinical trial acceleration platforms, enabling better patient engagement, real-time monitoring, and improved data accuracy
- The convenience of centralized trial management, remote monitoring of study sites, and secure data sharing across multiple stakeholders are key factors propelling the adoption of clinical trial acceleration platforms across pharmaceutical, biotechnology, and research organizations. The expansion of user-friendly, scalable, and cloud-based solutions further contributes to market growth
Restraint/Challenge
Concerns Regarding Data Security and High Initial Costs
- Concerns surrounding data privacy and regulatory compliance pose significant challenges to broader adoption of Clinical Trial Acceleration Platforms. As these platforms handle sensitive patient data, stringent security measures are required to prevent breaches and ensure compliance with HIPAA, GDPR, and other regulations
- For instance, reports of vulnerabilities in digital health platforms have made some organizations cautious about implementing fully integrated trial acceleration systems without robust cybersecurity safeguards
- Addressing these concerns through encryption, secure authentication, and continuous software updates is critical for building trust among users. In addition, the relatively high initial cost of advanced clinical trial acceleration platforms can be a barrier for smaller research organizations or developing region facilities. While cloud-based solutions are becoming more affordable, premium features such as advanced analytics and AI-assisted trial optimization often carry additional costs
- Although costs are gradually decreasing, perceived high investments may still hinder adoption, particularly for organizations not immediately benefiting from enhanced trial efficiency
- Overcoming these challenges through robust security protocols, regulatory compliance, and development of cost-effective, scalable clinical trial acceleration platforms will be essential for sustained market growth
Clinical Trial Acceleration Platforms Market Scope
The market is segmented on the basis of type, communication protocol, access & user interface, and application.
- By Type
Le marché des plateformes d'accélération des essais cliniques est segmenté, selon leur type, en systèmes de saisie électronique des données (EDC), systèmes de gestion des essais cliniques (CTMS), plateformes eCOA/ePRO, solutions de sécurité et de pharmacovigilance, plateformes de surveillance basée sur les risques et autres. Le segment des systèmes EDC a représenté la plus grande part de marché (41,5 %) en 2024, grâce à son rôle essentiel dans la transformation des flux de travail traditionnels de collecte de données en flux numériques. Ces plateformes contribuent à réduire les erreurs, à améliorer la précision des données et à renforcer la conformité aux exigences réglementaires strictes. Elles offrent des capacités de surveillance en temps réel, permettant aux équipes cliniques d'identifier et de résoudre rapidement les anomalies. Les systèmes EDC sont hautement évolutifs et prennent en charge des essais de tailles et de domaines thérapeutiques variés. Leur capacité d'intégration avec les CTMS, les solutions de sécurité et les outils d'analyse renforce l'efficacité opérationnelle. En définitive, les plateformes EDC demeurent essentielles aux opérations modernes des essais cliniques grâce à leur fiabilité, leur flexibilité et leurs fonctionnalités complètes.
Le segment des systèmes de gestion des essais cliniques (CTMS) devrait connaître le taux de croissance le plus rapide, soit 19,8 %, entre 2025 et 2032, sous l'effet du besoin croissant de gestion centralisée des essais cliniques. Les plateformes CTMS permettent aux promoteurs et aux CRO de planifier, suivre et gérer efficacement l'avancement des études, de la conception du protocole à l'inclusion des patients et à la gestion des centres. Ces systèmes offrent des fonctionnalités d'optimisation des ressources, de budgétisation et de gestion des risques, ce qui réduit les coûts opérationnels et améliore le respect des délais. L'intégration avec les plateformes EDC et eCOA renforce la cohérence des données et l'automatisation des flux de travail. La complexité croissante des essais, notamment des études multinationales, alimente encore davantage la demande. La combinaison des fonctionnalités d'analyse des performances, de suivi de la conformité et de reporting fait des CTMS un outil indispensable pour les promoteurs d'essais.
- Par protocole de communication
Selon le protocole de communication, le marché des plateformes d'accélération des essais cliniques se segmente en solutions cloud, sur site, hybrides, avec intégration API et autres. Le segment cloud détenait la plus grande part de marché (46,2 %) en 2024, grâce à son évolutivité, sa flexibilité et ses coûts initiaux réduits. Les plateformes cloud permettent aux équipes d'essais cliniques internationales d'accéder aux données en temps réel depuis n'importe quel endroit, renforçant ainsi la collaboration entre les sites et les pays. Elles facilitent également les mises à jour automatiques, la conformité aux normes de sécurité et les solutions de sauvegarde, allégeant la charge de gestion informatique. L'essor des essais décentralisés et hybrides, ainsi que les pratiques de télésurveillance, ont encore accéléré leur adoption. Les solutions cloud simplifient l'intégration avec d'autres systèmes d'essais, tels que les systèmes EDC, CTMS et les plateformes de pharmacovigilance, garantissant des flux de travail fluides. Leur capacité à fournir des données d'essais centralisées, sécurisées et facilement accessibles en fait une solution privilégiée par les promoteurs et les CRO du monde entier.
Le segment de l'intégration d'API devrait connaître le taux de croissance annuel composé (TCAC) le plus rapide, à 22,3 %, entre 2025 et 2032, porté par le besoin croissant d'interopérabilité entre les différentes plateformes d'essais cliniques. Les API permettent le transfert et la synchronisation sécurisés des données entre les systèmes EDC, CTMS, de pharmacovigilance et d'analyse, réduisant ainsi les interventions manuelles et les risques d'erreurs. Elles favorisent l'automatisation des flux de travail, les mises à jour en temps réel et une meilleure visibilité des opérations d'essais. Avec l'adoption croissante des écosystèmes multiplateformes, la capacité à connecter des systèmes hétérogènes devient essentielle. L'intégration via API permet également le déploiement rapide de nouveaux modules ou de solutions tierces sans perturber les opérations existantes. Cette flexibilité, associée à une efficacité opérationnelle accrue et à la réduction des silos de données, explique la croissance rapide de ce segment.
- Par accès et interface utilisateur
Le marché des plateformes d'accélération des essais cliniques est segmenté, selon le mode d'accès et l'interface utilisateur, en plateformes web, applications mobiles, applications de bureau, portails d'analyse/tableaux de bord et autres. Le segment web a représenté la plus grande part de marché (42,7 %) en 2024, grâce à son accessibilité universelle, sa facilité de déploiement et sa compatibilité multi-appareils. Les plateformes web permettent aux acteurs des essais de suivre leur progression, de gérer les données et de générer des rapports sans installation de logiciel. Elles offrent également un contrôle et des mises à jour centralisés, garantissant la conformité réglementaire et l'intégrité des données. L'accès web simplifie la formation et l'intégration du personnel d'étude sur plusieurs sites. La possibilité de mener des essais à distance et des opérations décentralisées a encore renforcé leur adoption. En résumé, les plateformes web sont privilégiées pour leur praticité, leur évolutivité et leur capacité à gérer efficacement les flux de travail complexes des essais cliniques.
Le segment des applications mobiles devrait connaître le taux de croissance annuel composé (TCAC) le plus rapide, à 24,1 %, entre 2025 et 2032, porté par l'adoption généralisée des smartphones et des tablettes pour les essais cliniques. Les applications mobiles permettent aux investigateurs, aux moniteurs et aux participants de saisir et d'accéder aux données d'essai en mobilité, garantissant ainsi la soumission et l'examen des données dans les délais impartis. Elles prennent souvent en charge les notifications push, les rappels et la messagerie sécurisée pour améliorer la conformité et la communication. L'intégration avec les dispositifs portables pour la collecte de données eCOA/ePRO renforce l'engagement des participants et la précision des données. Les applications mobiles réduisent la dépendance aux ordinateurs de bureau et aux visites sur site, permettant une gestion décentralisée des essais. Leur importance croissante dans les essais centrés sur le patient, la télésurveillance et l'analyse des données en temps réel contribue à cette croissance rapide.
- Sur demande
Selon leur application, le marché des plateformes d'accélération des essais cliniques se segmente en entreprises pharmaceutiques, sociétés de biotechnologie, organismes de recherche sous contrat (CRO), établissements universitaires et de recherche, organismes gouvernementaux et réglementaires, et autres. Le segment des entreprises pharmaceutiques représentait la plus grande part de marché (38,7 %) en 2024, grâce au nombre élevé d'essais cliniques et à leur volonté d'accélérer le développement des médicaments. Les entreprises pharmaceutiques investissent massivement dans les plateformes numériques pour améliorer leur efficacité opérationnelle, garantir la conformité réglementaire et générer des informations exploitables. Ces plateformes contribuent à rationaliser la gestion des essais sur plusieurs sites et dans plusieurs pays, facilitant ainsi l'inclusion des patients et la collecte des données. Le besoin de rapports en temps réel, de pistes d'audit et de gestion des risques stimule également leur adoption. En définitive, le recours aux plateformes avancées d'accélération des essais fait des entreprises pharmaceutiques le segment d'application dominant sur ce marché.
Le segment des CRO devrait connaître le taux de croissance annuel composé (TCAC) le plus rapide, à 20,9 %, entre 2025 et 2032, en raison de l'externalisation croissante des essais cliniques par les entreprises pharmaceutiques et biotechnologiques. Les CRO s'appuient sur des plateformes avancées pour gérer simultanément plusieurs études, suivre les performances des sites et fournir des rapports transparents aux promoteurs. Ces plateformes améliorent l'efficacité opérationnelle, réduisent les coûts et accélèrent la prise de décision. La nécessité d'intégrer diverses sources de données, de se conformer aux réglementations internationales et de gérer des essais à distance ou décentralisés accélère leur adoption. Les CRO bénéficient de tableaux de bord centralisés, d'un accès mobile et de modules d'analyse pour fournir des résultats d'essais de haute qualité. Cette dépendance croissante aux solutions technologiques stimule la croissance rapide de ce segment.
Analyse régionale du marché des plateformes d'accélération des essais cliniques
- L’Amérique du Nord a dominé le marché des plateformes d’accélération des essais cliniques avec la plus grande part de revenus, soit 46,6 %, en 2024.
- Soutenu par une infrastructure de soins de santé de pointe, une forte présence de sociétés pharmaceutiques de premier plan et une adoption précoce des solutions d'essais cliniques numériques
- La région bénéficie d'instituts de recherche bien établis, d'investissements importants dans le secteur de la santé et d'un environnement réglementaire favorable qui encourage l'innovation.
Aperçu du marché américain des plateformes d'accélération des essais cliniques
The U.S. clinical trial acceleration platforms market captured the largest share within North America, supported by innovations from both established technology providers and emerging startups. This has resulted in substantial growth in platform installations across the country. Pharmaceutical companies and contract research organizations are increasingly adopting cloud-based, AI-driven, and hybrid trial management solutions to enhance operational efficiency, streamline workflows, ensure regulatory compliance, and reduce clinical trial timelines. The strong presence of key market players, combined with robust funding for clinical research, continues to drive the expansion of the U.S. market.
Europe Clinical Trial Acceleration Platforms Market Insight
The Europe clinical trial acceleration platforms market is projected to witness significant growth at a substantial CAGR during the forecast period. This expansion is fueled by increasing investments in clinical research infrastructure, stringent regulatory standards, and the rising adoption of digital trial solutions. Germany and the U.K. are leading the region in deploying clinical trial acceleration platforms, with pharmaceutical and biotechnology companies leveraging these solutions to improve trial efficiency, enhance data quality, and strengthen patient engagement.
U.K. Clinical Trial Acceleration Platforms Market Insight
The U.K. clinical trial acceleration platforms market is expected to grow at a noteworthy CAGR, driven by the increasing adoption of digital trial management systems and decentralized clinical trial models. Supportive regulatory frameworks, combined with growing investments in clinical research, encourage pharmaceutical companies and academic institutions to implement platforms that streamline patient recruitment, optimize data management, and maintain compliance with international standards.
Germany Clinical Trial Acceleration Platforms Market Insight
The Germany clinical trial acceleration platforms market is anticipated to experience steady growth, supported by the country’s well-developed healthcare infrastructure, focus on digital innovation in clinical research, and rising demand for compliant and efficient trial management solutions. Pharmaceutical and biotechnology companies in Germany are increasingly leveraging AI-enabled and cloud-based platforms to optimize trial operations, improve data integrity, and accelerate study timelines.
Asia-Pacific Clinical Trial Acceleration Platforms Market Insight
The Asia-Pacific clinical trial acceleration platforms market is expected to emerge as the fastest-growing region during the forecast period. This growth is driven by rapid urbanization, increasing healthcare investment, expansion of clinical research facilities, and widespread adoption of cloud-based and AI-driven trial management solutions. Key countries such as China, Japan, and India are witnessing rapid adoption of digital platforms, supported by government initiatives, a growing presence of domestic and international research organizations, and increased investment in healthcare infrastructure.
Japan Clinical Trial Acceleration Platforms Market Insight
The Japan clinical trial acceleration platforms market is gaining momentum due to the country’s advanced healthcare infrastructure, technological innovation, and strong focus on patient-centric clinical trial management. The adoption of AI-powered and cloud-based platforms is accelerating, particularly in decentralized and hybrid trial models, helping enhance trial efficiency, optimize resource utilization, and improve patient engagement across both residential and commercial healthcare settings.
China Clinical Trial Acceleration Platforms Market Insight
The China clinical trial acceleration platforms market accounted for the largest revenue share in Asia-Pacific in 2024. This growth is fueled by the rapid expansion of clinical research facilities, increasing healthcare investment, and the widespread adoption of cloud-based and AI-driven trial management platforms. Strong government support for digital clinical trials, a growing middle class, and rising domestic pharmaceutical R&D activities are key factors propelling the market forward, making China a leading hub for clinical trial innovation in the region.
Clinical Trial Acceleration Platforms Market Share
The clinical trial acceleration platforms industry is primarily led by well-established companies, including:
- Medable (U.S.)
- Oracle (U.S.)
- Florence Healthcare (U.S.)
- Clario (U.S.)
- RealTime eClinical Solutions (U.S.)
- WCG Clinical Services (U.S.)
- ProPharma Group (U.S.)
- nference (U.S.)
- Dash Bio (U.S.)
- Takeda Pharmaceuticals (Japan)
- Medidata Solutions (U.S.)
- Veeva Systems (U.S.)
- IBM Clinical Development (U.S.)
- MasterControl (U.S.)
- nQuery (U.S.)
Latest Developments in Global Clinical Trial Acceleration Platforms Market
- In August 2025, Japanese pharmaceutical company Takeda announced plans to conduct global clinical trials in India to accelerate the introduction of its innovative drugs. This strategic move aims to leverage India's diverse patient population, cost advantages, and expanding hospital network, with projections indicating the country's clinical trials market will surpass $2 billion by 2030. Takeda's initiative includes exploring partnerships with local academic institutions, healthcare providers, and tech companies to integrate India's R&D capabilities into its global drug development pipeline
- En août 2024, Dash Bio, une start-up de services biotechnologiques cofondée par d'anciens cadres de Moderna, a lancé ses activités afin d'automatiser les tests et l'analyse d'échantillons d'essais cliniques grâce à la robotique, l'intelligence artificielle (IA) et des logiciels. Son laboratoire de robotique situé à Newton, dans le Massachusetts, vise à accélérer le processus décisionnel concernant le développement de composés dans les études cliniques, en réduisant les délais de plusieurs mois à quelques semaines. Dash Bio a levé 6,5 millions de dollars en financement d'amorçage pour soutenir son approche novatrice du développement de médicaments.
- En mai 2025, le gouvernement britannique a annoncé son intention d'utiliser l'application NHS pour étendre la participation aux essais cliniques en Angleterre. Cette initiative vise à renforcer significativement les capacités de recherche médicale et à attirer davantage d'entreprises pharmaceutiques en permettant aux individus de recevoir des notifications d'essais cliniques personnalisées en fonction de leurs données de santé et de leurs préférences. Cette stratégie s'inscrit dans le cadre du prochain plan de santé décennal, qui vise à rationaliser les procédures et à réduire les délais de mise en place des essais cliniques de 250 à 150 jours maximum d'ici mars 2026.
SKU-
Accédez en ligne au rapport sur le premier cloud mondial de veille économique
- Tableau de bord d'analyse de données interactif
- Tableau de bord d'analyse d'entreprise pour les opportunités à fort potentiel de croissance
- Accès d'analyste de recherche pour la personnalisation et les requêtes
- Analyse de la concurrence avec tableau de bord interactif
- Dernières actualités, mises à jour et analyse des tendances
- Exploitez la puissance de l'analyse comparative pour un suivi complet de la concurrence
Méthodologie de recherche
La collecte de données et l'analyse de l'année de base sont effectuées à l'aide de modules de collecte de données avec des échantillons de grande taille. L'étape consiste à obtenir des informations sur le marché ou des données connexes via diverses sources et stratégies. Elle comprend l'examen et la planification à l'avance de toutes les données acquises dans le passé. Elle englobe également l'examen des incohérences d'informations observées dans différentes sources d'informations. Les données de marché sont analysées et estimées à l'aide de modèles statistiques et cohérents de marché. De plus, l'analyse des parts de marché et l'analyse des tendances clés sont les principaux facteurs de succès du rapport de marché. Pour en savoir plus, veuillez demander un appel d'analyste ou déposer votre demande.
La méthodologie de recherche clé utilisée par l'équipe de recherche DBMR est la triangulation des données qui implique l'exploration de données, l'analyse de l'impact des variables de données sur le marché et la validation primaire (expert du secteur). Les modèles de données incluent la grille de positionnement des fournisseurs, l'analyse de la chronologie du marché, l'aperçu et le guide du marché, la grille de positionnement des entreprises, l'analyse des brevets, l'analyse des prix, l'analyse des parts de marché des entreprises, les normes de mesure, l'analyse globale par rapport à l'analyse régionale et des parts des fournisseurs. Pour en savoir plus sur la méthodologie de recherche, envoyez une demande pour parler à nos experts du secteur.
Personnalisation disponible
Data Bridge Market Research est un leader de la recherche formative avancée. Nous sommes fiers de fournir à nos clients existants et nouveaux des données et des analyses qui correspondent à leurs objectifs. Le rapport peut être personnalisé pour inclure une analyse des tendances des prix des marques cibles, une compréhension du marché pour d'autres pays (demandez la liste des pays), des données sur les résultats des essais cliniques, une revue de la littérature, une analyse du marché des produits remis à neuf et de la base de produits. L'analyse du marché des concurrents cibles peut être analysée à partir d'une analyse basée sur la technologie jusqu'à des stratégies de portefeuille de marché. Nous pouvons ajouter autant de concurrents que vous le souhaitez, dans le format et le style de données que vous recherchez. Notre équipe d'analystes peut également vous fournir des données sous forme de fichiers Excel bruts, de tableaux croisés dynamiques (Fact book) ou peut vous aider à créer des présentations à partir des ensembles de données disponibles dans le rapport.