Global Medical Device Testing Market
Taille du marché en milliards USD
TCAC :
% 
 USD
5.20 Billion
USD
11.82 Billion
202
2032
USD
5.20 Billion
USD
11.82 Billion
202
2032
| 203 –2032 | |
| USD 5.20 Billion | |
| USD 11.82 Billion | |
|
|
|
|
Segmentation du marché mondial des tests de dispositifs médicaux, par type de service (tests, inspection et certification), type de test (tests physiques, tests chimiques/biologiques, tests de cybersécurité, tests de microbiologie et de stérilité, etc.), phase (préclinique et clinique), type d'approvisionnement (interne et externalisé), classe de dispositif (classe I, classe II et classe III), produit (implant actif, dispositif actif, dispositif non actif, dispositif de diagnostic in vitro, dispositif ophtalmique, orthopédique et dentaire, dispositif vasculaire, etc.) - Tendances et prévisions du secteur jusqu'en 2032
Taille du marché des tests de dispositifs médicaux
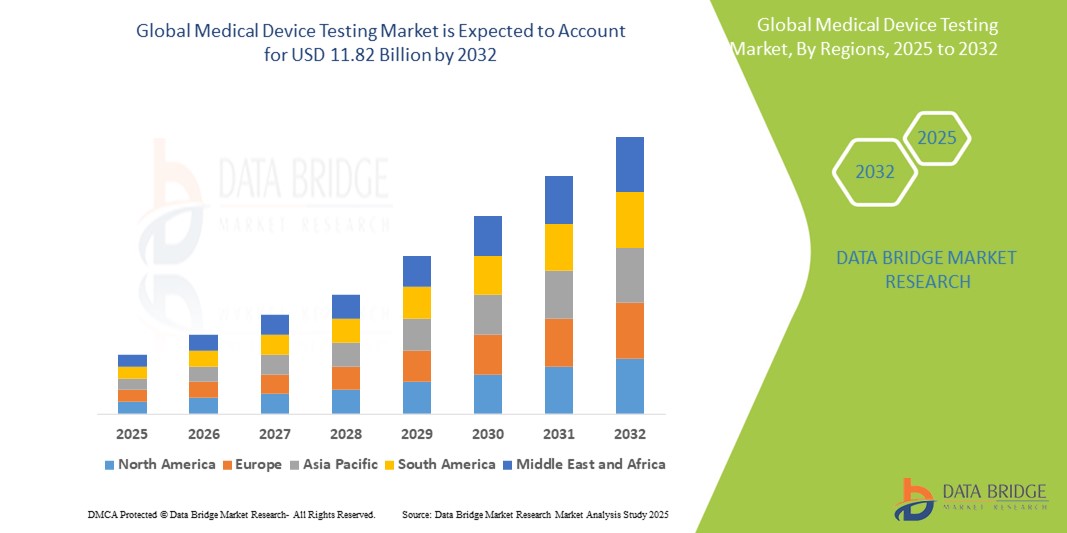
- La taille du marché mondial des tests de dispositifs médicaux était évaluée à 5,20 milliards USD en 2024 et devrait atteindre 11,82 milliards USD d'ici 2032 , à un TCAC de 10,80 % au cours de la période de prévision.
- Cette croissance est portée par la demande croissante de dispositifs médicaux plus sûrs et plus fiables, les avancées technologiques en matière de méthodologies de test et la multiplication des exigences réglementaires pour l'approbation des dispositifs médicaux à l'échelle mondiale. De plus, l'augmentation des maladies chroniques, le vieillissement de la population et l'expansion du secteur de la santé contribuent au besoin croissant de tests complets des dispositifs médicaux.
Analyse du marché des tests de dispositifs médicaux
- Les tests des dispositifs médicaux constituent une partie cruciale du cycle de développement des produits, garantissant que les dispositifs médicaux répondent aux normes réglementaires, sont sûrs pour l'utilisation des patients et fonctionnent comme prévu dans diverses applications de soins de santé, notamment les dispositifs de diagnostic, de surveillance et thérapeutiques.
- La demande de tests de dispositifs médicaux est principalement motivée par le nombre croissant d'innovations en matière de dispositifs médicaux, les exigences réglementaires strictes et les préoccupations croissantes concernant la sécurité des patients.
- L'Amérique du Nord domine le marché mondial des tests de dispositifs médicaux, représentant une part significative en 2024, estimée à environ 40,2 %. Cette domination s'explique par la présence de grands fabricants de dispositifs médicaux et par des cadres réglementaires bien établis.
- La région Asie-Pacifique (APAC) est celle qui connaît la croissance la plus rapide sur le marché mondial des tests de dispositifs médicaux. Cette croissance est due au développement rapide des infrastructures de santé, à la hausse des dépenses de santé et à la demande croissante de technologies médicales avancées dans des pays comme la Chine, l'Inde et le Japon.
- Le segment des tests de diagnostic in vitro (DIV) devrait dominer le marché mondial des tests de dispositifs médicaux, détenant environ 33 % de parts de marché. Cette domination est due à la demande croissante d'outils de diagnostic précis, notamment en réponse au fardeau croissant des maladies chroniques.
Portée du rapport et segmentation du marché des tests de dispositifs médicaux
|
Attributs |
Principales informations sur le marché des tests de dispositifs médicaux |
|
Segments couverts |
|
|
Pays couverts |
Amérique du Nord
Europe
Asie-Pacifique
Moyen-Orient et Afrique
Amérique du Sud
|
|
Principaux acteurs du marché |
|
|
Opportunités de marché |
|
|
Ensembles d'informations de données à valeur ajoutée |
Outre les informations sur les scénarios de marché tels que la valeur marchande, le taux de croissance, la segmentation, la couverture géographique et les principaux acteurs, les rapports de marché organisés par Data Bridge Market Research comprennent également une analyse des importations et des exportations, un aperçu de la capacité de production, une analyse de la consommation de production, une analyse des tendances des prix, un scénario de changement climatique, une analyse de la chaîne d'approvisionnement, une analyse de la chaîne de valeur, un aperçu des matières premières/consommables, des critères de sélection des fournisseurs, une analyse PESTLE, une analyse Porter et un cadre réglementaire. |
Tendances du marché des tests de dispositifs médicaux
« Intégration des solutions de santé numérique et de l'IA dans les tests d'appareils »
- L'intégration croissante des solutions de santé numériques et de l'intelligence artificielle (IA) dans les processus de test et de validation est une tendance majeure sur le marché des tests de dispositifs médicaux . Ces innovations améliorent la précision, l'efficacité et la rapidité des tests, tout en améliorant la sécurité des patients.
- L'intégration d'outils basés sur l'IA et d'analyses de données avancées permet une surveillance en temps réel, des tests prédictifs et une conformité réglementaire plus rapide, ce qui permet aux fabricants de tester plus facilement les appareils à différents stades de développement.
- Par exemple, en juillet 2023, Charles River Laboratories a introduit des services de test basés sur l'IA pour accélérer l'évaluation des dispositifs médicaux, améliorant ainsi la précision des tests et contribuant à répondre aux normes réglementaires en constante évolution aux États-Unis.
- Ces avancées transforment le processus de test des dispositifs médicaux, facilitent une meilleure prise de décision, réduisent le délai de mise sur le marché des dispositifs et aident les fabricants à adhérer à des exigences réglementaires strictes.
Dynamique du marché des tests de dispositifs médicaux
Conducteur
« Demande croissante de dispositifs médicaux de haute qualité et conformes »
- La demande croissante de dispositifs médicaux de haute qualité, fiables et conformes stimule considérablement le marché mondial des tests de dispositifs médicaux. Alors que les fabricants de dispositifs médicaux s'efforcent de respecter des normes réglementaires strictes et d'assurer la sécurité des patients, le besoin de solutions de test complètes pour diverses catégories de dispositifs, notamment les dispositifs de diagnostic, de surveillance et thérapeutiques, se fait de plus en plus sentir.
- Avec le développement des systèmes de santé à l'échelle mondiale, notamment dans les marchés émergents, la demande de technologies et d'appareils médicaux de pointe augmente. Cela incite les fabricants à adopter des protocoles de tests rigoureux pour se conformer à l'évolution de la réglementation et répondre aux besoins du marché.
- Les fabricants recherchent également de plus en plus des solutions de test spécialisées, conformes à la réglementation et personnalisables pour garantir que leurs produits répondent aux normes de sécurité et de performance du secteur de la santé.
Par exemple,
- En mars 2024, Charles River Laboratories s'est associé à un fabricant européen de dispositifs médicaux de premier plan pour offrir des services de tests avancés, garantissant la conformité réglementaire et la fiabilité des produits pour leur nouvelle gamme de dispositifs implantables.
- En raison du besoin croissant de dispositifs médicaux fiables et conformes, la demande de services complets de tests de dispositifs médicaux connaît une croissance significative, en particulier dans les régions où les infrastructures de santé et les exigences réglementaires sont en expansion.
Opportunité
« Intégration de l'IA et de l'automatisation dans les tests de dispositifs médicaux »
- L'intégration de l'IA et de l'automatisation dans les tests de dispositifs médicaux offre une opportunité significative d'améliorer l'efficacité, la précision et la rapidité des processus de test et de validation. Ces technologies permettent de rationaliser les procédures de tests répétitifs, d'améliorer l'analyse des données et de garantir une meilleure conformité des dispositifs aux normes réglementaires.
- Les systèmes basés sur l'IA peuvent analyser en continu les données de test, prédire les défaillances potentielles des dispositifs et automatiser le processus de documentation, réduisant ainsi les erreurs humaines et garantissant la cohérence des résultats de test. Cette automatisation permet une mise sur le marché plus rapide des dispositifs médicaux tout en garantissant leur conformité aux réglementations strictes.
- La capacité d'intégrer des analyses prédictives basées sur l'IA dans les systèmes de test devrait stimuler la demande de solutions de test de dispositifs médicaux plus avancées et plus rentables dans tous les secteurs.
Par exemple,
- En janvier 2024, Medistri SA s'est associé à la société technologique axée sur l'IA Veeva Systems pour introduire une nouvelle plate-forme de test pilotée par l'IA pour les dispositifs médicaux, permettant des contrôles automatisés de conformité réglementaire et une assurance qualité prédictive pour les dispositifs de santé critiques.
- L'intégration de l'IA et de l'automatisation dans les tests de dispositifs médicaux devrait améliorer considérablement l'efficacité des tests, réduire les coûts opérationnels et renforcer la fiabilité des dispositifs médicaux, conduisant à une adoption généralisée de ces technologies avancées sur le marché mondial des tests de dispositifs médicaux.
Retenue/Défi
« Coûts élevés des tests et de la conformité réglementaire »
- Les coûts élevés associés aux tests des dispositifs médicaux et à la conformité réglementaire représentent un défi important pour la croissance du marché, en particulier pour les petites et moyennes entreprises (PME) des marchés émergents.
- Les tests de dispositifs médicaux, notamment ceux de pointe ou à haut risque, nécessitent des investissements importants en équipements spécialisés, en main-d'œuvre qualifiée et le respect de réglementations internationales strictes. Cela peut représenter un fardeau financier important pour les entreprises disposant de budgets limités, notamment lorsque les tests impliquent des procédures complexes comme des essais cliniques ou des évaluations de performance à long terme.
- Les coûts permanents, y compris les tests pour divers organismes de réglementation (par exemple, la FDA, le marquage CE), ainsi que le maintien de la conformité aux normes de santé en constante évolution, peuvent encore aggraver les défis financiers pour les fabricants.
Par exemple,
- En mars 2024, un rapport d'Eurofins Scientific a souligné que les petits fabricants de dispositifs médicaux des marchés émergents sont confrontés à des difficultés pour respecter les normes réglementaires internationales en raison des coûts importants impliqués dans les processus complets de test et de certification.
- Ces obstacles financiers peuvent dissuader les entreprises d'investir dans les procédures de test nécessaires ou d'adopter de nouvelles technologies, ce qui entraîne des retards dans le lancement de produits ou une entrée sur le marché plus limitée pour les petits acteurs. Par conséquent, les coûts élevés associés aux tests de dispositifs médicaux pourraient freiner la croissance du marché à long terme.
Portée du marché des tests de dispositifs médicaux
Le marché est segmenté en fonction du type de service, du type de test, de la phase, du type d'approvisionnement, de la classe d'appareil et du produit.
|
Segmentation |
Sous-segmentation |
|
Par type de service |
|
|
Par type de test |
|
|
Par phase |
|
|
Par type d'approvisionnement |
|
|
Par classe d'appareil |
|
|
Par produit |
|
En 2025, le segment des diagnostics in vitro devrait dominer le marché des chaudières industrielles avec la plus grande part dans le segment des produits combustibles.
Le segment des tests de diagnostic in vitro (DIV) devrait dominer le marché mondial des tests de dispositifs médicaux, détenant environ 33 % du marché total. Cette domination s'explique par la demande croissante d'outils de diagnostic précis et rapides, notamment en réponse à la charge croissante des maladies chroniques et au besoin croissant de méthodes de test non invasives. Les solutions de diagnostic in vitro (DIV), telles que le diagnostic moléculaire, les tests au point de service et la médecine personnalisée, offrent une précision, une rapidité et une praticité élevées, ce qui en fait un choix privilégié pour les professionnels de santé comme pour les patients. De plus, les progrès constants de la santé numérique et de l'automatisation favorisent l'adoption généralisée des solutions de diagnostic in vitro (DIV) dans divers contextes de soins, des hôpitaux aux soins à domicile.
Les tests de cybersécurité devraient représenter la part la plus importante au cours de la période de prévision dans les segments de type test
Le segment des tests de cybersécurité devrait détenir une part significative du marché, estimée à environ 35 % en 2025. Cette domination s'explique par l'importance croissante de la protection des dispositifs médicaux contre les cybermenaces, les systèmes de santé étant de plus en plus interconnectés grâce à l'Internet des objets (IoT) et aux technologies cloud. Face à la multiplication des cyberattaques ciblant les établissements de santé et les dispositifs médicaux, la sécurité des appareils tels que les stimulateurs cardiaques, les pompes à insuline et les équipements de diagnostic est devenue une priorité absolue.
Analyse régionale du marché des tests de dispositifs médicaux
« L'Amérique du Nord détient la plus grande part du marché des tests de dispositifs médicaux »
- L'Amérique du Nord domine le marché mondial des tests de dispositifs médicaux, représentant environ 40,2 % de la part de marché en 2024
- Les États-Unis détiennent une part importante d'environ 35 % du marché mondial des tests de dispositifs médicaux en 2024. Cette domination est due à la forte demande de dispositifs médicaux avancés, à un système de santé bien établi et à des innovations continues dans les technologies des dispositifs médicaux et les solutions de test.
- La disponibilité de cadres réglementaires bien établis, tels que les processus d’approbation de la FDA, et les investissements croissants dans la recherche et le développement par les principaux fabricants de dispositifs médicaux renforcent encore le marché en Amérique du Nord.
- En outre, l’accent croissant mis sur la sécurité des patients, la conformité réglementaire et l’adoption de technologies de test de pointe, telles que l’IA et l’automatisation, alimentent l’expansion du marché dans toute la région.
« L'Asie-Pacifique devrait enregistrer le TCAC le plus élevé sur le marché des tests de dispositifs médicaux »
- La région Asie-Pacifique (APAC) devrait connaître le taux de croissance le plus élevé sur le marché mondial des tests de dispositifs médicaux, grâce au développement rapide des infrastructures de santé, à la demande croissante de dispositifs médicaux et aux exigences croissantes de conformité réglementaire.
- Des pays comme la Chine, l'Inde et le Japon émergent comme des marchés clés en raison de l'expansion de leurs systèmes de santé, de la demande croissante de technologies médicales avancées et de l'attention croissante portée à la sécurité des patients et aux normes réglementaires.
- La Chine, avec son important secteur de la santé et ses investissements importants dans la fabrication de dispositifs médicaux, génère une forte demande de services de tests de dispositifs médicaux. Le pays s'attache également à améliorer les normes réglementaires et la qualité des soins de santé, favorisant ainsi l'adoption de solutions de tests avancées.
- L'Inde, avec son secteur de la santé en plein essor et sa demande croissante de dispositifs médicaux abordables et innovants, connaît une adoption rapide de solutions de test de dispositifs médicaux pour répondre aux besoins croissants des patients.
- L'augmentation des initiatives gouvernementales et des investissements du secteur privé dans les infrastructures de santé contribue davantage à la croissance du marché dans la région.
Part de marché des tests de dispositifs médicaux
Le paysage concurrentiel du marché fournit des détails par concurrent. Il comprend la présentation de l'entreprise, ses données financières, son chiffre d'affaires, son potentiel de marché, ses investissements en recherche et développement, ses nouvelles initiatives commerciales, sa présence mondiale, ses sites et installations de production, ses capacités de production, ses forces et faiblesses, le lancement de nouveaux produits, leur ampleur et leur portée, ainsi que la domination de ses applications. Les données ci-dessus ne concernent que les activités des entreprises par rapport à leur marché.
Les principaux leaders du marché opérant sur le marché sont :
- Intertek Group plc (Royaume-Uni)
- SGS SA (Suisse)
- Bureau Veritas (France)
- TUV SUD (Allemagne)
- TUV Rheinland (Allemagne)
- Pace (États-Unis)
- Charles River Laboratories (États-Unis)
- Laboratoires de dispositifs biomédicaux (États-Unis)
- UL LLC (États-Unis)
- North American Science Associates, LLC (États-Unis)
- Medistri SA (Suisse)
- WuXi AppTec (Chine)
- NSF (États-Unis)
- Labcorp (États-Unis)
- Eurofins Scientifique (Luxembourg)
- Nelson Laboratories, LLC – Une société Sotera Health (États-Unis)
- Gateway Analytical (États-Unis)
- ITC ZLIN (République tchèque)
- Technologie des matériaux élémentaires (Royaume-Uni)
- EndoLab Mechanical Engineering GmbH (Allemagne)
- Hohenstein (Allemagne)
- Medical Engineering Technologies Ltd. (Royaume-Uni)
- Bioneeds (Inde)
- Cigniti (Inde)
- Arbro Pharmaceuticals Private Limited et Auriga Research Private Limited (Inde)
- Laboratoires Q (États-Unis)
- Laboratoires de tests IMR (États-Unis)
Derniers développements sur le marché mondial des tests de dispositifs médicaux
- En janvier 2025, le groupe IMQ a fait son entrée sur le marché indien en lançant Elettra Tech Labs, une coentreprise spécialisée dans les services de test et d'inspection des dispositifs médicaux et des produits électriques et électroniques. Cette expansion renforce la présence mondiale d'IMQ, aidant les entreprises indiennes à respecter des normes rigoureuses de qualité et de sécurité tout en facilitant leur accès aux marchés internationaux. Cette initiative s'inscrit dans le secteur croissant des dispositifs médicaux en Inde, s'appuyant sur des technologies de test avancées pour améliorer la conformité et l'innovation.
- En mars 2024, Stryker a agrandi son site de prototypage et d'essais en Inde, marquant ainsi une étape importante dans son développement en recherche et développement. Ce site de 5 200 m² intègre une infrastructure de pointe et des capacités microbiologiques avancées, renforçant ainsi l'assurance produit et l'innovation. Cette extension permet de réaliser des tests rigoureux du cycle de vie des dispositifs médicaux, garantissant ainsi leur conformité aux normes réglementaires mondiales. Le site dispose également d'outils de prototypage avancés, notamment l'impression 3D plastique et l'usinage des métaux, confirmant ainsi l'engagement de Stryker en faveur des avancées technologiques médicales.
- En mars 2024, TidalSense, fabricant britannique d'appareils respiratoires, a lancé une étude pilote pour évaluer son dispositif N-Tidal, conçu pour diagnostiquer l'asthme chez l'enfant. Menée en partenariat avec l'Université de Nottingham et le Nottingham University Hospitals NHS Trust, l'étude porte sur 75 enfants de moins de cinq ans souffrant d'asthme et de respiration sifflante virale. Contrairement aux tests de spirométrie traditionnels, qui nécessitent des manœuvres respiratoires complexes, N-Tidal utilise la capnographie pour mesurer les niveaux de CO₂ pendant une respiration normale, rendant le diagnostic plus facile et plus accessible.
- En juin 2023, TÜV SÜD a inauguré un laboratoire de microbiologie et de chimie de pointe à New Brighton, dans le Minnesota, réaffirmant ainsi son engagement en faveur de services de test de dispositifs médicaux de haute qualité. Accrédité ISO 17025, ce laboratoire est spécialisé dans les tests biologiques et chimiques et aide les entreprises de dispositifs médicaux à accélérer leur recherche et développement. Doté de technologies de pointe, le laboratoire propose des services de microbiologie, de tests de dispositifs réutilisables, de chimie, de biocompatibilité et d'évaluation des emballages. Cette expansion renforce le réseau mondial de laboratoires de TÜV SÜD, garantissant précision et conformité pour l'innovation médicale.
- En juillet 2022, Eurofins Scientific a acquis WESSLING Hongrie, renforçant ainsi ses capacités d'analyse de produits environnementaux, alimentaires et biopharmaceutiques en Europe. WESSLING Hongrie, laboratoire de premier plan, a réalisé un chiffre d'affaires de 15 millions d'euros en 2021 et employait plus de 300 personnes, confirmant ainsi l'engagement d'Eurofins en faveur de services d'analyse de haute qualité.
SKU-
Accédez en ligne au rapport sur le premier cloud mondial de veille économique
- Tableau de bord d'analyse de données interactif
- Tableau de bord d'analyse d'entreprise pour les opportunités à fort potentiel de croissance
- Accès d'analyste de recherche pour la personnalisation et les requêtes
- Analyse de la concurrence avec tableau de bord interactif
- Dernières actualités, mises à jour et analyse des tendances
- Exploitez la puissance de l'analyse comparative pour un suivi complet de la concurrence
Méthodologie de recherche
La collecte de données et l'analyse de l'année de base sont effectuées à l'aide de modules de collecte de données avec des échantillons de grande taille. L'étape consiste à obtenir des informations sur le marché ou des données connexes via diverses sources et stratégies. Elle comprend l'examen et la planification à l'avance de toutes les données acquises dans le passé. Elle englobe également l'examen des incohérences d'informations observées dans différentes sources d'informations. Les données de marché sont analysées et estimées à l'aide de modèles statistiques et cohérents de marché. De plus, l'analyse des parts de marché et l'analyse des tendances clés sont les principaux facteurs de succès du rapport de marché. Pour en savoir plus, veuillez demander un appel d'analyste ou déposer votre demande.
La méthodologie de recherche clé utilisée par l'équipe de recherche DBMR est la triangulation des données qui implique l'exploration de données, l'analyse de l'impact des variables de données sur le marché et la validation primaire (expert du secteur). Les modèles de données incluent la grille de positionnement des fournisseurs, l'analyse de la chronologie du marché, l'aperçu et le guide du marché, la grille de positionnement des entreprises, l'analyse des brevets, l'analyse des prix, l'analyse des parts de marché des entreprises, les normes de mesure, l'analyse globale par rapport à l'analyse régionale et des parts des fournisseurs. Pour en savoir plus sur la méthodologie de recherche, envoyez une demande pour parler à nos experts du secteur.
Personnalisation disponible
Data Bridge Market Research est un leader de la recherche formative avancée. Nous sommes fiers de fournir à nos clients existants et nouveaux des données et des analyses qui correspondent à leurs objectifs. Le rapport peut être personnalisé pour inclure une analyse des tendances des prix des marques cibles, une compréhension du marché pour d'autres pays (demandez la liste des pays), des données sur les résultats des essais cliniques, une revue de la littérature, une analyse du marché des produits remis à neuf et de la base de produits. L'analyse du marché des concurrents cibles peut être analysée à partir d'une analyse basée sur la technologie jusqu'à des stratégies de portefeuille de marché. Nous pouvons ajouter autant de concurrents que vous le souhaitez, dans le format et le style de données que vous recherchez. Notre équipe d'analystes peut également vous fournir des données sous forme de fichiers Excel bruts, de tableaux croisés dynamiques (Fact book) ou peut vous aider à créer des présentations à partir des ensembles de données disponibles dans le rapport.