Global Rare Disease Api Orphan Drug Substance Market
Taille du marché en milliards USD
TCAC :
% 
 USD
306.90 Million
USD
667.49 Million
2025
2033
USD
306.90 Million
USD
667.49 Million
2025
2033
| 2026 –2033 | |
| USD 306.90 Million | |
| USD 667.49 Million | |
|
|
|
|
Global Rare Disease API / Orphan Drug Substance Market Segmentation, Par IPA/Drug Type de substance (PIA biologiques, API à petites molécules, API à vecteurs viraux, API à base d'ARN et substances médicamenteuses liées à la thérapie cellulaire), Indications thérapeutiques (oncologie, troubles hématologiques, troubles neurologiques et neuromusculaires, troubles métaboliques et endocriniens, maladies immunologiques et infectieuses rares, troubles cardiovasculaires, ophtalmiques et autres troubles rares), Utilisateur final (sociétés biopharmaceutiques, organismes de développement et de fabrication de contrats, instituts de recherche et fabricants de spécialités) Tendances et prévisions de l'industrie à 2033
IPA sur les maladies rares / substance médicamenteuse orpheline Taille du marché
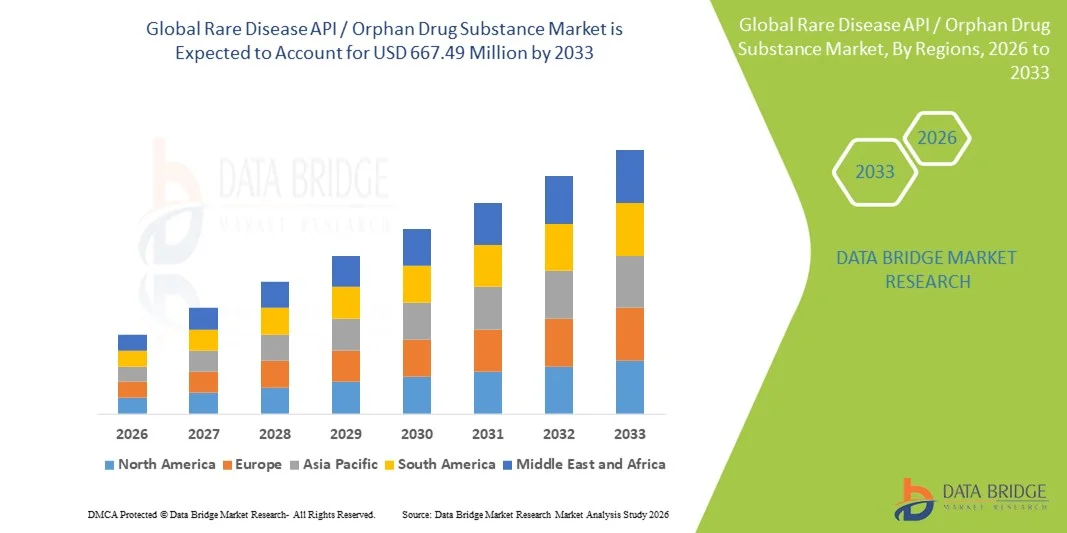
- La taille du marché mondial de l'API et de la substance médicamenteuse orpheline a été évaluée à306,90 millions de dollars en 2025et devrait atteindre667,49 millions de dollars en 2033, à unTCAC de 10,20 %pendant la période de prévision
- La croissance du marché s'explique en grande partie par l'augmentation de la prévalence des maladies rares, l'expansion des pipelines de médicaments orphelins et l'augmentation des incitations réglementaires qui encouragent le développement et la fabrication d'ingrédients pharmaceutiques actifs spécialisés pour des conditions rares et ultra-rares
- De plus, les investissements croissants dans les produits biologiques,thérapies génétiques, et d'autres modalités avancées, ainsi que la nécessité de substances médicamenteuses de haute qualité, de petites quantités et très puissantes, établissent des IPA orphelins comme composante essentielle du développement pharmaceutique moderne. Ces facteurs convergents accélèrent la demande d'IPA pour les maladies rares, ce qui stimule significativement la croissance de l'industrie
API sur les maladies rares / Analyse du marché des médicaments orphelins
- Les IPA des maladies rares et les substances pharmaceutiques orphelines, qui comprennent des ingrédients pharmaceutiques actifs hautement spécialisés pour le traitement des maladies rares et ultra-rares, deviennent de plus en plus critiques pour le développement pharmaceutique moderne en raison de leur rôle dans la promotion de thérapies ciblées, précises et vitales dans de multiples domaines thérapeutiques.
- L'augmentation de la demande d'IPA pour les maladies rares est principalement attribuable à la prévalence croissante de maladies rares, à l'expansion des pipelines de médicaments orphelins, à des mesures d'incitation réglementaires favorables et à l'augmentation des investissements dans des modalités avancées telles que les produits biologiques, les thérapies géniques et les traitements fondés sur l'ARN.
- L'Amérique du Nord a dominé le marché de l'API/des substances pharmaceutiques orphelines des maladies rares avec la plus grande part des revenus de 41,5 % en 2025, appuyée par un cadre de réglementation solide des médicaments orphelin, des dépenses élevées en R-D et une forte présence debiopharmaceutiqueles entreprises et les CDMO spécialisés, les États-Unis étant témoins d'une croissance importante dans la fabrication d'API orpheline à l'échelle clinique et commerciale
- On s'attend à ce que l'Asie-Pacifique soit la région qui connaît la croissance la plus rapide du marché des IPA des maladies rares au cours de la période de prévision en raison de l'externalisation croissante de la fabrication des IPA, de l'expansion des écosystèmes biotechnologiques, de l'amélioration de l'alignement réglementaire et de l'augmentation des investissements dans la mise au point de médicaments contre les maladies rares en Chine, au Japon, en Corée du Sud et en Inde
- Les IPA des produits biologiques ont dominé le marché des substances pharmaceutiques orphelines/API des maladies rares avec une part de marché de 58,3 % en 2025, en raison de leur utilisation généralisée dans les thérapies de remplacement enzymatiques,anticorps monoclonaux, et les traitements à base de gènes, ainsi que leur forte efficacité dans la lutte contre les maladies génétiques et métaboliques rares
Portée du rapport et maladies rares API / segmentation du marché des médicaments orphelins
| Attributs | IPA des maladies rares / substance médicamenteuse orpheline Principales perspectives du marché |
| Segments couverts |
|
| Pays couverts | Amérique du Nord
Europe
Asie-Pacifique
Moyen-Orient et Afrique
Amérique du Sud
|
| Principaux acteurs du marché |
|
| Possibilités de marché |
|
| Infos sur la valeur ajoutée | En plus des renseignements sur les scénarios du marché comme la valeur du marché, le taux de croissance, la segmentation, la couverture géographique et les principaux intervenants, les rapports de marché établis par Data Bridge Market Research comprennent également une analyse approfondie des experts, l'épidémiologie des patients, l'analyse des pipelines, l'analyse des prix et le cadre réglementaire. |
Tendances du marché de l'API sur les maladies rares et des médicaments orphelins
Changement vers des substances biologiques et génétiques avancées
- Une tendance significative et accélérée sur le marché mondial de l'API et des substances pharmaceutiques orphelines liées aux maladies rares est l'évolution croissante vers les produits biologiques, les thérapies géniques et les substances pharmaceutiques à base d'ARN, en raison de leur capacité à cibler avec une grande précision les causes génétiques sous-jacentes des maladies rares et ultra-rares.
- Par exemple, le nombre croissant d'approbations réglementaires pour les thérapies génétiques et cellulaires ciblant les troubles rares intensifie la demande d'API vectorielles virales, de protéines recombinantes et de substances pharmaceutiques biologiques hautement spécialisées fabriquées selon des normes de qualité rigoureuses
- L'avancement de la biologie moléculaire, de la génomique et des diagnostics complémentaires permet le développement de substances médicamenteuses orphelines hautement ciblées, permettant aux fabricants de concevoir des IPA adaptés à des mutations ou à des voies de maladie spécifiques, améliorant ainsi l'efficacité du traitement et les résultats des patients.
- L'adoption croissante d'approches de médecine de précision encourage les entreprises pharmaceutiques à investir dans la production d'API complexes, à faible volume et de grande valeur, nécessitant des installations spécialisées, des capacités d'analyse avancées et une stricte conformité réglementaire.
- L'essor des technologies de fabrication basées sur la plate-forme soutient la production flexible et évolutive d'APIs orphelines, permettant aux fabricants de gérer efficacement plusieurs programmes de maladies rares simultanément
- Cette tendance vers des substances pharmaceutiques orphelines plus complexes et personnalisées modifie les stratégies de fabrication de l'API, en mettant davantage l'accent sur la production de petits lots, la manipulation de puissance élevée et les capacités de changement rapide
- Par conséquent, des entreprises comme Lonza et Catalent élargissent leurs capacités en matière de produits biologiques et de thérapie génique pour soutenir la demande croissante de substances pharmaceutiques orphelines de pointe dans plusieurs cas de maladies rares.
API sur les maladies rares / Dynamique du marché des médicaments orphelins
Chauffeur
Élargir les pipelines de médicaments orphelins et les incitatifs réglementaires favorables
- Le nombre croissant de désignations et d'approbations de médicaments orphelins, appuyées par des incitatifs réglementaires favorables comme l'exclusivité du marché, les crédits d'impôt et les voies d'examen accélérées, est un facteur clé qui alimente la demande d'IPA pour les maladies rares.
- Par exemple, les cadres réglementaires aux États-Unis, en Europe et au Japon ont considérablement réduit les délais de développement des médicaments orphelins, encourageant les entreprises biopharmaceutiques à étendre leurs pipelines de maladies rares et à investir dans la fabrication d'API spécialisées.
- À mesure que la sensibilisation, le dépistage et les taux de diagnostic des maladies rares s'améliorent à l'échelle mondiale, la nécessité d'un approvisionnement constant et de haute qualité en substances médicamenteuses augmente, soutenant directement la croissance du marché des IPA orphelins
- De plus, un solide capital de risque et un financement public pour la recherche sur les maladies rares permettent aux petites entreprises de biotechnologie de faire progresser les programmes cliniques, de recourir de plus en plus à la fabrication externalisée d'IPA et à des ODM spécialisés.
- L'accent croissant mis sur la précision et les thérapies personnalisées, combiné au potentiel commercial à long terme en raison de la concurrence limitée, continue de favoriser une demande soutenue de substances pharmaceutiques orphelines
- L'augmentation du soutien gouvernemental et sans but lucratif au développement du traitement des maladies rares renforce la viabilité à long terme des investissements dans la fabrication de médicaments orphelins
- La capacité des médicaments orphelins à commander des prix élevés améliore le rendement de l'investissement, encourageant davantage l'expansion continue de la capacité de production d'API orphelin
Restriction/Défi
Complexité de la fabrication et obstacles à la conformité réglementaire
- La production d'IPA pour maladies rares implique souvent des procédés de fabrication complexes, des exigences de qualité strictes et une taille limitée des lots, ce qui peut augmenter considérablement les coûts de production et les risques techniques
- Par exemple, les substances pharmaceutiques biologiques et de thérapie génique nécessitent des installations spécialisées, du personnel hautement qualifié et des systèmes de confinement avancés, ce qui rend la fabrication plus difficile techniquement et exigeante en capital
- La conformité à la réglementation dans plusieurs régions ajoute à la complexité, car les substances pharmaceutiques orphelines doivent respecter des normes variées et en évolution en matière d'innocuité, de traçabilité et de contrôle de la qualité.
- Ces défis peuvent limiter le nombre de fournisseurs d'API qualifiés, ce qui pourrait entraîner des contraintes d'approvisionnement et des coûts plus élevés, limitant ainsi l'expansion du marché.
- La disponibilité limitée de matières premières et de réactifs spécialisés pour les API orphelines avancées peut perturber davantage les délais de production et accroître la dépendance à l'égard des fournisseurs spécialisés
- La nécessité d'une validation approfondie, de longs délais et de contrôles stricts des changements après approbation peut ralentir l'agilité de la fabrication et retarder l'offre commerciale de substances pharmaceutiques orphelines
IPA des maladies rares / substance médicamenteuse orpheline Portée du marché
Le marché est segmenté en fonction du type d'API/ substance médicamenteuse, de l'indication thérapeutique et de l'utilisateur final.
- Par IPA / Type de substance médicamenteuse
Sur la base du type d'API/substance médicamenteuse, le marché mondial des API/substance médicamenteuse orpheline est segmenté en API biologiques, API à petites molécules, API à vecteurs viraux, API à base d'ARN et substances médicamenteuses liées à la thérapie cellulaire. Le segment des API biologiques a dominé le marché avec la plus grande part des revenus de 58,3% en 2025, en raison de l'utilisation généralisée d'anticorps monoclonaux, de thérapies de remplacement enzymatiques et de protéines recombinantes dans le traitement de troubles génétiques et métaboliques rares. Les produits biologiques offrent une grande spécificité et une grande efficacité clinique, ce qui en fait le choix préféré pour de nombreux programmes pharmaceutiques orphelins. La forte présence de médicaments biologiques orphelins approuvés et la poursuite de l'expansion des pipelines appuient encore plus la domination de ce segment. De plus, les prix élevés et les traitements à long terme contribuent à accroître la production de revenus. L'expertise en fabrication établie et la connaissance de la réglementation des produits biologiques renforcent également leur position de leader.
Le segment des IPA vectorielles virales devrait connaître la croissance la plus rapide au cours de la période de prévision, alimentée par l'avancement rapide des thérapies génétiques pour les maladies rares et ultra-rares. L'augmentation de l'approbation des thérapies à base de vecteurs adéno-associés au virus (AVA) et à base de vecteurs lentiviraux entraîne une forte demande de production de vecteurs spécialisés. Les besoins médicaux élevés non satisfaits, le potentiel de traitement curatif et l'investissement croissant dans les plateformes de thérapie génique accélèrent l'expansion de ce segment. La disponibilité limitée des fournisseurs et les exigences complexes en matière de fabrication augmentent encore l'importance stratégique et l'élan de croissance des IPA vectorielles virales.
- Par indication thérapeutique
Sur la base de l'indication thérapeutique, le marché est segmenté en oncologie, troubles hématologiques, troubles neurologiques et neuromusculaires, troubles métaboliques et endocriniens, maladies infectieuses immunologiques et rares, et maladies cardiovasculaires, ophtalmiques et autres troubles rares. Le segment de l'oncologie a dominé le marché en 2025, en raison du grand nombre de désignations de médicaments orphelins pour les cancers rares et des investissements soutenus dans des thérapies contre le cancer ciblées. Les médicaments rares d'oncologie reposent souvent sur des IPA et des produits biologiques très puissants, ce qui contribue de façon significative à la demande globale d'IPA. Des pipelines cliniques solides, des approbations réglementaires accélérées et des coûts de traitement plus élevés soutiennent encore ce segment de la direction des revenus. En outre, les sociétés pharmaceutiques privilégient l'oncologie rare en raison du remboursement favorable et des avantages d'exclusivité du marché.
Le segment des troubles neurologiques et neuromusculaires devrait croître au rythme le plus rapide au cours de la période de prévision, en raison de la recherche croissante sur les affections neurologiques génétiques telles que l'atrophie musculaire de la colonne vertébrale, la dystrophie musculaire de Duchenne et les épilepsies rares. Les progrès dans la thérapie génique, les médicaments à base d'ARN et la médecine de précision transforment les approches thérapeutiques dans cet espace. L'augmentation des taux de diagnostic et un solide soutien en matière de plaidoyer stimulent davantage l'activité de développement. Comme bon nombre de ces thérapies nécessitent des IPA complexes, la demande de substances médicamenteuses spécialisées augmente rapidement au sein de ce segment.
- Par Utilisateur final
Sur la base de l'utilisateur final, le marché mondial de l'API et des substances médicamenteuses orphelines est segmenté en entreprises biopharmaceutiques, en organismes de développement et de fabrication de contrats (ODMC), en instituts de recherche et en fabricants spécialisés. Le segment des entreprises biopharmaceutiques a représenté la plus grande part de marché en 2025, en raison de leur propriété de pipelines de médicaments orphelins et du contrôle direct de la fabrication commerciale de thérapies de grande valeur. Les grandes et moyennes entreprises biopharmaceutiques investissent fortement dans l'obtention d'un approvisionnement fiable en API pour protéger les périodes d'exclusivité et assurer la qualité des produits. La fabrication interne d'API critiques est souvent préférée pour des raisons stratégiques et de propriété intellectuelle. La domination de ce segment est encore renforcée par de solides capacités financières et une expertise en matière de réglementation.
Le segment des CDMO devrait enregistrer la croissance la plus rapide au cours de la période de prévision, grâce à l'augmentation des tendances en matière d'externalisation parmi les entreprises de biotechnologie et les entreprises pharmaceutiques. La complexité des API orphelines, combinée à de petites tailles de lots et à des exigences élevées en matière de capital, encourage les promoteurs à s'appuyer sur des CDMO spécialisés. Les CDMO offrent une fabrication souple, un soutien réglementaire et des technologies de pointe adaptées aux substances médicamenteuses rares. Comme les petites entreprises de biotechnologie stimulent l'innovation dans les médicaments orphelins, la dépendance à l'égard de CDMO pour la production d'API évolutive et conforme s'accélère rapidement.
IPA sur les maladies rares / marché des médicaments orphelins Analyse régionale
- L'Amérique du Nord a dominé le marché de l'API et des substances médicamenteuses orphelines pour les maladies rares, avec la plus grande part des revenus de 41,5 % en 2025, appuyée par un solide cadre de réglementation des médicaments orphelin, des dépenses élevées en R-D et une forte présence d'entreprises biopharmaceutiques et d'ODM spécialisés.
- Les entreprises de la région accordent une grande valeur aux capacités de fabrication avancées, au respect rigoureux de la qualité et à l'offre fiable de substances médicamenteuses complexes, en particulier pour les produits biologiques, les thérapies géniques et les autres IPA orphelins de grande valeur.
- Ce leadership largement répandu sur le marché est encore appuyé par une forte concentration d'approbations de médicaments orphelins, un financement solide pour la recherche sur les maladies rares, et la présence de grandes sociétés biopharmaceutiques et d'OCMD spécialisés, établissant l'Amérique du Nord comme principale plaque tournante du développement et de la production d'API sur les maladies rares.
API sur les maladies rares des États-Unis / Aperçu du marché des médicaments orphelins
Le marché américain de l'API et des substances médicamenteuses orphelines en matière de maladies rares a remporté la plus grande part de revenus en Amérique du Nord en 2025, grâce à un solide cadre de réglementation des médicaments orphelins, à d'importants investissements en R-D et à une forte concentration d'entreprises biopharmaceutiques et de biotechnologie. Les fabricants accordent de plus en plus d'importance au développement et à l'approvisionnement en IPA complexes pour appuyer l'expansion des pipelines de médicaments orphelins. La présence d'incitations favorables telles que l'exclusivité du marché, les crédits d'impôt et les voies d'approbation accélérées continue de stimuler la demande de substances pharmaceutiques spécialisées. En outre, le rôle important des CDMO et des infrastructures manufacturières de pointe contribue de manière significative à une croissance soutenue du marché.
IPV pour les maladies rares en Europe / Aperçu du marché des médicaments orphelins
Le marché européen de l'API et des substances pharmaceutiques orphelines devrait s'étendre à un TCAC important au cours de la période de prévision, principalement en raison des politiques de soutien de l'EMA en matière de médicaments orphelins et de l'augmentation des investissements dans la recherche sur les maladies rares. Une sensibilisation accrue, des taux de diagnostic améliorés et des collaborations transfrontalières favorisent le développement de médicaments orphelins dans toute la région. Les fabricants européens mettent l'accent sur la qualité, la traçabilité et la conformité à la réglementation, en soutenant la demande constante d'API de grande valeur. On observe une croissance tant dans les modèles de fabrication axés sur l'innovation que dans les modèles sous-traités, en particulier pour les produits biologiques et les thérapies avancées.
U.K. IPV pour les maladies rares / Aperçu du marché des médicaments orphelins
Le marché de l'IPA/des substances pharmaceutiques orphelines des maladies rares du Royaume-Uni devrait croître à un TCAC remarquable au cours de la période de prévision, grâce à une solide collaboration entre les universités et l'industrie et à des initiatives gouvernementales sur les maladies rares. L'écosystème avancé des sciences de la vie du Royaume-Uni encourage le développement de médicaments orphelins en début de développement, ce qui accroît la demande d'IPA en phase clinique. Les investissements continus dans la recherche en biologie et en thérapie génique renforcent les perspectives du marché. En outre, l'alignement de la réglementation sur les normes mondiales renforce l'attrait du pays pour les partenariats de fabrication et de développement d'API orphelins.
Allemagne API sur les maladies rares / substance orpheline
Le marché allemand de l'API/des substances pharmaceutiques orphelines devrait connaître une expansion considérable au cours de la période de prévision, alimentée par une solide base de fabrication de produits pharmaceutiques et mettant fortement l'accent sur l'innovation et la qualité. Le leadership de l'Allemagne dans la production de produits biologiques et les technologies de fabrication de pointe soutient la demande constante de substances pharmaceutiques orphelines complexes. Le pays met l'accent sur la conformité, la sécurité et la fabrication de précision s'harmonise bien avec les exigences strictes des API maladies rares. L'augmentation des investissements dans les thérapies avancées renforce encore les perspectives de croissance du marché.
API sur les maladies rares en Asie-Pacifique / Aperçu du marché des médicaments orphelins
Le marché de l'API/des substances médicamenteuses orphelines en Asie et dans le Pacifique est sur le point de croître le plus rapidement possible durant la période de prévision, en raison de l'expansion des capacités en biotechnologie, de l'augmentation des investissements dans les soins de santé et de l'externalisation croissante des marchés occidentaux. Des pays comme la Chine, le Japon et l'Inde renforcent leurs cadres réglementaires sur les maladies rares et leurs infrastructures manufacturières. Les avantages de coûts de la région et l'expertise technique croissante attirent les entreprises biopharmaceutiques mondiales à la recherche d'une production d'API évolutive. Cette tendance accélère considérablement l'expansion du marché dans l'ensemble de l'APAC.
L'API sur les maladies rares au Japon / Aperçu du marché des médicaments orphelins
Le marché japonais de l'API/des substances pharmaceutiques orphelines est en pleine expansion en raison de l'appui fort du gouvernement à la mise au point de médicaments orphelines et aux capacités de fabrication pharmaceutique avancées. Le Japon accorde une grande importance à la qualité, à la sécurité et à l'innovation, ce qui stimule la demande de substances pharmaceutiques hautement spécialisées. Le pays met l'accent sur les maladies rares génétiques et neurologiques, ce qui accroît le besoin d'API complexes, y compris les produits biologiques et les substances à base d'ARN. Une population vieillissante et la prévalence croissante de troubles rares favorisent davantage la croissance du marché.
IPV pour les maladies rares en Inde / Aperçu du marché des médicaments orphelins
Le marché indien de l'API/des substances pharmaceutiques orphelines pour les maladies rares a représenté une part importante des revenus en Asie-Pacifique en 2025, attribuable à une solide expertise dans la fabrication de l'API, à la compétitivité des coûts et à l'expansion des investissements en biotechnologie. L'Inde est en train de devenir un fournisseur clé d'API de petites molécules et de plus en plus biologique pour les marchés mondiaux. Les initiatives gouvernementales soutenant le développement du traitement des maladies rares et la fabrication locale améliorent les perspectives du marché. La présence croissante d'ODCM et de fabricants de contrats nationaux renforce encore le rôle de l'Inde dans la chaîne mondiale d'approvisionnement en substances pharmaceutiques orphelines.
IPV des maladies rares / Part de marché des substances pharmaceutiques orphelines
L'industrie de l'API sur les maladies rares et des médicaments orphelins est principalement dirigée par des entreprises bien établies, notamment :
- Lonza Ltd (Suisse)
- Catalent, Inc. (États-Unis)
- WuXi AppTec Co., Ltd. (Chine)
- Pfizer Inc. (États-Unis)
- Novartis AG (Suisse)
- F. Hoffmann-La Roche Ltd (Suisse)
- Bristol-Myers Squibb Company (États-Unis)
- Amgen Inc. (États-Unis)
- Sanofi (France)
- Takeda Pharmaceutical Company Limited (Japon)
- AbbVie Inc. (États-Unis)
- GSK plc (Royaume-Uni)
- Bayer AG (Allemagne)
- Vertex Pharmaceuticals Incorporated (États-Unis)
- Biogen Inc. (États-Unis)
- PTC Therapeutics, Inc. (États-Unis)
- orphelin suédois Biovitrum AB (Suède)
- SOM Innovation Biotech, S.A. (Espagne)
- Ultragenyx Pharmaceutical Inc. (États-Unis)
Quelles sont les évolutions récentes de l'API mondiale sur les maladies rares / marché des médicaments orphelins?
- En août 2025, la FDA américaine a approuvé Papzimeos (zopapogene imadenovec), la première immunothérapie pour la papillomatose respiratoire récurrente (RPR), une affection rare désignée par les orphelins, sous-tendant les avancées immunothérapeutiques à base de gènes pour les maladies rares
- En avril 2025, l'Accélérateur de thérapies orphelines sans but lucratif a annoncé des partenariats clés visant à faire progresser le développement et la commercialisation des thérapies ultra-rares, à relever les défis historiques du financement et à faire avancer les candidats aux médicaments orphelin.
- En janvier 2024, le paysage des médicaments orphelins de la FDA a connu une expansion significative avec un nombre record d'approbations (28 nouveaux médicaments orphelins), y compris des thérapies de première classe pour des affections comme l'ataxie de Friedreich et le syndrome de Rett, mettant en évidence la croissance rapide du développement thérapeutique des maladies rares
- En août 2023, la FDA des États-Unis a approuvé le pozelimab (Veopoz) comme premier traitement de la maladie de CHAPLE, un trouble du système ultra-rare, représentant une nouvelle thérapie recombinante d'anticorps monoclonaux traitant d'une maladie par ailleurs fatale
- En mai 2023, la FDA des États-Unis a approuvé l'Adzynma (apadamtase alfa), un traitement de remplacement enzymatique ADAMTS13 recombinant pour la purpure thrombotique congénitale thrombopénique (TPc), marquant le premier traitement biologique approuvé contre ce trouble de coagulation sanguine ultra-rare et l'expansion des options de remplacement enzymatique pour les patients atteints de maladies rares
SKU-
Accédez en ligne au rapport sur le premier cloud mondial de veille économique
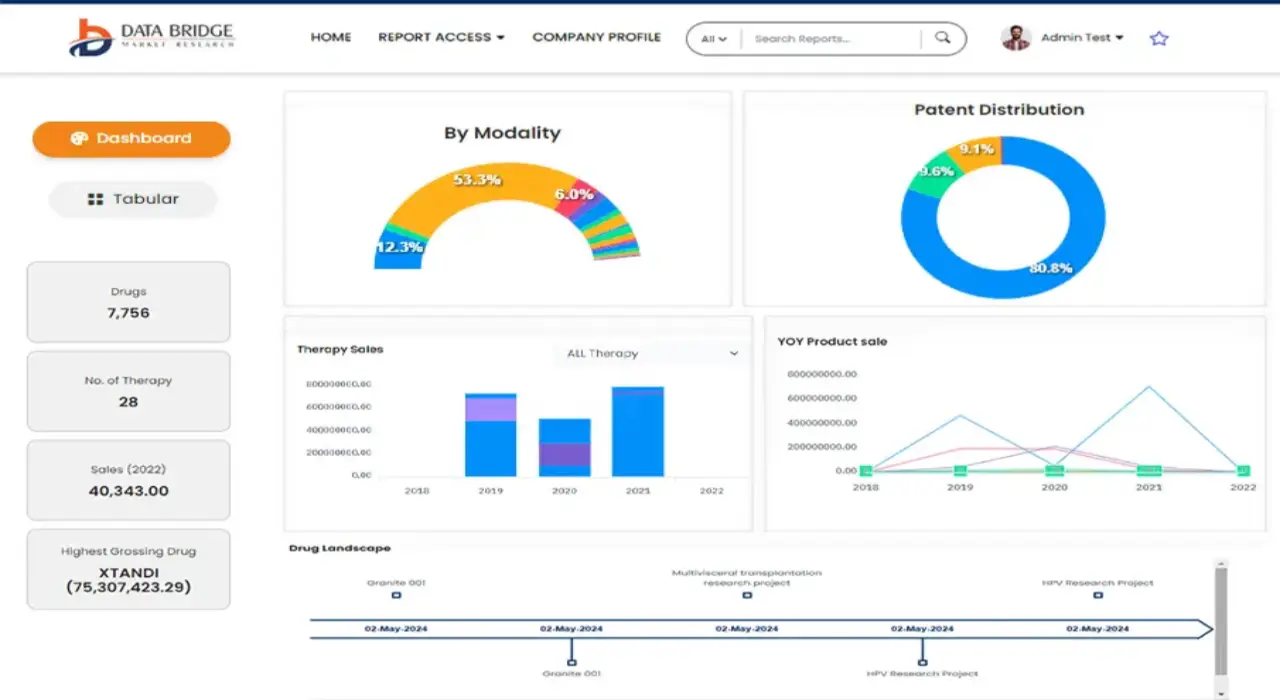
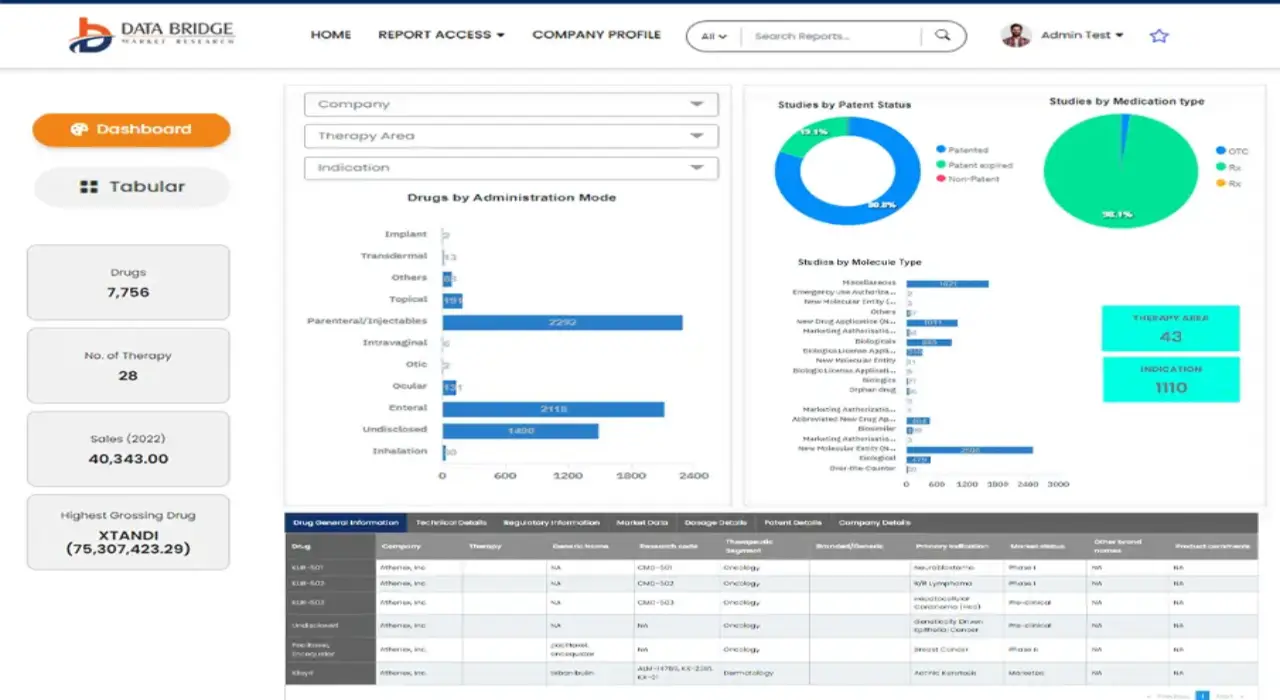
- Tableau de bord d'analyse de données interactif
- Tableau de bord d'analyse d'entreprise pour les opportunités à fort potentiel de croissance
- Accès d'analyste de recherche pour la personnalisation et les requêtes
- Analyse de la concurrence avec tableau de bord interactif
- Dernières actualités, mises à jour et analyse des tendances
- Exploitez la puissance de l'analyse comparative pour un suivi complet de la concurrence
Méthodologie de recherche
La collecte de données et l'analyse de l'année de base sont effectuées à l'aide de modules de collecte de données avec des échantillons de grande taille. L'étape consiste à obtenir des informations sur le marché ou des données connexes via diverses sources et stratégies. Elle comprend l'examen et la planification à l'avance de toutes les données acquises dans le passé. Elle englobe également l'examen des incohérences d'informations observées dans différentes sources d'informations. Les données de marché sont analysées et estimées à l'aide de modèles statistiques et cohérents de marché. De plus, l'analyse des parts de marché et l'analyse des tendances clés sont les principaux facteurs de succès du rapport de marché. Pour en savoir plus, veuillez demander un appel d'analyste ou déposer votre demande.
La méthodologie de recherche clé utilisée par l'équipe de recherche DBMR est la triangulation des données qui implique l'exploration de données, l'analyse de l'impact des variables de données sur le marché et la validation primaire (expert du secteur). Les modèles de données incluent la grille de positionnement des fournisseurs, l'analyse de la chronologie du marché, l'aperçu et le guide du marché, la grille de positionnement des entreprises, l'analyse des brevets, l'analyse des prix, l'analyse des parts de marché des entreprises, les normes de mesure, l'analyse globale par rapport à l'analyse régionale et des parts des fournisseurs. Pour en savoir plus sur la méthodologie de recherche, envoyez une demande pour parler à nos experts du secteur.
Personnalisation disponible
Data Bridge Market Research est un leader de la recherche formative avancée. Nous sommes fiers de fournir à nos clients existants et nouveaux des données et des analyses qui correspondent à leurs objectifs. Le rapport peut être personnalisé pour inclure une analyse des tendances des prix des marques cibles, une compréhension du marché pour d'autres pays (demandez la liste des pays), des données sur les résultats des essais cliniques, une revue de la littérature, une analyse du marché des produits remis à neuf et de la base de produits. L'analyse du marché des concurrents cibles peut être analysée à partir d'une analyse basée sur la technologie jusqu'à des stratégies de portefeuille de marché. Nous pouvons ajouter autant de concurrents que vous le souhaitez, dans le format et le style de données que vous recherchez. Notre équipe d'analystes peut également vous fournir des données sous forme de fichiers Excel bruts, de tableaux croisés dynamiques (Fact book) ou peut vous aider à créer des présentations à partir des ensembles de données disponibles dans le rapport.