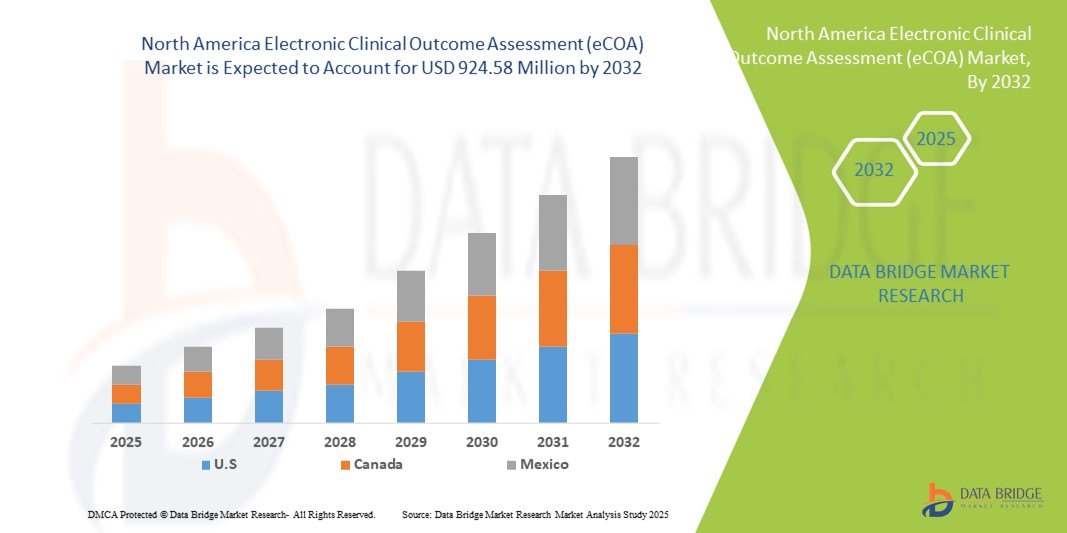
North America Electronic Clinical Outcome Assessment Ecoa Market
Taille du marché en milliards USD
TCAC :
% 
 USD
265.11 Million
USD
924.58 Million
2024
2032
USD
265.11 Million
USD
924.58 Million
2024
2032
| 2025 –2032 | |
| USD 265.11 Million | |
| USD 924.58 Million | |
|
|
|
|
Segmentation du marché nord-américain de l'évaluation électronique des résultats cliniques (eCOA), par produit (solutions sur site, solutions infonuagiques et solutions web), approche (évaluation des résultats rapportés par le clinicien (CLINRO), évaluation des résultats rapportés par le patient (PRO), évaluation des résultats rapportés par l'observateur (OBSRO) et évaluation des résultats de performance (PERFO)), utilisateur final (prestataires de services commerciaux, hôpitaux et centres de transplantation, laboratoires de recherche et établissements universitaires), plateforme (organismes de recherche sous contrat, sociétés pharmaceutiques et biopharmaceutiques , fabricants de dispositifs médicaux, hôpitaux et laboratoires cliniques, sociétés de conseil, recherche et universités, etc.) - Tendances et prévisions du secteur jusqu'en 2032
Taille du marché nord-américain de l'évaluation électronique des résultats cliniques (eCOA)
- La taille du marché nord-américain de l'évaluation électronique des résultats cliniques (eCOA) était évaluée à 265,11 millions USD en 2024 et devrait atteindre 924,58 millions USD d'ici 2032 , à un TCAC de 16,90 % au cours de la période de prévision.
- La croissance du marché est largement alimentée par la numérisation croissante des essais cliniques et l’adoption croissante de solutions de santé axées sur la technologie, conduisant à une efficacité, une précision et des approches centrées sur le patient améliorées dans les études cliniques.
- Par ailleurs, le besoin croissant de saisie de données patients en temps réel, de suivi à distance et de conformité réglementaire favorise l'adoption de solutions d'évaluation électronique des résultats cliniques (eCOA), stimulant ainsi considérablement la croissance du secteur. Ces facteurs convergents permettent aux entreprises pharmaceutiques et biotechnologiques, ainsi qu'aux organismes de recherche sous contrat, de rationaliser leurs opérations d'essais et d'améliorer les résultats cliniques globaux.
Analyse du marché nord-américain de l'évaluation électronique des résultats cliniques (eCOA)
- Les solutions d'évaluation électronique des résultats cliniques (eCOA) deviennent de plus en plus des composants essentiels des essais cliniques, offrant une collecte de données en temps réel, précise et centrée sur le patient pour améliorer la qualité des études, la conformité réglementaire et l'efficacité opérationnelle.
- L'adoption croissante de l'eCOA est principalement alimentée par la demande croissante d'essais cliniques décentralisés et à distance, l'accent croissant mis sur la recherche centrée sur le patient et le besoin d'une capture efficace des données sur plusieurs sites.
- Les États-Unis ont dominé le marché de l'évaluation électronique des résultats cliniques (eCOA), avec une part de chiffre d'affaires record de 79,01 % en 2024, grâce à la présence de grandes entreprises pharmaceutiques et biotechnologiques, à une infrastructure de recherche clinique de pointe et à des investissements importants dans les solutions de santé numérique. Les États-Unis, en particulier, ont connu une croissance substantielle des déploiements d'eCOA, soutenue par des pipelines d'essais cliniques à grande échelle, des initiatives gouvernementales encourageant l'adoption du numérique et un écosystème technologique robuste facilitant l'intégration avec les systèmes de saisie électronique des données et de gestion des essais.
- Le Canada devrait connaître la croissance la plus rapide sur le marché nord-américain de l'évaluation électronique des résultats cliniques (EERC) au cours de la période de prévision, grâce au soutien gouvernemental croissant aux solutions cliniques numériques, à l'externalisation croissante des essais cliniques et à l'adoption croissante des plateformes EEC infonuagiques et mobiles. L'expansion des réseaux de recherche et la sensibilisation croissante des professionnels de la santé aux technologies centrées sur le patient accélèrent encore la croissance du marché au pays.
- Le segment de l'évaluation des résultats rapportés par les patients (PRO) a dominé le marché de l'évaluation électronique des résultats cliniques (eCOA) avec la plus grande part de revenus du marché de 52,1 % en 2024, car les essais centrés sur les patients deviennent de plus en plus importants.
Portée du rapport et segmentation du marché de l'évaluation électronique des résultats cliniques (eCOA)
|
Attributs |
Évaluation électronique des résultats cliniques (eCOA) : principales perspectives du marché |
|
Segments couverts |
|
|
Pays couverts |
Amérique du Nord
|
|
Principaux acteurs du marché |
|
|
Opportunités de marché |
|
|
Ensembles d'informations de données à valeur ajoutée |
Outre les informations sur les scénarios de marché tels que la valeur marchande, le taux de croissance, la segmentation, la couverture géographique et les principaux acteurs, les rapports de marché organisés par Data Bridge Market Research comprennent également une analyse approfondie des experts, une analyse des prix, une analyse de la part de marque, une enquête auprès des consommateurs, une analyse démographique, une analyse de la chaîne d'approvisionnement, une analyse de la chaîne de valeur, un aperçu des matières premières/consommables, des critères de sélection des fournisseurs, une analyse PESTLE, une analyse Porter et un cadre réglementaire. |
Tendances du marché nord-américain de l'évaluation électronique des résultats cliniques (eCOA)
Adoption croissante des résultats numériques rapportés par les patients et de la surveillance à distance
- Une tendance significative et croissante sur le marché américain de l'évaluation électronique des résultats cliniques (eCOA) est l'adoption croissante des plateformes de rapports numériques des résultats des patients (ePRO) et des solutions de saisie de données à distance. Ces technologies améliorent la précision des données, le suivi en temps réel et l'engagement des patients dans les essais cliniques.
- Par exemple, la mise en œuvre de solutions eCOA dans des essais oncologiques de phase III multicentriques a permis une collecte transparente des données sur les symptômes des patients, réduisant ainsi les erreurs de saisie manuelle et améliorant la conformité aux évaluations définies par le protocole.
- Les plateformes de surveillance à distance permettent au personnel clinique de suivre les résultats rapportés par les patients en temps réel, permettant une intervention plus rapide, une meilleure surveillance des essais et des données plus fiables pour les soumissions réglementaires.
- L'intégration des systèmes eCOA basés sur le cloud avec les plateformes de gestion des essais cliniques garantit que les données collectées peuvent être consultées, agrégées et analysées efficacement sur plusieurs sites d'essai, prenant en charge la gestion centralisée des études.
- L'accent est de plus en plus mis sur les conceptions d'essais centrées sur le patient, où les solutions eCOA améliorent la commodité et l'adhésion, conduisant à une plus grande exhaustivité et qualité des données.
- Les organismes de réglementation et les promoteurs reconnaissent de plus en plus la valeur des évaluations électroniques des résultats pour améliorer l’efficacité des essais et accélérer la prise de décision, encourageant ainsi une adoption plus poussée de ces solutions.
Dynamique du marché nord-américain de l'évaluation électronique des résultats cliniques (eCOA)
Conducteur
Besoin croissant en raison de la demande croissante de saisie numérique des données cliniques et d'essais centrés sur le patient
- L'importance croissante accordée à la collecte de données cliniques précises et en temps réel, associée à l'évolution croissante vers des conceptions d'essais centrées sur le patient, constitue un facteur important de la demande accrue de solutions eCOA.
- Par exemple, en avril 2024, Medidata Solutions a annoncé le lancement d'une plateforme améliorée de rapports électroniques sur les résultats des patients, conçue pour s'intégrer parfaitement aux systèmes mondiaux de gestion des essais cliniques. Ces avancées, réalisées par des entreprises clés, devraient stimuler la croissance du secteur des rapports électroniques sur les résultats (eCOA) au cours de la période de prévision.
- Alors que les sponsors et les organismes de recherche clinique cherchent à améliorer l'efficacité et la conformité des essais, les plateformes eCOA offrent des fonctionnalités telles que la capture de données à distance, les notifications automatisées et la surveillance en temps réel des résultats rapportés par les patients, offrant ainsi une alternative convaincante aux méthodes traditionnelles sur papier.
- En outre, l’adoption croissante d’essais cliniques décentralisés et virtuels fait des systèmes eCOA un élément essentiel des conceptions d’études modernes, permettant aux participants de signaler les résultats depuis leur domicile ou leurs établissements de santé locaux.
- La commodité du suivi à distance, l'intégration aux plateformes d'analyse des essais cliniques et l'amélioration de la conformité réglementaire sont des facteurs clés qui favorisent l'adoption des solutions eCOA dans les secteurs pharmaceutique, biotechnologique et de la recherche contractuelle. La tendance à la transformation numérique des essais cliniques contribue également à la croissance du marché.
Retenue/Défi
Préoccupations concernant la sécurité des données, la conformité réglementaire et les coûts initiaux élevés de mise en œuvre
- Les préoccupations concernant la confidentialité des données, la cybersécurité et le respect des réglementations telles que HIPAA et RGPD constituent un défi majeur pour une pénétration plus large du marché. Les systèmes eCOA traitent des informations sensibles sur les patients, et les violations ou le non-respect pourraient entraîner des conséquences financières et juridiques substantielles.
- Par exemple, des audits réglementaires rigoureux et un contrôle accru des données cliniques numériques ont rendu certains sponsors prudents quant à l’adoption de nouvelles plateformes eCOA sans protocoles de sécurité validés.
- Répondre à ces préoccupations grâce à un chiffrement robuste, des méthodes d'authentification sécurisées et le respect des normes réglementaires mondiales est essentiel pour instaurer la confiance entre les promoteurs, les CRO et les sites cliniques. Des entreprises comme ERT et CRF Health mettent en avant leurs plateformes sécurisées et leurs certifications de conformité pour rassurer les parties prenantes.
- En outre, le coût initial relativement élevé des implémentations complètes d’eCOA peut constituer un obstacle pour les petites entreprises biopharmaceutiques ou les essais cliniques en phase précoce.
- Bien que les modèles d'abonnement et les plateformes basées sur le cloud réduisent progressivement les coûts initiaux, la prime perçue pour les solutions eCOA entièrement intégrées peut encore entraver l'adoption, en particulier sur les marchés émergents ou pour les organisations soucieuses de leur budget.
- Surmonter ces défis grâce à des mesures de sécurité des données renforcées, des programmes de formation pour le personnel clinique et le développement d'options eCOA évolutives et rentables sera essentiel pour une croissance soutenue du marché.
Portée du marché nord-américain de l'évaluation électronique des résultats cliniques (eCOA)
Le marché est segmenté sur la base du produit, de l’approche, de l’utilisateur final et de la plateforme.
- Par produit
En termes de produits, le marché de l'évaluation électronique des résultats cliniques (eCOA) est segmenté en solutions sur site, solutions cloud et solutions web. Le segment des solutions cloud a dominé le marché avec une part de chiffre d'affaires de 47,5 % en 2024, grâce à son évolutivité et sa flexibilité dans la gestion d'essais cliniques complexes. Les solutions cloud offrent un accès en temps réel aux données de plusieurs sites d'essai, permettant une prise de décision plus rapide et une efficacité opérationnelle améliorée. La possibilité d'intégrer des appareils mobiles et de garantir un stockage sécurisé des données a favorisé leur adoption par les laboratoires pharmaceutiques et les CRO. Les plateformes cloud réduisent les coûts d'infrastructure informatique et prennent en charge les modèles d'essais décentralisés et hybrides. Leurs interfaces conviviales et leurs outils de reporting automatisés améliorent encore la précision des données. La surveillance à distance et le contrôle centralisé en font la solution idéale pour les études multicentriques à grande échelle. Ce segment bénéficie d'une innovation continue et du soutien des fournisseurs, ce qui lui permet de maintenir sa position dominante sur le marché.
Le segment des solutions sur site devrait connaître le TCAC le plus rapide, soit 18,2 % entre 2025 et 2032, les organisations privilégiant le contrôle et la sécurité des données internes. Les plateformes sur site garantissent une conformité rigoureuse aux exigences réglementaires, permettant un contrôle total des données sensibles des patients et des essais. Elles peuvent être personnalisées pour répondre à des besoins spécifiques en matière de flux de travail et intégrées à l'infrastructure informatique existante des hôpitaux ou des établissements. Les solutions sur site sont particulièrement privilégiées pour les essais nécessitant des mesures de sécurité élevées, comme les études en oncologie ou sur les maladies rares. L'augmentation des investissements dans les capacités informatiques des hôpitaux et des centres de recherche stimule leur adoption. Ces systèmes offrent une confidentialité des données renforcée et une continuité opérationnelle en cas de panne de courant. Les mises à jour logicielles et le support technique continus renforcent encore la fiabilité. La transition croissante vers les essais cliniques numériques favorise l'adoption croissante des plateformes sur site.
- Par approche
Selon l'approche adoptée, le marché de l'évaluation électronique des résultats cliniques (eCOA) est segmenté en deux catégories : l'évaluation des résultats rapportés par le clinicien (CLINRO), l'évaluation des résultats rapportés par le patient (PRO), l'évaluation des résultats rapportés par l'observateur (OBSRO) et l'évaluation des résultats de performance (PERFO). Le segment de l'évaluation des résultats rapportés par le patient (PRO) détenait la plus grande part de chiffre d'affaires du marché, avec 52,1 % en 2024, les essais centrés sur le patient gagnant en importance. Les solutions PRO permettent aux participants de signaler directement leurs symptômes, leurs indicateurs de qualité de vie et leurs réponses au traitement, améliorant ainsi la précision des données et l'engagement. Les autorités réglementaires reconnaissent l'importance des données PRO pour l'approbation des médicaments et la surveillance post-commercialisation. L'intégration aux applications mobiles permet l'utilisation de rappels, de journaux électroniques et de rapports automatisés. Les évaluations PRO améliorent la surveillance en temps réel et la détection précoce des événements indésirables. Elles réduisent la dépendance à la collecte manuelle de données et améliorent l'efficacité des essais. Les promoteurs bénéficient d'informations exploitables pour des conceptions d'essais adaptatives. La flexibilité et la standardisation mondiale de ce segment contribuent à sa domination continue.
Le segment des évaluations des résultats cliniques (CLINRO) devrait connaître le TCAC le plus rapide, soit 16,4 % entre 2025 et 2032, grâce à une adoption croissante dans les études hospitalières et la recherche clinique complexe. Les outils CLINRO permettent aux cliniciens de fournir des évaluations structurées des résultats des patients, garantissant ainsi des données de haute qualité pour les essais impliquant des interventions complexes. Ces évaluations sont cruciales pour les soumissions réglementaires et la validation de l'efficacité thérapeutique. L'intégration aux dossiers médicaux électroniques et aux systèmes de gestion des essais cliniques améliore l'efficacité des flux de travail. Les plateformes numériques CLINRO réduisent les erreurs, rationalisent la documentation et permettent la saisie de données à distance. L'adoption croissante dans les études en oncologie, cardiologie et neurologie contribue à cette croissance. Des fonctionnalités de reporting et d'analyse améliorées offrent une meilleure compréhension de l'efficacité des traitements. Le segment bénéficie du développement des programmes de formation et du soutien réglementaire, ce qui accélère son adoption.
- Par utilisateur final
En fonction de l'utilisateur final, le marché de l'évaluation électronique des résultats cliniques (eCOA) est segmenté entre les prestataires de services commerciaux, les hôpitaux et centres de transplantation, ainsi que les laboratoires de recherche et les établissements universitaires. Le segment des hôpitaux et centres de transplantation a dominé le marché avec la plus grande part de chiffre d'affaires (49,3 %) en 2024, grâce au volume élevé d'essais cliniques menés dans ces établissements. Les hôpitaux bénéficient d'une infrastructure informatique intégrée, d'un personnel formé et de capacités d'essais multicentriques. Les solutions eCOA améliorent l'engagement des patients, réduisent la saisie manuelle des données et garantissent la conformité aux normes réglementaires. La surveillance à distance et les rapports automatisés améliorent l'efficacité opérationnelle. Les hôpitaux peuvent exploiter des informations en temps réel pour optimiser les protocoles d'étude. L'adoption croissante des essais hybrides et décentralisés soutient également la demande. L'intégration aux dossiers médicaux électroniques garantit une fluidité des flux de travail. Les analyses avancées au sein des systèmes hospitaliers accélèrent la prise de décision et optimisent les ressources.
Le segment des laboratoires de recherche et des établissements universitaires devrait connaître le TCAC le plus rapide, soit 17,1 %, entre 2025 et 2032, car ces entités adoptent de plus en plus de solutions numériques pour améliorer l'efficacité des études. Les établissements universitaires mènent divers essais cliniques et recherches collaboratives nécessitant une collecte de données précise et rapide. Les plateformes eCOA, cloud et sur site, permettent une coordination fluide entre plusieurs sites de recherche. Le financement public et privé stimule les investissements technologiques. L'adoption de l'eCOA permet un recrutement plus rapide, une meilleure implication des participants et une gestion efficace des données. Des rapports et des analyses avancés améliorent les connaissances de la recherche. Les établissements bénéficient de solutions évolutives prenant en charge divers protocoles d'essai. Le développement des partenariats entre le monde universitaire et l'industrie contribue à une adoption rapide. La maîtrise du numérique par les chercheurs facilite l'adoption et l'intégration dans les flux de travail des études.
- Par plateforme
Sur la base des plateformes, le marché de l'évaluation électronique des résultats cliniques (eCOA) est segmenté en organismes de recherche sous contrat, sociétés pharmaceutiques et biopharmaceutiques, fabricants de dispositifs médicaux, hôpitaux et laboratoires cliniques, sociétés de conseil, et recherche et milieu universitaire. Le segment des sociétés pharmaceutiques et biopharmaceutiques détenait la plus grande part de chiffre d'affaires du marché, soit 50,2 % en 2024, grâce à son rôle essentiel dans les essais cliniques mondiaux. Ces entreprises ont besoin d'un suivi précis des résultats des patients pour les soumissions réglementaires et les autorisations de mise sur le marché. Les plateformes eCOA offrent une surveillance en temps réel, un stockage sécurisé des données et une intégration aux systèmes de gestion des essais. Leur adoption est soutenue par d'importants budgets de R&D et des opérations d'essais à l'échelle mondiale. Les solutions cloud et hybrides permettent une coordination multi-sites et des conceptions d'essais adaptatives. L'automatisation des rapports améliore l'efficacité et minimise les erreurs humaines. La conformité réglementaire et la préparation aux audits sont assurées par des systèmes numériques sécurisés. L'accent croissant mis sur le développement de médicaments centrés sur le patient maintient la domination de ce segment.
Le segment des organismes de recherche sous contrat (ORC) devrait connaître le TCAC le plus rapide, soit 18,5 % entre 2025 et 2032, grâce à l'externalisation de la gestion des essais cliniques par les promoteurs pharmaceutiques. Les ORC exploitent les plateformes eCOA pour gérer efficacement des études complexes sur plusieurs sites. Les solutions cloud et mobiles facilitent la saisie et le suivi des données en temps réel. L'adoption est accélérée par des modèles d'essais décentralisés et hybrides. L'intégration de l'eCOA améliore l'engagement des patients, réduit les goulots d'étranglement opérationnels et garantit la conformité réglementaire. Les ORC investissent de plus en plus dans des outils d'analyse et de reporting avancés pour soutenir la prise de décision de leurs clients. La formation et la standardisation des flux de travail améliorent encore l'efficacité. L'expansion des réseaux d'essais mondiaux stimule l'adoption en Amérique du Nord. Les mises à niveau continues des plateformes et les innovations en matière de services soutiennent une croissance rapide.
Analyse régionale du marché nord-américain de l'évaluation électronique des résultats cliniques (eCOA)
- L'Amérique du Nord a dominé le marché de l'évaluation électronique des résultats cliniques (eCOA), enregistrant la plus grande part de chiffre d'affaires en 2024, grâce à la présence de grandes sociétés pharmaceutiques et biotechnologiques, à une infrastructure de recherche clinique de pointe et à des investissements importants dans les solutions de santé numériques. La région a connu une adoption rapide des plateformes cliniques numériques, notamment dans les essais cliniques à grande échelle et multicentriques, répondant ainsi à la demande de saisie de données en temps réel et de gestion simplifiée des essais.
- L'adoption généralisée de l'eCOA en Amérique du Nord est renforcée par un écosystème technologique robuste permettant une intégration transparente avec les systèmes de saisie électronique de données, les plateformes de gestion des essais cliniques et les solutions d'analyse. Grâce à ces plateformes numériques intégrées, les promoteurs et les CRO bénéficient d'une efficacité opérationnelle accrue, d'une conformité réglementaire accrue et d'un engagement accru des patients.
- Un financement élevé de la recherche, des initiatives gouvernementales favorisant l'adoption de la santé numérique et la présence de fournisseurs de technologies clés dans la région renforcent encore la position de leader de l'Amérique du Nord sur le marché mondial de l'eCOA.
Aperçu du marché américain de l'évaluation électronique des résultats cliniques (eCOA)
Le marché américain de l'évaluation électronique des résultats cliniques (eCOA) a dominé le marché nord-américain avec une part de chiffre d'affaires de 79,01 % en 2024, portée par l'adoption rapide des plateformes cliniques numériques, les pipelines d'essais cliniques à grande échelle et les initiatives gouvernementales soutenant l'intégration technologique dans les soins de santé. La forte présence des entreprises pharmaceutiques et biotechnologiques stimule une forte demande de solutions eCOA permettant de gérer efficacement des essais complexes et multicentriques. Le marché américain bénéficie d'une infrastructure de recherche clinique avancée, garantissant une saisie précise et conforme des données patients. L'augmentation des investissements dans les solutions de santé numérique, l'intégration de l'eCOA aux systèmes de saisie électronique des données (EDC) et la nécessité d'un suivi en temps réel des résultats rapportés par les patients stimulent davantage la croissance du marché. Aux États-Unis, les prestataires de soins de santé et les promoteurs d'essais cliniques privilégient de plus en plus les technologies centrées sur le patient, qui facilitent l'engagement, l'observance et la précision des rapports dans les essais, renforçant ainsi la position dominante du pays sur le marché.
Aperçu du marché canadien de l'évaluation électronique des résultats cliniques (eCOA)
Le marché canadien de l'évaluation électronique des résultats cliniques (EERC) devrait connaître la croissance la plus rapide en Amérique du Nord au cours de la période de prévision, grâce au soutien croissant des gouvernements aux solutions cliniques numériques et à l'externalisation croissante des essais cliniques auprès de prestataires de services spécialisés. L'adoption croissante de plateformes EERC infonuagiques et mobiles permet une collecte efficace des données des patients, une meilleure conformité réglementaire et une plus grande flexibilité pour les promoteurs d'essais cliniques partout au pays. L'expansion des réseaux de recherche, la sensibilisation croissante des prestataires de soins de santé aux technologies d'essais cliniques centrées sur le patient et la nécessité d'une saisie de données plus simplifiée dans les essais multicentriques accélèrent la croissance du marché de l'EERC au Canada. L'augmentation des investissements dans l'infrastructure numérique et des politiques de soutien renforce la trajectoire du Canada en tant que marché à la croissance la plus rapide pour les solutions EERC en Amérique du Nord.
Part de marché de l'évaluation électronique des résultats cliniques (eCOA) en Amérique du Nord
Le secteur de l’évaluation électronique des résultats cliniques (eCOA) est principalement dirigé par des entreprises bien établies, notamment :
- IQVIA (États-Unis)
- Clario (États-Unis)
- Medidata (États-Unis)
- Veeva Systems (États-Unis)
- Earth Resources Technology (États-Unis)
- Oracle Health Sciences (États-Unis)
- YPrime, LLC (États-Unis)
- ArisGlobal LLC (États-Unis)
- Castor EDC (Pays-Bas)
- eClinicalWorks (États-Unis)
- Medrio, Inc. (États-Unis)
- ClinOne (États-Unis)
- Signant Health (États-Unis)
- Clinical Ink, Inc. (États-Unis)
- Curebase, Inc. (États-Unis)
- Kayentis (France)
- Calice (Royaume-Uni)
- Datacubed Health (États-Unis)
- HealthDiary, Inc. (États-Unis)
Derniers développements sur le marché nord-américain de l'évaluation électronique des résultats cliniques (eCOA)
- En décembre 2023, ObvioHealth USA, Inc., société mondiale spécialisée dans les essais cliniques numériques, a lancé une solution d'évaluation électronique des résultats cliniques (eCOA). Cette plateforme intègre harmonieusement une technologie avancée de conception d'études à des services scientifiques et cliniques afin d'offrir des résultats plus fiables aux promoteurs d'essais.
- En mai 2025, Medidata, acteur majeur du secteur de l'eCOA, a été reconnu comme leader par l'évaluation PEAK Matrix d'Everest Group pour l'eCOA. Cette évaluation a mis en lumière l'accompagnement de Medidata auprès de plus d'un million de patients et sa capacité à réduire jusqu'à 50 % les délais de réalisation des études par rapport à la norme du secteur.
- En mars 2025, le Critical Path Institute (C-Path) a annoncé la conclusion réussie de l'initiative eCOA : Getting Better Together. Cette collaboration, portée par un engagement commun en faveur du développement de médicaments centrés sur le patient, a permis des changements significatifs et durables, bénéfiques pour toutes les parties prenantes de l'écosystème eCOA.
- En juin 2025, Medable Inc., fournisseur mondial de technologies de développement clinique, a lancé son nouveau Programme Partenaires. Cette initiative vise à doter les organismes de recherche sous contrat (ORC) et autres partenaires de capacités de création de certificats d'authenticité électroniques (COA) en libre-service, basés sur l'IA générative, pour des essais cliniques numériques.
SKU-
Accédez en ligne au rapport sur le premier cloud mondial de veille économique
- Tableau de bord d'analyse de données interactif
- Tableau de bord d'analyse d'entreprise pour les opportunités à fort potentiel de croissance
- Accès d'analyste de recherche pour la personnalisation et les requêtes
- Analyse de la concurrence avec tableau de bord interactif
- Dernières actualités, mises à jour et analyse des tendances
- Exploitez la puissance de l'analyse comparative pour un suivi complet de la concurrence
Méthodologie de recherche
La collecte de données et l'analyse de l'année de base sont effectuées à l'aide de modules de collecte de données avec des échantillons de grande taille. L'étape consiste à obtenir des informations sur le marché ou des données connexes via diverses sources et stratégies. Elle comprend l'examen et la planification à l'avance de toutes les données acquises dans le passé. Elle englobe également l'examen des incohérences d'informations observées dans différentes sources d'informations. Les données de marché sont analysées et estimées à l'aide de modèles statistiques et cohérents de marché. De plus, l'analyse des parts de marché et l'analyse des tendances clés sont les principaux facteurs de succès du rapport de marché. Pour en savoir plus, veuillez demander un appel d'analyste ou déposer votre demande.
La méthodologie de recherche clé utilisée par l'équipe de recherche DBMR est la triangulation des données qui implique l'exploration de données, l'analyse de l'impact des variables de données sur le marché et la validation primaire (expert du secteur). Les modèles de données incluent la grille de positionnement des fournisseurs, l'analyse de la chronologie du marché, l'aperçu et le guide du marché, la grille de positionnement des entreprises, l'analyse des brevets, l'analyse des prix, l'analyse des parts de marché des entreprises, les normes de mesure, l'analyse globale par rapport à l'analyse régionale et des parts des fournisseurs. Pour en savoir plus sur la méthodologie de recherche, envoyez une demande pour parler à nos experts du secteur.
Personnalisation disponible
Data Bridge Market Research est un leader de la recherche formative avancée. Nous sommes fiers de fournir à nos clients existants et nouveaux des données et des analyses qui correspondent à leurs objectifs. Le rapport peut être personnalisé pour inclure une analyse des tendances des prix des marques cibles, une compréhension du marché pour d'autres pays (demandez la liste des pays), des données sur les résultats des essais cliniques, une revue de la littérature, une analyse du marché des produits remis à neuf et de la base de produits. L'analyse du marché des concurrents cibles peut être analysée à partir d'une analyse basée sur la technologie jusqu'à des stratégies de portefeuille de marché. Nous pouvons ajouter autant de concurrents que vous le souhaitez, dans le format et le style de données que vous recherchez. Notre équipe d'analystes peut également vous fournir des données sous forme de fichiers Excel bruts, de tableaux croisés dynamiques (Fact book) ou peut vous aider à créer des présentations à partir des ensembles de données disponibles dans le rapport.