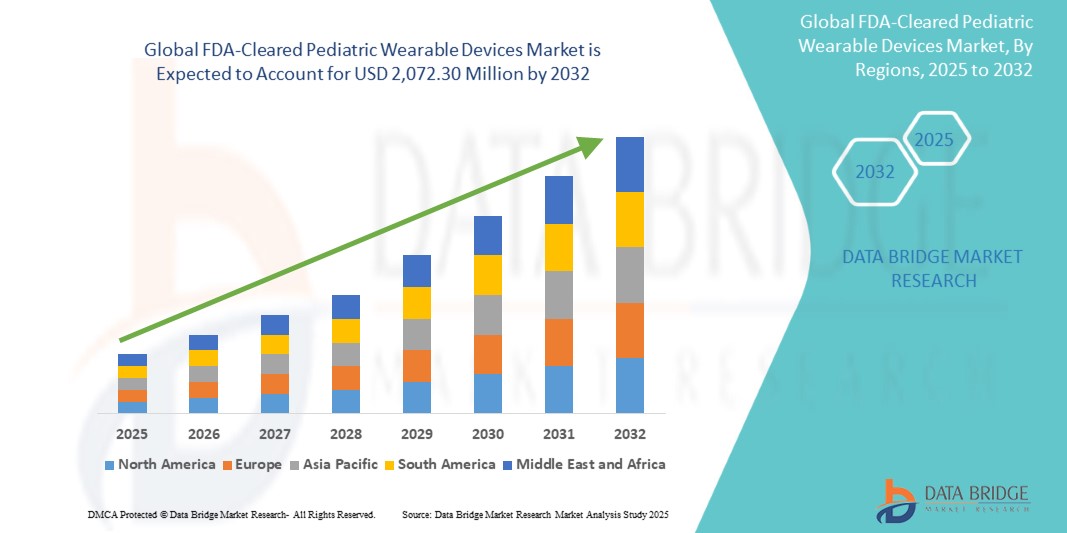
Global Fda Cleared Pediatric Wearable Devices Market
Tamanho do mercado em biliões de dólares
CAGR :
% 
 USD
495.00 Million
USD
2,072.30 Million
2024
2032
USD
495.00 Million
USD
2,072.30 Million
2024
2032
| 2025 –2032 | |
| USD 495.00 Million | |
| USD 2,072.30 Million | |
|
|
|
|
Segmentação do Mercado de Dispositivos Pediátricos Limpos do FDA Global, Por Tipo de Dispositivo (Oxímetros Pulse, Monitores Cardíacos / ECG Wearables, Monitores Respiratórios, Monitores Multi-Vitais, Monitoramento de Glucoses e Rastreadores do Sono), Uso Clínico (Monitoramento Cardíaco, Monitoramento Respiratório, Monitoramento de Glucoses, Monitoramento de Temperatura e SIDS Monitoramento Associado), Tecnologia (Optical (PPG), Elétrico (ECG), Accelerômetros e Bio-Impedância), Aplicação (Hospitales, Homecare / Caregivers e Ambulatory / Outpatient Clinics) - Tendências e Previsão da Indústria para 2032
Dispositivos de uso pediátrico limpos da FDA Tamanho do mercado
- O tamanho global do mercado de dispositivos wearable pediátricos liberados pela FDA foi avaliado emUSD 495,00 milhões em 2024e espera-se alcançarUSD 2.072,30 milhões até 2032, em umaCAGR de 19,60%durante o período de previsão
- O crescimento do mercado é em grande parte impulsionado pelo aumento das aprovações regulatórias de wearables com foco pediátrico, juntamente com avanços nas tecnologias de sensores que permitem o monitoramento preciso de sinais vitais, sono e funções respiratórias em crianças
- Além disso, a crescente demanda de cuidadores e prestadores de cuidados de saúde por soluções de monitoramento seguras, confiáveis e em tempo real está posicionando os wearables pediátricos liberados pela FDA como uma ferramenta essencial na saúde pediátrica. Esses fatores convergentes estão acelerando a adoção em ambientes clínicos e de cuidados domiciliares, aumentando significativamente o crescimento da indústria
Análise de Mercado de Dispositivos Vesíveis Pediátricos Livres do FDA
- Dispositivos vestíveis de pediatria, projetados para fornecer monitoramento em tempo real de sinais vitais, sono, saúde respiratória e outras condições pediátricas, estão se tornando cada vez mais vitais em ambientes clínicos e domiciliares devido à sua capacidade de fornecer dados precisos, contínuos e integração perfeita com plataformas de saúde digitais
- A crescente demanda por wearables pediátricos é alimentada principalmente por crescentes folgas regulatórias da FDA, avanços tecnológicos em sensores e conectividade, e crescente conscientização entre pais e prestadores de cuidados de saúde sobre a importância do monitoramento proativo da saúde pediátrica
- A América do Norte dominou o mercado de dispositivos wearable pediátricos com a maior parcela de receita de cerca de 39% em 2024, caracterizada por marcos regulatórios favoráveis, forte adoção de soluções digitais de saúde e presença de jogadores pioneiros, com os EUA experimentando uma captação substancial em ambientes hospitalares e domiciliares impulsionados por inovações no monitoramento infantil e gerenciamento remoto do paciente.
- Espera-se que a Ásia-Pacífico seja a região de crescimento mais rápido no mercado de dispositivos wearable pediátricos durante o período de previsão devido ao aumento do gasto em saúde, aumento das taxas de natalidade e adoção crescente de tecnologias de monitoramento da saúde infantil
- Os dispositivos de oxímetro de pulso dominaram o mercado de dispositivos wearable pediátricos em 2024, com uma participação estimada de 40% do mercado, impulsionada pelo seu papel crítico no monitoramento da saturação de oxigênio e da frequência cardíaca em neonatos e lactentes, juntamente com a expansão de clearances da FDA que suportam tanto a prescrição quanto over-the-counter use cases
Relatar Escopo e Segmentação de Mercado de Dispositivos Vestíveis Pediátricos Livres da FDA
| Atributos | Dispositivos Vestíveis Pediátricos Livres da FDA |
| Segmentos Cobertos |
|
| Países abrangidos | América do Norte
Europa
Ásia- Pacífico
Médio Oriente e África
América do Sul
|
| Jogadores do mercado chave |
|
| Oportunidades de Mercado |
|
| Informações sobre o Valor Adicionado | Além dos insights sobre cenários de mercado, como valor de mercado, taxa de crescimento, segmentação, cobertura geográfica e principais atores, os relatórios de mercado curados pela Data Bridge Market Research também incluem análise de especialistas em profundidade, análise de preços, análise de compartilhamento de marca, inquérito ao consumidor, análise demografia, análise da cadeia de suprimentos, análise da cadeia de valor, visão geral da matéria-prima/consumíveis, critérios de seleção de fornecedores, Análise de PESTLE, Análise de Porter e marco regulatório. |
Tendências de Mercado de Dispositivos Vesíveis Pediátricos Livres do FDA
Adoção crescente do monitoramento da saúde pediátrica em tempo real
- Uma tendência significativa e acelerada no mercado global de dispositivos wearable pediátricos é a crescente integração das tecnologias limpas pela FDA com plataformas digitais de saúde e aplicativos conectados, aumentando o monitoramento pediátrico em tempo real e o engajamento do cuidador
- Por exemplo, o Owlet Dream Sock recebeu a liberação da FDA De Novo, permitindo aos pais monitorar os níveis de oxigênio infantil e a frequência cardíaca através de um aplicativo móvel conectado, estabelecendo confiança em soluções acessíveis ao consumidor e medicamente validadas
- Os wearables pediátricos liberados pela FDA agora apresentam avançadosensorespara SpO2, ECG contínuo e monitorização respiratória, permitindo detecção proativa de anomalias e enviando alertas inteligentes para cuidadores e clínicos em tempo real
- A integração contínua desses dispositivos com plataformas de telessaúde permite que os profissionais de saúde monitorem remotamente os pacientes pediátricos, possibilitando a supervisão centralizada e reduzindo a necessidade de visitas hospitalares frequentes
- Essa tendência para wearables clinicamente validados, integrados digitalmente, está reformulando fundamentalmente o atendimento pediátrico. Consequentemente, empresas como Masimo estão desenvolvendo dispositivos pediátricos liberados pela FDA, como Stork, projetados para uso doméstico e clínico com capacidades de monitoramento conectadas.
- A demanda por wearables pediátricos que combinam a liberação da FDA, a acurácia clínica e a conveniência do cuidador está crescendo rapidamente em ambientes hospitalares e domiciliares, pois famílias e provedores priorizam cada vez mais a segurança infantil e a gestão proativa da saúde
Dinâmica de Mercado de Dispositivos de Uso Pediátricos Livres do FDA
Controlador
Aumento da demanda por soluções de monitoramento pediátrico seguras e confiáveis
- O aumento da prevalência de riscos à saúde neonatal e infantil, aliado ao aumento da consciência entre cuidadores, é um fator importante para a adoção crescente de wearables pediátricos liberados pela FDA.
- Por exemplo, em junho de 2023, a Owlet, Inc. anunciou a liberação da FDA para seu dispositivo BabySat, permitindo o uso de prescrição para monitorar a saturação de oxigênio em lactentes, marcando um avanço na expansão do monitoramento clínico para o ambiente domiciliar
- Como pais e clínicos buscam dados de saúde contínuos e confiáveis para crianças, os wearables liberados pela FDA fornecem recursos avançados, como monitoramento em tempo real, rastreamento de dados históricos e alertas de cuidador, oferecendo uma alternativa convincente aos métodos tradicionais de monitoramento intermitente.
- Além disso, o crescente ecossistema de saúde digital e a integração com os serviços de telemedicina estão fazendo dos wearables pediátricos parte integrante de modelos de cuidados proativos, oferecendo conexões perfeitas entre cuidadores, crianças e prestadores de cuidados de saúde
- A conveniência do monitoramento domiciliar, a redução da dependência hospitalar e a capacidade de compartilhar dados em tempo real com os clínicos são fatores fundamentais que impulsionam a adoção tanto em ambiente domiciliar quanto hospitalar. A tendência para programas de monitoramento remoto de pacientes e vias regulatórias de apoio contribui ainda mais para o crescimento do mercado
Restrição/Desafio
Questões de Sensibilidade da Pele e Conformidade Regulatória
- Preocupações em torno da potencial irritação cutânea do uso prolongado do dispositivo, especialmente em neonatos e lactentes, representam um desafio significativo para uma maior penetração no mercado de wearables pediátricos
- Por exemplo, revisões clínicas destacam que o uso contínuo de adesivos de monitoramento em crianças pode levar a desconforto cutâneo ou reações alérgicas, gerando hesitação entre pais e cuidadores em relação à adoção diária.
- Enfrentar essas preocupações através do uso de materiais hipoalergênicos, melhoria da ergonomia do dispositivo e testes regulares de segurança é crucial para construir confiança. Empresas como Masimo enfatizam seu design pediátrico e características focadas no conforto em seu marketing para tranquilizar os cuidadores
- Além disso, os elevados padrões regulatórios para dispositivos pediátricos e longos prazos de aprovação da FDA podem retardar a comercialização, criando barreiras para inovadores menores no espaço. Embora as aprovações estejam a acelerar, a conformidade continua a ser complexa e intensiva em recursos
- O custo relativamente maior dos wearables pediátricos liberados pela FDA em comparação aos monitores de consumo básicos também pode dificultar a adoção entre as famílias sensíveis aos preços, particularmente nas regiões em desenvolvimento. Embora se espere que os preços diminuam, o prémio percebido para dispositivos de grau clínico continua a ser um factor limitante
- Superar esses desafios através de um melhor design pediátrico específico, vias regulatórias mais rápidas e desenvolvimento de opções mais acessíveis será vital para o crescimento sustentado do mercado
Dispositivos de Uso Pediátrico Livre do FDA
O mercado é segmentado com base no tipo de dispositivo, uso clínico, tecnologia e aplicação.
- Por Tipo de Dispositivo
Com base no tipo de dispositivo, o mercado de dispositivos wearable pediátricos liberados pela FDA é segmentado em oxímetros de pulso, monitores cardíacos/ECG wearables, monitores respiratórios, monitores multivitais, monitores de glicose wearables e rastreadores de sono. O segmento de oxímetro de pulso dominou o mercado em 2024 com a maior parcela de receita de mercado de 40%, impulsionada pelo seu papel crítico no monitoramento da saúde neonatal e infantil. Os oxímetros de pulso são amplamente utilizados para rastrear saturação de oxigênio e frequência cardíaca, parâmetros vitais para detectar desconforto respiratório e problemas cardíacos congênitos em populações pediátricas. Sua dominância é reforçada ainda mais por vários desembaraços da FDA de dispositivos focados em bebês, como Owlet BabySat e Masimo Stork, que ganharam forte adoção tanto em ambiente clínico quanto domiciliar. O segmento beneficia-se de sua natureza não invasiva, design compacto e confiança do cuidador, tornando-o o tipo de wearable pediátrico mais amplamente adotado. À medida que mais hospitais e usuários de cuidados domiciliares integram o monitoramento de oxigênio em protocolos de cuidados pediátricos, os oxímetros de pulso continuam liderando a categoria tipo de dispositivo.
Prevê-se que o segmento de monitores multivitais testemunhe a taxa de crescimento mais rápida de 2025 a 2032, alimentado por avanços na fusão de sensores wearable e crescente demanda por soluções de monitoramento integradas. Esses dispositivos combinam múltiplos parâmetros – como SpO2, frequência cardíaca, frequência respiratória e temperatura – em um único wearable, fornecendo insights abrangentes sobre a saúde de uma criança. Sua capacidade de reduzir a necessidade de múltiplos dispositivos melhora a conveniência do cuidador e melhora a adoção em ambientes clínicos, particularmente para programas de monitoramento remoto do paciente. O impulso crescente para a saúde conectada e a necessidade de coleta contínua de dados pediátricos em tempo real estão acelerando a adoção. Além disso, espera-se que as aprovações contínuas da FDA de plataformas pediátricas multivitais ampliem o suporte clínico de aceitação e reembolso, tornando este o tipo de dispositivo de maior crescimento.
- Por Uso Clínico
Com base no uso clínico, o mercado de dispositivos vestíveis pediátricos liberados pela FDA é segmentado em monitoramento cardíaco, monitoramento respiratório, monitoramento de glicose, monitoramento de temperatura e monitoramento adjuvante da SIDS. O segmento de monitoramento respiratório dominou o mercado em 2024, impulsionado pela alta prevalência de complicações respiratórias neonatais e pela necessidade de monitoramento contínuo para detectar apneia e outras condições. Os wearables respiratórios pediátricos desempenham papel fundamental tanto no ambiente da UTIN quanto no monitoramento domiciliar, oferecendo alertas em tempo real aos cuidadores e clínicos. Dispositivos que rastreiam padrões respiratórios e níveis de oxigênio são particularmente vitais para prematuros, onde a intervenção precoce pode salvar vidas. Soluções limpas pela FDA, como as projetadas para vigilância respiratória infantil, têm cimentado o papel principal desse segmento. Sua dominância também é sustentada por forte validação clínica e adoção generalizada em unidades hospitalares neonatais em todo o mundo.
O segmento de monitoramento de glicose é projetado para crescer na taxa mais rápida durante o período de previsão, alimentado pela crescente incidência de diabetes pediátrico e aumentando as aprovações FDA de dispositivos de monitoramento contínuo de glicose (CGM) para crianças. As CGMs fornecem leituras de glicose em tempo real, alertas para hipoglicemia ou hiperglicemia e integração com os sistemas de liberação de insulina, tornando-os indispensáveis para o manejo do diabetes infantil. Os pais e clínicos estão cada vez mais adotando as CGMs para reduzir o teste de dedo-pau e melhorar a qualidade de vida das crianças com diabetes tipo 1. A liberação do FDA de dispositivos com indicações pediátricas específicas está aumentando a confiança e adoção. Com forte apoio do pagador e ampliação das diretrizes clínicas endossando o uso da CGM em crianças, esse segmento está definido para crescer no ritmo mais rápido.
- Por Tecnologia
Com base na tecnologia, o mercado de dispositivos wearable pediátricos liberados pela FDA é segmentado em óptica (PPG), elétrica (ECG), acelerômetros e bioimpedância. O segmento óptico (PPG) dominou o mercado em 2024, em grande parte devido ao seu uso na oximetria de pulso e monitoramento da frequência cardíaca para neonatos e lactentes. Dispositivos baseados em PPG são centrais para a maioria dos wearables pediátricos liberados pela FDA, oferecendo medidas não invasivas e contínuas de saturação de oxigênio e frequência cardíaca. A tecnologia é bem estabelecida, confiável e amplamente confiável tanto por cuidadores quanto por clínicos, tornando-se a escolha preferida para o monitoramento pediátrico crítico. Sua dominância é ainda suportada pela sua integração em dispositivos aprovados pela FDA e seu papel como base para muitas soluções de monitoramento domiciliar conectadas. À medida que os sensores PPG se tornam menores e mais precisos, eles continuam a impulsionar a maior parte da adoção pediátrica wearable.
Prevê-se que o segmento de bioimpedância registre o crescimento mais rápido de 2025 a 2032, impulsionado por suas aplicações em monitoramento de hidratação, esforço respiratório e qualidade do sono em populações pediátricas. A tecnologia de bioimpedância oferece insights sobre múltiplas funções fisiológicas que vão além do que os sensores tradicionais PPG e ECG fornecem. O crescente foco de pesquisa na saúde do sono pediátrico e no monitoramento respiratório está criando oportunidades para wearables baseados em bioimpedância. As vias do FDA estão cada vez mais acomodando dispositivos multiparamétricos, abrindo a porta para aprovações regulatórias mais amplas. Como esses dispositivos passam de ferramentas de pesquisa para uso clínico e de consumo mainstream, espera-se que os wearables de bioimpedância vejam uma rápida captação no segmento pediátrico.
- Por Aplicação
Com base na aplicação, o mercado de dispositivos vestíveis pediátricos liberados pela FDA é segmentado em hospitais, serviços domiciliares/cuidadores e ambulatórios/ambulatórios. O segmento hospitalar dominou o mercado em 2024, apoiado pela alta demanda de acompanhamento contínuo em unidades de terapia intensiva neonatal (NICUs) e enfermarias pediátricas. Os hospitais dependem de wearables limpos pela FDA para garantir precisão, conformidade e integração com sistemas de monitoramento mais amplos. A dominância do segmento decorre da necessidade crítica de soluções confiáveis de monitoramento pediátrico em cuidados agudos, onde intervenções oportunas podem impactar significativamente os desfechos em saúde. Os hospitais também servem como adotantes precoces de dispositivos avançados liberados pela FDA, definindo o padrão para validação clínica e confiança. Com fortes estruturas de reembolso e evidências clínicas, os hospitais mantêm a maior participação de receita nessa categoria.
Espera-se que o segmento de cuidados domiciliares/cuidadores cresça ao ritmo mais rápido durante o período de previsão, alimentado pelo aumento das aprovações da FDA para wearables pediátricos over-the-counter (OTC) e pela crescente preferência do cuidador pelo monitoramento domiciliar. Dispositivos como Owlet Dream Sock e Masimo Stork destacam a mudança para capacitar os pais com soluções de monitoramento confiáveis e limpas pela FDA fora do ambiente hospitalar. O crescimento desse segmento é ainda apoiado pelo aumento da conscientização sobre os riscos à saúde pediátrica, maior adoção da telessaúde e a conveniência de monitoramento contínuo no domicílio. Como os sistemas de saúde incentivam o monitoramento remoto do paciente para reduzir a carga hospitalar, o segmento de cuidado domiciliar é projetado para ser a categoria de aplicação de maior crescimento.
Análise Regional do Mercado de Dispositivos Vesíveis Pediátricos Livres do FDA
- A América do Norte dominou o mercado de dispositivos wearable pediátricos liberados pela FDA, com a maior parcela de receita de cerca de 39% em 2024, caracterizada por marcos regulatórios favoráveis, forte adoção de soluções digitais de saúde e presença de atores pioneiros
- Cuidadores e prestadores de cuidados de saúde na região valorizam muito a precisão, segurança e insights em tempo real oferecidos por wearables pediátricos limpos pela FDA, juntamente com sua integração perfeita em plataformas de monitoramento de pacientes remotos e de telessaúde
- Essa adoção generalizada é ainda apoiada pela infraestrutura de saúde avançada, alta conscientização do monitoramento da saúde pediátrica e programas de reembolso favoráveis, estabelecendo wearables pediátricos liberados pela FDA como solução confiável em ambientes clínicos e domiciliares.
US FDA-Limpado Dispositivos de Uso Pediátrico Insight
O mercado de dispositivos vestíveis pediátricos liberados pela FDA nos EUA capturou a maior parcela de receita de 79% em 2024 na América do Norte, alimentada por forte apoio regulatório da FDA e crescente demanda parental por ferramentas de monitoramento seguras e clinicamente validadas. Cada vez mais, os cuidadores priorizam o monitoramento contínuo dos sinais vitais, do sono e das condições crônicas através de dispositivos liberados pela FDA que garantem confiabilidade sobre os wearables de qualidade do consumidor. A tendência para a integração da telessaúde, aliada ao apoio ao seguro para o monitoramento remoto do paciente (RPM), está acelerando a adoção. Além disso, uma forte colaboração entre os fabricantes de dispositivos e os principais hospitais infantis está aumentando ainda mais a pegada do mercado.
EuropaDispositivos de Uso Pediátrico Livre do FDAPor Dentro do Mercado
Projeta-se que o mercado europeu de dispositivos wearable pediátricos livre da FDA se expanda em um CAGR substancial ao longo do período de previsão, impulsionado principalmente pelo aumento da digitalização da saúde, rigorosos padrões de segurança de dispositivos médicos e crescentes investimentos em monitoramento remoto pediátrico. Aumentar a conscientização dos pais sobre os riscos súbitos à saúde infantil e a importância da detecção precoce é alimentar a adoção. A região está testemunhando ampla aceitação de dispositivos liberados pela FDA não só em hospitais, mas também em ambientes de atenção domiciliar, com políticas de reembolso em determinados países apoiando acesso mais amplo. Os wearables pediátricos estão cada vez mais integrados em programas de manejo de doenças crônicas, fortalecendo ainda mais o crescimento do mercado.
U.K.Dispositivos de Uso Pediátrico Livre do FDAPor Dentro do Mercado
Prevê-se que o mercado de dispositivos wearable pediátricos limpos pela FDA do Reino Unido cresça em um notável CAGR durante o período de previsão, impulsionado pela adoção de soluções digitais de saúde dentro do NHS e pela crescente ênfase no monitoramento do bem-estar infantil. As preocupações com as condições respiratórias e cardíacas pediátricas são encorajadoras aos hospitais e pais, tais como a adoção de dispositivos clinicamente aprovados. A rápida adoção do Reino Unido de sistemas de saúde conectados e seu forte alinhamento regulatório com as normas médicas internacionais reforçam o crescimento. Espera-se que a expansão dos serviços de telessaúde e a tendência para o monitoramento domiciliar permaneçam os principais aceleradores de crescimento.
AlemanhaDispositivos de Uso Pediátrico Livre do FDAPor Dentro do Mercado
Espera-se que o mercado de dispositivos wearable pediátricos liberado pela FDA da Alemanha se expanda em um considerável CAGR durante o período de previsão, alimentado por forte demanda por sistemas de monitoramento tecnologicamente avançados e clinicamente confiáveis. A ênfase do país na inovação em saúde e na integração digital em saúde está impulsionando a adoção em hospitais e ambientes de atenção domiciliar. Os pais e fornecedores alemães valorizam a segurança, privacidade e precisão dos wearables pediátricos liberados pela FDA, alinhados com os altos padrões nacionais de tecnologia médica. A expansão dos programas de RPM pediátrico e as colaborações entre hospitais e fabricantes de dispositivos estão promovendo o crescimento.
Ásia- PacíficoDispositivos de Uso Pediátrico Livre do FDAPor Dentro do Mercado
O mercado de dispositivos wearable pediátricos limpo pela Asia-Pacific FDA está preparado para crescer no CAGR mais rápido de 23,5% durante o período de previsão de 2025 a 2032, impulsionado pela digitalização rápida da saúde, pelo aumento da conscientização sobre o monitoramento da saúde pediátrica, e pelo aumento das condições crônicas pediátricas em países como China, Japão e Índia. Iniciativas de saúde inteligentes apoiadas pelo governo e melhorar o acesso à saúde estão alimentando a adoção de dispositivos. O papel da região como centro de fabricação para wearables médicos também está permitindo acessibilidade e acessibilidade, trazendo wearables pediátricos para consumidores urbanos premium e populações emergentes de classe média.
JapãoDispositivos de Uso Pediátrico Livre do FDAPor Dentro do Mercado
O mercado de dispositivos wearable pediátricos liberado pela FDA no Japão está ganhando ímpeto devido à forte cultura do país de inovação médica, sistemas hospitalares avançados e alta adoção de tecnologias conectadas. Pais japoneses estão cada vez mais abraçando dispositivos clinicamente validados para monitorar apneia do sono, desconforto respiratório e saúde cardíaca em crianças. A integração dos wearables pediátricos com as plataformas hospitalar e domiciliar de IoT está acelerando a adoção. Além disso, o envelhecimento da população cuidadora do Japão está impulsionando a necessidade de soluções de monitoramento convenientes e automatizadas, fortalecendo o papel dos wearables pediátricos em ambientes domésticos e clínicos.
ÍndiaDispositivos de Uso Pediátrico Livre do FDAPor Dentro do Mercado
O mercado de dispositivos vestíveis pediátricos limpo pela FDA na Índia representou a maior participação de receita de mercado na Ásia-Pacífico em 2024, atribuída à urbanização rápida, aumento das taxas de natalidade e forte demanda por soluções de monitoramento da saúde infantil entre a classe média em expansão. O impulso do governo para a saúde digital e o crescimento de hospitais pediátricos privados estão impulsionando a adoção de wearables liberados pela FDA. A acessibilidade e a produção localizada de dispositivos de monitoramento incentivam ainda mais a captação, especialmente em centros urbanos. Espera-se que a sensibilização para os riscos súbitos para a saúde infantil, aliada ao aumento da aceitação das tecnologias de saúde baseadas no domicílio, conduza à expansão do mercado a longo prazo.
FDA-Limpado Dispositivos de Uso Pediátrico Market Share
A indústria de dispositivos wearable pediátricos liberados pela FDA é liderada principalmente por empresas bem estabelecidas, incluindo:
- Sibel Health, Inc. (EUA)
- Strados Labs (EUA)
- BioIntelliSense, Inc. (EUA)
- Masimo (EUA)
- Aevice Health Pte Ltd (Singapura)
- Empatica Inc. (EUA)
- CardiacSense Ltd (Israel)
- Owlet (EUA)
- Medtronic (Irlanda)
- Fitbit LLC (EUA)
- Grupo Internacional AMIT FZE. (Suíça)
- SAMSUNG. (Coreia do Sul)
- Abbott (EUA)
- Dexcom, Inc. (EUA)
- Koninklijke Philips N.V. (Países Baixos)
- NIHON KOHDEN CORPORAÇÃO (Japão)
- ResMed Inc. (EUA)
- AliveCor, Inc. (EUA)
- Compensações (França)
Quais são os Desenvolvimentos Recentes no Mercado Global de Dispositivos de Uso Pediátrico Livre da FDA?
- Em junho de 2025, o FDA aprovou a Banda Sonu por SoundHealth como o primeiro tratamento sem uso de drogas para congestão nasal moderada a grave em crianças de 12 anos ou mais, ampliando a indicação pediátrica para o dispositivo
- Em maio de 2025, o aeviceMD inteligente estetoscópio wearable da Aevice Health recebeu autorização do FDA dos EUA para uso em pacientes pediátricos com idade igual ou superior a 3 anos, tornando-se uma ferramenta respiratória doméstica de monitoramento contínuo para crianças
- Em novembro de 2024, Theranica recebeu uma indicação expandida da idade da FDA para seu dispositivo vestível Nerivio REN, permitindo o tratamento agudo da enxaqueca em crianças com 8 anos ou mais. Isso fez com que fosse a primeira terapia de neuromodulação não medicamentosa autorizada pela FDA especificamente indicada para enxaqueca pediátrica
- Em julho de 2024, a Strados Labs concluiu com sucesso um estudo pediátrico de validação de asma de sua tecnologia RESP Biossensor no Ann & Robert H. Lurie Children’s Hospital de Chicago para detectar chiado em crianças, um passo para garantir a liberação do FDA específico para pediátrico para o dispositivo
- Em fevereiro de 2024, Sibel Health anunciou que sua plataforma de monitoramento vestível ANNE One recebeu sua quarta liberação FDA 510 (k), estendendo o ECG ambulatorial contínuo, SpO2, medidas de temperatura e pressão arterial não invasiva para adolescentes com 12 anos ou mais, tanto para o ambiente hospitalar quanto domiciliar.
SKU-
Obtenha acesso online ao relatório sobre a primeira nuvem de inteligência de mercado do mundo
- Painel interativo de análise de dados
- Painel de análise da empresa para oportunidades de elevado potencial de crescimento
- Acesso de analista de pesquisa para personalização e customização. consultas
- Análise da concorrência com painel interativo
- Últimas notícias, atualizações e atualizações Análise de tendências
- Aproveite o poder da análise de benchmark para um rastreio abrangente da concorrência
Metodologia de Investigação
A recolha de dados e a análise do ano base são feitas através de módulos de recolha de dados com amostras grandes. A etapa inclui a obtenção de informações de mercado ou dados relacionados através de diversas fontes e estratégias. Inclui examinar e planear antecipadamente todos os dados adquiridos no passado. Da mesma forma, envolve o exame de inconsistências de informação observadas em diferentes fontes de informação. Os dados de mercado são analisados e estimados utilizando modelos estatísticos e coerentes de mercado. Além disso, a análise da quota de mercado e a análise das principais tendências são os principais fatores de sucesso no relatório de mercado. Para saber mais, solicite uma chamada de analista ou abra a sua consulta.
A principal metodologia de investigação utilizada pela equipa de investigação do DBMR é a triangulação de dados que envolve a mineração de dados, a análise do impacto das variáveis de dados no mercado e a validação primária (especialista do setor). Os modelos de dados incluem grelha de posicionamento de fornecedores, análise da linha de tempo do mercado, visão geral e guia de mercado, grelha de posicionamento da empresa, análise de patentes, análise de preços, análise da quota de mercado da empresa, normas de medição, análise global versus regional e de participação dos fornecedores. Para saber mais sobre a metodologia de investigação, faça uma consulta para falar com os nossos especialistas do setor.
Personalização disponível
A Data Bridge Market Research é líder em investigação formativa avançada. Orgulhamo-nos de servir os nossos clientes novos e existentes com dados e análises que correspondem e atendem aos seus objetivos. O relatório pode ser personalizado para incluir análise de tendências de preços de marcas-alvo, compreensão do mercado para países adicionais (solicite a lista de países), dados de resultados de ensaios clínicos, revisão de literatura, mercado remodelado e análise de base de produtos . A análise de mercado dos concorrentes-alvo pode ser analisada desde análises baseadas em tecnologia até estratégias de carteira de mercado. Podemos adicionar quantos concorrentes necessitar de dados no formato e estilo de dados que procura. A nossa equipa de analistas também pode fornecer dados em tabelas dinâmicas de ficheiros Excel em bruto (livro de factos) ou pode ajudá-lo a criar apresentações a partir dos conjuntos de dados disponíveis no relatório.