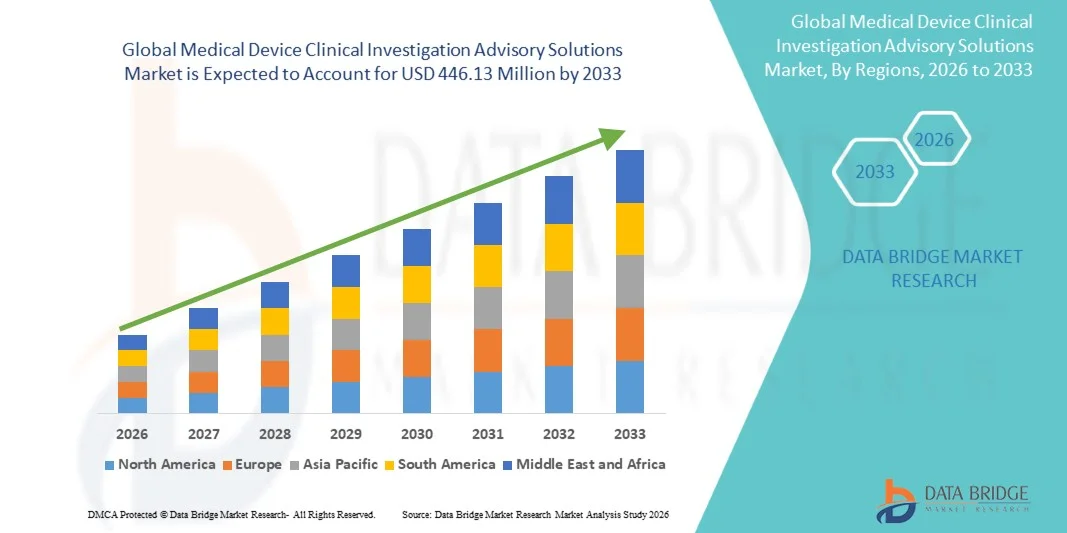
Global Medical Device Clinical Investigation Advisory Solutions Market
Tamanho do mercado em biliões de dólares
CAGR :
% 
 USD
186.21 Million
USD
446.13 Million
2025
2033
USD
186.21 Million
USD
446.13 Million
2025
2033
| 2026 –2033 | |
| USD 186.21 Million | |
| USD 446.13 Million | |
|
|
|
|
Segmentação do mercado global de soluções de consultoria para investigação clínica de dispositivos médicos, por tipo de serviço (consultoria regulatória e gestão de ensaios clínicos) e usuário final (empresas de dispositivos médicos e organizações de pesquisa contratada (CROs)) - Tendências e previsões do setor até 2033.
Tamanho do mercado de soluções de consultoria para investigação clínica de dispositivos médicos
- O mercado global de soluções de consultoria para investigação clínica de dispositivos médicos foi avaliado em US$ 186,21 milhões em 2025 e deverá atingir US$ 446,13 milhões até 2033 , com uma taxa de crescimento anual composta (CAGR) de 11,54% durante o período de previsão.
- O crescimento do mercado é impulsionado principalmente pela crescente complexidade dos marcos regulatórios na indústria de dispositivos médicos, juntamente com a adoção cada vez maior de serviços terceirizados de consultoria em investigação clínica para garantir aprovações de produtos mais rápidas e conformidade em mercados globais.
- Além disso, a crescente demanda por orientações sobre ensaios clínicos com boa relação custo-benefício e conduzidas por especialistas está levando os fabricantes de dispositivos médicos a recorrerem a soluções de consultoria especializadas, impulsionando significativamente o crescimento do setor.
Análise de mercado de soluções de consultoria para investigação clínica de dispositivos médicos
- As soluções de consultoria em investigação clínica de dispositivos médicos, que oferecem orientação especializada e suporte regulatório para ensaios clínicos, são cada vez mais vitais para que os fabricantes de dispositivos médicos acelerem as aprovações de produtos, garantam a conformidade e otimizem as operações clínicas em mercados globais.
- A crescente demanda por essas soluções de consultoria é impulsionada principalmente pela complexidade cada vez maior dos marcos regulatórios, pela necessidade de um tempo de lançamento no mercado mais rápido e pela crescente adoção da terceirização por empresas de dispositivos médicos que buscam suporte especializado e com boa relação custo-benefício para ensaios clínicos.
- A América do Norte dominou o mercado de soluções de consultoria para investigação clínica de dispositivos médicos, com a maior participação de receita, de 39,2% em 2025, caracterizada por uma forte presença de importantes empresas de dispositivos médicos, infraestrutura de pesquisa clínica consolidada e requisitos regulatórios rigorosos.
- Prevê-se que a região Ásia-Pacífico seja a de crescimento mais rápido no mercado durante o período de previsão, devido ao rápido crescimento da indústria de dispositivos médicos, ao aumento das atividades de ensaios clínicos e à maior terceirização de serviços regulatórios e de consultoria.
- O segmento de Consultoria Regulatória dominou a maior fatia de receita do mercado, com 58,4% em 2025, impulsionado pela crescente complexidade das regulamentações de dispositivos médicos em regiões como América do Norte, Europa e Ásia-Pacífico.
Escopo do relatório e segmentação do mercado de soluções de consultoria para investigação clínica de dispositivos médicos
|
Atributos |
Principais insights de mercado sobre soluções de consultoria para investigação clínica de dispositivos médicos |
|
Segmentos abrangidos |
|
|
Países abrangidos |
América do Norte
Europa
Ásia-Pacífico
Oriente Médio e África
Ámérica do Sul
|
|
Principais participantes do mercado |
|
|
Oportunidades de mercado |
|
|
Conjuntos de informações de dados de valor agregado |
Além das informações sobre cenários de mercado, como valor de mercado, taxa de crescimento, segmentação, cobertura geográfica e principais participantes, os relatórios de mercado elaborados pela Data Bridge Market Research também incluem análises aprofundadas de especialistas, epidemiologia de pacientes, análise de projetos em desenvolvimento, análise de preços e estrutura regulatória. |
Tendências do mercado de soluções de consultoria para investigação clínica de dispositivos médicos
“ Aumento da adoção de serviços avançados de consultoria em investigação clínica ”
- Uma tendência notável no mercado global de soluções de consultoria para investigação clínica de dispositivos médicos é a crescente adoção de serviços de consultoria especializados para apoiar ensaios clínicos, submissões regulatórias e vigilância pós-comercialização de dispositivos médicos.
- As empresas estão investindo cada vez mais em soluções que ajudam a otimizar o planejamento de estudos clínicos, o desenvolvimento de protocolos e a conformidade regulatória para reduzir o tempo de lançamento no mercado e mitigar riscos.
- Por exemplo, em 2024, vários fabricantes de dispositivos médicos na América do Norte firmaram parcerias com fornecedores de soluções de consultoria para otimizar suas estratégias de ensaios clínicos e garantir aprovações regulatórias mais rápidas.
- Há também uma crescente demanda por soluções integradas que combinem conhecimento científico, regulatório e operacional para auxiliar os fabricantes na condução eficiente de investigações clínicas de alta qualidade e em conformidade com as normas.
- Essa tendência reflete a crescente complexidade dos marcos regulatórios e a necessidade de orientação especializada ao longo de todo o ciclo de vida do produto, impulsionando a adoção de serviços de consultoria em investigação clínica em todo o mundo.
Dinâmica do mercado de soluções de consultoria para investigação clínica de dispositivos médicos
Motorista
“Crescente necessidade de conformidade regulatória e gestão eficiente de ensaios clínicos”
- O aumento das exigências regulatórias para dispositivos médicos, incluindo padrões rigorosos de segurança e eficácia, é um dos principais fatores que impulsionam a adoção de soluções de consultoria.
- Os fabricantes buscam apoio especializado para lidar com regulamentações complexas, preparar submissões e garantir a conformidade com órgãos como o FDA, a EMA e outras autoridades regionais.
- Por exemplo, no início de 2025, uma empresa europeia de dispositivos médicos contratou serviços de consultoria para facilitar o cumprimento das novas regulamentações do MDR da UE, reduzindo o risco de atrasos na aprovação.
- Além disso, a necessidade de otimizar a eficiência dos ensaios clínicos, reduzir os custos operacionais e encurtar os ciclos de desenvolvimento de produtos está impulsionando a demanda por essas soluções.
- A crescente conscientização sobre segurança do paciente, qualidade das evidências clínicas e gerenciamento de riscos está incentivando ainda mais os fabricantes a recorrerem a serviços de consultoria profissional para fortalecer o planejamento e os resultados dos estudos.
Restrição/Desafio
“ Custos elevados e disponibilidade limitada de conhecimento especializado ”
- O custo relativamente elevado da contratação de serviços de consultoria para investigação clínica de dispositivos médicos pode ser uma barreira para fabricantes de pequeno e médio porte, especialmente em mercados emergentes.
- Soluções de consultoria avançadas geralmente exigem contratos ou honorários de longo prazo, o que pode ser proibitivo para organizações com orçamentos limitados.
- Por exemplo, várias startups na Ásia adiaram a contratação de serviços de consultoria em 2023 devido a restrições orçamentárias, afetando o ritmo de suas investigações clínicas.
- A disponibilidade limitada de consultores qualificados e experientes em certas regiões também restringe a penetração no mercado e pode levar a atrasos nos projetos.
- Abordar esses desafios por meio de modelos de serviço com boa relação custo-benefício, expansão regional de empresas de consultoria e opções de consultoria remota será fundamental para o crescimento sustentável do mercado.
Escopo do mercado de soluções de consultoria para investigação clínica de dispositivos médicos
O mercado está segmentado com base no tipo de serviço e nos usuários finais.
• Por tipo de serviço
Com base no tipo de serviço, o mercado de Soluções de Consultoria para Investigação Clínica de Dispositivos Médicos é segmentado em Consultoria Regulatória e Gestão de Ensaios Clínicos. O segmento de Consultoria Regulatória dominou a maior participação de mercado em receita, com 58,4% em 2025, impulsionado pela crescente complexidade das regulamentações de dispositivos médicos em regiões como América do Norte, Europa e Ásia-Pacífico. As empresas de dispositivos médicos dependem fortemente de serviços de consultoria regulatória para navegar pelos processos de aprovação pré-mercado, conformidade pós-mercado e submissão. A crescente ênfase na segurança do paciente e nos padrões de qualidade do produto alimenta a demanda. Consultores regulatórios fornecem orientação sobre gerenciamento de riscos, rotulagem e documentação, garantindo um acesso mais rápido ao mercado. Requisitos rigorosos de conformidade de órgãos como FDA, EMA e PMDA aumentam a dependência desses serviços. Os avanços tecnológicos em submissões eletrônicas e rastreamento regulatório digital aumentam ainda mais a eficiência. O segmento se beneficia de contratos de longo prazo com os principais fabricantes de dispositivos médicos. O aumento no volume de lançamentos de dispositivos inovadores e instrumentos de diagnóstico de alto valor impulsiona uma demanda consistente. Os serviços de consultoria regulatória reduzem os riscos legais e operacionais para os fabricantes. O crescente foco na harmonização global de normas sustenta a dominância do segmento. A terceirização de conhecimento especializado em regulamentação permite que as empresas otimizem custos e acelerem o lançamento de seus produtos no mercado. Esses fatores, em conjunto, fazem da consultoria regulatória o maior segmento de serviços.
O segmento de Gestão de Ensaios Clínicos deverá apresentar a taxa de crescimento anual composta (CAGR) mais rápida, de 11,3%, entre 2026 e 2033, impulsionado pelo crescente número de ensaios clínicos e estudos pós-comercialização para dispositivos médicos novos e inovadores. A crescente adoção de plataformas digitais de gestão de ensaios clínicos garante um planejamento simplificado, recrutamento de pacientes, monitoramento e geração de relatórios. A terceirização da gestão de ensaios clínicos para provedores especializados reduz a carga operacional das empresas de dispositivos médicos. A crescente complexidade dos ensaios multicêntricos e a necessidade de captura de dados em tempo real sustentam o crescimento. As autoridades regulatórias estão enfatizando a integridade dos dados, a prontidão para auditorias e o monitoramento baseado em risco, o que aumenta a demanda. A expansão dos projetos de P&D de dispositivos médicos em mercados emergentes impulsiona a adoção. As CROs (Organizações de Pesquisa Clínica Contratadas) oferecem cada vez mais soluções de gestão de ensaios clínicos de ponta a ponta para maior eficiência. Análises avançadas e monitoramento baseado em IA na gestão de ensaios clínicos melhoram a precisão e reduzem os prazos. A demanda por soluções com boa relação custo-benefício durante o desenvolvimento de dispositivos também contribui para a adoção. A integração com registros eletrônicos de saúde e dispositivos vestíveis acelera a eficiência dos ensaios clínicos. A crescente tendência de ensaios clínicos centrados no paciente também impulsiona a adoção. Em conjunto, esses fatores fazem da gestão de ensaios clínicos o segmento de serviços que apresenta o crescimento mais rápido.
• Por usuários finais
Com base nos usuários finais, o mercado de Soluções de Consultoria para Investigação Clínica de Dispositivos Médicos é segmentado em Empresas de Dispositivos Médicos e Organizações de Pesquisa Contratada (CROs). O segmento de Empresas de Dispositivos Médicos representou a maior participação na receita de mercado, com 64,7% em 2025, impulsionado pelo crescente número de lançamentos de dispositivos médicos em todo o mundo e pela necessidade de cumprir normas regulatórias rigorosas. As empresas dependem fortemente de serviços de consultoria externa para acelerar a entrada no mercado e manter a conformidade. A crescente complexidade das classificações de produtos, testes de segurança e vigilância pós-comercialização alimenta a demanda. Fabricantes de dispositivos de grande e médio porte terceirizam expertise regulatória e clínica para otimizar custos e garantir agilidade no lançamento de produtos no mercado. A rápida inovação em dispositivos diagnósticos, cirúrgicos e implantáveis aumenta a dependência de soluções de consultoria. As empresas necessitam de suporte contínuo para alterações de rótulos, notificação de eventos adversos e preparação para auditorias. Iniciativas de harmonização global, como a ISO 13485 e o MDR, aumentam a adoção. Parcerias com CROs e empresas de consultoria aprimoram a eficiência operacional. Atrasos regulatórios são minimizados, reduzindo o risco comercial. Contratos de alto valor e parcerias de consultoria de longo prazo fortalecem a dominância do segmento. Empresas da América do Norte e da Europa lideram a adoção, mas os mercados emergentes estão contribuindo cada vez mais. Esses fatores, em conjunto, fazem das empresas de dispositivos médicos o segmento de usuários finais dominante.
O segmento de Organizações de Pesquisa Contratada (CROs) deverá apresentar a taxa de crescimento anual composta (CAGR) mais rápida, de 10,2%, entre 2026 e 2033, impulsionado pela crescente tendência de terceirização de ensaios clínicos e serviços de suporte regulatório. As CROs buscam cada vez mais soluções de consultoria para expandir sua oferta de serviços e melhorar a eficiência operacional. O aumento de ensaios clínicos multicêntricos e globais exige gerenciamento eficiente de ensaios e orientação em conformidade. A crescente colaboração entre fabricantes de dispositivos e CROs impulsiona o crescimento. Avanços tecnológicos, como monitoramento baseado em inteligência artificial e plataformas digitais para ensaios clínicos, aumentam a adoção. As CROs visam reduzir prazos e custos operacionais, garantindo a qualidade dos dados e a conformidade regulatória. A expansão dos serviços para mercados emergentes apoia a adoção. A forte demanda por conhecimento especializado em categorias de dispositivos de alto risco acelera o crescimento. As CROs contam com serviços de consultoria para garantir submissões regulatórias bem-sucedidas e mitigar riscos. Os crescentes investimentos em infraestrutura de saúde e os lançamentos de dispositivos inovadores aumentam ainda mais o potencial de mercado. A adoção de modelos de ensaios clínicos virtuais e híbridos promove a dependência de soluções de consultoria. Esses fatores, em conjunto, fazem das CROs o segmento de usuários finais de crescimento mais rápido.
Análise Regional do Mercado de Soluções de Consultoria para Investigação Clínica de Dispositivos Médicos
- A América do Norte dominou o mercado de soluções de consultoria para investigação clínica de dispositivos médicos, com a maior participação de receita, de 39,2% em 2025.
- Impulsionada por um ecossistema de saúde maduro, uma alta concentração de empresas de dispositivos médicos e fortes estruturas regulatórias que apoiam a pesquisa clínica.
- A região beneficia-se de infraestruturas avançadas para ensaios clínicos, profissionais de pesquisa altamente qualificados e sistemas de conformidade regulatória bem estabelecidos, o que incentiva a terceirização de serviços de consultoria para o desenvolvimento de dispositivos médicos, validação clínica e submissões regulatórias.
Análise de Mercado de Soluções de Consultoria para Investigação Clínica de Dispositivos Médicos nos EUA
O mercado de soluções de consultoria para investigação clínica de dispositivos médicos nos EUA capturou a maior parte da receita da América do Norte em 2025, impulsionado pela alta adoção de serviços terceirizados de consultoria clínica e pela crescente necessidade de conhecimento especializado em regulamentação para aprovações de dispositivos médicos. As empresas utilizam cada vez mais firmas de consultoria especializadas para planejar estudos clínicos, desenvolver estratégias regulatórias e gerenciar submissões de forma eficiente. Isso é particularmente importante para dispositivos inovadores que exigem aprovação pré-comercialização ou conformidade com as regulamentações do FDA. A sólida infraestrutura de pesquisa do país, aliada ao foco em inovação e agilização das aprovações de dispositivos, continua a impulsionar o crescimento do mercado.
Análise do Mercado Europeu de Soluções de Consultoria para Investigação Clínica de Dispositivos Médicos
Prevê-se que o mercado europeu de soluções de consultoria para investigação clínica de dispositivos médicos cresça a uma taxa composta de crescimento anual (CAGR) substancial durante o período de previsão, impulsionado por regulamentações rigorosas, como o Regulamento de Dispositivos Médicos da UE (MDR), pela crescente adoção de dispositivos médicos inovadores e pelo aumento das iniciativas de pesquisa clínica. As empresas estão cada vez mais terceirizando serviços de consultoria clínica para lidar com requisitos de conformidade complexos, gerenciar ensaios multicêntricos e acelerar as submissões regulatórias.
Análise de Mercado de Soluções de Consultoria para Investigação Clínica de Dispositivos Médicos no Reino Unido
Prevê-se que o mercado de soluções de consultoria para investigação clínica de dispositivos médicos no Reino Unido cresça de forma constante, impulsionado por um ecossistema de saúde maduro, uma infraestrutura robusta de pesquisa clínica e iniciativas governamentais que promovem a inovação em dispositivos médicos. O ambiente regulatório do país incentiva a terceirização para empresas de consultoria especializadas em gestão de ensaios clínicos, estratégia regulatória e conformidade com o Regulamento de Dispositivos Médicos do Reino Unido (UK MDR) e com as normas globais. O aumento no uso de dispositivos médicos minimamente invasivos e tecnologicamente avançados também impulsionou a demanda por orientação especializada em validação clínica e estratégias de entrada no mercado.
Análise do mercado de soluções de consultoria para investigação clínica de dispositivos médicos na Alemanha
O mercado alemão de soluções de consultoria para investigação clínica de dispositivos médicos é um dos principais impulsionadores do crescimento do mercado europeu, graças à sua infraestrutura de saúde consolidada, à alta adoção de tecnologias médicas e à forte ênfase em pesquisa e desenvolvimento. Os fabricantes alemães de dispositivos médicos dependem cada vez mais de soluções de consultoria para investigação clínica para cumprir as regulamentações do MDR (Regulamento de Dispositivos Médicos), projetar ensaios clínicos eficazes e obter aprovação mais rápida para dispositivos inovadores. O foco do país em medicina de precisão, tecnologias de saúde digital e diagnósticos de ponta acelera ainda mais a demanda por serviços de consultoria terceirizados.
Análise do Mercado de Soluções de Consultoria para Investigação Clínica de Dispositivos Médicos na Região Ásia-Pacífico
O mercado de soluções de consultoria para investigação clínica de dispositivos médicos na região Ásia-Pacífico deverá ser o de crescimento mais rápido durante o período de previsão, devido à rápida expansão da indústria de dispositivos médicos, ao aumento da terceirização de serviços de consultoria clínica e ao aumento das exigências regulatórias. A crescente infraestrutura de saúde, a expansão da fabricação de dispositivos médicos e o acesso econômico a consultoria especializada são os principais impulsionadores desse crescimento. Países como China, Índia e Japão estão testemunhando uma demanda crescente por serviços de consultoria clínica para garantir a conformidade e a aprovação de mercado de dispositivos inovadores em tempo hábil.
Análise do Mercado de Soluções de Consultoria para Investigação Clínica de Dispositivos Médicos no Japão
O crescimento do mercado japonês de soluções de consultoria para investigação clínica de dispositivos médicos é impulsionado pelo seu setor de saúde avançado, pelo envelhecimento da população e pela forte demanda por dispositivos médicos inovadores. As empresas de consultoria clínica apoiam os fabricantes de dispositivos com submissões regulatórias, planejamento de ensaios clínicos e conformidade com as normas locais, permitindo uma validação clínica eficiente e um acesso mais rápido ao mercado.
Análise do Mercado de Soluções de Consultoria para Investigação Clínica de Dispositivos Médicos na China
O mercado chinês de soluções de consultoria para investigação clínica de dispositivos médicos detinha a maior participação de mercado em receita na região Ásia-Pacífico em 2025, impulsionado por uma indústria nacional de dispositivos médicos em rápida expansão, iniciativas governamentais que promovem a conformidade regulatória e a colaboração com empresas de consultoria globais. Esse ambiente facilitou ciclos de aprovação mais curtos e melhorou o acesso ao mercado para dispositivos médicos, aumentando ainda mais a demanda por soluções de consultoria para investigação clínica.
Participação de mercado em soluções de consultoria para investigação clínica de dispositivos médicos
O setor de Soluções de Consultoria para Investigação Clínica de Dispositivos Médicos é liderado principalmente por empresas consolidadas, incluindo:
- Medpace (EUA)
- ICON plc (Irlanda)
- PPD Inc. (EUA)
- Parexel Internacional (EUA)
- Charles River Laboratories (EUA)
- Covance Inc. (EUA)
- Serviços de Ensaios Clínicos da Medtronic (EUA)
- Syneos Health (EUA)
- Eurofins Scientific (Luxemburgo)
- Desenvolvimento de Produtos Farmacêuticos (PPD) (EUA)
- Wuxi AppTec (China)
- SGS Life Sciences (Suíça)
- Labcorp Desenvolvimento de Medicamentos (EUA)
- Parexel International Corp (EUA)
- CRF Saúde (Reino Unido)
- PRA Health Sciences (EUA)
- Accenture Life Sciences (Irlanda)
- Covance (EUA)
- Clinipac (EUA)
Últimos desenvolvimentos no mercado global de soluções de consultoria para investigação clínica de dispositivos médicos
- Em janeiro de 2025, a Tigermed ampliou sua parceria estratégica com a Medidata para acelerar os ensaios clínicos de dispositivos médicos utilizando a plataforma digital da Medidata, automatizando a captura de dados e otimizando as operações de CROs em estudos clínicos globais, aprimorando a eficiência da gestão de ensaios.
- Em janeiro de 2025, a NAMSA adquiriu as operações de testes de dispositivos médicos da WuXi AppTec nos EUA, expandindo seu portfólio de soluções de pesquisa e testes clínicos para fornecer serviços de consultoria pré-clínica e clínica mais abrangentes para fabricantes de dispositivos que buscam aprovações regulatórias e preparação para o mercado.
- Em janeiro de 2025, a Canyon Labs concluiu a aquisição dos serviços de laboratório e consultoria da iuvo BioScience, fortalecendo seus serviços de suporte a CROs, como testes de biocompatibilidade e análises, que são componentes essenciais das soluções de consultoria ao longo do ciclo de vida de dispositivos médicos.
- Em fevereiro de 2025, a Arterex adquiriu a Phoenix, uma empresa italiana de design e desenvolvimento de dispositivos médicos, possibilitando um suporte aprimorado de ponta a ponta ao desenvolvimento clínico e serviços de consultoria para testes de dispositivos e conformidade regulatória nos mercados europeus.
- Em fevereiro de 2025, a Arterex também adquiriu a Adroit, expandindo suas capacidades globais de pesquisa e fabricação por contrato, facilitando assim o desenvolvimento clínico simplificado e os serviços de consultoria regulatória para empresas de dispositivos médicos.
- Em março de 2025, a InTandem Capital anunciou um investimento estratégico na Clinilabs, indicando o crescente interesse de investidores em CROs especializadas em pesquisa de dispositivos médicos, o que contribui indiretamente para serviços de consultoria em estratégia de investigação e regulamentação.
- Em março de 2025, a ICON plc expandiu seus serviços de terceirização regulatória na região da Ásia-Pacífico, com foco em consultoria regulatória mais rápida e específica para a região, além de suporte a testes clínicos para clientes de dispositivos médicos em mercados como China e Índia.
SKU-
Obtenha acesso online ao relatório sobre a primeira nuvem de inteligência de mercado do mundo
- Painel interativo de análise de dados
- Painel de análise da empresa para oportunidades de elevado potencial de crescimento
- Acesso de analista de pesquisa para personalização e customização. consultas
- Análise da concorrência com painel interativo
- Últimas notícias, atualizações e atualizações Análise de tendências
- Aproveite o poder da análise de benchmark para um rastreio abrangente da concorrência
Metodologia de Investigação
A recolha de dados e a análise do ano base são feitas através de módulos de recolha de dados com amostras grandes. A etapa inclui a obtenção de informações de mercado ou dados relacionados através de diversas fontes e estratégias. Inclui examinar e planear antecipadamente todos os dados adquiridos no passado. Da mesma forma, envolve o exame de inconsistências de informação observadas em diferentes fontes de informação. Os dados de mercado são analisados e estimados utilizando modelos estatísticos e coerentes de mercado. Além disso, a análise da quota de mercado e a análise das principais tendências são os principais fatores de sucesso no relatório de mercado. Para saber mais, solicite uma chamada de analista ou abra a sua consulta.
A principal metodologia de investigação utilizada pela equipa de investigação do DBMR é a triangulação de dados que envolve a mineração de dados, a análise do impacto das variáveis de dados no mercado e a validação primária (especialista do setor). Os modelos de dados incluem grelha de posicionamento de fornecedores, análise da linha de tempo do mercado, visão geral e guia de mercado, grelha de posicionamento da empresa, análise de patentes, análise de preços, análise da quota de mercado da empresa, normas de medição, análise global versus regional e de participação dos fornecedores. Para saber mais sobre a metodologia de investigação, faça uma consulta para falar com os nossos especialistas do setor.
Personalização disponível
A Data Bridge Market Research é líder em investigação formativa avançada. Orgulhamo-nos de servir os nossos clientes novos e existentes com dados e análises que correspondem e atendem aos seus objetivos. O relatório pode ser personalizado para incluir análise de tendências de preços de marcas-alvo, compreensão do mercado para países adicionais (solicite a lista de países), dados de resultados de ensaios clínicos, revisão de literatura, mercado remodelado e análise de base de produtos . A análise de mercado dos concorrentes-alvo pode ser analisada desde análises baseadas em tecnologia até estratégias de carteira de mercado. Podemos adicionar quantos concorrentes necessitar de dados no formato e estilo de dados que procura. A nossa equipa de analistas também pode fornecer dados em tabelas dinâmicas de ficheiros Excel em bruto (livro de factos) ou pode ajudá-lo a criar apresentações a partir dos conjuntos de dados disponíveis no relatório.