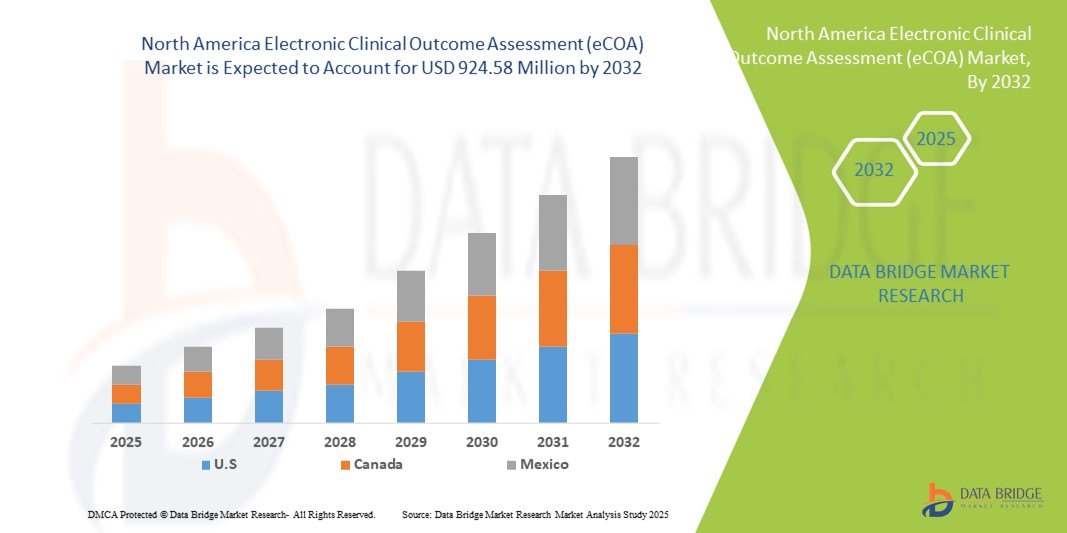
North America Electronic Clinical Outcome Assessment Ecoa Market
Tamanho do mercado em biliões de dólares
CAGR :
% 
 USD
265.11 Million
USD
924.58 Million
2024
2032
USD
265.11 Million
USD
924.58 Million
2024
2032
| 2025 –2032 | |
| USD 265.11 Million | |
| USD 924.58 Million | |
|
|
|
|
Segmentação do mercado de Avaliação Eletrônica de Resultados Clínicos (eCOA) na América do Norte, por produto (soluções locais, soluções baseadas em nuvem e soluções baseadas na Web), abordagem (avaliação de resultados relatados pelo médico (CLINRO), avaliação de resultados relatados pelo paciente (PRO), avaliação de resultados relatados pelo observador (OBSRO) e avaliação de resultados de desempenho (PERFO)), usuário final (provedores de serviços comerciais, hospitais e centros de transplante, laboratórios de pesquisa e instituições acadêmicas), plataforma (organizações de pesquisa contratadas, empresas farmacêuticas e biofarmacêuticas , fabricantes de dispositivos médicos, hospitais e laboratórios clínicos, empresas de serviços de consultoria, pesquisa e academia e outros) - tendências e previsões do setor até 2032
Tamanho do mercado de avaliação eletrônica de resultados clínicos (eCOA) na América do Norte
- O tamanho do mercado de avaliação eletrônica de resultados clínicos (eCOA) da América do Norte foi avaliado em US$ 265,11 milhões em 2024 e deve atingir US$ 924,58 milhões até 2032 , com um CAGR de 16,90% durante o período previsto.
- O crescimento do mercado é amplamente impulsionado pela crescente digitalização de ensaios clínicos e pela crescente adoção de soluções de saúde baseadas em tecnologia, levando a uma maior eficiência, precisão e abordagens centradas no paciente em estudos clínicos.
- Além disso, a crescente necessidade de captura de dados de pacientes em tempo real, monitoramento remoto e conformidade regulatória está impulsionando a adoção de soluções de Avaliação Eletrônica de Resultados Clínicos (eCOA), impulsionando significativamente o crescimento do setor. Esses fatores convergentes estão permitindo que empresas farmacêuticas e de biotecnologia, bem como organizações de pesquisa contratadas, otimizem as operações de ensaios clínicos e melhorem os resultados clínicos gerais.
Análise de mercado de avaliação eletrônica de resultados clínicos (eCOA) na América do Norte
- As soluções de Avaliação Eletrônica de Resultados Clínicos (eCOA) estão se tornando cada vez mais componentes essenciais em ensaios clínicos, oferecendo coleta de dados em tempo real, precisa e centrada no paciente para melhorar a qualidade do estudo, a conformidade regulatória e a eficiência operacional.
- A crescente adoção do eCOA é impulsionada principalmente pela crescente demanda por ensaios clínicos descentralizados e remotos, pelo foco crescente na pesquisa centrada no paciente e pela necessidade de captura eficiente de dados em vários locais.
- Os EUA dominaram o mercado de avaliação eletrônica de resultados clínicos (eCOA), com a maior participação na receita, de 79,01% em 2024, impulsionados pela presença de grandes empresas farmacêuticas e de biotecnologia, infraestrutura avançada de pesquisa clínica e forte investimento em soluções de saúde digital. Os EUA, em particular, experimentaram um crescimento substancial nas implementações de eCOA, apoiado por pipelines de ensaios clínicos em larga escala, iniciativas governamentais que incentivam a adoção digital e um ecossistema tecnológico robusto que facilita a integração com sistemas eletrônicos de captura de dados e gerenciamento de ensaios.
- Espera-se que o Canadá seja o país com crescimento mais rápido no mercado norte-americano de avaliação eletrônica de resultados clínicos (eCOA) durante o período previsto, devido ao crescente apoio governamental a soluções clínicas digitais, à crescente terceirização de ensaios clínicos e à crescente adoção de plataformas eCOA móveis e baseadas em nuvem. A expansão das redes de pesquisa e a crescente conscientização entre os profissionais de saúde sobre tecnologias centradas no paciente aceleram ainda mais o crescimento do mercado no país.
- O segmento de avaliação de resultados relatados pelo paciente (PRO) dominou o mercado de avaliação eletrônica de resultados clínicos (eCOA) com a maior participação de receita de mercado de 52,1% em 2024, à medida que os ensaios centrados no paciente se tornam cada vez mais importantes
Escopo do relatório e segmentação do mercado de avaliação eletrônica de resultados clínicos (eCOA)
|
Atributos |
Principais insights de mercado da Avaliação Eletrônica de Resultados Clínicos (eCOA) |
|
Segmentos abrangidos |
|
|
Países abrangidos |
América do Norte
|
|
Principais participantes do mercado |
|
|
Oportunidades de mercado |
|
|
Conjuntos de informações de dados de valor agregado |
Além dos insights sobre cenários de mercado, como valor de mercado, taxa de crescimento, segmentação, cobertura geográfica e principais participantes, os relatórios de mercado selecionados pela Data Bridge Market Research também incluem análises aprofundadas de especialistas, análises de preços, análises de participação de marca, pesquisas com consumidores, análises demográficas, análises da cadeia de suprimentos, análises da cadeia de valor, visão geral de matérias-primas/consumíveis, critérios de seleção de fornecedores, análise PESTLE, análise de Porter e estrutura regulatória. |
Tendências do mercado de Avaliação Eletrônica de Resultados Clínicos (eCOA) na América do Norte
Aumento da adoção de resultados digitais relatados por pacientes e monitoramento remoto
- Uma tendência significativa e crescente no mercado de Avaliação Eletrônica de Resultados Clínicos (eCOA) dos Estados Unidos é a crescente adoção de plataformas digitais de resultados relatados pelo paciente (ePRO) e soluções de captura remota de dados. Essas tecnologias estão aprimorando a precisão dos dados, o monitoramento em tempo real e o engajamento do paciente em ensaios clínicos.
- Por exemplo, a implementação de soluções eCOA em ensaios oncológicos de Fase III em vários locais permitiu a coleta contínua de dados de sintomas do paciente, reduzindo erros de entrada manual e melhorando a conformidade com avaliações definidas pelo protocolo.
- As plataformas de monitoramento remoto permitem que a equipe clínica acompanhe os resultados relatados pelos pacientes em tempo real, permitindo uma intervenção mais rápida, supervisão aprimorada dos testes e dados mais confiáveis para submissões regulatórias.
- A integração de sistemas eCOA baseados em nuvem com plataformas de gerenciamento de ensaios clínicos garante que os dados coletados possam ser acessados, agregados e analisados de forma eficiente em vários locais de ensaio, dando suporte ao gerenciamento centralizado de estudos.
- Há uma ênfase crescente em projetos de ensaios centrados no paciente, onde as soluções eCOA aumentam a conveniência e a adesão, levando a uma maior completude e qualidade dos dados
- As agências reguladoras e os patrocinadores estão cada vez mais reconhecendo o valor das avaliações eletrônicas de resultados para melhorar a eficiência dos testes e acelerar a tomada de decisões, incentivando a adoção dessas soluções.
Dinâmica do mercado de avaliação eletrônica de resultados clínicos (eCOA) na América do Norte
Motorista
Necessidade crescente devido à crescente demanda por captura digital de dados clínicos e ensaios centrados no paciente
- A ênfase crescente na coleta precisa de dados clínicos em tempo real, juntamente com a crescente mudança em direção a modelos de ensaios centrados no paciente, é um fator significativo para o aumento da demanda por soluções eCOA
- Por exemplo, em abril de 2024, a Medidata Solutions anunciou o lançamento de uma plataforma aprimorada de relatórios eletrônicos de resultados de pacientes, projetada para se integrar perfeitamente aos sistemas globais de gestão de ensaios clínicos. Espera-se que tais avanços por empresas importantes impulsionem o crescimento do setor de eCOA no período previsto.
- À medida que patrocinadores e organizações de pesquisa clínica buscam melhorar a eficiência e a conformidade dos testes, as plataformas eCOA oferecem recursos como captura remota de dados, notificações automatizadas e monitoramento em tempo real dos resultados relatados pelos pacientes, fornecendo uma alternativa atraente aos métodos tradicionais baseados em papel.
- Além disso, a crescente adoção de ensaios clínicos descentralizados e virtuais está tornando os sistemas eCOA um componente integral dos projetos de estudo modernos, permitindo que os participantes relatem os resultados de casa ou de instalações de saúde locais.
- A conveniência do monitoramento remoto, a integração com plataformas de análise de ensaios clínicos e a melhoria da conformidade regulatória são fatores-chave que impulsionam a adoção de soluções de eCOA em organizações farmacêuticas, de biotecnologia e de pesquisa contratada. A tendência de transformação digital em ensaios clínicos contribui ainda mais para o crescimento do mercado.
Restrição/Desafio
Preocupações com a segurança de dados, conformidade regulatória e altos custos iniciais de implementação
- Preocupações em torno da privacidade de dados, segurança cibernética e conformidade com regulamentações como HIPAA e GDPR representam um desafio significativo para uma penetração mais ampla no mercado. Os sistemas eCOA lidam com informações confidenciais de pacientes, e violações ou não conformidade podem levar a consequências financeiras e jurídicas substanciais.
- Por exemplo, auditorias regulatórias rigorosas e o escrutínio crescente sobre dados clínicos digitais tornaram alguns patrocinadores cautelosos quanto à adoção de novas plataformas eCOA sem protocolos de segurança validados.
- Abordar essas preocupações por meio de criptografia robusta, métodos de autenticação seguros e adesão aos padrões regulatórios globais é crucial para construir confiança entre patrocinadores, CROs e centros clínicos. Empresas como a ERT e a CRF Health enfatizam suas plataformas seguras e certificações de conformidade para tranquilizar as partes interessadas.
- Além disso, o custo inicial relativamente alto das implementações abrangentes de eCOA pode ser uma barreira para empresas biofarmacêuticas menores ou para ensaios clínicos em estágio inicial.
- Embora os modelos de assinatura e as plataformas baseadas em nuvem estejam reduzindo gradualmente os custos iniciais, o prêmio percebido para soluções eCOA totalmente integradas ainda pode dificultar a adoção, especialmente em mercados emergentes ou para organizações com orçamento limitado.
- Superar esses desafios por meio de medidas aprimoradas de segurança de dados, programas de treinamento para equipes clínicas e desenvolvimento de opções de eCOA escaláveis e econômicas será vital para o crescimento sustentado do mercado.
Escopo de mercado de avaliação eletrônica de resultados clínicos (eCOA) na América do Norte
O mercado é segmentado com base no produto, abordagem, usuário final e plataforma.
- Por produto
Com base no produto, o mercado de avaliação eletrônica de resultados clínicos (eCOA) é segmentado em soluções locais, soluções baseadas em nuvem e soluções baseadas na web. O segmento de soluções baseadas em nuvem dominou o mercado com a maior participação na receita de 47,5% em 2024, impulsionado por sua escalabilidade e flexibilidade no gerenciamento de ensaios clínicos complexos. As soluções em nuvem fornecem acesso em tempo real aos dados em vários locais de teste, permitindo uma tomada de decisão mais rápida e maior eficiência operacional. A capacidade de integrar dispositivos móveis e garantir o armazenamento seguro de dados aumentou a adoção entre empresas farmacêuticas e CROs. As plataformas em nuvem reduzem os custos de infraestrutura de TI e oferecem suporte a modelos de teste descentralizados e híbridos. Suas interfaces amigáveis e ferramentas de relatórios automatizados aumentam ainda mais a precisão dos dados. O monitoramento remoto e o controle centralizado os tornam ideais para estudos em larga escala e em vários locais. O segmento se beneficia da inovação contínua e do suporte dos fornecedores, mantendo seu domínio no mercado.
Espera-se que o segmento de soluções on-premise testemunhe o CAGR mais rápido, de 18,2%, de 2025 a 2032, à medida que as organizações priorizam o controle e a segurança de dados internos. As plataformas on-premise oferecem conformidade robusta com os requisitos regulatórios, permitindo controle total sobre dados confidenciais de pacientes e ensaios clínicos. Elas podem ser personalizadas para atender às necessidades especializadas de fluxo de trabalho e integradas à infraestrutura de TI existente de hospitais ou instituições. As soluções on-premise são particularmente favorecidas para ensaios clínicos que exigem medidas de alta segurança, como estudos de oncologia ou doenças raras. O crescente investimento em recursos de TI de hospitais e centros de pesquisa está impulsionando a adoção. Esses sistemas oferecem privacidade de dados aprimorada e continuidade operacional durante interrupções na internet. Atualizações contínuas de software e suporte técnico aumentam ainda mais a confiabilidade. A crescente mudança para ensaios clínicos digitais apoia a crescente adoção de plataformas on-premise.
- Por Abordagem
Com base na abordagem, o mercado de avaliação eletrônica de resultados clínicos (eCOA) é segmentado em Avaliação de Resultados Relatada pelo Clínico (CLINRO), Avaliação de Resultados Relatada pelo Paciente (PRO), Avaliação de Resultados Relatada pelo Observador (OBSRO) e Avaliação de Resultados de Desempenho (PERFO). O segmento de Avaliação de Resultados Relatada pelo Paciente (PRO) deteve a maior participação de mercado na receita, de 52,1% em 2024, à medida que os ensaios clínicos centrados no paciente se tornam cada vez mais importantes. As soluções PRO permitem que os participantes relatem sintomas, métricas de qualidade de vida e respostas ao tratamento diretamente, melhorando a precisão e o engajamento dos dados. As autoridades regulatórias reconhecem os dados PRO como essenciais para a aprovação de medicamentos e a vigilância pós-comercialização. A integração com aplicativos móveis permite lembretes, diários eletrônicos e relatórios automatizados. As avaliações PRO aprimoram o monitoramento em tempo real e a detecção precoce de eventos adversos. Elas reduzem a dependência da coleta manual de dados e melhoram a eficiência dos ensaios clínicos. Os patrocinadores se beneficiam de insights acionáveis para desenhos de ensaios clínicos adaptativos. A flexibilidade e a padronização global do segmento contribuem para seu domínio contínuo.
Espera-se que o segmento de avaliação de resultados relatados por clínicos (CLINRO) testemunhe o CAGR mais rápido de 16,4% entre 2025 e 2032, impulsionado pela crescente adoção em estudos hospitalares e pesquisas clínicas complexas. As ferramentas CLINRO permitem que os clínicos forneçam avaliações estruturadas dos resultados dos pacientes, garantindo dados de alta qualidade para ensaios envolvendo intervenções complexas. Essas avaliações são cruciais para submissões regulatórias e validação da eficácia terapêutica. A integração com registros eletrônicos de saúde e sistemas de gerenciamento de ensaios clínicos melhora a eficiência do fluxo de trabalho. As plataformas digitais CLINRO reduzem erros, agilizam a documentação e permitem a entrada remota de dados. A crescente adoção em estudos de oncologia, cardiologia e neurologia está contribuindo para o crescimento. Recursos aprimorados de relatórios e análises fornecem insights mais profundos sobre a eficácia do tratamento. O segmento se beneficia da expansão de programas de treinamento e suporte regulatório, acelerando a adoção.
- Por usuário final
Com base no usuário final, o mercado de avaliação eletrônica de resultados clínicos (eCOA) é segmentado em prestadores de serviços comerciais, hospitais e centros de transplante, laboratórios de pesquisa e instituições acadêmicas. O segmento de hospitais e centros de transplante dominou o mercado com a maior participação na receita de 49,3% em 2024, devido ao alto volume de ensaios clínicos realizados nessas instalações. Os hospitais se beneficiam de infraestrutura de TI integrada, equipe treinada e recursos de ensaios clínicos em vários locais. As soluções de eCOA aumentam o engajamento do paciente, reduzem a entrada manual de dados e garantem a conformidade com os padrões regulatórios. O monitoramento remoto e os relatórios automatizados melhoram a eficiência operacional. Os hospitais podem aproveitar insights em tempo real para otimizar os protocolos de estudo. A crescente adoção de ensaios clínicos híbridos e descentralizados apoia ainda mais a demanda. A integração com prontuários médicos eletrônicos garante um fluxo de trabalho contínuo. A análise avançada nos sistemas hospitalares auxilia na tomada de decisões mais rápidas e na otimização de recursos.
Espera-se que o segmento de laboratórios de pesquisa e instituições acadêmicas testemunhe o CAGR mais rápido de 17,1% de 2025 a 2032, à medida que essas entidades adotam cada vez mais soluções digitais para melhorar a eficiência dos estudos. Instituições acadêmicas conduzem diversos ensaios clínicos e pesquisas colaborativas que exigem coleta de dados precisa e oportuna. Plataformas eCOA em nuvem e no local permitem coordenação perfeita entre vários locais de pesquisa. O financiamento de fontes governamentais e privadas está impulsionando os investimentos em tecnologia. A adoção do eCOA permite inscrições mais rápidas, melhor engajamento dos participantes e gerenciamento eficiente de dados. Relatórios e análises avançados aprimoram os insights da pesquisa. As instituições se beneficiam de soluções escaláveis que suportam vários designs de ensaios. Parcerias crescentes entre a academia e a indústria contribuem para a rápida adoção. A alfabetização digital entre pesquisadores facilita a adoção e a integração em fluxos de trabalho de estudo.
- Por plataforma
Com base na plataforma, o mercado de avaliação eletrônica de resultados clínicos (eCOA) é segmentado em Organizações de Pesquisa Contratadas, Empresas Farmacêuticas e Biofarmacêuticas, Fabricantes de Dispositivos Médicos, Hospitais e Laboratórios Clínicos, Empresas de Serviços de Consultoria e Pesquisa e Academia. O segmento de Empresas Farmacêuticas e Biofarmacêuticas deteve a maior participação de mercado na receita, de 50,2% em 2024, impulsionado por seu papel fundamental em ensaios clínicos globais. Essas empresas exigem rastreamento preciso dos resultados dos pacientes para submissões regulatórias e aprovações de medicamentos. As plataformas eCOA fornecem monitoramento em tempo real, armazenamento seguro de dados e integração com sistemas de gerenciamento de ensaios. A adoção é apoiada por grandes orçamentos de P&D e operações globais de ensaios. Soluções em nuvem e híbridas permitem coordenação multi-local e projetos de ensaios adaptativos. Relatórios automatizados aumentam a eficiência e minimizam erros humanos. A conformidade regulatória e a prontidão para auditoria são garantidas por sistemas digitais seguros. O foco crescente no desenvolvimento de medicamentos centrado no paciente sustenta a dominância neste segmento.
Espera-se que o segmento de Organizações de Pesquisa Contratadas (CROs) testemunhe o CAGR mais rápido, de 18,5%, de 2025 a 2032, impulsionado pela terceirização da gestão de ensaios clínicos por patrocinadores farmacêuticos. As CROs utilizam plataformas eCOA para gerenciar estudos complexos em múltiplos locais com eficiência. Soluções baseadas em nuvem e habilitadas para dispositivos móveis facilitam a captura e o monitoramento de dados em tempo real. A adoção é acelerada por modelos de ensaios descentralizados e híbridos. A integração com eCOA melhora o engajamento do paciente, reduz gargalos operacionais e garante a conformidade regulatória. As CROs investem cada vez mais em ferramentas avançadas de análise e relatórios para apoiar a tomada de decisões dos clientes. Treinamentos e fluxos de trabalho padronizados aumentam ainda mais a eficiência. A expansão das redes globais de ensaios impulsiona a adoção na América do Norte. Atualizações contínuas de plataforma e inovações em serviços sustentam o rápido crescimento.
Análise regional do mercado de avaliação eletrônica de resultados clínicos (eCOA) na América do Norte
- A América do Norte dominou o mercado de avaliação eletrônica de resultados clínicos (eCOA), com a maior participação na receita em 2024, impulsionada pela presença de grandes empresas farmacêuticas e de biotecnologia, infraestrutura avançada de pesquisa clínica e forte investimento em soluções de saúde digital. A região testemunhou a rápida adoção de plataformas clínicas digitais, particularmente em ensaios clínicos de larga escala e em múltiplos locais, atendendo à demanda por captura de dados em tempo real e gerenciamento simplificado de ensaios clínicos.
- A ampla adoção do eCOA na América do Norte é ainda mais reforçada por um ecossistema tecnológico robusto que permite a integração perfeita com sistemas eletrônicos de captura de dados, plataformas de gerenciamento de ensaios clínicos e soluções analíticas. Patrocinadores e CROs se beneficiam de maior eficiência operacional, conformidade regulatória e maior engajamento do paciente por meio dessas plataformas digitais integradas.
- Alto financiamento para pesquisa, iniciativas governamentais que promovem a adoção da saúde digital e a presença de importantes fornecedores de tecnologia na região reforçam ainda mais a posição de liderança da América do Norte no mercado global de eCOA
Visão do mercado de avaliação eletrônica de resultados clínicos (eCOA) dos EUA
O mercado de avaliação eletrônica de resultados clínicos (eCOA) dos EUA dominou o mercado norte-americano, com a maior participação na receita de 79,01% em 2024, impulsionado pela rápida adoção de plataformas clínicas digitais, pipelines de ensaios clínicos em larga escala e iniciativas governamentais de apoio à integração tecnológica na área da saúde. A ampla presença de empresas farmacêuticas e de biotecnologia impulsiona uma demanda substancial por soluções de eCOA para gerenciar ensaios clínicos complexos e multicêntricos com eficiência. O mercado norte-americano se beneficia de uma infraestrutura avançada de pesquisa clínica, garantindo a captura precisa e em conformidade dos dados dos pacientes. O aumento do investimento em soluções de saúde digital, a integração do eCOA com sistemas de captura eletrônica de dados (EDC) e a necessidade de monitoramento em tempo real dos resultados relatados pelos pacientes impulsionam ainda mais o crescimento do mercado. Provedores de saúde e patrocinadores de ensaios clínicos nos EUA estão priorizando cada vez mais tecnologias centradas no paciente, que facilitam o melhor engajamento, a adesão e a precisão dos relatórios dos ensaios clínicos, reforçando a posição dominante do país no mercado.
Visão do mercado de Avaliação Eletrônica de Resultados Clínicos (eCOA) do Canadá
Espera-se que o mercado canadense de avaliação eletrônica de resultados clínicos (eCOA) seja o de crescimento mais rápido no mercado norte-americano durante o período previsto, impulsionado pelo crescente apoio governamental a soluções clínicas digitais e pela crescente terceirização de ensaios clínicos para prestadores de serviços especializados. A crescente adoção de plataformas eCOA móveis e baseadas em nuvem permite a coleta eficiente de dados de pacientes, melhor conformidade regulatória e maior flexibilidade para patrocinadores de ensaios clínicos em todo o país. A expansão das redes de pesquisa, a crescente conscientização entre os profissionais de saúde sobre tecnologias de ensaios clínicos centradas no paciente e a necessidade de captura de dados mais simplificada em ensaios clínicos multicêntricos aceleram o crescimento do mercado de eCOA no Canadá. O aumento do investimento em infraestrutura digital e políticas de apoio reforçam ainda mais a trajetória do Canadá como o mercado de soluções de eCOA de crescimento mais rápido na América do Norte.
Participação no mercado de Avaliação Eletrônica de Resultados Clínicos (eCOA) na América do Norte
O setor de avaliação eletrônica de resultados clínicos (eCOA) é liderado principalmente por empresas bem estabelecidas, incluindo:
- IQVIA (EUA)
- Clario (EUA)
- Medidata (EUA)
- Veeva Systems (EUA)
- Tecnologia de Recursos Terrestres (EUA)
- Oracle Health Sciences (EUA)
- YPrime, LLC (EUA)
- ArisGlobal LLC (EUA)
- Castor EDC (Holanda)
- eClinicalWorks (EUA)
- Medrio, Inc. (EUA)
- ClinOne (EUA)
- Signant Health (EUA)
- Clinical Ink, Inc. (EUA)
- Curebase, Inc. (EUA)
- Kayentis (França)
- Calyx (Reino Unido)
- Datacubed Health (EUA)
- HealthDiary, Inc. (EUA)
Últimos desenvolvimentos no mercado de avaliação eletrônica de resultados clínicos (eCOA) na América do Norte
- Em dezembro de 2023, a ObvioHealth USA, Inc., empresa global de ensaios clínicos digitais, lançou uma solução de avaliação eletrônica de resultados clínicos (eCOA). Essa plataforma integra perfeitamente tecnologia avançada de design de estudos com serviços científicos e clínicos para fornecer resultados mais robustos para patrocinadores de ensaios clínicos.
- Em maio de 2025, a Medidata, uma empresa de destaque no segmento de eCOA, foi reconhecida como líder na Avaliação PEAK Matrix do Everest Group para eCOA. A avaliação destacou o suporte da Medidata a mais de 1 milhão de pacientes e sua capacidade de reduzir os prazos de desenvolvimento de estudos em até 50% em comparação com o padrão do setor.
- Em março de 2025, o Critical Path Institute (C-Path) anunciou a conclusão bem-sucedida da iniciativa eCOA: Getting Better Together. Essa colaboração, impulsionada por um compromisso compartilhado com o avanço do desenvolvimento de medicamentos com foco no paciente, resultou em mudanças significativas e duradouras que beneficiaram todas as partes interessadas do ecossistema eCOA.
- Em junho de 2025, a Medable Inc., fornecedora global de tecnologia para desenvolvimento clínico, lançou seu novo Programa de Parceiros. Esta iniciativa visa capacitar organizações de pesquisa contratadas (CROs) e outros parceiros com recursos de construção de eCOA generativos, baseados em IA e autoatendimento, para ensaios clínicos digitalmente habilitados.
SKU-
Obtenha acesso online ao relatório sobre a primeira nuvem de inteligência de mercado do mundo
- Painel interativo de análise de dados
- Painel de análise da empresa para oportunidades de elevado potencial de crescimento
- Acesso de analista de pesquisa para personalização e customização. consultas
- Análise da concorrência com painel interativo
- Últimas notícias, atualizações e atualizações Análise de tendências
- Aproveite o poder da análise de benchmark para um rastreio abrangente da concorrência
Metodologia de Investigação
A recolha de dados e a análise do ano base são feitas através de módulos de recolha de dados com amostras grandes. A etapa inclui a obtenção de informações de mercado ou dados relacionados através de diversas fontes e estratégias. Inclui examinar e planear antecipadamente todos os dados adquiridos no passado. Da mesma forma, envolve o exame de inconsistências de informação observadas em diferentes fontes de informação. Os dados de mercado são analisados e estimados utilizando modelos estatísticos e coerentes de mercado. Além disso, a análise da quota de mercado e a análise das principais tendências são os principais fatores de sucesso no relatório de mercado. Para saber mais, solicite uma chamada de analista ou abra a sua consulta.
A principal metodologia de investigação utilizada pela equipa de investigação do DBMR é a triangulação de dados que envolve a mineração de dados, a análise do impacto das variáveis de dados no mercado e a validação primária (especialista do setor). Os modelos de dados incluem grelha de posicionamento de fornecedores, análise da linha de tempo do mercado, visão geral e guia de mercado, grelha de posicionamento da empresa, análise de patentes, análise de preços, análise da quota de mercado da empresa, normas de medição, análise global versus regional e de participação dos fornecedores. Para saber mais sobre a metodologia de investigação, faça uma consulta para falar com os nossos especialistas do setor.
Personalização disponível
A Data Bridge Market Research é líder em investigação formativa avançada. Orgulhamo-nos de servir os nossos clientes novos e existentes com dados e análises que correspondem e atendem aos seus objetivos. O relatório pode ser personalizado para incluir análise de tendências de preços de marcas-alvo, compreensão do mercado para países adicionais (solicite a lista de países), dados de resultados de ensaios clínicos, revisão de literatura, mercado remodelado e análise de base de produtos . A análise de mercado dos concorrentes-alvo pode ser analisada desde análises baseadas em tecnologia até estratégias de carteira de mercado. Podemos adicionar quantos concorrentes necessitar de dados no formato e estilo de dados que procura. A nossa equipa de analistas também pode fornecer dados em tabelas dinâmicas de ficheiros Excel em bruto (livro de factos) ou pode ajudá-lo a criar apresentações a partir dos conjuntos de dados disponíveis no relatório.