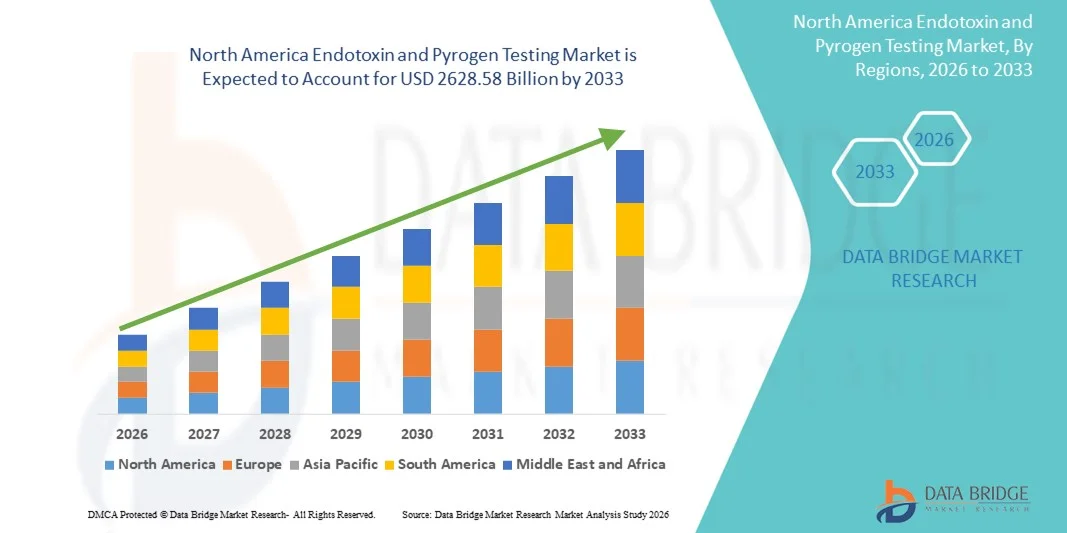
North America Endotoxin And Pyrogen Testing Market
Tamanho do mercado em biliões de dólares
CAGR :
% 
 USD
1,262.52 Billion
USD
2,628.58 Billion
2025
2033
USD
1,262.52 Billion
USD
2,628.58 Billion
2025
2033
| 2026 –2033 | |
| USD 1,262.52 Billion | |
| USD 2,628.58 Billion | |
|
|
|
|
Segmentação do mercado de testes de endotoxinas e pirogênios na América do Norte, por tipo de produto (kits e reagentes de detecção, instrumentos, sistemas e softwares, serviços de teste de endotoxinas e consumíveis e acessórios), tipo de teste (teste de lisado de amebócitos de Limulus (LAL), teste de talco, teste de ativação de monócitos (MAT), teste de pirogênio em coelhos e ensaio de proteína C recombinante (RFC)), aplicação (fabricação farmacêutica, fabricação de dispositivos médicos, produção de matérias-primas e fabricação de embalagens), método (teste de endotoxina em gel coagulado, teste de endotoxina cromogênico e teste de endotoxina turbidimétrico), modo de compra (grandes grupos, grupos médios e pequenos e individual), produto final (vacinas e/ou terapias gênicas e celulares, produtos biológicos, injetáveis e outros), usuário final (empresas farmacêuticas, empresas de biotecnologia, empresas biomédicas, empresas de dispositivos médicos, organizações de pesquisa contratada (CRO) e organizações de fabricação contratada (CMO)) - Tendências e previsões do setor até 2033.
Tamanho do mercado de testes de endotoxinas e pirogênios na América do Norte
- O mercado de testes de endotoxinas e pirogênios na América do Norte foi avaliado em US$ 1.262,52 bilhões em 2025 e deverá atingir US$ 2.628,58 bilhões até 2033 , com uma taxa de crescimento anual composta (CAGR) de 9,60% durante o período de previsão.
- O crescimento do mercado é impulsionado principalmente pela crescente ênfase na segurança do paciente, pelos rigorosos requisitos regulatórios e pelos padrões de controle de qualidade cada vez mais elevados na fabricação de produtos farmacêuticos, biotecnológicos e de dispositivos médicos, o que leva a uma maior adoção de soluções confiáveis para testes de endotoxinas e pirogênios em ambientes clínicos e industriais.
- Além disso, a crescente demanda por métodos de teste rápidos, precisos e em conformidade com as normas — juntamente com os avanços em tecnologias de teste de pirogênios recombinantes e alternativas — está posicionando os testes de endotoxinas e pirogênios como um componente crítico dos modernos sistemas de garantia da qualidade, impulsionando significativamente o crescimento geral do setor.
Análise do mercado de testes de endotoxinas e pirogênios na América do Norte
- As soluções para testes de endotoxinas e pirogênios desempenham um papel fundamental na garantia da segurança de produtos farmacêuticos, biológicos e dispositivos médicos, pois ajudam a detectar toxinas bacterianas nocivas que podem causar reações adversas em pacientes. Isso as torna essenciais para o controle de qualidade e a conformidade regulatória em ambientes clínicos e industriais.
- A crescente demanda por testes de endotoxinas e pirogênios é impulsionada principalmente por diretrizes regulatórias mais rigorosas, pelo aumento da produção de medicamentos injetáveis e produtos biológicos e pela crescente conscientização sobre a segurança do paciente, juntamente com uma mudança gradual para métodos de teste avançados e sem o uso de animais, como os ensaios de fator C recombinante (rFC).
- Os EUA dominaram o mercado de testes de endotoxinas e pirogênios, com a maior participação na receita, de aproximadamente 41,8% em 2025. Esse crescimento foi impulsionado por seu forte ecossistema de fabricação farmacêutica e biotecnológica, alta concentração de instalações regulamentadas pelo FDA, robustos investimentos em P&D e ampla adoção de tecnologias avançadas de testes de endotoxinas e pirogênios na produção de medicamentos, produtos biológicos e dispositivos médicos.
- Prevê-se que o Canadá seja o país com o crescimento mais rápido no mercado de testes de endotoxinas e pirogênios durante o período de previsão, registrando uma taxa de crescimento anual composta (CAGR) estimada em cerca de 7,9%. Esse crescimento é impulsionado pela expansão da capacidade de produção de produtos biológicos e vacinas, pelo aumento do apoio governamental às ciências da vida, pela crescente terceirização para organizações de testes contratadas e pela maior adequação aos padrões globais de qualidade e segurança.
- O segmento de Grandes Empresas dominou o mercado com uma participação de 48,3% na receita em 2025, impulsionado por instituições de saúde consolidadas e grandes organizações farmacêuticas que necessitam de compras em grande volume para atender à alta demanda por testes.
Escopo do relatório e segmentação do mercado de testes de endotoxinas e pirogênios
|
Atributos |
Análises Essenciais do Mercado de Testes de Endotoxinas e Pirógenos |
|
Segmentos abrangidos |
|
|
Países abrangidos |
América do Norte
|
|
Principais participantes do mercado |
• Charles River Laboratories (EUA) |
|
Oportunidades de mercado |
|
|
Conjuntos de informações de dados de valor agregado |
Além das informações sobre cenários de mercado, como valor de mercado, taxa de crescimento, segmentação, cobertura geográfica e principais participantes, os relatórios de mercado elaborados pela Data Bridge Market Research também incluem análises aprofundadas de especialistas, epidemiologia de pacientes, análise de projetos em desenvolvimento, análise de preços e estrutura regulatória. |
Tendências do mercado de testes de endotoxinas e pirogênios na América do Norte
Adoção crescente de métodos avançados de detecção de endotoxinas e pirogênios
- Uma tendência significativa e crescente no mercado de testes de endotoxinas e pirogênios é a adoção cada vez maior de métodos de detecção avançados, incluindo testes microbiológicos rápidos e ensaios de fator C recombinante (rFC), para melhorar a precisão dos testes e o tempo de resposta.
- Por exemplo, em 2023, diversas empresas farmacêuticas no Brasil ampliaram o uso de testes de endotoxina baseados no fator C recombinante para atender às expectativas regulatórias globais, reduzindo a dependência dos testes tradicionais de LAL (nível de atividade da laringe).
- Laboratórios em toda a região estão se concentrando em aprimorar a eficiência e a sensibilidade dos testes para garantir a segurança de produtos farmacêuticos, biológicos e dispositivos médicos.
- A mudança para métodos de teste alternativos e sustentáveis também está ganhando força devido a preocupações éticas e incentivos regulatórios.
- Essa tendência está reformulando as práticas de controle de qualidade na América do Sul, apoiando uma produção de medicamentos mais segura e a preparação para exportação para os mercados internacionais.
Dinâmica do mercado de testes de endotoxinas e pirogênios na América do Norte
Motorista
Crescimento das atividades de fabricação de produtos farmacêuticos e biológicos
- A expansão constante das atividades de fabricação farmacêutica, biotecnológica e de dispositivos médicos na América do Sul, em consonância com as tendências globais de produção, é um fator-chave que impulsiona a demanda por soluções para testes de endotoxinas e pirogênios.
- Por exemplo, em 2024, um dos principais fabricantes brasileiros de produtos biológicos expandiu sua capacidade de realizar testes de endotoxinas internamente para dar suporte à produção em larga escala de vacinas injetáveis e biossimilares destinados tanto ao mercado interno quanto ao mercado internacional.
- Requisitos regulatórios harmonizados globalmente, que enfatizam a garantia de esterilidade e a segurança do paciente, exigem testes de rotina para endotoxinas e pirogênios em todas as fases de desenvolvimento, fabricação clínica e produção comercial de medicamentos.
- O aumento dos investimentos públicos e privados em infraestrutura de saúde, pesquisa em ciências da vida e produção farmacêutica local em economias emergentes e desenvolvidas está fortalecendo ainda mais a demanda por soluções de teste confiáveis e validadas.
- O aumento das exportações de produtos farmacêuticos e biológicos da América do Norte para mercados regulamentados, como os da América do Norte e da Europa, exige o cumprimento rigoroso das normas internacionais de qualidade e segurança, reforçando, assim, a adoção de protocolos de teste de endotoxinas e pirogênios.
Restrição/Desafio
Altos custos de teste e conhecimento técnico limitado.
- Os elevados custos de capital e operacionais associados aos sistemas avançados de teste de endotoxinas e pirogênios continuam a representar uma restrição significativa, particularmente para laboratórios de pequeno e médio porte na América do Norte e em outras regiões do mundo sensíveis a custos.
- Por exemplo, diversos laboratórios de testes terceirizados na Argentina relataram atrasos na adoção de tecnologias de testes rápidos e alternativas devido a restrições orçamentárias, altos custos de equipamentos e despesas contínuas de manutenção.
- A disponibilidade limitada de profissionais qualificados e treinados para realizar, validar e interpretar testes complexos de endotoxinas e pirogênios restringe ainda mais a penetração no mercado.
- As diferenças nas normas de fiscalização e nas diretrizes de testes entre os países criam desafios para a obtenção de práticas de teste padronizadas, especialmente para fabricantes que operam em diversos mercados globais.
- Superar esses desafios por meio do desenvolvimento de soluções de teste com boa relação custo-benefício, iniciativas ampliadas de treinamento da força de trabalho e maior harmonização regulatória internacional será essencial para sustentar o crescimento do mercado global de testes de endotoxinas e pirogênios.
Escopo do mercado de testes de endotoxinas e pirogênios na América do Norte
O mercado é segmentado com base no tipo de produto, tipo de teste, aplicação, método, modo de compra, produto final e usuário final.
- Por tipo de produto
Com base no tipo de produto, o mercado de testes de endotoxinas e pirogênios é segmentado em kits e reagentes de detecção, instrumentos, sistemas e softwares, serviços de teste de endotoxinas e consumíveis e acessórios. O segmento de kits e reagentes de detecção dominou a maior participação na receita de mercado, com 41,6% em 2025, principalmente devido ao seu uso essencial e recorrente nos processos de fabricação farmacêutica, biotecnológica e de dispositivos médicos. Esses produtos são necessários em várias etapas, incluindo testes de matéria-prima, verificações de qualidade durante o processo e testes de liberação do produto final. As autoridades regulatórias exigem kits e reagentes validados, garantindo uma demanda consistente, independentemente da escala de produção. A alta frequência de testes em ambientes de fabricação estéreis aumenta ainda mais os volumes de consumo. Os kits de detecção são comparativamente econômicos, tornando-os acessíveis tanto a grandes quanto a pequenos laboratórios. A inovação contínua, que aprimora a sensibilidade e a especificidade, fortalece a adoção. A compatibilidade com múltiplos métodos de teste aumenta a flexibilidade. A expansão global da fabricação de medicamentos injetáveis sustenta o crescimento da demanda. O aumento da produção de produtos biológicos também contribui significativamente. Redes de fornecedores estabelecidas garantem disponibilidade ininterrupta. A forte dependência regulatória assegura o domínio a longo prazo.
Prevê-se que o segmento de sistemas e softwares apresente o crescimento mais rápido, com uma taxa composta de crescimento anual (CAGR) de 19,1% entre 2026 e 2033, impulsionado pela rápida adoção da automação laboratorial e de ferramentas digitais de conformidade. Os fabricantes farmacêuticos priorizam cada vez mais soluções automatizadas para minimizar erros humanos e melhorar a eficiência dos testes. As plataformas de software oferecem suporte à integridade dos dados, trilhas de auditoria e documentação regulatória. A integração com sistemas LIMS aumenta a transparência operacional. A crescente ênfase em laboratórios inteligentes acelera a adoção. Grandes fabricantes investem fortemente na transformação digital. A automação reduz o tempo de liberação de lotes. As inspeções regulatórias favorecem cada vez mais os registros digitais. Os sistemas baseados em nuvem melhoram a escalabilidade. A demanda é especialmente forte entre as Organizações de Fabricação por Contrato (CMOs). O aumento do investimento em sistemas avançados de qualidade sustenta o crescimento contínuo.
- Por tipo de teste
Com base no tipo de teste, o mercado de testes de endotoxinas e pirogênios é segmentado em teste de lisado de amebócitos de Limulus (LAL), teste TAL, teste de ativação de monócitos (MAT), teste de pirogênio em coelhos e ensaio de fator C recombinante (RFC). O segmento de teste LAL detinha a maior participação na receita de mercado, com 47,3% em 2025, devido à sua longa aceitação regulatória nos EUA, Europa e Ásia. O teste é amplamente utilizado para medicamentos injetáveis, vacinas e dispositivos médicos implantáveis. Sua comprovada confiabilidade e sensibilidade impulsionam a preferência contínua. A disponibilidade nos formatos gel-coagulante, cromogênico e turbidimétrico aumenta a versatilidade. As empresas farmacêuticas confiam no LAL para testes de rotina em lotes. Protocolos estabelecidos reduzem a complexidade da validação. Dados históricos robustos comprovam a conformidade. A disponibilidade de fornecedores garante acesso consistente. A alta familiaridade entre os profissionais de laboratório fortalece a dominância. A relação custo-benefício em comparação com métodos mais recentes facilita a adoção. A harmonização global de padrões apoia o uso.
O segmento de ensaios de fator C recombinante (RFC) deverá apresentar o crescimento mais rápido, com uma taxa composta de crescimento anual (CAGR) de 22,6% entre 2026 e 2033, impulsionado pela mudança global em direção a métodos de teste sem o uso de animais. Preocupações éticas relacionadas à coleta de caranguejos-ferradura impulsionam a adoção. Agências reguladoras apoiam cada vez mais métodos alternativos. O RFC oferece maior especificidade e reprodutibilidade. A menor variabilidade melhora a consistência dos resultados. Fabricantes biofarmacêuticos preferem o RFC para terapias avançadas. O melhor desempenho dos ensaios aumenta a confiança. Os avanços tecnológicos aprimoram a sensibilidade. Iniciativas de sustentabilidade aceleram a demanda. A crescente aprovação regulatória fortalece a adoção. A expansão dos portfólios de produtos biológicos impulsiona o crescimento. Benefícios ecológicos a longo prazo reforçam a aceitação do mercado.
- Por meio de aplicação
Com base na aplicação, o mercado de testes de endotoxinas e pirogênios é segmentado em fabricação farmacêutica, fabricação de dispositivos médicos, produção de matérias-primas e fabricação de embalagens. O segmento de fabricação farmacêutica dominou o mercado com uma participação de 44,8% da receita em 2025, impulsionado pelos rigorosos requisitos de esterilidade e controle de endotoxinas. Os testes de endotoxinas são obrigatórios durante todo o desenvolvimento e comercialização de medicamentos. Altos volumes de produção aumentam a frequência dos testes. O crescimento de medicamentos injetáveis e biológicos sustenta a demanda. Inspeções regulatórias garantem a conformidade. Protocolos de liberação de lotes exigem testes validados. A expansão das instalações globais de fabricação farmacêutica impulsiona a adoção. O monitoramento contínuo do processo aumenta o uso dos testes. Uma forte supervisão regulatória garante a dominância sustentada. Operações em larga escala impulsionam a demanda por volume. O investimento em garantia da qualidade fortalece o uso.
Prevê-se que o segmento de fabricação de dispositivos médicos cresça à taxa composta de crescimento anual (CAGR) mais rápida, de 19,8%, de 2026 a 2033, devido ao aumento da produção de dispositivos implantáveis e invasivos. O aumento da fiscalização regulatória exige testes de pirogênios. A expansão global das exportações de dispositivos médicos impulsiona a demanda. O crescimento de procedimentos minimamente invasivos sustenta a expansão do mercado. Padrões mais elevados de segurança do paciente impulsionam a adoção de testes. Os mercados emergentes aumentam a capacidade de produção. A harmonização regulatória aprimora os requisitos de conformidade. Materiais avançados exigem testes rigorosos. Os mercados crescentes de dispositivos ortopédicos e cardiovasculares sustentam o crescimento. O aumento da terceirização para Organizações de Fabricação Contratada (CMOs) acelera a demanda por testes. A inovação no design de dispositivos aumenta a complexidade dos testes.
- Por método
Com base no método, o mercado de testes de endotoxinas e pirogênios é segmentado em teste de endotoxina por gel coagulante, teste de endotoxina cromogênico e teste de endotoxina turbidimétrico. O segmento de teste de endotoxina por gel coagulante representou a maior participação na receita, com 39,5% em 2025, devido à sua simplicidade e aceitação regulatória. O método requer instrumentação mínima. É econômico para testes de rotina. Amplamente utilizado em laboratórios de pequeno e médio porte. Os resultados qualitativos atendem às necessidades básicas de conformidade. O longo histórico de validação gera confiança. A fácil interpretação fortalece a adoção. Adequado para testes de baixo volume. Os requisitos mínimos de treinamento beneficiam os laboratórios. O desempenho consistente garante confiabilidade. O amplo reconhecimento regulatório sustenta a dominância.
O segmento de testes cromogênicos de endotoxinas deverá apresentar o crescimento mais rápido, com uma taxa composta de crescimento anual (CAGR) de 20,9% entre 2026 e 2033, impulsionado pela demanda por testes quantitativos e de alta sensibilidade. As empresas farmacêuticas priorizam a medição precisa de endotoxinas. A compatibilidade com automação aumenta a produtividade. Adequado para produtos biológicos complexos. A maior precisão garante a conformidade regulatória. A alta reprodutibilidade reduz a variabilidade. O aumento da produção de produtos biológicos acelera a adoção. A integração com sistemas automatizados aumenta a eficiência. Formulações avançadas exigem detecção sensível. O crescimento da produção em larga escala sustenta a demanda. Os avanços tecnológicos aprimoram o desempenho.
- Por modalidade de compra
Com base na forma de compra, o mercado de testes de endotoxinas e pirogênios é segmentado em grandes grupos, grupos de médio e pequeno porte e indivíduos. O segmento de grandes grupos dominou o mercado com uma participação de 48,3% da receita em 2025, impulsionado por instituições de saúde consolidadas e grandes organizações farmacêuticas que necessitam de compras em grande volume para atender à alta demanda por testes. Os grandes grupos se beneficiam de contratos de longo prazo com fornecedores, economias de escala e processos de validação simplificados. Operações centralizadas de controle de qualidade e ciclos contínuos de produção exigem testes frequentes. A forte conformidade regulatória e as auditorias de rotina reforçam a adoção dos testes. A alta capacidade de investimento permite o acesso a tecnologias de teste avançadas. A integração com laboratórios internos aumenta a eficiência e a precisão. O segmento também apresenta demanda consistente de empresas multinacionais com operações globais. Procedimentos Operacionais Padrão (POPs) e sistemas de gestão da qualidade estabelecidos fortalecem sua posição dominante.
O segmento Individual deverá apresentar a taxa de crescimento anual composta (CAGR) mais rápida, de 19,4%, entre 2026 e 2033, impulsionado pela crescente adoção entre pequenas empresas de biotecnologia, startups e institutos de pesquisa. Indivíduos buscam cada vez mais opções de terceirização para reduzir despesas de capital. O número crescente de ensaios clínicos conduzidos por entidades menores alimenta a demanda. A adoção é acelerada por modelos de serviço flexíveis e testes sob demanda. A maior conscientização regulatória garante testes em conformidade com as normas. A expansão dos pipelines de produtos biológicos e terapia celular e gênica em pequenas organizações sustenta o crescimento. O acesso a pedidos digitais e relatórios simplificados aumenta o apelo do mercado. Mercados emergentes e o crescimento de startups contribuem ainda mais para a expansão do mercado. Clientes individuais frequentemente utilizam serviços de CRO/CMO, aumentando a frequência de testes.
- Por produto final
Com base no produto final, o mercado de Testes de Endotoxinas e Pirógenos é segmentado em Vacinas e/ou Terapia Celular e Gênica (TCG), Produtos Biológicos, Injetáveis e Outros. O segmento de Produtos Biológicos dominou o mercado com uma participação de 42,6% da receita em 2025, impulsionado pelo uso generalizado de produtos biológicos em aplicações terapêuticas e pelos rigorosos requisitos regulatórios para testes de esterilidade e endotoxinas. A produção em larga escala de anticorpos monoclonais, proteínas recombinantes e enzimas terapêuticas impulsiona os testes de rotina. Auditorias regulatórias e programas de garantia da qualidade asseguram ciclos de testes frequentes. O alto investimento em P&D e ensaios clínicos reforça a demanda. A presença de fabricantes líderes em biotecnologia facilita a adoção de métodos de teste avançados. A produção de produtos biológicos requer estruturas robustas de controle de qualidade para prevenir a contaminação. A infraestrutura estabelecida na América do Norte e na Europa fortalece a posição dominante. Parcerias com organizações de testes terceirizadas expandem o alcance. A adoção pelo mercado é ainda mais impulsionada pela crescente conscientização sobre a segurança dos produtos biológicos.
Prevê-se que o segmento de Vacinas e/ou Terapia Celular e Gênica (TCG) apresente a taxa de crescimento anual composta (CAGR) mais rápida, de 22,3%, entre 2026 e 2033, impulsionado pelo desenvolvimento acelerado de novas vacinas e terapias celulares e gênicas avançadas. Iniciativas globais de saúde, preparação para pandemias e o aumento dos programas de imunização elevam a demanda por testes. Os produtos de TCG exigem testes de endotoxinas altamente sensíveis devido aos complexos processos de fabricação. A expansão da medicina personalizada e das terapias direcionadas impulsiona a adoção. A terceirização para CROs e laboratórios especializados garante a conformidade. O foco regulatório em produtos medicinais de terapia avançada impulsiona o crescimento. A inovação em tecnologias de mRNA e vetores virais impulsiona o volume. Empresas de biotecnologia emergentes buscam ativamente soluções de testes de alto rendimento. O aumento do financiamento para P&D de vacinas apoia a expansão do mercado. A adoção de plataformas de testes automatizadas e rápidas acelera a eficiência.
- Por usuário final
Com base no usuário final, o mercado de testes de endotoxinas e pirogênios é segmentado em empresas farmacêuticas, empresas de biotecnologia, empresas biomédicas, empresas de dispositivos médicos, CROs e CMOs. As empresas farmacêuticas dominaram o mercado com uma participação de 45,7% da receita em 2025, devido às extensas operações internas de controle de qualidade. Grandes volumes de produção aumentam as necessidades de testes. Auditorias regulatórias exigem validação frequente. O investimento em laboratórios internos fortalece o domínio. Ciclos contínuos de produção impulsionam a demanda. Altos padrões de conformidade exigem testes de rotina. A expansão dos pipelines de produtos biológicos apoia o uso. Forte capacidade financeira permite a adoção de testes avançados. A presença global aumenta a escala de testes. Estruturas de qualidade estabelecidas reforçam o domínio.
Prevê-se que o segmento de CROs e CMOs apresente o crescimento mais rápido, com uma taxa composta de crescimento anual (CAGR) de 21,7% entre 2026 e 2033, impulsionado pela crescente tendência de terceirização. As empresas farmacêuticas buscam a otimização de custos. Os testes terceirizados melhoram a eficiência. As CMOs expandem sua capacidade global. A conformidade regulatória impulsiona a demanda por serviços. Pequenas empresas de biotecnologia dependem de CROs. A expertise especializada aumenta a adoção. O crescimento da fabricação por contrato acelera o volume de testes. Modelos de serviço flexíveis atraem clientes. A expansão para mercados emergentes sustenta o crescimento. O aumento da atividade de ensaios clínicos eleva a demanda.
Análise Regional do Mercado de Testes de Endotoxinas e Pirógenos na América do Norte
- A América do Norte dominou o mercado de testes de endotoxinas e pirogênios, com uma participação de receita em constante expansão em 2025, impulsionada pela crescente base de fabricação farmacêutica e biotecnológica em toda a região, juntamente com a ênfase regulatória cada vez maior na segurança do produto e na conformidade com os padrões de qualidade.
- Os fabricantes de produtos farmacêuticos e dispositivos médicos na América do Norte estão adotando cada vez mais testes de endotoxinas e pirogênios para atender a padrões internacionais como USP, EP e JP, principalmente para medicamentos injetáveis, produtos biológicos e dispositivos médicos implantáveis.
- O crescimento do mercado é ainda impulsionado pelo aumento dos gastos com saúde, pela expansão dos laboratórios de análises terceirizados e pelo crescente investimento em infraestrutura de controle de qualidade, posicionando os testes de endotoxinas e pirogênios como um componente crítico para garantir a segurança do paciente em toda a região.
Análise do Mercado de Testes de Endotoxinas e Pirógenos nos EUA
O mercado de testes de endotoxinas e pirogênios dos EUA dominou o mercado da América do Norte, com a maior participação de receita, de aproximadamente 41,8% em 2025. Esse crescimento é impulsionado pelo forte ecossistema de fabricação farmacêutica e biotecnológica do país, pela alta concentração de instalações regulamentadas pelo FDA, pelos robustos investimentos em P&D e pela ampla adoção de tecnologias avançadas de testes de endotoxinas e pirogênios na produção de medicamentos, produtos biológicos e dispositivos médicos. Os fabricantes dependem cada vez mais de testes de endotoxinas e pirogênios para atender aos padrões internacionais de conformidade, garantindo a segurança de medicamentos injetáveis, produtos biológicos e dispositivos implantáveis. A crescente demanda por vacinas e produtos biológicos impulsiona ainda mais a adoção desses testes. O mercado americano se beneficia de infraestrutura laboratorial avançada, fornecimento de reagentes e instrumentos de alta qualidade e colaboração com CROs globais. Plataformas de teste automatizadas e gerenciamento digital de dados melhoram a precisão e reduzem erros humanos. Investimentos em tecnologias de ensaio de alta sensibilidade e em métodos de teste cromogênicos, de gel-coagulação e recombinantes reforçam a confiabilidade. O mercado também apresenta crescimento devido às organizações de testes por contrato que atendem a diversas empresas farmacêuticas e biotecnológicas. A aplicação rigorosa das normas regulamentares garante a adoção consistente de protocolos de teste padronizados, reforçando os EUA como o principal contribuinte para a receita na América do Norte.
Análise do Mercado de Testes de Endotoxinas e Pirógenos no Canadá
O mercado canadense de testes de endotoxinas e pirogênios deverá ser o de crescimento mais rápido na América do Norte durante o período de previsão, registrando uma taxa de crescimento anual composta (CAGR) estimada em 7,9%. O crescimento é impulsionado pela expansão da capacidade de produção de produtos biológicos e vacinas, pelo aumento do apoio governamental às ciências da vida, pela crescente terceirização para organizações de testes por contrato e pelo alinhamento cada vez maior com os padrões regulatórios globais de qualidade e segurança. A expansão da capacidade de produção nacional de biossimilares, vacinas e medicamentos parenterais acelera a adoção de soluções de testes de endotoxinas e pirogênios. Empresas farmacêuticas e de biotecnologia canadenses estão investindo em plataformas de testes automatizadas e de alta sensibilidade. A maior conformidade com as diretrizes da FDA, EMA e Health Canada garante a adoção consistente de protocolos de testes padronizados. Parcerias com CROs e CMOs internacionais proporcionam acesso a tecnologias de testes avançadas. O foco crescente na segurança do paciente, garantia da qualidade e automação laboratorial também contribui para o crescimento. A inovação contínua em métodos de ensaio, relatórios digitais e gerenciamento de fluxo de trabalho aprimora a eficiência e a precisão. As iniciativas do Canadá na área das ciências da vida e os investimentos em infraestrutura de P&D posicionam o país como um mercado de alto crescimento no setor de testes de endotoxinas e pirogênios na América do Norte.
Participação de mercado de testes de endotoxinas e pirogênios na América do Norte
O setor de testes de endotoxinas e pirogênios é liderado principalmente por empresas consolidadas, incluindo:
• Charles River Laboratories (EUA)
• Lonza Group (Suíça)
• Thermo Fisher Scientific (EUA)
• Merck KGaA (Alemanha)
• Associates of Cape Cod (EUA)
• WuXi AppTec (China)
• Eurofins Scientific (Luxemburgo)
• BioMérieux (França)
• ToxinSensor (EUA)
• Hyglos GmbH (Alemanha)
• Fujifilm Wako Chemicals (Japão)
• GenScript Biotech (China)
• Seikagaku Corporation (Japão)
• Pacific BioLabs (EUA)
• Cambrex Corporation (EUA)
• SGS SA (Suíça)
• Kinetic-QCL (EUA)
• Nelson Laboratories (EUA)
• RANDOX Laboratories (Reino Unido)
• Creative Diagnostics (EUA)
Novidades no mercado de testes de endotoxinas e pirogênios na América do Norte
- Em abril de 2021, a Associates of Cape Cod, Inc. lançou o reagente recombinante LAL PyroSmart NextGen, um produto sustentável para testes de endotoxinas bacterianas, projetado para melhorar a consistência dos ensaios e, ao mesmo tempo, reduzir a dependência de materiais de origem animal.
- Em junho de 2021, a Comissão da Farmacopeia Europeia anunciou uma medida regulamentar para eliminar o teste de pirogênio em coelhos da Farmacopeia Europeia (Ph. Eur.) em cinco anos, recomendando alternativas como o Teste de Ativação de Monócitos (MAT) para atender aos padrões em constante evolução.
- Em janeiro de 2024, a FUJIFILM Wako Chemicals USA Corporation atualizou seu portfólio de reagentes de lisado de amebócitos de Limulus (LAL) para oferecer maior sensibilidade e menor variabilidade, aprimorando a confiabilidade dos testes de endotoxinas em medicamentos parenterais e dispositivos médicos.
- Em fevereiro de 2024, a Charles River Laboratories lançou plataformas aprimoradas para o Teste de Ativação de Monócitos (MAT, na sigla em inglês) com integração de automação, aumentando a produtividade e a reprodutibilidade dos fluxos de trabalho de detecção de pirogênios em testes de produtos biológicos e terapia celular.
- Em março de 2024, o Grupo Lonza expandiu sua oferta de testes de endotoxinas e pirogênios com o lançamento de um novo kit de ensaio baseado no Fator C recombinante (rFC), alinhando-se às tendências da indústria em direção a métodos de teste sustentáveis e sem o uso de animais.
SKU-
Obtenha acesso online ao relatório sobre a primeira nuvem de inteligência de mercado do mundo
- Painel interativo de análise de dados
- Painel de análise da empresa para oportunidades de elevado potencial de crescimento
- Acesso de analista de pesquisa para personalização e customização. consultas
- Análise da concorrência com painel interativo
- Últimas notícias, atualizações e atualizações Análise de tendências
- Aproveite o poder da análise de benchmark para um rastreio abrangente da concorrência
Metodologia de Investigação
A recolha de dados e a análise do ano base são feitas através de módulos de recolha de dados com amostras grandes. A etapa inclui a obtenção de informações de mercado ou dados relacionados através de diversas fontes e estratégias. Inclui examinar e planear antecipadamente todos os dados adquiridos no passado. Da mesma forma, envolve o exame de inconsistências de informação observadas em diferentes fontes de informação. Os dados de mercado são analisados e estimados utilizando modelos estatísticos e coerentes de mercado. Além disso, a análise da quota de mercado e a análise das principais tendências são os principais fatores de sucesso no relatório de mercado. Para saber mais, solicite uma chamada de analista ou abra a sua consulta.
A principal metodologia de investigação utilizada pela equipa de investigação do DBMR é a triangulação de dados que envolve a mineração de dados, a análise do impacto das variáveis de dados no mercado e a validação primária (especialista do setor). Os modelos de dados incluem grelha de posicionamento de fornecedores, análise da linha de tempo do mercado, visão geral e guia de mercado, grelha de posicionamento da empresa, análise de patentes, análise de preços, análise da quota de mercado da empresa, normas de medição, análise global versus regional e de participação dos fornecedores. Para saber mais sobre a metodologia de investigação, faça uma consulta para falar com os nossos especialistas do setor.
Personalização disponível
A Data Bridge Market Research é líder em investigação formativa avançada. Orgulhamo-nos de servir os nossos clientes novos e existentes com dados e análises que correspondem e atendem aos seus objetivos. O relatório pode ser personalizado para incluir análise de tendências de preços de marcas-alvo, compreensão do mercado para países adicionais (solicite a lista de países), dados de resultados de ensaios clínicos, revisão de literatura, mercado remodelado e análise de base de produtos . A análise de mercado dos concorrentes-alvo pode ser analisada desde análises baseadas em tecnologia até estratégias de carteira de mercado. Podemos adicionar quantos concorrentes necessitar de dados no formato e estilo de dados que procura. A nossa equipa de analistas também pode fornecer dados em tabelas dinâmicas de ficheiros Excel em bruto (livro de factos) ou pode ajudá-lo a criar apresentações a partir dos conjuntos de dados disponíveis no relatório.