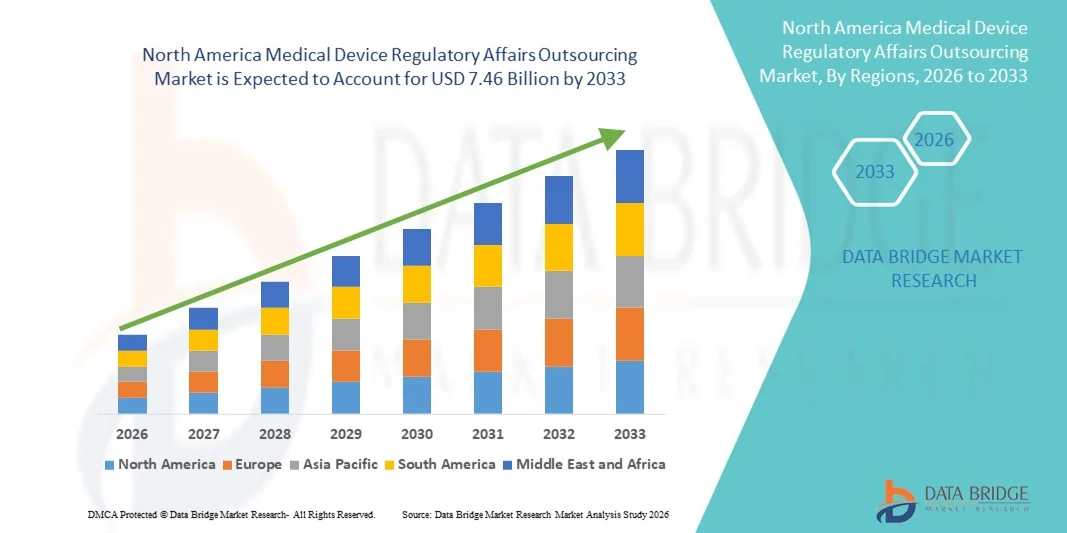
North America Medical Device Regulatory Affairs Outsourcing Market
Размер рынка в млрд долларов США
CAGR :
% 
 USD
2.93 Billion
USD
7.46 Billion
2025
2033
USD
2.93 Billion
USD
7.46 Billion
2025
2033
| 2026 –2033 | |
| USD 2.93 Billion | |
| USD 7.46 Billion | |
|
|
|
|
Сегментация рынка аутсорсинга услуг по регулированию медицинских изделий в Северной Америке по видам услуг (услуги по регулированию, консультации по качеству и медицинское написание текстов), продуктам (готовая продукция, электроника и сырье), типам устройств (классы I, II и III), областям применения (кардиология, диагностическая визуализация, ортопедия, диагностика in vitro, офтальмология, общая и пластическая хирургия, доставка лекарств, стоматология, эндоскопия, лечение диабета и другие), конечным пользователям (малые, средние и крупные компании-производители медицинских изделий) — тенденции отрасли и прогноз до 2033 года.
Размер рынка аутсорсинга услуг по регулированию медицинских изделий в Северной Америке
- Объем рынка аутсорсинга услуг по регулированию медицинских изделий в Северной Америке в 2025 году оценивался в 2,93 млрд долларов США и, как ожидается, достигнет 7,46 млрд долларов США к 2033 году , демонстрируя среднегодовой темп роста в 12,40% в течение прогнозируемого периода.
- Рост рынка в значительной степени обусловлен растущей сложностью нормативных требований в фармацевтической, биотехнологической и медицинской отраслях, что побуждает компании обращаться к специализированным аутсорсинговым услугам для управления соответствием нормативным требованиям.
- Кроме того, растущий спрос на экономически эффективные, действенные и своевременные регуляторные документы стимулирует внедрение решений по аутсорсингу в сфере регулирования. Эти факторы в совокупности ускоряют распространение услуг аутсорсинга в сфере регулирования, тем самым значительно способствуя росту отрасли в глобальном масштабе.
Анализ рынка аутсорсинга услуг по регулированию медицинских изделий в Северной Америке
- Рынок аутсорсинга в сфере регулирования медицинских изделий, предполагающий делегирование разработки регуляторной стратегии, подготовки документации по соблюдению нормативных требований, регистрации продукции и постмаркетингового надзора специализированным поставщикам услуг, приобретает все большее значение для компаний, производящих медицинские изделия и работающих в условиях сложных и постоянно меняющихся нормативных рамок на Ближнем Востоке.
- Ужесточение регулирования медицинских изделий, растущий спрос на ускоренное получение разрешений и потребность в локальной экспертизе в области регулирования являются ключевыми факторами, стимулирующими внедрение услуг аутсорсинга в сфере регулирования медицинских изделий. Компании используют партнеров по аутсорсингу для минимизации рисков, связанных с соблюдением нормативных требований, оптимизации сроков получения разрешений и сосредоточения внимания на разработке и коммерциализации основных продуктов.
- США доминировали на рынке аутсорсинга услуг по регулированию медицинских изделий, занимая наибольшую долю выручки — приблизительно 42,5% в 2025 году. Это стало возможным благодаря хорошо развитой экосистеме здравоохранения и медицинских изделий, жесткому надзору со стороны FDA, большому объему медицинских процедур и присутствию ведущих консалтинговых фирм в области регулирования. Акцент страны на соблюдении нормативных требований, своевременном получении разрешений и надежных процессах регистрации на рынке значительно повысил спрос на специализированные услуги аутсорсинга.
- Ожидается, что Канада станет самым быстрорастущим рынком, демонстрируя среднегодовой темп роста около 10,1% в течение прогнозируемого периода, чему способствуют быстрая модернизация здравоохранения, растущее присутствие международных производителей медицинских изделий и развивающаяся нормативно-правовая база Министерства здравоохранения Канады. Растущая осведомленность об эффективных решениях в области аутсорсинга и упрощенных регуляторных процессах еще больше способствует расширению рынка по всей стране.
- В 2025 году сегмент готовой продукции занимал наибольшую долю рынка по выручке — 52,1%, поскольку готовые медицинские изделия подлежат строгим процедурам предварительного одобрения и послепродажного надзора.
Обзор отчета и сегментация рынка аутсорсинга в сфере регулирования медицинских изделий.
|
Атрибуты |
Аутсорсинг вопросов регулирования медицинских изделий: ключевые рыночные тенденции. |
|
Охваченные сегменты |
|
|
Охваченные страны |
Северная Америка
|
|
Ключевые игроки рынка |
|
|
Рыночные возможности |
|
|
Информационные наборы данных, представляющие добавленную стоимость |
Помимо анализа рыночных сценариев, таких как рыночная стоимость, темпы роста, сегментация, географический охват и основные игроки, отчеты о рынке, подготовленные Data Bridge Market Research, также включают углубленный экспертный анализ, эпидемиологию пациентов, анализ перспективных разработок, анализ ценообразования и нормативно-правовую базу. |
Тенденции рынка аутсорсинга в сфере регулирования медицинских изделий в Северной Америке
Возрастающая сложность регулирования медицинских изделий в разных регионах.
- Значительной и быстро развивающейся тенденцией на рынке аутсорсинга услуг по регулированию медицинских изделий является растущая сложность и постоянная эволюция нормативно-правовых рамок, регулирующих медицинские изделия. Страны региона усиливают процессы утверждения, требования к постмаркетинговому надзору и стандарты соответствия, стремясь к более тесному соответствию международным стандартам.
- Например, регулирующие органы стран Совета сотрудничества стран Персидского залива (ССГПЗ) и Южной Африки внедрили более структурированные системы регистрации медицинских изделий, что побудило производителей полагаться на специализированных партнеров по аутсорсингу в сфере регулирования для эффективного прохождения местных процедур подачи заявок и выполнения требований к документации.
- Растущее внедрение международных стандартов, таких как ISO 13485 и системы классификации на основе рисков, стимулирует спрос на внешних экспертов для управления подготовкой нормативной документации, технической документации и обеспечением соответствия стандартам качества. Партнеры по аутсорсингу предоставляют знания, специфичные для конкретного региона, что помогает сократить сроки получения разрешений и регуляторные риски.
- Кроме того, расширение деятельности транснациональных компаний по производству медицинских изделий на рынки Ближнего Востока и Африки стимулирует использование услуг сторонних регуляторов для управления регистрацией продукции в нескольких странах посредством централизованного и экономически эффективного подхода.
- Тенденция к использованию профессиональных услуг по сопровождению нормативных требований меняет подход производителей к выходу на рынок и соблюдению нормативных требований, при этом аутсорсинг становится стратегической необходимостью, а не дополнительной услугой в регионе.
- В условиях усиления регуляторного контроля спрос на специализированных поставщиков услуг в области регулирования, обладающих региональной экспертизой, продолжает расти как среди глобальных, так и среди местных производителей медицинских изделий.
Динамика рынка аутсорсинга в сфере регулирования медицинских изделий в Северной Америке
Водитель
Рост рынка медицинских изделий и ужесточение регулирования
- Быстрое расширение сектора медицинских изделий во всем мире, обусловленное ростом инвестиций в здравоохранение, увеличением численности населения и ростом распространенности хронических заболеваний, является основным фактором, стимулирующим развитие услуг аутсорсинга в сфере регулирования.
- Например, растущее развитие инфраструктуры здравоохранения в таких странах, как Саудовская Аравия, ОАЭ и Южная Африка, привело к увеличению спроса на медицинские изделия, что, в свою очередь, увеличило нагрузку на регулирующие органы, стремящиеся своевременно получить разрешение на вывод продукции на рынок.
- В связи с ужесточением требований регулирующих органов к соблюдению нормативных требований, производители все чаще передают контрольную деятельность специализированным фирмам, чтобы обеспечить точность, согласованность и ускоренное утверждение продукции.
- Кроме того, малым и средним компаниям-производителям медицинских изделий часто не хватает собственных специалистов по регулированию в различных региональных нормативных актах, что делает аутсорсинг практичным решением для управления затратами и снижения рисков, связанных с соблюдением нормативных требований.
- Необходимость поддержания соответствия нормативным требованиям на протяжении всего жизненного цикла продукта, включая продление лицензий, внесение изменений и послепродажный надзор, продолжает поддерживать устойчивый спрос на услуги аутсорсинга в регионе.
Сдержанность/Вызов
Ограниченная гармонизация нормативных требований и нехватка квалифицированных специалистов.
- Одной из ключевых проблем на рынке аутсорсинга услуг по регулированию медицинских изделий является отсутствие согласованных нормативных рамок в разных странах, что увеличивает сложность и требования к ресурсам как для поставщиков услуг, так и для производителей.
- Например, различные форматы подачи документов, сроки утверждения и требования регулирующих органов на рынках Африки и Ближнего Востока могут приводить к задержкам и увеличению операционных расходов, даже при передаче регуляторных функций на аутсорсинг.
- Еще одним существенным ограничением является ограниченная доступность высококвалифицированных специалистов в области регулирования, обладающих глубокими знаниями как местных нормативных актов, так и международных стандартов, особенно на развивающихся африканских рынках.
- Кроме того, опасения, связанные с конфиденциальностью данных, пробелами в коммуникации и зависимостью от сторонних поставщиков услуг, могут заставить некоторых производителей колебаться, прежде чем полностью передать функции регулирования на аутсорсинг.
- Преодоление этих проблем за счет наращивания потенциала в сфере регулирования, региональных инициатив по гармонизации и инвестиций в развитие квалифицированных кадров будет иметь решающее значение для долгосрочного роста и эффективности рынка аутсорсинга в сфере регулирования медицинских изделий на Ближнем Востоке и в Африке.
Обзор рынка аутсорсинга услуг в сфере регулирования медицинских изделий в Северной Америке
Рынок сегментирован по видам услуг, продукции, типам устройств, областям применения и конечным пользователям.
- Услуги
Рынок аутсорсинга услуг в области регулирования медицинских изделий сегментирован по видам услуг на услуги по регулированию, консультации по качеству и медицинское написание. Сегмент услуг по регулированию занимал наибольшую долю рынка, составляющую 46,8% выручки в 2025 году, благодаря растущей сложности регулирования медицинских изделий в таких основных регионах, как Северная Америка, Европа и Азиатско-Тихоокеанский регион. Компании полагаются на аутсорсинговые услуги в области регулирования для подготовки заявок на регистрацию перед выходом на рынок, технической документации и управления соответствием требованиям после выхода на рынок. Растущие нормативные требования к изделиям класса II и III стимулируют спрос. Глобализация операций с медицинскими изделиями и трансграничная регистрация продукции также способствуют развитию сегмента. Аутсорсинг услуг по регулированию снижает операционные затраты, обеспечивая при этом соответствие рекомендациям FDA, EU MDR и IVDR. Сегмент выигрывает от увеличения количества регуляторных проверок и частых обновлений стандартов документации. Управление жизненным циклом изделий, отчетность по надзору и снижение рисков являются критически важными факторами. Компании все чаще отдают приоритет аутсорсингу для ускорения выхода на рынок при одновременном снижении нагрузки на внутренние ресурсы. Растущее внедрение передовых медицинских устройств и стремительные инновации в продукции еще больше укрепляют лидирующие позиции. Выход на развивающиеся рынки создает устойчивый спрос на услуги в области регулирования.
Ожидается, что сегмент медицинского копирайтинга продемонстрирует самый быстрый среднегодовой темп роста в 11,4% в период с 2026 по 2033 год, обусловленный растущим мировым спросом на высококачественные отчеты о клинических оценках, технические файлы и нормативную документацию. Малые и средние компании-производители медицинских изделий все больше зависят от услуг внештатных медицинских копирайтеров. Регулирующие органы требуют точной и соответствующей требованиям документации для утверждения медицинских изделий, что стимулирует рост. Внедрение электронных платформ для подачи документов ускоряет аутсорсинг. Рост числа клинических испытаний, сбора данных из реальной клинической практики и отчетности по данным после выхода продукции на рынок повышает спрос. Цифровизация и инструменты медицинского копирайтинга с использованием ИИ способствуют более быстрой подготовке документов. Компании стремятся к гибким договорам на аутсорсинг, чтобы снизить нагрузку на внутренний персонал. Расширение терапевтических областей, включая кардиологию, ортопедию и устройства для диагностики in vitro, еще больше стимулирует рост. Усиление международной гармонизации регулирования поддерживает потребности в трансграничном аутсорсинге. В целом, сегмент выигрывает от растущей сложности регулирования и возрастающей важности точной медицинской документации.
- По продукту
Рынок аутсорсинга услуг по регулированию медицинских изделий сегментируется по видам продукции: готовая продукция, электроника и сырье. В 2025 году сегмент готовой продукции занимал наибольшую долю рынка – 52,1%, поскольку готовые медицинские изделия проходят строгие процедуры предварительного одобрения и постмаркетингового надзора. Компании передают на аутсорсинг регуляторные процессы для обеспечения бесперебойного соблюдения требований FDA, EU MDR и других региональных нормативных актов. Готовая продукция включает в себя устройства для кардиологии, ортопедии, диагностики in vitro и офтальмологии. Аутсорсинг помогает снизить внутреннюю нагрузку, обеспечивая при этом соблюдение стандартов качества и безопасности. Производители ищут экспертную поддержку в вопросах маркировки, документации, валидации и подготовки клинических доказательств. Усиленный контроль за комбинированными продуктами, устройствами с интегрированным программным обеспечением и подключенными медицинскими устройствами способствует доминированию на рынке. Глобальное расширение операций с медицинскими изделиями стимулирует заключение долгосрочных контрактов на аутсорсинг. Аутсорсинг снижает риски, связанные с аудитами и штрафами за несоблюдение требований. Компании отдают приоритет скорости вывода продукции на рынок без ущерба для соответствия нормативным требованиям. Дополнительные факторы, стимулирующие этот процесс, включают в себя постмаркетинговый мониторинг и отчетность о нежелательных побочных эффектах. Производители стремятся оптимизировать распределение ресурсов и повысить экономическую эффективность за счет аутсорсинга.
Ожидается, что сегмент электроники продемонстрирует самый быстрый среднегодовой темп роста в 10,7% в период с 2026 по 2033 год благодаря растущей интеграции программного обеспечения и цифровых компонентов в медицинские устройства. Соблюдение нормативных требований в отношении программного обеспечения, микропрограмм и кибербезопасности подключенных устройств является сложной и постоянно развивающейся задачей. Аутсорсинг предпочтителен для обеспечения готовности к регулированию и ускорения получения разрешений. Рост рынка носимых устройств, систем удаленного мониторинга и цифровых решений для здравоохранения поддерживает этот сегмент. Стартапы и малые и средние предприятия все чаще полагаются на экспертов по регулированию в отношении устройств с большим количеством электроники. Внедрение ИИ и машинного обучения в медицинские устройства увеличивает требования к документации и тестированию. Трансграничная коммерциализация стимулирует спрос на стандартизированную нормативную документацию. Тенденция развития решений для подключенного здравоохранения ускоряет аутсорсинг деятельности по обеспечению соответствия нормативным требованиям. Компании стремятся снизить внутреннюю операционную нагрузку, соблюдая при этом глобальные нормативные стандарты. Расширение использования телемедицинских устройств и медицинских устройств с поддержкой IoT дополнительно способствует росту.
- По типу устройства
Рынок аутсорсинга услуг по регулированию медицинских изделий сегментируется по типу устройства на устройства класса I, класса II и класса III. Сегмент устройств класса II доминировал на рынке с долей выручки в 41,6% в 2025 году благодаря большому объему устройств со средней степенью регулирования, поступающих на рынок. Регуляторные заявки для устройств класса II включают документацию, техническую документацию и соответствие требованиям FDA 510(k) или маркировки CE. Аутсорсинг помогает производителям оптимизировать процесс получения разрешений и снизить внутреннюю нагрузку. Ортопедические, диагностические и мониторинговые устройства составляют значительную часть продукции класса II. Компании используют услуги аутсорсинга для управления жизненным циклом продукта, постмаркетингового надзора и регуляторных аудитов. Глобализация операций с медицинскими изделиями и растущие инновации дополнительно стимулируют спрос. Ключевыми преимуществами являются снижение затрат, эффективность и своевременный выход на рынок. Сложность регулирования в различных регионах усиливает зависимость от аутсорсинга. Деятельность по управлению жизненным циклом, включая модификации, обновления и отчетность устройств, способствует развитию сегмента. Растущее внедрение медицинских изделий на развивающихся рынках способствует их доминированию. Для изделий класса II характерен баланс между инновациями и сложностью регулирования, что делает аутсорсинг необходимым.
Прогнозируется, что сегмент устройств класса III будет расти самыми быстрыми темпами, достигая среднегодового темпа роста в 12,8% в период с 2026 по 2033 год, чему способствует растущая разработка имплантируемых, жизнеобеспечивающих и высокорисковых устройств. Для этих устройств требуются обширные клинические данные, валидационные исследования и разрешения регулирующих органов. Аутсорсинг вопросов регулирования минимизирует задержки в получении разрешений и обеспечивает соответствие мировым стандартам. Тщательная проверка высокорисковых устройств, включая кардиоимплантаты и нейромодуляционные устройства, стимулирует рост рынка. Производители полагаются на партнеров по регулированию в вопросах документации, отчетов о клинических оценках и технической документации. Растущая тенденция к использованию комбинированных продуктов увеличивает спрос на аутсорсинг. Непрерывный постмаркетинговый надзор и требования к отчетности о нежелательных явлениях дополнительно способствуют расширению. Обновления нормативных требований в рамках MDR и IVDR усиливают рост сегмента. Малые и средние компании все чаще передают на аутсорсинг вопросы соответствия требованиям для устройств класса III из-за их сложности. Инновации в биосовместимых материалах и интеллектуальных имплантатах способствуют ускорению развития сегмента. Высокая стоимость продукции и регуляторные риски сегмента обеспечивают устойчивый спрос на аутсорсинг.
- По заявлению
Рынок аутсорсинга услуг по регулированию медицинских изделий сегментирован по областям применения: кардиология, диагностическая визуализация, ортопедия, диагностика in vitro (IVD), офтальмология, общая и пластическая хирургия, доставка лекарств, стоматология, эндоскопия, лечение диабета и другие. В 2025 году сегмент IVD занимал наибольшую долю рынка, составляющую 30,2%, благодаря растущему спросу на диагностическое тестирование и персонализированную медицину. Аутсорсинг имеет решающее значение из-за строгих требований соответствия Регламенту ЕС по диагностике in vitro (IVDR) и FDA. Производители зависят от экспертов по регулированию в вопросах одобрения, валидации, маркировки и постмаркетингового надзора за медицинскими изделиями. Расширение диагностических центров, клинических лабораторий и молекулярно-диагностических учреждений способствует росту. Увеличение распространенности хронических заболеваний повышает спрос на точные диагностические устройства. Компании стремятся снизить операционные издержки и минимизировать регуляторные риски. Глобализация дистрибуции IVD-устройств еще больше усиливает потребность в аутсорсинге. Быстрые инновации в продуктах требуют своевременной регуляторной поддержки. Классификация IVD-устройств на основе рисков стимулирует использование аутсорсинга. Регуляторные проверки, маркировка CE и разрешения FDA способствуют росту рыночной активности. Сегмент выигрывает от растущих инвестиций в раннюю диагностику заболеваний и прецизионную медицину.
Ожидается, что сегмент «Уход за диабетом» продемонстрирует самый быстрый среднегодовой темп роста в 13,3% в период с 2026 по 2033 год, чему способствуют глобальный рост распространенности диабета и внедрение подключенных систем мониторинга уровня глюкозы. Нормативные требования к устройствам непрерывного мониторинга уровня глюкозы и интеллектуальным устройствам доставки инсулина сложны, что увеличивает спрос на аутсорсинг. Стартапы и средние производители полагаются на экспертов-партнеров в вопросах документации, технической документации и соответствия требованиям. Устройства для управления диабетом с интегрированным ИИ требуют дополнительной нормативной поддержки. Рост рынка носимых устройств и решений для домашнего ухода способствует расширению сегмента. Выход на трансграничный рынок требует согласованных нормативных документов. Цифровая терапия и интеграция телемедицины еще больше стимулируют аутсорсинг. Послепродажный мониторинг и управление рисками являются критически важными факторами. Внимание правительств и медицинских учреждений к управлению диабетом укрепляет рынок. Увеличение венчурного финансирования цифровых решений для лечения диабета ускоряет рост. Мелкие производители получают выгоду от снижения внутренних затрат на соблюдение нормативных требований. Недостаток знаний о нормативных требованиях среди новых компаний способствует широкому внедрению аутсорсинга.
- Конечным пользователем
Рынок аутсорсинга услуг по регулированию медицинских изделий сегментируется по конечным пользователям на малые, средние и крупные компании. Крупные компании доминировали на рынке с долей выручки в 44,9% в 2025 году благодаря обширному портфелю продукции и глобальным операциям. Аутсорсинг поддерживает подачу заявок в регулирующие органы в разных странах и обеспечивает соответствие различным стандартам. Частые запуски продуктов и мероприятия по управлению жизненным циклом требуют экспертной поддержки. Компании используют аутсорсинг для оптимизации распределения ресурсов и снижения внутренней нагрузки по соблюдению нормативных требований. Крупные игроки сталкиваются с высоким уровнем регуляторного контроля в отношении устройств классов II и III, что способствует росту сегмента. Постмаркетинговый надзор, клинические оценки и техническая документация передаются на аутсорсинг специализированным фирмам. Регуляторные аудиты, маркировка CE и одобрения FDA 510(k) способствуют увеличению использования аутсорсинга. Снижение рисков, экономическая эффективность и более быстрый выход на рынок обеспечивают доминирование. Расширение на развивающиеся рынки требует экспертных знаний в области аутсорсинга. Интеграция программного обеспечения и подключенных устройств еще больше увеличивает спрос. Аутсорсинг позволяет крупным компаниям сосредоточиться на исследованиях и разработках, обеспечивая при этом соблюдение нормативных требований.
Ожидается, что сегмент малых компаний по производству медицинских изделий будет расти самыми быстрыми темпами (CAGR 13,1%) в период с 2026 по 2033 год, что обусловлено ограниченной внутренней экспертизой в области регулирования. Стартапы и компании на ранних стадиях развития в значительной степени полагаются на услуги аутсорсинга для выполнения глобальных требований соответствия. Аутсорсинг помогает сократить сроки получения разрешений и операционные расходы. Росту способствует инновационность носимых, диагностических и домашних медицинских устройств. Сложная документация, клиническая оценка и требования послепродажного обслуживания делают аутсорсинг необходимым. Компании, финансируемые венчурным капиталом, ищут экономически эффективные решения в области регулирования. Расширение глобального рынка требует экспертных знаний в региональных нормативных актах. Быстро меняющиеся требования MDR и IVDR ускоряют внедрение аутсорсинга. Инструменты регулирования с использованием искусственного интеллекта помогают малым компаниям эффективно оформлять документацию. Снижение рисков, связанных с соблюдением нормативных требований, является основным фактором роста сегмента. Стартапы используют аутсорсинг для ускорения выхода на рынок и снижения внутренней рабочей нагрузки. Расширение партнерских отношений с CRO и консультантами по вопросам регулирования укрепляет перспективы роста.
Региональный анализ рынка аутсорсинга в сфере регулирования медицинских изделий в Северной Америке.
- Прогнозируется, что рынок аутсорсинга услуг по регулированию медицинских изделий в Северной Америке будет стабильно расти в течение прогнозируемого периода благодаря укреплению нормативно-правовой базы, увеличению числа одобрений медицинских изделий и расширению инфраструктуры здравоохранения в регионе.
- Правительства все чаще уделяют особое внимание соблюдению нормативных требований, регистрации продукции и послепродажному надзору для обеспечения безопасности пациентов и стандартов качества. В результате производители медицинских изделий все чаще передают функции по регулированию на аутсорсинг специализированным компаниям, чтобы эффективно справляться со сложными и постоянно меняющимися нормативными требованиями.
- Растущие инвестиции в модернизацию здравоохранения в сочетании с расширением внедрения передовых медицинских технологий еще больше увеличивают спрос на услуги аутсорсинга в сфере регулирования в Северной Америке.
Анализ рынка аутсорсинга услуг по регулированию медицинских изделий в США.
Рынок аутсорсинга услуг по регулированию медицинских изделий в США доминировал на этом рынке, занимая примерно 42,5% региональной выручки в 2025 году . Это доминирование в первую очередь обусловлено хорошо развитой экосистемой здравоохранения и медицинских изделий, строгим регуляторным надзором со стороны FDA, большим объемом медицинских процедур и наличием ведущих консалтинговых фирм в области регулирования. Акцент страны на соблюдении нормативных требований, своевременном получении разрешений и надежных процессах авторизации на рынке значительно повысил спрос на специализированные услуги аутсорсинга.
Анализ рынка аутсорсинга услуг по регулированию медицинских изделий в Канаде.
Ожидается, что
рынок аутсорсинга услуг по регулированию медицинских изделий в Канаде продемонстрирует самый быстрый рост в Северной Америке, с прогнозируемым среднегодовым темпом роста около 10,1% в течение прогнозируемого периода. Этот рост поддерживается быстрой модернизацией здравоохранения, растущим присутствием международных производителей медицинских изделий и развивающейся нормативно-правовой базой Министерства здравоохранения Канады. Растущая осведомленность об эффективных решениях по аутсорсингу и упрощенных процессах регулирования еще больше способствует расширению рынка по всей стране.
Доля рынка аутсорсинга услуг по регулированию медицинских изделий в Северной Америке
В отрасли аутсорсинга услуг по регулированию медицинских изделий лидируют преимущественно хорошо зарекомендовавшие себя компании, в том числе:
- Компания Accell Clinical Research, LLC (США)
- Genpact (США)
- CRITERIUM, INC. (США)
- Promedica International (США)
- WuXiAppTec (Китай)
- Medpace (США)
- PPD Inc. (США)
- Лаборатории Чарльз-Ривер (США)
- ICON plc (США)
- Covance (США)
- Parexel International Corporation (США)
- Фрейр
- Navitas Clinical Research, Inc. (США)
- Меделис, Инк. (США)
- Sciformix (США)
- Тех Таммина (США)
- Компания Acorn Regulatory Consultancy Services Ltd. (Ирландия)
- BIOMAPAS (Литва)
- Специалисты по регулированию (Австралия)
- CompareNetworks, Inc. (США)
Последние тенденции на рынке аутсорсинга в сфере регулирования медицинских изделий в Северной Америке.
- In January 2023, Medistri SA, a Switzerland‑based medtech service provider, introduced an integrated regulatory affairs and quality management consulting solution tailored for small and mid‑sized medical device manufacturers. This offering simplified pathways to compliance by providing cost‑effective support for CE marking, technical file preparation, and post‑market surveillance, addressing a key need for companies lacking full in‑house regulatory teams
- In March 2023, ICON plc launched a new Regulatory Intelligence platform designed to assist medical device companies in tracking evolving global regulations, managing submission strategies, and accessing compliance templates. The platform was aimed at improving regulatory strategy and operational efficiency for complex multi‑jurisdictional filings
- In March 2023, Freyr Solutions opened a new global regulatory services hub in the Asia‑Pacific region, expanding its capacity to support medical device companies with end‑to‑end compliance for country‑specific approvals. This enhanced regional service offering highlighted the rapid growth of regulatory outsourcing demand in emerging markets
- In April 2023, Parexel International Corporation expanded its global regulatory consulting services to better support medical device and combination product developers grappling with the increasingly complex requirements under the EU Medical Device Regulation (MDR) and In Vitro Diagnostic Regulation (IVDR). This strategic enhancement reflected heightened industry demand for specialized MDR/IVDR expertise
- In March 2024, Emergo by UL established a new regulatory consulting center in Singapore focused on serving the growing Asia‑Pacific medical device market, particularly supporting ASEAN regulatory harmonization initiatives and multi‑country approvals. This move underscored strong geographic expansion in outsourced regulatory services
- In July 2024, Parexel International launched its Digital Regulatory Platform, integrating artificial intelligence and machine learning to streamline medical device regulatory submissions, provide cloud‑based document management, and improve collaboration between sponsors and regulators
- In September 2024, IQVIA expanded its regulatory affairs capabilities through the acquisition of Pharm‑Olam’s regulatory consulting division, bolstering its global medical device regulatory expertise and enhancing services across Asia‑Pacific and Latin America—especially for emerging market regulatory strategies
- In January 2025, ProPharma Group partnered with MedTech Europe to develop specialized regulatory training programs for medical device regulatory professionals, addressing critical skills gaps following implementation of more stringent regulatory frameworks such as MDR
- В феврале 2025 года компания IQVIA объявила о стратегическом партнерстве с европейским производителем медицинских изделий для поддержки подготовки регуляторных досье и отчетности по клиническим оценкам в соответствии с Регламентом ЕС о медицинских изделиях (EU MDR), что еще больше укрепило зависимость отрасли от привлечения сторонних экспертов для подготовки сложной документации по соблюдению нормативных требований.
- В марте 2025 года анализ рынка показал, что компания ICON plc расширила свои услуги по аутсорсингу в сфере регулирования в Азиатско-Тихоокеанском регионе, отвечая на растущий локальный спрос на консультации по вопросам регулирования и поддержку клинических испытаний на быстрорастущих рынках, таких как Китай и Индия.
SKU-
Получите онлайн-доступ к отчету на первой в мире облачной платформе рыночной аналитики
- Интерактивная панель анализа данных
- Панель анализа компании для возможностей с высоким потенциалом роста
- Доступ аналитика-исследователя для настройки и запросов
- Анализ конкурентов с помощью интерактивной панели
- Последние новости, обновления и анализ тенденций
- Используйте возможности сравнительного анализа для комплексного отслеживания конкурентов
Методология исследования
Сбор данных и анализ базового года выполняются с использованием модулей сбора данных с большими размерами выборки. Этап включает получение рыночной информации или связанных данных из различных источников и стратегий. Он включает изучение и планирование всех данных, полученных из прошлого заранее. Он также охватывает изучение несоответствий информации, наблюдаемых в различных источниках информации. Рыночные данные анализируются и оцениваются с использованием статистических и последовательных моделей рынка. Кроме того, анализ доли рынка и анализ ключевых тенденций являются основными факторами успеха в отчете о рынке. Чтобы узнать больше, пожалуйста, запросите звонок аналитика или оставьте свой запрос.
Ключевой методологией исследования, используемой исследовательской группой DBMR, является триангуляция данных, которая включает в себя интеллектуальный анализ данных, анализ влияния переменных данных на рынок и первичную (отраслевую экспертную) проверку. Модели данных включают сетку позиционирования поставщиков, анализ временной линии рынка, обзор рынка и руководство, сетку позиционирования компании, патентный анализ, анализ цен, анализ доли рынка компании, стандарты измерения, глобальный и региональный анализ и анализ доли поставщика. Чтобы узнать больше о методологии исследования, отправьте запрос, чтобы поговорить с нашими отраслевыми экспертами.
Доступна настройка
Data Bridge Market Research является лидером в области передовых формативных исследований. Мы гордимся тем, что предоставляем нашим существующим и новым клиентам данные и анализ, которые соответствуют и подходят их целям. Отчет можно настроить, включив в него анализ ценовых тенденций целевых брендов, понимание рынка для дополнительных стран (запросите список стран), данные о результатах клинических испытаний, обзор литературы, обновленный анализ рынка и продуктовой базы. Анализ рынка целевых конкурентов можно проанализировать от анализа на основе технологий до стратегий портфеля рынка. Мы можем добавить столько конкурентов, о которых вам нужны данные в нужном вам формате и стиле данных. Наша команда аналитиков также может предоставить вам данные в сырых файлах Excel, сводных таблицах (книга фактов) или помочь вам в создании презентаций из наборов данных, доступных в отчете.