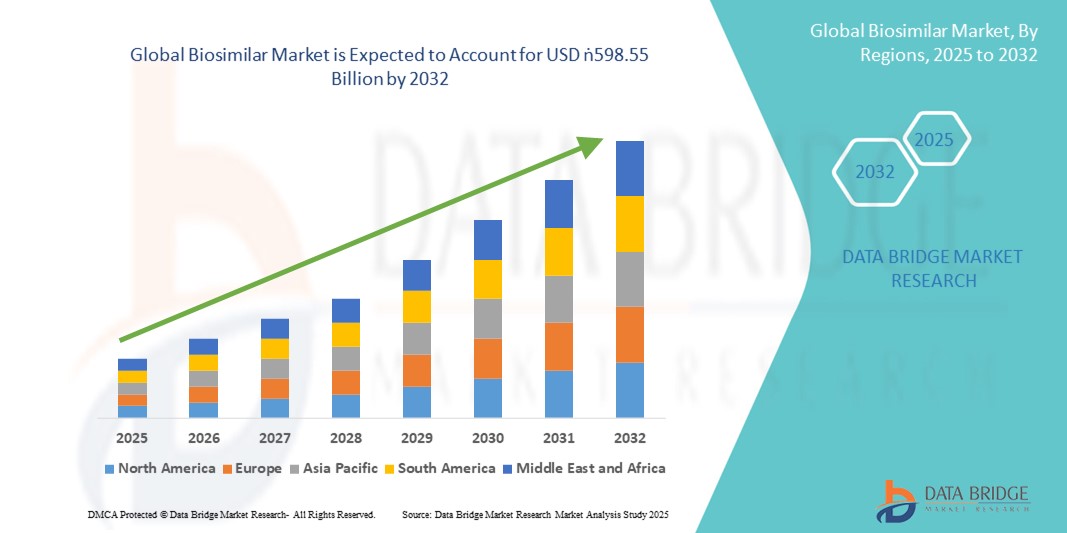
Global Biosimilar Market
市场规模(十亿美元)
CAGR :
% 
 USD
64.93 Billion
USD
598.55 Billion
2024
2032
USD
64.93 Billion
USD
598.55 Billion
2024
2032
| 2025 –2032 | |
| USD 64.93 Billion | |
| USD 598.55 Billion | |
|
|
|
|
全球生物同位素市场分化,按产品类型(磁共振成像扫描器、计算成像仪扫描器、位置射线成像仪扫描器、生物同位素(EEG)、电学装置、磁共振装置、外向多普勒装置、外向多普勒压力监测器、电极、传感器和地格和电缆)、药物类(胰岛素、再生人生长激素(RHGH)、外向分泌物-刺激因子、间向分泌物、肾上腺素、肾上腺素、肾上腺素、抗体、Follitopropopropin、Glucagon、Calcitonin、Teriparatoparin Sodium)、制造型(室内制造和合同制造)、程序(内向和外向分泌物、程序、非内向分泌物)、疾病(分泌物、脱氧和肾上腺素)、抗体抗体抗体抗体抗体抗体抗体抗体抗体抗体抗体抗体抗体抗体抗体抗体抗体抗体抗体抗体抗体抗
生物类似市场大小
- 全球生物类似市场规模价值2024年649.3亿美元并可望达到5.9855亿美元, 以美元计CAGR为32.00%.预测期间
- 市场扩张的主要动力是:封锁生物学的专利流出日益增多,癌症、自体免疫障碍和糖尿病等慢性疾病的发病率上升,这些都刺激了对成本效益高的替代品的需求。
- 此外,有利的监管框架、增加制药公司的投资和增加保健提供者的接受程度,正在加速全世界生物同物的开发和采用。 这些趋势极大地促进了生物类似工业的强劲增长轨迹。
生物类似市场分析
- 生物同位素被设计成与核准的生物类药物高度相似并具有成本效益的替代品,正在成为全球保健系统的一个关键部分,因为这些药物能够提高治疗的可获性,降低保健费用并拓宽慢性和危及生命的疾病,如癌症、自体免疫障碍和糖尿病的患者范围。
- 对生物同质物需求的增加主要由块块生物学的专利到期浪潮、保健支出压力的加大以及提供者和病人对生物同质物作为安全有效的治疗选择的接受程度的提高所推动。
- 北美主宰了全球生物类似市场,2024年收入份额最大,为42.8%,美国FDA提供强有力的监管支持,生物类似物越来越多地进入高价值的治疗类别,寻找昂贵的生物学替代物的支付者也加大了采纳力度. 特别是由于有利的政策转变、竞争性定价以及主要制药公司的存在,美国经历了迅速的市场渗透。
- 由于扩大保健基础设施、慢性疾病发病率上升以及中国、印度和韩国等国政府采取支持性举措,预计亚太区域在预测期内将成为生物市场增长最快的区域。
- 肿瘤部分在2024年占了生物相似市场42.2%的收入份额,其驱动力是参考生物学成本高,全球癌症发病率不断上升,以及生物相似单克隆抗体和辅助疗法的迅速接受。
范围和类似生物市场分割报告
| 属性 | 生物类似关键市场观察 |
| 覆盖部分 |
|
| 涵盖国家 | 北美
欧洲
亚太
中东和非洲
南美洲
|
| 关键市场玩家 |
|
| 市场机会 |
|
| 添加数据信息集的值 | 除了对市场价值、增长率、分块化、地域覆盖和主要参与者等市场假设的见解之外,数据桥市场研究所编写的市场报告还包括深入的专家分析、定价分析、品牌份额分析、消费者调查、人口分析、供应链分析、价值链分析、原材料/可消耗品概览、供应商选择标准、PESTLE分析、波特分析以及监管框架。 |
类似生物市场趋势
通过优惠条例和节省费用扩大无障碍环境
- 全球生物类似市场的一个重要而正在加速的趋势是扩大监管支持和政策框架,鼓励更快地批准和更广泛地采用生物类似物作为高价生物学的成本效益替代品。 这正在改变不同治疗领域治疗的可负担性和患者可获得性
- 例如,2023年,美国FDA发布了新的可互换性指南,以简化生物同物进入市场的程序,而欧洲药品署(EMA)继续以全世界生物同物批准数量最多为首。 这些措施加强了行业信心并推动了竞争性市场进入
- 越来越多的保健费用压力迫使付款者和政府优先采用类似生物方法。 例如,在美国,与Humira相似的Amgen's Amjevita在2023年以比AbbVie的参考生物学低得多的成本进入市场,为扩大吸收创造了先例。 同样地,Biocon和Viatris也在亚太地区以无障碍价格点积极推出肿瘤学和糖尿病生物同位素。
- 医师信心的提高加强了这一趋势,因为更现实的证据表明,生物类似物可提供与原生生物相似的安全和功效。 广泛的医生和病人教育运动正在进一步加快在肿瘤学、自体免疫疾病和糖尿病等治疗领域的收养
- 此外,全球药厂公司和区域行为者之间的伙伴关系正在促进具有成本效益的发展和分销。 例如,三星Bioepis通过与Organon和Biogen的合作,扩大了其覆盖范围,以加强其在免疫学和眼科方面的生物同质组合
- 这种向类似生物的采用推进的监管和经济压力从根本上改变了全球生物学市场,发达和新兴经济体的需求迅速上升,因为利益攸关方越来越优先考虑节约成本和获得治疗。
生物类似市场动态
驱动程序
生物专利过期和慢性疾病负担引起的需求增加
- 生物同类需求激增主要是由于胡米拉、赫鲁平和阿瓦斯丁等块块生物学专利专有权的丧失,为低成本生物类似物创造机会,以获取巨大的市场份额。
- 例如,2023年美国从Amgen、Boehringer Ingelheim和Sandoz等公司推出多种Humira生物同位素,从而形成竞争性定价环境并拓宽患者接触范围。
- 癌症、自体免疫障碍和糖尿病等慢性病的全球负担日益加重,更加需要负担得起的生物疗法,将生物同物定位为保健系统可持续性的关键
- 政府和保险商越来越多地实施补偿奖励和替代政策,以鼓励生物同类吸收,为制造商创造一个有利的环境
- 医生和病人对生物同源物的功效和安全等同的认识得到保健当局不断开展的教育举措的支持,这进一步加强了收养工作
限制/挑战
互换性障碍和制造复杂性
- 尽管增长前景强劲,但围绕可互换性和监管复杂性的挑战继续限制广泛采用。 在美国,可互换性指定仍然是一个关键障碍,因为并非所有生物相似物都获得药店一级的自动替代权。
- 例如,当Amgen的Amjevita进入美国市场时,它最初并不具有可互换性地位,与传统通用产品相比,替代速度放慢。 这对试图迅速获得牵引力的新生来说仍然是一项挑战
- 生物同型制造也带来了高技术壁垒,因为生物学是需要先进生产和质量控制系统的大型复杂分子. 生产工艺的任何变化都会引起监管问题并延误批准
- 此外,由于对生物效能和安全的误解依然存在,某些地区的医生仍然不情愿和病人犹豫不决。 持续教育和现实世界数据对克服这些观念至关重要
- 激烈竞争导致的价格下跌是另一项挑战,因为公司在管理高额开发和生产费用的同时面临降低成本的压力。 这可以限制小玩家进入市场的盈利能力
- 通过更明确的监管途径、提高制造能力和加强利益攸关方教育来克服这些障碍,对于生物部门实现持续增长至关重要。
生物类似市场范围
市场按产品类型、毒品类别、制造类型、程序、疾病、指示、治疗类型和最终用户划分。
- 按产品类型
根据产品类型,生物同型市场被分割成磁共振成像扫描仪、计算成的成像扫描仪、正体排放成像扫描仪、生物同型(EEG)、电磁学装置、磁脑平面学装置、转动多普勒装置、颅内压力监测器、电极、传感器、凝胶和电缆。 磁共振成像扫描仪部分在2024年占据了市场主导地位,收入份额最大,其驱动力在于其在肿瘤学和神经学中对于高分辨率成像和疾病监测的关键作用. 对核磁共振的需求由于广泛用于检测肿瘤、关节紊乱和心血管疾病而进一步加剧,这与慢性病发病率的上升是一致的。 医院和诊断中心更喜欢以核磁共振为基础的生物同位素,因为它们具有可靠性、安全性并增强了诊断准确性。 此外,发达市场的优惠补偿政策支持在临床环境中更多地采用核磁共振技术。
由于各种诊断程序广泛使用电极,预计电极部分在2025-2032年期间增长最快。 它们的可负担性、可处置性以及神经和心脏病学需求的增加使它们在成本效益至关重要的新兴市场具有很高的吸引力。 快速城市化和需要EEG和EMG监测的病人人数不断增加,也推动了收养。 此外,护理点诊断和便携式监测装置的趋势正在扩大使用这些消耗品。 该部分的成长也得到了材料科学进步的支持,这些进步提高了电极敏感性和病人的舒适度.
- 按毒品类别
以药物类为基础,生物同型市场被分化为胰岛素,再生人生长激素(RHGH),颗粒细胞聚-刺激因子(G-CSF),干涉素,红霉素,异能素,单克隆抗体,活体素,克卢卡贡,克罗西通宁,三硝基丙二酸酯和克罗西帕林钠. 单克隆抗体部分由于在肿瘤学,免疫学和自体免疫障碍中至关重要,于2024年主导了市场. 块状单克隆抗体药物的专利过期,加之治疗成本高,为生物同型发展创造了强大的动力. 这些生物学被广泛用于治疗癌症,风湿性关节炎和炎症性肠道疾病,使得它们成为生物相仿制造商的最高选择. 这一部分还得益于鼓励更快批准和临床接受的监管途径。
2025年至2032年,由于全球糖尿病发病率不断上升,胰岛素部分预计将增长最快。 全球,特别是亚太区域的糖尿病患者人数不断增加,正在产生对负担得起的胰岛素替代品的强烈需求。 一些胰岛素生物同位素获得了监管认可,加快了市场渗透. 各国政府和保健系统正在积极推广同胰岛素生物同位素,以降低治疗费用并增加患者的可获得性。 此外,改进的制造技术和制药公司之间的伙伴关系正在促进更多的供应。
- 按制造业类型
以制造类型为基础,将生物同型市场分入内部制造和合同制造. 内部制造部门在2024年主导了市场,因为主要制药公司保持对生产的控制,以确保质量和遵守严格的生物类似条例。 拥有内部设施使企业能够管理知识产权,控制供应链物流,长期优化生产成本. 它还确保产品质量一致,这对于获得医生和病人对生物相似物的信任至关重要。 拥有既定生物学基础设施的大型制药公司继续严重依赖内部系统来维护竞争优势。
由于中小型生物同类开发商的外包趋势增加,预计合同制造部门在预测期间增长最快。 合同制造组织提供专门知识、可扩展性和成本效益,使新的参与者能够更快地进入市场。 生物类似物的管道不断增长,加上新兴市场的研发活动不断增加,正在推动对外包伙伴关系的需求。 此外,化管组织正在扩大能力,建立先进的生物反应系统和符合监管要求的设施,以满足全球客户的需要。 制药公司和CMO之间的战略合作进一步推动了这一部门的增长轨迹。
- 根据程序
根据程序,生物同型市场被分割成入侵和非入侵. 非入侵部分在2024年占据了市场主导地位,收入份额最大,原因是病人越来越倾向于减少痛苦、更安全和更方便的治疗选择。 非侵入性方法被广泛用于肿瘤学和慢性病管理中,患者遵守规定至关重要. 由于并发症风险降低,住院时间缩短,治疗费用降低,监管机构和医院也倾向于非侵入性治疗。 先进成像、诊断生物同位素和定向疗法的兴起进一步巩固了这一类的主导地位。
2025-2032年期间,由于对心血管和神经紊乱等复杂疾病进行精确干预的需求日益增加,入侵部分预计将出现最快的增长率。 在需要直接提供生物记录的高级手术和定向疗法中,入侵生物相似性至关重要。 需要外科手术的重要护理病人人数不断增加,这助长了收养。 此外,最低侵入性外科技术的进步正在改善安全情况,从而获得更广泛的接受。 在发展中国家,保健基础设施投资的增加也支持了该部门的增长。
- 按疾病分列
基于疾病,生物相似市场被分化为中风,痴呆和癫痫. 2024年中风分会占据了市场主导地位,收入份额最高,主要原因是全球缺血和出血性中风的发生率不断上升. 生物类似物在提高中风后护理中使用的先进疗法的可负担性方面发挥关键作用。 医院和康复中心越来越依赖生物同种疗法来管理恢复结果并减轻病人的经济负担。 政府旨在增加获得负担得起的中风治疗机会的倡议进一步加强了这一阶层的主导地位。
由于全球人口迅速老化,阿尔茨海默症和相关疾病发病率不断上升,痴呆症部分预计将在2025年至2032年期间增长最快。 由于保健系统承受着管理痴呆症护理费用上升的压力,生物相似性为长期治疗提供了成本效益高的替代办法。 制药公司正积极开发单克隆抗体生物同位素,针对的是与痴呆有关的β-酰胺和陶蛋白. 此外,早期诊断工具与生物同型疗法相结合,正在扩大临床应用。 该部分的增长得到针对神经退化性疾病的政策倡议和研究资金的进一步支持。
- 通过指示
根据指示,生物相仿的市场被分割成一个地心分化缺陷(ASD),心心分化缺陷(VSD),专利 foramen ovale(PFO),主动阀定质等. 由于心血管病的流行程度高并需要负担得起的生物学干预,主动脉瓣激素分会于2024年主导了市场. 生物类似物有助于减少阀门替换和相关疗法的总体成本负担,使治疗更容易获得。 发达经济体和新兴经济体的日益采用正在加强这种支配地位。 医院也倾向于采用类似生物的干预措施,因为事实证明,在大量病人中,这种干预措施是有效的,可以节省费用。
由于婴儿和儿童的先天性心脏病发病率上升,预计2025-2032年期间,口腔静脉功能缺陷部分将以最快的速度增长。 生物同位素由于价格可承受和可获取性而日益被纳入处理协议. 新兴经济体的儿科心脏护理的改善和保健支出的增长正在加速采用。 此外,生物同类开发者与儿科医院之间加强合作有助于扩大治疗渠道。 围绕先天性心脏疾病开展的提高认识的运动也促进了这种增长。
- 按治疗类型
根据治疗类型,生物同型市场被分化为肿瘤学,免疫学,血液学,激素疗法,代谢失调等. 肿瘤部分在2024年占据了市场主导地位,收入份额最大,为42.2%,在癌症治疗中广泛使用单克隆抗体生物类似物为支撑. 全球癌症负担日益加重,加上有品牌的生物学成本高,正在推动生物相似的接受。 管理机构将肿瘤生物相似性的审批途径列为优先事项,使患者能够更快地获得治疗。 医院和癌症中心正在迅速将生物类似物纳入治疗规程,以提高可负担性和获得治疗的机会。 肿瘤生物类似物的不断增长进一步强化了这一部分的强大市场地位。
2025-2032年,由于风湿性关节炎、发作和发作性肠道疾病等自发性免疫疾病的发病率上升,免疫学部分预计将增长最快。 生物类似物为TNF抑制剂和IL靶向疗法等昂贵的生物学提供了成本效益高的替代品. 推动免疫学替代的辅助性监管框架进一步推动了这一部分。 患者对长期和负担得起的治疗方案的需求也支持快速吸收。 有了强有力的临床数据验证疗效,免疫学生物同位素正在被医生广泛接受.
- 按终端用户
在最终用户的基础上,生物市场被分割成医院、诊所、诊断中心等。 医院部分在2024年占据了市场主导地位,因为它们是管理肿瘤学、心脏病学和神经学的生物类似疗法的主要中心。 医院受益于大宗购买力,并与生物同类制造商建立了伙伴关系,使它们能够大幅降低治疗费用。 政府资助的医院方案和保险报销政策进一步促进了在这种环境下的类似生物收养。 此外,医院为安全处理复杂的生物学提供必要的基础设施和专门知识。
由于门诊护理的上升趋势以及慢性病管理专科诊所的扩大,预计诊所部分在2025年至2032年期间增长最快。 诊所越来越多地采用生物同位素,因为它们的成本较低,容易融入常规治疗规程。 病人更喜欢诊所提供方便、更短的等候时间和个性化的护理方法。 此外,诊所在扩大郊区和农村地区类似生物接触方面发挥着重要作用。 类似生物开发者与诊所网络之间的伙伴关系正在进一步推动收养。
生物类似市场区域分析
- 北美在全球生物同类市场占据了主导地位,2024年收入份额最大,为42.8%,由美国FDA的有力监管支持所带动,生物同类产品越来越多地进入高价值治疗类别,以及寻找昂贵生物记录学可负担得起的替代品的付款人被更多采纳.
- 该区域的既定管理框架,特别是林业发展局的生物类似批准途径,鼓励了强有力的市场进入,并促进了制药厂商的创新。
- 高保健支出、先进的保健基础设施和强有力的保险范围进一步支持迅速吸收生物同物作为品牌生物学的可负担得起的替代品
美国的生物市场透视
美国的生物类似市场在2024年收获了北美最大的83%的收入份额,这是由于对具有成本效益的生物学替代品的强烈需求以及肿瘤学和免疫学中治疗应用的迅速扩展所推动的. 医生和病人越来越多地采用生物同位素,因为这些生物同位素已证明是安全和有效的,而且与品牌生物学相比,它们节省了大量费用。 林业发展局提供的有利的监管支持以及保险商日益接受,正在加快医院和专科诊所的渗透。 此外,主要制药公司的进入和扩大报销范围,极大地促进了市场增长。
欧洲生物市场观察
在整个预测期间,欧洲生物类似市场预计将在相当规模的CAGR扩展,其动力是各种既定的监管途径和关键治疗类别的早期采用。 德国、法国和英国等国家在生物利用方面处于领先地位,因为政府采取了强有力的举措减少保健开支。 慢性病发病率的上升,加上对负担得起的治疗的推动,正在促进肿瘤学、内分泌学和风湿病学的吸收。 医生信心的增强和竞争性定价战略也正在推动生物类似地渗透到医院和零售药店渠道。
英国生物市场观察
预计在预测期间,英国的生物同类市场将在一个值得注意的CAGR上增长,并辅之以积极促进生物同类的采纳的有利的NHS政策。 由于费用压力和病人获得治疗的必要性,保健提供者越来越多地转向肿瘤学、免疫学和代谢失调方面的生物相似性。 开处方者和病人日益接受,加上竞争性招标和降低价格,预计将加快市场渗透。 此外,NHS和生物类似制造商之间的合作正在增强信心并促使进一步采用。
德国 生物市场观察
在预测期间,由于德国作为欧洲最早采用生物同物的国家之一的地位,德国的生物同物市场预计将在相当大的CAGR扩展。 强有力的保健政策鼓励替代,加上竞争性定价,使德国成为跨治疗领域生物相似渗透的领先者。 强调降低保健费用并增加获得生物记录学的机会,有助于肿瘤学和自发免疫疾病的快速感染。 此外,地方创新、提高医生认识方案和结构化偿还框架正在加强市场的增长。
亚太生物市场观察
在2025至2032年的预测期间,由于慢性疾病负担不断加重,医疗基础设施不断扩大,以及中国、日本和印度等国的生物同质物的承受能力不断提高,亚太生物同质市场有望以25%的速度增长。 有利的政府举措,加上当地制造能力,正在使更多的病人更容易获得类似生物物质。 此外,国内和国际行为者之间的战略合作正在促进创新和确保监管批准。 该地区的中产阶级人口正在扩大,保健投资也在增加,这进一步加速了生物相似的采用。
日本生物市场观察
由于政府大力支持、人口老化需求、癌症和自发性免疫疾病的发病率不断上升,日本的生物同类市场正在形成势头。 日本的监管机构简化了审批途径,增加了跨治疗地区生物同位素的供应. 医院和专科诊所的收养日益增多,加上医生的信任度不断提高,正在刺激需求。 此外,该国先进的保健基础设施和对控制费用的重视正在鼓励更广泛的市场吸收。 日本同全球生物制药公司之间的伙伴关系进一步支持了市场的扩大。
印度生物市场观察
印度的生物类似市场在2024年占了亚太地区最大的市场收入份额,国内制造业生态系统强劲,对负担得起的生物学的需求不断增加。 印度已成为全球生物类似发展和生产中心,供应国内和国际市场。 糖尿病、癌症和自发性免疫疾病病例的增加正在推动整个治疗领域的收养。 此外,政府为促进获得保健服务而采取的举措,以及当地主要行动者的存在,正在推动强有力的生物渗透。 竞争性定价战略和医生信心的提高正在进一步推动市场增长。
类似生物市场份额
生物产业主要由历史悠久的公司领导,其中包括:
- 诺华公司(瑞士)
- 猎户座制药公司(瑞典)
- 辉瑞股份有限公司(美国)
- 三星活佛(韩国)
- Coherus生物科学公司(美国)
- 阿姆根股份有限公司(美国)
- Lilly USA, LLC (美国).
- 武田制药有限公司(日本)
- 布里斯托-迈尔斯·斯奎布公司(美国)
- 默克·克加阿(德国)
- 特瓦制药工业有限公司(美国)
- Biocon(印度)
- 拜耳公司(德国)
- AbbVie Inc. (美国).
- Reddy博士实验室有限公司(印度)
- Boehringer Ingelheim国际有限公司(德国)
- Biogen (美国).
全球生物市场的最新发展是什么?
- 2025年5月,FDA批准Starjemza(ustekinumab-hmny)为斯泰拉拉(ustekinumab)的第八生物同体,为患者提供风湿和胃肠病的强化治疗方案. 这一批准突出显示了ustekinumab生物类的继续扩展,并支持更多地获得这些疗法。
- 2025年2月,FDA指定与Stelara(ustekinumab)生物相似的Selarsdi为可互换. 这意味着药剂师可以代之以斯泰拉拉,而无需处方干预 一旦专有期结束,大大简化了患者的获取和收养
- 2025年2月,FDA批准了Merilog(胰岛素-aspart-szjj),这是与诺沃洛克(胰岛素为分)最早的快速活化的胰岛素生物同型活化(胰岛素为分型),既有预填笔版,也有小瓶版. 这是扩大糖尿病患者负担得起的胰岛素选择的一个里程碑。
- 2024年12月,FDA批准Steqeyma(英语:ustekinumab-stba)为与Stelara(英语:ustekinumab)的第七生物相似物,使得在自体免疫和炎症护理方面有更多的竞争和扩大治疗选择.
- 2024年10月,Agree BioPharma, Inc.宣布FDA批准Imuldosa(ustekinumab-srlf),这是与Stelara(ustekinumab)相似的生物,用于所有相同的慢性炎症症状——包括发作、发作性关节炎、克罗恩病和溃疡性结肠炎。
SKU-
研究方法
数据收集和基准年分析是使用具有大样本量的数据收集模块完成的。该阶段包括通过各种来源和策略获取市场信息或相关数据。它包括提前检查和规划从过去获得的所有数据。它同样包括检查不同信息源中出现的信息不一致。使用市场统计和连贯模型分析和估计市场数据。此外,市场份额分析和关键趋势分析是市场报告中的主要成功因素。要了解更多信息,请请求分析师致电或下拉您的询问。
DBMR 研究团队使用的关键研究方法是数据三角测量,其中包括数据挖掘、数据变量对市场影响的分析和主要(行业专家)验证。数据模型包括供应商定位网格、市场时间线分析、市场概览和指南、公司定位网格、专利分析、定价分析、公司市场份额分析、测量标准、全球与区域和供应商份额分析。要了解有关研究方法的更多信息,请向我们的行业专家咨询。
可定制
Data Bridge Market Research 是高级形成性研究领域的领导者。我们为向现有和新客户提供符合其目标的数据和分析而感到自豪。报告可定制,包括目标品牌的价格趋势分析、了解其他国家的市场(索取国家列表)、临床试验结果数据、文献综述、翻新市场和产品基础分析。目标竞争对手的市场分析可以从基于技术的分析到市场组合策略进行分析。我们可以按照您所需的格式和数据样式添加您需要的任意数量的竞争对手数据。我们的分析师团队还可以为您提供原始 Excel 文件数据透视表(事实手册)中的数据,或者可以帮助您根据报告中的数据集创建演示文稿。