Global Rare Disease Api Orphan Drug Substance Market
市场规模(十亿美元)
CAGR :
% 
 USD
306.90 Million
USD
667.49 Million
2025
2033
USD
306.90 Million
USD
667.49 Million
2025
2033
| 2026 –2033 | |
| USD 306.90 Million | |
| USD 667.49 Million | |
|
|
|
|
全球稀有疾病API/孤儿药物市场分化,由API/药物类型(生物活化物APIs,小分子活化物APIs,活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活性活 2033年工业趋势和预测
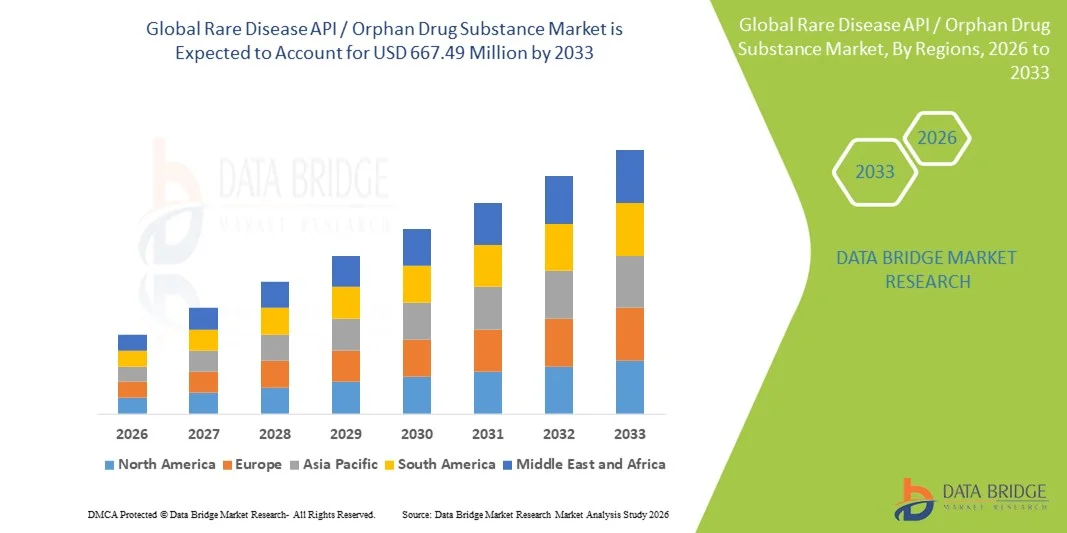
罕见疾病 API/孤儿药物市场规模
- 全球罕见疾病API/无主药物市场规模价值2025年3.0690亿美元并可望达到截至2033年的66,749万美元, 以美元计CAGR为10.20%预测期间
- 市场增长主要受稀有疾病发病率不断上升,孤儿药物管线不断扩大等推动,监管激励措施不断增强,鼓励为稀有和超稀有情况开发和制造专用活性药物成分.
- 此外,生物学方面的投资不断增加,基因疗法以及其他先进模式,加上需要高质量、小批量和强效药物,正在建立孤儿API,作为现代制药发展的重要组成部分。 这些趋同因素正在加速对罕见疾病API的需求,从而大大地推动了该行业的增长.
罕见疾病 API/孤儿药物市场分析
- 罕见疾病API和由治疗稀有和超罕见病症的高度专业活性药物成分组成的孤儿药物,由于它们在多种治疗领域促进有针对性、精确和救生疗法的作用,对现代药物发展越来越重要
- 对稀有疾病API的需求不断增长,主要由稀有疾病日益普遍,孤儿药物管道不断扩大,监管性鼓励措施,以及对生物学、基因疗法和基于RNA的治疗等先进模式增加投资所驱动.
- 北美主导了罕见疾病API/无主药物市场,2025年收入份额最大,为41.5%,辅以强有力的无主药物监管框架、高额研发支出和强有力的存在。生物药品美国在临床阶段和商业规模的孤儿API制造方面都取得了显著增长
- 在预测期间,亚太预计将是罕见疾病API市场中增长最快的区域,其驱动力是增加API制造业的外包、扩大生物技术生态系统、改善监管协调以及增加对中国、日本、韩国和印度罕见疾病药物开发的投资。
- 2025年,由于在酶替代疗法中广泛使用,生物活化剂占了罕见疾病API/孤儿药物市场的58.3%的市场份额,单克隆抗体和基于基因的治疗及其在处理复杂的遗传和代谢罕见疾病方面的强效性
范围和罕见疾病报告 API/孤儿药物市场分割
| 属性 | 罕见疾病 API / 孤儿药物 |
| 覆盖部分 |
|
| 涵盖国家 | 北美
欧洲
亚太
中东和非洲
南美洲
|
| 关键市场玩家 |
|
| 市场机会 |
|
| 添加数据信息集的值 | 除了对市场价值、增长率、分块化、地域覆盖和主要参与者等市场假设的深刻见解外,数据桥市场研究编写的市场报告还包括深入的专家分析、病人流行病学、管道分析、定价分析和监管框架。 |
罕见疾病 API/孤儿药物市场趋势
转向先进生物和遗传药物
- 全球稀有疾病API/无主药物市场的一个显著而加速的趋势是,由于生物药物能够高精度地针对罕见和超罕见疾病的基本遗传原因,向生物学、基因疗法和基于RNA的药物转移。
- 例如,针对稀有病症的基因和细胞疗法的监管批准越来越多,这增加了对病毒病媒API、重组蛋白和高度专业化的生物药物的需求,这些药物是根据严格的质量标准制造的
- 分子生物学,基因组学和伴生诊断学的进步,使高针对性的无主药物得到开发,使制造商能够设计出适合特定突变或疾病路径的API,从而提高治疗效果和病人结果.
- 日益采用精密医学方法,正鼓励制药公司投资生产复杂,数量少,价值高的API,需要专门设施,具备先进的分析能力,严格规范合规.
- 基于平台的制造技术的兴起支持了孤儿API的灵活而可扩展的生产,使制造商能够高效地同时处理多种罕见疾病程序.
- 这种更为复杂和定制的无主药物的趋势正在改变API的制造战略,更加重视小批量生产、高强度处理和快速转变能力。
- 因此,Lonza和Catalent等公司正在扩大其生物学和基因疗法API能力,以支持对多种罕见疾病症状的先进无主药物的需求不断增长。
罕见疾病 API/孤儿药物市场动态
驱动程序
扩大孤儿药物管道和有利的监管奖励
- 越来越多的无主药物指定和批准得到有利的监管奖励措施的支持,如市场专有、税收减免和加快审查途径,是刺激罕见疾病API需求的一个关键驱动因素
- 例如,美国、欧洲和日本的监管框架大大缩短了孤儿药物的开发时限,鼓励生物制药公司扩大其罕见疾病管道,并投资于专门的API制造。
- 随着全球罕见疾病的认识、筛查和诊断率的提高,对持续和高质量药物供应的需求正在增加,直接支持孤儿API市场的增长。
- 此外,为罕见疾病研究提供强大的风险资本和公共资金,使小型生物技术公司能够推进临床方案,日益依赖外包的API制造和专门的CDMO
- 由于竞争有限,越来越注重精确和个性化疗法,加上长期商业潜力,继续推动对无主药物的持续需求
- 增加政府和非政府对罕见疾病治疗发展的支持,正在加强无主药物制造投资的长期活力。
- 孤儿药物控制溢价的能力正在提高投资收益,进一步鼓励继续扩大孤儿API生产能力
限制/挑战
制造业的复杂性和监管合规障碍
- 罕见病API的生产往往涉及复杂的制造工艺,严格的质量要求,以及有限的批量尺寸,这可以大大提高生产成本和技术风险.
- 例如,生物和基因疗法药物需要专门设施、高技能人员和先进的遏制系统,使制造规模的扩大在技术上具有挑战性和资本密集型
- 多个区域遵守管制规定的情况使情况更加复杂,因为无主药物必须达到与安全、可追踪性和质量控制有关的不同和不断发展的标准
- 这些挑战可限制合格的API供应商的数量,可能导致供应受限和成本上升,从而限制市场扩大。
- 先进孤儿API专用原材料和试剂供应有限,可能进一步打乱生产时间表并增加对特殊供应商的依赖
- 需要进行广泛的验证、较长的筹备时间以及严格的批准后改变控制,会减缓制造业的敏捷性并延误无主药物的商业供应。
罕见疾病 API/孤儿药物市场范围
市场根据API/药物物质类型、治疗指示和最终用户划分。
- 根据API/药物类型
根据API / 药物物质类型,全球罕见病API / 孤儿药物市场被分入生物活性API,小分子活性API,病毒活性活性API,基于RNA的API,和与细胞疗法有关的药物物质. 由于广泛使用单克隆抗体,酶取代疗法,再生蛋白在治疗稀有遗传和代谢紊乱时被广泛使用,生物生物学API部分在2025年收入份额最大,为58.3%. 生物学提供了高度的特异性和临床疗效,使它们成为许多孤儿药物方案的首选. 核准的生物学孤儿药物的强大存在和管道的继续扩展进一步支持了这一部分的主导地位。 此外,溢价定价和长期治疗办法有助于增加创收。 现有的制造专门知识和对生物学的监管熟悉也加强了它们的领先地位。
由于罕见和超罕见疾病基因疗法的迅速发展,病毒病媒API部分预计在预测期间增长最快。 越来越多的人批准与甲型病毒和扁豆病媒疗法,这正推动对专业化病媒生产的强烈需求。 高水平的未满足医疗需求、治疗潜力以及对基因治疗平台的不断增长的投资正在加速这一部分的扩展。 供应商的有限供应和复杂的制造要求进一步提高了病毒病媒活性成分的战略重要性和增长势头。
- 治疗指示
根据治疗指标,市场分为肿瘤、血液疾病、神经和神经肌肉疾病、代谢和内分泌疾病、免疫和罕见传染病以及心血管、眼科和其他罕见疾病。 肿瘤部分在2025年占据了市场主导地位,因为罕见癌症的孤儿药物指定数量很多,并且持续投资于有针对性的癌症疗法。 罕见的肿瘤药物往往依赖强效的API和生物学,对API的总体需求做出了重大贡献. 强大的临床管线,加快监管审批,提高治疗成本,进一步支撑了这一部分的收入领导. 此外,制药公司优先考虑罕见的肿瘤学,因为有有利的补偿和市场专属利益。
神经和神经肌肉紊乱部分预计将在预测期间以最快的速度增长,其驱动力是越来越多地研究脊髓肌萎缩,杜切内肌肉萎缩等遗传神经条件,以及罕见的癫痫. 基因疗法、RNA药物和精密医学的进步正在改变这个空间中的治疗方法。 诊断率的上升和强有力的宣传支持正在进一步推动发展活动。 由于许多这些疗法需要复杂的API,在这一环节内对专门药物的需求正在迅速扩大。
- 按终端用户
以最终用户为基础,全球罕见疾病API/孤儿药物市场被分入生物制药公司,合同开发和制造组织,以及研究机构和特产制造商. 生物制药公司部分在2025年占有最大的市场份额,其动力是拥有无主药物管道,直接控制高价值疗法的商业制造。 大型和中型生药公司投入大量资金,确保可靠的API供应,以保护排他性时期,确保产品质量一致。 由于战略和知识产权的原因,往往倾向于在内部制造关键的API。 强有力的金融能力和监管专门知识进一步加强了这一部门的主导地位。
CDMOs部分预计将在预测期间增长最快,得到生物技术和制药公司外包趋势增加的支持。 孤儿API的复杂性,加上批量小和资本要求高,正在鼓励赞助者依赖专门的CDMO. CDMO提供灵活的制造,监管支持,以及适合稀有疾病药物的先进技术. 随着小型生物技术公司推动无主药物创新,依赖CDMO进行可扩展和符合要求的API生产正在迅速加速。
罕见疾病 API/孤儿药物市场区域分析
- 北美主导了罕见疾病API/孤儿药物市场,2025年收入份额最大,为41.5%,辅以强大的孤儿药物监管框架、高研发支出以及生物制药公司和专门的CDMO的强大存在
- 本区域各公司高度重视先进制造能力、严格遵守质量要求和可靠供应复杂的药物,特别是生物记录、基因疗法和其他高价值孤儿API
- 这种广泛的市场领导地位进一步得到以下因素的支持:孤儿药品审批的高度集中,罕见疾病研究资金雄厚,主要生物制药公司和专门的CDMO的存在,将北美确立为罕见疾病API开发和生产的主要枢纽.
美国稀有疾病 API/孤儿药物市场透视
美国罕见疾病API/孤儿药物市场在2025年获得了北美最大的收入份额,其驱动力是强大的孤儿药物监管框架,广泛的研发投资,生物制药和生物技术公司高度集中. 制造商越来越多地优先考虑发展和保障复杂的API的供应,以支持扩大无主药物管道。 市场排他性、税收抵免和加速批准途径等有利的激励措施的存在继续刺激对专门药物的需求。 此外,CDMOs和先进制造业基础设施的强大作用也极大地促进了市场的持续增长。
欧洲罕见疾病API/孤儿药物市场透视
预测在预测期间,欧洲罕见疾病API/孤儿药物市场将在一个实质性的CAGR市场扩大,这主要是由支持性EMA孤儿药物政策和增加对罕见疾病研究的投资所推动的。 提高认识、提高诊断率和跨界合作正在整个区域促进无主药物的发展。 欧洲制造商强调质量、可追踪性和遵守监管,支持对高价值API的稳定需求。 创新驱动的和外包的制造模式都出现了增长,特别是在生物记录学和先进疗法方面。
英国罕见疾病API/孤儿药物市场透视
英国的罕见疾病API/孤儿药物市场预计将在预测期间以值得注意的CAGR增长,并辅之以强有力的学术-产业合作和政府支持的罕见疾病倡议。 英国先进的生命科学生态系统鼓励早期的孤儿药物开发,增加了临床阶段API的需求. 生物学和基因疗法研究方面的持续投资正在加强市场前景。 此外,与全球标准相协调的监管提高了该国对孤儿API制造和发展伙伴关系的吸引力。
德国罕见疾病API/孤儿药物市场透视
在预测期间,德国的罕见疾病API/无主药物市场预计将在相当可观的CAGR扩展,这得益于强大的药品制造基础和对创新和质量的大力强调。 德国在生物生产和先进制造技术方面的领导作用支持了对复杂无主药物的稳定需求. 国家专注于遵守、安全和精准制造,这与罕见疾病API的严格要求非常相符合。 增加对先进疗法的投资会进一步加强市场增长前景。
亚太稀有疾病API/孤儿药物市场观察
亚太稀有疾病API/无主药物市场在预测期间增长最快的CAGR市场,其动力是生物技术能力的扩大、保健投资的增加以及西方市场外包的增加。 中国、日本和印度等国家正在加强其罕见疾病监管框架和制造业基础设施。 本区域的成本优势和不断增长的技术专长正在吸引全球生物制药公司寻求可扩展的API生产。 这一趋势正在大大地加快整个APAC的市场扩张.
日本罕见疾病API/孤儿药物市场透视
日本罕见疾病API/孤儿药物市场由于政府对孤儿药物开发的有力支持和先进的药物制造能力而日益强劲. 日本高度重视质量、安全和创新,推动对高度专业化药物的需求。 该国对遗传和神经稀有疾病的关注增加了对包括生物学和RNA类物质在内的复杂API的需求. 人口老化和罕见疾病发病率上升进一步支持了市场增长。
印度罕见疾病 API/孤儿药物市场透视
2025年,印度罕见疾病API/无主药物市场在亚太占了相当大的收入份额,原因是API具有强大的制造专长、成本竞争力并扩大了生物技术投资。 印度正在成为全球市场小分子和日益生物化孤儿API的主要供应国。 支持稀有疾病治疗发展和地方制造业的政府举措正在改善市场前景。 国内CDMO和合同制造商越来越多,这进一步加强了印度在全球无主药物供应链中的作用。
罕见疾病 API/孤儿药物市场份额
稀有疾病API/孤儿药物行业主要由老牌公司领导,包括:
- 隆扎有限公司(瑞士)
- 加泰罗尼亚集团公司(美国)
- WuXi AppTec有限公司(中国)
- 辉瑞股份有限公司(美国)
- 诺华公司(瑞士)
- F. Hoffmann-La Roche有限公司(瑞士)
- 布里斯托-迈尔斯·斯奎布公司(美国)
- 阿姆根股份有限公司(美国)
- 萨诺菲(法国)
- 武田制药有限公司(日本)
- AbbVie Inc. (美国).
- GSK plc (英国).
- 拜耳公司(德国)
- Vertex制药公司(美国)
- Biogen Inc. (美国).
- PTC治疗有限公司(美国)
- 瑞典孤儿Biovitrum AB(瑞典)
- SOM 创新生物技术,S.A.(西班牙)
- Ultragnyx制药公司(美国)
全球罕见疾病API/孤儿药物市场的最新动态是什么?
- 2025年8月,美国FDA批准Papzimeos(zopapogene imadenovec),这是第一种用于反复呼吸道apillomatosis(RRP)的免疫疗法,这是一种孤儿指定的罕见病症,它强调了基于基因的罕见疾病免疫进展.
- 2025年4月,非营利的"孤儿治疗加速器"宣布了关键伙伴关系,旨在推进超罕见疾病疗法的发展和商业化路径,应对历史上在资助和引导孤儿药物候选者方面的难题.
- 2024年1月,FDA的孤儿药物景观大幅扩张,批准数量创下新纪录(28种新型孤儿药物),包括Friedrich的Axia和Rett综合症等疾病的一流疗法,突出罕见疾病治疗发展迅速增长.
- 2023年8月,美国FDA批准Pozelimab (Veopoz)作为首个治疗CHAPLE疾病,一种超罕见补充系统障碍,代表一种新的重组单克隆抗体疗法,应对本来致命的疾病.
- 2023年5月,美国FDA批准了Adzynma(apadamtase alfa),这是针对先天性血栓性血栓性血栓性purpura(cTTP)的重组ADAMTS13酶替代疗法,标志着第一个获得批准的生物学解决了这种超罕见血栓性障碍,并扩展了罕见疾病患者的酶替代方案.
SKU-
研究方法
数据收集和基准年分析是使用具有大样本量的数据收集模块完成的。该阶段包括通过各种来源和策略获取市场信息或相关数据。它包括提前检查和规划从过去获得的所有数据。它同样包括检查不同信息源中出现的信息不一致。使用市场统计和连贯模型分析和估计市场数据。此外,市场份额分析和关键趋势分析是市场报告中的主要成功因素。要了解更多信息,请请求分析师致电或下拉您的询问。
DBMR 研究团队使用的关键研究方法是数据三角测量,其中包括数据挖掘、数据变量对市场影响的分析和主要(行业专家)验证。数据模型包括供应商定位网格、市场时间线分析、市场概览和指南、公司定位网格、专利分析、定价分析、公司市场份额分析、测量标准、全球与区域和供应商份额分析。要了解有关研究方法的更多信息,请向我们的行业专家咨询。
可定制
Data Bridge Market Research 是高级形成性研究领域的领导者。我们为向现有和新客户提供符合其目标的数据和分析而感到自豪。报告可定制,包括目标品牌的价格趋势分析、了解其他国家的市场(索取国家列表)、临床试验结果数据、文献综述、翻新市场和产品基础分析。目标竞争对手的市场分析可以从基于技术的分析到市场组合策略进行分析。我们可以按照您所需的格式和数据样式添加您需要的任意数量的竞争对手数据。我们的分析师团队还可以为您提供原始 Excel 文件数据透视表(事实手册)中的数据,或者可以帮助您根据报告中的数据集创建演示文稿。