Global Electronic Clinical Outcome Assessment Ecoa Market
Taille du marché en milliards USD
TCAC :
% 
 USD
1.70 Billion
USD
5.52 Billion
2024
2032
USD
1.70 Billion
USD
5.52 Billion
2024
2032
| 2025 –2032 | |
| USD 1.70 Billion | |
| USD 5.52 Billion | |
|
|
|
|
Segmentation du marché mondial de l'évaluation électronique des résultats cliniques (eCOA), par type (évaluation des résultats rapportés par le clinicien (CLINRO), évaluation des résultats rapportés par le patient (PRO), évaluation des résultats rapportés par l'observateur (OBSRO) et évaluation des résultats de performance (PERFO)), modalité (solutions sur site, solutions Web et portables), utilisateur final (organismes de recherche sous contrat (CRO), sociétés pharmaceutiques et biotechnologiques, fabricants de dispositifs médicaux, hôpitaux/prestataires de soins de santé, sociétés de conseil, instituts universitaires et de recherche, etc.), mode de diffusion (cloud et hébergé sur le Web) - Tendances et prévisions du secteur jusqu'en 2032
Taille du marché de l'évaluation électronique des résultats cliniques (eCOA)
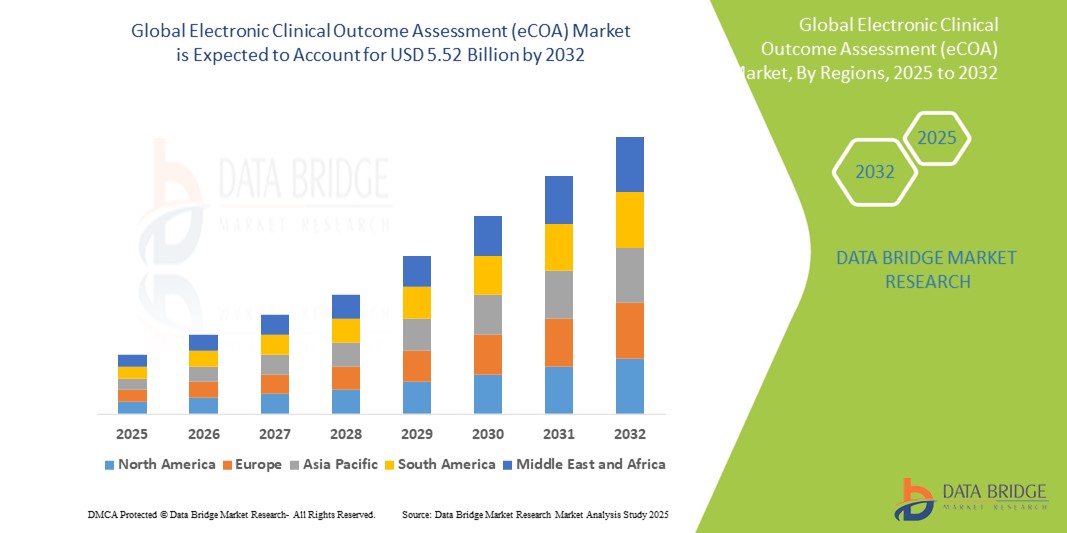
- La taille du marché mondial de l'évaluation électronique des résultats cliniques (eCOA) était évaluée à 1,70 milliard USD en 2024 et devrait atteindre 5,52 milliards USD d'ici 2032 , à un TCAC de 15,80 % au cours de la période de prévision.
- La croissance du marché est principalement tirée par l'adoption croissante des technologies numériques dans les essais cliniques et la recherche en soins de santé, facilitant une collecte et un suivi plus précis et plus efficaces des données des patients.
- En outre, la demande croissante d'informations sur les patients en temps réel, d'amélioration de la conformité réglementaire et d'amélioration de l'intégrité des données propulse l'adoption des solutions eCOA dans les sociétés pharmaceutiques, les organismes de recherche sous contrat (CRO) et les prestataires de soins de santé.
Analyse du marché de l'évaluation électronique des résultats cliniques (eCOA)
- Les solutions eCOA, permettant la capture électronique des données de résultats cliniques directement auprès des patients, des soignants ou des cliniciens, sont des composants de plus en plus essentiels des essais cliniques modernes et de la recherche en soins de santé en raison de leur précision accrue des données, de leurs capacités de surveillance en temps réel et de leur intégration transparente avec les écosystèmes de santé numérique.
- La demande croissante d'eCOA est principalement alimentée par l'adoption généralisée des technologies de santé numériques, l'importance croissante accordée aux essais centrés sur le patient et une préférence croissante pour les méthodes de collecte de données à distance et conviviales qui améliorent l'efficacité et la conformité des essais.
- L'Amérique du Nord domine le marché de l'évaluation électronique des résultats cliniques (eCOA) avec la plus grande part de revenus de 43,5 % en 2024, caractérisée par l'adoption précoce de solutions d'essais cliniques numériques, des secteurs pharmaceutiques et biotechnologiques forts et des cadres réglementaires soutenant la capture électronique des données, les États-Unis connaissant une croissance substantielle tirée par les innovations des fournisseurs établis et des fournisseurs de technologies émergents se concentrant sur les plateformes mobiles et basées sur le cloud.
- L'Asie-Pacifique devrait être la région connaissant la croissance la plus rapide sur le marché de l'évaluation électronique des résultats cliniques (eCOA) au cours de la période de prévision en raison de l'augmentation des activités d'essais cliniques, de l'augmentation des investissements dans les soins de santé et de la sensibilisation croissante aux avantages des outils numériques sur les marchés émergents tels que la Chine et l'Inde.
- Le segment Patient Reported Outcome Assessment (PRO) domine le marché de l'évaluation électronique des résultats cliniques (eCOA) avec une part de marché de 48,5 % en 2024, grâce à son rôle essentiel dans la capture des points de vue des patients sur l'efficacité du traitement et la qualité de vie, qui sont de plus en plus prioritaires pour les sponsors et les agences de réglementation.
Portée du rapport et segmentation du marché de l'évaluation électronique des résultats cliniques (eCOA)
|
Attributs |
Évaluation électronique des résultats cliniques (eCOA) : principales perspectives du marché |
|
Segments couverts |
|
|
Pays couverts |
Amérique du Nord
Europe
Asie-Pacifique
Moyen-Orient et Afrique
Amérique du Sud
|
|
Principaux acteurs du marché |
|
|
Opportunités de marché |
|
|
Ensembles d'informations de données à valeur ajoutée |
Outre les informations sur les scénarios de marché tels que la valeur marchande, le taux de croissance, la segmentation, la couverture géographique et les principaux acteurs, les rapports de marché organisés par Data Bridge Market Research comprennent également une analyse approfondie des experts, une analyse des prix, une analyse de la part de marque, une enquête auprès des consommateurs, une analyse démographique, une analyse de la chaîne d'approvisionnement, une analyse de la chaîne de valeur, un aperçu des matières premières/consommables, des critères de sélection des fournisseurs, une analyse PESTLE, une analyse Porter et un cadre réglementaire. |
Tendances du marché de l'évaluation électronique des résultats cliniques (eCOA)
« Amélioration de l'efficacité des essais cliniques grâce à l'IA et à la surveillance à distance des patients »
- Une tendance significative et croissante sur le marché mondial de l'eCOA est l'intégration croissante de l'intelligence artificielle (IA) et des technologies de télésurveillance des patients au sein des plateformes de collecte de données d'essais cliniques. Cette fusion des technologies améliore considérablement la précision, la rapidité et la centralité des évaluations des résultats cliniques.
- Par exemple, les principaux fournisseurs d'eCOA tels que Medidata et ERT intègrent des analyses basées sur l'IA pour identifier des tendances dans les données rapportées par les patients, permettant ainsi une détection précoce des événements indésirables et une meilleure prise de décision dans les essais. De même, les appareils portables associés aux plateformes eCOA facilitent le suivi continu et en temps réel des indicateurs de santé des patients, au-delà des visites sur site traditionnelles.
- L'intégration de l'IA dans eCOA permet des fonctionnalités telles que l'analyse prédictive pour l'observance du traitement, l'automatisation des contrôles de qualité des données et la génération d'alertes intelligentes en cas de réactions inhabituelles. De plus, les capacités de surveillance à distance offrent aux patients des interfaces pratiques et intuitives pour communiquer leurs résultats depuis leur domicile, améliorant ainsi l'exhaustivité des données et l'engagement.
- L'intégration transparente des systèmes eCOA avec des plateformes plus vastes de santé numérique et de gestion des essais cliniques permet aux promoteurs de centraliser la gestion des données et de rationaliser les flux de travail des essais. Grâce à des tableaux de bord unifiés, les équipes cliniques peuvent suivre en temps réel les données des patients, les performances des sites et la conformité réglementaire.
- Cette tendance vers des solutions de résultats cliniques plus intelligentes, connectées et conviviales pour les patients transforme fondamentalement les attentes en matière de collecte de données d'essais cliniques. Par conséquent, des entreprises comme Oracle Health et CRF Health développent des plateformes eCOA basées sur l'IA, dotées de capacités prédictives améliorées et de fonctionnalités de collecte de données à distance.
- La demande de solutions eCOA intégrant l'IA et la surveillance à distance des patients augmente rapidement dans les secteurs pharmaceutique, biotechnologique et des dispositifs médicaux, car les parties prenantes accordent de plus en plus la priorité à l'efficacité des essais, à l'exactitude des données et à l'expérience des patients.
Dynamique du marché de l'évaluation électronique des résultats cliniques (eCOA)
Conducteur
« Demande croissante d'essais centrés sur le patient et de précision des données numériques »
- L'accent croissant mis sur les essais cliniques centrés sur le patient, combiné au besoin croissant de collecte de données numériques précises et en temps réel, est un facteur important de la demande accrue de solutions d'évaluation électronique des résultats cliniques (eCOA)
- Par exemple, en janvier 2024, Medidata, filiale de Dassault Systèmes, a introduit de nouvelles améliorations basées sur l'IA pour sa plateforme eCOA afin d'améliorer l'observance des patients et la qualité des données dans les essais décentralisés. Ces innovations, mises en œuvre par des acteurs clés du secteur, devraient stimuler la croissance du marché eCOA durant la période de prévision.
- Alors que les sociétés pharmaceutiques et biotechnologiques cherchent à rationaliser les processus d'essais cliniques et à réduire les délais de mise sur le marché, les plateformes eCOA offrent des fonctionnalités avancées telles que la capture de données en temps réel, la création de rapports à distance sur les patients et la validation automatisée, offrant une amélioration substantielle par rapport aux méthodes traditionnelles sur papier.
- En outre, l’adoption croissante de modèles d’essais cliniques décentralisés et hybrides positionne l’eCOA comme un composant essentiel pour la collecte de données à distance, améliorant l’engagement des patients tout en maintenant des normes élevées de conformité réglementaire.
- La capacité des plateformes eCOA à améliorer l'efficacité des essais grâce à la collecte électronique des données, au support multilingue et à l'intégration avec des appareils portables ou des applications mobiles est un facteur clé de leur adoption par les CRO, les laboratoires pharmaceutiques et les instituts de recherche. L'importance croissante accordée à la réduction des taux d'abandon des essais cliniques et à l'amélioration de l'intégrité des données favorise l'intégration généralisée des solutions eCOA dans la recherche clinique moderne.
Retenue/Défi
« Préoccupations concernant la confidentialité des données, la conformité réglementaire et les coûts élevés de mise en œuvre »
- Les préoccupations concernant la confidentialité des données, la conformité réglementaire et les coûts initiaux élevés de mise en œuvre des plateformes d'évaluation électronique des résultats cliniques (eCOA) posent des défis importants à une adoption plus large du marché.
- Étant donné que les systèmes eCOA impliquent la capture et la transmission électroniques de données de santé sensibles des patients, ils sont soumis à des réglementations strictes en matière de protection des données telles que HIPAA, GDPR et 21 CFR Part 11, ce qui rend la conformité complexe et gourmande en ressources pour les sponsors et les CRO.
- Par exemple, plusieurs promoteurs d’essais cliniques ont exprimé leur prudence quant à la transition complète vers les systèmes eCOA en raison des incertitudes entourant les règles de localisation des données et de la complexité de la garantie de la conformité des données transfrontalières, en particulier dans les essais multirégionaux.
- Relever ces défis nécessite une infrastructure de sécurité des données robuste, des audits réguliers et le respect des normes de conformité internationales. Les principaux fournisseurs d'eCOA, tels qu'Oracle Health et Signant Health, investissent massivement dans des plateformes chiffrées et des formations réglementaires afin de limiter les risques et de maintenir la confiance des parties prenantes des essais cliniques.
- De plus, le coût initial élevé associé au déploiement des systèmes eCOA – incluant les frais de licence, l'achat de matériel, la formation du personnel et l'intégration des systèmes – peut constituer un obstacle à l'entrée, en particulier pour les organismes de recherche de petite et moyenne taille. Bien que les avantages à long terme, tels qu'une meilleure précision des données et une réduction de la durée des essais, soient largement reconnus, le fardeau financier initial peut limiter l'adoption par les institutions aux ressources limitées.
- Surmonter ces défis grâce à des modèles de tarification évolutifs, une livraison basée sur le cloud et une innovation continue dans des plateformes sécurisées et conviviales sera essentiel pour favoriser une adoption plus large et durable des solutions eCOA dans le paysage de la recherche clinique.
Portée du marché de l'évaluation électronique des résultats cliniques (eCOA)
Le marché est segmenté en fonction du type, de la modalité, de l'utilisateur final et du mode de livraison
- Par type
Sur la base du type, le marché de l'évaluation électronique des résultats cliniques (eCOA) est segmenté en résultats rapportés par les patients (PRO), résultats rapportés par les cliniciens (ClinRO), résultats rapportés par les observateurs (ObsRO) et résultats de performance (PerfO). Le segment des résultats rapportés par les patients (PRO) détenait la plus grande part de chiffre d'affaires du marché, soit 48,5 % en 2024, grâce à son approche centrée sur le patient, qui permet de recueillir des informations de première main sur son expérience, ses symptômes et les résultats de son traitement. Les outils PRO permettent aux patients de communiquer directement leurs données de santé en temps réel via des plateformes électroniques, améliorant ainsi la précision des données et l'implication des patients, améliorant ainsi la qualité des études cliniques.
Le segment des résultats rapportés par les cliniciens (ClinRO) devrait connaître une croissance substantielle au cours de la période de prévision, en raison de la complexité croissante des essais cliniques et du besoin de méthodes de collecte de données précises et standardisées. ClinRO implique des évaluations réalisées par des professionnels de santé qualifiés, fournissant des données objectives et fiables pour l'évaluation des interventions cliniques, notamment lorsque l'auto-évaluation par les patients n'est pas possible.
- Par modalité
En fonction des modalités, le marché de l'évaluation électronique des résultats cliniques (eCOA) est segmenté en solutions sur site, solutions web et appareils portables. Le segment des solutions web a représenté la plus grande part de chiffre d'affaires en 2024, grâce à ses interfaces conviviales, sa facilité d'accès et ses faibles besoins d'investissement. Les solutions hébergées web stockent les données clients sur des serveurs cloud, accessibles via le web avec un matériel informatique de base et une connexion internet, offrant ainsi une flexibilité de personnalisation et permettant une adaptation aux besoins spécifiques des clients.
Le segment des appareils portables devrait connaître une croissance significative au cours de la période de prévision, portée par l'adoption croissante des technologies mobiles dans les essais cliniques. Les appareils portables facilitent la saisie des données en temps réel et améliorent l'observance thérapeutique des patients, ce qui en fait une option intéressante pour les études cliniques décentralisées et à distance.
- Par utilisateur final
En fonction de l'utilisateur final, le marché de l'évaluation électronique des résultats cliniques (eCOA) est segmenté entre les entreprises pharmaceutiques et biotechnologiques, les organismes de recherche sous contrat (CRO), les fabricants de dispositifs médicaux, les hôpitaux/prestataires de soins, les sociétés de conseil, les universités et les instituts de recherche, etc. Le segment des entreprises pharmaceutiques et biotechnologiques domine le marché, représentant 50,66 % de parts de marché en 2024. Cette domination s'explique par le rôle essentiel des solutions eCOA dans la simplification de la collecte et de l'analyse des données lors du développement des médicaments, la garantie du respect des normes réglementaires et l'amélioration de la précision des données des essais cliniques.
Le segment des organismes de recherche sous contrat (ORC) devrait connaître une croissance substantielle au cours de la période de prévision, portée par la tendance croissante des grandes entreprises biopharmaceutiques et de dispositifs médicaux à externaliser la gestion de leur recherche clinique. Les ORC offrent des services complets englobant la conception des études, le recrutement des patients, la collecte et l'analyse des données, ce qui en fait des acteurs incontournables du secteur de l'eCOA.
Par mode de livraison
En fonction du mode de prestation, le marché de l'évaluation électronique des résultats cliniques (eCOA) est segmenté en solutions cloud et hébergées en ligne. Le segment des solutions hébergées en ligne détenait la plus grande part de marché, avec 58,9 % en 2025, grâce à sa rentabilité par rapport aux solutions cloud. Les plateformes hébergées en ligne impliquent des investissements d'infrastructure initiaux moindres pour les utilisateurs finaux, réduisant ainsi les dépenses d'investissement des laboratoires pharmaceutiques, des CRO et des prestataires de soins de santé.
Le segment des solutions cloud devrait connaître une croissance significative au cours de la période de prévision, grâce à son évolutivité, sa flexibilité et sa rentabilité. Les plateformes cloud facilitent et accélèrent l'accès aux données pour les acteurs des essais cliniques, où qu'ils soient, ce qui est crucial pour les essais multicentriques.
Analyse régionale du marché de l'évaluation électronique des résultats cliniques (eCOA)
- L'Amérique du Nord domine le marché de l'évaluation électronique des résultats cliniques (eCOA) avec la plus grande part de revenus de 43,5 % en 2024, grâce à l'adoption précoce de solutions d'essais cliniques numériques, à des secteurs pharmaceutiques et biotechnologiques forts et à des cadres réglementaires soutenant la saisie électronique des données.
- La région bénéficie d'un cadre réglementaire solide qui soutient la transformation numérique de la recherche clinique, encourageant les sociétés pharmaceutiques et les organismes de recherche sous contrat à adopter les plateformes eCOA pour améliorer l'exactitude des données et la conformité réglementaire.
- De plus, des investissements importants en R&D, une infrastructure de santé solide et l'adoption précoce d'essais cliniques décentralisés et centrés sur le patient contribuent significativement à la croissance du marché. La présence de fournisseurs de solutions eCOA et d'ORC leaders accélère encore l'expansion régionale des outils électroniques d'évaluation des résultats cliniques.
Aperçu du marché américain de l'évaluation électronique des résultats cliniques (eCOA)
Le marché américain de l'évaluation électronique des résultats cliniques (eCOA) a représenté la plus grande part de chiffre d'affaires en Amérique du Nord en 2024, avec 79,6 %, grâce au leadership du pays en matière d'essais cliniques et à la numérisation rapide des pratiques de recherche clinique. Les organismes de réglementation tels que la FDA préconisent fortement l'utilisation d'outils numériques pour améliorer la qualité des données et l'engagement des patients, contribuant ainsi à l'adoption généralisée des systèmes d'eCOA. De plus, le besoin croissant de modèles d'essais cliniques décentralisés et hybrides alimente la demande de plateformes de collecte de données patients à distance et en temps réel. Le marché américain bénéficie également d'un important financement de la R&D, d'une forte présence de géants pharmaceutiques et d'une infrastructure informatique de santé sophistiquée.
Aperçu du marché européen de l'évaluation électronique des résultats cliniques (eCOA)
Le marché européen de l'évaluation électronique des résultats cliniques (eCOA) devrait connaître une croissance annuelle moyenne (TCAC) substantielle tout au long de la période de prévision, alimentée par l'importance croissante accordée par la réglementation aux données probantes en situation réelle, à l'orientation patient et à la standardisation des données dans les essais cliniques. Le besoin croissant de solutions numériques multilingues et culturellement adaptées dans l'UE accélère l'adoption de plateformes eCOA flexibles et évolutives. De plus, l'augmentation des collaborations de recherche universitaire, conjuguée à des politiques favorables à la transformation numérique de la santé, soutient la croissance régionale. Des pays comme l'Allemagne, le Royaume-Uni et la France sont en tête de l'adoption de technologies au sein de leurs écosystèmes d'essais respectifs.
Aperçu du marché britannique de l'évaluation électronique des résultats cliniques (eCOA)
Le marché britannique de l'évaluation électronique des résultats cliniques (eCOA) devrait connaître une croissance annuelle moyenne (TCAC) remarquable au cours de la période de prévision, soutenu par la vigueur du secteur de la R&D biopharmaceutique et les stratégies proactives du NHS en matière de santé numérique. La multiplication des essais décentralisés et la clarté réglementaire autour de la saisie électronique des données favorisent l'adoption par le marché. Grâce à un paysage de recherche clinique avancé et à des investissements importants en informatique de santé, le Royaume-Uni assiste à une adoption rapide des technologies d'eCOA pour garantir la conformité, améliorer l'engagement des patients et permettre un suivi efficace des résultats.
Aperçu du marché allemand de l'évaluation électronique des résultats cliniques (eCOA)
Le marché allemand de l'évaluation électronique des résultats cliniques (eCOA) devrait connaître une croissance annuelle moyenne (TCAC) considérable au cours de la période de prévision, porté par la réputation d'excellence du pays en matière d'essais cliniques et par une législation stricte en matière de protection des données. Les organismes de réglementation allemands mettent l'accent sur la fiabilité et la sécurité des données cliniques, ce qui incite les promoteurs et les CRO à investir dans des solutions d'eCOA sécurisées et validées. De plus, la demande croissante de l'Allemagne pour la saisie de données en temps réel dans les essais de phases I à IV et la solidité de son infrastructure informatique de santé favorisent une intégration accrue des technologies d'eCOA dans la recherche sur les dispositifs médicaux et la recherche pharmaceutique.
Analyse du marché de l'évaluation électronique des résultats cliniques (eCOA) en Asie-Pacifique
Le marché de l'évaluation électronique des résultats cliniques (eCOA) en Asie-Pacifique devrait connaître son taux de croissance annuel composé le plus élevé au cours de la période de prévision 2025-2032, porté par l'intensification de la recherche clinique et la transformation numérique des soins de santé dans des pays comme la Chine, l'Inde, la Corée du Sud et le Japon. L'expansion des essais multinationaux et la diversité des populations de patients favorisent la croissance régionale. Les mesures incitatives gouvernementales en faveur des plateformes de santé numérique et la demande croissante de solutions mobiles facilitent et généralisent l'adoption de l'eCOA dans les zones urbaines et semi-urbaines. Les partenariats locaux entre les CRO et les entreprises pharmaceutiques mondiales contribuent à la mise en œuvre de l'eCOA.
Aperçu du marché japonais de l'évaluation électronique des résultats cliniques (eCOA)
Le marché japonais de l'évaluation électronique des résultats cliniques (eCOA) prend de l'ampleur grâce à la sophistication technologique du pays, au vieillissement de la population et à l'importance accordée à la qualité des données dans les essais cliniques. L'organisme de réglementation japonais, la PMDA, est de plus en plus réceptif aux terminaux numériques et aux outils de saisie de données à distance. Le marché est également façonné par l'augmentation des essais cliniques à domicile et en ambulatoire, ce qui accroît le besoin de systèmes d'eCOA précis et conviviaux pour les patients. L'intégration à des écosystèmes eClinical plus vastes et à des outils d'engagement des patients basés sur l'IA devraient encore accélérer la croissance.
Aperçu du marché indien de l'évaluation électronique des résultats cliniques (eCOA)
Le marché indien de l'évaluation électronique des résultats cliniques (eCOA) représentait la plus grande part de chiffre d'affaires en Asie-Pacifique en 2024, porté par une forte activité d'essais cliniques, une population férue de technologie et le développement des capacités de fabrication pharmaceutique. Le paysage CRO rentable de l'Inde et les politiques gouvernementales favorables à la numérisation de la santé encouragent les sponsors internationaux à déployer les outils eCOA dans les essais nationaux. La pénétration croissante des smartphones, le développement de la télémédecine et l'amélioration de la connectivité Internet dans les zones urbaines et semi-urbaines rendent les plateformes eCOA mobiles et hébergées dans le cloud plus accessibles et largement adoptées.
Part de marché de l'évaluation électronique des résultats cliniques (eCOA)
Le secteur de l'évaluation électronique des résultats cliniques (eCOA) est principalement dirigé par des entreprises bien établies, notamment :
- IQVIA (États-Unis)
- Clario (États-Unis)
- Medidata (États-Unis)
- Veeva Systems (États-Unis)
- Earth Resources Technology (États-Unis)
- Oracle Health Sciences (États-Unis)
- YPrime, LLC (États-Unis)
- ArisGlobal LLC (États-Unis)
- Castor EDC (Pays-Bas)
- eClinicalWorks (États-Unis)
- Medrio, Inc. (États-Unis)
- ClinOne (États-Unis)
- Signant Health (États-Unis)
- Clinical Ink, Inc. (États-Unis)
- Curebase, Inc. (États-Unis)
- Kayentis (France)
- Calice (Royaume-Uni)
- Datacubed Health (États-Unis)
- HealthDiary, Inc. (États-Unis)
Derniers développements sur le marché mondial de l'évaluation électronique des résultats cliniques (eCOA)
- En mai 2025, Clario (États-Unis) a acquis l'activité eCOA de WCG Clinical (États-Unis). Cette acquisition stratégique vise à renforcer son leadership dans les solutions de données numériques de point final, notamment pour les essais cliniques en neurosciences. Cette acquisition élargit la plateforme complète de données de point final de Clario, lui permettant de mieux prendre en charge les environnements d'essais complexes et de consolider sa position dans le secteur en constante évolution des eCOA.
- En mai 2025, le Critical Path Institute (États-Unis) a poursuivi son initiative « eCOA : Getting Better Together », visant à fédérer les sponsors, les fournisseurs de technologies et les régulateurs. Cet effort collaboratif, qui se poursuivra jusqu'en mars 2025, vise à établir des bonnes pratiques préconcurrentielles et un lexique commun pour la saisie des données eCOA, à promouvoir la normalisation et à accélérer l'adoption dans diverses régions.
- En novembre 2023, Clinical Ink a enrichi sa suite d'engagement patient en intégrant l'outil de diagnostic comportemental SPUR d'Observia. Cette intégration associe l'évaluation comportementale à la modification du mode de vie, à l'eCOA, à l'eSource et aux biomarqueurs numériques, afin d'offrir une compréhension plus globale du comportement des patients et d'améliorer les résultats des essais.
- En octobre 2023, Clario a conclu un partenariat stratégique avec Trial Data, un prestataire de services d'essais cliniques décentralisés (DCT). Cette collaboration renforce la présence de Clario sur le marché chinois des essais cliniques, en combinant leurs expertises pour proposer des solutions d'essais décentralisés de pointe et promouvoir des approches centrées sur le patient dans la région.
- En décembre 2022, Suvoda LLC, société spécialisée dans la technologie des évaluations électroniques des résultats cliniques (eCOA), a lancé sa boîte à outils de conception d'évaluations électroniques des résultats cliniques (eCOA). Cette boîte à outils est conçue pour s'intégrer parfaitement à Suvoda IRT et eConsent, comblant ainsi les lacunes historiques de la mise en œuvre de l'eCOA et visant à simplifier le processus de conception.
SKU-
Accédez en ligne au rapport sur le premier cloud mondial de veille économique
- Tableau de bord d'analyse de données interactif
- Tableau de bord d'analyse d'entreprise pour les opportunités à fort potentiel de croissance
- Accès d'analyste de recherche pour la personnalisation et les requêtes
- Analyse de la concurrence avec tableau de bord interactif
- Dernières actualités, mises à jour et analyse des tendances
- Exploitez la puissance de l'analyse comparative pour un suivi complet de la concurrence
Méthodologie de recherche
La collecte de données et l'analyse de l'année de base sont effectuées à l'aide de modules de collecte de données avec des échantillons de grande taille. L'étape consiste à obtenir des informations sur le marché ou des données connexes via diverses sources et stratégies. Elle comprend l'examen et la planification à l'avance de toutes les données acquises dans le passé. Elle englobe également l'examen des incohérences d'informations observées dans différentes sources d'informations. Les données de marché sont analysées et estimées à l'aide de modèles statistiques et cohérents de marché. De plus, l'analyse des parts de marché et l'analyse des tendances clés sont les principaux facteurs de succès du rapport de marché. Pour en savoir plus, veuillez demander un appel d'analyste ou déposer votre demande.
La méthodologie de recherche clé utilisée par l'équipe de recherche DBMR est la triangulation des données qui implique l'exploration de données, l'analyse de l'impact des variables de données sur le marché et la validation primaire (expert du secteur). Les modèles de données incluent la grille de positionnement des fournisseurs, l'analyse de la chronologie du marché, l'aperçu et le guide du marché, la grille de positionnement des entreprises, l'analyse des brevets, l'analyse des prix, l'analyse des parts de marché des entreprises, les normes de mesure, l'analyse globale par rapport à l'analyse régionale et des parts des fournisseurs. Pour en savoir plus sur la méthodologie de recherche, envoyez une demande pour parler à nos experts du secteur.
Personnalisation disponible
Data Bridge Market Research est un leader de la recherche formative avancée. Nous sommes fiers de fournir à nos clients existants et nouveaux des données et des analyses qui correspondent à leurs objectifs. Le rapport peut être personnalisé pour inclure une analyse des tendances des prix des marques cibles, une compréhension du marché pour d'autres pays (demandez la liste des pays), des données sur les résultats des essais cliniques, une revue de la littérature, une analyse du marché des produits remis à neuf et de la base de produits. L'analyse du marché des concurrents cibles peut être analysée à partir d'une analyse basée sur la technologie jusqu'à des stratégies de portefeuille de marché. Nous pouvons ajouter autant de concurrents que vous le souhaitez, dans le format et le style de données que vous recherchez. Notre équipe d'analystes peut également vous fournir des données sous forme de fichiers Excel bruts, de tableaux croisés dynamiques (Fact book) ou peut vous aider à créer des présentations à partir des ensembles de données disponibles dans le rapport.