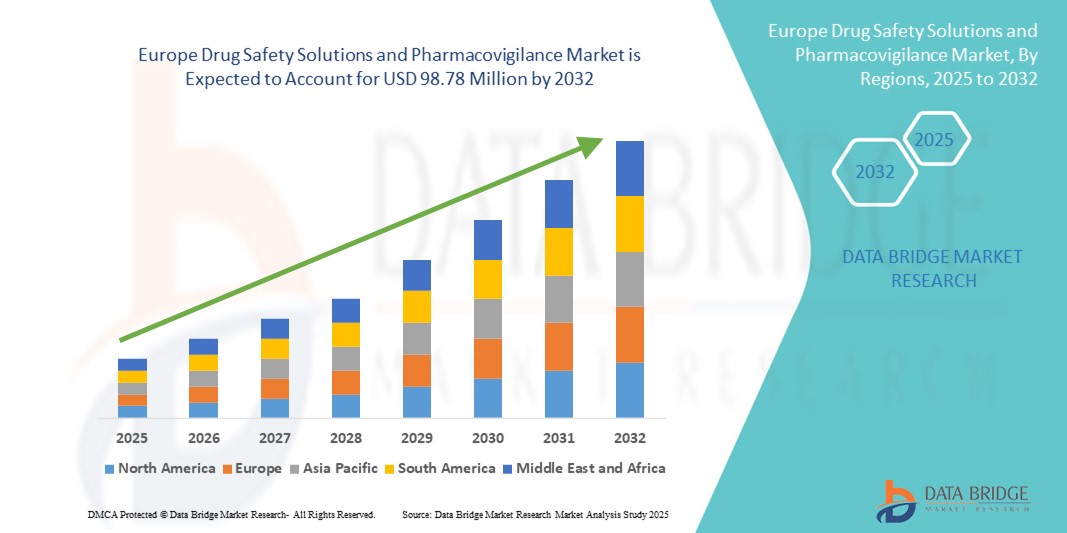
Europe Drug Safety Solutions And Pharmacovigilance Market
Tamanho do mercado em biliões de dólares
CAGR :
% 
 USD
57.06 Million
USD
98.78 Million
2024
2032
USD
57.06 Million
USD
98.78 Million
2024
2032
| 2025 –2032 | |
| USD 57.06 Million | |
| USD 98.78 Million | |
|
|
|
|
Segmentação do mercado de soluções de segurança de medicamentos e farmacovigilância na Europa, por tipo (software e serviços), produto (formato padrão e forma personalizada), funcionalidade (software de relatórios de eventos adversos, software de auditorias de segurança de medicamentos e software de rastreamento de problemas), entrega (modo de entrega no local e modo de entrega sob demanda/baseado em nuvem (SAAS)), usuários finais (biotecnologia e produtos farmacêuticos, organizações de pesquisa contratadas (CROS), hospitais, KPOs/BPOs e provedores de saúde), canal de distribuição (vendas diretas e vendas no varejo) - tendências do setor e previsão até 2032
Tamanho do mercado de soluções de segurança de medicamentos e farmacovigilância na Europa
- O tamanho do mercado europeu de soluções de segurança de medicamentos e farmacovigilância foi avaliado em US$ 57,06 milhões em 2024 e deve atingir US$ 98,78 milhões até 2032 , com um CAGR de 7,10% durante o período previsto.
- O crescimento do mercado é amplamente impulsionado por requisitos regulatórios rigorosos, como a Diretiva de Farmacovigilância da UE, aumento dos gastos com saúde, expansão das atividades de pesquisa clínica e maior conscientização sobre práticas de segurança de medicamentos em toda a região.
- Além disso, a crescente demanda de empresas farmacêuticas e organizações de pesquisa contratadas por soluções robustas, fáceis de usar e integradas de segurança de medicamentos e farmacovigilância está consolidando essas plataformas como ferramentas essenciais para monitorar eventos adversos e garantir a segurança dos pacientes. Esses fatores convergentes estão acelerando a adoção de sistemas avançados de farmacovigilância, impulsionando significativamente o crescimento do setor.
Análise do Mercado de Soluções de Segurança de Medicamentos e Farmacovigilância na Europa
- Soluções de segurança de medicamentos e plataformas de farmacovigilância, que fornecem monitoramento, relatórios e gerenciamento abrangentes de reações adversas a medicamentos, são componentes cada vez mais vitais das operações farmacêuticas modernas e sistemas de saúde em ambientes clínicos e pós-comercialização devido ao seu papel crítico em garantir a segurança do paciente, conformidade regulatória e integridade de dados.
- A crescente demanda por soluções de farmacovigilância é alimentada principalmente por requisitos regulatórios rigorosos na UE, aumento das atividades de ensaios clínicos, aumento da complexidade do desenvolvimento de medicamentos e crescente conscientização sobre a segurança do paciente e a gestão de riscos de medicamentos.
- A Alemanha dominou o mercado europeu de soluções de segurança de medicamentos e farmacovigilância com a maior participação na receita de 39% em 2024, impulsionada por seus altos gastos com saúde, forte presença de empresas farmacêuticas e organizações de pesquisa contratadas bem estabelecidas que adotam ativamente sistemas avançados de monitoramento de segurança.
- Espera-se que a França seja o país com crescimento mais rápido no mercado europeu de soluções de segurança de medicamentos e farmacovigilância durante o período previsto, devido à expansão da infraestrutura de pesquisa clínica, ao aumento dos investimentos em saúde e à crescente adoção de ferramentas digitais de farmacovigilância.
- O segmento de software de relatórios de eventos adversos (AERS) dominou o mercado europeu de soluções de segurança de medicamentos e farmacovigilância com uma participação de mercado de 43,5% em 2024, impulsionado por seu papel essencial na captura, processamento e análise eficiente de dados de segurança em ensaios clínicos e vigilância pós-comercialização.
Escopo do Relatório e Segmentação do Mercado de Soluções de Segurança de Medicamentos e Farmacovigilância na Europa
|
Atributos |
Soluções de Segurança de Medicamentos na Europa e Principais Insights de Mercado de Farmacovigilância |
|
Segmentos abrangidos |
|
|
Países abrangidos |
Europa
|
|
Principais participantes do mercado |
|
|
Oportunidades de mercado |
|
|
Conjuntos de informações de dados de valor agregado |
Além dos insights sobre cenários de mercado, como valor de mercado, taxa de crescimento, segmentação, cobertura geográfica e principais participantes, os relatórios de mercado selecionados pela Data Bridge Market Research também incluem análises aprofundadas de especialistas, análises de preços, análises de participação de marca, pesquisas com consumidores, análises demográficas, análises da cadeia de suprimentos, análises da cadeia de valor, visão geral de matérias-primas/consumíveis, critérios de seleção de fornecedores, análise PESTLE, análise de Porter e estrutura regulatória. |
Tendências do mercado de soluções de segurança de medicamentos e farmacovigilância na Europa
Eficiência aprimorada por meio de IA e plataformas baseadas em nuvem
- Uma tendência significativa e crescente no mercado europeu de soluções de segurança de medicamentos e farmacovigilância é a crescente integração de inteligência artificial (IA) e plataformas baseadas em nuvem em sistemas de monitoramento de segurança e notificação de eventos adversos. Essa integração está aprimorando significativamente a eficiência operacional, a precisão dos dados e a conformidade regulatória.
- Por exemplo, plataformas de farmacovigilância habilitadas por IA podem detectar e categorizar automaticamente reações adversas a medicamentos a partir de múltiplas fontes de dados, reduzindo a carga de trabalho manual e acelerando os prazos de relatórios de segurança. Soluções baseadas em nuvem permitem acesso contínuo a dados de segurança em tempo real em múltiplos departamentos e locais.
- A integração com IA permite análises preditivas de segurança, detecção de sinais e priorização inteligente de eventos adversos de alto risco, enquanto plataformas em nuvem facilitam o gerenciamento centralizado de casos de segurança, auditorias e submissões regulatórias. Essa combinação permite que as empresas farmacêuticas respondam de forma mais proativa às preocupações com a segurança.
- A integração perfeita dos sistemas de farmacovigilância com registros eletrônicos de saúde (EHRs), sistemas de gerenciamento de ensaios clínicos (CTMS) e portais de relatórios regulatórios cria uma plataforma unificada para gerenciamento de segurança de medicamentos de ponta a ponta, melhorando a conformidade e a eficiência operacional.
- Essa tendência em direção a sistemas de farmacovigilância mais inteligentes, automatizados e interconectados está remodelando as expectativas da indústria em relação ao monitoramento da segurança de medicamentos. Consequentemente, empresas como a ArisGlobal e a Oracle Health Sciences estão desenvolvendo soluções habilitadas para IA com processamento automatizado de casos, detecção de sinais e recursos de relatórios baseados em nuvem.
- A demanda por soluções de farmacovigilância baseadas em IA e integradas à nuvem está crescendo rapidamente entre empresas farmacêuticas e organizações de pesquisa contratadas, à medida que reguladores e partes interessadas priorizam cada vez mais a segurança do paciente e a geração oportuna de relatórios de segurança.
Soluções de segurança de medicamentos na Europa e dinâmica do mercado de farmacovigilância
Motorista
Aumento dos requisitos regulatórios e aumento das atividades de pesquisa clínica
- O crescente rigor dos requisitos regulamentares na UE, combinado com um aumento nos ensaios clínicos e na vigilância pós-comercialização, é um impulsionador significativo para a crescente procura de soluções de farmacovigilância
- Por exemplo, em 2024, várias empresas farmacêuticas sediadas na UE adotaram plataformas de farmacovigilância habilitadas por IA para cumprir as diretrizes atualizadas de Boas Práticas de Farmacovigilância (BPF) da UE. Espera-se que tais estratégias proativas de conformidade impulsionem o crescimento do mercado no período previsto.
- À medida que os reguladores impõem padrões de relatórios de segurança mais rigorosos, as plataformas de segurança de medicamentos que fornecem relatórios automatizados, rastreamento de casos e painéis em tempo real estão se tornando ferramentas essenciais para as empresas farmacêuticas.
- Além disso, a crescente complexidade dos pipelines de medicamentos, produtos biológicos e terapias combinadas está a impulsionar a adopção de soluções avançadas de farmacovigilância, capazes de gerir grandes volumes de dados de segurança de forma eficiente.
- Plataformas centralizadas e baseadas em nuvem que facilitam a colaboração entre os departamentos clínicos, regulatórios e de segurança aumentam a eficiência geral e a precisão do gerenciamento de segurança de medicamentos, impulsionando ainda mais a adoção pelo mercado
Restrição/Desafio
Preocupações com a privacidade de dados e altos custos de implementação
- Preocupações com a privacidade dos dados dos pacientes, a conformidade com o GDPR e a segurança das plataformas de farmacovigilância baseadas em nuvem representam desafios significativos para uma adoção mais ampla pelo mercado. Informações sensíveis dos pacientes exigem criptografia rigorosa, controles de acesso e armazenamento seguro de dados para manter a confiança e cumprir as regulamentações.
- Por exemplo, violações de dados de alto perfil em sistemas de TI de saúde aumentaram a conscientização sobre riscos potenciais, tornando algumas empresas cautelosas na adoção de novas soluções digitais de farmacovigilância.
- Enfrentar esses desafios por meio de medidas robustas de segurança cibernética, auditorias regulares de sistemas e treinamento de funcionários sobre protocolos de conformidade é fundamental para gerar confiança entre os usuários. Além disso, o alto investimento inicial necessário para implementar sistemas avançados de farmacovigilância baseados em nuvem e baseados em IA pode ser uma barreira, especialmente para pequenas e médias empresas farmacêuticas.
- Embora as soluções modulares e baseadas em assinatura estejam ajudando a reduzir os custos iniciais, a despesa percebida de plataformas sofisticadas de farmacovigilância ainda pode dificultar a adoção, especialmente entre organizações preocupadas com os custos.
- Superar esses desafios por meio de soluções seguras, escaláveis e econômicas, juntamente com o suporte à conformidade regulatória e o treinamento do usuário, será vital para o crescimento sustentado no mercado europeu de soluções de segurança de medicamentos e farmacovigilância.
Escopo do mercado de soluções de segurança de medicamentos e farmacovigilância na Europa
O mercado é segmentado com base no tipo, produto, funcionalidade, entrega, usuários finais e canal de distribuição.
- Por tipo
Com base no tipo, o mercado europeu de soluções de segurança de medicamentos e farmacovigilância é segmentado em software e serviços. O segmento de software dominou o mercado, com a maior participação na receita, de 57,4% em 2024, impulsionado pela crescente adoção de sistemas automatizados para notificação de eventos adversos, detecção de sinais e conformidade regulatória. Essas soluções de software são cada vez mais preferidas por empresas farmacêuticas e organizações de pesquisa contratadas (CROs) devido à sua capacidade de lidar com grandes volumes de dados de segurança, garantir monitoramento em tempo real e integrar-se perfeitamente a prontuários eletrônicos de saúde (PEPs), sistemas de gerenciamento de ensaios clínicos (CTMS) e portais de relatórios regulatórios.
Prevê-se que o segmento de serviços apresente a taxa de crescimento mais rápida, de 11,8%, entre 2025 e 2032, impulsionado pela crescente demanda por atividades terceirizadas de farmacovigilância, incluindo processamento de casos, auditorias de segurança, suporte a submissões regulatórias e gerenciamento de sinais. Isso é particularmente evidente entre pequenas e médias empresas farmacêuticas que podem não ter a infraestrutura ou a expertise para gerenciar a farmacovigilância internamente, o que leva a uma maior dependência de prestadores de serviços terceirizados.
- Por produto
Com base no produto, o mercado europeu de soluções de segurança de medicamentos e farmacovigilância é segmentado em soluções de formulário padrão e formulário personalizado. O segmento de formulário padrão deteve a maior participação de mercado na receita em 2024, devido à sua ampla aplicabilidade, facilidade de implantação e conformidade com os requisitos regulatórios comuns em todos os países da UE. Soluções padronizadas fornecem uma estrutura consistente para a notificação de eventos adversos, simplificando o treinamento e garantindo o alinhamento regulatório.
Espera-se que o segmento de formulários personalizados apresente um crescimento mais acelerado entre 2025 e 2032, impulsionado pela crescente necessidade de fluxos de trabalho de farmacovigilância personalizados, alinhados aos processos internos, protocolos de ensaios clínicos e sistemas de gerenciamento de dados de empresas farmacêuticas e de biotecnologia específicas. Soluções personalizadas permitem flexibilidade para portfólios de medicamentos complexos, áreas terapêuticas especializadas e requisitos de relatórios exclusivos, o que está se tornando um diferencial fundamental no cenário competitivo.
- Por funcionalidade
Com base na funcionalidade, o mercado europeu de soluções de segurança de medicamentos e farmacovigilância é segmentado em software de notificação de eventos adversos (AERS), software de auditoria de segurança de medicamentos e software de rastreamento de problemas. O segmento AERS dominou o mercado com uma participação de 43,5% em 2024, sendo fundamental para a captura, o processamento e a análise eficientes de relatórios de reações adversas a medicamentos nas fases clínica e pós-comercialização. O AERS garante a conformidade com as diretrizes da EMA e facilita a notificação de segurança em tempo hábil.
A previsão é de que o software de rastreamento de problemas registre forte crescimento durante o período previsto, auxiliando organizações no monitoramento, investigação e resolução rápida de problemas de segurança, minimizando riscos e garantindo a adesão às diretrizes da Agência Europeia de Medicamentos (EMA) e outras estruturas regulatórias. Essa funcionalidade apoia a gestão proativa de riscos e aumenta a confiabilidade dos sistemas de farmacovigilância.
- Por entrega
Com base na entrega, o mercado europeu de soluções de segurança de medicamentos e farmacovigilância é segmentado em modo de entrega no local e modo de entrega sob demanda/baseado em nuvem (SaaS). O segmento sob demanda/baseado em nuvem dominou em 2024, com uma participação de receita de 52%, devido a benefícios como escalabilidade, atualizações em tempo real, acesso centralizado aos dados, menor investimento inicial e capacidade de oferecer suporte a equipes geograficamente distribuídas. Plataformas baseadas em nuvem também facilitam atualizações de software, integração com análises baseadas em IA e relatórios regulatórios integrados.
O segmento on-premise continua a crescer de forma constante durante o período previsto, sendo preferido por organizações com protocolos rigorosos de segurança de dados, infraestrutura interna de TI e requisitos de conformidade rigorosos que exigem hospedagem local de dados sensíveis de farmacovigilância. Elas oferecem hospedagem local de dados sensíveis de farmacovigilância e maior controle sobre conformidade e fluxos de trabalho internos.
- Por usuários finais
Com base nos usuários finais, o mercado europeu de soluções de segurança de medicamentos e farmacovigilância é segmentado em empresas de biotecnologia e farmacêuticas, organizações de pesquisa contratadas (CROs), hospitais, KPOs/BPOs e prestadores de serviços de saúde. As empresas de biotecnologia e farmacêuticas detiveram a maior fatia da receita, 46%, em 2024, impulsionadas pelo alto volume de dados de segurança de medicamentos gerados durante ensaios clínicos e vigilância pós-comercialização, bem como pela necessidade crítica de cumprir as rigorosas regulamentações de farmacovigilância da UE.
Prevê-se que as CROs testemunhem o crescimento mais rápido devido à crescente terceirização de tarefas de farmacovigilância, à rápida expansão das atividades de ensaios clínicos e à adoção de soluções de IA e monitoramento em nuvem para gerenciar dados de segurança em diversos clientes e países. A expansão dos ensaios clínicos e a adoção de soluções de IA e monitoramento em nuvem para gerenciar dados de segurança em diversos clientes e países são os principais impulsionadores.
- Por canal de distribuição
Com base no canal de distribuição, o mercado europeu de soluções de segurança de medicamentos e farmacovigilância é segmentado em vendas diretas e vendas no varejo. O segmento de vendas diretas dominou em 2024, respondendo por 65% da receita do mercado, visto que empresas farmacêuticas e de biotecnologia preferem comprar soluções diretamente de fornecedores para garantir personalização, suporte dedicado, serviços de integração e garantia de conformidade. Isso garante personalização, suporte dedicado, serviços de integração e garantia de conformidade regulatória.
As vendas no varejo, incluindo revendedores e distribuidores terceirizados, estão crescendo de forma constante durante o período previsto, principalmente para soluções de software padronizadas adotadas por provedores de saúde de menor porte, empresas farmacêuticas emergentes e CROs. O crescimento das vendas no varejo é sustentado por modelos baseados em assinatura, ofertas em pacote e maior conscientização sobre soluções de farmacovigilância com boa relação custo-benefício no mercado. O crescimento é ainda sustentado por modelos baseados em assinatura, ofertas em pacote e pela crescente conscientização sobre soluções de farmacovigilância com boa relação custo-benefício.
Análise regional do mercado de soluções de segurança de medicamentos e farmacovigilância na Europa
- A Alemanha dominou o mercado europeu de soluções de segurança de medicamentos e farmacovigilância com a maior participação na receita de 39% em 2024, impulsionada por seus altos gastos com saúde, forte presença de empresas farmacêuticas e organizações de pesquisa contratadas bem estabelecidas que adotam ativamente sistemas avançados de monitoramento de segurança.
- Empresas na Alemanha estão adotando cada vez mais softwares e serviços avançados de farmacovigilância para garantir a conformidade com as Boas Práticas de Farmacovigilância (BPF) da UE e outros requisitos regulatórios. Essa adoção é ainda apoiada pela sólida infraestrutura de pesquisa do país, pelo alto volume de ensaios clínicos e pelo foco crescente na segurança do paciente e na gestão de riscos.
- A adopção generalizada destas soluções em toda a Europa é apoiada por uma supervisão regulamentar rigorosa, pela crescente consciencialização sobre a segurança dos medicamentos e pela crescente complexidade dos processos de desenvolvimento de medicamentos, tornando os sistemas de farmacovigilância ferramentas essenciais para garantir a conformidade e a segurança dos doentes, tanto nas fases clínica como pós-comercialização.
Visão do mercado de soluções de segurança de medicamentos e farmacovigilância na Alemanha
O mercado alemão de soluções de segurança de medicamentos e farmacovigilância captou a maior fatia da receita, de 39%, em 2024, impulsionado pela indústria farmacêutica consolidada do país, por uma estrutura regulatória robusta e pelo aumento das atividades de ensaios clínicos. Empresas farmacêuticas e organizações de pesquisa contratadas (CROs) estão priorizando a adoção de soluções de farmacovigilância habilitadas por IA e baseadas em nuvem para garantir a conformidade com as Boas Práticas de Farmacovigilância (BPF) da UE e agilizar a notificação de eventos adversos. A ênfase na segurança do paciente, na gestão de riscos e na integração com prontuários eletrônicos de saúde (PEPs) e sistemas de gestão de ensaios clínicos impulsiona ainda mais o crescimento do mercado.
Visão do mercado de soluções de segurança de medicamentos e farmacovigilância na França
O mercado francês de soluções de segurança de medicamentos e farmacovigilância deverá crescer a um CAGR substancial durante o período previsto, impulsionado pelo aumento dos investimentos em saúde, pela expansão da infraestrutura de pesquisa clínica e pela crescente demanda por monitoramento automatizado da segurança de medicamentos. As empresas farmacêuticas francesas estão adotando plataformas de farmacovigilância baseadas em nuvem para melhorar a eficiência operacional, garantir a conformidade regulatória e permitir o monitoramento centralizado de eventos adversos em vários locais.
Insights sobre o mercado de soluções de segurança de medicamentos e farmacovigilância no Reino Unido
O mercado de soluções de segurança de medicamentos e farmacovigilância do Reino Unido deverá crescer a uma taxa composta de crescimento anual (CAGR) expressiva, impulsionado pela adoção de softwares e serviços avançados de farmacovigilância tanto em empresas farmacêuticas quanto em provedores de saúde. O foco crescente na segurança do paciente, a supervisão regulatória rigorosa e o crescente volume de ensaios clínicos estão incentivando o uso de plataformas de processamento de casos, detecção de sinais e relatórios baseados em nuvem, impulsionadas por IA. Uma infraestrutura digital robusta e um ecossistema robusto de pesquisa contratada estão impulsionando ainda mais a adoção.
Soluções de segurança de medicamentos e visão de mercado de farmacovigilância na Itália
Espera-se que o mercado italiano de soluções de segurança de medicamentos e farmacovigilância se expanda de forma constante durante o período previsto, impulsionado pela crescente conscientização sobre segurança de medicamentos, iniciativas governamentais para aprimorar as práticas de farmacovigilância e pela crescente terceirização de atividades de monitoramento de segurança para CROs. A adoção de soluções de software padronizadas e personalizadas para relatórios de eventos adversos e gestão de conformidade está ganhando força entre as empresas farmacêuticas que operam na Itália.
Visão do mercado de soluções de segurança de medicamentos e farmacovigilância na Espanha
O mercado espanhol de soluções de segurança de medicamentos e farmacovigilância está crescendo devido ao crescente número de ensaios clínicos, ao aumento dos gastos com saúde e à necessidade de sistemas eficientes de gestão de eventos adversos. Plataformas de farmacovigilância baseadas em nuvem e serviços terceirizados estão sendo cada vez mais adotados para agilizar a geração de relatórios, garantir a conformidade regulatória e gerenciar dados de segurança com eficiência em diversas unidades de saúde e organizações de pesquisa.
Participação no mercado de soluções de segurança de medicamentos e farmacovigilância na Europa
O setor de soluções de segurança de medicamentos e farmacovigilância da Europa é liderado principalmente por empresas bem estabelecidas, incluindo:
- IQVIA (EUA)
- Parexel International (MA) Corporation (EUA)
- Syneos Health (EUA)
- ICON plc (Irlanda)
- Cognizant (EUA)
- Accenture (Irlanda)
- ArisGlobal (EUA)
- Genpact (EUA)
- Flex Databases (Reino Unido)
- Asphalion (Espanha)
- Teste em tempo real (Reino Unido)
- Biologit (Bélgica)
- Eurocept Pharmaceuticals (Holanda)
- Qinecsa (Reino Unido)
- Grupo Aixial (França)
- Shionogi BV (Holanda)
- F. Hoffmann-La Roche Ltd (Suíça)
- CSL (Austrália)
Quais são os desenvolvimentos recentes no mercado europeu de soluções de segurança de medicamentos e farmacovigilância?
- Em julho de 2025, a Comissão Europeia adotou um Regulamento de Execução que atualiza as regras para as atividades de farmacovigilância. Este regulamento, que entrará em vigor no início de 2026, visa esclarecer e fortalecer a farmacovigilância, reduzindo também os encargos administrativos. As principais atualizações incluem a exigência de que os titulares de autorização de introdução no mercado documentem apenas desvios "maiores ou críticos" no seu Ficheiro Mestre do Sistema de Farmacovigilância (PSMF) e uma clarificação das suas obrigações de utilização de dados da base de dados EudraVigilance para a gestão de sinais.
- Em junho de 2025, a Comissão Europeia apresentou o Pacote Farmacêutico da UE de 2025, que inclui regulamentos para a autorização e supervisão de medicamentos e regras para a Agência Europeia de Medicamentos. Este pacote visa agilizar procedimentos e impulsionar o desenvolvimento de medicamentos na UE.
- Em maio de 2025, um relatório preliminar destacou o papel crescente da Inteligência Artificial (IA) e do Aprendizado de Máquina (AM) na farmacovigilância. O relatório descreve as principais etapas para que empresas de ciências da vida implementem IA em atividades de segurança pós-comercialização, enfatizando a necessidade de conformidade com a Lei de IA da UE e o cenário regulatório em evolução nos EUA.
- Em agosto de 2024, a Agência Europeia de Medicamentos (EMA) implementou a revisão do Módulo XVI das Boas Práticas de Farmacovigilância (BPF). Esta atualização introduziu o Adendo II, que fornece orientações detalhadas sobre a avaliação da eficácia das medidas de minimização de riscos por meio de fontes de dados estruturadas e métodos de busca avançados.
- Em julho de 2021, a Asphalion, consultoria líder europeia em assuntos regulatórios, lançou uma nova Rede de Contatos Locais da UE para fornecer suporte local à farmacovigilância em todos os países da UE. Esta iniciativa teve como objetivo implementar soluções globais para a externalização de serviços de farmacovigilância, incluindo a Pessoa Qualificada Europeia para Farmacovigilância (EU-QPPv) e a Terceirização de Sistemas de Farmacovigilância.
SKU-
Obtenha acesso online ao relatório sobre a primeira nuvem de inteligência de mercado do mundo
- Painel interativo de análise de dados
- Painel de análise da empresa para oportunidades de elevado potencial de crescimento
- Acesso de analista de pesquisa para personalização e customização. consultas
- Análise da concorrência com painel interativo
- Últimas notícias, atualizações e atualizações Análise de tendências
- Aproveite o poder da análise de benchmark para um rastreio abrangente da concorrência
Metodologia de Investigação
A recolha de dados e a análise do ano base são feitas através de módulos de recolha de dados com amostras grandes. A etapa inclui a obtenção de informações de mercado ou dados relacionados através de diversas fontes e estratégias. Inclui examinar e planear antecipadamente todos os dados adquiridos no passado. Da mesma forma, envolve o exame de inconsistências de informação observadas em diferentes fontes de informação. Os dados de mercado são analisados e estimados utilizando modelos estatísticos e coerentes de mercado. Além disso, a análise da quota de mercado e a análise das principais tendências são os principais fatores de sucesso no relatório de mercado. Para saber mais, solicite uma chamada de analista ou abra a sua consulta.
A principal metodologia de investigação utilizada pela equipa de investigação do DBMR é a triangulação de dados que envolve a mineração de dados, a análise do impacto das variáveis de dados no mercado e a validação primária (especialista do setor). Os modelos de dados incluem grelha de posicionamento de fornecedores, análise da linha de tempo do mercado, visão geral e guia de mercado, grelha de posicionamento da empresa, análise de patentes, análise de preços, análise da quota de mercado da empresa, normas de medição, análise global versus regional e de participação dos fornecedores. Para saber mais sobre a metodologia de investigação, faça uma consulta para falar com os nossos especialistas do setor.
Personalização disponível
A Data Bridge Market Research é líder em investigação formativa avançada. Orgulhamo-nos de servir os nossos clientes novos e existentes com dados e análises que correspondem e atendem aos seus objetivos. O relatório pode ser personalizado para incluir análise de tendências de preços de marcas-alvo, compreensão do mercado para países adicionais (solicite a lista de países), dados de resultados de ensaios clínicos, revisão de literatura, mercado remodelado e análise de base de produtos . A análise de mercado dos concorrentes-alvo pode ser analisada desde análises baseadas em tecnologia até estratégias de carteira de mercado. Podemos adicionar quantos concorrentes necessitar de dados no formato e estilo de dados que procura. A nossa equipa de analistas também pode fornecer dados em tabelas dinâmicas de ficheiros Excel em bruto (livro de factos) ou pode ajudá-lo a criar apresentações a partir dos conjuntos de dados disponíveis no relatório.