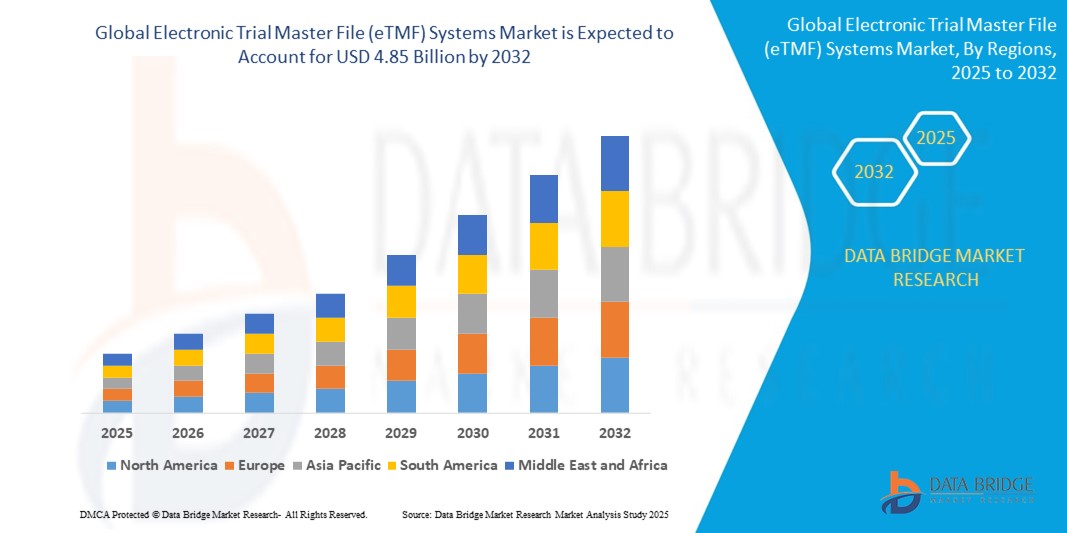
Global Electronic Trial Master File Etmf Systems Market
Размер рынка в млрд долларов США
CAGR :
% 
 USD
1.84 Billion
USD
4.85 Billion
2024
2032
USD
1.84 Billion
USD
4.85 Billion
2024
2032
| 2025 –2032 | |
| USD 1.84 Billion | |
| USD 4.85 Billion | |
|
|
|
|
Сегментация мирового рынка систем электронных основных файлов судебных решений (eTMF) по компонентам (услуги и программное обеспечение), способу доставки (облачный eTMF и локальный eTMF), конечному пользователю (фармацевтические и биотехнологические компании, CRO и другие) — тенденции отрасли и прогноз до 2032 года
Размер рынка систем электронных судебных мастер-файлов (eTMF)
- Объем мирового рынка систем электронных основных файлов судебных разбирательств (eTMF) оценивался в 1,84 млрд долларов США в 2024 году и, как ожидается , достигнет 4,85 млрд долларов США к 2032 году при среднегодовом темпе роста 12,90% в течение прогнозируемого периода.
- Рост рынка во многом обусловлен растущим спросом на централизованное управление данными клинических испытаний, соблюдением нормативных требований и растущим внедрением цифровых платформ в клинических исследованиях в фармацевтическом и биотехнологическом секторах.
- Растущее число клинических испытаний во всем мире, особенно на развивающихся рынках, и потребность в доступе к документам испытаний в режиме реального времени еще больше ускоряют внедрение систем электронных мастер-файлов испытаний (eTMF) среди спонсоров и контрактных исследовательских организаций.
Анализ рынка систем электронных судебных мастер-файлов (eTMF)
- Рынок электронных систем основных файлов клинических испытаний демонстрирует устойчивый рост, поскольку фармацевтические и биотехнологические компании все чаще внедряют цифровые решения для управления клиническими документами.
- Рост активности клинических испытаний и необходимость эффективных процессов обеспечения соответствия нормативным требованиям побуждают организации переходить от бумажных систем к облачным платформам.
- Северная Америка доминировала на рынке систем электронных основных файлов клинических испытаний (eTMF) с наибольшей долей выручки в 49,5% в 2024 году, что обусловлено высокой концентрацией фармацевтических и биотехнологических компаний, значительными инвестициями в НИОКР, хорошо развитой ИТ-инфраструктурой здравоохранения и растущим числом сложных клинических испытаний, требующих эффективного документирования и соблюдения требований.
- Ожидается, что Азиатско-Тихоокеанский регион станет свидетелем самых высоких темпов роста мирового рынка систем электронных основных файлов судебных разбирательств (eTMF), что обусловлено ростом урбанизации, ростом располагаемых доходов, технологическим прогрессом в таких странах, как Китай, Япония и Индия, а также растущей популярностью умных домов, поддерживаемой государственными инициативами по цифровизации.
- Сегмент услуг занял самую большую долю рынка в 2024 году благодаря существенным предложениям на протяжении всего жизненного цикла системы, включая внедрение, обучение, техническую поддержку и миграцию данных.
Сегментация рынка систем сферы охвата отчета и электронного основного файла судебного разбирательства (eTMF)
|
Атрибуты |
Ключевые аспекты рынка систем электронного судебного мастер-файла (eTMF) |
|
Охваченные сегменты |
|
|
Страны действия |
Северная Америка
Европа
Азиатско-Тихоокеанский регион
Ближний Восток и Африка
Южная Америка
|
|
Ключевые игроки рынка |
|
|
Рыночные возможности |
|
|
Информационные наборы данных с добавленной стоимостью |
Помимо информации о рыночных сценариях, таких как рыночная стоимость, темпы роста, сегментация, географический охват и основные игроки, рыночные отчеты, подготовленные Data Bridge Market Research, также включают в себя углубленный экспертный анализ, географически представленные данные о производстве и мощностях компаний, схемы сетей дистрибьюторов и партнеров, подробный и обновленный анализ ценовых тенденций и анализ дефицита цепочки поставок и спроса. |
Тенденции рынка систем электронных судебных мастер-файлов (eTMF)
«Интеграция искусственного интеллекта для автоматизации рабочих процессов»
- Искусственный интеллект все чаще интегрируется в электронные системы основных файлов судебных дел для автоматизации повторяющихся задач, таких как классификация документов и маркировка метаданных.
- Эта тенденция повышает эффективность и сокращает количество ошибок, совершаемых вручную, позволяя специалистам по клиническим исследованиям больше сосредоточиться на стратегических задачах и задачах, связанных с соблюдением требований.
- Например, платформы на базе искусственного интеллекта могут автоматически индексировать документы клинических испытаний и отмечать недостающие файлы, обеспечивая большую точность и соответствие нормативным требованиям.
- Такие компании, как Veeva Systems и Phlexglobal, внедряют возможности искусственного интеллекта для оптимизации процессов eTMF и предоставления информации о статусе испытаний в режиме реального времени.
- С ростом объемов клинических данных интеграция ИИ становится необходимым условием для улучшения процесса принятия решений и ускорения жизненного цикла клинических испытаний.
Динамика рынка систем электронных судебных мастер-файлов (eTMF)
Водитель
«Переход к цифровизации в управлении клиническими испытаниями»
- Переход к цифровизации стимулирует внедрение электронных систем основных файлов клинических испытаний, поскольку клинические испытания становятся все более сложными и требуют более эффективного управления документами.
- Эти системы обеспечивают централизованный доступ к пробным документам, что позволяет ускорить поиск, организовать совместную работу в режиме реального времени и улучшить контроль версий в разных группах.
- Например, крупные фармацевтические компании, такие как Pfizer, внедрили цифровые платформы управления испытаниями для оптимизации документации и обеспечения соответствия нормативным требованиям.
- Цифровые системы помогают снизить риски, связанные с ошибками, допущенными вручную, утерей документов и задержкой подачи документов, что в конечном итоге повышает качество и сроки судебных разбирательств.
- Удаленный доступ и функции безопасного облачного хранения делают эти системы незаменимыми для организаций, стремящихся повысить эффективность работы и соответствовать мировым нормативным стандартам.
Сдержанность/Вызов
«Проблемы безопасности данных и соответствия требованиям»
- Проблемы безопасности данных и соблюдения нормативных требований остаются основными препятствиями для внедрения электронных систем основных файлов испытаний в индустрии клинических исследований.
- Данные клинических испытаний крайне конфиденциальны, и любое нарушение может привести к серьезным последствиям, таким как задержка судебных процессов, правовые последствия и ущерб репутации организации.
- Например, сообщение об утечке данных в европейской организации клинических исследований привело к регулирующим расследованиям и задержке сроков испытаний, что подчеркнуло связанные с этим риски.
- Соблюдение меняющихся международных правил, таких как Общий регламент по защите данных и Закон о переносимости и подотчетности медицинского страхования, требует постоянных обновлений и региональных протоколов.
- Малые и средние организации часто сталкиваются с трудностями в обеспечении необходимой инфраструктуры и экспертных знаний в области кибербезопасности, что ограничивает их возможность полного перехода на облачные платформы eTMF.
Сфера применения систем электронного судебного мастер-файла (eTMF) на рынке
Рынок сегментирован по принципу компонентов, способа доставки и конечного пользователя.
- По компонентам
По компонентному составу рынок систем eTMF сегментируется на услуги и программное обеспечение. Сегмент услуг занял наибольшую долю рынка в 2024 году благодаря предложениям на протяжении всего жизненного цикла системы, включая внедрение, обучение, техническую поддержку и миграцию данных.
Прогнозируется, что сегмент программного обеспечения будет демонстрировать самые быстрые темпы роста в период с 2025 по 2032 год, поскольку организации все чаще используют специализированные платформы eTMF для централизованного управления документами и соблюдения нормативных требований.
- По способу доставки
По способу доставки рынок систем eTMF сегментируется на облачные eTMF и локальные eTMF. Сегмент облачных eTMF занял наибольшую долю рынка в 2024 году благодаря повышенной доступности, гибкости, экономической эффективности и масштабируемости.
Прогнозируется, что сегмент локальных eTMF-решений будет демонстрировать самые высокие темпы роста в период с 2025 по 2032 год и по-прежнему будет актуален для организаций, отдающих приоритет полному контролю над безопасностью данных и инфраструктурой, что часто обусловлено особой нормативной или внутренней ИТ-политикой.
- Конечным пользователем
По типу конечного пользователя рынок систем eTMF сегментируется на фармацевтические и биотехнологические компании, контрактные исследовательские организации (CRO) и другие. Сегмент фармацевтических и биотехнологических компаний занял наибольшую долю рынка по выручке в 2024 году благодаря всё более сложным клиническим испытаниям, глобализации и строгим нормативным требованиям.
Прогнозируется, что контрактные исследовательские организации (КИО) будут демонстрировать самые высокие темпы роста в период с 2025 по 2032 год, поскольку они все чаще используют системы eTMF для эффективного управления разнообразными испытаниями для разных спонсоров.
Региональный анализ рынка систем электронных судебных мастер-файлов (eTMF)
- Северная Америка доминировала на рынке систем электронных основных файлов клинических испытаний (eTMF) с наибольшей долей выручки в 49,5% в 2024 году, что обусловлено высокой концентрацией фармацевтических и биотехнологических компаний, значительными инвестициями в НИОКР, хорошо развитой ИТ-инфраструктурой здравоохранения и растущим числом сложных клинических испытаний, требующих эффективного документирования и соблюдения требований.
- Строгая нормативно-правовая база и особое внимание к целостности данных, что способствует созданию надежных и соответствующих требованиям eTMF решений для удовлетворения требований FDA и других органов здравоохранения.
- Широкое внедрение передовых облачных технологий и инициатив цифровой трансформации в организациях, проводящих клинические исследования, еще больше ускоряет внедрение и использование системы eTMF.
Обзор рынка систем электронного судебного мастер-файла (eTMF) в США
Рынок систем eTMF в США в 2024 году занимал самую большую долю выручки в Северной Америке (81%), чему способствовали строгие нормативные требования, растущая сложность и объём данных клинических исследований, а также повышенное внимание к готовности к аудиту. Активное внедрение облачных решений и государственная поддержка исследований и разработок в сфере здравоохранения дополнительно стимулируют расширение рынка.
Обзор рынка систем электронных судебных мастер-файлов (eTMF) в Европе
Прогнозируется, что европейский рынок будет демонстрировать самые высокие темпы роста в период с 2025 по 2032 год, что обусловлено растущим спросом на облачные решения, необходимостью улучшения обмена данными и взаимодействия между заинтересованными сторонами, а также меняющимися требованиями регулирующих органов. Регион также выигрывает от сильного акцента на инновациях и цифровой трансформации в секторе наук о жизни.
Обзор рынка систем электронных судебных мастер-файлов (eTMF) в Великобритании
Ожидается, что рынок систем eTMF в Великобритании будет демонстрировать самые высокие темпы роста в период с 2025 по 2032 год, что обусловлено увеличением числа клинических испытаний, особенно с учётом растущего акцента на децентрализованных и виртуальных исследованиях. Развитая фармацевтическая промышленность страны и проактивный подход к инициативам в области цифрового здравоохранения способствуют росту рынка.
Обзор рынка систем электронных судебных мастер-файлов (eTMF) в Германии
Прогнозируется, что рынок систем eTMF в Германии будет демонстрировать самые высокие темпы роста в период с 2025 по 2032 год, чему будут способствовать повышение осведомлённости о цифровой безопасности, строгие требования к соблюдению нормативных требований и спрос на технологически передовые решения в развитом фармацевтическом секторе страны. Акцент Германии на инновациях и мощная промышленная база дополнительно способствуют внедрению eTMF.
Обзор рынка систем электронных судебных мастер-файлов (eTMF) в Азиатско-Тихоокеанском регионе
Прогнозируется, что рынок систем eTMF в Азиатско-Тихоокеанском регионе будет демонстрировать самые высокие темпы роста в период с 2025 по 2032 год, что обусловлено ростом урбанизации, ростом располагаемых доходов и значительным технологическим прогрессом в таких странах, как Китай, Япония и Индия. Растущая в регионе тенденция к интеллектуальным клиническим операциям, поддерживаемая государственными инициативами по цифровизации, способствует внедрению систем eTMF.
Обзор рынка систем электронного судебного мастер-файла (eTMF) в Японии
Прогнозируется, что рынок систем eTMF в Японии будет демонстрировать самые высокие темпы роста в период с 2025 по 2032 год благодаря высокотехнологичной культуре страны, быстрой урбанизации и растущему вниманию к целостности данных и соблюдению нормативных требований. Рынок уделяет большое внимание безопасности и эффективности, а его внедрение обусловлено ростом числа клинических испытаний и интеграцией eTMF с другими цифровыми клиническими решениями.
Обзор рынка систем электронных судебных мастер-файлов (eTMF) в Китае
В 2024 году китайский рынок систем eTMF обеспечил наибольшую долю выручки в Азиатско-Тихоокеанском регионе, что обусловлено ростом среднего класса в стране, быстрой урбанизацией и высокими темпами внедрения технологий в здравоохранение. Китай является важным центром клинических исследований благодаря развитым отечественным производителям и государственной поддержке цифровой трансформации, что способствует внедрению eTMF в жилых, коммерческих и исследовательских учреждениях.
Доля рынка систем электронных судебных мастер-файлов (eTMF)
Лидерами отрасли систем электронных основных судебных файлов (eTMF) являются в первую очередь хорошо зарекомендовавшие себя компании, в том числе:
- IQVIA Inc. (США)
- Labcorp Drug Development (США)
- TransPerfect (США)
- Oracle (США)
- Phlexglobal (США)
- SureClinical Inc. (США)
- Aurea, Inc. (США)
- Veeva Systems (США)
- MasterControl Solutions, Inc. (США)
- Clinevo Technologies (Индия)
- Фонд медицинского образования и исследований Майо (MFMER) (США)
- Montrium Inc. (США)
- NCGD Inc. (США)
- PharmaVigilance (США)
Последние разработки на мировом рынке систем электронных судебных мастер-файлов (eTMF)
- В феврале 2023 года компания Vial совместно с Egnyte интегрировала решение Egnyte eTMF в свою платформу. Это решение призвано оптимизировать обработку документов и данных, обеспечить соответствие требованиям 21 CFR Часть 11 и повысить готовность к аудиту для компаний в области естественных наук, что в конечном итоге повысит эффективность и соблюдение нормативных требований в клинических исследованиях.
- В сентябре 2022 года компания Montrium запустила услуги и образовательные тренинги по TMF под руководством экспертов. Эта инициатива направлена на поддержку клинических операций и команд TMF на протяжении всего процесса клинической разработки, предоставляя необходимую поддержку и знания для оптимизации управления исследованиями и обеспечения целостности данных на рынке.
- В июне 2022 года компания Anju Software Inc. запустила eTMF Master, новое облачное программное обеспечение eTMF. Это решение упрощает взаимодействие между спонсорами, CRO и исследовательскими центрами для эффективного и безопасного управления контентом клинических исследований с соблюдением нормативных требований, тем самым ускоряя рабочие процессы и улучшая общее соответствие требованиям клинических исследований.
- В апреле 2021 года компания Phlexglobal анонсировала решение TMF Quality Review. Это решение, предназначенное для фармацевтических компаний, особенно мировых лидеров, помогает оценивать и минимизировать регуляторные риски при слияниях и поглощениях, значительно повышая готовность к проверкам и обеспечивая качество данных на всем рынке.
SKU-
Получите онлайн-доступ к отчету на первой в мире облачной платформе рыночной аналитики
- Интерактивная панель анализа данных
- Панель анализа компании для возможностей с высоким потенциалом роста
- Доступ аналитика-исследователя для настройки и запросов
- Анализ конкурентов с помощью интерактивной панели
- Последние новости, обновления и анализ тенденций
- Используйте возможности сравнительного анализа для комплексного отслеживания конкурентов
Содержание
1 ВВЕДЕНИЕ
1.1 ЦЕЛИ ИССЛЕДОВАНИЯ
1.2 ОПРЕДЕЛЕНИЕ РЫНКА
1.3 ОБЗОР МИРОВОГО РЫНКА СИСТЕМ ЭЛЕКТРОННЫХ СУДЕБНЫХ МАСТЕРА (ETMF)
1.4 ВАЛЮТА И ЦЕНЫ
1.5 ОГРАНИЧЕНИЕ
1.6 ОХВАТЫВАЕМЫЕ РЫНКИ
2 СЕГМЕНТАЦИЯ РЫНКА
2.1 ОСНОВНЫЕ ВЫВОДЫ
2.2 ВЫХОД НА ГЛОБАЛЬНЫЙ РЫНОК СИСТЕМ ЭЛЕКТРОННЫХ СУДЕБНЫХ МАСТЕРА (ETMF)
2.2.1 СЕТКА ПОЗИЦИОНИРОВАНИЯ ПОСТАВЩИКА
2.2.2 КРИВАЯ ЛИНИИ ЖИЗНИ ТЕХНОЛОГИЙ
2.2.3 РУКОВОДСТВО ПО РЫНКУ
2.2.4 АНАЛИЗ РЫНОЧНОЙ ДОЛИ КОМПАНИИ
2.2.5 МНОГОМЕРНОЕ МОДЕЛИРОВАНИЕ
2.2.6 АНАЛИЗ СВЕРХУ ВНИЗ
2.2.7 СТАНДАРТЫ ИЗМЕРЕНИЯ
2.2.8 ТОЧКИ ДАННЫХ ИЗ КЛЮЧЕВЫХ ПЕРВИЧНЫХ ИНТЕРВЬЮ
2.2.9 ТОЧКИ ДАННЫХ ИЗ КЛЮЧЕВЫХ ВТОРИЧНЫХ БАЗ ДАННЫХ
2.3 Глобальный рынок систем электронных судебных дел (ETMF): обзор исследования
2.4 ПРЕДПОЛОЖЕНИЯ
3 ОБЗОР РЫНКА
3.1 ВОДИТЕЛИ
3.2 ОГРАНИЧЕНИЯ
3.3 ВОЗМОЖНОСТИ
3.4 ПРОБЛЕМЫ
4 КРАТКОЕ ОПИСАНИЕ
5 ПРЕМИАЛЬНЫХ ИНСАЙТОВ
5.1 ПЯТЬ СИЛ ПОРТЕРА
5.2 НОРМАТИВНЫЕ СТАНДАРТЫ
5.3 ТЕХНОЛОГИЧЕСКИЕ ТРЕНДЫ
5.4 ПАТЕНТНЫЙ АНАЛИЗ
5.5 ПРИМЕР ИЗ ПРАКТИКИ
5.6 АНАЛИЗ ЦЕПОЧКИ СОЗДАНИЯ СТОИМОСТИ
5.7 СРАВНИТЕЛЬНЫЙ АНАЛИЗ КОМПАНИЙ
5.8 АНАЛИЗ ЦЕН
6 ГЛОБАЛЬНЫЙ РЫНОК СИСТЕМ ЭЛЕКТРОННЫХ СУДЕБНЫХ МАСТЕРА (ETMF), ПРЕДЛАГАЯ
6.1 ОБЗОР
6.2 ПРОГРАММНОЕ ОБЕСПЕЧЕНИЕ
6.3 УСЛУГИ
6.3.1 ПРОФЕССИОНАЛЬНЫЕ УСЛУГИ
6.3.1.1. ОБУЧЕНИЕ И КОНСУЛЬТИРОВАНИЕ
6.3.1.2.РЕАЛИЗАЦИЯ
6.3.1.3. ПОДДЕРЖКА И ОБСЛУЖИВАНИЕ
6.3.2 УПРАВЛЯЕМЫЕ УСЛУГИ
7 МИРОВОЙ РЫНОК СИСТЕМ ЭЛЕКТРОННЫХ СУДЕБНЫХ МАСТЕРА (ETMF), ПО УРОВНЮ ДОКУМЕНТОВ
7.1 ОБЗОР
7.2 ДОКУМЕНТЫ УРОВНЯ ИССЛЕДОВАНИЯ
7.3 ДОКУМЕНТЫ НА УРОВНЕ СТРАНЫ
7.4 ДОКУМЕНТЫ УРОВНЯ САЙТА
8 ГЛОБАЛЬНЫЙ РЫНОК СИСТЕМ ЭЛЕКТРОННЫХ СУДЕБНЫХ МАСТЕРА (ETMF) ПО ОПЕРАЦИОННЫМ СИСТЕМАМ
8.1 ОБЗОР
8.2 ОКНА
8.3 ЛИНУКС
8.4 МАКС
8.5 МОБИЛЬНЫЕ
8.5.1 АНДРОИД
8.5.2 iPhone
8.5.3 iPad
9 ГЛОБАЛЬНЫЙ РЫНОК СИСТЕМ ЭЛЕКТРОННЫХ СУДЕБНЫХ ОСНОВНЫХ ФАЙЛОВ (ETMF) ПО РЕЖИМУ РАЗВЕРТЫВАНИЯ
9.1 ОБЗОР
9.2 НА ПОМЕЩЕНИИ
9.3 ОБЛАКО
9.3.1 ОБЩЕСТВЕННОСТЬ
9.3.2 ЧАСТНЫЙ
9.3.3 ГИБРИД
10 МИРОВОЙ РЫНОК СИСТЕМ ЭЛЕКТРОННЫХ СУДЕБНЫХ МАСТЕРА (ETMF) ПО ФУНКЦИОНАЛЬНОСТИ
10.1 ОБЗОР
10.2 КОМПЛЕКСНАЯ БЕЗОПАСНОСТЬ
10.3 ЗАГРУЗКА/СОЗДАНИЕ ДОКУМЕНТОВ
10.4 АУДИТ
10.5 МЕТАДАННЫЕ
10.6 КЛАССИФИКАЦИЯ И ИНДЕКСИРОВАНИЕ ДОКУМЕНТОВ
10.7 ХРАНЕНИЕ ДОКУМЕНТОВ
10.8 СБОР ДАННЫХ
10.9 ПОИСК И ИЗВЛЕЧЕНИЕ
10.1 ДРУГИЕ
11 МИРОВОЙ РЫНОК СИСТЕМ ЭЛЕКТРОННЫХ СУДЕБНЫХ МАСТЕРА (ETMF) ПО МОДЕЛИ ЦЕНООБРАЗОВАНИЯ
11.1 ОБЗОР
11.2 БЕСПЛАТНО
11.3 НА ОСНОВЕ ПОДПИСКИ
11.3.1 ГОДОВАЯ ПОДПИСКА
11.3.2 ЕЖЕМЕСЯЧНАЯ ПОДПИСКА
12 Глобальный рынок систем электронных судебных дел (ETMF) по конечному пользователю
12.1 ОБЗОР
12.2 БИОТЕХНОЛОГИЧЕСКИЕ И ФАРМАЦЕВТИЧЕСКИЕ КОМПАНИИ
12.2.1 ПУТЕМ ПРЕДЛОЖЕНИЯ
12.2.1.1. ПРОГРАММНОЕ ОБЕСПЕЧЕНИЕ
12.2.1.2.УСЛУГИ
12.2.1.2.1. ПРОФЕССИОНАЛЬНЫЕ УСЛУГИ
12.2.1.2.1.1 ОБУЧЕНИЕ И КОНСУЛЬТИРОВАНИЕ
12.2.1.2.1.2 РЕАЛИЗАЦИЯ
12.2.1.2.1.3 ПОДДЕРЖКА И ОБСЛУЖИВАНИЕ
12.2.1.2.2. УПРАВЛЯЕМЫЕ УСЛУГИ
12.3 КОНТРАКТНЫЕ ИССЛЕДОВАТЕЛЬСКИЕ ОРГАНИЗАЦИИ
12.3.1 ПУТЕМ ПРЕДЛОЖЕНИЯ
12.3.1.1. ПРОГРАММНОЕ ОБЕСПЕЧЕНИЕ
12.3.1.2.УСЛУГИ
12.3.1.2.1. ПРОФЕССИОНАЛЬНЫЕ УСЛУГИ
12.3.1.2.1.1 ОБУЧЕНИЕ И КОНСУЛЬТИРОВАНИЕ
12.3.1.2.1.2 РЕАЛИЗАЦИЯ
12.3.1.2.1.3 ПОДДЕРЖКА И ОБСЛУЖИВАНИЕ
12.3.1.2.2. УПРАВЛЯЕМЫЕ УСЛУГИ
12.4 СПОНСОРЫ
12.4.1 ПУТЕМ ПРЕДЛОЖЕНИЯ
12.4.1.1. ПРОГРАММНОЕ ОБЕСПЕЧЕНИЕ
12.4.1.2.УСЛУГИ
12.4.1.2.1. ПРОФЕССИОНАЛЬНЫЕ УСЛУГИ
12.4.1.2.1.1 ОБУЧЕНИЕ И КОНСУЛЬТИРОВАНИЕ
12.4.1.2.1.2 РЕАЛИЗАЦИЯ
12.4.1.2.1.3 ПОДДЕРЖКА И ОБСЛУЖИВАНИЕ
12.4.1.2.2. УПРАВЛЯЕМЫЕ УСЛУГИ
12.5 ДРУГИЕ
13 МИРОВОЙ РЫНОК СИСТЕМ ЭЛЕКТРОННЫХ СУДЕБНЫХ МАСТЕРА (ETMF) ПО ГЕОГРАФИИ
13.1 ГЛОБАЛЬНЫЙ РЫНОК СИСТЕМ ЭЛЕКТРОННЫХ СУДЕБНЫХ МАСТЕР-ФАЙЛОВ (ETMF) (ВСЯ СЕГМЕНТАЦИЯ, УКАЗАННАЯ ВЫШЕ, ПРЕДСТАВЛЕНА В ЭТОЙ ГЛАВЕ ПО СТРАНАМ)
13.1.1 СЕВЕРНАЯ АМЕРИКА
13.1.1.1. США
13.1.1.2.КАНАДА
13.1.1.3.МЕКСИКА
13.1.2 ЕВРОПА
13.1.2.1. ГЕРМАНИЯ
13.1.2.2.ФРАНЦИЯ
13.1.2.3.Великобритания
13.1.2.4.ИТАЛИЯ
13.1.2.5.ИСПАНИЯ
13.1.2.6.РОССИЯ
13.1.2.7. ТУРЦИЯ
13.1.2.8.БЕЛЬГИЯ
13.1.2.9. НИДЕРЛАНДЫ
13.1.2.10. НОРВЕГИЯ
13.1.2.11. ФИНЛЯНДИЯ
13.1.2.12. ШВЕЙЦАРИЯ
13.1.2.13. ДАНИЯ
13.1.2.14.ШВЕЦИЯ
13.1.2.15.ПОЛЬША
13.1.2.16. ОСТАЛЬНАЯ ЕВРОПА
13.1.3 АЗИАТСКО-ТИХООКЕАНСКИЙ РЕГИОН
13.1.3.1. ЯПОНИЯ
13.1.3.2.КИТАЙ
13.1.3.3. ЮЖНАЯ КОРЕЯ
13.1.3.4. ИНДИЯ
13.1.3.5. АВСТРАЛИЯ
13.1.3.6. НОВАЯ ЗЕЛАНДИЯ
13.1.3.7. СИНГАПУР
13.1.3.8.ТАИЛАНД
13.1.3.9. МАЛАЙЗИЯ
13.1.3.10. ИНДОНЕЗИЯ
13.1.3.11. ФИЛИППИНЫ
13.1.3.12. ТАЙВАНЬ
13.1.3.13. ВЬЕТНАМ
13.1.3.14. ОСТАЛЬНЫЕ СТРАНЫ АЗИАТСКО-ТИХООКЕАНСКОГО РЕГИОНА
13.1.4 ЮЖНАЯ АМЕРИКА
13.1.4.1. БРАЗИЛИЯ
13.1.4.2. АРГЕНТИНА
13.1.4.3 ОСТАЛЬНАЯ ЧАСТЬ ЮЖНОЙ АМЕРИКИ
13.1.5 БЛИЖНИЙ ВОСТОК И АФРИКА
13.1.5.1. ЮЖНАЯ АФРИКА
13.1.5.2.ЕГИПЕТ
13.1.5.3. САУДОВСКАЯ АРАВИЯ
13.1.5.4. ОАЭ
13.1.5.5. ОМАН
13.1.5.6. БАХРЕЙН
13.1.5.7.ИЗРАИЛЬ
13.1.5.8.КУВЕЙТ
13.1.5.9. КАТАР
13.1.5.10. ОСТАЛЬНОЙ БЛИЖНИЙ ВОСТОК И АФРИКА
13.2 ОСНОВНЫЕ ПЕРВИЧНЫЕ ПОКАЗАТЕЛИ: ПО ОСНОВНЫМ СТРАНАМ
14 Глобальный рынок систем электронных судебных дел (ETMF), ландшафт компаний
14.1 АНАЛИЗ АКЦИЙ КОМПАНИИ: ГЛОБАЛЬНЫЙ
14.2 АНАЛИЗ АКЦИЙ КОМПАНИИ: СЕВЕРНАЯ АМЕРИКА
14.3 АНАЛИЗ АКЦИЙ КОМПАНИИ: ЕВРОПА
14.4 АНАЛИЗ АКЦИЙ КОМПАНИИ: АЗИАТСКО-ТИХООКЕАНСКИЙ РЕГИОН
14.5 СЛИЯНИЯ И ПОГЛОЩЕНИЯ
14.6 РАЗРАБОТКА И УТВЕРЖДЕНИЕ НОВЫХ ПРОДУКТОВ
14.7 РАСШИРЕНИЯ
14.8 ИЗМЕНЕНИЯ В НОРМАТИВНОМ ПРАВЕ
14.9 ПАРТНЕРСТВО И ДРУГИЕ СТРАТЕГИЧЕСКИЕ РАЗВИТИЯ
15 Глобальный рынок систем электронных судебных решений (ETMF), SWOT-анализ и анализ DBMR
16 ГЛОБАЛЬНЫЙ РЫНОК СИСТЕМ ЭЛЕКТРОННЫХ СУДЕБНЫХ МАСТЕРА (ETMF), ПРОФИЛЬ КОМПАНИИ
16.1 АДИ Б
16.1.1 ОБЗОР КОМПАНИИ
16.1.2 АНАЛИЗ ДОХОДОВ
16.1.3 ГЕОГРАФИЧЕСКОЕ ПРИСУТСТВИЕ
16.1.4 ПОРТФЕЛЬ ПРОДУКТОВ
16.1.5 ПОСЛЕДНИЕ РАЗВИТИЯ
16.2 VEEVA MEDTECH (VEEVA SYSTEMS, INC)
16.2.1 ОБЗОР КОМПАНИИ
16.2.2 АНАЛИЗ ДОХОДОВ
16.2.3 ГЕОГРАФИЧЕСКОЕ ПРИСУТСТВИЕ
16.2.4 ПОРТФЕЛЬ ПРОДУКТОВ
16.2.5 ПОСЛЕДНИЕ РАЗВИТИЯ
16.3 ИНТЕРАКТИВНЫЙ ПРОБНЫЙ ВАРИАНТ
16.3.1 ОБЗОР КОМПАНИИ
16.3.2 АНАЛИЗ ДОХОДОВ
16.3.3 ГЕОГРАФИЧЕСКОЕ ПРИСУТСТВИЕ
16.3.4 ПОРТФЕЛЬ ПРОДУКТОВ
16.3.5 ПОСЛЕДНИЕ РАЗВИТИЯ
16.4 МЕДИДАНЫЕ (DASSAULT SYSTEMES)
16.4.1 ОБЗОР КОМПАНИИ
16.4.2 АНАЛИЗ ДОХОДОВ
16.4.3 ГЕОГРАФИЧЕСКОЕ ПРИСУТСТВИЕ
16.4.4 ПОРТФЕЛЬ ПРОДУКТОВ
16.4.5 ПОСЛЕДНИЕ РАЗВИТИЯ
16.5 OCTALSOFT (ГЛОРАНТ, ООО)
16.5.1 ОБЗОР КОМПАНИИ
16.5.2 АНАЛИЗ ДОХОДОВ
16.5.3 ГЕОГРАФИЧЕСКОЕ ПРИСУТСТВИЕ
16.5.4 ПОРТФЕЛЬ ПРОДУКТОВ
16.5.5 ПОСЛЕДНИЕ РАЗВИТИЯ
16.6 MASTERCONTROL SOLUTIONS, INC
16.6.1 ОБЗОР КОМПАНИИ
16.6.2 АНАЛИЗ ДОХОДОВ
16.6.3 ГЕОГРАФИЧЕСКОЕ ПРИСУТСТВИЕ
16.6.4 ПОРТФЕЛЬ ПРОДУКТОВ
16.6.5 ПОСЛЕДНИЕ РАЗВИТИЯ
16.7 IQVIA INC
16.7.1 ОБЗОР КОМПАНИИ
16.7.2 АНАЛИЗ ДОХОДОВ
16.7.3 ГЕОГРАФИЧЕСКОЕ ПРИСУТСТВИЕ
16.7.4 ПОРТФЕЛЬ ПРОДУКТОВ
16.7.5 ПОСЛЕДНИЕ РАЗВИТИЯ
16.8 CLOUDBYZ
16.8.1 ОБЗОР КОМПАНИИ
16.8.2 АНАЛИЗ ДОХОДОВ
16.8.3 ГЕОГРАФИЧЕСКОЕ ПРИСУТСТВИЕ
16.8.4 ПОРТФЕЛЬ ПРОДУКТОВ
16.8.5 ПОСЛЕДНИЕ РАЗВИТИЯ
16.9 ТЕХНОЛОГИИ CLINEVO
16.9.1 ОБЗОР КОМПАНИИ
16.9.2 АНАЛИЗ ДОХОДОВ
16.9.3 ГЕОГРАФИЧЕСКОЕ ПРИСУТСТВИЕ
16.9.4 ПОРТФЕЛЬ ПРОДУКТОВ
16.9.5 ПОСЛЕДНИЕ РАЗВИТИЯ
16.1 ЗДРАВООХРАНЕНИЕ ФЛОРЕНЦИИ
16.10.1 ОБЗОР КОМПАНИИ
16.10.2 АНАЛИЗ ДОХОДОВ
16.10.3 ГЕОГРАФИЧЕСКОЕ ПРИСУТСТВИЕ
16.10.4 ПОРТФЕЛЬ ПРОДУКТОВ
16.10.5 ПОСЛЕДНИЕ РАЗВИТИЯ
16.11 ОРАКУЛ
16.11.1 ОБЗОР КОМПАНИИ
16.11.2 АНАЛИЗ ДОХОДОВ
16.11.3 ГЕОГРАФИЧЕСКОЕ ПРИСУТСТВИЕ
16.11.4 ПОРТФЕЛЬ ПРОДУКТОВ
16.11.5 ПОСЛЕДНИЕ РАЗВИТИЯ
16.12 АРИСГЛОБАЛ ООО
16.12.1 ОБЗОР КОМПАНИИ
16.12.2 АНАЛИЗ ДОХОДОВ
16.12.3 ГЕОГРАФИЧЕСКОЕ ПРИСУТСТВИЕ
16.12.4 ПОРТФЕЛЬ ПРОДУКТОВ
16.12.5 ПОСЛЕДНИЕ РАЗВИТИЯ
16.13 МОНТРИУМ ИНК.
16.13.1 ОБЗОР КОМПАНИИ
16.13.2 АНАЛИЗ ДОХОДОВ
16.13.3 ГЕОГРАФИЧЕСКОЕ ПРИСУТСТВИЕ
16.13.4 ПОРТФЕЛЬ ПРОДУКТОВ
16.13.5 ПОСЛЕДНИЕ РАЗВИТИЯ
16.14 ВАЖНЕЙШИЕ РЕШЕНИЯ ДЛЯ ДАННЫХ
16.14.1 ОБЗОР КОМПАНИИ
16.14.2 АНАЛИЗ ДОХОДОВ
16.14.3 ГЕОГРАФИЧЕСКОЕ ПРИСУТСТВИЕ
16.14.4 ПОРТФЕЛЬ ПРОДУКТОВ
16.14.5 ПОСЛЕДНИЕ РАЗВИТИЯ
16.15 KEY2COMPLIANCE AB (SYMBIOTEQ)
16.15.1 ОБЗОР КОМПАНИИ
16.15.2 АНАЛИЗ ДОХОДОВ
16.15.3 ГЕОГРАФИЧЕСКОЕ ПРИСУТСТВИЕ
16.15.4 ПОРТФЕЛЬ ПРОДУКТОВ
16.15.5 ПОСЛЕДНИЕ РАЗВИТИЯ
16.16 DATARIVER SRL
16.16.1 ОБЗОР КОМПАНИИ
16.16.2 АНАЛИЗ ДОХОДОВ
16.16.3 ГЕОГРАФИЧЕСКОЕ ПРИСУТСТВИЕ
16.16.4 ПОРТФЕЛЬ ПРОДУКТОВ
16.16.5 ПОСЛЕДНИЕ РАЗВИТИЯ
16.17 ЭТИКА КРО
16.17.1 ОБЗОР КОМПАНИИ
16.17.2 АНАЛИЗ ДОХОДОВ
16.17.3 ГЕОГРАФИЧЕСКОЕ ПРИСУТСТВИЕ
16.17.4 ПОРТФЕЛЬ ПРОДУКТОВ
16.17.5 ПОСЛЕДНИЕ РАЗВИТИЯ
16.18 ИСПЫТАНИЕ (CLINBLOCKS BV)
16.18.1 ОБЗОР КОМПАНИИ
16.18.2 АНАЛИЗ ДОХОДОВ
16.18.3 ГЕОГРАФИЧЕСКОЕ ПРИСУТСТВИЕ
16.18.4 ПОРТФЕЛЬ ПРОДУКТОВ
16.18.5 ПОСЛЕДНИЕ РАЗВИТИЯ
16.19 ПРЕМЬЕР КОНСАЛТИНГ
16.19.1 ОБЗОР КОМПАНИИ
16.19.2 АНАЛИЗ ДОХОДОВ
16.19.3 ГЕОГРАФИЧЕСКОЕ ПРИСУТСТВИЕ
16.19.4 ПОРТФЕЛЬ ПРОДУКТОВ
16.19.5 ПОСЛЕДНИЕ РАЗВИТИЯ
16.2 PHLEXGLOBAL (компания PHARMALEX)
16.20.1 ОБЗОР КОМПАНИИ
16.20.2 АНАЛИЗ ДОХОДОВ
16.20.3 ГЕОГРАФИЧЕСКОЕ ПРИСУТСТВИЕ
16.20.4 ПОРТФЕЛЬ ПРОДУКТОВ
16.20.5 ПОСЛЕДНИЕ РАЗВИТИЯ
16.21 SURECLINICAL INC.
16.21.1 ОБЗОР КОМПАНИИ
16.21.2 АНАЛИЗ ДОХОДОВ
16.21.3 ГЕОГРАФИЧЕСКОЕ ПРИСУТСТВИЕ
16.21.4 ПОРТФЕЛЬ ПРОДУКТОВ
16.21.5 ПОСЛЕДНИЕ РАЗВИТИЯ
ПРИМЕЧАНИЕ: СПИСОК КОМПАНИЙ, ПРЕДСТАВЛЕННЫХ В ПРОФИЛЕ, НЕ ЯВЛЯЕТСЯ ПОЛНЫМ И СООТВЕТСТВУЕТ ТРЕБОВАНИЯМ НАШИХ ПРЕДЫДУЩИХ КЛИЕНТОВ. В НАШЕМ ИССЛЕДОВАНИИ МЫ РАССМАТРИВАЕМ БОЛЕЕ 100 КОМПАНИЙ, ПОЭТОМУ СПИСОК КОМПАНИЙ МОЖЕТ БЫТЬ ИЗМЕНЕН ИЛИ ЗАМЕНЕН ПО ЗАПРОСУ.
17 ЗАКЛЮЧЕНИЕ
18 АНКЕТА
19 СВЯЗАННЫХ ОТЧЕТОВ
20 О МАРКЕТИНГОВЫХ ИССЛЕДОВАНИЯХ DATA BRIDGE
Методология исследования
Сбор данных и анализ базового года выполняются с использованием модулей сбора данных с большими размерами выборки. Этап включает получение рыночной информации или связанных данных из различных источников и стратегий. Он включает изучение и планирование всех данных, полученных из прошлого заранее. Он также охватывает изучение несоответствий информации, наблюдаемых в различных источниках информации. Рыночные данные анализируются и оцениваются с использованием статистических и последовательных моделей рынка. Кроме того, анализ доли рынка и анализ ключевых тенденций являются основными факторами успеха в отчете о рынке. Чтобы узнать больше, пожалуйста, запросите звонок аналитика или оставьте свой запрос.
Ключевой методологией исследования, используемой исследовательской группой DBMR, является триангуляция данных, которая включает в себя интеллектуальный анализ данных, анализ влияния переменных данных на рынок и первичную (отраслевую экспертную) проверку. Модели данных включают сетку позиционирования поставщиков, анализ временной линии рынка, обзор рынка и руководство, сетку позиционирования компании, патентный анализ, анализ цен, анализ доли рынка компании, стандарты измерения, глобальный и региональный анализ и анализ доли поставщика. Чтобы узнать больше о методологии исследования, отправьте запрос, чтобы поговорить с нашими отраслевыми экспертами.
Доступна настройка
Data Bridge Market Research является лидером в области передовых формативных исследований. Мы гордимся тем, что предоставляем нашим существующим и новым клиентам данные и анализ, которые соответствуют и подходят их целям. Отчет можно настроить, включив в него анализ ценовых тенденций целевых брендов, понимание рынка для дополнительных стран (запросите список стран), данные о результатах клинических испытаний, обзор литературы, обновленный анализ рынка и продуктовой базы. Анализ рынка целевых конкурентов можно проанализировать от анализа на основе технологий до стратегий портфеля рынка. Мы можем добавить столько конкурентов, о которых вам нужны данные в нужном вам формате и стиле данных. Наша команда аналитиков также может предоставить вам данные в сырых файлах Excel, сводных таблицах (книга фактов) или помочь вам в создании презентаций из наборов данных, доступных в отчете.