Global Tumor Agnostic Oncology Drug Market
市场规模(十亿美元)
CAGR :
% 
 USD
22.32 Billion
USD
69.72 Billion
2024
2032
USD
22.32 Billion
USD
69.72 Billion
2024
2032
| 2025 –2032 | |
| USD 22.32 Billion | |
| USD 69.72 Billion | |
|
|
|
|
全球腫瘤不可知腫瘤藥物市場細分,按藥物類型(免疫檢查點抑制劑、標靶治療等)、適應症(非小細胞肺癌 (NSCLC)、結直腸癌、甲狀腺癌、乳腺癌、胰腺癌、NTRK 融合實體瘤等)、生物標誌物類型(MSI-H/dMMR、NTRK 基因融合、RET 基因變異、BRAFF600 診室等研究中心產業趨勢和預測至 2032 年
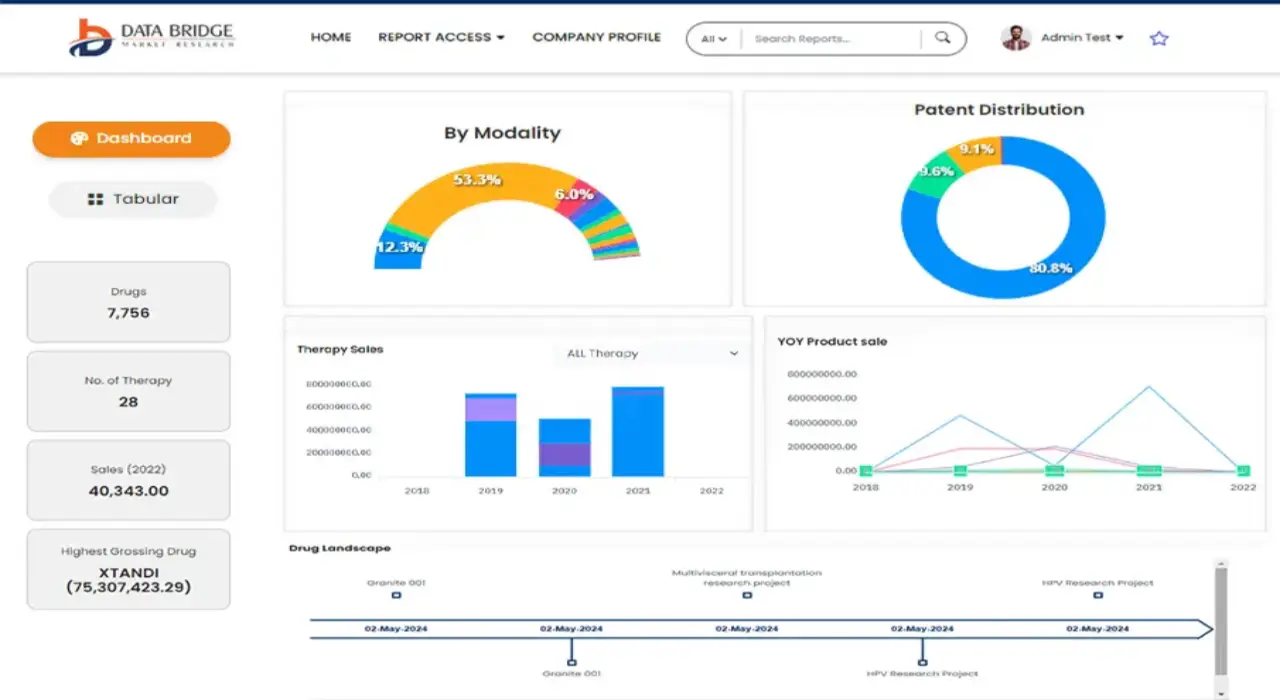
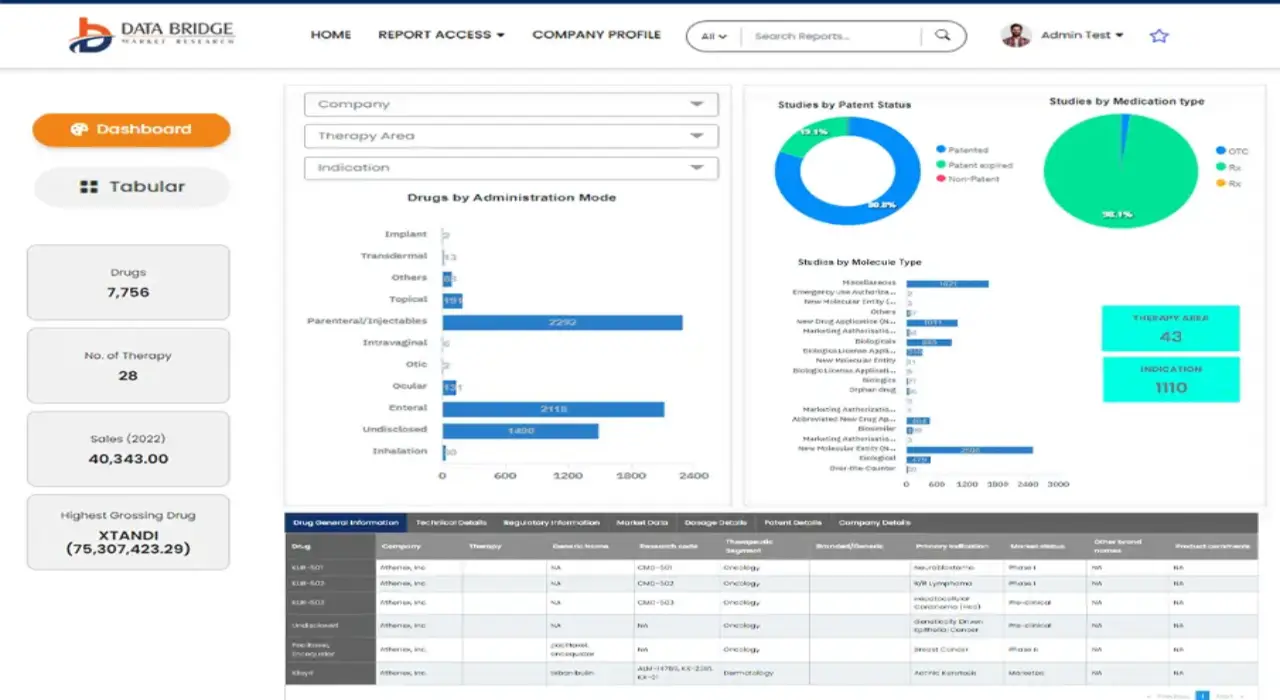
腫瘤無關腫瘤藥物市場規模
- 2024 年全球腫瘤無關腫瘤藥物市場規模為223.2 億美元 ,預計 到 2032 年將達到 697.2 億美元,預測期內 複合年增長率為 15.30%。
- 市場成長主要得益於精準醫療的進步以及對不同腫瘤類型可操作基因生物標記物的識別不斷增加,從而實現了更加個性化的癌症治療方法
- 此外,監管審批的不斷增加、對生物標記驅動療法的投資不斷增加以及臨床試驗管線的不斷擴展,正在加速腫瘤無關藥物在醫療體系中的應用。這些發展使得腫瘤無關療法成為腫瘤治療模式的關鍵轉變,從而顯著促進該行業的成長。
腫瘤無關腫瘤藥物市場分析
- 腫瘤不可知性腫瘤藥物旨在針對特定的基因突變或生物標記物,無論癌症類型或來源如何,由於其精準性、廣泛的適用性以及對多種腫瘤類型的患者療效的改善,正在成為現代癌症治療的關鍵。
- 對腫瘤不可知療法的需求不斷增長,主要原因是可操作生物標記的日益普及、基因組研究的投資不斷增加,以及醫療保健提供者對個人化、突變特異性治療方案的認識不斷提高
- 北美在腫瘤不可知腫瘤藥物市場佔據主導地位,2024 年其收入份額最高,為 47%,這得益於先進的診斷基礎設施、精準醫療的早期採用以及 FDA 等機構的強有力監管支持,美國各大癌症治療中心對已獲批准的腫瘤不可知藥物的接受度顯著提高
- 由於醫療保健覆蓋範圍擴大、癌症負擔增加以及中國、日本和印度等國家越來越多地採用基於生物標誌物的篩檢,預計亞太地區將成為預測期內腫瘤不可知腫瘤藥物市場成長最快的地區
- MSI-H/dMMR 生物標記領域在腫瘤不可知腫瘤藥物市場佔據主導地位,2024 年的份額為 38.7%,這得益於其對多種癌症類型的廣泛檢測,以及在腫瘤不可知適應症下批准的相關免疫檢查點抑製劑的臨床成功
報告範圍和腫瘤無關腫瘤藥物市場細分
|
屬性 |
腫瘤無關腫瘤藥物關鍵市場洞察 |
|
涵蓋的領域 |
|
|
覆蓋國家 |
北美洲
歐洲
亞太
中東和非洲
南美洲
|
|
主要市場參與者 |
|
|
市場機會 |
|
|
加值資料資訊集 |
除了對市場價值、成長率、細分、地理覆蓋範圍和主要參與者等市場情景的洞察之外,Data Bridge Market Research 策劃的市場報告還包括深入的專家分析、定價分析、品牌份額分析、消費者調查、人口統計分析、供應鏈分析、價值鏈分析、原材料/消耗品概述、供應商選擇標準、PESTLE 分析、波特分析和監管框架。 |
腫瘤無關腫瘤藥物市場趨勢
“精準腫瘤學和生物標記驅動療法的需求不斷增長”
- 全球腫瘤不可知論腫瘤藥物市場一個顯著且加速發展的趨勢是,基於生物標記檢測的精準腫瘤學日益普及,這使得治療決策能夠基於特定的基因變異而非腫瘤來源。這種模式轉變正在重塑癌症治療的臨床方法,透過推廣針對多種癌症類型的個人化治療。
- 例如,Larotrectinib 和 Entrectinib 等藥物已被證明對 NTRK 基因融合的實體瘤有效,無論腫瘤部位如何,並且已獲得 FDA 腫瘤無關性批准。同樣,派姆單抗是首個獲準用於治療具有 MSI-H 或 dMMR 生物標記(而非特定部位標準)的腫瘤的抗癌藥物。
- 製藥公司正增加對生物標記驅動的研發管線的投資,瞄準罕見但可操作的突變,例如 RET、NTRK、BRAF V600 等。這促使新一代定序 (NGS) 成為一種標準診斷工具,簡化了腫瘤不可知療法適用患者的識別流程。
- 學術機構、生技公司和全球製藥公司正在與診斷公司合作,共同開發伴隨診斷技術,以支持其臨床應用和監管審批。基因組學、診斷學和治療學的這種整合正在提高精準度,減少反覆試驗治療,並改善患者預後。
- 腫瘤無關適應症的趨勢正在從根本上重塑腫瘤藥物的開發和監管框架。基於共同生物標記評估多種癌症類型單一療法的臨床試驗數量不斷增加,預計將在未來幾年擴大腫瘤無關藥物組合。
- 隨著醫療保健提供者和患者尋求更個人化、有效且基於基因組的癌症治療方案,這種轉變正在全球腫瘤中心迅速興起。因此,腫瘤無關藥物正成為下一代癌症療法的基石。
腫瘤無關腫瘤藥物市場動態
司機
“增加監管審批並關注個人化癌症治療”
- 由於生物標記特異性藥物試驗的成功,腫瘤無關療法的監管批准數量不斷增加,這是推動市場成長的重要因素。美國FDA和EMA等監管機構目前正積極透過快速通道支持腫瘤無關藥物的開發,因為他們認識到標靶分子改變而非腫瘤組織學的臨床價值。
- 例如,帕博利珠單抗和拉羅替尼因其在多種腫瘤類型中均表現出強大的生物標記驅動療效而獲得加速審批。這為製藥公司設計全腫瘤臨床試驗開創了先例,簡化了市場准入,並鼓勵了進一步的創新。
- 隨著對癌症基因組學理解的不斷深入,腫瘤學家和研究人員正從基於器官的治療轉向標靶治療,從而發現新的可操作突變和治療標靶。這增加了對廣譜藥物的需求,這些藥物可以根據基因特徵治療患者,無論腫瘤來源如何。
- 全球癌症發生率的上升,加上生物標記檢測的增多,正在擴大腫瘤無關藥物的適用患者族群。已開發地區和發展中地區醫療投資的不斷增長、患者意識的提升以及先進診斷技術的普及,進一步推動了這一發展勢頭。
克制/挑戰
“生物標誌物普及率有限且開發成本高昂”
- 儘管腫瘤無關藥物前景光明,但由於某些可操作的生物標記在各種腫瘤類型中都較為稀缺,它們仍面臨挑戰,這限制了符合條件的患者數量,並限制了其廣泛應用。 NTRK 或 RET 等融合基因的低發生率意味著許多腫瘤無關療法可能僅適用於一小部分患者。
- 此外,次世代定序(NGS)和伴隨診斷測試的高成本仍然是中低收入國家獲得先進分子診斷的障礙
- 該領域的藥物開發還需要大規模基因組研究、多腫瘤臨床試驗以及複雜的監管導航,所有這些都導致研發成本高且週期延長。例如,臨床試驗需要招募不同癌症類型的罕見生物標記陽性患者,這使得試驗設計和入組工作變得複雜。
- 此外,腫瘤非特異性藥物的高昂價格可能會對醫療保健預算造成壓力,並導致報銷困難。這可能會影響患者的就醫管道,尤其是在保險覆蓋範圍或公共醫療資金有限的地區。
- 透過更廣泛地獲取基因組檢測、創新試驗設計和全球監管協調來克服這些挑戰,對於充分發揮腫瘤不可知論腫瘤療法的潛力並推動全球公平採用至關重要
腫瘤無關腫瘤藥物市場範圍
市場根據藥物類型、適應症、生物標記類型和最終用戶進行細分。
- 依藥物類型
根據藥物類型,腫瘤無關腫瘤藥物市場細分為免疫檢查點抑制劑、標靶治療藥物和其他藥物。免疫檢查點抑制劑憑藉其在多種存在MSI-H或dMMR生物標記的腫瘤類型中取得的顯著臨床成功和廣泛療效,在2024年佔據了市場主導地位,收入份額最高。像派姆單抗這樣的藥物開創了腫瘤無關適應症的先例,推動了全球主要癌症治療中心的採用。它們能夠利用人體免疫系統,並在多種癌症中產生持久的療效,這增強了它們的臨床和商業實力。
預計標靶治療領域將在2025年至2032年間實現最快增長,這得益於針對NTRK、RET和BRAF突變等罕見基因變異的藥物獲批數量的增加。標靶治療在特定基因患者群體中的精準度和有效性,以及伴隨診斷工具的不斷擴展,正在加速已開發市場和新興市場對標靶治療的需求。
- 按適應症
根據適應症,腫瘤無關腫瘤藥物市場細分為非小細胞肺癌 (NSCLC)、大腸直腸癌、甲狀腺癌、乳腺癌、胰臟癌、NTRK 融合實體瘤及其他。 2024 年,NTRK 融合實體瘤佔據了最大的收入份額,這得益於拉羅替尼和恩曲替尼等療法的獲批,這些療法已證明對各種 NTRK 融合陽性腫瘤均有效,無論其來源為何。 NTRK 融合基因罕見但具有跨癌種適用性,加上監管部門的積極支持,推動了該藥物的早期臨床應用。
預計非小細胞肺癌 (NSCLC) 領域將在預測期內以最快的速度增長,這得益於發病率的上升、生物標誌物檢測率的高增長,以及針對 NSCLC 中常見突變(如 RET 和 BRAF 變異)的腫瘤不可知藥物的不斷增長。
- 依生物標誌類型
根據生物標記類型,腫瘤無關腫瘤藥物市場細分為MSI-H/dMMR、NTRK基因融合、RET基因變異、BRAF V600突變等。 MSI-H/dMMR細分市場在2024年佔據了最大的市場份額,達到38.7%,這得益於其在多種腫瘤類型中的較高發病率,以及針對該生物標誌物的免疫療法早期獲批。這些標誌物是檢查點抑制劑適格性的關鍵指標,有助於其在臨床上的廣泛應用。
由於NGS診斷技術的日益普及以及針對此生物標記的臨床試驗數量的不斷增長,NTRK基因融合領域預計將在2025年至2032年間實現最高增長。儘管NTRK融合罕見,但它存在於多種腫瘤類型中,這使得該領域有望透過泛癌種的適應症快速擴張。
- 按最終用戶
根據最終用戶,腫瘤無關腫瘤藥物市場細分為醫院、癌症研究機構、專科診所、門診手術中心和其他。 2024年,醫院佔據了市場主導地位,這得益於其在腫瘤治療中的核心作用、先進的診斷基礎設施以及獲得最新獲批療法的便利性。醫院通常是進行生物標記檢測和腫瘤無關藥物資格認定的首選地點。
預計癌症研究機構領域將在預測期內實現最快的成長,這得益於臨床試驗、基因組研究以及與製藥公司合作以早期獲得創新療法的投資不斷增加。這些機構在推動腫瘤無關藥物研發和精準腫瘤學計畫的早期患者招募方面發揮著至關重要的作用。
腫瘤無關腫瘤藥物市場區域分析
- 北美在腫瘤不可知腫瘤藥物市場佔據主導地位,2024 年其收入份額最高,為 47%,這得益於先進的診斷基礎設施、精準醫療的早期採用以及 FDA 等機構的強有力監管支持,美國各大癌症治療中心對已獲批准的腫瘤不可知藥物的接受度顯著提高
- 該地區的患者和醫療服務提供者越來越青睞腫瘤不可知療法,因為它們具有針對性的療效、能夠治療多種癌症類型的罕見突變,並且支持伴隨診斷,從而簡化治療決策
- 積極的監管框架(例如 FDA 批准)、強大的藥物管道以及腫瘤學家的高度認知進一步支持了這種廣泛的接受度,將腫瘤無關藥物定位為學術和社區醫療環境中現代癌症治療的重要組成部分
美國腫瘤不可知腫瘤藥物市場洞察
2024年,美國腫瘤不可知論腫瘤藥物市場佔據北美地區87%的最高收入份額,這得益於精準醫療的早期應用以及FDA批准的腫瘤不可知論療法在臨床上的強勁應用。美國醫療保健體系在基因檢測和生物標記驅動治療方面高度先進,從而能夠更廣泛地獲得個人化癌症治療。此外,廣泛的臨床試驗活動、病患權益倡議以及支持性報銷框架進一步加速了市場成長,使美國成為腫瘤不可知論腫瘤學創新的全球領導者。
歐洲腫瘤不可知腫瘤藥物市場洞察
預計歐洲腫瘤不可知藥物市場在整個預測期內將以顯著的複合年增長率擴張,這得益於基因組檢測的普及、監管機構對腫瘤不可知藥物審批的開放程度,以及對個體化癌症治療的日益關注。在製藥公司和診斷公司合作的支持下,該地區的醫療保健系統正在逐步整合基於生物標記的治療途徑。腫瘤中心的主要市場成長顯著,腫瘤不可知藥物正被納入現代精準醫療計畫。
英國腫瘤不可知腫瘤藥物市場洞察
英國腫瘤不可知論腫瘤藥物市場預計在預測期內將以顯著的複合年增長率增長,這得益於英國國家醫療服務體系 (NHS) 對個性化癌症治療的重視以及基因組篩檢覆蓋範圍的擴大。英國基因組學協會 (Genomics England) 等組織致力於將全基因組定序整合到癌症治療中,這有助於早期發現可操作的突變。加之公眾意識的不斷提升和強大的研究生態系統,這些舉措正使英國成為腫瘤不可知論療法的蓬勃發展市場。
德國腫瘤不可知腫瘤藥物市場洞察
預計在預測期內,德國腫瘤無關藥物市場將以可觀的複合年增長率擴張,這得益於其高標準的癌症治療、分子診斷技術的早期應用以及資金雄厚的醫療保健體系。德國強大的生物技術和製藥產業正在加速伴隨診斷和創新療法的普及。隨著醫生對腫瘤無關藥物的熟悉程度不斷提高以及患者獲得先進療法的管道不斷拓寬,腫瘤無關藥物在大學醫院和專科腫瘤診所中都日益普及。
亞太地區腫瘤不可知腫瘤藥物市場洞察
在2025年至2032年的預測期內,亞太地區腫瘤無關腫瘤藥物市場預計將以26.8%的複合年增長率保持高速增長,這得益於癌症發病率的上升、基因組檢測能力的提升以及醫療改革的利好。中國、日本和印度等國家正在大力投資精準腫瘤學,並在政府的支持下推出旨在促進早期診斷和生物標記指導治療的措施。 NGS技術的日益普及以及製藥公司之間的合作,使得腫瘤無關療法在整個地區更加觸手可及。
日本腫瘤不可知腫瘤藥物市場洞察
日本腫瘤非特異性腫瘤藥物市場正蓬勃發展,得益於其在癌症研究領域的領先地位、人口老化以及對精準醫療的投入。日本在腫瘤非特異性治療領域批准並整合了恩曲替尼和帕博利珠單抗等藥物,反映了監管和臨床領域向突變特異性療法的轉變。先進診斷技術的廣泛應用以及與國家癌症治療指南的整合,正在推動公立和私立醫療機構的市場擴張。
印度腫瘤不可知腫瘤藥物市場洞察
2024年,印度腫瘤無關藥物市場佔據亞太地區最大市場份額,這得益於中產階級的壯大、腫瘤學基礎設施的不斷完善以及基因組檢測價格的日益親民。由於癌症負擔高企以及人們對生物標記標靶療法的認知度不斷提升,印度正迅速成為腫瘤無關藥物的關鍵市場。本土基因組檢測實驗室的興起、政府支持的醫療保健計劃以及與全球製藥公司的戰略合作夥伴關係,正在推動腫瘤無關藥物在城市中心和二線城市的普及和應用。
腫瘤無關腫瘤藥物市場份額
腫瘤無關腫瘤藥物產業主要由知名公司主導,包括:
- F. Hoffmann-La Roche Ltd(瑞士)
- 默克公司(美國)
- 拜耳公司(德國)
- 衛材株式會社(日本)
- 輝瑞公司(美國)
- 諾華公司(瑞士)
- Blueprint Medicines Corporation(美國)
- 葛蘭素史克公司(英國)
- 武田藥品工業株式會社(日本)
- 百時美施貴寶公司(美國)
- Foundation Medicine, Inc.(美國)
- 第一三共株式會社(日本)
- 基因泰克公司(美國)
- 安進公司(美國)
- 再生元製藥公司(美國)
- Illumina公司(美國)
- Tempus Labs, Inc.(美國)
- Guardant Health, Inc.(美國)
- 精確科學公司(美國)
全球腫瘤無關腫瘤藥物市場的最新發展是什麼?
- 2024年5月,羅氏宣布啟動一項全球III期臨床試驗,評估其新型腫瘤無關療法Rozartinib,該療法針對多種實體瘤的RET基因融合。該研究標誌著公司在拓展精準腫瘤學產品組合方面邁出的重要一步,並凸顯了其基於分子改變而非腫瘤起源開發療法的策略重點。此舉鞏固了羅氏在腫瘤無關療法領域的領導地位,並鞏固了其透過創新療法應對罕見致癌驅動因素的承諾。
- 2024年3月,拜耳公司與歐洲和亞洲的部分腫瘤中心合作,啟動了其在研NTRK抑制劑Vitrakinib的擴展可及性計畫。該計劃旨在為治療選擇有限的攜帶NTRK融合基因的晚期實體瘤患者提供早期治療機會。這項進展彰顯了拜耳致力於擴大精準醫療可及性的決心,同時也展現了拜耳致力於收集真實世界證據以支持監管途徑和未來審批的決心。
- 2024年2月,羅氏旗下子公司Foundation Medicine, Inc.宣布推出一項基於新一代定序(NGS)的綜合基因組分析(CGP)檢測,旨在支持腫瘤無關療法的選擇。此檢測可識別MSI-H、NTRK、RET和BRAF突變等關鍵生物標記物,從而更有效率地對患者進行分層,以便進行標靶治療。這項進展凸顯了診斷創新在推動腫瘤無關療法臨床實施方面日益重要的作用。
- 2024年1月,衛材株式會社與默克公司聯合公佈了LEAP-101試驗的積極結果,該試驗評估了崙伐替尼聯合帕博利珠單抗治療伴有MSI-H或dMMR突變的實體瘤患者。數據顯示,該療法在多種腫瘤類型中均獲得了持久緩解,支持進一步提交針對腫瘤無關適應症的註冊申請。此次合作強化了聯合療法作為增強特定基因族群療效的策略的趨勢。
- 2023年12月,Blueprint Medicines Corporation的在研藥物BLU-945獲得FDA快速通道認定,該藥物針對治療RET基因突變癌症中的抗藥性突變。該公司正在探索該療法在腫瘤無關領域的應用,其早期數據顯示該療法在多種RET基因突變驅動的腫瘤類型中有效。 FDA的此項認可凸顯了泛癌種標靶療法日益增長的勢頭,並支持加快開發以滿足高需求患者群體的需求。
SKU-
研究方法
数据收集和基准年分析是使用具有大样本量的数据收集模块完成的。该阶段包括通过各种来源和策略获取市场信息或相关数据。它包括提前检查和规划从过去获得的所有数据。它同样包括检查不同信息源中出现的信息不一致。使用市场统计和连贯模型分析和估计市场数据。此外,市场份额分析和关键趋势分析是市场报告中的主要成功因素。要了解更多信息,请请求分析师致电或下拉您的询问。
DBMR 研究团队使用的关键研究方法是数据三角测量,其中包括数据挖掘、数据变量对市场影响的分析和主要(行业专家)验证。数据模型包括供应商定位网格、市场时间线分析、市场概览和指南、公司定位网格、专利分析、定价分析、公司市场份额分析、测量标准、全球与区域和供应商份额分析。要了解有关研究方法的更多信息,请向我们的行业专家咨询。
可定制
Data Bridge Market Research 是高级形成性研究领域的领导者。我们为向现有和新客户提供符合其目标的数据和分析而感到自豪。报告可定制,包括目标品牌的价格趋势分析、了解其他国家的市场(索取国家列表)、临床试验结果数据、文献综述、翻新市场和产品基础分析。目标竞争对手的市场分析可以从基于技术的分析到市场组合策略进行分析。我们可以按照您所需的格式和数据样式添加您需要的任意数量的竞争对手数据。我们的分析师团队还可以为您提供原始 Excel 文件数据透视表(事实手册)中的数据,或者可以帮助您根据报告中的数据集创建演示文稿。