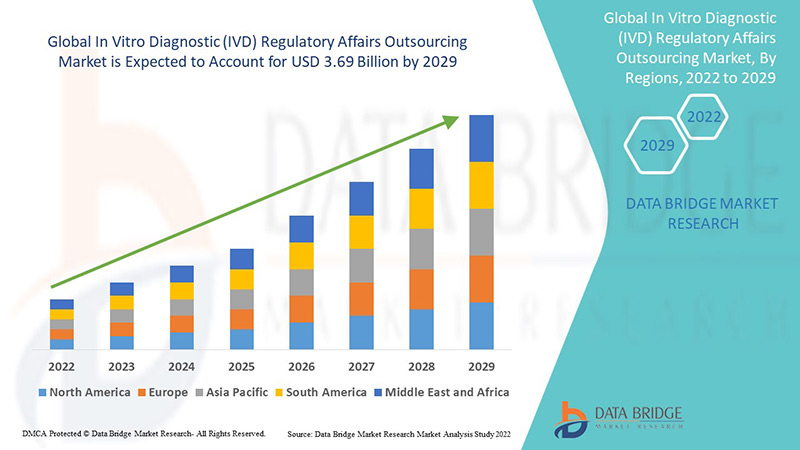
Global In Vitro Diagnostic Ivd Regulatory Affairs Outsourcing Market
حجم السوق بالمليار دولار أمريكي
CAGR :
% 
 USD
674,277.97 Thousand
USD
1,830,957.45 Thousand
2021
2029
USD
674,277.97 Thousand
USD
1,830,957.45 Thousand
2021
2029
| 2022 –2029 | |
| USD 674,277.97 Thousand | |
| USD 1,830,957.45 Thousand | |
|
|
|
|
السوق العالمية لخدمات الاستعانة بمصادر خارجية للشؤون التنظيمية للتشخيص المخبري (IVD)، حسب الخدمة (الكتابة والتقديمات التنظيمية، التسجيل التنظيمي وطلبات التجارب السريرية ، الاستشارات التنظيمية، التمثيل القانوني، خدمات إدارة البيانات، خدمات تصنيع وضوابط الكيمياء (CMC)، وغيرها)، المؤشرات (علم الأورام، طب الأعصاب، أمراض القلب، الكيمياء السريرية والمقايسات المناعية، الطب الدقيق، الأمراض المعدية، داء السكري، الاختبارات الجينية، فيروس نقص المناعة البشرية/الإيدز، أمراض الدم، اختبارات الأدوية/علم الصيدلة الجيني، نقل الدم، نقطة الرعاية، وغيرها)، طريقة النشر (السحابة وفي الموقع)، حجم المؤسسة (الشركات الصغيرة والمتوسطة والكبيرة)، المرحلة (السريرية، ما قبل السريرية، وما بعد ترخيص التسويق)، الفئة (الفئة الأولى، الفئة الثانية، والفئة الثالثة)، المستخدم النهائي (شركات الأدوية، الأجهزة الطبية). الشركات، وشركات التكنولوجيا الحيوية، وغيرها) - اتجاهات الصناعة وتوقعاتها حتى عام 2029
تحليل السوق والحجم
واجهت شركات الرعاية الصحية تحديات في مواكبة المعايير التنظيمية، لا سيما بسبب جائحة كوفيد-19 (فيروس كورونا). ولضمان ثقافة الجودة في شركات التكنولوجيا الطبية، تستخدم شركات الاستشارات برامج أنظمة إدارة الجودة. وتقدم الشركات المعنية بالاستعانة بمصادر خارجية للشؤون التنظيمية للتشخيص المخبري (IVD) دعمًا قائمًا على المشاريع لمؤسسات الرعاية الصحية.
أدى تطبيق نظام الاستعانة بمصادر خارجية إلى إبرام اتفاقيات طويلة الأجل. وقد قُدّرت قيمة سوق الاستعانة بمصادر خارجية للشؤون التنظيمية للتشخيص المخبري (IVD) العالمي بـ 1.6 مليار دولار أمريكي في عام 2021، ومن المتوقع أن تصل إلى 3.69 مليار دولار أمريكي بحلول عام 2029، مسجلةً معدل نمو سنوي مركب قدره 11% خلال الفترة المتوقعة 2022-2029. ومن المتوقع أن تشهد شركات الأدوية نموًا كبيرًا بفضل زيادة عدد الموافقات السريرية.
تعريف السوق
تلعب الشؤون التنظيمية دورًا بالغ الأهمية في صناعة أجهزة التشخيص المختبري (IVD). تُعنى هذه الشؤون بدورة حياة مختلف منتجات الرعاية الصحية، وتُقدم الدعم والتوجيه الاستراتيجي والتكتيكي والتشغيلي لشركات التصنيع للعمل ضمن الإطار التنظيمي.
نطاق التقرير وتقسيم السوق
|
مقياس التقرير |
تفاصيل |
|
فترة التنبؤ |
من 2022 إلى 2029 |
|
سنة الأساس |
2021 |
|
السنوات التاريخية |
2020 (قابلة للتخصيص حتى 2019 - 2014) |
|
الوحدات الكمية |
الإيرادات بالملايين من الدولارات الأمريكية، والحجم بالوحدات، والتسعير بالدولار الأمريكي |
|
القطاعات المغطاة |
الخدمة (الكتابة التنظيمية والتقديمات، التسجيل التنظيمي وطلبات التجارب السريرية، الاستشارات التنظيمية، التمثيل القانوني، خدمات إدارة البيانات، خدمات تصنيع وضوابط الكيمياء (CMC)، وغيرها)، المؤشرات (علم الأورام، طب الأعصاب، أمراض القلب، الكيمياء السريرية والمقايسات المناعية، الطب الدقيق، الأمراض المعدية، داء السكري، الاختبارات الجينية، فيروس نقص المناعة البشرية/الإيدز، أمراض الدم، اختبار الأدوية/علم الصيدلة الجيني، نقل الدم، نقطة الرعاية، وغيرها)، وضع النشر (السحابي والمحلي)، حجم المؤسسة (الشركات الصغيرة والمتوسطة والكبيرة)، المرحلة (السريرية، ما قبل السريرية، وما بعد ترخيص التسويق)، الفئة (الفئة الأولى، الفئة الثانية، والفئة الثالثة)، المستخدم النهائي (شركات الأدوية، شركات الأجهزة الطبية، شركات التكنولوجيا الحيوية، وغيرها). |
|
الدول المغطاة |
الولايات المتحدة وكندا والمكسيك في أمريكا الشمالية، ألمانيا، فرنسا، المملكة المتحدة، هولندا، سويسرا، بلجيكا، روسيا، إيطاليا، إسبانيا، تركيا، بقية أوروبا في أوروبا، الصين، اليابان، الهند، كوريا الجنوبية، سنغافورة، ماليزيا، أستراليا، تايلاند، إندونيسيا، الفلبين، بقية دول آسيا والمحيط الهادئ (APAC) في منطقة آسيا والمحيط الهادئ (APAC)، المملكة العربية السعودية، الإمارات العربية المتحدة، جنوب أفريقيا، مصر، إسرائيل، بقية دول الشرق الأوسط وأفريقيا (MEA) كجزء من الشرق الأوسط وأفريقيا (MEA)، البرازيل والأرجنتين وبقية دول أمريكا الجنوبية كجزء من أمريكا الجنوبية. |
|
الجهات الفاعلة في السوق المغطاة |
Freyr Solutions (الهند)، PPD Inc. (الولايات المتحدة)، EMERGO (الولايات المتحدة)، ICON (الرعاية الصحية)، Parexel International Corporation (الولايات المتحدة)، CRITERIUM, INC. (الولايات المتحدة)، Groupe ProductLife SA (فرنسا)، Labcorp Drug Development (الولايات المتحدة)، WuXi AppTec (الصين)، Genpact (الولايات المتحدة)، Medpace (الولايات المتحدة)، Dor Pharmaceutical Services (إسرائيل)، Qserve (هولندا)، وغيرها. |
|
فرص السوق |
|
ديناميكيات سوق الاستعانة بمصادر خارجية للشؤون التنظيمية للتشخيص المختبري (IVD)
يتناول هذا القسم فهم محركات السوق، ومزاياه، وفرصه، ومعوقاته، وتحدياته. ويُناقش كل ذلك بالتفصيل على النحو التالي:
- الاستخدام العالي في صناعة الرعاية الصحية
يُعدّ ازدياد استخدام خدمات التعهيد الخارجي في قطاع الرعاية الصحية أحد العوامل الرئيسية الدافعة لنمو سوق تعهيد الشؤون التنظيمية للتشخيص المخبري (IVD). كما أن ازدياد أنشطة التوسع الجغرافي الهادفة إلى تسريع الموافقات في الأسواق المحلية يُسهم في هذا النمو.
- البحث والتطوير
إن الزيادة في أنشطة البحث والتطوير التي تزيد من حجم طلبات التجارب السريرية وتسجيل المنتجات تعمل على تسريع نمو السوق.
- الموافقات السريرية
يشهد الطلب على الاستعانة بمصادر خارجية لإدارة الشؤون التنظيمية للتشخيص المخبري (IVD) تزايدًا ملحوظًا، إذ تتعرض الشركات لضغوط مستمرة للحصول على الموافقات السريرية من الجهات التنظيمية في الوقت المناسب. ويتزايد الطلب على خدمات الشؤون التنظيمية نتيجةً لهذه الإجراءات.
فرص
علاوة على ذلك، فإن تطوير المؤشرات الحيوية والاختبارات الخاصة بالأمراض، وأهمية التشخيصات المصاحبة، يوفر فرصًا مربحة للاعبين في السوق في الفترة المتوقعة من 2022 إلى 2029. كما أن الزيادة في الاستثمارات ستؤدي إلى توسيع السوق بشكل أكبر.
القيود/التحديات
من ناحية أخرى، من المتوقع أن تُعيق اللوائح المتغيرة المتعلقة بالأجهزة الطبية والاستعانة بمصادر خارجية لتنظيم شؤون التشخيص المخبري (IVD) نمو السوق. كما يُتوقع أن يُشكل نقص البنية التحتية في خدمات الرعاية الصحية تحديًا لسوق الاستعانة بمصادر خارجية لتنظيم شؤون التشخيص المخبري (IVD) في الفترة المتوقعة 2022-2029.
يقدم هذا التقرير عن سوق الاستعانة بمصادر خارجية للشؤون التنظيمية للتشخيص المخبري (IVD) تفاصيل عن أحدث التطورات، واللوائح التجارية، وتحليل الاستيراد والتصدير، وتحليل الإنتاج، وتحسين سلسلة القيمة، وحصة السوق، وتأثير الجهات الفاعلة المحلية والمحلية، ويحلل الفرص من حيث مصادر الإيرادات الناشئة، والتغيرات في لوائح السوق، وتحليل النمو الاستراتيجي للسوق، وحجم السوق، ونمو فئات السوق، ومجالات التطبيق والهيمنة، وموافقات المنتجات، وإطلاق المنتجات، والتوسعات الجغرافية، والابتكارات التكنولوجية في السوق. لمزيد من المعلومات حول سوق الاستعانة بمصادر خارجية للشؤون التنظيمية للتشخيص المخبري (IVD)، تواصل مع شركة Data Bridge Market Research للحصول على موجز محلل، وسيساعدك فريقنا في اتخاذ قرار سوقي مدروس لتحقيق نمو السوق.
تأثير كوفيد-19 على سوق الاختبارات التشخيصية
كان لجائحة كوفيد-19 تأثير سلبي على قطاع الرعاية الصحية. وقد لجأت الجهات الفاعلة الرئيسية إلى تبني استراتيجيات مبتكرة لمواجهة الوضع المتغير بسرعة خلال تفشي كوفيد-19. وحرصت الدول على إجراء تغييرات جوهرية في قطاع الرعاية الصحية حتى تراجعت آثار الأزمة. ومن المتوقع أن تشهد إصلاحات الرعاية الصحية احتواءً للتكاليف، وزيادة في إمكانية الوصول، وتقدمًا تكنولوجيًا في السنوات القادمة. وقد ازداد الطلب على الاستعانة بمصادر خارجية للشؤون التنظيمية للتشخيص المخبري (IVD) نظرًا للتركيز على أهمية التشخيص والرعاية والاستشارات عن بُعد. وتخفف هذه الخدمات العبء عن المستشفيات في مرحلة ما بعد الجائحة.
التطورات الأخيرة
- أدرجت مجلة USA-9 للتكنولوجيا شركة Freyr ضمن "أفضل 10 مزودي حلول تكنولوجية لعام 2021" في نوفمبر 2021. وقد أدرج موقع USA-9.com، وهي مجلة تقنية، شركة Freyr Solutions، الرائدة عالميًا في مجال الحلول التنظيمية والخدمات، ضمن "أفضل 10 مزودي حلول تكنولوجية لعام 2021"، حيث تواصل Fryer تصميم حلول برمجية مبتكرة ودعم العملاء في تحقيق أهدافهم المتعلقة بالامتثال. وقد ساهم ذلك في تعزيز شعبية الشركة.
نطاق وحجم سوق الاستعانة بمصادر خارجية للشؤون التنظيمية للتشخيص المختبري العالمي
يُقسّم سوق الاستعانة بمصادر خارجية للشؤون التنظيمية للتشخيص المخبري (IVD) بناءً على الخدمات، والمؤشرات، وطريقة النشر، وحجم المؤسسة، والمرحلة، والفئة، والمستخدم النهائي. سيساعدك نمو هذه القطاعات على تحليل قطاعات النمو المتواضعة في هذه الصناعات، وتزويد المستخدمين بنظرة عامة قيّمة على السوق ورؤى ثاقبة لمساعدتهم على اتخاذ قرارات استراتيجية لتحديد تطبيقات السوق الرئيسية.
خدمات
- الكتابة التنظيمية والتقديمات
- التسجيل التنظيمي وتطبيقات التجارب السريرية
- الاستشارات التنظيمية
- التمثيل القانوني
- خدمات إدارة البيانات
- خدمات التصنيع والتحكم الكيميائي (CMC)
- آحرون
على أساس الخدمات، يتم تقسيم سوق الاستعانة بمصادر خارجية للشؤون التنظيمية للتشخيص المخبري (IVD) العالمي إلى الكتابة التنظيمية والتقديمات، والتسجيل التنظيمي وتطبيقات التجارب السريرية، والاستشارات التنظيمية، والتمثيل القانوني، وخدمات إدارة البيانات، وخدمات التصنيع الكيميائي والضوابط (CMC)، وغيرها.
إشارة
- علم الأورام
- علم الأعصاب
- طب القلب
- الكيمياء السريرية والاختبارات المناعية
- الطب الدقيق
- الأمراض المعدية
- السكري
- الاختبارات الجينية
- فيروس نقص المناعة البشرية/الإيدز
- أمراض الدم
- اختبار الأدوية/علم الصيدلة الجيني
- نقل الدم
- نقطة الرعاية
- آحرون
على أساس المؤشر، يتم تقسيم سوق الاستعانة بمصادر خارجية للشؤون التنظيمية للتشخيص المختبري (IVD) العالمي إلى علم الأورام، وعلم الأعصاب، وأمراض القلب، والكيمياء السريرية والمقايسات المناعية، والطب الدقيق، والأمراض المعدية، والسكري، والاختبارات الجينية، وفيروس نقص المناعة البشرية / الإيدز، وأمراض الدم، واختبار الأدوية / علم الأدوية الجيني، ونقل الدم، ونقطة الرعاية ، وغيرها.
وضع النشر
- سحاب
- في الموقع
على أساس وضع النشر، يتم تقسيم سوق الاستعانة بمصادر خارجية لتنظيم التشخيص المختبري (IVD) العالمي إلى السحابة والمحلية.
حجم المنظمة
- الشركات الصغيرة والمتوسطة
- الشركات الكبيرة
على أساس حجم المنظمة، يتم تقسيم سوق الاستعانة بمصادر خارجية للشؤون التنظيمية للتشخيص المختبري (IVD) العالمي إلى الشركات الصغيرة والمتوسطة (SMES) والشركات الكبيرة.
منصة
- سريري
- ما قبل السريرية
- PMA (الترخيص بعد التسويق)
على أساس المرحلة، يتم تقسيم سوق الاستعانة بمصادر خارجية لتنظيم التشخيص المختبري (IVD) العالمي إلى السريرية، وما قبل السريرية، وPMA (ترخيص ما بعد التسويق).
فصل
- الصف الأول
- الصف الثاني
- الصف الثالث
على أساس الفئة، يتم تقسيم سوق الاستعانة بمصادر خارجية للشؤون التنظيمية للتشخيص المختبري (IVD) العالمي إلى الفئة الأولى والفئة الثانية والفئة الثالثة.
المستخدم النهائي
- شركات الأدوية
- شركات الأجهزة الطبية
- شركات التكنولوجيا الحيوية
- آحرون
على أساس المستخدم النهائي، يتم تقسيم سوق الاستعانة بمصادر خارجية للشؤون التنظيمية للتشخيص المختبري (IVD) العالمي إلى شركات الأدوية وشركات الأجهزة الطبية وشركات التكنولوجيا الحيوية وغيرها.
تحليل/رؤى إقليمية لسوق الاستعانة بمصادر خارجية للشؤون التنظيمية للتشخيص المختبري (IVD)
يتم تحليل سوق الاستعانة بمصادر خارجية للشؤون التنظيمية للتشخيص المختبري (IVD) وتوفير رؤى حجم السوق واتجاهاتها حسب البلد والخدمات والمؤشر وطريقة النشر وحجم المنظمة والمرحلة والفئة والمستخدم النهائي كما هو مذكور أعلاه.
الدول التي يغطيها تقرير سوق الاستعانة بمصادر خارجية للشؤون التنظيمية للتشخيص المختبري (IVD) هي الولايات المتحدة وكندا والمكسيك في أمريكا الشمالية وألمانيا وفرنسا والمملكة المتحدة وهولندا وسويسرا وبلجيكا وروسيا وإيطاليا وإسبانيا وتركيا وبقية أوروبا في أوروبا والصين واليابان والهند وكوريا الجنوبية وسنغافورة وماليزيا وأستراليا وتايلاند وإندونيسيا والفلبين وبقية دول آسيا والمحيط الهادئ (APAC) في منطقة آسيا والمحيط الهادئ (APAC) والمملكة العربية السعودية والإمارات العربية المتحدة وجنوب إفريقيا ومصر وإسرائيل وبقية دول الشرق الأوسط وأفريقيا (MEA) كجزء من الشرق الأوسط وأفريقيا (MEA) والبرازيل والأرجنتين وبقية دول أمريكا الجنوبية كجزء من أمريكا الجنوبية.
تهيمن منطقة آسيا والمحيط الهادئ (APAC) على سوق الاستعانة بمصادر خارجية لتنظيم التشخيص المختبري (IVD) بسبب الارتفاع في عدد التجارب السريرية والعدد المتزايد من الشركات داخل المنطقة.
ومن المتوقع أن تشهد أمريكا الشمالية نموًا كبيرًا خلال الفترة المتوقعة من 2022 إلى 2029 بسبب وجود شركات الأدوية والأجهزة الطبية الرئيسية وارتفاع الإنفاق على البحث والتطوير في المنطقة.
يقدم قسم الدولة في التقرير أيضًا العوامل المؤثرة على السوق المحلية، والتغيرات في اللوائح التنظيمية، والتي تؤثر على اتجاهات السوق الحالية والمستقبلية. وتُستخدم بيانات مثل تحليل سلسلة القيمة النهائية والنهائية، والاتجاهات الفنية، وتحليل قوى بورتر الخمس، ودراسات الحالة، كمؤشرات للتنبؤ بسيناريو السوق لكل دولة على حدة. كما يُراعى وجود العلامات التجارية العالمية وتوافرها، والتحديات التي تواجهها بسبب المنافسة الكبيرة أو النادرة من العلامات التجارية المحلية، وتأثير التعريفات الجمركية المحلية، وطرق التجارة، عند تقديم تحليل تنبؤي لبيانات الدولة.
نمو البنية التحتية للرعاية الصحية والقاعدة المركبة واختراق التكنولوجيا الجديدة
يوفر سوق الاستعانة بمصادر خارجية للشؤون التنظيمية للتشخيص المخبري (IVD) تحليلاً مفصلاً للسوق لنمو الإنفاق على المعدات الرأسمالية في كل دولة، والقاعدة المُركّبة من مختلف أنواع المنتجات المُستخدمة في سوق الاستعانة بمصادر خارجية للشؤون التنظيمية للتشخيص المخبري (IVD)، وتأثير التكنولوجيا المُستخدمة في منحنيات خط الحياة، والتغيرات في سيناريوهات تنظيم الرعاية الصحية وتأثيرها على سوق الاستعانة بمصادر خارجية للشؤون التنظيمية للتشخيص المخبري (IVD). البيانات متاحة للفترة التاريخية 2010-2020.
تحليل حصة سوق الاستعانة بمصادر خارجية للشؤون التنظيمية للتشخيص المختبري (IVD) في ظل المنافسة
يقدم المشهد التنافسي لسوق الاستعانة بمصادر خارجية للشؤون التنظيمية للتشخيص المخبري (IVD) تفاصيل لكل منافس. تشمل هذه التفاصيل لمحة عامة عن الشركة، وبياناتها المالية، وإيراداتها المحققة، وإمكانياتها السوقية، واستثماراتها في البحث والتطوير، ومبادراتها التسويقية الجديدة، وحضورها العالمي، ومواقع ومرافق الإنتاج، وقدراتها الإنتاجية، ونقاط قوتها وضعفها، وإطلاق المنتجات، ونطاقها، وهيمنة تطبيقاتها. وتتعلق البيانات المذكورة أعلاه فقط بتركيز الشركات على سوق الاستعانة بمصادر خارجية للشؤون التنظيمية للتشخيص المخبري (IVD).
بعض اللاعبين الرئيسيين العاملين في سوق الاستعانة بمصادر خارجية للشؤون التنظيمية للتشخيص المختبري (IVD) هم:
- حلول فريير (الهند)
- شركة بي بي دي (الولايات المتحدة)
- إيميرغو (الولايات المتحدة)
- أيقونة (الرعاية الصحية)
- شركة باركسيل الدولية (الولايات المتحدة)
- كريتيريوم، المحدودة (الولايات المتحدة)
- Groupe ProductLife SA (فرنسا)
- شركة لابكورب لتطوير الأدوية (الولايات المتحدة)
- ووشي أبتيك (الصين)
- جينباكت (الولايات المتحدة)
- ميدبايس (الولايات المتحدة)
- شركة دور للخدمات الصيدلانية (إسرائيل)
- Qserve (هولندا)
SKU-
احصل على إمكانية الوصول عبر الإنترنت إلى التقرير الخاص بأول سحابة استخبارات سوقية في العالم
- لوحة معلومات تحليل البيانات التفاعلية
- لوحة معلومات تحليل الشركة للفرص ذات إمكانات النمو العالية
- إمكانية وصول محلل الأبحاث للتخصيص والاستعلامات
- تحليل المنافسين باستخدام لوحة معلومات تفاعلية
- آخر الأخبار والتحديثات وتحليل الاتجاهات
- استغل قوة تحليل المعايير لتتبع المنافسين بشكل شامل
Table of Content
1. المقدمة
1.1 أهداف الدراسة
1.2 تعريف السوق
1.3 نظرة عامة على سوق الاستعانة بمصادر خارجية لتنظيم التشخيص المخبري (IVD) العالمي
1.4 العملة والتسعير
1.5 القيود
1.6 الأسواق المغطاة
2. تقسيم السوق
2.1 أهم النقاط المستفادة
2.2 الوصول إلى حجم سوق الاستعانة بمصادر خارجية للشؤون التنظيمية للتشخيص المخبري (IVD) العالمي
2.2.1 شبكة تحديد مواقع البائعين
2.2.2 منحنى خط حياة التكنولوجيا
2.2.3 النمذجة متعددة المتغيرات
2.2.4 التحليل من الأعلى إلى الأسفل
2.2.5 معايير القياس
2.2.6 تحليل حصة البائع
2.2.7 نقاط البيانات من المقابلات الأولية الرئيسية
2.2.8 نقاط البيانات من قواعد البيانات الثانوية الرئيسية
2.3 سوق الاستعانة بمصادر خارجية لتنظيم التشخيص المخبري (IVD) العالمي: لمحة بحثية
2.4 الافتراضات
3. نظرة عامة على السوق
3.1 السائقين
3.2 القيود
3.3 الفرص
3.4 التحديات
4. رؤى مميزة
4.1 تحليل بيستل
4.2 نموذج بورتر للقوى الخمس
5. رؤى الصناعة
5.1 العوامل الاقتصادية الجزئية والكلي
5.2 رسم خرائط آفاق الاختراق والنمو
5.3 استراتيجيات التسعير الرئيسية
5.4 المقابلات مع المتخصصين
5.5 التحليل والتوصية
6. محفظة الملكية الفكرية
6.1 جودة وقوة براءة الاختراع
6.2 عائلات براءات الاختراع
6.3 الترخيص والتعاون
6.4 المشهد التنافسي
6.5 استراتيجية وإدارة الملكية الفكرية
6.6 أخرى
7. تفاصيل تحليل التكلفة
8. خريطة طريق التكنولوجيا
9. متتبع الابتكار والتحليل الاستراتيجي
9.1 تحليل الصفقات الكبرى والتحالفات الاستراتيجية
9.1.1 المشاريع المشتركة
9.1.2 عمليات الدمج والاستحواذ
9.1.3 الترخيص والشراكة
9.1.4 التعاون التكنولوجي
9.1.5 عمليات التخارج الاستراتيجية
9.2 عدد المنتجات قيد التطوير
9.3 مرحلة التطوير
9.4 الجداول الزمنية والمعالم
9.5 استراتيجيات ومنهجيات الابتكار
9.6 تقييم المخاطر والتخفيف منها
9.7 التوقعات المستقبلية
10. الامتثال التنظيمي
10.1 الهيئات التنظيمية
10.2 التصنيفات التنظيمية
10.2.1 الفئة الأولى
10.2.2 الفئة الثانية
10.2.3 الفئة الثالثة
10.3 التقديمات التنظيمية
10.4 التناغم الدولي
10.5 أنظمة الامتثال وإدارة الجودة
10.6 التحديات والاستراتيجيات التنظيمية
11. إطار السداد
12. تحليل خريطة الفرص
13. بيانات القاعدة المُثبّتة
14. تحليل سلسلة القيمة
15. اقتصاد الرعاية الصحية
15.1 نفقات الرعاية الصحية
15.2 النفقات الرأسمالية
15.3 اتجاهات الإنفاق الرأسمالي
15.4 تخصيص النفقات الرأسمالية
15.5 مصادر التمويل
15.6 معايير الصناعة
15.7 نسبة الناتج المحلي الإجمالي إلى الناتج المحلي الإجمالي
15.8 هيكل نظام الرعاية الصحية
15.9 سياسات الحكومة
15.10 التنمية الاقتصادية
16. سوق الاستعانة بمصادر خارجية لتنظيم التشخيص المخبري (IVD) العالمي، حسب الخدمة
16.1 نظرة عامة
16.2 الكتابة التنظيمية والتقديمات
16.3 التسجيل التنظيمي وطلبات التجارب السريرية
16.4 الاستشارات التنظيمية
16.5 التمثيل القانوني
16.6 خدمات إدارة البيانات
16.7 خدمات تصنيع وتحكم الكيمياء (CMC)
16.8 آخرون
17. سوق الاستعانة بمصادر خارجية لتنظيم التشخيص المختبري (IVD) عالميًا، حسب المؤشرات
17.1 نظرة عامة
17.2 علم الأورام
17.3 علم الأعصاب
17.4 أمراض القلب
17.5 الكيمياء السريرية والاختبارات المناعية
17.6 الطب الدقيق
17.7 الأمراض المعدية
17.7.1 تعفن الدم
17.7.2 علم الفيروسات
17.7.3 علم البكتيريا
17.7.4 علم الأحياء الدقيقة والفطريات
17.7.5 التهاب الكبد الوبائي ب
17.7.6 التهاب الكبد الوبائي سي
17.7.7 مرض الزهري
17.7.8 مرض السل
17.7.9 الملاريا
17.7.10 عدوى فيروس الورم الحليمي البشري (HPV)
17.7.11 آخرون
17.8 مرض السكري
17.9 الاختبارات الجينية
17.10 فيروس نقص المناعة البشرية/الإيدز
17.11 أمراض الدم
17.12 اختبار الأدوية/علم الصيدلة الجيني
17.13 نقل الدم
17.14 آخرون
18. سوق الاستعانة بمصادر خارجية لتنظيم التشخيص المختبري (IVD) العالمي، حسب المرحلة
18.1 نظرة عامة
18.2 ما قبل السريرية
18.3 السريرية
18.4 PMA (تفويض ما بعد التسويق)
19. سوق الاستعانة بمصادر خارجية لتنظيم التشخيص المخبري (IVD) العالمي، حسب الفئة
19.1 نظرة عامة
19.2 الفئة الأولى
19.3 الفئة الثانية
19.4 الفئة الثالثة
20. سوق الاستعانة بمصادر خارجية لتنظيم التشخيص المختبري (IVD) عالميًا، حسب النوع
20.1 نظرة عامة
20.2 منتج التشخيص المخبري في نقطة الرعاية (POC)
20.3 منتجات الاختبارات المعملية (LDTS) IVD
20.4 منتج التشخيص المصاحب IVD
20.5 اختبار المنتج IVD مباشرة إلى المستهلك (DTC)
20.6 منتجات IVD أخرى
21. سوق الاستعانة بمصادر خارجية لتنظيم التشخيص المخبري (IVD) العالمي، حسب طريقة النشر
21.1 نظرة عامة
21.2 السحابة
21.3 في الموقع
22. سوق الاستعانة بمصادر خارجية لتنظيم التشخيص المختبري (IVD) عالميًا، حسب حجم المنظمة
22.1 نظرة عامة
22.2 الشركات الصغيرة والمتوسطة
22.3 الشركات الكبيرة
23. سوق الاستعانة بمصادر خارجية لتنظيم التشخيص المختبري (IVD) العالمي، حسب المستخدم النهائي
23.1 نظرة عامة
23.2 شركات الأدوية
23.2.1 حسب حجم المنظمة
23.2.1.1. الشركات الصغيرة والمتوسطة
23.2.1.2. الشركات الكبيرة
23.2.2 حسب الخدمة
23.2.2.1. الكتابة التنظيمية والتقديمات
23.2.2.2. التسجيل التنظيمي وطلبات التجارب السريرية
23.2.2.3. الاستشارات التنظيمية
23.2.2.4. التمثيل القانوني
23.2.2.5. خدمات إدارة البيانات
23.2.2.6. خدمات تصنيع وضبط الكيمياء (CMC)
23.2.2.7. آخرون
23.3 شركات الأجهزة الطبية
23.3.1 حسب حجم المنظمة
23.3.1.1. الشركات الصغيرة والمتوسطة
23.3.1.2. الشركات الكبيرة
23.3.2 حسب الخدمة
23.3.2.1. الكتابة التنظيمية والتقديمات
23.3.2.2. التسجيل التنظيمي وطلبات التجارب السريرية
23.3.2.3. الاستشارات التنظيمية
23.3.2.4. التمثيل القانوني
23.3.2.5. خدمات إدارة البيانات
23.3.2.6. خدمات تصنيع وضبط الكيمياء (CMC)
23.3.2.7. آخرون
23.4 شركات التكنولوجيا الحيوية
23.4.1 حسب حجم المنظمة
23.4.1.1. الشركات الصغيرة والمتوسطة
23.4.1.2. الشركات الكبيرة
23.4.2 حسب الخدمة
23.4.2.1. الكتابة التنظيمية والتقديمات
23.4.2.2. التسجيل التنظيمي وطلبات التجارب السريرية
23.4.2.3. الاستشارات التنظيمية
23.4.2.4. التمثيل القانوني
23.4.2.5. خدمات إدارة البيانات
23.4.2.6. خدمات تصنيع وضبط الكيمياء (CMC)
23.4.2.7. آخرون
23.5 آخرون
24. سوق الاستعانة بمصادر خارجية لتنظيم التشخيص المختبري (IVD) عالميًا، حسب المنطقة
24.1 سوق الاستعانة بمصادر خارجية للشؤون التنظيمية للتشخيص المخبري (IVD) العالمي، (جميع التقسيمات المذكورة أعلاه مُمثلة في هذا الفصل حسب البلد)
24.1.1 أمريكا الشمالية
24.1.1.1. الولايات المتحدة
24.1.1.2. كندا
24.1.1.3. المكسيك
24.1.2 أوروبا
24.1.2.1. ألمانيا
24.1.2.2. فرنسا
24.1.2.3. المملكة المتحدة
24.1.2.4. إيطاليا
24.1.2.5. إسبانيا
24.1.2.6. روسيا
24.1.2.7. تركيا
24.1.2.8. بلجيكا
24.1.2.9. هولندا
24.1.2.10. سويسرا
24.1.2.11. بقية أوروبا
24.1.3 منطقة آسيا والمحيط الهادئ
24.1.3.1. اليابان
24.1.3.2. الصين
24.1.3.3. كوريا الجنوبية
24.1.3.4. الهند
24.1.3.5. أستراليا
24.1.3.6. سنغافورة
24.1.3.7. تايلاند
24.1.3.8. ماليزيا
24.1.3.9. إندونيسيا
24.1.3.10. الفلبين
24.1.3.11. بقية منطقة آسيا والمحيط الهادئ
24.1.4 أمريكا الجنوبية
24.1.4.1. البرازيل
24.1.4.2. الأرجنتين
24.1.4.3. بقية أمريكا الجنوبية
24.1.5 الشرق الأوسط وأفريقيا
24.1.5.1. جنوب أفريقيا
24.1.5.2. مصر
24.1.5.3. إسرائيل
24.1.5.4. الإمارات العربية المتحدة
24.1.5.5. المملكة العربية السعودية
24.1.5.6. بقية دول الشرق الأوسط وأفريقيا
24.1.6 الرؤى الأولية الرئيسية: حسب البلدان الرئيسية
25. سوق الاستعانة بمصادر خارجية لتنظيم التشخيص المخبري (IVD) العالمي، ومشهد الشركة
25.1 تحليل أسهم الشركة: عالميًا
25.2 تحليل أسهم الشركة: أمريكا الشمالية
25.3 تحليل أسهم الشركة: أوروبا
25.4 تحليل أسهم الشركة: منطقة آسيا والمحيط الهادئ
25.5 عمليات الدمج والاستحواذ
25.6 تطوير المنتجات الجديدة والموافقات عليها
25.7 التوسعات
25.8 التغييرات التنظيمية
25.9 الشراكة والتطورات الاستراتيجية الأخرى
26. سوق الاستعانة بمصادر خارجية لتنظيم التشخيص المخبري (IVD) العالمي، نبذة عن الشركة
26.1 حلول فراير
26.1.1 نظرة عامة على الشركة
26.1.2 لمحة عامة عن الشركة
26.1.3 تحليل الإيرادات
26.1.4 محفظة المنتجات
26.1.5 التطورات الأخيرة
26.2 شركة أكسورس للاستشارات
26.2.1 نظرة عامة على الشركة
26.2.2 لمحة عامة عن الشركة
26.2.3 تحليل الإيرادات
26.2.4 محفظة المنتجات
26.2.5 التطورات الأخيرة
26.3 مجموعة لورينز لعلوم الحياة
26.3.1 نظرة عامة على الشركة
26.3.2 لمحة عامة عن الشركة
26.3.3 تحليل الإيرادات
26.3.4 محفظة المنتجات
26.3.5 التطورات الأخيرة
26.4 شركة لابوراتوري كوربوريشن أوف أمريكا القابضة
26.4.1 نظرة عامة على الشركة
26.4.2 لمحة عامة عن الشركة
26.4.3 تحليل الإيرادات
26.4.4 محفظة المنتجات
26.4.5 التطورات الأخيرة
26.5 شركة ريج اي كيو المحدودة
26.5.1 نظرة عامة على الشركة
26.5.2 لمحة عامة عن الشركة
26.5.3 تحليل الإيرادات
26.5.4 محفظة المنتجات
26.5.5 التطورات الأخيرة
26.6 بروميديكا الدولية، وهي شركة كاليفورنيا (IUVO Biosciences)
26.6.1 نظرة عامة على الشركة
26.6.2 لمحة عامة عن الشركة
26.6.3 تحليل الإيرادات
26.6.4 محفظة المنتجات
26.6.5 التطورات الأخيرة
26.7 ماكروكير
26.7.1 نظرة عامة على الشركة
26.7.2 لمحة عامة عن الشركة
26.7.3 تحليل الإيرادات
26.7.4 محفظة المنتجات
26.7.5 التطورات الأخيرة
26.8 EMERGO بواسطة UL
26.8.1 نظرة عامة على الشركة
26.8.2 لمحة عامة عن الشركة
26.8.3 تحليل الإيرادات
26.8.4 محفظة المنتجات
26.8.5 التطورات الأخيرة
26.9 شركة ايكون بي ال سي
26.9.1 نظرة عامة على الشركة
26.9.2 لمحة عامة عن الشركة
26.9.3 تحليل الإيرادات
26.9.4 محفظة المنتجات
26.9.5 التطورات الأخيرة
26.10 ووشي أبتيك
26.10.1 نظرة عامة على الشركة
26.10.2 لمحة عامة عن الشركة
26.10.3 تحليل الإيرادات
26.10.4 محفظة المنتجات
26.10.5 التطورات الأخيرة
26.11 شركة ثيرمو فيشر العلمية
26.11.1 نظرة عامة على الشركة
26.11.2 لمحة عامة عن الشركة
26.11.3 تحليل الإيرادات
26.11.4 محفظة المنتجات
26.11.5 التطورات الأخيرة
26.12 مختبرات تشارلز ريفر.
26.12.1 نظرة عامة على الشركة
26.12.2 لمحة عامة عن الشركة
26.12.3 تحليل الإيرادات
26.12.4 محفظة المنتجات
26.12.5 التطورات الأخيرة
26.13 شركة أكسل للأبحاث السريرية، ذ.م.م.
26.13.1 نظرة عامة على الشركة
26.13.2 لمحة عامة عن الشركة
26.13.3 تحليل الإيرادات
26.13.4 محفظة المنتجات
26.13.5 التطورات الأخيرة
26.14 شركة باركسيل الدولية (MA)
26.14.1 نظرة عامة على الشركة
26.14.2 لمحة عامة عن الشركة
26.14.3 تحليل الإيرادات
26.14.4 محفظة المنتجات
26.14.5 التطورات الأخيرة
26.15 ميتيكون جي إم بي إتش
26.15.1 نظرة عامة على الشركة
26.15.2 لمحة عامة عن الشركة
26.15.3 تحليل الإيرادات
26.15.4 محفظة المنتجات
26.15.5 التطورات الأخيرة
26.16 جينباكت
26.16.1 نظرة عامة على الشركة
26.16.2 لمحة عامة عن الشركة
26.16.3 تحليل الإيرادات
26.16.4 محفظة المنتجات
26.16.5 التطورات الأخيرة
26.17 كريتيريوم، المحدودة
26.17.1 نظرة عامة على الشركة
26.17.2 لمحة عامة عن الشركة
26.17.3 تحليل الإيرادات
26.17.4 محفظة المنتجات
26.17.5 التطورات الأخيرة
26.18 ميدبيس
26.18.1 نظرة عامة على الشركة
26.18.2 لمحة عامة عن الشركة
26.18.3 تحليل الإيرادات
26.18.4 محفظة المنتجات
26.18.5 التطورات الأخيرة
26.19 مجموعة برودكت لايف ش.م.
26.19.1 نظرة عامة على الشركة
26.19.2 لمحة عامة عن الشركة
26.19.3 تحليل الإيرادات
26.19.4 محفظة المنتجات
26.19.5 التطورات الأخيرة
26.20 خدمات دور الصيدلانية
26.20.1 نظرة عامة على الشركة
26.20.2 لمحة عامة عن الشركة
26.20.3 تحليل الإيرادات
26.20.4 محفظة المنتجات
26.20.5 التطورات الأخيرة
26.21 خدمة QSERVE
26.21.1 نظرة عامة على الشركة
26.21.2 لمحة عامة عن الشركة
26.21.3 تحليل الإيرادات
26.21.4 محفظة المنتجات
26.21.5 التطورات الأخيرة
26.22 التشخيص السريري العظمي.
26.22.1 نظرة عامة على الشركة
26.22.2 لمحة عامة عن الشركة
26.22.3 تحليل الإيرادات
26.22.4 محفظة المنتجات
26.22.5 التطورات الأخيرة
26.23 شركة أنجستروم للتكنولوجيا الحيوية المحدودة
26.23.1 نظرة عامة على الشركة
26.23.2 لمحة عامة عن الشركة
26.23.3 تحليل الإيرادات
26.23.4 محفظة المنتجات
26.23.5 التطورات الأخيرة
26.24 ر.ق.+
26.24.1 نظرة عامة على الشركة
26.24.2 لمحة عامة عن الشركة
26.24.3 تحليل الإيرادات
26.24.4 محفظة المنتجات
26.24.5 التطورات الأخيرة
26.25 شركاء الامتثال التنظيمي (SOTERA HEALTH)
26.25.1 نظرة عامة على الشركة
26.25.2 لمحة عامة عن الشركة
26.25.3 تحليل الإيرادات
26.25.4 محفظة المنتجات
26.25.5 التطورات الأخيرة
26.26 ريسيرش دي اكس
26.26.1 نظرة عامة على الشركة
26.26.2 لمحة عامة عن الشركة
26.26.3 تحليل الإيرادات
26.26.4 محفظة المنتجات
26.26.5 التطورات الأخيرة
26.27 شركة سي إم آي سي القابضة المحدودة
26.27.1 نظرة عامة على الشركة
26.27.2 لمحة عامة عن الشركة
26.27.3 تحليل الإيرادات
26.27.4 محفظة المنتجات
26.27.5 التطورات الأخيرة
26.28 جمعية العلوم الأمريكية الشمالية، ذ.م.م
26.28.1 نظرة عامة على الشركة
26.28.2 لمحة عامة عن الشركة
26.28.3 تحليل الإيرادات
26.28.4 محفظة المنتجات
26.28.5 التطورات الأخيرة
26.29 كاراد بي في
26.29.1 نظرة عامة على الشركة
26.29.2 لمحة عامة عن الشركة
26.29.3 تحليل الإيرادات
26.29.4 محفظة المنتجات
26.29.5 التطورات الأخيرة
26.30 نص
26.30.1 نظرة عامة على الشركة
26.30.2 لمحة عامة عن الشركة
26.30.3 تحليل الإيرادات
26.30.4 محفظة المنتجات
26.30.5 التطورات الأخيرة
26.31 CLIN-R+
26.31.1 نظرة عامة على الشركة
26.31.2 لمحة عامة عن الشركة
26.31.3 تحليل الإيرادات
26.31.4 محفظة المنتجات
26.31.5 التطورات الأخيرة
26.32 VCLS
26.32.1 نظرة عامة على الشركة
26.32.2 لمحة عامة عن الشركة
26.32.3 تحليل الإيرادات
26.32.4 محفظة المنتجات
26.32.5 التطورات الأخيرة
26.33 مجموعة بروفارما
26.33.1 نظرة عامة على الشركة
26.33.2 لمحة عامة عن الشركة
26.33.3 تحليل الإيرادات
26.33.4 محفظة المنتجات
26.33.5 التطورات الأخيرة
26.34 شركة أرييلو أيرلندا المحدودة
26.34.1 نظرة عامة على الشركة
26.34.2 لمحة عامة عن الشركة
26.34.3 تحليل الإيرادات
26.34.4 محفظة المنتجات
26.34.5 التطورات الأخيرة
ملاحظة: قائمة الشركات المذكورة ليست شاملة، بل هي بناءً على متطلبات عملائنا السابقين. لقد أعددنا أكثر من 100 شركة في دراستنا، وبالتالي، يمكن تعديل قائمة الشركات أو استبدالها عند الطلب.
27. التقارير ذات الصلة
28. الاستبيان
29. حول أبحاث سوق جسر البيانات
منهجية البحث
يتم جمع البيانات وتحليل سنة الأساس باستخدام وحدات جمع البيانات ذات أحجام العينات الكبيرة. تتضمن المرحلة الحصول على معلومات السوق أو البيانات ذات الصلة من خلال مصادر واستراتيجيات مختلفة. تتضمن فحص وتخطيط جميع البيانات المكتسبة من الماضي مسبقًا. كما تتضمن فحص التناقضات في المعلومات التي شوهدت عبر مصادر المعلومات المختلفة. يتم تحليل بيانات السوق وتقديرها باستخدام نماذج إحصائية ومتماسكة للسوق. كما أن تحليل حصة السوق وتحليل الاتجاهات الرئيسية هي عوامل النجاح الرئيسية في تقرير السوق. لمعرفة المزيد، يرجى طلب مكالمة محلل أو إرسال استفسارك.
منهجية البحث الرئيسية التي يستخدمها فريق بحث DBMR هي التثليث البيانات والتي تتضمن استخراج البيانات وتحليل تأثير متغيرات البيانات على السوق والتحقق الأولي (من قبل خبراء الصناعة). تتضمن نماذج البيانات شبكة تحديد موقف البائعين، وتحليل خط زمني للسوق، ونظرة عامة على السوق ودليل، وشبكة تحديد موقف الشركة، وتحليل براءات الاختراع، وتحليل التسعير، وتحليل حصة الشركة في السوق، ومعايير القياس، وتحليل حصة البائعين على المستوى العالمي مقابل الإقليمي. لمعرفة المزيد عن منهجية البحث، أرسل استفسارًا للتحدث إلى خبراء الصناعة لدينا.
التخصيص متاح
تعد Data Bridge Market Research رائدة في مجال البحوث التكوينية المتقدمة. ونحن نفخر بخدمة عملائنا الحاليين والجدد بالبيانات والتحليلات التي تتطابق مع هدفهم. ويمكن تخصيص التقرير ليشمل تحليل اتجاه الأسعار للعلامات التجارية المستهدفة وفهم السوق في بلدان إضافية (اطلب قائمة البلدان)، وبيانات نتائج التجارب السريرية، ومراجعة الأدبيات، وتحليل السوق المجدد وقاعدة المنتج. ويمكن تحليل تحليل السوق للمنافسين المستهدفين من التحليل القائم على التكنولوجيا إلى استراتيجيات محفظة السوق. ويمكننا إضافة عدد كبير من المنافسين الذين تحتاج إلى بيانات عنهم بالتنسيق وأسلوب البيانات الذي تبحث عنه. ويمكن لفريق المحللين لدينا أيضًا تزويدك بالبيانات في ملفات Excel الخام أو جداول البيانات المحورية (كتاب الحقائق) أو مساعدتك في إنشاء عروض تقديمية من مجموعات البيانات المتوفرة في التقرير.