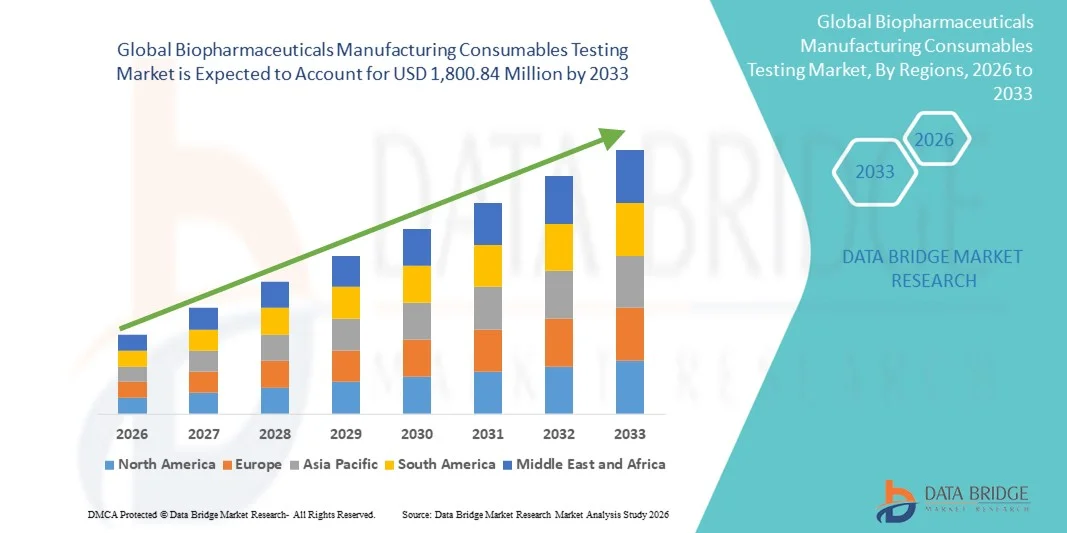
Global Biopharmaceuticals Manufacturing Consumables Testing Market
Marktgröße in Milliarden USD
CAGR :
% 
 USD
714.47 Million
USD
1,800.84 Million
2025
2033
USD
714.47 Million
USD
1,800.84 Million
2025
2033
| 2026 –2033 | |
| USD 714.47 Million | |
| USD 1,800.84 Million | |
|
|
|
|
Marktsegmentierung des globalen Marktes für die Prüfung von Verbrauchsmaterialien in der biopharmazeutischen Herstellung nach Dienstleistung (Laborprüfungen, kundenspezifische Prüfungen/herstellerspezifische Prüfungen und Arzneibuch- und Multi-Arzneibuch-Laborprüfungen), Rohstoffart (Formulierungshilfsstoffe, pharmazeutische Wirkstoffe (API) und Arzneibuchmethoden (USP/EP/JP)) – Unterstützung durch Lieferantenqualifizierungsprogramme – Branchentrends und Prognose bis 2033
Marktgröße für Verbrauchsmaterialien zur Prüfung in der biopharmazeutischen Herstellung
- Der globale Markt für Testmaterialien für die biopharmazeutische Herstellung hatte im Jahr 2025 einen Wert von 714,47 Millionen US-Dollar und wird voraussichtlich bis 2033 auf 1.800,84 Millionen US-Dollar anwachsen , was einer durchschnittlichen jährlichen Wachstumsrate (CAGR) von 12,25 % im Prognosezeitraum entspricht.
- Das Marktwachstum wird primär durch die steigende biopharmazeutische Produktion, strenge regulatorische Anforderungen und den dringenden Bedarf an hochwertigen Verbrauchsmaterialien für die Prüfung angetrieben, um Produktsicherheit, Wirksamkeit und Zuverlässigkeit zu gewährleisten.
- Zudem steigern steigende Investitionen in Biologika, personalisierte Medizin und Auftragsfertigungsunternehmen (CMOs) die Nachfrage nach fortschrittlichen Testlösungen für Verbrauchsmaterialien, wodurch die Einführung robuster Qualitätskontrollmaßnahmen beschleunigt und das Marktwachstum vorangetrieben wird.
Marktanalyse für Verbrauchsmaterialien zur Prüfung in der biopharmazeutischen Herstellung
- Die Prüfung von Verbrauchsmaterialien für die Herstellung von Biopharmazeutika, einschließlich Labortests, kundenspezifischer Tests sowie Tests nach Arzneibuchvorgaben und mehreren Arzneibuchvorgaben, entwickelt sich zu einem unverzichtbaren Bestandteil der Biologika-Produktion und gewährleistet Produktsicherheit, Konformität und Prozesszuverlässigkeit in Produktionsanlagen jeder Größenordnung.
- Die steigende Nachfrage nach Biopharmazeutika und die strengen regulatorischen Anforderungen von Behörden wie der FDA und der EMA treiben die Einführung fortschrittlicher Testverfahren für Verbrauchsmaterialien voran, um Kontaminationsrisiken zu minimieren und die Chargenkonsistenz zu gewährleisten.
- Nordamerika dominierte den Markt für Testmaterialien für die biopharmazeutische Herstellung mit dem größten Umsatzanteil von 39,4 % im Jahr 2025, unterstützt durch eine ausgereifte Biopharma-Industrie, bedeutende F&E-Investitionen und eine starke Präsenz wichtiger Dienstleister, insbesondere in den USA, wo Innovationen bei Labortests und Anbieterqualifizierungsprogrammen rasant voranschreiten.
- Der asiatisch-pazifische Raum dürfte im Prognosezeitraum die am schnellsten wachsende Region auf dem Markt sein. Dies ist auf die Expansion von Auftragsfertigungsunternehmen (CMOs), die steigende Produktion von Biologika und den zunehmenden regulatorischen Fokus auf Qualität und Sicherheit in aufstrebenden Märkten wie China und Indien zurückzuführen.
- Das Segment der Labortests dominierte den Markt mit einem Anteil von 42,6 % im Jahr 2025. Dies ist auf seine entscheidende Rolle bei der Überprüfung der Qualität von Hilfsstoffen für die Formulierung, pharmazeutischen Wirkstoffen (APIs) und der Unterstützung von Lieferantenqualifizierungsprogrammen gemäß Arzneibuchmethoden (USP/EP/JP) zurückzuführen. Dadurch werden Compliance und Produktsicherheit in der modernen biopharmazeutischen Herstellung gewährleistet.
Berichtsumfang und Marktsegmentierung für Testmaterialien zur Herstellung von Biopharmazeutika
|
Attribute |
Testen von Verbrauchsmaterialien für die biopharmazeutische Herstellung – Wichtigste Markteinblicke |
|
Abgedeckte Segmente |
|
|
Abgedeckte Länder |
Nordamerika
Europa
Asien-Pazifik
Naher Osten und Afrika
Südamerika
|
|
Wichtige Marktteilnehmer |
|
|
Marktchancen |
|
|
Mehrwertdaten-Infosets |
Neben Einblicken in Marktszenarien wie Marktwert, Wachstumsrate, Segmentierung, geografische Abdeckung und Hauptakteure enthalten die von Data Bridge Market Research erstellten Marktberichte auch detaillierte Expertenanalysen, Patientenepidemiologie, Pipeline-Analysen, Preisanalysen und Informationen zum regulatorischen Rahmen. |
Markttrends für Verbrauchsmaterialien und Tests in der biopharmazeutischen Herstellung
Umstellung auf fortschrittliche analytische und kundenspezifische Testdienstleistungen
- Ein bedeutender und sich beschleunigender Trend auf dem globalen Markt für die Prüfung von Verbrauchsmaterialien in der biopharmazeutischen Herstellung ist die zunehmende Anwendung fortschrittlicher Analysemethoden und kundenspezifischer Prüfdienstleistungen, um eine höhere Genauigkeit, Reproduzierbarkeit und die Einhaltung sich entwickelnder regulatorischer Standards zu gewährleisten.
- Unternehmen wie SGS Life Sciences bieten beispielsweise maßgeschneiderte Testlösungen für Einwegsysteme, Filtrationseinheiten und Rohstoffe an, um spezifische Kundenanforderungen zu erfüllen und so die Prozessintegrität und Produktsicherheit zu gewährleisten.
- Die Integration von Hochdurchsatz-Testplattformen mit automatisierter Analytik ermöglicht die schnellere Erkennung von Verunreinigungen, Kontaminationen oder Abweichungen in pharmazeutischen Wirkstoffen (APIs) und Hilfsstoffen, wodurch Produktionsverzögerungen reduziert und eine gleichbleibende Chargenqualität unterstützt werden.
- Diese fortschrittlichen Testverfahren ermöglichen eine zentrale Qualitätskontrolle und erlauben es Herstellern, mehrere Verbrauchsmaterialien und Rohstoffeigenschaften über einen einzigen Arbeitsablauf zu überwachen und dadurch die Produktionseffizienz und die Einhaltung von Vorschriften zu optimieren.
- Dieser Trend hin zu präziseren, skalierbaren und kundenspezifischen Testlösungen verändert die Erwartungen der Hersteller an Qualitätssicherung und regulatorische Konformität. Daher erweitern Dienstleister wie Eurofins ihre KI-gestützten Testplattformen, um die prädiktive Analytik für die Rohmaterialleistung und Lieferantenqualifizierungsprogramme zu verbessern.
- Die Nachfrage nach anspruchsvollen Labor- und kundenspezifischen Testdienstleistungen wächst rasant – sowohl bei Auftragsherstellern (CMOs) als auch in der hauseigenen biopharmazeutischen Produktion –, da Unternehmen Prozesssicherheit, regulatorische Konformität und Produktsicherheit zunehmend priorisieren.
Marktdynamik für Verbrauchsmaterialien und Tests in der biopharmazeutischen Herstellung
Treiber
Steigerung der biopharmazeutischen Produktion und der regulatorischen Aufsicht
- Die weltweit steigende Nachfrage nach Biopharmazeutika sowie die strengen regulatorischen Anforderungen von Behörden wie der FDA und der EMA sind ein wesentlicher Treiber für die Einführung von Testdienstleistungen für Verbrauchsmaterialien.
- Beispielsweise erweiterte Charles River Laboratories im März 2025 seine Testkapazitäten für Hilfsstoffe und Wirkstoffe in der Arzneimittelherstellung mit dem Ziel, die Einhaltung der USP-, EP- und JP-Standards zu gewährleisten und so Hersteller von Biologika zu unterstützen.
- Da Hersteller bestrebt sind, Kontaminationsrisiken zu minimieren und eine gleichbleibende Produktqualität zu gewährleisten, liefern Tests von Verbrauchsmaterialien wichtige Validierungs- und Überwachungsfunktionen für Rohstoffe und Einwegkomponenten.
- Darüber hinaus erfordert der zunehmende Einsatz von Auftragsherstellern (CMOs) und komplexen Produktionsabläufen für Biologika zuverlässige und skalierbare Testdienstleistungen, um die Chargenkonsistenz und die Einhaltung regulatorischer Vorgaben zu gewährleisten.
- Die zunehmende Betonung der Produktion hochwertiger Biologika, verbunden mit der verstärkten Auslagerung von Testdienstleistungen, macht Labor- und kundenspezifische Tests zu einem integralen Bestandteil moderner biopharmazeutischer Herstellungsprozesse.
- Technologische Fortschritte bei Testmethoden, wie z. B. der schnelle Nachweis von Mikroorganismen und hochempfindliche Assays, ermöglichen eine schnellere Validierung und fördern die Akzeptanz in großtechnischen Produktionsanlagen.
Zurückhaltung/Herausforderung
Hohe Kosten und Bedarf an Spezialausrüstung
- Die hohen Betriebskosten im Zusammenhang mit der Prüfung fortschrittlicher Verbrauchsmaterialien und dem Bedarf an spezialisierter Analyseausrüstung stellen eine erhebliche Herausforderung für die Marktexpansion dar.
- Beispielsweise erfordert die Durchführung von Labortests gemäß mehreren Arzneibüchern für Wirkstoffe und Hilfsstoffe Investitionen in hochpräzise Instrumente, qualifiziertes Personal sowie die kontinuierliche Kalibrierung und Wartung.
- Kleinere Hersteller oder Auftragsfertiger in Schwellenländern könnten aufgrund der erheblichen Vorab- und laufenden Kosten auf Hindernisse bei der Markteinführung stoßen, was die Marktdurchdringung in preissensiblen Regionen einschränkt.
- Darüber hinaus erfordert die strikte Einhaltung zahlreicher regulatorischer Standards, darunter USP, EP und JP, kontinuierliche Schulungen und Validierungen, was die betriebliche Komplexität und die Kosten weiter erhöhen kann. Die Bewältigung dieser Herausforderungen durch skalierbare Testlösungen, Technologie-Sharing-Modelle und strategische Partnerschaften ist entscheidend für die Ausweitung der Marktreichweite bei gleichzeitiger Aufrechterhaltung von Qualität und Konformität.
- Die begrenzte Verfügbarkeit von geschultem Personal mit Fachkenntnissen in spezialisierten Testverfahren kann die Einführung von Dienstleistungen verlangsamen, insbesondere in aufstrebenden Regionen mit wachsender biopharmazeutischer Produktionstätigkeit.
- Schwankungen in der Rohstoffversorgung und Qualitätsschwankungen können zu zusätzlichem Aufwand und Kosten bei den Prüfungen führen und die gleichbleibende Servicequalität sowie die betriebliche Effizienz beeinträchtigen.
Marktumfang für Verbrauchsmaterialien und Tests in der biopharmazeutischen Herstellung
Der Markt ist nach Dienstleistungs- und Rohstoffart segmentiert.
- Durch den Service
Basierend auf den angebotenen Dienstleistungen ist der Markt in Labortests, kundenspezifische Tests und Arzneibuch- bzw. Multi-Arzneibuch-Labortests unterteilt. Das Segment der Labortests dominierte den Markt mit einem Umsatzanteil von 42,6 % im Jahr 2025. Dies ist auf seine entscheidende Rolle bei der Sicherstellung von Qualität, Sicherheit und Konformität biopharmazeutischer Verbrauchsmaterialien zurückzuführen. Routinemäßige Labortests validieren Hilfsstoffe, Wirkstoffe (APIs) und Einwegsysteme, um die Einhaltung strenger regulatorischer Anforderungen zu gewährleisten. Sie liefern Herstellern zuverlässige Daten, um die Chargenkonsistenz zu sichern und Kontaminationen zu vermeiden. Das Segment profitiert von einer hohen Akzeptanz bei Auftragsherstellern (CMOs) und großen biopharmazeutischen Produktionsstätten, die Wert auf robuste Qualitätskontrollprozesse legen. Darüber hinaus bieten Labortests skalierbare Lösungen, die es den Einrichtungen ermöglichen, große Probenmengen mit standardisierten Verfahren zu bearbeiten. Die breite Anwendung wird zusätzlich durch regulatorische Vorgaben wie die Konformitätsanforderungen von USP, EP und JP gefördert und macht Labortests zu einem Eckpfeiler der modernen biopharmazeutischen Produktion.
Das Segment der kundenspezifischen Prüfungen wird voraussichtlich von 2026 bis 2033 das schnellste Wachstum verzeichnen, getrieben durch die steigende Nachfrage nach spezialisierten und kundenspezifischen Prüflösungen. Hersteller und Auftragshersteller (CMOs) suchen nach maßgeschneiderten Prüfdienstleistungen für einzigartige Formulierungen, firmeneigene Hilfsstoffe und neuartige Biologika. Kundenspezifische Prüfungen gewährleisten die präzise Einhaltung von Kundenspezifikationen und regulatorischen Anforderungen und ermöglichen gleichzeitig Innovationen in der biopharmazeutischen Entwicklung. Die zunehmende Komplexität der Biologika-Produktion sowie der Trend zum Outsourcing von Prüfdienstleistungen treiben die Nutzung dieser Dienstleistungen voran. Anbieter flexibler, schneller und skalierbarer kundenspezifischer Prüflösungen gewinnen deutlich an Bedeutung. Darüber hinaus ermöglichen technologische Fortschritte bei analytischen Instrumenten präzisere und effizientere kundenspezifische Prüfungen und beschleunigen so das Marktwachstum in diesem Segment zusätzlich.
- Nach Rohmaterialart
Basierend auf der Art des Rohmaterials ist der Markt in Formulierungshilfsstoffe, pharmazeutische Wirkstoffe (API) und Unterstützung von Lieferantenqualifizierungsprogrammen gemäß Arzneibuchmethoden (USP/EP/JP) unterteilt. Das Segment der API-Prüfungen dominierte den Markt im Jahr 2025 aufgrund der entscheidenden Bedeutung der Überprüfung von Reinheit, Wirksamkeit und Stabilität pharmazeutischer Wirkstoffe vor deren Verwendung in der Biologika-Herstellung. Präzise API-Prüfungen verhindern Kontaminationen, gewährleisten die therapeutische Wirksamkeit und unterstützen die Einhaltung regulatorischer Vorgaben. Das Segment profitiert von einer hohen Akzeptanz in allen Phasen der Arzneimittelentwicklung, von der präklinischen Phase bis zur kommerziellen Produktion. Hersteller priorisieren API-Prüfungen, um Risiken in der Biologika-Produktion zu minimieren und Qualitätsstandards über mehrere Chargen hinweg aufrechtzuerhalten. Die weltweit strengen regulatorischen Rahmenbedingungen verstärken die Dominanz dieses Segments zusätzlich. Fortschrittliche Analysemethoden und automatisierte Plattformen verbessern die Effizienz und Zuverlässigkeit von API-Prüfungen und tragen so zu seiner anhaltenden Marktführerschaft bei.
Der Bereich der auf Arzneibuchmethoden basierenden Lieferantenqualifizierungsprogramme wird voraussichtlich von 2026 bis 2033 das schnellste Wachstum verzeichnen. Treiber dieser Entwicklung ist der steigende Bedarf an standardisierten Testprotokollen zur Qualifizierung von Rohstofflieferanten. Programme, die auf den Richtlinien von USP, EP und JP basieren, unterstützen Hersteller dabei, sicherzustellen, dass alle Materialien globalen Qualitätsstandards entsprechen. Das Wachstum der Auftragsfertigung und internationaler Lieferketten treibt die Nachfrage nach solchen Programmen an, um die Einhaltung von Vorschriften zu gewährleisten und Lieferkettenrisiken zu reduzieren. Darüber hinaus legen Aufsichtsbehörden im Rahmen der GMP-Konformität zunehmend Wert auf die Lieferantenqualifizierung, was die Akzeptanz weiter erhöht. Unternehmen, die integrierte Lösungen für die Lieferantenqualifizierung und -prüfung, einschließlich der Unterstützung mehrerer Arzneibücher, anbieten, erschließen sich neue Marktchancen. Fortschrittliche Datenmanagement- und Reporting-Tools steigern die Effizienz und Attraktivität dieses wachsenden Segments zusätzlich.
Regionale Analyse des Marktes für Verbrauchsmaterialien und Tests in der biopharmazeutischen Herstellung
- Nordamerika dominierte den Markt für Testmaterialien für die biopharmazeutische Herstellung mit dem größten Umsatzanteil von 39,4 % im Jahr 2025, unterstützt durch eine ausgereifte Biopharma-Industrie, bedeutende Investitionen in Forschung und Entwicklung sowie eine starke Präsenz wichtiger Dienstleister.
- Hersteller und Auftragshersteller in der Region legen großen Wert auf strenge Tests von Hilfsstoffen, Wirkstoffen und Einwegsystemen, um Produktsicherheit, Qualität und die Einhaltung globaler Standards zu gewährleisten.
- Diese breite Akzeptanz wird zusätzlich durch hohe Investitionen in Forschung und Entwicklung, eine fortschrittliche analytische Infrastruktur und die Präsenz führender Prüfdienstleister unterstützt, wodurch Nordamerika sich als wichtigstes Zentrum für hochwertige und zuverlässige Prüfdienstleistungen für Verbrauchsmaterialien etabliert.
Einblick in den US-amerikanischen Markt für Verbrauchsmaterialien und Tests in der biopharmazeutischen Herstellung
Der US-amerikanische Markt für die Prüfung von Verbrauchsmaterialien in der biopharmazeutischen Produktion wird 2025 mit 82 % den größten Umsatzanteil in Nordamerika erzielen. Treiber dieses Wachstums sind die etablierte biopharmazeutische Industrie des Landes und die strenge regulatorische Aufsicht durch die FDA. Hersteller legen zunehmend Wert auf qualitativ hochwertige Prüfungen von Hilfsstoffen, Wirkstoffen und Einwegsystemen, um Produktsicherheit, Konformität und Prozesszuverlässigkeit zu gewährleisten. Die wachsende Nutzung von Auftragsherstellern (CMOs) und fortschrittlichen Produktionsabläufen für Biologika treibt das Marktwachstum zusätzlich an. Darüber hinaus verbessert die Integration automatisierter Hochdurchsatz-Testtechnologien Effizienz und Genauigkeit und unterstützt so großtechnische Produktionsverfahren. Starke Investitionen in Forschung und Entwicklung, die Verfügbarkeit qualifizierter Fachkräfte und die Präsenz führender Prüfdienstleister festigen die Position der USA als wichtigen Standort für die Prüfung von Verbrauchsmaterialien.
Einblick in den europäischen Markt für Verbrauchsmaterialien und Tests in der biopharmazeutischen Herstellung
Der europäische Markt für Testmaterialien für die biopharmazeutische Produktion wird im Prognosezeitraum voraussichtlich ein deutliches Wachstum verzeichnen. Haupttreiber sind die strengen regulatorischen Anforderungen der EMA und die steigende Nachfrage nach qualitativ hochwertigen Biologika. Die zunehmende Urbanisierung und die Expansion von Auftragsherstellern (CMOs) in Ländern wie Deutschland, Frankreich und der Schweiz fördern die Nutzung fortschrittlicher Testdienstleistungen. Europäische Hersteller konzentrieren sich zudem auf die Einhaltung der Arzneibuchstandards von USP, EP und JP, um die Zuverlässigkeit ihrer Produktionsprozesse zu verbessern. Die Region verzeichnet ein signifikantes Wachstum sowohl bei kleinen als auch bei großen Biologika-Produktionsstätten, wobei Testdienstleistungen in neue Projekte und Erweiterungen integriert werden. Darüber hinaus fördern staatliche Initiativen zur Unterstützung von Innovationen und Qualitätskontrolle in der Pharmaindustrie die Marktentwicklung zusätzlich.
Einblick in den britischen Markt für Verbrauchsmaterialien und Tests in der biopharmazeutischen Herstellung
Der Markt für Testmaterialien für die biopharmazeutische Produktion in Großbritannien wird im Prognosezeitraum voraussichtlich ein beachtliches Wachstum verzeichnen. Treiber dieser Entwicklung sind die steigende Nachfrage nach hochwertigen Biologika und die strengen regulatorischen Vorgaben. Das wachsende Bewusstsein für Sicherheit, Qualität und Wirksamkeit veranlasst Hersteller und Auftragshersteller (CMOs) zur Nutzung fortschrittlicher Labor- und kundenspezifischer Testdienstleistungen. Das starke pharmazeutische Forschungsökosystem Großbritanniens in Kombination mit zuverlässigen Auftragsprüfdienstleistungen dürfte das Marktwachstum weiterhin beflügeln. Darüber hinaus erfordern die Ausweitung der Biologika-Produktion und die zunehmende Komplexität der Formulierungen anspruchsvolle Testlösungen für Verbrauchsmaterialien, um eine gleichbleibende Produktqualität und die Einhaltung regulatorischer Vorgaben zu gewährleisten.
Einblick in den deutschen Markt für Verbrauchsmaterialien und Tests in der biopharmazeutischen Herstellung
Der deutsche Markt für Testmaterialien für die biopharmazeutische Produktion wird im Prognosezeitraum voraussichtlich ein beachtliches Wachstum verzeichnen. Treiber dieser Entwicklung sind der starke Fokus des Landes auf Innovation, hohe Produktionsstandards und die Einhaltung regulatorischer Vorgaben. Die ausgereifte pharmazeutische und biotechnologische Infrastruktur Deutschlands fördert die Nutzung von Labor-, kundenspezifischen und Arzneibuch-Testdienstleistungen, insbesondere in der großtechnischen Biologika-Produktion. Die Integration von Testabläufen mit automatisierten Qualitätskontrollsystemen schreitet zunehmend voran und steigert Effizienz und Genauigkeit. Lokale Hersteller und Auftragshersteller (CMOs) legen zudem Wert auf ökologische Nachhaltigkeit und Prozessoptimierung und treiben so die Anwendung fortschrittlicher Testmethoden voran.
Markteinblicke für Verbrauchsmaterialien und Tests in der biopharmazeutischen Herstellung im asiatisch-pazifischen Raum
Der Markt für die Prüfung von Verbrauchsmaterialien in der biopharmazeutischen Produktion im asiatisch-pazifischen Raum wird im Prognosezeitraum von 2026 bis 2033 voraussichtlich mit einer jährlichen Wachstumsrate (CAGR) von 23 % am schnellsten wachsen. Treiber dieses Wachstums sind die steigende Produktion von Biologika, die Expansion von Auftragsherstellern (CMOs) und der zunehmende regulatorische Fokus in Ländern wie China, Japan und Indien. Die wachsende pharmazeutische Produktionskapazität der Region, kombiniert mit staatlichen Initiativen zur Förderung von Compliance und Qualitätssicherung, treibt die Nutzung von Testdienstleistungen voran. Darüber hinaus macht die Verfügbarkeit kostengünstiger Testlösungen und lokaler Dienstleister die Prüfung von Verbrauchsmaterialien in Schwellenländern zugänglicher. Technologische Fortschritte und der steigende Bedarf an hochwertigen Biologika tragen zusätzlich zum Marktwachstum bei.
Einblick in den japanischen Markt für Verbrauchsmaterialien und Tests in der biopharmazeutischen Herstellung
Der japanische Markt für die Prüfung von Verbrauchsmaterialien in der biopharmazeutischen Produktion gewinnt aufgrund des hochentwickelten pharmazeutischen Forschungsökosystems, der steigenden Biologika-Produktion und der strengen regulatorischen Rahmenbedingungen zunehmend an Dynamik. Hersteller setzen verstärkt auf hochpräzise Labor- und kundenspezifische Prüfdienstleistungen, um die Einhaltung von Vorschriften und die Zuverlässigkeit ihrer Produkte zu gewährleisten. Die Integration von Prüfabläufen mit automatisierter Analytik und Lieferantenqualifizierungsprogrammen steigert die betriebliche Effizienz. Die Nachfrage nach strengen Prüfungen wird zudem durch Japans Fokus auf Qualität, Sicherheit und Prozessstandardisierung sowohl in Eigenproduktionsstätten als auch in Auftragsfertigungsanlagen (CMOs) befeuert. Darüber hinaus fördert die Einführung innovativer Biologika und komplexer Formulierungen das Wachstum spezialisierter Prüfdienstleistungen.
Einblick in den indischen Markt für Verbrauchsmaterialien und Tests in der biopharmazeutischen Herstellung
Der Markt für Testmaterialien für die biopharmazeutische Produktion in Indien wird 2025 den größten Umsatzanteil im asiatisch-pazifischen Raum erzielen. Dies ist auf den expandierenden pharmazeutischen Produktionssektor des Landes, die rasante Produktion von Biologika und das steigende Bewusstsein für regulatorische Anforderungen zurückzuführen. Indien entwickelt sich zu einem wichtigen Zentrum für Auftragshersteller (CMOs) und Prüfdienstleister und unterstützt sowohl nationale als auch internationale Kunden. Das Bestreben nach der Einhaltung globaler Qualitätsstandards, steigende Investitionen in die analytische Infrastruktur und die Verfügbarkeit kostengünstiger Testlösungen fördern die Akzeptanz. Darüber hinaus treibt die wachsende Nachfrage nach hochwertigen Biologika und personalisierten Arzneimitteln den Bedarf an Labor-, kundenspezifischen und Arzneibuchprüfungen in Indien an.
Marktanteil bei Verbrauchsmaterialien für die Prüfung in der biopharmazeutischen Herstellung
Die Branche für Testmaterialien in der biopharmazeutischen Herstellung wird hauptsächlich von etablierten Unternehmen dominiert, darunter:
- Alcami Corporation (USA)
- Merck KGaA (Deutschland)
- Eurofins Scientific (Luxemburg)
- Agilent Technologies, Inc. (USA)
- Charles River Laboratories (USA)
- Catalent, Inc. (USA)
- Element Materials Technology (UK)
- Pace Analytical Services, LLC (USA)
- Nelson Laboratories, LLC (USA)
- BioSpectra, Inc. (USA)
- Avomeen Analytical Services (USA)
- MabPlex International Ltd. (UK)
- SGS SA (Schweiz)
- Lonza (Schweiz)
- TOXIKON (USA)
- Boston Scientific Corporation (USA)
- STERIS (USA)
- Pharmetric Laboratory (UK)
- Albany Molecular Research Inc. (USA)
- Triclinic Labs, Inc. (USA)
Welche aktuellen Entwicklungen gibt es auf dem globalen Markt für Testmaterialien zur Herstellung biopharmazeutischer Produkte?
- Im September 2024 erweiterte Eurofins Scientific sein Netzwerk für die Prüfung von Biopharmazeutika-Produkten in den USA durch die Übernahme von Infinity Laboratories, Inc. (acht Labore in den USA). Dadurch vergrößerte das Unternehmen seine Reichweite im Bereich der mikrobiologischen, chemischen und Verpackungsprüfung von Biopharmazeutika-Verbrauchsmaterialien und stärkte somit seine Kapazitäten für die Prüfung von Verbrauchsmaterialien.
- Im April 2024 kündigte Charles River Laboratories die Einführung alternativer Testmethoden an, um die Abhängigkeit von Tierversuchen bei seinen Testdienstleistungen für Biopharmazeutika und Verbrauchsmaterialien zu verringern. Dies spiegelt einen Wandel hin zu fortschrittlicheren und ethischeren Testverfahren für Verbrauchsmaterialien wider.
- Im Februar 2024 kündigte Eurofins in seinem Rohstofflabor in Lancaster, Pennsylvania, einen neuen „Plattformansatz“ für die schnelle GMP-konforme Rohstoffprüfung (Chemie/Biochemie/Mikrobiologie/Viren) an, der auch Hochrisikokomponenten abdeckt. Dies bedeutet ein erweitertes Angebot für die Prüfung von Rohstoffen und Verbrauchsmaterialien für die Herstellung von Biologika.
- Im Januar 2024 reichte Rapid Micro Biosystems seinen 10-K-Bericht ein, in dem die Verfügbarkeit seiner automatisierten Verbrauchsmaterialien zur Unterstützung mikrobiologischer QC-Workflows für Biologika/Verbrauchsmaterialien hervorgehoben und die zunehmende Innovation bei Testwerkzeugen für Verbrauchsmaterialien verdeutlicht wurde.
- Im März 2022 kündigte die Intertek Group plc die Übernahme von SASTech LLC an, um ihre Dienstleistungen im Bereich der pharmazeutischen und biopharmazeutischen Testverfahren auszubauen und die Kapazitäten für die Prüfung von Verbrauchsmaterialien in der biopharmazeutischen Lieferkette zu stärken.
SKU-
Erhalten Sie Online-Zugriff auf den Bericht zur weltweit ersten Market Intelligence Cloud
- Interaktives Datenanalyse-Dashboard
- Unternehmensanalyse-Dashboard für Chancen mit hohem Wachstumspotenzial
- Zugriff für Research-Analysten für Anpassungen und Abfragen
- Konkurrenzanalyse mit interaktivem Dashboard
- Aktuelle Nachrichten, Updates und Trendanalyse
- Nutzen Sie die Leistungsfähigkeit der Benchmark-Analyse für eine umfassende Konkurrenzverfolgung
Forschungsmethodik
Die Datenerfassung und Basisjahresanalyse werden mithilfe von Datenerfassungsmodulen mit großen Stichprobengrößen durchgeführt. Die Phase umfasst das Erhalten von Marktinformationen oder verwandten Daten aus verschiedenen Quellen und Strategien. Sie umfasst die Prüfung und Planung aller aus der Vergangenheit im Voraus erfassten Daten. Sie umfasst auch die Prüfung von Informationsinkonsistenzen, die in verschiedenen Informationsquellen auftreten. Die Marktdaten werden mithilfe von marktstatistischen und kohärenten Modellen analysiert und geschätzt. Darüber hinaus sind Marktanteilsanalyse und Schlüsseltrendanalyse die wichtigsten Erfolgsfaktoren im Marktbericht. Um mehr zu erfahren, fordern Sie bitte einen Analystenanruf an oder geben Sie Ihre Anfrage ein.
Die wichtigste Forschungsmethodik, die vom DBMR-Forschungsteam verwendet wird, ist die Datentriangulation, die Data Mining, die Analyse der Auswirkungen von Datenvariablen auf den Markt und die primäre (Branchenexperten-)Validierung umfasst. Zu den Datenmodellen gehören ein Lieferantenpositionierungsraster, eine Marktzeitlinienanalyse, ein Marktüberblick und -leitfaden, ein Firmenpositionierungsraster, eine Patentanalyse, eine Preisanalyse, eine Firmenmarktanteilsanalyse, Messstandards, eine globale versus eine regionale und Lieferantenanteilsanalyse. Um mehr über die Forschungsmethodik zu erfahren, senden Sie eine Anfrage an unsere Branchenexperten.
Anpassung möglich
Data Bridge Market Research ist ein führendes Unternehmen in der fortgeschrittenen formativen Forschung. Wir sind stolz darauf, unseren bestehenden und neuen Kunden Daten und Analysen zu bieten, die zu ihren Zielen passen. Der Bericht kann angepasst werden, um Preistrendanalysen von Zielmarken, Marktverständnis für zusätzliche Länder (fordern Sie die Länderliste an), Daten zu klinischen Studienergebnissen, Literaturübersicht, Analysen des Marktes für aufgearbeitete Produkte und Produktbasis einzuschließen. Marktanalysen von Zielkonkurrenten können von technologiebasierten Analysen bis hin zu Marktportfoliostrategien analysiert werden. Wir können so viele Wettbewerber hinzufügen, wie Sie Daten in dem von Ihnen gewünschten Format und Datenstil benötigen. Unser Analystenteam kann Ihnen auch Daten in groben Excel-Rohdateien und Pivot-Tabellen (Fact Book) bereitstellen oder Sie bei der Erstellung von Präsentationen aus den im Bericht verfügbaren Datensätzen unterstützen.