Global Fda Cleared Pediatric Wearable Devices Market
Marktgröße in Milliarden USD
CAGR :
% 
 USD
495.00 Million
USD
2,072.30 Million
2024
2032
USD
495.00 Million
USD
2,072.30 Million
2024
2032
| 2025 –2032 | |
| USD 495.00 Million | |
| USD 2,072.30 Million | |
|
|
|
|
Global FDA-Cleared Pediatric Wearable Devices Market Segmentation, By Device Type (Pulse Oximeter, Cardiac Monitore / ECG Wearables, Respiratory Monitore, Multi-Vital Monitore, Glucose Monitoring Wearables, und Sleep Trackers), Klinische Verwendung (Cardiac Monitoring, Respiratory Monitoring, Glucose Monitoring, Temperaturüberwachung und SIDS-Technologie
FDA-Cleared Pediatric Wearable Devices Marktgröße
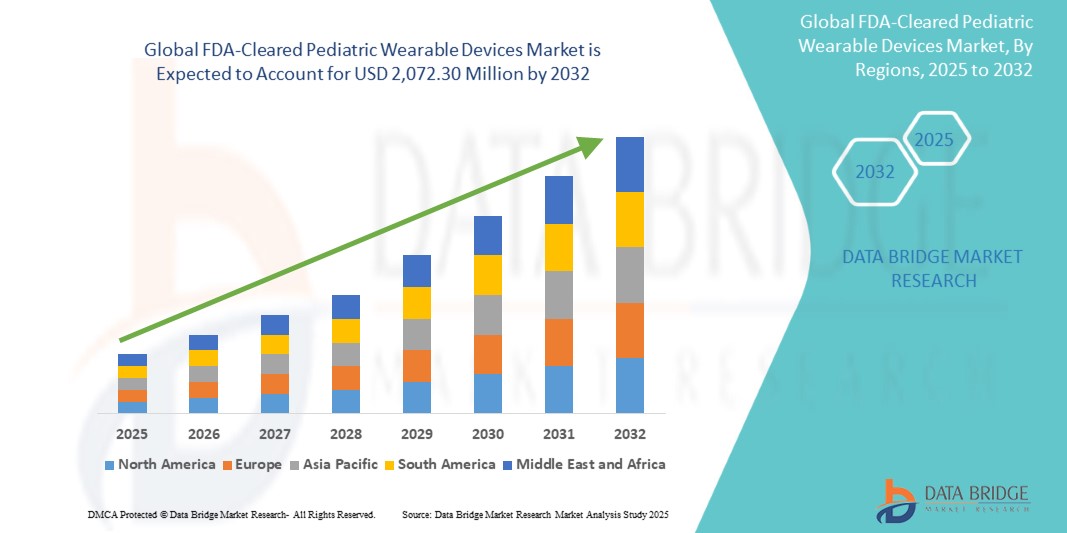
- Die globale FDA-geklärte pädiatrische Wearable Devices Marktgröße wurde bei495,00 Mio. USD in 2024und wird voraussichtlich erreichen2,072,30 Mio. USD bis 2032, beiCAGR von 19,60%während des Prognosezeitraums
- Das Marktwachstum wird weitgehend durch die zunehmende regulatorische Zulassung von pädiatrisch-fokussierten Wearables gefördert, zusammen mit Fortschritten in Sensortechnologien, die eine genaue Überwachung von Vitalzeichen, Schlaf und Atemfunktionen bei Kindern ermöglichen
- Darüber hinaus stellt die steigende Nachfrage sowohl von Pflegepersonen als auch von Gesundheitsdienstleistern für sichere, zuverlässige und Echtzeit-Überwachungslösungen die Positionierung von FDA-geklärten pädiatrischen Wearables als wesentliches Werkzeug in der Kindergesundheit dar. Diese konvergierenden Faktoren beschleunigen die Adoption in klinischen und hauseigenen Einstellungen, wodurch das Wachstum der Industrie deutlich erhöht wird
FDA-Cleared Pediatric Wearable Devices Marktanalyse
- Pädiatrische Wearable-Geräte, die eine Echtzeit-Überwachung von Vitalzeichen, Schlaf, Atemwegserkrankung und anderen pädiatrischen Bedingungen ermöglichen sollen, werden aufgrund ihrer Fähigkeit, genaue, kontinuierliche Daten und nahtlose Integration mit digitalen Gesundheitsplattformen zu liefern, immer wichtiger.
- Die eskalierende Nachfrage nach pädiatrischen Wearables wird in erster Linie durch die zunehmende regulatorische Absicherung der FDA, technologische Fortschritte bei Sensoren und Konnektivität und zunehmendes Bewusstsein bei Eltern und Gesundheitsdienstleistern über die Bedeutung einer proaktiven pädiatrischen Gesundheitsüberwachung gefördert.
- Nordamerika dominierte den pädiatrischen Wearable Devices-Markt mit dem größten Umsatzanteil von rund 39% im Jahr 2024, gekennzeichnet durch günstige regulatorische Rahmenbedingungen, starke Einführung von digitalen Gesundheitslösungen und die Präsenz von Pionieren, mit den USA erleben erhebliche Aufnahme in Krankenhaus- und Heimpflege-Umgebungen durch Innovationen in der Babyüberwachung und Remote-Patientenmanagement
- Asia-Pacific wird voraussichtlich die am schnellsten wachsende Region auf dem Markt für pädiatrische tragbare Geräte während der Prognosezeit aufgrund steigender Gesundheitsausgaben, steigender Geburtenraten und zunehmender Einführung von Technologien zur Überwachung der Kindergesundheit sein.
- Pulsoximeter-Geräte dominierten den Markt für pädiatrische tragbare Geräte im Jahr 2024 mit einem geschätzten Anteil von 40% des Marktes, angetrieben durch ihre kritische Rolle bei der Überwachung von Sauerstoffsättigung und Herzfrequenz in Neonaten und Säuglingen, zusammen mit der Erweiterung von FDA-Abteilungen, die sowohl verschreibungspflichtige als auch überzählige Anwendungsfälle unterstützen
Report Scope und FDA-Cleared Pediatric Wearable Devices Marktsegmentierung
| Attribute | FDA-Cleared Pediatric Wearable Devices Key Market Insights |
| Verdeckte Segmente |
|
| Überarbeitete Länder | Nordamerika
Europa
Asien-Pazifik
Naher Osten und Afrika
Südamerika
|
| Key Market Players |
|
| Marktmöglichkeiten |
|
| Daten Infos zum Wert hinzugefügt | Neben den Erkenntnissen über Marktszenarien wie Marktwert, Wachstumsrate, Segmentierung, geographische Erfassung und wichtige Akteure umfassen die Marktberichte, die von der Data Bridge Market Research kuratiert wurden, auch eingehende Expertenanalyse, Preisanalyse, Markenanteilsanalyse, Verbraucherumfrage, Demographieanalyse, Supply Chain Analyse, Wertschöpfungskettenanalyse, Rohstoff-/Verbrauchsübersicht, Herstellerauswahlkriterien, PESTLE Analyse, Porter Analysis und regulatorische Rahmenbedingungen. |
FDA-Cleared Pediatric Wearable Devices Markttrends
Steigende Annahme der Echtzeit-Pädiatrische Gesundheitsüberwachung
- Ein bedeutender und beschleunigter Trend im globalen Markt für pädiatrische Wearable Devices ist die zunehmende Integration von FDA-geklärten Technologien mit digitalen Gesundheitsplattformen und vernetzten Apps, die Verbesserung der Echtzeit-Pädiatrische Überwachung und Pflegemitteilung
- So erhielt der Owlet Dream Sock die Freigabe von FDA De Novo, so dass Eltern über eine angeschlossene mobile App Baby-Sauerstoffwerte und Herzfrequenz überwachen können und Vertrauen in verbrauchertaugliche, medizinisch validierte Lösungen schaffen
- FDA-geklärte pädiatrische Wearables verfügen jetzt über fortgeschritteneSensorenfür kontinuierliche SpO2, EKG und Atemüberwachung, ermöglicht eine proaktive Erkennung von Anomalien und sendet intelligente Alarme an Pflegekräfte und Kliniker in Echtzeit
- Die nahtlose Integration dieser Geräte mit Tele-Gesundheitsplattformen ermöglicht es Gesundheitsanbietern, Kinderpatienten fernzubeobachten, die zentrale Aufsicht und die Notwendigkeit von häufigen Krankenhausbesuchen ermöglichen
- Dieser Trend zu klinisch validierten, digital integrierten Wearables ist grundsätzlich eine Neuformung der pädiatrischen Versorgung. Daher entwickeln Unternehmen wie Masimo FDA-geklärte Kinderarzneimittel wie Stork, die sowohl für den Heim- als auch für den klinischen Einsatz mit vernetzten Überwachungsfunktionen konzipiert sind.
- Die Nachfrage nach pädiatrischen Wearables, die FDA-Freiheit, klinische Genauigkeit und Pflegekomfort kombinieren, wächst sowohl im Krankenhaus- als auch im Pflegebereich rapide, da Familien und Anbieter zunehmend Kindersicherheit und proaktives Gesundheitsmanagement priorisieren
FDA-Cleared Pediatric Wearable Devices Market Dynamics
Fahrer
steigende Nachfrage nach sicheren und zuverlässigen Pediatric Monitoring Lösungen
- Die zunehmende Prävalenz von neonatalen und Säuglingsgesundheitsrisiken, verbunden mit einer verstärkten Sensibilisierung unter den Pflegepersonen, ist ein bedeutender Treiber für die zunehmende Übernahme von FDA-geklärten Kinderarzneimitteln
- Zum Beispiel, im Juni 2023, Owlet, Inc. kündigte FDA-Freigabe für sein BabySat-Gerät an, die verschreibungspflichtige Verwendung für die Überwachung der Sauerstoffsättigung in Säuglingen ermöglicht, einen Durchbruch bei der Erweiterung der klinischen Qualitätsüberwachung in die Heimatumgebung.
- Da Eltern und Kliniker kontinuierliche, zuverlässige Gesundheitsdaten für Kinder suchen, bieten FDA-geklärte Wearables erweiterte Funktionen wie Echtzeit-Überwachung, historische Datenverfolgung und Pflegepersonal-Benachrichtigungen, die eine überzeugende Alternative zu traditionellen intermittierenden Überwachungsmethoden bieten
- Darüber hinaus sind das wachsende digitale Gesundheits-Ökosystem und die Integration mit Telemedizin-Diensten ein integraler Bestandteil von proaktiven Pflegemodellen, die nahtlose Verbindungen zwischen Pflegepersonen, Kindern und Gesundheitsdienstleistern bieten.
- Die Bequemlichkeit der Heimüberwachung, reduzierte Krankenhausabhängigkeit und die Fähigkeit, Echtzeitdaten mit Klinikern zu teilen, sind wichtige Faktoren, die die Annahme sowohl in der Pflege als auch im Krankenhaus fördern. Der Trend zu fernen Patientenüberwachungsprogrammen und unterstützenden Regulierungswegen trägt weiter zum Marktwachstum bei
Zurückhaltung/Challenge
Hautempfindlichkeitsprobleme und regulierende Compliance-Hürden
- Belange, die potenzielle Hautreizung durch längere Gerätenutzung, insbesondere bei Neonaten und Säuglingen, umgeben, stellen eine bedeutende Herausforderung für eine breitere Marktdurchdringung von pädiatrischen Wearables dar.
- Zum Beispiel haben klinische Bewertungen hervorgehoben, dass die kontinuierliche Verwendung von klebebasierten Monitoring-Patches bei Kindern zu Hautbeschwerden oder allergischen Reaktionen führen kann, wodurch Hesitanz bei Eltern und Pflegepersonen in Bezug auf die tägliche Adoption
- Diese Bedenken durch die Verwendung von hypoallergenen Materialien zu behandeln, ist eine verbesserte Geräteergonomie und regelmäßige Sicherheitstests für das Vertrauen im Gebäude entscheidend. Unternehmen wie Masimo betonen ihr pädiatrisches Design und komfortorientierte Funktionen in ihrem Marketing, um Pflegekräfte zu beruhigen
- Darüber hinaus können die hohen Regulierungsstandards für pädiatrische Geräte und lange FDA-Zulassungszeiträume die Kommerzialisierung verzögern und Hindernisse für kleinere Innovatoren im Raum schaffen. Während die Zulassungen beschleunigt werden, bleibt die Compliance komplex und ressourcenintensiv
- Die relativ höheren Kosten für FDA-geklärte Kindertragfähigkeiten im Vergleich zu Basis-Verbrauchermonitoren können auch die Übernahme von preisempfindlichen Familien, insbesondere in Entwicklungsregionen, behindern. Obwohl die Preise voraussichtlich sinken, bleibt die wahrgenommene Prämie für klinische Geräte ein begrenzender Faktor
- Die Bewältigung dieser Herausforderungen durch ein verbessertes pädiatrisches Design, schnellere regulatorische Wege und die Entwicklung günstigerer Optionen wird für ein nachhaltiges Marktwachstum von entscheidender Bedeutung sein
FDA-Cleared Pediatric Wearable Devices Market Scope
Der Markt wird auf der Grundlage von Gerätetyp, klinischer Verwendung, Technologie und Anwendung segmentiert.
- Mit Gerätetyp
Auf der Grundlage des Gerätetyps wird der FDA-geklärte Kindertragegerätemarkt in Pulsoximeter, Herzmonitore/ECG-Träger, Atemmonitore, Multivitalmonitore, Glukoseüberwachungsträger und Schlaftracker segmentiert. Das Segment Pulsoximeter dominierte den Markt im Jahr 2024 mit dem größten Marktanteil von 40%, der durch seine kritische Rolle bei der neonatalen und Säuglingsgesundheitsüberwachung getrieben wurde. Pulsoximeter sind weit verbreitet, um Sauerstoffsättigung und Herzfrequenz zu verfolgen, Parameter, die für die Erkennung von Atemnot und angeborenen Herzproblemen in Kinderpopulationen unerlässlich sind. Ihre Dominanz wird durch mehrere FDA-Reparaturen von Säuglingsgeräte wie Owlet BabySat und Masimo Stork verstärkt, die sowohl in der klinischen als auch in der Pflege stark angenommen haben. Das Segment profitiert von seiner nicht-invasiven Natur, kompaktem Design und Pflege Vertrauen, so dass es die am weitesten verbreitete pädiatrische Wearable Art. Da mehr Krankenhäuser und Heimpflegenutzer die Sauerstoffüberwachung in Kinderpflegeprotokolle integrieren, führen Pulsoximeter weiterhin die Gerätetypkategorie.
Das Segment Multivital Monitore wird voraussichtlich die schnellste Wachstumsrate von 2025 bis 2032 beobachten, die durch Fortschritte bei der verschleißbaren Sensorfusion und der steigenden Nachfrage nach integrierten Überwachungslösungen gefördert wird. Diese Geräte kombinieren mehrere Parameter – wie z.B. SpO2, Herzfrequenz, Atemfrequenz und Temperatur – in eine einzige verschleißbare, umfassende Einblicke in die Gesundheit eines Kindes. Ihre Fähigkeit, den Bedarf an mehreren Geräten zu reduzieren, verbessert den Pflegekomfort und verbessert die Adoption in klinischen Einstellungen, insbesondere für entfernte Patientenüberwachungsprogramme. Der steigende Schub für die vernetzte Gesundheit und die Notwendigkeit einer kontinuierlichen, Echtzeit-Pädiatriedatenerhebung beschleunigen die Annahme. Darüber hinaus werden laufende FDA-Zulassungen von multi-vitalen pädiatrischen Plattformen erwartet, um die klinische Akzeptanz und Rückerstattung Unterstützung zu erweitern, so dass dies der am schnellsten wachsende Gerätetyp.
- Durch klinische Anwendung
Auf Basis des klinischen Einsatzes wird der Markt der FDA-geklärten pädiatrischen Wearable Devices in die Herzüberwachung, die Atemüberwachung, die Glukoseüberwachung, die Temperaturüberwachung und die SIDS-Adjunct-Überwachung segmentiert. Das Segment der Atemüberwachung dominierte den Markt im Jahr 2024, angetrieben durch die hohe Prävalenz neonataler Atemkomplikationen und die Notwendigkeit einer kontinuierlichen Überwachung, um Apnoe und andere Bedingungen zu erkennen. Pädiatrische Atemwegserkrankungen spielen sowohl bei NICU-Einstellungen als auch bei der Hausüberwachung eine wichtige Rolle und bieten Echtzeitalarmungen für Pflegekräfte und Kliniker. Geräte, die Atemmuster und Sauerstoffspiegel verfolgen, sind besonders wichtig für vorzeitige Säuglinge, wo frühe Eingriffe lebensrettend sein können. FDA-geklärte Lösungen, wie sie für die Überwachung der Säuglingsattraktion bestimmt sind, haben die führende Rolle dieses Segments eingeprägt. Seine Dominanz wird auch durch eine starke klinische Validierung und weit verbreitete Adoption in Krankenhaus-Neonatal-Pflegeeinheiten weltweit unterstützt.
Das Segment der Glucoseüberwachung wird in der Prognosezeit mit dem schnellsten Tempo wachsen, das durch den steigenden Auftreten von pädiatrischen Diabetes und die Erhöhung der FDA-Zulassungen der kontinuierlichen Glukoseüberwachung (CGM)-Geräte für Kinder hervorgerufen wird. CGMs liefern Echtzeit-Glucoselesungen, Alarme für Hypoglykämie oder Hyperglykämie und Integration mit Insulinliefersystemen, so dass sie für Kinderdiatrie-Management unerlässlich. Eltern und Kliniker übernehmen zunehmend CGMs, um Finger-Stick-Tests zu reduzieren und die Lebensqualität für Kinder mit Diabetes Typ 1 zu verbessern. Die Freigabe von Geräten mit pädiatrischen Indikationen erhöht das Vertrauen und die Annahme. Mit einer starken Payer-Unterstützung und der Erweiterung der klinischen Richtlinien, die CGM-Nutzung bei Kindern beenden, wird dieses Segment am schnellsten Tempo wachsen.
- Von der Technik
Auf Basis der Technik wird der FDA-geclearte pädiatrische Wearable Devices-Markt in optische (PPG), elektrische (ECG), Beschleunigungsmesser und Bioimpedanz segmentiert. Das optische (PPG) Segment dominierte den Markt im Jahr 2024, vor allem wegen seiner Verwendung in Pulsoximetrie und Herzfrequenzüberwachung für Neonate und Säuglinge. PPG-basierte Geräte sind von zentraler Bedeutung für die meisten FDA-geklärten pädiatrischen Wearables und bieten nicht-invasive und kontinuierliche Messungen von Sauerstoffsättigung und Herzfrequenz. Die Technologie ist sowohl von Pflegepersonen als auch von Klinikern gut etabliert, zuverlässig und weit vertraut, so dass sie die bevorzugte Wahl für die kritische pädiatrische Überwachung ist. Seine Dominanz wird durch die Integration in führende FDA-genehmigte Geräte und ihre Rolle als Grundlage für viele vernetzte Heimüberwachungslösungen weiter unterstützt. Da PPG-Sensoren kleiner und genauer werden, fahren sie weiterhin den größten Teil der pädiatrischen Wearable Adoption.
Das Bioimpedanz-Segment wird voraussichtlich das schnellste Wachstum von 2025 bis 2032 aufnehmen, das von seinen wachsenden Anwendungen bei der Überwachung von Hydratation, Atemanstrengung und Schlafqualität in Kinderpopulationen angetrieben wird. Bio-Impedanz-Technologie bietet Einblicke in mehrere physiologische Funktionen, die über das hinausgehen, was traditionelle PPG- und ECG-Sensoren bieten. Der steigende Forschungsschwerpunkt auf Kinderschlafgesundheit und Atemüberwachung schafft Möglichkeiten für bio-impedanzbasierte Wearables. Die FDA-Wege nehmen immer mehr parametrische Geräte auf und öffnen die Tür für größere regulatorische Genehmigungen. Da diese Geräte von Forschungswerkzeugen auf den gängigen klinischen und verbraucherbezogenen Einsatz übergehen, wird erwartet, dass Bio-Impedanz-Verschleißstoffe eine rasche Aufnahme im pädiatrischen Segment sehen.
- Anwendung
Auf der Grundlage der Anwendung wird der Markt für pädiatrische Wearable-Geräte in Krankenhäuser, Heimpflege/Kliniken und ambulante/ambulante Kliniken segmentiert. Das Krankenhaussegment dominierte den Markt im Jahr 2024, unterstützt durch die hohe Nachfrage nach kontinuierlicher Überwachung in neonatalen Intensivstationen (NICUs) und Kinderstationen. Krankenhäuser verlassen sich auf FDA-geklärte Wearables, um Genauigkeit, Compliance und Integration mit breiteren Überwachungssystemen zu gewährleisten. Die Dominanz des Segments beruht auf dem kritischen Bedarf an zuverlässigen pädiatrischen Monitoringlösungen in der akuten Pflege, wo rechtzeitige Eingriffe die gesundheitlichen Ergebnisse erheblich beeinflussen können. Krankenhäuser dienen auch als Frühanwender von fortschrittlichen FDA-geklärten Geräten und setzen den Standard für klinische Validierung und Vertrauen. Mit starken Rückzahlungsstrukturen und klinischen Nachweisen halten Krankenhäuser den größten Umsatzanteil in dieser Kategorie.
Das Homecare/Caregivers-Segment wird in der Vorausschätzungsperiode mit dem schnellsten Tempo wachsen, das durch die Erhöhung der FDA-Zulassungen für über-the-counter (OTC) Kindertrag- und wachsende Pflegemittelpräferenzen für die On-Home-Überwachung gefördert wird. Geräte wie Owlet Dream Sock und Masimo Stork unterstreichen den Übergang zur Stärkung von Eltern mit zuverlässigen, FDA-geklärten Überwachungslösungen außerhalb der Krankenhausumgebung. Das Wachstum dieses Segments wird durch steigendes Bewusstsein für Kindergesundheitsrisiken, eine höhere Akzeptanz der Telegesundheit und die Bequemlichkeit der ständigen Überwachung zu Hause unterstützt. Da Gesundheitssysteme die Fernüberwachung von Patienten fördern, um die Krankenhausbelastung zu reduzieren, wird das Homecare-Segment als die am schnellsten wachsende Anwendungskategorie projiziert.
FDA-Cleared Pediatric Wearable Devices Markt Regionale Analyse
- Nordamerika dominierte mit dem größten Umsatzanteil von rund 39 % im Jahr 2024 den Markt für pädiatrische Wearable Devices, der sich durch günstige regulatorische Rahmenbedingungen, starke Einführung digitaler Gesundheitslösungen und die Präsenz von Pionieren auszeichnete.
- Caregivers und Healthcare-Anbieter in der Region schätzen die Genauigkeit, Sicherheit und Echtzeit-Einsichten, die von FDA-geklärten pädiatrischen Wearables angeboten werden, sowie ihre nahtlose Integration in Tele- und Remote-Patienten-Monitoring-Plattformen.
- Diese weit verbreitete Adoption wird weiter unterstützt durch fortgeschrittene Gesundheitsinfrastruktur, hohes Bewusstsein für pädiatrische Gesundheitsüberwachung und günstige Erstattungsprogramme, die Schaffung von FDA-geklärten pädiatrischen Wearables als vertrauenswürdige Lösung sowohl in klinischen als auch in der Pflegeumgebung
US FDA-Cleared Kindergeräte Markt Insight
Der US FDA-geclearte Kindertragegerätemarkt erfasste den größten Umsatzanteil von 79% im Jahr 2024 in Nordamerika, der durch eine starke FDA-Regulierungsunterstützung und eine steigende elterliche Nachfrage nach sicheren, klinisch validierten Monitoring-Tools getrieben wurde. Caregivers priorisieren zunehmend die kontinuierliche Überwachung von Vitalzeichen, Schlaf und chronischen Bedingungen durch FDA-geklärte Geräte, die eine Zuverlässigkeit gegenüber verbrauchertauglichen Wearables gewährleisten. Der Trend zur Integration von Tele-Gesundheit, kombiniert mit der Unterstützung von Versicherungen für Remote-Patienten Monitoring (RPM), beschleunigt die Adoption. Darüber hinaus erweitert die starke Zusammenarbeit zwischen Geräteherstellern und führenden Kinderkliniken den Marktfußabdruck weiter.
EuropaFDA-Cleared Pediatric Wearable DevicesMarktaufsicht
Der Markt für pädiatrische Wearable-Geräte in Europa wird im gesamten Prognosezeitraum mit einem beträchtlichen CAGR ausgebaut, vor allem durch die Erhöhung der Gesundheitsdigitalisierung, strenge Sicherheitsstandards für medizinische Geräte und steigende Investitionen in die pädiatrische Fernüberwachung. Die zunehmende Sensibilisierung der Eltern hinsichtlich der plötzlichen Kindergesundheitsrisiken und der Bedeutung der Früherkennung ist die Annahme. Die Region erlebt eine weit verbreitete Aufnahme von FDA-geklärten Geräten nicht nur in Krankenhäusern, sondern auch in Heimpflege-Einstellungen, wobei die Erstattungspolitiken in bestimmten Ländern einen breiteren Zugang unterstützen. Pädiatrische Wearables werden zunehmend in chronische Krankheitsmanagementprogramme integriert, wodurch das Marktwachstum weiter gestärkt wird.
U.K.FDA-Cleared Pediatric Wearable DevicesMarktaufsicht
Der US-amerikanische FDA-geclearte Kinderarzneimittelmarkt wird voraussichtlich während der Prognosezeit mit einem bemerkenswerten CAGR wachsen, der von der Annahme digitaler Gesundheitslösungen im NHS und der zunehmenden Betonung auf die Kinderbetreuungs-Wellnessüberwachung angetrieben wird. In Bezug auf die pädiatrischen Atemwegs- und Herzbedingungen sind die Ermutigung von Krankenhäusern und Eltern, wie die Annahme von klinisch zugelassenen Geräten. Die rasche Einführung von vernetzten Gesundheitssystemen und ihre starke regulatorische Ausrichtung mit internationalen medizinischen Standards unterstützen das Wachstum weiter. Der Ausbau der Telegesundheitsdienste und der Trend zur Heimüberwachung sollen weiterhin wichtige Wachstumsbeschleuniger sein.
DeutschlandFDA-Cleared Pediatric Wearable DevicesMarktaufsicht
Der Deutschland-FDA-geklärte Kindertragegerätemarkt wird voraussichtlich während des Prognosezeitraums mit einem beträchtlichen CAGR expandieren, was durch eine starke Nachfrage nach technologisch fortschrittlichen, klinisch zuverlässigen Überwachungssystemen bedingt ist. Der Schwerpunkt des Landes auf Innovationen im Gesundheitswesen und die digitale Gesundheitsintegration treibt die Adoption in Krankenhäusern und Pflegeumgebungen voran. Deutsche Eltern und Anbieter schätzen die Sicherheit, die Privatsphäre und die Präzision von FDA-geklärten pädiatrischen Wearables und richten sich an die hohen Standards der Nation für medizinische Technologie. Die Erweiterung von Kinderprogrammen und Kooperationen zwischen Krankenhäusern und Geräteherstellern fördern das Wachstum.
Asien-PazifikFDA-Cleared Pediatric Wearable DevicesMarktaufsicht
Der asiatisch-pazifische FDA-geklärte Kindertrage-Geräte-Markt ist bereit, in der Prognosezeit von 2025 bis 2032 am schnellsten CAGR von 23,5% zu wachsen, angetrieben durch schnelle Gesundheits-Digitalisierung, steigendes Bewusstsein für Kindergesundheitsüberwachung und einen Anstieg der pädiatrischen chronischen Bedingungen in Ländern wie China, Japan und Indien. Regierungsgestützte intelligente Gesundheitsinitiativen und die Verbesserung des Gesundheitszugangs sind die Übernahme von Geräten. Die Rolle der Region als Herstellungszentrum für medizinische Wearables ermöglicht auch die Erreichbarkeit und Zugänglichkeit und bringt pädiatrische Wearables sowohl für Premium-Stadtverbraucher als auch für aufstrebende Mittelschichtpopulationen.
JapanFDA-Cleared Pediatric Wearable DevicesMarktaufsicht
Der Japan FDA-geklärte pädiatrische Wearable Devices-Markt gewinnt aufgrund der starken Kultur der medizinischen Innovation, fortgeschrittenen Krankenhaussysteme und der hohen Einführung vernetzter Technologien an Dynamik. Japanische Eltern vereinen zunehmend klinisch validierte Geräte zur Überwachung von Schlafapnoe, Atemnot und Herzgesundheit bei Kindern. Die Integration von pädiatrischen Wearables mit IoT-basierten Krankenhaus- und Heimpflege-Plattformen beschleunigt die Adoption. Darüber hinaus treibt die alternde Pflegeperson Japans die Notwendigkeit von komfortablen, automatisierten Überwachungslösungen an, wodurch die Rolle der Kindertragfähigkeiten in der privaten und der klinischen Umgebung gestärkt wird.
IndienFDA-Cleared Pediatric Wearable DevicesMarktaufsicht
Der Markt für pädiatrische Wearable-Geräte in Indien entfiel 2024 auf den größten Marktanteil des Marktes in Asien-Pazifik, was einer schnellen Urbanisierung, steigenden Geburtenraten und einer starken Nachfrage nach Lösungen zur Überwachung der Kindergesundheit in der wachsenden Mittelschicht zuzuschreiben ist. Der Einfluss der Regierung auf die digitale Gesundheit und das Wachstum der privaten Kinderkliniken erhöhen die Annahme von FDA-geklärten Wearables. Erschwinglichkeit und lokalisierte Produktion von Überwachungsgeräten fördern die Aufnahme, insbesondere in städtischen Zentren. Es wird erwartet, dass das Bewusstsein für plötzliche Gesundheitsrisiken bei Säuglingskindern, kombiniert mit zunehmender Akzeptanz von hausbasierten Gesundheitstechnologien, eine langfristige Markterweiterung vorangetrieben wird.
FDA-Cleared Pediatric Wearable Devices Market Share
Die FDA-geklärte pädiatrische Wearable Devices-Industrie wird in erster Linie von etablierten Unternehmen geleitet, darunter:
- Sibel Health, Inc. (USA)
- Strados Labs (USA)
- BioIntelliSense, Inc. (USA)
- Masimo (USA)
- Aevice Health Pte Ltd (Singapur)
- Empatica Inc. (USA)
- CardiacSense Ltd (Israel)
- Owlet (USA)
- Medtronic (Irland)
- Fitbit LLC (USA)
- AMIT International Group FZE. (Schweiz)
- (Südkorea)
- Abbott (USA)
- Dexcom, Inc. (USA)
- Koninklijke Philips N.V. (Niederländische)
- NIHON KOHDEN CORPORATION (Japan)
- ResMed Inc. (USA)
- AliveCor, Inc. (USA)
- (Frankreich)
Was sind die jüngsten Entwicklungen im globalen FDA-Cleared Kindertragzeugmarkt?
- Im Juni 2025 genehmigte die FDA die Sonu Band von SoundHealth als erste tragbare, drogenfreie Behandlung für mittelschwere nasale Verstopfung bei Kindern im Alter von 12 und älter, Erweiterung der Kinderanzeige für das Gerät
- Im Mai 2025 erhielt Aevice Health's AeviceMD smart wearable Stethoscope die Freilassung der US FDA für den Einsatz in Kinderpatienten im Alter von 3 Jahren und älter, so dass es ein kontinuierlich überwachendes Heimrespirationswerkzeug für Kinder
- Im November 2024 erhielt Theranica eine erweiterte FDA Altersanzeige für sein Nerivio REN Wearable Gerät, so dass akute Migräne Behandlung bei Kindern im Alter von 8 und älter. Dies machte es die erste FDA-geklärte, nicht-drug Neuromodulationstherapie speziell für Kinder Migräne angegeben
- Im Juli 2024 absolvierte Strados Labs erfolgreich eine pädiatrische Validierungsasthma-Studie seiner RESP Biosensor-Technologie im Ann & Robert H. Lurie Kinderklinik von Chicago, um die Blutung bei Kindern zu erkennen, einen Schritt zur Sicherung der pädiatrischen FDA-Freigabe für das Gerät
- Im Februar 2024 kündigte Sibel Health seine ANNE One Wearable Monitoring-Plattform an, die ihre 4. FDA 510(k) Clearance erhielt, die kontinuierliche ambulante EKG, SpO2, Temperatur- und nicht-invasive Blutdruckmessungen an Jugendliche im Alter von 12 Jahren und darüber für Krankenhaus- und Heimeinstellungen verlängerte.
SKU-
Erhalten Sie Online-Zugriff auf den Bericht zur weltweit ersten Market Intelligence Cloud
- Interaktives Datenanalyse-Dashboard
- Unternehmensanalyse-Dashboard für Chancen mit hohem Wachstumspotenzial
- Zugriff für Research-Analysten für Anpassungen und Abfragen
- Konkurrenzanalyse mit interaktivem Dashboard
- Aktuelle Nachrichten, Updates und Trendanalyse
- Nutzen Sie die Leistungsfähigkeit der Benchmark-Analyse für eine umfassende Konkurrenzverfolgung
Forschungsmethodik
Die Datenerfassung und Basisjahresanalyse werden mithilfe von Datenerfassungsmodulen mit großen Stichprobengrößen durchgeführt. Die Phase umfasst das Erhalten von Marktinformationen oder verwandten Daten aus verschiedenen Quellen und Strategien. Sie umfasst die Prüfung und Planung aller aus der Vergangenheit im Voraus erfassten Daten. Sie umfasst auch die Prüfung von Informationsinkonsistenzen, die in verschiedenen Informationsquellen auftreten. Die Marktdaten werden mithilfe von marktstatistischen und kohärenten Modellen analysiert und geschätzt. Darüber hinaus sind Marktanteilsanalyse und Schlüsseltrendanalyse die wichtigsten Erfolgsfaktoren im Marktbericht. Um mehr zu erfahren, fordern Sie bitte einen Analystenanruf an oder geben Sie Ihre Anfrage ein.
Die wichtigste Forschungsmethodik, die vom DBMR-Forschungsteam verwendet wird, ist die Datentriangulation, die Data Mining, die Analyse der Auswirkungen von Datenvariablen auf den Markt und die primäre (Branchenexperten-)Validierung umfasst. Zu den Datenmodellen gehören ein Lieferantenpositionierungsraster, eine Marktzeitlinienanalyse, ein Marktüberblick und -leitfaden, ein Firmenpositionierungsraster, eine Patentanalyse, eine Preisanalyse, eine Firmenmarktanteilsanalyse, Messstandards, eine globale versus eine regionale und Lieferantenanteilsanalyse. Um mehr über die Forschungsmethodik zu erfahren, senden Sie eine Anfrage an unsere Branchenexperten.
Anpassung möglich
Data Bridge Market Research ist ein führendes Unternehmen in der fortgeschrittenen formativen Forschung. Wir sind stolz darauf, unseren bestehenden und neuen Kunden Daten und Analysen zu bieten, die zu ihren Zielen passen. Der Bericht kann angepasst werden, um Preistrendanalysen von Zielmarken, Marktverständnis für zusätzliche Länder (fordern Sie die Länderliste an), Daten zu klinischen Studienergebnissen, Literaturübersicht, Analysen des Marktes für aufgearbeitete Produkte und Produktbasis einzuschließen. Marktanalysen von Zielkonkurrenten können von technologiebasierten Analysen bis hin zu Marktportfoliostrategien analysiert werden. Wir können so viele Wettbewerber hinzufügen, wie Sie Daten in dem von Ihnen gewünschten Format und Datenstil benötigen. Unser Analystenteam kann Ihnen auch Daten in groben Excel-Rohdateien und Pivot-Tabellen (Fact Book) bereitstellen oder Sie bei der Erstellung von Präsentationen aus den im Bericht verfügbaren Datensätzen unterstützen.