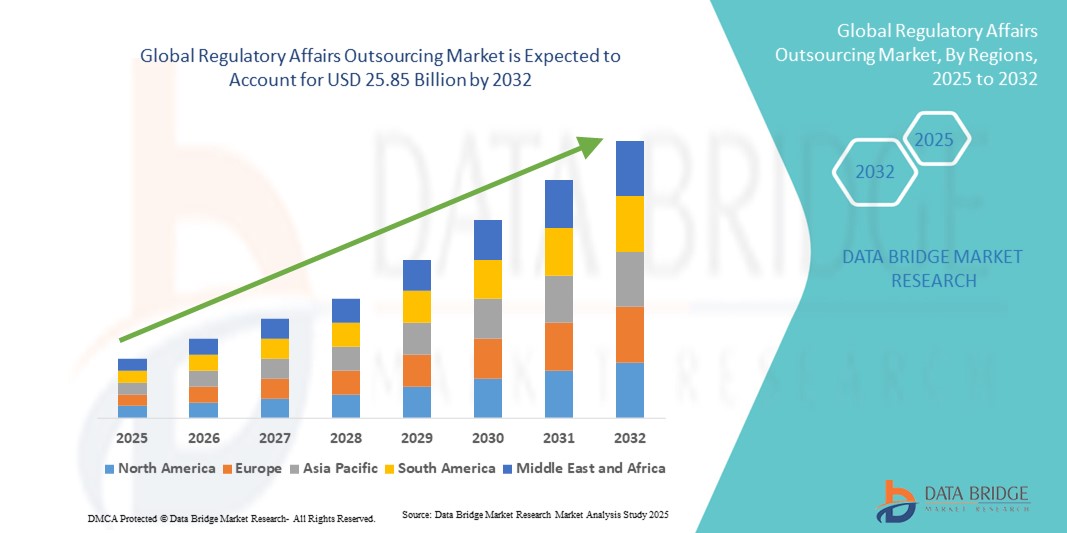
Global Regulatory Affairs Outsourcing Market
Marktgröße in Milliarden USD
CAGR :
% 
 USD
11.49 Billion
USD
25.85 Billion
2024
2032
USD
11.49 Billion
USD
25.85 Billion
2024
2032
| 2025 –2032 | |
| USD 11.49 Billion | |
| USD 25.85 Billion | |
|
|
|
|
Globale Marktsegmente für das Outsourcing von regulatorischen Angelegenheiten, nach Dienstleistungsausblick (Regulierungsberatung, Rechtsvertretung, Verfassen und Veröffentlichen von regulatorischen Unterlagen, Produktregistrierung, Anträge für klinische Studien und andere Dienstleistungen), Größe (klein, mittel und groß), Kategorie (Medikamente, Generika, Innovatoren, Biologika, Biotechnologie, ATMPs, Medizinprodukte, Therapeutika und Diagnostik), Indikation (Onkologie, Neurologie, Kardiologie, Immunologie und andere), Stadium (präklinisch, klinisch und PMA (nach der Marktzulassung), Endbenutzer (Medizinproduktehersteller, Pharmaunternehmen und Biotechnologieunternehmen) – Branchentrends und Prognose bis 2032
Marktgröße für das Outsourcing von regulatorischen Angelegenheiten
- Der globale Markt für das Outsourcing von regulatorischen Angelegenheiten wurde im Jahr 2024 auf 11,49 Milliarden US-Dollar geschätzt und soll bis 2032 25,85 Milliarden US-Dollar erreichen , bei einer CAGR von 10,66 % im Prognosezeitraum.
- Das Marktwachstum wird maßgeblich durch die zunehmende Komplexität der regulatorischen Anforderungen in der Pharma-, Biotechnologie- und Medizinproduktebranche vorangetrieben, was Unternehmen dazu veranlasst, spezialisierte Outsourcing-Dienste für das Compliance-Management zu suchen.
- Darüber hinaus treibt die steigende Nachfrage nach kostengünstigen, effizienten und zeitnahen Zulassungsanträgen die Nutzung von Regulatory Affairs Outsourcing-Lösungen voran. Diese konvergierenden Faktoren beschleunigen die Nutzung von Regulatory Affairs Outsourcing-Dienstleistungen und fördern damit das globale Branchenwachstum erheblich.
Marktanalyse für Regulatory Affairs Outsourcing
- Das Outsourcing von Regulatory Affairs, also die Ausgliederung von Compliance-, Einreichungs- und Dokumentationsaufgaben an spezialisierte Dienstleister, wird für Pharma-, Biotechnologie- und Medizinprodukteunternehmen zu einem wesentlichen Bestandteil, wenn sie komplexe globale Vorschriften effizient bewältigen möchten.
- Die steigende Nachfrage nach regulatorischer Expertise und die zunehmende Komplexität der Genehmigungsverfahren in verschiedenen Regionen fördern die Nutzung von Regulatory Affairs Outsourcing-Dienstleistungen. Unternehmen nutzen diese Dienstleistungen, um einen zeitnahen Marktzugang zu gewährleisten, Compliance-Risiken zu reduzieren und sich auf ihre Kernaktivitäten in Forschung und Entwicklung zu konzentrieren.
- Nordamerika dominierte den Markt für Regulatory Affairs Outsourcing mit dem größten Umsatzanteil von 40,5 % im Jahr 2024. Dies ist auf die Präsenz führender Pharma- und Biotech-Unternehmen, strenge FDA-Vorschriften und die hohe Anzahl klinischer Studien zurückzuführen, die spezialisierte regulatorische Unterstützung erfordern. Die USA sind aufgrund ihrer gut ausgebauten Infrastruktur, umfangreicher regulatorischer Richtlinien und der hohen Nachfrage nach fachkundigen Outsourcing-Lösungen führend auf dem regionalen Markt.
- Der asiatisch-pazifische Raum dürfte im Prognosezeitraum die am schnellsten wachsende Region im Markt für Regulatory Affairs Outsourcing sein. Dies ist auf die wachsende Pharmaproduktion, steigende Investitionen im Gesundheitswesen und das wachsende Bewusstsein für die Einhaltung gesetzlicher Vorschriften in Ländern wie China, Indien und Japan zurückzuführen. Kostengünstige Outsourcing-Lösungen und zunehmende klinische Studien beschleunigen das Marktwachstum zusätzlich.
- Das Segment „Groß“ dominierte den Markt für Regulatory Affairs Outsourcing mit dem größten Umsatzanteil von 45 % im Jahr 2024, angetrieben durch die umfangreichen globalen Aktivitäten multinationaler Pharma-, Biotech- und Medizintechnikunternehmen. Große Unternehmen lagern häufig regulatorische Funktionen aus, um große Mengen an Produktregistrierungen zu verwalten, die Compliance in mehreren Regionen aufrechtzuerhalten und die betriebliche Effizienz zu optimieren.
Berichtsumfang und Marktsegmentierung für das Outsourcing regulatorischer Angelegenheiten
|
Eigenschaften |
Wichtige Markteinblicke zum Outsourcing von Regulierungsangelegenheiten |
|
Abgedeckte Segmente |
|
|
Abgedeckte Länder |
Nordamerika
Europa
Asien-Pazifik
Naher Osten und Afrika
Südamerika
|
|
Wichtige Marktteilnehmer |
|
|
Marktchancen |
|
|
Wertschöpfungsdaten-Infosets |
Zusätzlich zu den Einblicken in Marktszenarien wie Marktwert, Wachstumsrate, Segmentierung, geografische Abdeckung und wichtige Akteure enthalten die von Data Bridge Market Research kuratierten Marktberichte auch ausführliche Expertenanalysen, Preisanalysen, Markenanteilsanalysen, Verbraucherumfragen, demografische Analysen, Lieferkettenanalysen, Wertschöpfungskettenanalysen, eine Übersicht über Rohstoffe/Verbrauchsmaterialien, Kriterien für die Lieferantenauswahl, PESTLE-Analysen, Porter-Analysen und regulatorische Rahmenbedingungen. |
Markttrends im Bereich Regulatory Affairs Outsourcing
Wachsende Nachfrage nach spezialisierter regulatorischer Expertise
- Ein bedeutender und sich beschleunigender Trend im globalen Outsourcing-Markt für regulatorische Angelegenheiten ist die zunehmende Abhängigkeit von spezialisierten Dienstleistern für die Verwaltung komplexer regulatorischer Einreichungen, Compliance-Dokumente und Genehmigungsprozesse. Dieser Trend wird durch die Notwendigkeit eines zeitnahen Marktzugangs und der Einhaltung sich entwickelnder Vorschriften in verschiedenen Regionen vorangetrieben.
- Pharma-, Biotechnologie- und Medizintechnikunternehmen lagern zunehmend regulatorische Aufgaben aus, um Betriebsabläufe zu rationalisieren, Compliance-Risiken zu reduzieren und sich stärker auf die Kernaktivitäten in Forschung und Entwicklung zu konzentrieren.
- Wichtige Dienstleister auf dem Markt erweitern ihr Angebot um eine umfassende regulatorische Unterstützung, einschließlich Dossiervorbereitung, Einreichungsmanagement, Überwachung nach dem Inverkehrbringen und regulatorischer Informationen, um sicherzustellen, dass die Kunden die regionalen und globalen Anforderungen einhalten.
- Die zunehmende Komplexität der Vorschriften, gepaart mit strengen Richtlinien von Behörden wie der FDA, EMA und PMDA, treibt die Nachfrage nach Outsourcing-Lösungen voran, die Fachwissen zu globalen Regulierungsstrategien und schnelleren Einreichungsfristen bieten.
- Darüber hinaus treiben zunehmende klinische Studien und eine steigende Zahl von Produktzulassungen in Nordamerika, Europa und im asiatisch-pazifischen Raum das Marktwachstum voran, da Unternehmen nach kostengünstigen und zuverlässigen regulatorischen Unterstützungsdiensten suchen.
- Der Markt für Regulatory Affairs Outsourcing erlebt sowohl bei großen Pharmaunternehmen als auch bei kleinen und mittleren Unternehmen eine Expansion. Dies unterstreicht die breite Akzeptanz und die entscheidende Rolle ausgelagerter Expertise bei der Beschleunigung der Produktentwicklung und -vermarktung.
Marktdynamik im Bereich Regulatory Affairs Outsourcing
Treiber
Wachsender Bedarf aufgrund zunehmender regulatorischer Komplexität und globaler Expansion
- Die zunehmende Komplexität der regulatorischen Anforderungen in der Pharma-, Biotechnologie- und Medizinproduktebranche sowie die globale Expansion der Gesundheitsmärkte sind ein wesentlicher Treiber für die gestiegene Nachfrage nach Outsourcing von regulatorischen Angelegenheiten.
- So kündigte beispielsweise ein führendes CRO im April 2024 eine Erweiterung seiner regulatorischen Beratungsleistungen um KI-gestütztes Einreichungs-Tracking und Compliance-Monitoring für globale Märkte an. Solche Strategien wichtiger Unternehmen dürften das Wachstum der Regulatory Affairs Outsourcing-Branche im Prognosezeitraum vorantreiben.
- Da Pharma- und Biotech-Unternehmen mit strengeren Compliance-Standards und häufigen Aktualisierungen der regulatorischen Rahmenbedingungen konfrontiert sind, bietet Outsourcing Zugang zu spezialisiertem Fachwissen für die Produktregistrierung, klinische Studienanträge und die Zulassung nach dem Inverkehrbringen und stellt damit eine attraktive Alternative zum Inhouse-Management dar.
- Darüber hinaus macht der zunehmende Trend zu globalen Produkteinführungen und grenzüberschreitenden klinischen Studien das Outsourcing regulatorischer Angelegenheiten zu einem integralen Bestandteil der Betriebsstrategie. Dies ermöglicht es Unternehmen, sich effizient in unterschiedlichen regulatorischen Landschaften zurechtzufinden und rechtzeitige Genehmigungen sicherzustellen.
- Die bequeme Zusammenarbeit mit erfahrenen Regulierungsexperten, die Reduzierung des internen Compliance-Aufwands und der Zugriff auf aktuelle Leitlinien zu sich ändernden Vorschriften sind Schlüsselfaktoren für die Auslagerung regulatorischer Angelegenheiten sowohl bei großen Pharmaunternehmen als auch bei aufstrebenden Biotech-Unternehmen. Der Trend zu strategischen Partnerschaften und die zunehmende Verfügbarkeit flexibler Outsourcing-Optionen tragen zusätzlich zum Marktwachstum bei.
Einschränkung/Herausforderung
Bedenken hinsichtlich der Datensicherheit und hoher Servicekosten
- Bedenken hinsichtlich der Vertraulichkeit und Sicherheit sensibler klinischer und regulatorischer Daten stellen eine erhebliche Herausforderung für die breitere Nutzung des Outsourcings regulatorischer Angelegenheiten dar. Da das Outsourcing auf externe Dienstleister und digitale Plattformen angewiesen ist, besteht das potenzielle Risiko von Datenschutzverletzungen oder unbefugtem Zugriff. Dies weckt bei Unternehmen Bedenken hinsichtlich der Einhaltung von Vorschriften und des Schutzes geistigen Eigentums.
- Beispielsweise haben Berichte über Cybersicherheitslücken in Datenmanagementplattformen einige Unternehmen vorsichtiger gemacht, was das Outsourcing von Regulierungsfunktionen angeht.
- Die Berücksichtigung dieser Bedenken durch robuste Verschlüsselung, sichere Authentifizierungsprotokolle und die Einhaltung globaler Datenschutzstandards (z. B. DSGVO, HIPAA) ist entscheidend für den Aufbau des Kundenvertrauens. Unternehmen wie Parexel und Medpace betonen in ihren Serviceangeboten ihre fortschrittlichen Datensicherheitsmaßnahmen und Compliance-Frameworks, um potenzielle Kunden zu beruhigen.
- Darüber hinaus können die im Vergleich zu internen Teams relativ hohen Kosten umfassender regulatorischer Outsourcing-Dienste ein Hindernis für kleine und mittelgroße Unternehmen darstellen, insbesondere in Schwellenländern.
- Während die Servicegebühren allmählich wettbewerbsfähiger werden, kann der wahrgenommene Aufpreis für das Outsourcing spezialisierter regulatorischer Expertise immer noch die Akzeptanz behindern, insbesondere für Unternehmen mit begrenztem Budget oder solche, die ein kleines Produktportfolio verwalten.
- Die Bewältigung dieser Herausforderungen durch verbesserte Datensicherheitsprotokolle, die Aufklärung der Kunden über bewährte Compliance-Praktiken und die Entwicklung kostengünstiger Lösungen für das regulatorische Outsourcing wird für ein nachhaltiges Marktwachstum von entscheidender Bedeutung sein.
Marktumfang des Outsourcings von regulatorischen Angelegenheiten
Der Markt ist auf der Grundlage von Serviceaussichten, Größe, Kategorie, Indikation, Phase und Endbenutzer segmentiert.
- Von Services Outlook
Auf der Grundlage der Dienstleistungsaussichten ist der Markt in regulatorische Beratung, Rechtsvertretung, Verfassen und Veröffentlichen von regulatorischen Unterlagen, Produktregistrierung, Anträge auf klinische Studien und andere Dienstleistungen segmentiert. Das Segment regulatorische Beratung dominierte den Markt mit dem größten Umsatzanteil von 42,5 % im Jahr 2024. Diese Dominanz ist darauf zurückzuführen, dass Pharma- und Biotechnologieunternehmen zunehmend auf fachkundige Beratung angewiesen sind, um sich in den komplexen globalen regulatorischen Rahmenbedingungen zurechtzufinden. Die regulatorische Beratung bietet strategische Unterstützung bei der Dossiererstellung, der Einreichung von Zulassungsanträgen und dem Compliance-Management, was schnellere Genehmigungen und ein geringeres Ablehnungsrisiko gewährleistet. Die starke Präsenz des Segments wird durch die wachsende Zahl von Produktpipelines, die Einführung neuer Medikamente und steigende F&E-Investitionen verstärkt. Multinationale Unternehmen bevorzugen häufig Beratungsdienste, da diese in der Lage sind, regionsübergreifendes regulatorisches Wissen und maßgeschneiderte Lösungen bereitzustellen. Die Notwendigkeit, die Compliance in einem sich entwickelnden regulatorischen Umfeld aufrechtzuerhalten, hat die Position der regulatorischen Beratung als führender Dienstleister weiter gefestigt.
Das Segment der Anträge auf klinische Studien wird voraussichtlich von 2025 bis 2032 die höchste durchschnittliche jährliche Wachstumsrate (CAGR) von 22,1 % verzeichnen. Grund hierfür sind die zunehmende Komplexität der Einreichungen klinischer Studien und strengere Vorschriften. Durch das Outsourcing von Anträgen auf klinische Studien können Unternehmen Einreichungen effizient verwalten, globale Richtlinien einhalten und Zulassungen in mehreren Regionen verfolgen. Die steigende Zahl onkologischer, neurologischer und immunologischer Studien sowie die zunehmende Nutzung digitaler Einreichungsplattformen treiben die Nachfrage an. Unternehmen bevorzugen Outsourcing, um Risiken zu minimieren, die Effizienz zu steigern und Genauigkeit zu gewährleisten. Das Wachstum wird auch durch kleine und mittelständische Unternehmen unterstützt, die Fachwissen suchen, ohne große interne Regulierungsteams zu unterhalten, was das hohe Potenzial des Segments unterstreicht.
- Nach Größe
Der Markt wird nach Größe in kleine, mittlere und große Unternehmen unterteilt. Das Segment „groß“ dominierte den Markt mit dem größten Umsatzanteil von 45 % im Jahr 2024, angetrieben durch die umfangreichen globalen Aktivitäten multinationaler Pharma-, Biotech- und Medizintechnikunternehmen. Große Unternehmen lagern häufig regulatorische Funktionen aus, um große Mengen an Produktregistrierungen zu verwalten, die Compliance in mehreren Regionen aufrechtzuerhalten und die betriebliche Effizienz zu optimieren. Dank ihrer starken finanziellen und technischen Ressourcen können diese Unternehmen erstklassige Dienstleister beauftragen, die komplexe regulatorische Aufgaben bewältigen können. Große Unternehmen profitieren zudem von einem geringeren Risiko regulatorischer Verzögerungen und können sich auf ihre Kernkompetenzen in Forschung und Entwicklung sowie auf strategische Prioritäten konzentrieren. Die Nachfrage nach Regulatory Affairs Outsourcing in großen Unternehmen steigt aufgrund wachsender Produktpipelines, mehrerer Produkteinführungen und strenger globaler Vorschriften weiter an.
Das Kleinsegment wird voraussichtlich von 2025 bis 2032 mit 20,8 % die höchste durchschnittliche jährliche Wachstumsrate (CAGR) verzeichnen, da aufstrebende Biotech- und Pharma-Start-ups zunehmend auf Outsourcing setzen. Kleine Unternehmen verfügen oft nicht über große interne Regulierungsteams und bevorzugen externe Expertise für Produktregistrierung, Compliance und klinische Einreichungen. Das Wachstum in diesem Segment wird durch das zunehmende Bewusstsein für regulatorische Anforderungen, die steigende Zahl klinischer Studien und kostengünstige Outsourcing-Lösungen gefördert. Besonders stark ist der Trend in Regionen mit aufstrebenden Biotech-Zentren, in denen das interne regulatorische Wissen begrenzt ist. Outsourcing bietet kleinen Unternehmen Zugang zu erfahrenen Fachkräften und schnellere Zulassungen ohne hohe operative Investitionen.
- Nach Kategorie
Der Markt ist nach Kategorien in Arzneimittel, Generika, Innovatoren, Biologika, Biotechnologie, ATMPs, Medizinprodukte, Therapeutika und Diagnostika unterteilt. Das Arzneimittelsegment dominierte den Markt mit dem größten Umsatzanteil von 41,7 % im Jahr 2024, was auf die hohe Anzahl neuer chemischer Substanzen und die Notwendigkeit umfangreicher Zulassungsanträge zurückzuführen ist. Regulatorisches Outsourcing in diesem Segment ermöglicht es Unternehmen, die Einhaltung der FDA-, EMA- und PMDA-Richtlinien sicherzustellen und gleichzeitig die Markteinführungszeit zu verkürzen. Unternehmen profitieren von einem fachkundigen Dokumentationsmanagement, globalen Einreichungsstrategien und einer Zulassungsverfolgung. Die Dominanz wird durch hohe F&E-Investitionen, große Produktpipelines und die weltweit steigende Zahl von Zulassungen verstärkt. Outsourcing trägt dazu bei, das Risiko von Einreichungsfehlern und regulatorischen Verzögerungen zu minimieren, was dieses Segment zu einem wichtigen Wachstumstreiber macht.
Das Segment ATMPs (Arzneimittel für neuartige Therapien) wird voraussichtlich von 2025 bis 2032 die höchste durchschnittliche jährliche Wachstumsrate (CAGR) von 23,4 % verzeichnen, angetrieben durch Innovationen in den Bereichen Gen- und Zelltherapien. Regulatorische Outsourcing-Dienstleistungen bieten spezialisiertes Fachwissen für komplexe Dokumentation, klinische Studienanträge und die Einhaltung der Vorschriften nach der Markteinführung. Steigende Investitionen in Forschung und Entwicklung, zunehmende Zulassungen und die regulatorische Komplexität neuartiger Therapien machen externe Unterstützung unabdingbar. Unternehmen nutzen Outsourcing, um die Vorschriften mehrerer Regionen effizient zu bewältigen und so schnellere Produkteinführungen und eine verbesserte Compliance zu gewährleisten. Die Einführung von ATMPs in der Onkologie, Immunologie und bei seltenen Krankheiten beschleunigt das Wachstum in diesem Segment zusätzlich.
- Nach Indikation
Auf Basis der Indikation ist der Markt in Onkologie, Neurologie, Kardiologie, Immunologie und andere segmentiert. Das Segment Onkologie dominierte mit dem größten Umsatzanteil von 44,2 % im Jahr 2024 aufgrund hoher globaler F&E-Investitionen in Krebstherapien und der steigenden Zahl von Zulassungen onkologischer Medikamente. Regulatorisches Outsourcing in der Onkologie hilft Unternehmen, Einreichungsvolumen, komplexe Dokumentation und die Einhaltung länderübergreifender Vorschriften effizient zu bewältigen. Die zunehmende Verbreitung von Krebs und Innovationen bei zielgerichteten Therapien haben die Nachfrage nach Outsourcing angekurbelt. Das Segment profitiert von starker staatlicher Unterstützung, beschleunigten Zulassungsverfahren und groß angelegten klinischen Studien und gilt damit als die lukrativste Indikation. Outsourcing ermöglicht schnellere Zulassungen und reduzierte Risiken in einem stark regulierten und wettbewerbsintensiven Onkologiemarkt.
Das Segment Immunologie wird voraussichtlich von 2025 bis 2032 die höchste durchschnittliche jährliche Wachstumsrate (CAGR) von 21,6 % verzeichnen, angetrieben durch die Entwicklung neuartiger Immuntherapien, Impfstoffe und Biologika. Regulatorisches Outsourcing bietet Expertise bei der Einreichung von Studien, der Dokumentation und der Einhaltung regulatorischer Vorschriften für neue Therapien. Steigendes Bewusstsein, steigende Investitionen in Forschung und Entwicklung im Bereich Immunologie und die Einführung innovativer Biologika treiben das Wachstum voran. Unternehmen nutzen Outsourcing, um interne Ressourcenengpässe zu überwinden und gleichzeitig regulatorische Effizienz zu gewährleisten. Das schnelle Wachstum des Segments wird zudem durch expandierende globale Märkte und die steigende Nachfrage nach fortschrittlichen immunologischen Behandlungen unterstützt.
- Nach Phase
Der Markt wird nach Phasen in präklinische, klinische und PMA-Phasen (Post Market Authorization) unterteilt. Das klinische Segment dominierte mit dem größten Umsatzanteil von 43 % im Jahr 2024, getrieben durch die hohe Anzahl globaler klinischer Studien und die strengen regulatorischen Compliance-Anforderungen. Durch das Outsourcing klinischer Phasenaktivitäten können Unternehmen Studienprotokolle, Einreichungen und Genehmigungen regionsübergreifend effizient verwalten. Die hohe Nachfrage nach onkologischen, neurologischen und kardiologischen Studien treibt das Wachstum zusätzlich an. Unternehmen profitieren von schnelleren behördlichen Prüfungen, präziser Dokumentation und Zugang zu erfahrenen Fachkräften, was den operativen Aufwand reduziert. Die Komplexität und der Umfang der regulatorischen Arbeit in der klinischen Phase machen dieses Segment weiterhin zu einem dominanten Treiber des Marktes.
Das Segment PMA (Post Market Authorization) wird voraussichtlich von 2025 bis 2032 die höchste durchschnittliche jährliche Wachstumsrate (CAGR) von 20,9 % verzeichnen. Dies ist auf steigende Anforderungen an die Überwachung nach der Markteinführung, die Meldung unerwünschter Ereignisse und die fortlaufenden Compliance-Verpflichtungen für Arzneimittel und Medizinprodukte zurückzuführen. Durch das Outsourcing von PMA-bezogenen Aktivitäten können Unternehmen die Sicherheitsüberwachung sicherstellen, die Dokumentation aktualisieren und sich entwickelnde Vorschriften effizient einhalten. Das Wachstum wird durch die steigenden Zulassungen für Biologika, Medizinprodukte und neuartige Therapien zusätzlich unterstützt, sodass PMA-Outsourcing für eine nachhaltige Compliance von entscheidender Bedeutung ist.
- Nach Endbenutzer
Auf Basis der Endnutzer ist der Markt in Medizintechnikunternehmen, Pharmaunternehmen und Biotechnologieunternehmen segmentiert. Das Segment der Pharmaunternehmen dominierte mit dem größten Marktanteil von 46 % im Jahr 2024, unterstützt durch eine hohe Anzahl an Arzneimittelzulassungen, umfangreiche klinische Studien und globale regulatorische Anforderungen. Outsourcing ermöglicht es Pharmaunternehmen, sich auf ihre Kernforschung und -entwicklung zu konzentrieren und gleichzeitig die Einhaltung internationaler Vorschriften zu gewährleisten. Unternehmen profitieren von Risikominimierung, reduzierten Betriebskosten und schnelleren Produkteinführungen. Diese Dominanz wird durch groß angelegte globale Aktivitäten und Multi-Produkt-Pipelines verstärkt, was Pharmaunternehmen zu den größten Nutzern von regulatorischen Outsourcing-Dienstleistungen macht.
Das Segment der Biotechnologieunternehmen wird voraussichtlich von 2025 bis 2032 die höchste durchschnittliche jährliche Wachstumsrate (CAGR) von 22,7 % verzeichnen, angetrieben durch schnelle Innovationen in den Bereichen Gentherapie, Biologika und anderen biotechnologischen Produkten. Das Outsourcing regulatorischer Funktionen hilft Biotech-Unternehmen, interne Kapazitätsengpässe zu überwinden und Zulassungsanträge in mehreren Ländern effizient zu bearbeiten. Steigende Investitionen in die biotechnologische Forschung und Entwicklung, neu entstehende Biotech-Zentren und ein zunehmendes Bewusstsein für regulatorische Best Practices treiben das Wachstum zusätzlich voran. Biotech-Unternehmen sind auf spezialisierte Dienstleister angewiesen, um Zulassungen zu beschleunigen und die Einhaltung der Vorschriften in einem stark regulierten und dynamischen Umfeld sicherzustellen.
Regionale Analyse des Outsourcing-Marktes für regulatorische Angelegenheiten
- Nordamerika dominierte den Markt für das Outsourcing von regulatorischen Angelegenheiten mit dem größten Umsatzanteil von 40,5 % im Jahr 2024, angetrieben durch die steigende Nachfrage nach spezialisierten regulatorischen Dienstleistungen in den Bereichen Pharma, Biotechnologie und Medizinprodukte.
- Die ausgereifte Gesundheitsinfrastruktur der Region, die Präsenz großer globaler Auftragsforschungsinstitute und die frühzeitige Einführung innovativer Regulierungsstrategien tragen zur Marktführerschaft bei
- Unternehmen in Nordamerika lagern zunehmend Dienstleistungen wie regulatorische Beratung, Produktregistrierung und klinische Studienanträge aus, um die Einhaltung der strengen Vorschriften der FDA und Health Canada sicherzustellen. Ein hohes Bewusstsein für regulatorische Komplexitäten, kombiniert mit fundierter rechtlicher und technischer Unterstützung, stärkt die Akzeptanz sowohl in kleinen als auch in großen Unternehmen.
Einblicke in den US-Markt für das Outsourcing von Regulierungsfragen
Der US-Markt für das Outsourcing von regulatorischen Angelegenheiten erzielte 2024 mit 81 % den größten Umsatzanteil innerhalb Nordamerikas. Dies ist auf die wachsende Zahl von Zulassungen für Pharmazeutika, Biotechnologie und Medizinprodukte zurückzuführen, die spezialisierte regulatorische Unterstützung erfordern. Der Markt profitiert von fortschrittlichen regulatorischen Rahmenbedingungen, einer starken Präsenz von CROs und einer hohen Nachfrage nach Dienstleistungen wie der Erstellung von Zulassungsunterlagen, der Rechtsvertretung und dem Post-Market-Authorization-Management. Große, mittlere und kleine Unternehmen aus den Bereichen Onkologie, Neurologie, Kardiologie, Immunologie und anderen Therapiebereichen setzen zunehmend auf Outsourcing, um präklinische, klinische und Post-Market-Regulierungsphasen effizient zu bewältigen.
Einblicke in den europäischen Markt für Regulatory Affairs Outsourcing
Der europäische Markt für das Outsourcing von regulatorischen Angelegenheiten wird im Prognosezeitraum voraussichtlich mit einer deutlichen jährlichen Wachstumsrate wachsen. Dies ist vor allem auf die komplexen regulatorischen Rahmenbedingungen in der EU und den zunehmenden Fokus auf die Compliance bei innovativen Therapien wie Biologika, ATMPs und Medizinprodukten zurückzuführen. Unternehmen in Deutschland, Frankreich und anderen EU-Ländern lagern regulatorische Dienstleistungen wie Anträge für klinische Studien, Produktregistrierung und regulatorische Beratung aus, um Kosten zu kontrollieren und rechtzeitige Zulassungen sicherzustellen. Die zunehmende Urbanisierung, die zunehmende F&E-Aktivität und die Präsenz spezialisierter Anbieter von regulatorischen Dienstleistungen fördern das Marktwachstum bei kleinen, mittleren und großen Unternehmen.
Einblicke in den britischen Outsourcing-Markt für regulatorische Angelegenheiten
Der britische Markt für Regulatory Affairs Outsourcing wird im Prognosezeitraum voraussichtlich mit einer bemerkenswerten jährlichen Wachstumsrate wachsen, angetrieben durch die steigende Nachfrage nach Dienstleistungen zur Einhaltung regulatorischer Vorschriften von Pharma- und Biotechnologieunternehmen. Outsourcing-Dienstleistungen wie das Verfassen und Veröffentlichen von Regulierungen, das Management von Anträgen auf klinische Studien und die Produktregistrierung helfen Unternehmen, die MHRA-Vorschriften effizient zu erfüllen. Das robuste Gesundheitsökosystem, gepaart mit etablierten CROs und umfassender Expertise in der regulatorischen Beratung, unterstützt das Wachstum in verschiedenen Therapiebereichen, darunter Onkologie, Kardiologie und Immunologie.
Markteinblicke im Bereich Regulatory Affairs Outsourcing in Deutschland
Der deutsche Markt für Regulatory Affairs Outsourcing wird im Prognosezeitraum voraussichtlich mit einer deutlichen jährlichen Wachstumsrate wachsen. Dies ist auf das wachsende Bewusstsein für die Einhaltung regulatorischer Vorschriften, strenge europäische Vorschriften und die Notwendigkeit eines kosteneffizienten Managements präklinischer, klinischer und post-market-Zulassungsprozesse zurückzuführen. Deutsche Pharma-, Biotech- und Medizintechnikunternehmen greifen zunehmend auf Outsourcing-Dienstleistungen wie Rechtsvertretung, regulatorische Beratung und Produktregistrierung zurück. Die Präsenz spezialisierter CROs und strenger Industriestandards fördert die Akzeptanz bei kleinen, mittleren und großen Unternehmen und deckt dabei unterschiedliche Indikationen und Therapiebereiche ab.
Markteinblicke zum Outsourcing regulatorischer Angelegenheiten im asiatisch-pazifischen Raum
Der Markt für das Outsourcing regulatorischer Angelegenheiten im asiatisch-pazifischen Raum wird im Prognosezeitraum 2025 bis 2032 voraussichtlich die höchste jährliche Wachstumsrate aufweisen. Dies ist auf die rasante Expansion der Pharma-, Biotechnologie- und Medizinprodukteindustrie in Ländern wie China, Indien und Japan zurückzuführen. Die wachsende Gesundheitsinfrastruktur, staatliche Initiativen zur Unterstützung klinischer Studien und steigende F&E-Aktivitäten fördern die Nutzung von Outsourcing-Dienstleistungen für regulatorische Beratung, Anträge für klinische Studien und das Post-Market-Authorization-Management. Kleine, mittlere und große Unternehmen nutzen diese Dienstleistungen zunehmend, um die Einhaltung lokaler und internationaler regulatorischer Anforderungen in verschiedenen Therapiebereichen sicherzustellen.
Einblicke in den japanischen Outsourcing-Markt für regulatorische Angelegenheiten
Der japanische Markt für Regulatory Affairs Outsourcing gewinnt aufgrund der fortschrittlichen Gesundheits- und Biotechnologiebranche, strenger regulatorischer Anforderungen und wachsender Forschungs- und Entwicklungsaktivitäten des Landes an Dynamik. Unternehmen lagern Dienstleistungen wie Produktregistrierung, regulatorisches Schreiben und klinisches Studienmanagement aus, um die PMDA-Vorschriften effektiv zu erfüllen. Das Marktwachstum wird durch die Nachfrage in verschiedenen Indikationen wie Onkologie, Kardiologie und Neurologie unterstützt und wird von kleinen, mittleren und großen Pharma-, Biotech- und Medizintechnikunternehmen genutzt.
Einblicke in den chinesischen Outsourcing-Markt für regulatorische Angelegenheiten
Der chinesische Markt für das Outsourcing von regulatorischen Angelegenheiten hatte 2024 den größten Marktanteil im asiatisch-pazifischen Raum, was auf die expandierende Pharma- und Biotechnologiebranche des Landes, die rasante Urbanisierung und steigende F&E-Ausgaben zurückzuführen ist. Outsourcing-Dienstleistungen wie regulatorische Beratung, Anträge für klinische Studien, Produktregistrierung und Post-Market-Authorization-Management sind stark nachgefragt und ermöglichen Unternehmen die effiziente Einhaltung der NMPA-Vorschriften. Kleine, mittlere und große Unternehmen aus den Bereichen Arzneimittel, Biologika, Medizinprodukte und ATMPs nutzen zunehmend regulatorisches Outsourcing, um Produktzulassungen und Markteinführungen zu beschleunigen.
Marktanteile im Bereich Regulatory Affairs Outsourcing
Die Outsourcing-Branche für regulatorische Angelegenheiten wird hauptsächlich von etablierten Unternehmen geführt, darunter:
- Accell Clinical Research, LLC (USA)
- Genpact (USA)
- CRITERIUM, INC. (USA)
- Promedica International (USA)
- WuXiAppTec (China)
- Medpace (USA)
- PPD Inc. (USA)
- Charles River Laboratories (USA)
- ICON plc (USA)
- Parexel International (MA) Corporation (USA)
- Freyr (USA)
- Navitas Clinical Research, Inc. (USA)
- Medelis, Inc. (USA)
- Sciformix (USA)
- Tech Tammina (USA)
- Acorn Regulatory Consultancy Services Ltd. (Irland)
- BIOMAPAS (Litauen)
- REGULATORY PROFESSIONALS (Australien)
- CompareNetworks, Inc. (USA)
Neueste Entwicklungen im globalen Outsourcing-Markt für regulatorische Angelegenheiten
- Im Juli 2025 gab die britische Arzneimittel- und Gesundheitsprodukte-Zulassungsbehörde MHRA bekannt, dass sie rund 40 % ihrer Zulassungsanträge für Arzneimittel und Medizinprodukte an vertrauenswürdige ausländische Zulassungsbehörden auslagert. Ziel dieser Maßnahme war es, Ressourcen zu sparen und sich auf innovative Bereiche wie künstliche Intelligenz im Gesundheitswesen und fortschrittliche Therapien zu konzentrieren. Das im April 2024 eingeführte „internationale Anerkennungsverfahren“ der MHRA ermöglichte schnellere Zulassungen auf Grundlage von Entscheidungen von Regulierungsbehörden in der EU, den USA oder Australien.
- Im Februar 2021 erwarb ICON plc PRA Health Sciences, Inc. in einer Bar- und Aktientransaktion im Wert von rund 12 Milliarden US-Dollar. Diese Übernahme stärkte das Angebot des Unternehmens im Bereich der medizinischen Dienstleistungen.
- Im August 2021 übernahm die ProPharma Group das in Indien ansässige Unternehmen iSafety Systems. Diese Übernahme soll die Position der ProPharma Group als führender globaler Anbieter von Beratung zu regulatorischen und Compliance-Anforderungen, Pharmakovigilanz, klinischen Forschungsdienstleistungen und medizinischen Informationen stärken.
SKU-
Erhalten Sie Online-Zugriff auf den Bericht zur weltweit ersten Market Intelligence Cloud
- Interaktives Datenanalyse-Dashboard
- Unternehmensanalyse-Dashboard für Chancen mit hohem Wachstumspotenzial
- Zugriff für Research-Analysten für Anpassungen und Abfragen
- Konkurrenzanalyse mit interaktivem Dashboard
- Aktuelle Nachrichten, Updates und Trendanalyse
- Nutzen Sie die Leistungsfähigkeit der Benchmark-Analyse für eine umfassende Konkurrenzverfolgung
Forschungsmethodik
Die Datenerfassung und Basisjahresanalyse werden mithilfe von Datenerfassungsmodulen mit großen Stichprobengrößen durchgeführt. Die Phase umfasst das Erhalten von Marktinformationen oder verwandten Daten aus verschiedenen Quellen und Strategien. Sie umfasst die Prüfung und Planung aller aus der Vergangenheit im Voraus erfassten Daten. Sie umfasst auch die Prüfung von Informationsinkonsistenzen, die in verschiedenen Informationsquellen auftreten. Die Marktdaten werden mithilfe von marktstatistischen und kohärenten Modellen analysiert und geschätzt. Darüber hinaus sind Marktanteilsanalyse und Schlüsseltrendanalyse die wichtigsten Erfolgsfaktoren im Marktbericht. Um mehr zu erfahren, fordern Sie bitte einen Analystenanruf an oder geben Sie Ihre Anfrage ein.
Die wichtigste Forschungsmethodik, die vom DBMR-Forschungsteam verwendet wird, ist die Datentriangulation, die Data Mining, die Analyse der Auswirkungen von Datenvariablen auf den Markt und die primäre (Branchenexperten-)Validierung umfasst. Zu den Datenmodellen gehören ein Lieferantenpositionierungsraster, eine Marktzeitlinienanalyse, ein Marktüberblick und -leitfaden, ein Firmenpositionierungsraster, eine Patentanalyse, eine Preisanalyse, eine Firmenmarktanteilsanalyse, Messstandards, eine globale versus eine regionale und Lieferantenanteilsanalyse. Um mehr über die Forschungsmethodik zu erfahren, senden Sie eine Anfrage an unsere Branchenexperten.
Anpassung möglich
Data Bridge Market Research ist ein führendes Unternehmen in der fortgeschrittenen formativen Forschung. Wir sind stolz darauf, unseren bestehenden und neuen Kunden Daten und Analysen zu bieten, die zu ihren Zielen passen. Der Bericht kann angepasst werden, um Preistrendanalysen von Zielmarken, Marktverständnis für zusätzliche Länder (fordern Sie die Länderliste an), Daten zu klinischen Studienergebnissen, Literaturübersicht, Analysen des Marktes für aufgearbeitete Produkte und Produktbasis einzuschließen. Marktanalysen von Zielkonkurrenten können von technologiebasierten Analysen bis hin zu Marktportfoliostrategien analysiert werden. Wir können so viele Wettbewerber hinzufügen, wie Sie Daten in dem von Ihnen gewünschten Format und Datenstil benötigen. Unser Analystenteam kann Ihnen auch Daten in groben Excel-Rohdateien und Pivot-Tabellen (Fact Book) bereitstellen oder Sie bei der Erstellung von Präsentationen aus den im Bericht verfügbaren Datensätzen unterstützen.