Global Electronic Trial Master File Etmf Systems Market
Taille du marché en milliards USD
TCAC :
% 
 USD
1.84 Billion
USD
4.85 Billion
2024
2032
USD
1.84 Billion
USD
4.85 Billion
2024
2032
| 2025 –2032 | |
| USD 1.84 Billion | |
| USD 4.85 Billion | |
|
|
|
|
Segmentation du marché mondial des systèmes de dossiers maîtres d'essais cliniques électroniques (eTMF), par composant (services et logiciels), mode de déploiement (eTMF dans le cloud et eTMF sur site), utilisateur final (entreprises pharmaceutiques et biotechnologiques, CRO et autres) - Tendances du secteur et prévisions jusqu'en 2032
Taille du marché des systèmes de dossiers maîtres électroniques d'essais (eTMF)
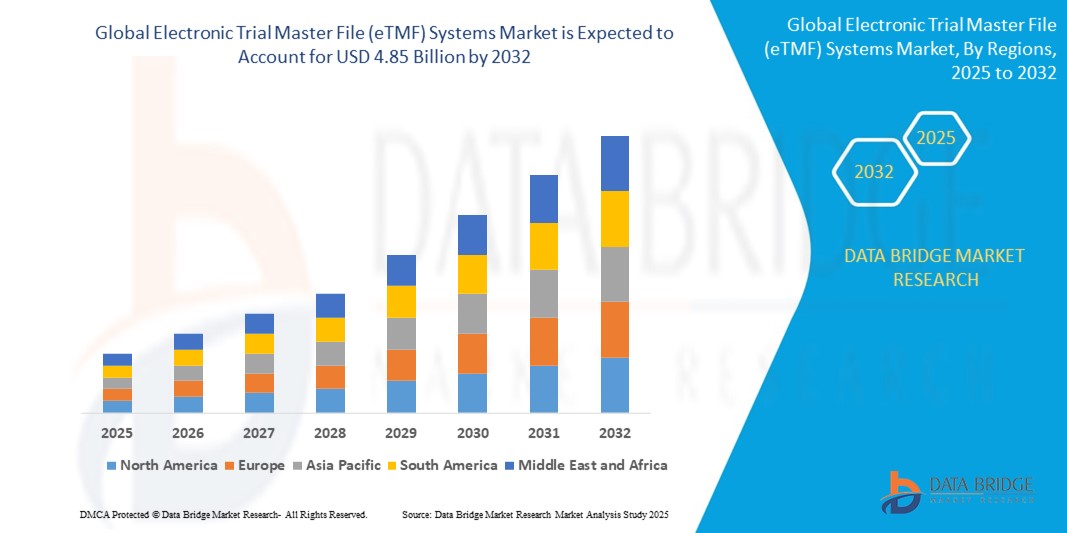
- Le marché mondial des systèmes de dossiers électroniques maîtres de procès (eTMF) était évalué à 1,84 milliard de dollars américains en 2024 et devrait atteindre 4,85 milliards de dollars américains d'ici 2032 , avec un TCAC de 12,90 % au cours de la période de prévision.
- La croissance du marché est largement alimentée par la demande croissante de gestion centralisée des données d'essais cliniques, de conformité réglementaire et d'adoption croissante des plateformes numériques dans la recherche clinique au sein des secteurs pharmaceutique et biotechnologique.
- L'augmentation du nombre d'essais cliniques à l'échelle mondiale, notamment sur les marchés émergents, et la nécessité d'un accès en temps réel aux documents d'essai accélèrent encore l'adoption des systèmes de dossiers maîtres d'essais électroniques (eTMF) par les promoteurs et les organismes de recherche sous contrat.
Analyse du marché des systèmes de dossiers maîtres électroniques d'essais (eTMF)
- Le marché des systèmes de gestion électronique des dossiers de référence des essais cliniques connaît une croissance soutenue, les entreprises pharmaceutiques et biotechnologiques adoptant de plus en plus les solutions numériques pour la gestion des documents cliniques.
- L'augmentation des activités d'essais cliniques et la nécessité de processus de conformité réglementaire efficaces incitent les organisations à passer des systèmes papier aux plateformes cloud.
- L'Amérique du Nord a dominé le marché des systèmes de dossiers maîtres électroniques d'essais cliniques (eTMF) en 2024, avec la plus grande part de revenus (49,5 %). Cette domination s'explique par une forte concentration d'entreprises pharmaceutiques et biotechnologiques, des investissements importants en R&D, une infrastructure informatique de santé bien développée et un nombre croissant d'essais cliniques complexes nécessitant une documentation et une conformité efficaces.
- La région Asie-Pacifique devrait connaître le taux de croissance le plus élevé du marché mondial des systèmes de dossiers électroniques de procès (eTMF), sous l'effet de l'urbanisation croissante, de la hausse des revenus disponibles, des progrès technologiques dans des pays comme la Chine, le Japon et l'Inde, et d'un intérêt grandissant pour les maisons intelligentes, soutenu par les initiatives de numérisation des gouvernements.
- Le segment des services a détenu la plus grande part de revenus de marché en 2024, grâce à des offres essentielles tout au long du cycle de vie du système, notamment la mise en œuvre, la formation, le support technique et la migration des données.
Portée du rapport et segmentation du marché des systèmes de dossiers maîtres d'essais électroniques (eTMF)
|
Attributs |
Systèmes de dossiers maîtres d'essais électroniques (eTMF) : principaux enseignements du marché |
|
Segments couverts |
|
|
Pays couverts |
Amérique du Nord
Europe
Asie-Pacifique
Moyen-Orient et Afrique
Amérique du Sud
|
|
Acteurs clés du marché |
|
|
Opportunités de marché |
|
|
Ensembles d'informations de données à valeur ajoutée |
En plus des informations sur les scénarios de marché tels que la valeur du marché, le taux de croissance, la segmentation, la couverture géographique et les principaux acteurs, les rapports de marché élaborés par Data Bridge Market Research comprennent également une analyse approfondie d'experts, la production et la capacité par entreprise représentées géographiquement, les schémas de réseau des distributeurs et des partenaires, une analyse détaillée et mise à jour des tendances des prix et une analyse des déficits de la chaîne d'approvisionnement et de la demande. |
Tendances du marché des systèmes de dossiers maîtres d'essais électroniques (eTMF)
« L’intégration de l’intelligence artificielle pour l’automatisation des flux de travail »
- L'intelligence artificielle est de plus en plus intégrée aux systèmes de gestion électronique des dossiers de procès afin d'automatiser les tâches répétitives telles que la classification des documents et l'étiquetage des métadonnées.
- Cette tendance améliore l'efficacité et réduit les erreurs manuelles, permettant aux professionnels de la recherche clinique de se concentrer davantage sur les tâches stratégiques et de conformité.
- Par exemple, les plateformes basées sur l'IA peuvent indexer automatiquement les documents d'essais cliniques et signaler les fichiers manquants, garantissant ainsi une plus grande précision et une meilleure conformité réglementaire.
- Des entreprises comme Veeva Systems et Phlexglobal adoptent des capacités d'IA pour rationaliser les processus eTMF et fournir des informations en temps réel sur l'état des essais cliniques.
- Face à l'augmentation des volumes de données cliniques, l'intégration de l'IA devient essentielle pour améliorer la prise de décision et accélérer le cycle de vie des essais cliniques.
Dynamique du marché des systèmes de dossiers maîtres électroniques d'essais (eTMF)
Conducteur
« Évolution vers la numérisation dans la gestion des essais cliniques »
- La transition vers la numérisation favorise l'adoption de systèmes de fichiers maîtres électroniques pour les essais cliniques, à mesure que ces derniers deviennent plus complexes et nécessitent une gestion documentaire plus efficace.
- Ces systèmes offrent un accès centralisé aux documents de procès, permettant une récupération plus rapide, une collaboration en temps réel et un meilleur contrôle des versions entre les équipes.
- Par exemple, de grandes entreprises pharmaceutiques comme Pfizer ont adopté des plateformes numériques de gestion des essais cliniques afin de rationaliser la documentation et de garantir la conformité réglementaire.
- Les systèmes numériques contribuent à réduire les risques liés aux erreurs manuelles, aux pertes de documents et aux retards de soumission, améliorant ainsi la qualité et les délais des procès.
- L'accès à distance et les fonctionnalités de stockage cloud sécurisé rendent ces systèmes essentiels pour les organisations qui cherchent à améliorer leur efficacité opérationnelle et à se conformer aux normes réglementaires internationales.
Retenue/Défi
« Problèmes de sécurité et de conformité des données »
- Les préoccupations liées à la sécurité des données et à la conformité réglementaire demeurent des freins majeurs à l'adoption des systèmes de fichiers maîtres électroniques pour les essais cliniques dans l'ensemble du secteur de la recherche clinique.
- Les données des essais cliniques sont extrêmement sensibles et toute violation peut entraîner de graves conséquences telles que des retards d'essais, des répercussions juridiques et une atteinte à la crédibilité de l'organisation.
- Par exemple, une fuite de données signalée au sein d'un organisme européen de recherche clinique a entraîné des enquêtes réglementaires et des retards dans le calendrier des essais, soulignant les risques encourus.
- Le respect des réglementations internationales en constante évolution, telles que le Règlement général sur la protection des données (RGPD) et la loi HIPAA (Health Insurance Portability and Accountability Act), exige des mises à jour constantes et des protocoles spécifiques à chaque région.
- Les petites et moyennes entreprises sont souvent confrontées à des difficultés pour financer l'infrastructure et l'expertise nécessaires en cybersécurité, ce qui limite leur capacité à migrer pleinement vers des plateformes eTMF basées sur le cloud.
Étendue du marché des systèmes de dossiers maîtres d'essais électroniques (eTMF)
Le marché est segmenté en fonction du composant, du mode de livraison et de l'utilisateur final.
- Par composant
Le marché des systèmes eTMF est segmenté, selon les composants, en services et logiciels. Le segment des services a représenté la plus grande part de revenus en 2024, grâce à des offres essentielles couvrant l'ensemble du cycle de vie du système, notamment la mise en œuvre, la formation, le support technique et la migration des données.
Le segment des logiciels devrait connaître le taux de croissance le plus rapide entre 2025 et 2032, les organisations adoptant de plus en plus des plateformes eTMF dédiées à la gestion centralisée des documents et à la conformité réglementaire.
- Par mode de livraison
Selon le mode de déploiement, le marché des systèmes eTMF se divise en eTMF cloud et eTMF sur site. Le segment eTMF cloud détenait la plus grande part de revenus en 2024, grâce à une accessibilité, une flexibilité, une rentabilité et une évolutivité accrues.
Le segment eTMF sur site devrait connaître le taux de croissance le plus rapide entre 2025 et 2032 et reste pertinent pour les organisations qui privilégient un contrôle total sur la sécurité des données et l'infrastructure, souvent en raison de politiques réglementaires ou informatiques internes spécifiques.
- Par l'utilisateur final
Selon l'utilisateur final, le marché des systèmes eTMF se divise en trois segments : les entreprises pharmaceutiques et biotechnologiques, les CRO et autres. Le segment des entreprises pharmaceutiques et biotechnologiques détenait la plus grande part de revenus en 2024, sous l'effet de la complexité croissante des essais cliniques, de la mondialisation et du durcissement des exigences réglementaires.
Les organismes de recherche sous contrat (CRO) devraient connaître le taux de croissance le plus rapide entre 2025 et 2032, car ils utilisent de plus en plus les systèmes eTMF pour gérer efficacement divers essais pour différents commanditaires.
Analyse régionale du marché des systèmes de dossiers maîtres électroniques d'essais cliniques (eTMF)
- L'Amérique du Nord a dominé le marché des systèmes de dossiers maîtres électroniques d'essais cliniques (eTMF) en 2024, avec la plus grande part de revenus (49,5 %). Cette domination s'explique par une forte concentration d'entreprises pharmaceutiques et biotechnologiques, des investissements importants en R&D, une infrastructure informatique de santé bien développée et un nombre croissant d'essais cliniques complexes nécessitant une documentation et une conformité efficaces.
- Un environnement réglementaire rigoureux et l'accent mis sur l'intégrité des données incitent à développer des solutions eTMF robustes et conformes aux exigences de la FDA et des autres autorités sanitaires.
- L'adoption massive des technologies cloud avancées et des initiatives de transformation numérique au sein des organismes de recherche clinique accélère encore la mise en œuvre et l'utilisation du système eTMF.
Analyse du marché américain des systèmes de dossiers maîtres d'essais électroniques (eTMF)
En 2024, le marché américain des systèmes eTMF représentait 81 % des revenus en Amérique du Nord, porté par des exigences réglementaires strictes, la complexité et le volume croissants des données d'essais cliniques, ainsi qu'une forte priorité accordée à la préparation aux audits. L'adoption massive des solutions cloud et le soutien gouvernemental à la recherche et au développement dans le secteur de la santé contribuent également à l'expansion de ce marché.
Analyse du marché européen des systèmes de dossiers maîtres d'essais électroniques (eTMF)
Le marché européen devrait connaître la croissance la plus rapide entre 2025 et 2032, portée par la demande croissante de solutions cloud, la nécessité d'améliorer le partage des données et la collaboration entre les acteurs, ainsi que par l'évolution des réglementations. La région bénéficie également d'une forte orientation vers l'innovation et la transformation numérique dans le secteur des sciences de la vie.
Analyse du marché britannique des systèmes de dossiers maîtres d'essais électroniques (eTMF)
Le marché britannique des systèmes eTMF devrait connaître la croissance la plus rapide entre 2025 et 2032, portée par le nombre croissant d'essais cliniques, notamment grâce à l'importance accrue accordée aux essais décentralisés et virtuels. La vigueur du secteur pharmaceutique britannique et une approche proactive en matière de santé numérique contribuent également à cette croissance.
Analyse du marché allemand des systèmes de dossiers maîtres d'essais électroniques (eTMF)
Le marché allemand des systèmes eTMF devrait connaître la croissance la plus rapide entre 2025 et 2032, portée par une sensibilisation accrue à la sécurité numérique, des exigences réglementaires strictes et une demande de solutions technologiques de pointe au sein de son secteur pharmaceutique performant. L'accent mis par l'Allemagne sur l'innovation et sa solide base industrielle favorisent également l'adoption des systèmes eTMF.
Analyse du marché des systèmes de dossiers maîtres d'essais électroniques (eTMF) en Asie-Pacifique
Le marché des systèmes eTMF en Asie-Pacifique devrait connaître la croissance la plus rapide entre 2025 et 2032, sous l'effet de l'urbanisation croissante, de la hausse des revenus disponibles et des progrès technologiques significatifs réalisés dans des pays comme la Chine, le Japon et l'Inde. L'intérêt grandissant de la région pour les pratiques cliniques intelligentes, soutenu par les initiatives gouvernementales en faveur de la numérisation, favorise l'adoption des systèmes eTMF.
Analyse du marché japonais des systèmes de fichiers maîtres d'essais électroniques (eTMF)
Le marché japonais des systèmes eTMF devrait connaître la croissance la plus rapide entre 2025 et 2032, grâce à la culture de pointe du pays en matière de technologies, à son urbanisation rapide et à l'importance croissante accordée à l'intégrité des données et à la conformité réglementaire. La sécurité et l'efficacité sont des critères essentiels pour ce marché, dont l'adoption est stimulée par le nombre croissant d'essais cliniques et l'intégration de l'eTMF à d'autres solutions cliniques numériques.
Analyse du marché des systèmes de fichiers maîtres d'essais électroniques (eTMF) en Chine
En 2024, le marché chinois des systèmes eTMF représentait la plus grande part de revenus en Asie-Pacifique, grâce à l'essor de la classe moyenne, à l'urbanisation rapide et au fort taux d'adoption des technologies dans le secteur de la santé. La Chine constitue un pôle majeur de la recherche clinique, et la vigueur de ses fabricants nationaux ainsi que le soutien gouvernemental à la transformation numérique favorisent l'adoption des systèmes eTMF dans les milieux résidentiels, commerciaux et de recherche.
Part de marché des systèmes de dossiers maîtres électroniques d'essais (eTMF)
Le secteur des systèmes de dossiers électroniques de procès (eTMF) est principalement dominé par des entreprises bien établies, notamment :
- IQVIA Inc. (États-Unis)
- Développement de médicaments Labcorp (États-Unis)
- TransPerfect (États-Unis)
- Oracle (États-Unis)
- Phlexglobal (États-Unis)
- SureClinical Inc. (États-Unis)
- Aurea, Inc. (États-Unis)
- Veeva Systems (États-Unis)
- MasterControl Solutions, Inc. (États-Unis)
- Clinevo Technologies (Inde)
- Fondation Mayo pour l'éducation et la recherche médicales (MFMER) (États-Unis)
- Montrium Inc. (États-Unis)
- NCGD Inc. (États-Unis)
- PharmaVigilance (États-Unis)
Dernières évolutions du marché mondial des systèmes de dossiers maîtres de procès électroniques (eTMF)
- En février 2023, Vial a collaboré avec Egnyte pour intégrer la solution eTMF d'Egnyte à sa plateforme. L'objectif est de rationaliser le traitement des documents et des données, de garantir la conformité à la norme 21 CFR Part 11 et de renforcer la préparation aux audits pour les entreprises des sciences de la vie, améliorant ainsi l'efficacité et le respect des réglementations dans les essais cliniques.
- En septembre 2022, Montrium a lancé des services et des formations TMF animés par des experts. Cette initiative vise à renforcer les équipes opérationnelles cliniques et TMF tout au long du processus de développement clinique, en leur fournissant le soutien et les connaissances essentiels pour optimiser la gestion des essais et l'intégrité des données sur le marché.
- En juin 2022, Anju Software Inc. a lancé eTMF Master, un nouveau logiciel eTMF basé sur le cloud. Cette solution facilite la collaboration entre les promoteurs, les CRO et les centres d'essais cliniques pour une gestion efficace et sécurisée du contenu des essais cliniques, tout en respectant les normes réglementaires. Elle permet ainsi d'accélérer les flux de travail et d'améliorer la conformité globale dans la recherche clinique.
- En avril 2021, Phlexglobal a annoncé sa solution d'analyse de la qualité des TMF. Destinée aux entreprises pharmaceutiques, notamment aux leaders mondiaux, cette solution permet d'évaluer et de minimiser les risques réglementaires lors des fusions-acquisitions, améliorant ainsi considérablement la préparation aux inspections et garantissant la qualité des données sur l'ensemble du marché.
SKU-
Accédez en ligne au rapport sur le premier cloud mondial de veille économique
- Tableau de bord d'analyse de données interactif
- Tableau de bord d'analyse d'entreprise pour les opportunités à fort potentiel de croissance
- Accès d'analyste de recherche pour la personnalisation et les requêtes
- Analyse de la concurrence avec tableau de bord interactif
- Dernières actualités, mises à jour et analyse des tendances
- Exploitez la puissance de l'analyse comparative pour un suivi complet de la concurrence
Table des matières
1 INTRODUCTION
1.1 OBJECTIFS DE L'ÉTUDE
1.2 DÉFINITION DU MARCHÉ
1.3 APERÇU DU MARCHÉ MONDIAL DES SYSTÈMES DE FICHIERS MAÎTRES D'ESSAI ÉLECTRONIQUES (ETMF)
1.4 DEVISES ET TARIFICATION
1.5 LIMITATION
1,6 MARCHÉS COUVERTS
2. SEGMENTATION DU MARCHÉ
2.1 POINTS CLÉS À RETENIR
2.2 ACCÈS AU MARCHÉ MONDIAL DES SYSTÈMES DE FICHIERS MAÎTRES D'ESSAI ÉLECTRONIQUES (ETMF)
2.2.1 GRILLE DE POSITIONNEMENT DES FOURNISSEURS
2.2.2 COURBE DE LA LIGNE DE VIE TECHNOLOGIQUE
2.2.3 GUIDE DU MARCHÉ
2.2.4 ANALYSE DE LA PART DE MARCHÉ DE L'ENTREPRISE
2.2.5 MODÉLISATION MULTIVARIÉE
2.2.6 ANALYSE DE HAUT EN BAS
2.2.7 NORMES DE MESURE
2.2.8 POINTS DE DONNÉES ISSUS DES ENTRETIENS PRIMAIRES CLÉS
2.2.9 POINTS DE DONNÉES PROVENANT DE BASES DE DONNÉES SECONDAIRES CLÉS
2.3 MARCHÉ MONDIAL DES SYSTÈMES DE FICHIERS MAÎTRES D'ESSAI ÉLECTRONIQUES (ETMF) : APERÇU DE LA RECHERCHE
2.4 HYPOTHÈSES
3. APERÇU DU MARCHÉ
3.1 CONDUCTEURS
3.2 MESURES DE RETENUE
3.3 OPPORTUNITÉS
3.4 DÉFIS
4. RÉSUMÉ
5 ANALYSES PREMIUM
5.1 LES CINQ FORCES DE PORTER
5.2 NORMES RÉGLEMENTAIRES
5.3 TENDANCES TECHNOLOGIQUES
5.4 ANALYSE DES BREVETS
5.5 ÉTUDE DE CAS
5.6 ANALYSE DE LA CHAÎNE DE VALEUR
5.7 ANALYSE COMPARATIVE DES ENTREPRISES
5.8 ANALYSE DES PRIX
6 MARCHÉ MONDIAL DES SYSTÈMES DE FICHIERS MAÎTRES D'ESSAI ÉLECTRONIQUES (ETMF), PAR L'OFFRE
6.1 APERÇU
6.2 LOGICIEL
6.3 SERVICES
6.3.1 SERVICES PROFESSIONNELS
6.3.1.1. FORMATION ET CONSEIL
6.3.1.2. MISE EN ŒUVRE
6.3.1.3. SUPPORT ET MAINTENANCE
6.3.2 SERVICES GÉRÉS
7 MARCHÉ MONDIAL DES SYSTÈMES DE FICHIERS MAÎTRES D'ESSAI ÉLECTRONIQUES (ETMF), PAR NIVEAU DE DOCUMENTS
7.1 APERÇU
7.2 DOCUMENTS DE NIVEAU D'ÉTUDE
7.3 DOCUMENTS AU NIVEAU DU PAYS
7.4 DOCUMENTS AU NIVEAU DU SITE
8 MARCHÉ MONDIAL DES SYSTÈMES DE FICHIERS MAÎTRES D'ESSAI ÉLECTRONIQUES (ETMF), PAR SYSTÈME D'EXPLOITATION
8.1 APERÇU
8.2 WINDOWS
8.3 LINUX
8.4 MAC
8.5 MOBILE
8.5.1 ANDROID
8.5.2 IPHONE
iPad 8.5.3
9 MARCHÉ MONDIAL DES SYSTÈMES DE FICHIERS MAÎTRES D'ESSAI ÉLECTRONIQUES (ETMF), PAR MODE DE DÉPLOIEMENT
9.1 APERÇU
9.2 SUR LOCAL
9.3 CLOUD
9.3.1 PUBLIC
9.3.2 PRIVÉ
9.3.3 HYBRIDE
10 MARCHÉS MONDIAUX DES SYSTÈMES DE FICHIERS MAÎTRES D'ESSAI ÉLECTRONIQUES (ETMF), PAR FONCTIONNALITÉ
10.1 APERÇU
10.2 SÉCURITÉ COMPLÈTE
10.3 TÉLÉCHARGEMENT/CRÉATION DE DOCUMENTS
10.4 AUDIT
10.5 MÉTADONNÉES
10.6 CLASSIFICATION ET INDEXATION DES DOCUMENTS
10.7 STOCKAGE DE DOCUMENTS
10.8 CAPTURE DE DONNÉES
10.9 RECHERCHE ET RÉCUPÉRATION
10.1 AUTRES
11 MARCHÉ MONDIAL DES SYSTÈMES DE FICHIERS MAÎTRES D'ESSAI ÉLECTRONIQUES (ETMF), PAR MODÈLE DE TARIFICATION
11.1 APERÇU
11.2 GRATUIT
11.3 PAR ABONNEMENT
11.3.1 ABONNEMENT ANNUEL
11.3.2 ABONNEMENT MENSUEL
12 MARCHÉ MONDIAL DES SYSTÈMES DE FICHIERS MAÎTRES D'ESSAI ÉLECTRONIQUES (ETMF), PAR UTILISATEUR FINAL
12.1 APERÇU
12.2 ENTREPRISES DE BIOTECHNOLOGIE ET PHARMACEUTIQUE
12.2.1 EN OFFRANT
12.2.1.1. LOGICIEL
12.2.1.2. SERVICES
12.2.1.2.1. SERVICES PROFESSIONNELS
12.2.1.2.1.1 FORMATION ET CONSEIL
12.2.1.2.1.2 MISE EN ŒUVRE
12.2.1.2.1.3 SUPPORT ET MAINTENANCE
12.2.1.2.2. SERVICES GÉRÉS
12.3 ORGANISMES DE RECHERCHE CONTRACTUELS
12.3.1 EN OFFRANT
12.3.1.1. LOGICIEL
12.3.1.2. SERVICES
12.3.1.2.1. SERVICES PROFESSIONNELS
12.3.1.2.1.1 FORMATION ET CONSEIL
12.3.1.2.1.2 MISE EN ŒUVRE
12.3.1.2.1.3 SUPPORT ET MAINTENANCE
12.3.1.2.2. SERVICES GÉRÉS
12.4 SPONSORS
12.4.1 EN OFFRANT
12.4.1.1. LOGICIEL
12.4.1.2. SERVICES
12.4.1.2.1. SERVICES PROFESSIONNELS
12.4.1.2.1.1 FORMATION ET CONSEIL
12.4.1.2.1.2 MISE EN ŒUVRE
12.4.1.2.1.3 SUPPORT ET MAINTENANCE
12.4.1.2.2. SERVICES GÉRÉS
12,5 AUTRES
13 MARCHÉ MONDIAL DES SYSTÈMES DE FICHIERS MAÎTRES D'ESSAI ÉLECTRONIQUES (ETMF), PAR GÉOGRAPHIE
13.1 MARCHÉ MONDIAL DES SYSTÈMES DE FICHIERS MAÎTRES D'ESSAI ÉLECTRONIQUES (ETMF), (TOUTE LA SEGMENTATION PRÉSENTÉE CI-DESSUS EST REPRÉSENTÉE DANS CE CHAPITRE PAR PAYS)
13.1.1 AMÉRIQUE DU NORD
13.1.1.1. États-Unis
13.1.1.2. CANADA
13.1.1.3. MEXIQUE
13.1.2 EUROPE
13.1.2.1. ALLEMAGNE
13.1.2.2. FRANCE
13.1.2.3. Royaume-Uni
13.1.2.4. ITALIE
13.1.2.5. ESPAGNE
13.1.2.6. RUSSIE
13.1.2.7. TURQUIE
13.1.2.8. BELGIQUE
13.1.2.9. PAYS-BAS
13.1.2.10. NORVÈGE
13.1.2.11. FINLAND
13.1.2.12. SUISSE
13.1.2.13. DANEMARK
13.1.2.14. SUÈDE
13.1.2.15. POLOGNE
13.1.2.16. RESTE DE L'EUROPE
13.1.3 ASIE-PACIFIQUE
13.1.3.1. JAPON
13.1.3.2. CHINE
13.1.3.3. CORÉE DU SUD
13.1.3.4. INDE
13.1.3.5. AUSTRALIE
13.1.3.6. NOUVELLE-ZÉLANDE
13.1.3.7. SINGAPOUR
13.1.3.8. THAÏLANDE
13.1.3.9. MALAISIE
13.1.3.10. INDONÉSIE
13.1.3.11. PHILIPPINES
13.1.3.12. TAIWAN
13.1.3.13. VIETNAM
13.1.3.14. RESTE DE L'ASIE-PACIFIQUE
13.1.4 AMÉRIQUE DU SUD
13.1.4.1. BRÉSIL
13.1.4.2. ARGENTINE
13.1.4.3. RESTE DE L'AMÉRIQUE DU SUD
13.1.5 MOYEN-ORIENT ET AFRIQUE
13.1.5.1. AFRIQUE DU SUD
13.1.5.2. ÉGYPTE
13.1.5.3. ARABIE SAOUDITE
13.1.5.4. Émirats arabes unis
13.1.5.5. OMAN
13.1.5.6. BAHREÏN
13.1.5.7. ISRAËL
13.1.5.8. KOWEÏT
13.1.5.9. QATAR
13.1.5.10. RESTE DU MOYEN-ORIENT ET DE L'AFRIQUE
13.2 PRINCIPAUX ENSEIGNEMENTS : PAR GRANDS PAYS
14 MARCHÉ MONDIAL DES SYSTÈMES DE FICHIERS MAÎTRES D'ESSAI ÉLECTRONIQUES (ETMF), PAYSAGE DES ENTREPRISES
14.1 ANALYSE DES ACTIONS DE LA SOCIÉTÉ : MONDIALE
14.2 ANALYSE DES ACTIONS DE LA SOCIÉTÉ : AMÉRIQUE DU NORD
14.3 ANALYSE DES ACTIONS DE LA SOCIÉTÉ : EUROPE
14.4 ANALYSE DES ACTIONS DE LA SOCIÉTÉ : ASIE-PACIFIQUE
14.5 FUSIONS ET ACQUISITIONS
14.6 DÉVELOPPEMENT ET HOMOLOGIE DE NOUVEAUX PRODUITS
14.7 EXTENSIONS
14.8 MODIFICATIONS RÉGLEMENTAIRES
14.9 PARTENARIATS ET AUTRES DÉVELOPPEMENTS STRATÉGIQUES
15 ANALYSE DU MARCHÉ MONDIAL DES SYSTÈMES DE FICHIERS MAÎTRES D'ESSAI ÉLECTRONIQUES (ETMF), ANALYSE SWOT ET DBMR
16 MARCHÉ MONDIAL DES SYSTÈMES DE FICHIERS MAÎTRES D'ESSAI ÉLECTRONIQUES (ETMF), PROFIL DE L'ENTREPRISE
16.1 ADLIB
16.1.1 APERÇU DE L'ENTREPRISE
16.1.2 ANALYSE DES REVENUS
16.1.3 PRÉSENCE GÉOGRAPHIQUE
16.1.4 PORTEFEUILLE DE PRODUITS
16.1.5 ÉVOLUTION RÉCENTE
16.2 VEEVA MEDTECH (VEEVA SYSTEMS, INC)
16.2.1 APERÇU DE L'ENTREPRISE
16.2.2 ANALYSE DES REVENUS
16.2.3 PRÉSENCE GÉOGRAPHIQUE
16.2.4 PORTEFEUILLE DE PRODUITS
16.2.5 ÉVOLUTION RÉCENTE
16.3 ESSAI INTERACTIF
16.3.1 APERÇU DE L'ENTREPRISE
16.3.2 ANALYSE DES REVENUS
16.3.3 PRÉSENCE GÉOGRAPHIQUE
16.3.4 PORTEFEUILLE DE PRODUITS
16.3.5 ÉVOLUTION RÉCENTE
16.4 MÉDIDONNÉES (DASSAULT SYSTEMES)
16.4.1 APERÇU DE L'ENTREPRISE
16.4.2 ANALYSE DES REVENUS
16.4.3 PRÉSENCE GÉOGRAPHIQUE
16.4.4 PORTEFEUILLE DE PRODUITS
16.4.5 ÉVOLUTION RÉCENTE
16.5 OCTALSOFT (GLORANT, LLC)
16.5.1 APERÇU DE L'ENTREPRISE
16.5.2 ANALYSE DES REVENUS
16.5.3 PRÉSENCE GÉOGRAPHIQUE
16.5.4 PORTEFEUILLE DE PRODUITS
16.5.5 ÉVOLUTION RÉCENTE
16.6 MASTERCONTROL SOLUTIONS, INC
16.6.1 APERÇU DE L'ENTREPRISE
16.6.2 ANALYSE DES REVENUS
16.6.3 PRÉSENCE GÉOGRAPHIQUE
16.6.4 PORTEFEUILLE DE PRODUITS
16.6.5 ÉVOLUTION RÉCENTE
16,7 IQVIA INC
16.7.1 APERÇU DE L'ENTREPRISE
16.7.2 ANALYSE DES REVENUS
16.7.3 PRÉSENCE GÉOGRAPHIQUE
16.7.4 PORTEFEUILLE DE PRODUITS
16.7.5 ÉVOLUTION RÉCENTE
16.8 CLOUDBYZ
16.8.1 APERÇU DE L'ENTREPRISE
16.8.2 ANALYSE DES REVENUS
16.8.3 PRÉSENCE GÉOGRAPHIQUE
16.8.4 PORTEFEUILLE DE PRODUITS
16.8.5 ÉVOLUTION RÉCENTE
16.9 TECHNOLOGIES CLINEVO
16.9.1 APERÇU DE L'ENTREPRISE
16.9.2 ANALYSE DES REVENUS
16.9.3 PRÉSENCE GÉOGRAPHIQUE
16.9.4 PORTEFEUILLE DE PRODUITS
16.9.5 ÉVOLUTION RÉCENTE
16.1 FLORENCE HEALTHCARE
16.10.1 APERÇU DE L'ENTREPRISE
16.10.2 ANALYSE DES REVENUS
16.10.3 PRÉSENCE GÉOGRAPHIQUE
16.10.4 PORTEFEUILLE DE PRODUITS
16.10.5 ÉVOLUTION RÉCENTE
16.11 ORACLE
16.11.1 APERÇU DE L'ENTREPRISE
16.11.2 ANALYSE DES REVENUS
16.11.3 PRÉSENCE GÉOGRAPHIQUE
16.11.4 PORTEFEUILLE DE PRODUITS
16.11.5 ÉVOLUTION RÉCENTE
16.12 ARISGLOBAL LLC
16.12.1 APERÇU DE L'ENTREPRISE
16.12.2 ANALYSE DES REVENUS
16.12.3 PRÉSENCE GÉOGRAPHIQUE
16.12.4 PORTEFEUILLE DE PRODUITS
16.12.5 ÉVOLUTION RÉCENTE
16.13 MONTRIUM INC
16.13.1 APERÇU DE L'ENTREPRISE
16.13.2 ANALYSE DES REVENUS
16.13.3 PRÉSENCE GÉOGRAPHIQUE
16.13.4 PORTEFEUILLE DE PRODUITS
16.13.5 ÉVOLUTION RÉCENTE
16.14 SOLUTIONS DE DONNÉES CRUCIALES
16.14.1 APERÇU DE L'ENTREPRISE
16.14.2 ANALYSE DES REVENUS
16.14.3 PRÉSENCE GÉOGRAPHIQUE
16.14.4 PORTEFEUILLE DE PRODUITS
16.14.5 ÉVOLUTION RÉCENTE
16.15 KEY2COMPLIANCE AB (SYMBIOTEQ)
16.15.1 APERÇU DE L'ENTREPRISE
16.15.2 ANALYSE DES REVENUS
16.15.3 PRÉSENCE GÉOGRAPHIQUE
16.15.4 PORTEFEUILLE DE PRODUITS
16.15.5 ÉVOLUTION RÉCENTE
16.16 DATARIVER SRL
16.16.1 APERÇU DE L'ENTREPRISE
16.16.2 ANALYSE DES REVENUS
16.16.3 PRÉSENCE GÉOGRAPHIQUE
16.16.4 PORTEFEUILLE DE PRODUITS
16.16.5 ÉVOLUTION RÉCENTE
16.17 ETHICA CRO
16.17.1 APERÇU DE L'ENTREPRISE
16.17.2 ANALYSE DES REVENUS
16.17.3 PRÉSENCE GÉOGRAPHIQUE
16.17.4 PORTEFEUILLE DE PRODUITS
16.17.5 ÉVOLUTION RÉCENTE
16.18 ESSAI (CLINBLOCKS BV)
16.18.1 APERÇU DE L'ENTREPRISE
16.18.2 ANALYSE DES REVENUS
16.18.3 PRÉSENCE GÉOGRAPHIQUE
16.18.4 PORTEFEUILLE DE PRODUITS
16.18.5 ÉVOLUTION RÉCENTE
16.19 PREMIER CONSULTING
16.19.1 APERÇU DE L'ENTREPRISE
16.19.2 ANALYSE DES REVENUS
16.19.3 PRÉSENCE GÉOGRAPHIQUE
16.19.4 PORTEFEUILLE DE PRODUITS
16.19.5 DÉVELOPPEMENTS RÉCENTS
16.2 PHLEXGLOBAL (UNE SOCIÉTÉ PHARMALEX)
16.20.1 APERÇU DE L'ENTREPRISE
16.20.2 ANALYSE DES REVENUS
16.20.3 PRÉSENCE GÉOGRAPHIQUE
16.20.4 PORTEFEUILLE DE PRODUITS
16.20.5 DÉVELOPPEMENTS RÉCENTS
16.21 SURECLINICAL INC.
16.21.1 APERÇU DE L'ENTREPRISE
16.21.2 ANALYSE DES REVENUS
16.21.3 PRÉSENCE GÉOGRAPHIQUE
16.21.4 PORTEFEUILLE DE PRODUITS
16.21.5 ÉVOLUTION RÉCENTE
REMARQUE : La liste des entreprises présentées n’est pas exhaustive et correspond aux besoins de nos clients précédents. Nous analysons plus de 100 entreprises dans le cadre de nos études ; cette liste peut donc être modifiée ou remplacée sur demande.
17 CONCLUSION
18 QUESTIONNAIRE
19 RAPPORTS CONNEXES
20 À PROPOS DE DATA BRIDGE MARKET RESEARCH
Méthodologie de recherche
La collecte de données et l'analyse de l'année de base sont effectuées à l'aide de modules de collecte de données avec des échantillons de grande taille. L'étape consiste à obtenir des informations sur le marché ou des données connexes via diverses sources et stratégies. Elle comprend l'examen et la planification à l'avance de toutes les données acquises dans le passé. Elle englobe également l'examen des incohérences d'informations observées dans différentes sources d'informations. Les données de marché sont analysées et estimées à l'aide de modèles statistiques et cohérents de marché. De plus, l'analyse des parts de marché et l'analyse des tendances clés sont les principaux facteurs de succès du rapport de marché. Pour en savoir plus, veuillez demander un appel d'analyste ou déposer votre demande.
La méthodologie de recherche clé utilisée par l'équipe de recherche DBMR est la triangulation des données qui implique l'exploration de données, l'analyse de l'impact des variables de données sur le marché et la validation primaire (expert du secteur). Les modèles de données incluent la grille de positionnement des fournisseurs, l'analyse de la chronologie du marché, l'aperçu et le guide du marché, la grille de positionnement des entreprises, l'analyse des brevets, l'analyse des prix, l'analyse des parts de marché des entreprises, les normes de mesure, l'analyse globale par rapport à l'analyse régionale et des parts des fournisseurs. Pour en savoir plus sur la méthodologie de recherche, envoyez une demande pour parler à nos experts du secteur.
Personnalisation disponible
Data Bridge Market Research est un leader de la recherche formative avancée. Nous sommes fiers de fournir à nos clients existants et nouveaux des données et des analyses qui correspondent à leurs objectifs. Le rapport peut être personnalisé pour inclure une analyse des tendances des prix des marques cibles, une compréhension du marché pour d'autres pays (demandez la liste des pays), des données sur les résultats des essais cliniques, une revue de la littérature, une analyse du marché des produits remis à neuf et de la base de produits. L'analyse du marché des concurrents cibles peut être analysée à partir d'une analyse basée sur la technologie jusqu'à des stratégies de portefeuille de marché. Nous pouvons ajouter autant de concurrents que vous le souhaitez, dans le format et le style de données que vous recherchez. Notre équipe d'analystes peut également vous fournir des données sous forme de fichiers Excel bruts, de tableaux croisés dynamiques (Fact book) ou peut vous aider à créer des présentations à partir des ensembles de données disponibles dans le rapport.