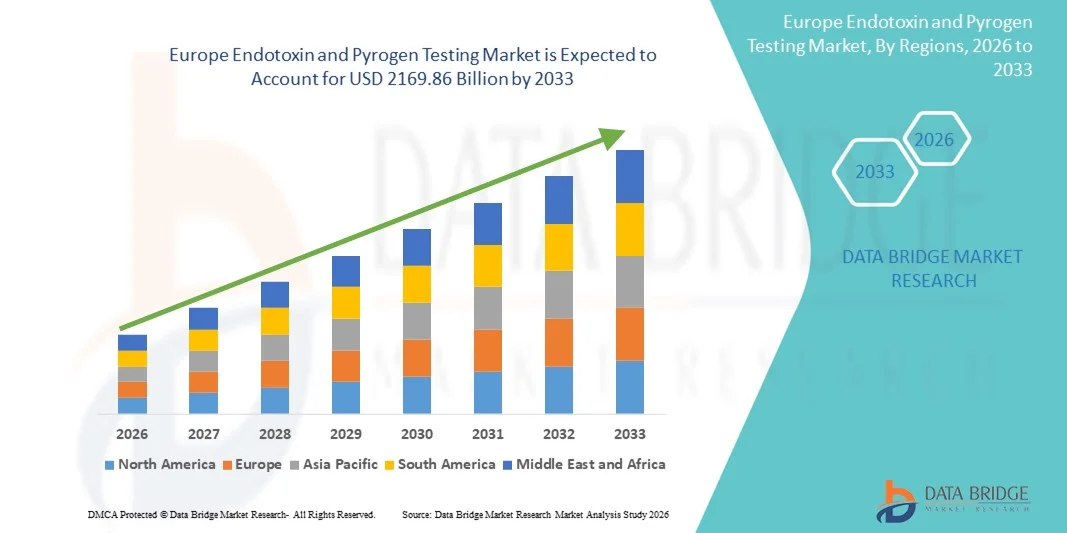
欧州エンドトキシン・パイロジェン検査市場規模、シェア、トレンド分析レポート
Market Size in USD Billion
CAGR :
% 
 USD
1,136.47 Billion
USD
2,169.86 Billion
2025
2033
USD
1,136.47 Billion
USD
2,169.86 Billion
2025
2033
| 2026 –2033 | |
| USD 1,136.47 Billion | |
| USD 2,169.86 Billion | |
|
|
|
|
欧州エンドトキシンおよびパイロジェン検査市場セグメンテーション、製品タイプ別(検出キットおよび試薬、機器、システムおよびソフトウェア、エンドトキシン検査サービスおよび消耗品およびアクセサリ)、検査タイプ別(リムルスアメーボサイトライセート(LAL)検査、Tal検査、単球活性化試験(MAT)、ウサギパイロジェン検査および組換えC(RFC)アッセイ)、用途別(医薬品製造、医療機器製造、原材料生産および包装製造)、方法別(ゲルクロットエンドトキシン検査、発色性エンドトキシン検査および比濁法エンドトキシン検査)、購入形態別(大規模グループ、中小規模グループおよび個人)、最終製品別(ワクチンおよび/またはCGT、生物製剤、注射剤およびその他)、エンドユーザー別(製薬会社、バイオテクノロジー会社、バイオメディカル会社、医療機器会社、受託研究機関(CRO)、受託製造機関(CMO)) - 業界動向および2025年までの予測2033
欧州のエンドトキシンおよびパイロジェン検査市場規模
- ヨーロッパのエンドトキシンおよびパイロジェン検査市場規模は2025年に11,364.7億米ドルと評価され、予測期間中に8.42%のCAGRで成長し、2033年には21,698.6億米ドル に達すると予想されています。
- 市場の成長は、患者の安全性、厳格な規制要件、製薬、バイオテクノロジー、医療機器製造における品質管理基準の向上への重点の高まりによって主に推進されており、臨床および産業の両方の環境で信頼性の高いエンドトキシンおよび発熱物質検査ソリューションの採用が拡大しています。
- さらに、迅速で正確かつコンプライアンスに準拠した試験方法に対する需要の高まりと、組み換えおよび代替発熱物質試験技術の進歩により、エンドトキシンおよび発熱物質試験は現代の品質保証システムの重要な要素として位置付けられ、業界全体の成長を大幅に促進しています。
欧州エンドトキシンおよびパイロジェン検査市場分析
- エンドトキシンおよび発熱物質検査ソリューションは、有害な細菌毒素を検出し、患者に有害な反応を引き起こす可能性があるため、医薬品、生物製剤、医療機器の安全性を確保する上で重要な役割を果たしており、臨床環境と産業環境の両方で品質管理と規制遵守に不可欠な要素となっています。
- エンドトキシンおよび発熱物質検査の需要増加の主な要因は、厳格な規制ガイドライン、注射薬および生物製剤の生産増加、患者の安全性に関する意識の高まり、そして組換え因子C(rFC)アッセイなどの高度な動物を使わない検査方法への段階的な移行です。
- 英国は、確立された製薬およびバイオテクノロジー産業、強力な規制枠組み、多額の研究開発投資、生物製剤、ワクチン、医療機器製造における高度なエンドトキシンおよびパイロジェン検査技術の採用率の高さにより、2025年には約38.7%という最大の収益シェアでエンドトキシンおよびパイロジェン検査市場を支配しました。
- ドイツは、医薬品およびバイオテクノロジー製造インフラの拡大、ライフサイエンスに対する政府の取り組みの増加、契約研究および試験サービスの増加、厳格なEUおよび国際品質基準への準拠に支えられ、予測期間中にエンドトキシンおよびパイロジェン検査市場で最も急速に成長する国になると予想されており、推定CAGR約8.3%を記録すると予想されています。
- 大規模グループセグメントは、大量の検査需要を満たすために大量調達を必要とする既存の医療機関や大手製薬組織によって牽引され、2025年には48.3%の収益シェアで市場を支配しました。
レポートの範囲とエンドトキシンおよびパイロジェン検査市場のセグメンテーション
|
属性 |
エンドトキシンおよびパイロジェン試験の主要市場洞察 |
|
対象セグメント |
|
|
対象国 |
ヨーロッパ
|
|
主要な市場プレーヤー |
• Charles River Laboratories (米国) |
|
市場機会 |
|
|
付加価値データ情報セット |
Data Bridge Market Research がまとめた市場レポートには、市場価値、成長率、セグメンテーション、地理的範囲、主要プレーヤーなどの市場シナリオに関する洞察に加えて、専門家による詳細な分析、患者の疫学、パイプライン分析、価格分析、規制の枠組みも含まれています。 |
欧州のエンドトキシンおよびパイロジェン検査市場の動向
高度なエンドトキシンおよび発熱物質検出法の採用増加
- エンドトキシンおよびパイロジェン検査市場における重要な加速傾向として、迅速な微生物学的検査や組み換え因子C(rFC)アッセイなどの高度な検出方法の採用が増加し、検査精度とターンアラウンドタイムが改善されています。
- 例えば、2023年にはブラジルの複数の製薬メーカーが、従来のLAL試験への依存を減らしながら、世界的な規制の要求を満たすために、組み換え因子Cに基づくエンドトキシン試験の使用を拡大しました。
- 地域全体の研究所は、医薬品、生物製剤、医療機器の製品安全性を確保するために、試験の効率と感度の向上に重点を置いています。
- 倫理的な懸念と規制の奨励により、代替的で持続可能な試験方法への移行も勢いを増している。
- この傾向は南米における品質管理の実践を変革し、より安全な医薬品の生産と国際市場への輸出準備を支援している。
欧州のエンドトキシンおよびパイロジェン検査市場の動向
ドライバ
医薬品および生物製剤の製造活動の拡大
- 南米全域における医薬品、バイオテクノロジー、医療機器製造活動の着実な拡大は、世界的な生産動向と足並みを揃えており、エンドトキシンおよび発熱物質検査ソリューションの需要を加速させる重要な原動力となっている。
- 例えば、2024年にはブラジルの大手バイオ医薬品メーカーが、国内および海外市場向けの注射ワクチンやバイオシミラーの大規模生産をサポートするために、社内のエンドトキシン検査能力を拡大しました。
- 無菌性の保証と患者の安全性を重視する世界的に調和された規制要件により、医薬品開発、臨床製造、商業生産段階を通じて、エンドトキシンと発熱物質の定期的な検査が義務付けられています。
- 新興国および先進国における医療インフラ、ライフサイエンス研究、現地での医薬品製造への公的および民間投資の増加により、信頼性が高く検証済みの検査ソリューションに対する需要がさらに高まっています。
- 欧州や欧州などの規制市場への医薬品や生物製剤の輸出増加により、国際的な品質および安全基準への厳格な遵守が必要となり、エンドトキシンおよび発熱物質の試験プロトコルの採用が強化されている。
抑制/挑戦
高いテストコストと限られた技術的専門知識
- 高度なエンドトキシンおよび発熱物質検査システムに関連する高額な資本コストと運用コストは、特にヨーロッパや世界中のコストに敏感な地域の中小規模の研究所にとって、依然として大きな制約となっています。
- 例えば、アルゼンチンのいくつかの契約検査機関は、予算の制約、設備費の高騰、継続的なメンテナンス費用のために、迅速検査技術や代替検査技術の導入が遅れていると報告している。
- 複雑なエンドトキシンおよび発熱物質検査を実施、検証、解釈できる熟練した訓練を受けた専門家の数が限られているため、市場への浸透がさらに制限されている。
- 各国の規制執行と試験ガイドラインの違いにより、特に複数のグローバル市場で事業を展開するメーカーにとって、標準化された試験方法の実現が困難になっています。
- 費用対効果の高い試験ソリューションの開発、人材育成イニシアチブの拡大、国際的な規制の調和の強化を通じてこれらの課題を克服することは、世界のエンドトキシンおよびパイロジェン試験市場の持続的な成長を支えるために不可欠です。
欧州のエンドトキシンおよびパイロジェン検査市場の展望
市場は、製品タイプ、テストタイプ、アプリケーション、方法、購入モード、最終製品、およびエンドユーザーに基づいてセグメント化されています。
- 製品タイプ別
製品タイプ別に見ると、エンドトキシンおよびパイロジェン検査市場は、検出キットおよび試薬、機器、システムおよびソフトウェア、エンドトキシン検査サービス、消耗品および付属品に分類されます。検出キットおよび試薬セグメントは、2025年には41.6%という最大の市場収益シェアを占めました。これは主に、医薬品、バイオテクノロジー、医療機器の製造プロセスにおいて不可欠かつ繰り返し使用されるためです。これらの製品は、原材料試験、工程内品質検査、最終製品出荷試験など、複数の段階で必要とされます。規制当局は検証済みのキットおよび試薬の使用を義務付けており、生産規模に関わらず安定した需要を確保しています。無菌製造環境での高頻度検査は、消費量をさらに増加させます。検出キットは比較的費用対効果が高く、大規模な研究室でも小規模な研究室でも利用できます。感度と特異性を向上させる継続的なイノベーションは、導入を促進します。複数の検査方法との互換性は、柔軟性を高めます。注射剤製造の世界的な拡大は、需要の増加を支えています。生物製剤の生産増加も、需要の伸びに大きく貢献しています。確立されたサプライヤーネットワークにより、途切れることのない供給が保証されます。また、規制への強い依存度により、長期的な優位性が確保されます。
システムおよびソフトウェア分野は、ラボ自動化とデジタルコンプライアンスツールの急速な導入に牽引され、2026年から2033年にかけて年平均成長率(CAGR)19.1%と最も高い成長が見込まれています。製薬メーカーは、人的ミスを最小限に抑え、試験効率を向上させるため、自動化ソリューションをますます重視しています。ソフトウェアプラットフォームは、データの整合性、監査証跡、規制文書をサポートします。LIMSシステムとの統合により、運用の透明性が向上します。スマートラボへの関心の高まりが、導入を加速させています。大手メーカーはデジタル変革に多額の投資を行っています。自動化により、バッチリリースのターンアラウンドタイムが短縮されます。規制当局による査察では、デジタル記録がますます重視されるようになっています。クラウドベースのシステムは拡張性を向上させます。特にCMO(最高マーケティング責任者)の間で需要が高まっています。高度な品質システムへの投資の増加が、持続的な成長を支えています。
- テストの種類別
エンドトキシンおよびパイロジェン試験市場は、試験の種類に基づいて、リムルスアメーボサイトライセート(LAL)試験、TAL試験、単球活性化試験(MAT)、ウサギパイロジェン試験、および組換えC因子(RFC)アッセイに分類されます。LAL試験セグメントは、米国、ヨーロッパ、アジアで長年にわたる規制の承認により、2025年には47.3%という最大の市場収益シェアを占めました。この試験は、注射薬、ワクチン、および埋め込み型医療機器に広く使用されています。実証済みの信頼性と感度により、継続的な選好が推進されています。ゲル凝固法、発色法、および比濁法の形式で利用できるため、汎用性が向上します。製薬会社は、日常的なバッチ試験にLALを利用しています。確立されたプロトコルにより、検証の複雑さが軽減されます。強力な履歴データがコンプライアンスをサポートします。サプライヤーの可用性により、一貫したアクセスが保証されます。実験室の専門家の間での熟知度が高いため、優位性が強化されます。新しい方法と比較して費用対効果が高いため、採用が促進されます。標準の世界的な調和が使用をサポートしています。
組み換えC因子(RFC)アッセイ分野は、動物を使用しない試験法への世界的な移行を背景に、2026年から2033年にかけて22.6%という最も高いCAGRで成長すると予想されています。カブトガニの採取に関する倫理的懸念が、RFCの導入を促進しています。規制当局は代替法の支持を強めています。RFCは高い特異性と再現性を提供します。変動性の低減は結果の一貫性を向上させます。バイオ医薬品メーカーは、先進的な治療にRFCを採用しています。アッセイ性能の向上は信頼性を高めます。技術の進歩は感度を向上させます。持続可能性への取り組みは需要を加速させます。規制当局の承認の増加は導入を促進します。生物製剤パイプラインの拡大は成長を支えます。長期的な環境的メリットは、市場での受け入れを強化します。
- アプリケーション別
エンドトキシンおよびパイロジェン検査市場は、用途別に、医薬品製造、医療機器製造、原材料生産、包装製造に分類されます。医薬品製造セグメントは、厳格な無菌性とエンドトキシン管理要件の強化により、2025年には44.8%の収益シェアで市場を席巻しました。エンドトキシン検査は、医薬品の開発および商業化の過程において必須です。生産量の増加は検査頻度を高めます。注射剤および生物学的製剤の増加は需要を維持します。規制当局による査察はコンプライアンスを強化します。バッチリリースプロトコルには検証済みの検査が必要です。世界的な医薬品製造施設の拡大は、採用を促進します。継続的なプロセス監視は検査の利用を増加させます。強力な規制監督は、持続的な優位性を確保します。大規模な操業は、需要の増加を促進します。品質保証への投資は、利用を強化します。
医療機器製造分野は、インプラント機器および侵襲性機器の生産増加により、2026年から2033年にかけて19.8%という最も高いCAGRで成長すると予測されています。規制当局の監視強化により、発熱物質検査が義務付けられています。医療機器輸出の世界的な拡大が需要を牽引しています。低侵襲手術の増加が市場拡大を支えています。患者安全基準の強化が検査の導入を促進しています。新興市場では製造能力が拡大しています。規制の調和化により、コンプライアンス要件が強化されています。先端材料には厳格な試験が必要です。整形外科用および心血管機器市場の拡大が成長を支えています。CMOへのアウトソーシングの増加が試験需要を加速させています。機器設計の革新により、試験の複雑さが増しています。
- 方法別
エンドトキシンおよびパイロジェン試験市場は、方法に基づいて、ゲル凝固エンドトキシン試験、発色性エンドトキシン試験、および比濁法エンドトキシン試験に分類されます。ゲル凝固エンドトキシン試験セグメントは、その簡便性と規制当局の承認により、2025年には39.5%という最大の収益シェアを占めました。この方法は、最小限の機器で済みます。日常的な検査において費用対効果が高く、中小規模の検査室で広く使用されています。定性的な結果は、基本的なコンプライアンスニーズを満たします。長い検証履歴が信頼性を支え、解釈が容易なため、導入が促進されます。少量の検査に適しています。最小限のトレーニング要件で検査室にメリットをもたらします。一貫した性能が信頼性を保証します。幅広い規制当局の承認が、優位性を維持しています。
クロモジェニックエンドトキシン検査分野は、定量検査と高感度検査の需要に牽引され、2026年から2033年にかけて20.9%という最も高いCAGRで成長すると予想されています。製薬会社は、高精度なエンドトキシン測定を求めています。自動化への対応により、スループットが向上します。複雑な生物製剤にも適しています。精度の向上により、規制遵守をサポートします。高い再現性により、ばらつきが低減します。生物製剤の生産量の増加により、導入が加速します。自動化システムとの統合により、効率が向上します。高度な製剤には、高感度な検出が求められます。大規模製造の成長が需要を支え、技術の向上により、パフォーマンスが向上します。
- 購入方法別
購入方法に基づいて、エンドトキシンおよびパイロジェン検査市場は、大規模グループ、中規模および小規模グループ、および個人に分類されます。大規模グループセグメントは、大量の検査需要を満たすために大量調達を必要とする既存の医療機関と大手製薬組織に牽引され、2025年には48.3%の収益シェアで市場を支配しました。大規模グループは、長期サプライヤー契約、規模の経済、合理化された検証プロセスの恩恵を受けています。集中化された品質管理業務と継続的な生産サイクルには、頻繁な検査が必要です。強力な規制遵守と定期的な監査は、検査の採用を強化します。高い投資能力は、高度な検査技術へのアクセスを可能にします。社内研究所との統合は、効率と精度を高めます。このセグメントでは、グローバルに事業を展開する多国籍企業からの一貫した需要も見られます。確立されたSOPと品質管理システムが優位性を強化しています。
個人セグメントは、小規模バイオテクノロジー企業、新興企業、研究機関における導入拡大を背景に、2026年から2033年にかけて19.4%という最も高いCAGR(年平均成長率)を達成すると予想されています。個人は、設備投資削減のため、アウトソーシングの選択肢をますます求めています。小規模企業による臨床試験の増加も需要を牽引しています。柔軟なサービスモデルとオンデマンド試験によって、導入が加速しています。規制意識の高まりにより、コンプライアンス重視の試験が確保されています。小規模組織における生物製剤および細胞・遺伝子治療のパイプラインの拡大も、成長を支えています。デジタル発注と合理化されたレポート作成へのアクセスは、顧客の魅力を高めています。新興市場と新興企業の成長も、市場拡大に寄与しています。個人顧客は、CRO/CMOサービスを活用し、試験頻度を高めることがよくあります。
- 最終製品別
最終製品に基づいて、エンドトキシンおよびパイロジェン検査市場は、ワクチンおよび/または細胞および遺伝子治療(CGT)、生物製剤、注射剤、およびその他に分類されます。生物製剤セグメントは、治療用途における生物製剤の広範な使用と、無菌性およびエンドトキシン検査に関する厳格な規制要件に支えられ、2025年には42.6%の収益シェアで市場を支配しました。モノクローナル抗体、組み換えタンパク質、および治療用酵素の大規模生産は、日常的な検査を促進します。規制監査および品質保証プログラムにより、頻繁な検査サイクルが保証されます。研究開発および臨床試験への多額の投資が需要を強化します。大手バイオテクノロジーメーカーの存在は、高度な検査方法の採用を促進します。生物製剤の製造には、汚染を防ぐための堅牢な品質管理フレームワークが必要です。北米とヨーロッパに確立されたインフラストラクチャが優位性を強化します。契約検査機関との提携により、リーチが拡大します。生物製剤の安全性に対する意識の高まりにより、市場での採用はさらに促進されます。
ワクチンおよび/または細胞・遺伝子治療(CGT)セグメントは、新規ワクチンと高度な細胞・遺伝子治療の開発加速に牽引され、2026年から2033年にかけて22.3%という最速のCAGRを達成すると予想されています。世界的な健康イニシアチブ、パンデミックへの備え、および増加する予防接種プログラムにより、検査の需要が高まっています。CGT製品は、複雑な製造プロセスのため、非常に感度の高いエンドトキシン検査が必要です。個別化医療と標的療法の拡大が採用を促しています。CROや専門ラボへのアウトソーシングにより、コンプライアンスが確保されます。高度な治療医薬品に対する規制の焦点が成長を後押ししています。mRNAおよびウイルスベクター技術の革新により、生産量が押し上げられています。新興バイオテクノロジー企業は、ハイスループット検査ソリューションを積極的に模索しています。ワクチン研究開発への資金提供の増加は、市場拡大を支えています。自動化された迅速な検査プラットフォームの採用により、効率性が加速します。
- エンドユーザー別
エンドユーザーに基づいて、エンドトキシンおよびパイロジェン検査市場は、製薬会社、バイオテクノロジー会社、バイオメディカル会社、医療機器会社、CRO、CMOに分類されます。製薬会社は、広範な社内品質管理体制により、2025年には45.7%の収益シェアで市場を支配しました。大量生産は検査ニーズの増加につながります。規制監査には頻繁な検証が必要です。社内研究所への投資は優位性を強化します。継続的な生産サイクルは需要を促進します。高いコンプライアンス基準は、日常的な検査を必要とします。生物製剤パイプラインの拡大は、その利用を支えています。強力な財務力は、高度な検査の導入を可能にします。グローバルなプレゼンスにより、検査規模が拡大します。確立された品質フレームワークは、優位性を強化します。
CROおよびCMOセグメントは、アウトソーシングのトレンド拡大に牽引され、2026年から2033年にかけて21.7%という最も高いCAGRで成長すると予想されています。製薬会社はコスト最適化を追求し、アウトソーシングによる試験は効率性を向上させます。CMOはグローバルなキャパシティを拡大します。規制遵守はサービス需要を押し上げます。小規模バイオテクノロジー企業はCROに依存しています。専門知識は導入を促進します。受託製造の増加は試験量を加速させます。柔軟なサービスモデルは顧客を引き付けます。新興市場への進出は成長を支え、臨床試験活動の増加は需要を高めます。
欧州エンドトキシン・パイロジェン検査市場地域分析
- ヨーロッパのエンドトキシンおよびパイロジェン検査市場は、主に厳格な規制基準と安全で高品質の医薬品、生物製剤、医療機器に対する需要の増加により、予測期間を通じて大幅なCAGRで拡大すると予測されています。
- 都市化の進展、バイオテクノロジーおよび製薬業界の成長、そして品質管理への強いこだわりにより、地域全体でエンドトキシンおよびパイロジェン検査の導入が促進されています。欧州のメーカーは、USP、EP、JPのガイドラインに準拠するために、ゲル化技術、発色法、組換え技術などの高度な検査プラットフォームの導入をますます進めています。自動検査システム、デジタルレポート、ラボインフラへの投資により、効率性、信頼性、コンプライアンスがさらに向上しています。病院、CRO、CMO、製薬会社など、幅広い分野で需要があり、特に注射剤、ワクチン、生物製剤への需要が高まっています。
- 医療関係者における患者の安全性と品質保証への意識の高まりが、市場拡大の原動力となっています。標準化された検査プロトコルは、新規施設と既存検査室の改修の両方で広く導入されています。また、製薬会社と受託試験機関との連携強化も、最先端の検査技術へのアクセスを確保し、導入を後押ししています。欧州における持続可能性とイノベーションへの注力は、エンドトキシンおよびパイロジェン検査サービスのあらゆる分野における着実な成長を促進しています。
英国のエンドトキシンおよびパイロジェン検査市場の洞察
英国のエンドトキシンおよびパイロジェン検査市場は、確立された製薬およびバイオテクノロジー産業、強力な規制の枠組み、多大な研究開発投資、生物製剤、ワクチン、医療機器製造における高度なエンドトキシンおよびパイロジェン検査技術の高い採用により、 2025年にはヨーロッパのエンドトキシンおよびパイロジェン検査市場で約38.7 %という最大の収益シェアを占めました。英国の製造業者は、国際的な品質基準を満たすために、自動化された検査プラットフォームと高感度アッセイをますます活用しています。政府がライフサイエンスと生物医学研究の支援に重点を置いていることは、さらなる市場の拡大を促しています。契約検査サービス、高度な実験室機器、デジタルワークフロー管理の広範な採用により、運用効率が向上しています。注射剤、バイオシミラー、ワクチンの生産増加により、検査の需要が高まっています。検査プロトコルの標準化と、FDA、EMA、USP規制の遵守により高い信頼性が保証されます。市場は製薬会社と専門CROとの連携からも恩恵を受けています。患者の安全、コンプライアンス、品質保証への重点的な取り組みにより、英国は引き続き欧州のエンドトキシンおよびパイロジェン検査市場において最大の収益を生み出す国となっています。
ドイツのエンドトキシンおよびパイロジェン検査市場の洞察 ドイツ
のエンドトキシンおよびパイロジェン検査市場は、予測期間中にヨーロッパのエンドトキシンおよびパイロジェン検査市場の中で最も急速に成長する国になると予想されており、推定CAGRは約8.3%です。成長は、医薬品およびバイオテクノロジー製造インフラの拡大、ライフサイエンスに対する政府の取り組みの増加、委託研究および試験サービスの増加、および厳格なEUおよび国際品質基準への準拠によって支えられています。発色性アッセイ、ゲル凝固アッセイ、および組み換えアッセイを含む自動検査システムの採用により、高い精度と規制遵守が保証されます。ワクチン、生物製剤、および非経口薬の国内生産の増加は、エンドトキシンおよびパイロジェン検査の需要を加速させます。ドイツはイノベーション、研究室のデジタル化、および持続可能性を重視しており、市場の成長を促進しています。企業は、研究室の近代化、デジタル報告システム、およびハイスループット検査プラットフォームに投資しています。世界的なCROおよびCMOとのコラボレーションにより、高度な検査技術へのアクセスが可能になります。 EMAおよび世界的な安全基準との規制の整合により、標準化された検査プロトコルの広範な導入が確保されています。患者安全への意識の高まり、品質管理体制の強化、そして病院、製薬会社、受託検査機関における自動検査ソリューションの統合も、市場をさらに牽引しています。
ヨーロッパにおけるエンドトキシンおよびパイロジェン検査の市場シェア
エンドトキシンおよびパイロジェン検査業界は、主に、次のような定評のある企業によって牽引されています。
• Charles River Laboratories(米国)
• Lonza Group(スイス)
• Thermo Fisher Scientific(米国)
• Merck KGaA(ドイツ)
• Associates of Cape Cod(米国)
• WuXi AppTec(中国)
• Eurofins Scientific(ルクセンブルク)
• BioMérieux(フランス)
• ToxinSensor(米国)
• Hyglos GmbH(ドイツ)
• Fujifilm Wako Chemicals(日本)
• GenScript Biotech(中国)
•生化学工業株式会社(日本)
• Pacific BioLabs(米国)
• Cambrex Corporation(米国)
• SGS SA(スイス)
• Kinetic-QCL(米国)
• Nelson Laboratories(米国)
• RANDOX Laboratories(英国)
• Creative Diagnostics(米国)
欧州のエンドトキシンおよびパイロジェン検査市場の最新動向
- 2021年4月、アソシエイツ・オブ・ケープコッド社は、動物由来原料への依存を減らしながらアッセイの一貫性を向上させるように設計された持続可能な細菌エンドトキシン検査製品であるPyroSmart NextGen組換えLAL試薬を発売しました。
- 2021年6月、欧州薬局方委員会は、5年以内にウサギ発熱物質試験を欧州薬局方から廃止する規制上の動きを発表し、進化する基準に準拠するために単球活性化試験(MAT)などの代替法を推奨しました。
- 2024年1月、FUJIFILM Wako Chemicals USA Corporationは、リムルス・アメーボサイト・ライセート(LAL)試薬ポートフォリオをアップグレードし、感度の向上と変動性の低減を実現し、非経口医薬品および医療機器におけるエンドトキシン試験の信頼性を高めました。
- 2024年2月、チャールズリバーラボラトリーズは、自動化統合を備えた強化された単球活性化試験(MAT)プラットフォームを導入し、生物製剤および細胞療法試験における発熱物質検出ワークフローのスループットと再現性を向上させました。
- 2024年3月、ロンザグループは、動物を使わない持続可能な試験方法への業界のトレンドに合わせて、新しい組み換え因子C(rFC)ベースのアッセイキットを発売し、エンドトキシンおよびパイロジェン試験の提供を拡大しました。
SKU-
世界初のマーケットインテリジェンスクラウドに関するレポートにオンラインでアクセスする
- インタラクティブなデータ分析ダッシュボード
- 成長の可能性が高い機会のための企業分析ダッシュボード
- カスタマイズとクエリのためのリサーチアナリストアクセス
- インタラクティブなダッシュボードによる競合分析
- 最新ニュース、更新情報、トレンド分析
- 包括的な競合追跡のためのベンチマーク分析のパワーを活用
調査方法
データ収集と基準年分析は、大規模なサンプル サイズのデータ収集モジュールを使用して行われます。この段階では、さまざまなソースと戦略を通じて市場情報または関連データを取得します。過去に取得したすべてのデータを事前に調査および計画することも含まれます。また、さまざまな情報ソース間で見られる情報の不一致の調査も含まれます。市場データは、市場統計モデルと一貫性モデルを使用して分析および推定されます。また、市場シェア分析と主要トレンド分析は、市場レポートの主要な成功要因です。詳細については、アナリストへの電話をリクエストするか、お問い合わせをドロップダウンしてください。
DBMR 調査チームが使用する主要な調査方法は、データ マイニング、データ変数が市場に与える影響の分析、および一次 (業界の専門家) 検証を含むデータ三角測量です。データ モデルには、ベンダー ポジショニング グリッド、市場タイムライン分析、市場概要とガイド、企業ポジショニング グリッド、特許分析、価格分析、企業市場シェア分析、測定基準、グローバルと地域、ベンダー シェア分析が含まれます。調査方法について詳しくは、お問い合わせフォームから当社の業界専門家にご相談ください。
カスタマイズ可能
Data Bridge Market Research は、高度な形成的調査のリーダーです。当社は、既存および新規のお客様に、お客様の目標に合致し、それに適したデータと分析を提供することに誇りを持っています。レポートは、対象ブランドの価格動向分析、追加国の市場理解 (国のリストをお問い合わせください)、臨床試験結果データ、文献レビュー、リファービッシュ市場および製品ベース分析を含めるようにカスタマイズできます。対象競合他社の市場分析は、技術ベースの分析から市場ポートフォリオ戦略まで分析できます。必要な競合他社のデータを、必要な形式とデータ スタイルでいくつでも追加できます。当社のアナリスト チームは、粗い生の Excel ファイル ピボット テーブル (ファクト ブック) でデータを提供したり、レポートで利用可能なデータ セットからプレゼンテーションを作成するお手伝いをしたりすることもできます。