コンテンツライセンス市場における電子臨床アウトカム評価(eCOA)の世界規模、シェア、トレンド分析レポート
Market Size in USD Billion
CAGR :
% 
 USD
543.06 Million
USD
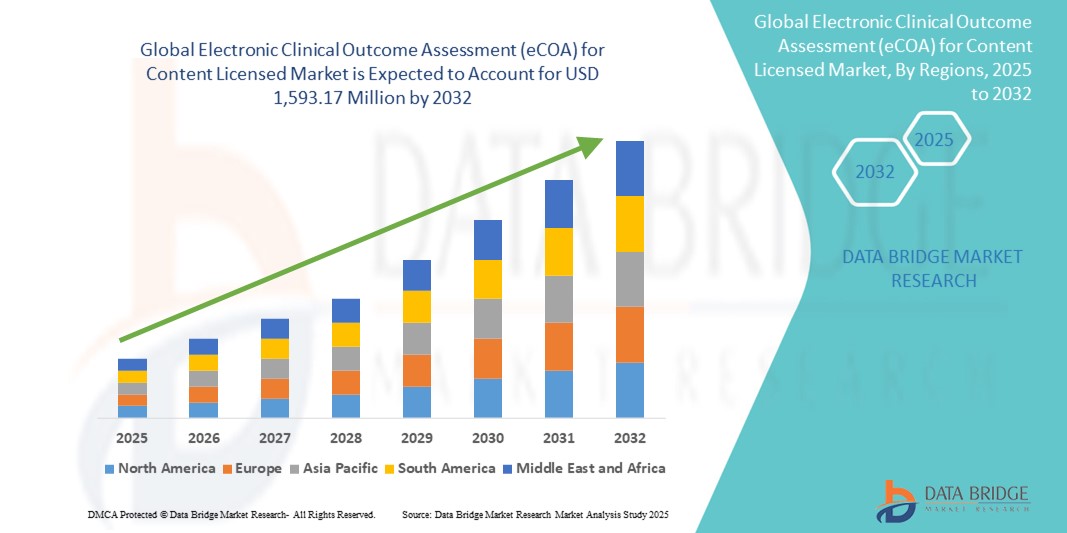
1,593.17 Million
2024
2032
USD
543.06 Million
USD
1,593.17 Million
2024
2032
| 2025 –2032 | |
| USD 543.06 Million | |
| USD 1,593.17 Million | |
|
|
|
|
コンテンツライセンス市場におけるグローバル電子臨床アウトカムアセスメント(eCOA)のセグメンテーション、製品別(オンプレミスソリューション、クラウドベースソリューション、ウェブベースソリューション)、アプローチ別(臨床医報告アウトカムアセスメント(ClinRO)、患者報告アウトカムアセスメント(PRO)、観察者報告アウトカムアセスメント(ObsRO)、パフォーマンスアウトカムアセスメント(PerfO))、エンドユーザー別(商業サービスプロバイダー、病院および移植センター、研究機関および学術機関)、プラットフォーム別(開発業務委託機関、製薬およびバイオ医薬品企業、医療機器メーカー、病院および臨床検査機関、コンサルティングサービス企業、研究機関および学術機関、その他) - 2032年までの業界動向および予測
コンテンツライセンス市場規模における電子臨床アウトカム評価(eCOA)
- コンテンツライセンス市場規模の世界的な電子臨床アウトカム評価(eCOA)は、2024年に5億4,306万米ドルと評価され、予測期間中に14.40%のCAGRで 成長し 、2032年までに15億9,317万米ドルに達すると予想されています。
- 市場の成長は、臨床試験におけるデジタル変革の需要の高まりと、試験の品質とコンプライアンスを向上させるリアルタイムの患者中心のデータ収集への重点の高まりによって主に推進されています。
- さらに、規制当局による支援の拡大と、標準化・検証済みのeCOAコンテンツの製薬業界における採用の増加により、ライセンス供与されたeCOAソリューションは、臨床エンドポイントの取得における優先的な方法として位置づけられています。これらの要因が相まって、ライセンス供与されたeCOAツールの普及が加速し、業界の成長を大きく後押ししています。
コンテンツライセンス市場分析のための電子臨床アウトカム評価(eCOA)
- 患者報告、臨床医報告、観察者報告の結果をデジタルで取得するライセンス取得済みのeCOAソリューションは、データの精度の向上、リアルタイムアクセス、分散型試験モデルとの互換性により、現代の臨床研究に不可欠なツールになりつつあります。
- ライセンス供与されたeCOAコンテンツの需要の高まりは、主に臨床試験の複雑化、標準化され検証されたデータ収集方法に対する規制の重視、製薬会社やバイオテクノロジー会社によるデジタルヘルスプラットフォームの採用の増加によって促進されています。
- 北米は、強力な規制インフラ、デジタル臨床技術の早期導入、主要な臨床研究組織とeCOAソリューションプロバイダーの存在により、2024年にコンテンツライセンス市場の電子臨床アウトカム評価(eCOA)で最大の収益シェア46.8%を獲得し、市場をリードしました。
- アジア太平洋地域は、臨床研究活動の拡大、規制の調和、患者中心のデータ収集への関心の高まりにより、予測期間中にコンテンツライセンス市場の電子臨床アウトカム評価(eCOA)で最も急速に成長する地域になると予想されています。
- 患者報告アウトカム評価(PRO)セグメントは、治療効果と患者の健康状態を評価する上で重要な役割を果たし、試験プロトコルにおける患者の直接的な意見の収集に重点が置かれていることから、2024年にはコンテンツライセンス市場の電子臨床アウトカム評価(eCOA)のシェアを50.2%で占めました。
コンテンツライセンス市場のセグメンテーションに関するレポートの範囲と電子臨床結果評価(eCOA)
|
属性 |
コンテンツライセンスの主要市場インサイトのための電子臨床アウトカム評価(eCOA) |
|
対象セグメント |
|
|
対象国 |
北米
ヨーロッパ
アジア太平洋
中東およびアフリカ
南アメリカ
|
|
主要な市場プレーヤー |
|
|
市場機会 |
|
|
付加価値データ情報セット |
データブリッジマーケットリサーチがまとめた市場レポートには、市場価値、成長率、セグメンテーション、地理的範囲、主要プレーヤーなどの市場シナリオに関する洞察に加えて、専門家による詳細な分析、価格設定分析、ブランドシェア分析、消費者調査、人口統計分析、サプライチェーン分析、バリューチェーン分析、原材料/消耗品の概要、ベンダー選択基準、PESTLE分析、ポーター分析、規制の枠組みも含まれています。 |
コンテンツライセンス市場における電子臨床アウトカム評価(eCOA)の動向
「臨床試験におけるデジタル標準化とAI主導の強化」
- コンテンツライセンス市場におけるeCOAの世界的な重要かつ進化するトレンドの一つは、人工知能(AI)と標準化されたデジタルコンテンツの統合です。これにより、臨床試験におけるデータ品質、規制遵守、そして患者エンゲージメントが向上します。この融合により、データ収集が効率化され、試験の効率が向上します。
- 例えば、Medidata SolutionsやERTなどの企業は、AIを活用したライセンス供与されたeCOAソリューションを提供しており、患者の入力内容をリアルタイムでモニタリングし、予測分析によって試験結果の予測精度を向上させることができます。AI対応プラットフォームは、データの異常を検出し、再検証を促し、適応型の試験設計をサポートします。
- ライセンス供与されたeCOAコンテンツは、患者報告、医師報告、観察者報告のすべてのアウトカムが規制および科学基準を満たすことを保証し、多国籍研究における一貫性と信頼性を促進します。これらのコンテンツライセンスは、高度なeCOAプラットフォームとバンドルされ、ターンキーソリューションを提供することが増えています。
- eConsentプラットフォームやウェアラブルデバイスとの統合により、データ取得ワークフローの自動化により、患者のコンプライアンスがさらに向上し、医療機関の負担が軽減されます。例えば、Signant Healthは、認可されたPRO指標をウェアラブルデバイスの生体データと連携させることで、治療効果をより包括的に把握することを可能にします。
- AI対応eCOAプラットフォームにおけるデジタル化・検証済みコンテンツへのトレンドは、関係者によるグローバル臨床試験の実施・管理方法に変革をもたらしています。その結果、IQVIAやKayentisといった企業は、ユーザーフレンドリーでAI強化されたプラットフォームに組み込まれた、拡張性の高い多言語ライセンスコンテンツライブラリへの投資を行っています。
- スポンサーやCROがインテリジェントなデジタルツールを通じて試験のリスクを軽減し、患者体験とデータの正確性の両方を向上させようとしているため、事前承認された規制準拠コンテンツを備えたeCOAソリューションの需要が急速に高まっています。
コンテンツライセンス市場の動向に関する電子臨床アウトカム評価(eCOA)
ドライバ
「臨床研究における規制上の要求の高まりとデジタルシフト」
- 臨床試験におけるデータ標準化と規制遵守への重点の高まりと、臨床研究プロセスのデジタル変革は、ライセンスされたeCOAコンテンツ市場の主な推進力となっています。
- 例えば、2024年3月、Clinical Inkは、グローバルな試験向けにライセンス供与された、事前検証済みのeCOA機器群を発売しました。これにより、セットアップ時間の効率化と規制リスクの軽減が実現しました。こうした取り組みは、業界が検証済みのデジタルデータ取得手法を推進していることを浮き彫りにしています。
- 治験スポンサーと規制当局は患者中心の成果と堅牢なエビデンスの生成を優先するため、ライセンスを受けたeCOA機器は、規制当局の期待を満たす科学的に検証された方法論を提供し、治験承認やデータ提出の遅延を軽減します。
- 分散型およびハイブリッド型の臨床試験への移行が進むにつれ、多様な地域や集団にわたって一貫した患者データ収集を保証するデジタルツールの需要も高まっています。デジタルプラットフォームに統合されたライセンスコンテンツは、拡張性とコンプライアンスの両方を向上させます。
- さらに、モバイルデバイスを通じたeCOAツールへのアクセス性の向上、直感的なインターフェース、多言語サポートの組み合わせにより、世界中の試験参加者の間での導入が促進され、患者のエンゲージメントとデータの信頼性の向上に貢献しています。
抑制/挑戦
「複雑なライセンスモデルと統合の障壁」
- ライセンス供与されたeCOAコンテンツの導入における主要な課題の一つは、ライセンス契約と臨床システムへの統合の複雑さです。複数の利害関係者、高額な費用、そして地域ごとの規制の違いにより、導入が遅れたり複雑化したりする可能性があります。
- 例えば、EQ-5DやSF-36などの特定の標準化されたPROのライセンスを取得するには、特に多国間の試験で使用される場合、コンテンツ所有者との複雑な交渉が必要になる可能性があり、プロジェクトのスケジュールとコストが増加します。
- さらに、ライセンスされたコンテンツを既存の電子データキャプチャ(EDC)またはeSourceプラットフォームに統合するには、多くの場合、カスタム開発またはミドルウェアが必要となり、技術的な遅延や運用上の負担の増加につながる可能性があります。
- ライセンスを受けたeCOA機器とスポンサー/CROシステム間の相互運用性を確保することは、特に多様なデバイス、試験設定、患者集団を管理する際に技術的なハードルとして残っています。
- 検証済みコンテンツライブラリの初期費用と継続的なライセンス料が高いため、予算が限られている小規模バイオテクノロジー企業や学術研究者による導入が妨げられる可能性もあります。
- 統一されたライセンスフレームワーク、クラウドベースの展開モデル、ユーザーフレンドリーな統合ツールを通じてこれらの障壁を克服することは、将来の臨床研究においてライセンスされたeCOAコンテンツの使用を拡大する上で非常に重要になります。
コンテンツライセンス市場向け電子臨床アウトカム評価(eCOA)スコープ
市場は、製品、アプローチ、エンドユーザー、プラットフォームに基づいてセグメント化されています。
- 製品別
製品別に見ると、コンテンツライセンス市場向けの電子臨床アウトカム評価(eCOA)は、オンプレミス型ソリューション、クラウドベースソリューション、ウェブベースソリューションに分類されます。クラウドベースソリューションは、その拡張性、導入の容易さ、そして分散型およびハイブリッド型の臨床試験への対応力により、2024年には最大の市場収益シェアを獲得し、市場を席巻しました。スポンサーやCROは、リアルタイムのデータキャプチャ、リモートアクセス、そして他のeClinicalシステムとのシームレスな統合を提供しながら、インフラコストとITの複雑さを軽減できるため、クラウドベースのeCOAプラットフォームをますます好むようになっています。
ウェブベースのソリューションセグメントは、インターネット普及率の向上、世界的な試験の拡大、そして最小限の設定でブラウザからアクセス可能なプラットフォームへの需要に牽引され、2025年から2032年にかけて最も高い成長率を示すと予想されています。ウェブベースのeCOAツールは、地域やデバイスの種類を問わず、患者と試験実施機関に幅広いアクセスを提供し、多国籍研究における導入を促進します。
- アプローチ別
コンテンツライセンス市場における電子臨床アウトカム評価(eCOA)は、アプローチに基づいて、臨床医報告アウトカム評価(ClinRO)、患者報告アウトカム評価(PRO)、観察者報告アウトカム評価(ObsRO)、パフォーマンスアウトカム評価(PerfO)に分類されます。患者報告アウトカム(PRO)セグメントは、規制当局が臨床研究における患者の視点の考慮をますます義務付けているため、2024年には50.2%という最大の収益シェアで市場を席巻しました。ライセンス供与されたPRO機器は、患者の視点から生活の質、症状、治療効果を評価するための検証済み・標準化された手法を提供し、より強力な臨床エビデンスと規制当局への申請に貢献します。
パフォーマンスアウトカム評価(PerfO)セグメントは、臨床試験における客観的評価と機能的評価の需要増加により、2025年から2032年にかけて最も高い成長率を示すと予想されています。PerfOツールは、患者がデジタルデバイスやウェアラブルデバイスなどを用いて行うタスクに基づいてリアルタイムデータを取得し、より正確な有効性評価と試験エンドポイントをサポートします。
- エンドユーザー別
エンドユーザー別に見ると、コンテンツライセンス市場における電子臨床アウトカム評価(eCOA)は、商業サービスプロバイダー、病院・移植センター、研究機関、学術機関に分類されます。商業サービスプロバイダーセグメントは、2024年に最大のシェアを占めました。これは、契約研究機関(CRO)、データマネジメント企業、テクノロジープロバイダーによるeCOAプラットフォームの広範な利用が牽引したためです。これらのサービスプロバイダーは、スポンサーと臨床施設の間の仲介役として機能し、ライセンスコンテンツソリューションを大規模に実装し、試験プロトコルと国際基準への準拠を確保します。
学術機関セグメントは、学術機関主導の研究イニシアチブの増加、デジタル臨床ツールへの資金提供の拡大、そして業界パートナーとの共同試験の増加を背景に、2025年から2032年にかけて最も高い成長率を示すと予想されています。学術研究においてライセンスコンテンツを備えたeCOAツールを導入することで、データの精度と再現性が向上します。
- プラットフォーム別
プラットフォーム別に見ると、コンテンツライセンス市場向けの電子臨床アウトカム評価(eCOA)は、開発業務受託機関(CRO)、製薬・バイオ医薬品企業、医療機器メーカー、病院・臨床検査室、コンサルティングサービス企業、研究・学術機関、その他に分類されます。2024年には、製薬・バイオ医薬品企業セグメントが市場を席巻しました。これらの企業は、世界の臨床試験の大部分を主導し、患者中心のアウトカムを実現するために、検証済みで規制に準拠したeCOAソリューションを必要としているからです。ライセンスコンテンツへの投資は、試験の効率性、世界的な一貫性、そして規制当局の承認を向上させます。
臨床開発におけるアウトソーシングのトレンドに支えられ、2025年から2032年にかけて、契約研究機関(CRO)セグメントは最も急速な成長を遂げると予測されています。CROは、統合ライセンスコンテンツを備えたターンキーeCOAプラットフォームを導入するケースが増えており、特に標準化されたアウトカム指標が不可欠な複数国にまたがる試験において、スポンサーにエンドツーエンドの試験管理サービスを提供しています。
コンテンツライセンス市場における電子臨床アウトカム評価(eCOA)の地域分析
- 北米は、強力な規制インフラ、デジタル臨床技術の早期導入、主要な臨床研究組織とeCOAソリューションプロバイダーの存在により、2024年にコンテンツライセンス市場の電子臨床アウトカム評価(eCOA)で最大の収益シェア46.8%を獲得し、市場をリードしました。
- 製薬会社、CRO、学術機関を含むこの地域の利害関係者は、FDAとEMAの期待を満たすために検証済みの標準化された成果指標の使用を優先しており、ライセンスを受けたeCOAソリューションの需要が高まっています。
- この地域の優位性は、多額の研究開発投資、高度なeClinicalエコシステム、分散型およびハイブリッド試験の増加によってさらに支えられており、ライセンスされたeCOAコンテンツは、現代の臨床試験におけるデータの正確性、コンプライアンス、患者の関与を確保するための重要な要素として確立されています。
コンテンツライセンス市場洞察のための米国電子臨床アウトカム評価(eCOA)
米国のコンテンツライセンス市場における電子臨床アウトカム評価(eCOA)は、2024年に北米最大の収益シェア(79.5%)を獲得しました。これは、臨床試験活動における米国のリーダーシップと、標準化されたアウトカム指標への規制遵守が牽引役となっています。FDAによる患者中心の医薬品開発と検証済みのPROツールの推進は、ライセンス供与されたeCOAツールの普及を継続的に促進しています。さらに、分散型試験の普及と、スポンサーおよびCROによるデジタルヘルス技術の急速な導入は、ライセンス供与され規制に準拠したコンテンツが組み込まれたeCOAプラットフォームの需要をさらに押し上げています。
欧州電子臨床アウトカム評価(eCOA)コンテンツライセンス市場インサイト
欧州におけるコンテンツライセンス市場向けの電子臨床アウトカム評価(eCOA)は、予測期間を通じて大幅なCAGRで拡大すると予測されています。これは主に、EMA(欧州医薬品庁)に基づく欧州の規制調和と、患者中心の研究への投資増加によるものです。複数国にまたがる試験の増加と、多言語対応で検証済みのPROおよびObsROコンテンツへの需要が、eCOAの導入を促進しています。同意取得やアウトカム評価を含む臨床試験のあらゆる側面のデジタル化への傾向は、治療領域および臨床研究ネットワーク全体にわたる市場拡大を支えています。
英国電子臨床アウトカム評価(eCOA)コンテンツライセンス市場インサイト
英国のコンテンツライセンス市場における電子臨床アウトカム評価(eCOA)は、NHS(国民保健サービス)が支援するデジタルヘルスイニシアチブとリアルワールドエビデンス創出への注力に支えられ、予測期間中に注目すべきCAGRで成長すると予想されています。標準化されたデジタル形式で患者のアウトカムを記録することへの注力は、製薬会社や研究機関によるライセンス供与されたeCOA機器への投資を促しています。さらに、強力な学術研究エコシステムと全国的な臨床試験への積極的な参加が、eCOAの普及を促進しています。
ドイツ電子臨床アウトカム評価eCOA コンテンツライセンス市場洞察
ドイツのコンテンツライセンス市場における電子臨床アウトカム評価(eCOA)は、予測期間中、同国が規制遵守、臨床データの品質、そしてデジタルヘルスケアにおけるイノベーションを重視していることから、大幅なCAGRで拡大すると予想されています。ドイツの製薬業界と医療技術業界は、特に腫瘍学および希少疾患の臨床試験において、検証済みのeCOAコンテンツを早期に導入しています。同国の精密医療とデータプライバシーへの取り組みは、安全で標準化されたアウトカムキャプチャを提供するライセンス供与されたeCOAソリューションと密接に連携しています。
アジア太平洋地域における電子臨床アウトカム評価(eCOA)コンテンツライセンス市場インサイト
アジア太平洋地域のコンテンツライセンス市場における電子臨床アウトカム評価(eCOA)は、新興国における臨床試験活動の急増とデジタルヘルスインフラへの投資増加を背景に、2025年から2032年の予測期間中に23.2%という最も高いCAGRで成長すると見込まれています。中国、日本、インドなどの国々では、グローバル試験への参加、ライセンスコンテンツのローカライズ、そして患者中心の多言語eCOAソリューションに対するニーズの高まりにより、eCOAの導入が加速しています。
日本における電子臨床アウトカム評価(eCOA)コンテンツライセンス市場インサイト
日本のコンテンツライセンス市場における電子臨床アウトカム評価(eCOA)は、医療イノベーション、高齢者ケア、そして厳格な規制監督への日本の重点的な取り組みにより、急速に成長しています。日本の製薬会社は、後期試験および市販後調査における質の高いデータを確保するため、ライセンス供与されたPROおよびClinROツールを導入しています。eCOAシステムをより広範なeClinicalプラットフォームやIoT医療機器と統合することで、患者エンゲージメントとアウトカムモニタリングの強化が期待されます。
インドにおける電子臨床アウトカム評価(eCOA)コンテンツライセンス市場インサイト
インドのコンテンツライセンス市場における電子臨床アウトカム評価(eCOA)は、2024年にアジア太平洋地域最大の市場収益シェアを占めました。これは、同国における臨床試験環境の拡大、急速なデジタル変革、そしてCROによる費用対効果の高いサービス提供によるものです。政府主導の医療デジタル化と国内のeClinicalテクノロジープロバイダーの台頭により、ライセンス供与されたeCOAツールの導入が加速しています。インドの多言語人口と多様な医療環境も、地域の試験ニーズに合わせて調整された柔軟で検証済みのコンテンツに対する需要を促進しています。
コンテンツライセンス市場シェアの電子臨床アウトカム評価(eCOA)
コンテンツ ライセンス業界向けの電子臨床結果評価 (eCOA) は、主に次のような定評のある企業によって主導されています。
- メディデータソリューションズ社(米国)
- シグナント・ヘルス(米国)
- IQVIA Inc.(米国)
- YPrime, Inc.(米国)
- クラリオ(米国)
- Clinical Ink, Inc.(米国)
- ERT社(米国)
- カイエンティスSAS(フランス)
- Veeva Systems Inc.(米国)
- オラクル・ヘルス・サイエンス(米国)
- パレクセルインターナショナルコーポレーション(米国)
- eResearch Technology, Inc.(米国)
- アリスグローバルLLC(米国)
- Calyx(米国)
- カストルEDC(オランダ)
- Datatrak International, Inc.(米国)
- メドリオ社(米国)
- OpenClinica LLC(米国)
- トライアル・バイ・ファイア・ソリューションズLLC(米国)
コンテンツライセンス市場における世界的な電子臨床結果評価 (eCOA) の最近の動向は何ですか?
- 2024年5月、ダッソー・システムズ傘下のメディデータ・ソリューションズは、myMedidataプラットフォームの拡張版をリリースしました。このバージョンでは、グローバルな試験におけるライセンス供与された臨床アウトカム評価のサポートが拡張されています。このアップデートには、eConsentやウェアラブルデータとシームレスに統合された、多言語対応の検証済みeCOAツールが含まれており、分散型の試験実施を効率化します。このリリースは、メディデータが、治療領域全体にわたって患者エンゲージメントとデータインテグリティを向上させる、統合型で規制に準拠したソリューションを提供するというコミットメントを強化するものです。
- 2024年4月、Signant Healthは、複数のPRO指標ライセンサーとの新たな契約を通じて、ライセンスコンテンツライブラリの拡張を発表しました。これにより、特に腫瘍学および中枢神経系研究において、eCOAプラットフォーム内で標準化されたアウトカム指標をより迅速に展開できるようになります。この開発は、Signantが検証済みデータ取得能力を強化し、グローバル試験のセットアップ時間を短縮するという戦略を裏付けています。
- 2024年3月、IQVIAは、リアルワールド研究および臨床研究におけるデータ収集を最適化するために、ライセンス供与されたPROと統合されたAI強化eCOAスイートを発表しました。このプラットフォームは、予測分析とインテリジェントな患者プロンプトを用いて、回答率の向上とデータギャップの最小化を実現します。これは、デジタル試験におけるイノベーションと規制遵守へのIQVIAの注力を反映しています。
- 2024年2月、YPrimeは複数の学術機関と提携し、希少疾患試験向けの承認済みeCOAソリューションを提供することで、試験開始の迅速化と規制遵守の向上に貢献しました。この提携により、入手困難なアウトカム指標への幅広いアクセスが可能になり、十分なサービスが提供されていない治療領域における研究能力の拡大に対するYPrimeのコミットメントが強調されます。
- Clinical Inkは2024年1月、分散型試験での使用を目的とした、検証済み・ライセンス取得済みのeCOA機器へのターンキーアクセスを提供する新たなデジタルプラットフォームを立ち上げました。グローバル展開を簡素化するために設計されたこのソリューションには、組み込みの翻訳機能と自動コンプライアンス追跡機能が含まれており、eCOA導入をより効率的かつ拡張可能にし、進化する規制要件に適合させるという同社の目標を反映しています。
SKU-
世界初のマーケットインテリジェンスクラウドに関するレポートにオンラインでアクセスする
- インタラクティブなデータ分析ダッシュボード
- 成長の可能性が高い機会のための企業分析ダッシュボード
- カスタマイズとクエリのためのリサーチアナリストアクセス
- インタラクティブなダッシュボードによる競合分析
- 最新ニュース、更新情報、トレンド分析
- 包括的な競合追跡のためのベンチマーク分析のパワーを活用
調査方法
データ収集と基準年分析は、大規模なサンプル サイズのデータ収集モジュールを使用して行われます。この段階では、さまざまなソースと戦略を通じて市場情報または関連データを取得します。過去に取得したすべてのデータを事前に調査および計画することも含まれます。また、さまざまな情報ソース間で見られる情報の不一致の調査も含まれます。市場データは、市場統計モデルと一貫性モデルを使用して分析および推定されます。また、市場シェア分析と主要トレンド分析は、市場レポートの主要な成功要因です。詳細については、アナリストへの電話をリクエストするか、お問い合わせをドロップダウンしてください。
DBMR 調査チームが使用する主要な調査方法は、データ マイニング、データ変数が市場に与える影響の分析、および一次 (業界の専門家) 検証を含むデータ三角測量です。データ モデルには、ベンダー ポジショニング グリッド、市場タイムライン分析、市場概要とガイド、企業ポジショニング グリッド、特許分析、価格分析、企業市場シェア分析、測定基準、グローバルと地域、ベンダー シェア分析が含まれます。調査方法について詳しくは、お問い合わせフォームから当社の業界専門家にご相談ください。
カスタマイズ可能
Data Bridge Market Research は、高度な形成的調査のリーダーです。当社は、既存および新規のお客様に、お客様の目標に合致し、それに適したデータと分析を提供することに誇りを持っています。レポートは、対象ブランドの価格動向分析、追加国の市場理解 (国のリストをお問い合わせください)、臨床試験結果データ、文献レビュー、リファービッシュ市場および製品ベース分析を含めるようにカスタマイズできます。対象競合他社の市場分析は、技術ベースの分析から市場ポートフォリオ戦略まで分析できます。必要な競合他社のデータを、必要な形式とデータ スタイルでいくつでも追加できます。当社のアナリスト チームは、粗い生の Excel ファイル ピボット テーブル (ファクト ブック) でデータを提供したり、レポートで利用可能なデータ セットからプレゼンテーションを作成するお手伝いをしたりすることもできます。