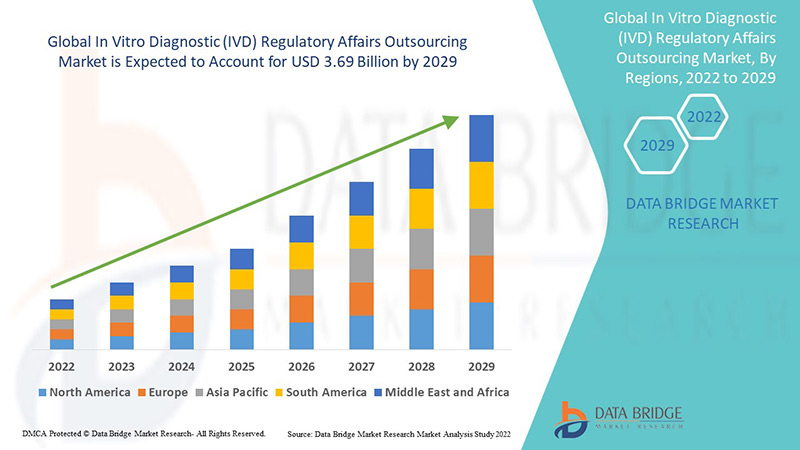
Global In Vitro Diagnostic Ivd Regulatory Affairs Outsourcing Market
Tamanho do mercado em biliões de dólares
CAGR :
% 
 USD
674,277.97 Thousand
USD
1,830,957.45 Thousand
2021
2029
USD
674,277.97 Thousand
USD
1,830,957.45 Thousand
2021
2029
| 2022 –2029 | |
| USD 674,277.97 Thousand | |
| USD 1,830,957.45 Thousand | |
|
|
|
|
Mercado global de terceirização de assuntos regulatórios para diagnóstico in vitro (IVD), por serviço (redação e submissões regulatórias, registro regulatório e aplicações para ensaios clínicos , consultoria regulatória, representação legal, serviços de gerenciamento de dados, serviços de fabricação e controle de produtos químicos (CMC) e outros), indicação (oncologia, neurologia, cardiologia, química clínica e imunoensaios, medicina de precisão, doenças infecciosas, diabetes, testes genéticos, HIV/AIDS, hematologia, testes de drogas/farmacogenômica, transfusão de sangue, ponto de atendimento e outros), modo de implantação (nuvem e local), tamanho da organização (pequenas e médias empresas (PMEs) e grandes empresas), estágio (clínico, pré-clínico e PMA (autorização pós-mercado)), classe (classe I, classe II e classe III), usuário final (empresas farmacêuticas, empresas de dispositivos médicos, empresas de biotecnologia e outras) - tendências do setor e previsão para 2029
Análise e Tamanho do Mercado
As empresas de saúde enfrentaram desafios para se manterem em dia com os padrões regulatórios, especialmente devido à pandemia de COVID-19 (coronavírus). Para promover uma cultura de qualidade para empresas de tecnologia médica, as empresas de consultoria utilizam softwares de sistema de gestão da qualidade (SGQ). Empresas envolvidas na terceirização de assuntos regulatórios para diagnóstico in vitro (DIV) fornecem suporte baseado em projetos para organizações de saúde.
A implantação da terceirização está resultando no início de contratos de terceirização de longo prazo. O mercado global de terceirização de assuntos regulatórios para diagnóstico in vitro (IVD) foi avaliado em US$ 1,6 bilhão em 2021 e deve atingir US$ 3,69 bilhões até 2029, registrando um CAGR de 11% durante o período previsto de 2022-2029. Espera-se que as empresas farmacêuticas testemunhem um alto crescimento devido ao aumento no número de aprovações clínicas.
Definição de Mercado
Assuntos regulatórios desempenham um papel crucial na indústria de dispositivos de diagnóstico in vitro (IVD). Esses assuntos envolvem o ciclo de vida de diversos produtos para a saúde e oferecem suporte e direcionamento estratégico, tático e operacional para que as empresas de manufatura trabalhem dentro da estrutura regulatória.
Escopo do Relatório e Segmentação de Mercado
|
Métrica de Relatório |
Detalhes |
|
Período de previsão |
2022 a 2029 |
|
Ano base |
2021 |
|
Anos Históricos |
2020 (personalizável para 2019 - 2014) |
|
Unidades quantitativas |
Receita em milhões de dólares americanos, volumes em unidades, preços em dólares americanos |
|
Segmentos abrangidos |
Serviço (Redação e Submissões Regulatórias, Registro Regulatório e Aplicações para Ensaios Clínicos, Consultoria Regulatória, Representação Legal, Serviços de Gerenciamento de Dados, Serviços de Fabricação e Controles Químicos (CMC) e Outros), Indicação (Oncologia, Neurologia, Cardiologia, Química Clínica e Imunoensaios, Medicina de Precisão, Doenças Infecciosas, Diabetes, Testes Genéticos, HIV/AIDS, Hematologia, Testes de Medicamentos/Farmacogenômica, Transfusão de Sangue, Ponto de Atendimento e Outros), Modo de Implantação (Nuvem e Local), Tamanho da Organização (Pequenas e Médias Empresas (PMEs) e Grandes Empresas), Estágio (Clínico, Pré-clínico e PMA (Autorização Pós-Comercialização)), Classe (Classe I, Classe II e Classe III), Usuário Final (Empresas Farmacêuticas, Empresas de Dispositivos Médicos, Empresas de Biotecnologia e Outras) |
|
Países abrangidos |
EUA, Canadá e México na América do Norte, Alemanha, França, Reino Unido, Holanda, Suíça, Bélgica, Rússia, Itália, Espanha, Turquia, Resto da Europa na Europa, China, Japão, Índia, Coreia do Sul, Cingapura, Malásia, Austrália, Tailândia, Indonésia, Filipinas, Resto da Ásia-Pacífico (APAC) na Ásia-Pacífico (APAC), Arábia Saudita, Emirados Árabes Unidos, África do Sul, Egito, Israel, Resto do Oriente Médio e África (MEA) como parte do Oriente Médio e África (MEA), Brasil, Argentina e Resto da América do Sul como parte da América do Sul. |
|
Participantes do mercado cobertos |
Freyr Solutions (Índia), PPD Inc. (EUA), EMERGO (EUA), ICON (Saúde), Parexel International Corporation (EUA), CRITERIUM, INC. (EUA), Groupe ProductLife SA (França), Labcorp Drug Development (EUA), WuXi AppTec (China), Genpact (EUA), Medpace (EUA), Dor Pharmaceutical Services (Israel), Qserve (Holanda), entre outros |
|
Oportunidades de mercado |
|
Dinâmica de mercado de terceirização de assuntos regulatórios para diagnóstico in vitro (IVD)
Esta seção aborda a compreensão dos impulsionadores, vantagens, oportunidades, restrições e desafios do mercado. Tudo isso é discutido em detalhes a seguir:
- Alto uso na indústria da saúde
O aumento da implantação de serviços de terceirização no setor da saúde atua como um dos principais fatores que impulsionam o crescimento do mercado de terceirização de assuntos regulatórios para diagnóstico in vitro (IVD). O aumento nas atividades de expansão geográfica, visando aprovações rápidas em mercados locais, contribui ainda mais para o crescimento.
- Pesquisa e Desenvolvimento
O aumento nas atividades de pesquisa e desenvolvimento, aumentando o volume de solicitações de ensaios clínicos e registros de produtos, acelera o crescimento do mercado.
- Aprovações Clínicas
A demanda por terceirização de assuntos regulatórios para diagnóstico in vitro (IVD) está aumentando, visto que as empresas estão sob constante pressão para obter aprovações clínicas oportunas dos órgãos reguladores. A demanda por serviços de assuntos regulatórios está aumentando devido a essas ações.
Oportunidades
Além disso, o desenvolvimento de biomarcadores e testes específicos para doenças e a importância dos diagnósticos complementares ampliam oportunidades lucrativas para os participantes do mercado no período previsto de 2022 a 2029. Além disso, o aumento nos investimentos expandirá ainda mais o mercado.
Restrições/Desafios
Por outro lado, espera-se que as mudanças nas regulamentações relativas a dispositivos médicos e à terceirização de assuntos regulatórios para diagnóstico in vitro (IVD) obstruam o crescimento do mercado. Além disso, projeta-se que a falta de infraestrutura nos serviços de saúde desafie o mercado de terceirização de assuntos regulatórios para diagnóstico in vitro (IVD) no período previsto de 2022 a 2029.
Este relatório de mercado de terceirização de assuntos regulatórios para diagnóstico in vitro (IVD) fornece detalhes sobre novos desenvolvimentos recentes, regulamentações comerciais, análise de importação e exportação, análise de produção, otimização da cadeia de valor, participação de mercado, impacto de participantes do mercado doméstico e local, análise de oportunidades em termos de bolsões de receita emergentes, mudanças nas regulamentações de mercado, análise estratégica de crescimento de mercado, tamanho de mercado, crescimento de mercado por categoria, nichos de aplicação e dominância, aprovações de produtos, lançamentos de produtos, expansões geográficas e inovações tecnológicas no mercado. Para obter mais informações sobre o mercado de terceirização de assuntos regulatórios para diagnóstico in vitro (IVD), entre em contato com a Data Bridge Market Research para um Briefing de Analista. Nossa equipe ajudará você a tomar uma decisão de mercado informada para alcançar o crescimento do mercado.
Impacto da Covid-19 no mercado de testes diagnósticos
A COVID-19 teve um impacto negativo no setor da saúde. Os principais players adaptaram estratégias inovadoras à situação em rápida mudança durante o surto da COVID-19. Os países adotaram mudanças críticas na área da saúde até que a crise ficou em segundo plano. Espera-se que as reformas na área da saúde testemunhem contenção de custos, maior acesso e progresso tecnológico nos próximos anos. Houve um aumento na demanda por terceirização de assuntos regulatórios para diagnóstico in vitro (DIV) devido à ênfase na importância do diagnóstico, atendimento e consulta remotos. Esses serviços reduzem a carga sobre os hospitais no cenário pós-pandemia.
Desenvolvimentos recentes
- A revista de tecnologia USA-9 listou a Freyr entre os "10 Melhores Provedores de Soluções de Tecnologia de 2021" em novembro de 2021. A USA-9.com é uma revista de tecnologia que listou a Freyr Solutions, fornecedora líder global de soluções e serviços regulatórios, entre os "10 Melhores Provedores de Soluções de Tecnologia de 2021", enquanto a Fryer continua a desenvolver soluções de software inovadoras e a apoiar os clientes em seus respectivos objetivos de conformidade. Isso ajudou a empresa a aumentar sua popularidade.
Escopo e tamanho do mercado global de terceirização de assuntos regulatórios para diagnóstico in vitro (IVD)
O mercado de terceirização de assuntos regulatórios para diagnóstico in vitro (IVD) é segmentado com base em serviços, indicação, modo de implantação, porte da organização, estágio, classe e usuário final. O crescimento entre esses segmentos ajudará você a analisar segmentos de crescimento escassos nos setores e fornecerá aos usuários uma visão geral e insights valiosos do mercado para ajudá-los a tomar decisões estratégicas para identificar as principais aplicações de mercado.
Serviços
- Redação e Submissões Regulatórias
- Registro Regulatório e Aplicações de Ensaios Clínicos
- Consultoria Regulatória
- Representação Legal
- Serviços de gerenciamento de dados
- Serviços de Fabricação e Controle de Produtos Químicos (CMC)
- Outros
Com base nos serviços, o mercado global de terceirização de assuntos regulatórios para diagnóstico in vitro (IVD) é segmentado em redação e submissões regulatórias, registro regulatório e solicitações de ensaios clínicos, consultoria regulatória, representação legal, serviços de gerenciamento de dados, serviços de fabricação e controle de produtos químicos (CMC) e outros.
Indicação
- Oncologia
- Neurologia
- Cardiologia
- Química Clínica e Imunoensaios
- Medicina de Precisão
- Doenças Infecciosas
- Diabetes
- Testes genéticos
- HIV/AIDS
- Hematologia
- Teste de drogas/farmacogenômica
- Transfusão de sangue
- Ponto de atendimento
- Outros
Com base na indicação, o mercado global de terceirização de assuntos regulatórios de diagnóstico in vitro (IVD) é segmentado em oncologia, neurologia, cardiologia, química clínica e imunoensaios, medicina de precisão, doenças infecciosas, diabetes, testes genéticos, HIV/AIDS, hematologia, testes de medicamentos/farmacogenômica, transfusão de sangue, ponto de atendimento e outros.
Modo de implantação
- Nuvem
- No local
Com base no modo de implantação, o mercado global de terceirização de assuntos regulatórios de diagnóstico in vitro (IVD) é segmentado em nuvem e local.
Tamanho da organização
- Pequenas e Médias Empresas (PMEs)
- Grandes Empresas
Com base no tamanho da organização, o mercado global de terceirização de assuntos regulatórios de diagnóstico in vitro (IVD) é segmentado em pequenas e médias empresas (PMEs) e grandes empresas.
Estágio
- Clínico
- Pré-clínico
- PMA (Autorização Pós-Comercialização)
Com base no estágio, o mercado global de terceirização de assuntos regulatórios de diagnóstico in vitro (IVD) é segmentado em clínico, pré-clínico e PMA (autorização pós-comercialização).
Aula
- Classe I
- Classe II
- Classe III
Com base na classe, o mercado global de terceirização de assuntos regulatórios de diagnóstico in vitro (IVD) é segmentado em classe I, classe II e classe III.
Usuário final
- Empresas Farmacêuticas
- Empresas de dispositivos médicos
- Empresas de Biotecnologia
- Outros
Com base no usuário final, o mercado global de terceirização de assuntos regulatórios de diagnóstico in vitro (IVD) é segmentado em empresas farmacêuticas, empresas de dispositivos médicos, empresas de biotecnologia e outras.
Análise/Insights Regionais de Mercado de Terceirização de Assuntos Regulatórios para Diagnóstico In Vitro (IVD)
O mercado de terceirização de assuntos regulatórios de diagnóstico in vitro (IVD) é analisado e insights e tendências sobre o tamanho do mercado são fornecidos por país, serviços, indicação, modo de implantação, tamanho da organização, estágio, classe e usuário final, conforme referenciado acima.
Os países abrangidos pelo relatório de mercado de terceirização de assuntos regulatórios de diagnóstico in vitro (IVD) são EUA, Canadá e México na América do Norte, Alemanha, França, Reino Unido, Holanda, Suíça, Bélgica, Rússia, Itália, Espanha, Turquia, Resto da Europa na Europa, China, Japão, Índia, Coreia do Sul, Cingapura, Malásia, Austrália, Tailândia, Indonésia, Filipinas, Resto da Ásia-Pacífico (APAC) na Ásia-Pacífico (APAC), Arábia Saudita, Emirados Árabes Unidos, África do Sul, Egito, Israel, Resto do Oriente Médio e África (MEA) como parte do Oriente Médio e África (MEA), Brasil, Argentina e Resto da América do Sul como parte da América do Sul.
A Ásia-Pacífico (APAC) domina o mercado de terceirização de assuntos regulatórios de diagnóstico in vitro (IVD) devido ao aumento do número de ensaios clínicos e ao número crescente de empresas na região.
Espera-se que a América do Norte testemunhe um crescimento significativo durante o período previsto de 2022 a 2029 devido à presença de importantes empresas farmacêuticas e de dispositivos médicos e ao aumento nos gastos com pesquisa e desenvolvimento na região.
A seção sobre países do relatório também apresenta fatores individuais que impactam o mercado e mudanças na regulamentação do mercado doméstico, que impactam as tendências atuais e futuras do mercado. Pontos de dados como análise da cadeia de valor a montante e a jusante, tendências técnicas, análise das cinco forças de Porter e estudos de caso são alguns dos indicadores utilizados para prever o cenário de mercado para cada país. Além disso, a presença e a disponibilidade de marcas globais e seus desafios enfrentados devido à concorrência forte ou escassa de marcas locais e nacionais, o impacto de tarifas domésticas e rotas comerciais são considerados na análise de previsão dos dados do país.
Crescimento da infraestrutura de saúde Base instalada e penetração de novas tecnologias
O mercado de terceirização de assuntos regulatórios para diagnóstico in vitro (IVD) também oferece análises detalhadas de mercado para o crescimento de cada país nos gastos com equipamentos de capital em saúde, base instalada de diferentes tipos de produtos para o mercado de terceirização de assuntos regulatórios para diagnóstico in vitro (IVD), impacto da tecnologia utilizando curvas de linha de vida e mudanças nos cenários regulatórios para saúde, e seu impacto no mercado de terceirização de assuntos regulatórios para diagnóstico in vitro (IVD). Os dados estão disponíveis para o período histórico de 2010 a 2020.
Análise do cenário competitivo e da participação de mercado em terceirização de assuntos regulatórios para diagnóstico in vitro (IVD)
O cenário competitivo do mercado de terceirização de assuntos regulatórios para diagnóstico in vitro (IVD) fornece detalhes por concorrente. Os detalhes incluem visão geral da empresa, finanças, receita gerada, potencial de mercado, investimento em pesquisa e desenvolvimento, novas iniciativas de mercado, presença global, locais e instalações de produção, capacidades de produção, pontos fortes e fracos da empresa, lançamento de produto, abrangência e amplitude do produto e domínio da aplicação. Os dados acima são apenas referentes ao foco das empresas no mercado de terceirização de assuntos regulatórios para diagnóstico in vitro (IVD).
Alguns dos principais participantes que operam no mercado de terceirização de assuntos regulatórios de diagnóstico in vitro (IVD) são:
- Freyr Solutions (Índia)
- PPD Inc. (EUA)
- EMERGO (EUA)
- ÍCONE (Saúde)
- Parexel International Corporation (EUA)
- CRITERIUM, INC. (EUA)
- Grupo ProductLife SA (França)
- Labcorp Drug Development (EUA)
- WuXi AppTec (China)
- Genpact (EUA)
- Medpace (EUA)
- Dor Pharmaceutical Services (Israel)
- Qserve (Holanda)
SKU-
Obtenha acesso online ao relatório sobre a primeira nuvem de inteligência de mercado do mundo
- Painel interativo de análise de dados
- Painel de análise da empresa para oportunidades de elevado potencial de crescimento
- Acesso de analista de pesquisa para personalização e customização. consultas
- Análise da concorrência com painel interativo
- Últimas notícias, atualizações e atualizações Análise de tendências
- Aproveite o poder da análise de benchmark para um rastreio abrangente da concorrência
Índice
1. INTRODUÇÃO
1.1 OBJETIVOS DO ESTUDO
1.2 DEFINIÇÃO DE MERCADO
1.3 VISÃO GERAL DO MERCADO GLOBAL DE TERCEIRIZAÇÃO DE ASSUNTOS REGULAMENTARES DE DIAGNÓSTICO IN VITRO (IVD)
1.4 MOEDA E PREÇOS
1.5 LIMITAÇÃO
1.6 MERCADOS COBERTOS
2. SEGMENTAÇÃO DE MERCADO
2.1 PRINCIPAIS CONCLUSÕES
2.2 CHEGANDO AO TAMANHO DO MERCADO GLOBAL DE TERCEIRIZAÇÃO DE ASSUNTOS REGULAMENTARES DE DIAGNÓSTICO IN VITRO (IVD)
2.2.1 GRADE DE POSICIONAMENTO DE FORNECEDORES
2.2.2 CURVA DA LINHA DE VIDA DA TECNOLOGIA
2.2.3 MODELAGEM MULTIVARIADA
2.2.4 ANÁLISE DE CIMA PARA BAIXO
2.2.5 PADRÕES DE MEDIÇÃO
2.2.6 ANÁLISE DA PARTICIPAÇÃO DO FORNECEDOR
2.2.7 PONTOS DE DADOS DAS ENTREVISTAS PRIMÁRIAS PRINCIPAIS
2.2.8 PONTOS DE DADOS DE BASES DE DADOS SECUNDÁRIAS PRINCIPAIS
2.3 MERCADO GLOBAL DE TERCEIRIZAÇÃO DE ASSUNTOS REGULAMENTARES DE DIAGNÓSTICO IN VITRO (IVD): RESUMO DA PESQUISA
2.4 PREMISSAS
3. VISÃO GERAL DO MERCADO
3.1 MOTORISTAS
3.2 RESTRIÇÕES
3.3 OPORTUNIDADES
3.4 DESAFIOS
4. INFORMAÇÕES PREMIUM
4.1 ANÁLISE PESTEL
4.2 MODELO DAS CINCO FORÇAS DE PORTER
5. INFORMAÇÕES DO SETOR
5.1 FATORES MICRO E MACRO ECONÔMICOS
5.2 MAPEAMENTO DE PENETRAÇÃO E PERSPECTIVAS DE CRESCIMENTO
5.3 PRINCIPAIS ESTRATÉGIAS DE PREÇOS
5.4 ENTREVISTAS COM ESPECIALISTAS
5.5 ANÁLISE E RECOMENDAÇÃO
6. PORTFÓLIO DE PROPRIEDADE INTELECTUAL (PI)
6.1 QUALIDADE E RESISTÊNCIA DA PATENTE
6.2 FAMÍLIAS DE PATENTES
6.3 LICENCIAMENTO E COLABORAÇÕES
6.4 CENÁRIO COMPETITIVO
6.5 ESTRATÉGIA E GESTÃO DE PI
6.6 OUTROS
7. ANÁLISE DE CUSTOS DETALHADA
8. ROTEIRO DE TECNOLOGIA
9. RASTREADOR DE INOVAÇÃO E ANÁLISE ESTRATÉGICA
9.1 ANÁLISE DE GRANDES NEGÓCIOS E ALIANÇAS ESTRATÉGICAS
9.1.1 JOINT VENTURES
9.1.2 FUSÕES E AQUISIÇÕES
9.1.3 LICENCIAMENTO E PARCERIA
9.1.4 COLABORAÇÕES DE TECNOLOGIA
9.1.5 DESINVESTIMENTOS ESTRATÉGICOS
9.2 NÚMERO DE PRODUTOS EM DESENVOLVIMENTO
9.3 ESTÁGIO DE DESENVOLVIMENTO
9.4 CRONOGRAMAS E MARCOS
9.5 ESTRATÉGIAS E METODOLOGIAS DE INOVAÇÃO
9.6 AVALIAÇÃO E MITIGAÇÃO DE RISCOS
9.7 PERSPECTIVAS FUTURAS
10. CONFORMIDADE REGULAMENTAR
10.1 AUTORIDADES REGULADORAS
10.2 CLASSIFICAÇÕES REGULAMENTARES
10.2.1 CLASSE I
10.2.2 CLASSE II
10.2.3 CLASSE III
10.3 SUBMISSÕES REGULAMENTARES
10.4 HARMONIZAÇÃO INTERNACIONAL
10.5 SISTEMAS DE GESTÃO DA CONFORMIDADE E DA QUALIDADE
10.6 DESAFIOS E ESTRATÉGIAS REGULAMENTARES
11. ESTRUTURA DE REEMBOLSO
12. ANÁLISE DO MAPA DE OPORTUNIDADES
13. DADOS DA BASE INSTALADA
14. ANÁLISE DA CADEIA DE VALOR
15. ECONOMIA DA SAÚDE
15.1 DESPESAS COM SAÚDE
15.2 DESPESAS DE CAPITAL
15.3 TENDÊNCIAS DE CAPEX
15.4 ALOCAÇÃO DE CAPEX
15.5 FONTES DE FINANCIAMENTO
15.6 REFERÊNCIAS DO SETOR
15,7% DO PIB NO PIB TOTAL
15.8 ESTRUTURA DO SISTEMA DE SAÚDE
15.9 POLÍTICAS GOVERNAMENTAIS
15.10 DESENVOLVIMENTO ECONÔMICO
16. MERCADO GLOBAL DE TERCEIRIZAÇÃO DE ASSUNTOS REGULATÓRIOS DE DIAGNÓSTICO IN VITRO (IVD), POR SERVIÇO
16.1 VISÃO GERAL
16.2 REDAÇÃO E SUBMISSÕES REGULAMENTARES
16.3 REGISTRO REGULAMENTAR E PEDIDOS DE ENSAIOS CLÍNICOS
16.4 CONSULTORIA REGULAMENTAR
16.5 REPRESENTAÇÃO LEGAL
16.6 SERVIÇOS DE GESTÃO DE DADOS
16.7 SERVIÇOS DE FABRICAÇÃO E CONTROLES DE PRODUTOS QUÍMICOS (CMC)
16.8 OUTROS
17. MERCADO GLOBAL DE TERCEIRIZAÇÃO DE ASSUNTOS REGULAMENTARES DE DIAGNÓSTICO IN VITRO (IVD), POR INDICAÇÃO
17.1 VISÃO GERAL
17.2 ONCOLOGIA
17.3 NEUROLOGIA
17.4 CARDIOLOGIA
17.5 QUÍMICA CLÍNICA E IMUNOENSAIOS
17.6 MEDICINA DE PRECISÃO
17.7 DOENÇAS INFECCIOSAS
17.7.1 SEPSE
17.7.2 VIROLOGIA
17.7.3 BACTERIOLOGIA
17.7.4 MICROBIOLOGIA E MICOLOGIA
17.7.5 HEPATITE B
17.7.6 HEPATITE C
17.7.7 SÍFILIS
17.7.8 TUBERCULOSE
17.7.9 MALÁRIA
17.7.10 INFECÇÃO POR PAPILOMAVÍRUS HUMANO (HPV)
17.7.11 OUTROS
17.8 DIABETES
17.9 TESTES GENÉTICOS
17.10 HIV/AIDS
17.11 HEMATOLOGIA
17.12 TESTES DE MEDICAMENTOS/FARMACOGENÔMICA
17.13 TRANSFUSÃO DE SANGUE
17.14 OUTROS
18. MERCADO GLOBAL DE TERCEIRIZAÇÃO DE ASSUNTOS REGULATÓRIOS DE DIAGNÓSTICO IN VITRO (IVD), POR ESTÁGIO
18.1 VISÃO GERAL
18.2 PRÉ-CLÍNICO
18.3 CLÍNICA
18.4 PMA (AUTORIZAÇÃO PÓS-COMERCIALIZAÇÃO)
19. MERCADO GLOBAL DE TERCEIRIZAÇÃO DE ASSUNTOS REGULATÓRIOS DE DIAGNÓSTICO IN VITRO (IVD), POR CLASSE
19.1 VISÃO GERAL
19.2 CLASSE I
19.3 CLASSE II
19.4 CLASSE III
20. MERCADO GLOBAL DE TERCEIRIZAÇÃO DE ASSUNTOS REGULATÓRIOS DE DIAGNÓSTICO IN VITRO (IVD), POR TIPO
20.1 VISÃO GERAL
20.2 PRODUTO IVD NO PONTO DE ATENDIMENTO (POC)
20.3 TESTES DESENVOLVIDOS EM LABORATÓRIO (LDTS) PRODUTO IVD
20.4 PRODUTO DE DIAGNÓSTICO IVD COMPANHEIRO
20.5 TESTE DIRETO AO CONSUMIDOR (DTC) DE PRODUTOS IVD
20.6 OUTROS PRODUTOS IVD
21. MERCADO GLOBAL DE TERCEIRIZAÇÃO DE ASSUNTOS REGULAMENTARES DE DIAGNÓSTICO IN VITRO (IVD), POR MODO DE IMPLANTAÇÃO
21.1 VISÃO GERAL
21.2 NUVEM
21.3 NO LOCAL
22. MERCADO GLOBAL DE TERCEIRIZAÇÃO DE ASSUNTOS REGULATÓRIOS DE DIAGNÓSTICO IN VITRO (IVD), POR TAMANHO DA ORGANIZAÇÃO
22.1 VISÃO GERAL
22.2 PEQUENAS E MÉDIAS EMPRESAS (PMEs)
22.3 GRANDES EMPRESAS
23. MERCADO GLOBAL DE TERCEIRIZAÇÃO DE ASSUNTOS REGULAMENTARES DE DIAGNÓSTICO IN VITRO (IVD), POR USUÁRIO FINAL
23.1 VISÃO GERAL
23.2 EMPRESAS FARMACÊUTICAS
23.2.1 POR TAMANHO DA ORGANIZAÇÃO
23.2.1.1. PEQUENAS E MÉDIAS EMPRESAS (PMEs)
23.2.1.2. GRANDES EMPRESAS
23.2.2 POR SERVIÇO
23.2.2.1. REDAÇÃO E SUBMISSÕES REGULAMENTARES
23.2.2.2. REGISTRO REGULAMENTAR E PEDIDOS DE ENSAIOS CLÍNICOS
23.2.2.3. CONSULTORIA REGULAMENTAR
23.2.2.4. REPRESENTAÇÃO LEGAL
23.2.2.5. SERVIÇOS DE GESTÃO DE DADOS
23.2.2.6. SERVIÇOS DE FABRICAÇÃO E CONTROLE DE PRODUTOS QUÍMICOS (CMC)
23.2.2.7. OUTROS
23.3 EMPRESAS DE DISPOSITIVOS MÉDICOS
23.3.1 POR TAMANHO DA ORGANIZAÇÃO
23.3.1.1. PEQUENAS E MÉDIAS EMPRESAS (PMEs)
23.3.1.2. GRANDES EMPRESAS
23.3.2 POR SERVIÇO
23.3.2.1. REDAÇÃO E SUBMISSÕES REGULAMENTARES
23.3.2.2. REGISTRO REGULAMENTAR E PEDIDOS DE ENSAIOS CLÍNICOS
23.3.2.3. CONSULTORIA REGULAMENTAR
23.3.2.4. REPRESENTAÇÃO LEGAL
23.3.2.5. SERVIÇOS DE GESTÃO DE DADOS
23.3.2.6. SERVIÇOS DE FABRICAÇÃO E CONTROLE DE PRODUTOS QUÍMICOS (CMC)
23.3.2.7. OUTROS
23.4 EMPRESAS DE BIOTECNOLOGIA
23.4.1 POR TAMANHO DA ORGANIZAÇÃO
23.4.1.1. PEQUENAS E MÉDIAS EMPRESAS (PMEs)
23.4.1.2. GRANDES EMPRESAS
23.4.2 POR SERVIÇO
23.4.2.1. REDAÇÃO E SUBMISSÕES REGULAMENTARES
23.4.2.2. REGISTRO REGULAMENTAR E PEDIDOS DE ENSAIOS CLÍNICOS
23.4.2.3. CONSULTORIA REGULAMENTAR
23.4.2.4. REPRESENTAÇÃO LEGAL
23.4.2.5. SERVIÇOS DE GESTÃO DE DADOS
23.4.2.6. SERVIÇOS DE FABRICAÇÃO E CONTROLE DE PRODUTOS QUÍMICOS (CMC)
23.4.2.7. OUTROS
23,5 OUTROS
24. MERCADO GLOBAL DE TERCEIRIZAÇÃO DE ASSUNTOS REGULATÓRIOS DE DIAGNÓSTICO IN VITRO (IVD), POR REGIÃO
24.1 MERCADO GLOBAL DE TERCEIRIZAÇÃO DE ASSUNTOS REGULATÓRIOS DE DIAGNÓSTICO IN VITRO (IVD) (TODA A SEGMENTAÇÃO FORNECIDA ACIMA É REPRESENTADA NESTE CAPÍTULO POR PAÍS)
24.1.1 AMÉRICA DO NORTE
24.1.1.1. EUA
24.1.1.2. CANADÁ
24.1.1.3. MÉXICO
24.1.2 EUROPA
24.1.2.1. ALEMANHA
24.1.2.2. FRANÇA
24.1.2.3. Reino Unido
24.1.2.4. ITÁLIA
24.1.2.5. ESPANHA
24.1.2.6. RÚSSIA
24.1.2.7. TURQUIA
24.1.2.8. BÉLGICA
24.1.2.9. PAÍSES BAIXOS
24.1.2.10. SUÍÇA
24.1.2.11. RESTO DA EUROPA
24.1.3 ÁSIA-PACÍFICO
24.1.3.1. JAPÃO
24.1.3.2. CHINA
24.1.3.3. COREIA DO SUL
24.1.3.4. ÍNDIA
24.1.3.5. AUSTRÁLIA
24.1.3.6. SINGAPURA
24.1.3.7. TAILÂNDIA
24.1.3.8. MALÁSIA
24.1.3.9. INDONÉSIA
24.1.3.10. FILIPINAS
24.1.3.11. RESTANTE DA ÁSIA-PACÍFICO
24.1.4 AMÉRICA DO SUL
24.1.4.1. BRASIL
24.1.4.2. ARGENTINA
24.1.4.3. RESTO DA AMÉRICA DO SUL
24.1.5 ORIENTE MÉDIO E ÁFRICA
24.1.5.1. ÁFRICA DO SUL
24.1.5.2. EGITO
24.1.5.3. ISRAEL
24.1.5.4. Emirados Árabes Unidos
24.1.5.5. ARÁBIA SAUDITA
24.1.5.6. RESTANTE DO ORIENTE MÉDIO E ÁFRICA
24.1.6 PRINCIPAIS INFORMAÇÕES: POR PAÍSES PRINCIPAIS
25. TERCEIRIZAÇÃO DE ASSUNTOS REGULAMENTARES DE DIAGNÓSTICO IN VITRO (IVD) GLOBAL, CENÁRIO DA EMPRESA
25.1 ANÁLISE DE AÇÕES DA EMPRESA: GLOBAL
25.2 ANÁLISE DE AÇÕES DA EMPRESA: AMÉRICA DO NORTE
25.3 ANÁLISE DE AÇÕES DA EMPRESA: EUROPA
25.4 ANÁLISE DE AÇÕES DA EMPRESA: ÁSIA-PACÍFICO
25.5 FUSÕES E AQUISIÇÕES
25.6 DESENVOLVIMENTO E APROVAÇÕES DE NOVOS PRODUTOS
25.7 EXPANSÕES
25.8 ALTERAÇÕES REGULAMENTARES
25.9 PARCERIA E OUTROS DESENVOLVIMENTOS ESTRATÉGICOS
26. MERCADO DE TERCEIRIZAÇÃO DE ASSUNTOS REGULAMENTARES GLOBAIS DE DIAGNÓSTICO IN VITRO (IVD), PERFIL DA EMPRESA
26.1 SOLUÇÕES FREYR
26.1.1 VISÃO GERAL DA EMPRESA
26.1.2 RESUMO DA EMPRESA
26.1.3 ANÁLISE DE RECEITA
26.1.4 PORTFÓLIO DE PRODUTOS
26.1.5 DESENVOLVIMENTOS RECENTES
26.2 AXSOURCE CONSULTING INC.
26.2.1 VISÃO GERAL DA EMPRESA
26.2.2 RESUMO DA EMPRESA
26.2.3 ANÁLISE DE RECEITA
26.2.4 PORTFÓLIO DE PRODUTOS
26.2.5 DESENVOLVIMENTOS RECENTES
26.3 GRUPO DE CIÊNCIAS DA VIDA LORENZ
26.3.1 VISÃO GERAL DA EMPRESA
26.3.2 RESUMO DA EMPRESA
26.3.3 ANÁLISE DE RECEITA
26.3.4 PORTFÓLIO DE PRODUTOS
26.3.5 DESENVOLVIMENTOS RECENTES
26.4 CORPORAÇÃO DE LABORATÓRIOS DA AMERICA HOLDINGS
26.4.1 VISÃO GERAL DA EMPRESA
26.4.2 RESUMO DA EMPRESA
26.4.3 ANÁLISE DE RECEITA
26.4.4 PORTFÓLIO DE PRODUTOS
26.4.5 DESENVOLVIMENTOS RECENTES
26.5 REG IQ PTY LTD.
26.5.1 VISÃO GERAL DA EMPRESA
26.5.2 RESUMO DA EMPRESA
26.5.3 ANÁLISE DE RECEITA
26.5.4 PORTFÓLIO DE PRODUTOS
26.5.5 DESENVOLVIMENTOS RECENTES
26.6 PROMEDICA INTERNATIONAL, UMA CORPORAÇÃO DA CALIFÓRNIA (IUVO BIOSCIENCES)
26.6.1 VISÃO GERAL DA EMPRESA
26.6.2 RESUMO DA EMPRESA
26.6.3 ANÁLISE DE RECEITA
26.6.4 PORTFÓLIO DE PRODUTOS
26.6.5 DESENVOLVIMENTOS RECENTES
26.7 MAKROCARE
26.7.1 VISÃO GERAL DA EMPRESA
26.7.2 RESUMO DA EMPRESA
26.7.3 ANÁLISE DE RECEITA
26.7.4 PORTFÓLIO DE PRODUTOS
26.7.5 DESENVOLVIMENTOS RECENTES
26.8 EMERGÊNCIA POR UL
26.8.1 VISÃO GERAL DA EMPRESA
26.8.2 RESUMO DA EMPRESA
26.8.3 ANÁLISE DE RECEITA
26.8.4 PORTFÓLIO DE PRODUTOS
26.8.5 DESENVOLVIMENTOS RECENTES
26.9 ICON PLC
26.9.1 VISÃO GERAL DA EMPRESA
26.9.2 RESUMO DA EMPRESA
26.9.3 ANÁLISE DE RECEITA
26.9.4 PORTFÓLIO DE PRODUTOS
26.9.5 DESENVOLVIMENTOS RECENTES
26.10 WUXI APPTEC
26.10.1 VISÃO GERAL DA EMPRESA
26.10.2 RESUMO DA EMPRESA
26.10.3 ANÁLISE DE RECEITA
26.10.4 PORTFÓLIO DE PRODUTOS
26.10.5 DESENVOLVIMENTOS RECENTES
26.11 THERMO FISHER SCIENTIFIC INC.
26.11.1 VISÃO GERAL DA EMPRESA
26.11.2 RESUMO DA EMPRESA
26.11.3 ANÁLISE DE RECEITA
26.11.4 PORTFÓLIO DE PRODUTOS
26.11.5 DESENVOLVIMENTOS RECENTES
26.12 LABORATÓRIOS CHARLES RIVER.
26.12.1 VISÃO GERAL DA EMPRESA
26.12.2 RESUMO DA EMPRESA
26.12.3 ANÁLISE DE RECEITA
26.12.4 PORTFÓLIO DE PRODUTOS
26.12.5 DESENVOLVIMENTOS RECENTES
26.13 ACCELL PESQUISA CLÍNICA, LLC
26.13.1 VISÃO GERAL DA EMPRESA
26.13.2 RESUMO DA EMPRESA
26.13.3 ANÁLISE DE RECEITA
26.13.4 PORTFÓLIO DE PRODUTOS
26.13.5 DESENVOLVIMENTOS RECENTES
26.14 CORPORAÇÃO INTERNACIONAL PAREXEL (MA)
26.14.1 VISÃO GERAL DA EMPRESA
26.14.2 RESUMO DA EMPRESA
26.14.3 ANÁLISE DE RECEITA
26.14.4 PORTFÓLIO DE PRODUTOS
26.14.5 DESENVOLVIMENTOS RECENTES
26.15 METECON GMBH
26.15.1 VISÃO GERAL DA EMPRESA
26.15.2 RESUMO DA EMPRESA
26.15.3 ANÁLISE DE RECEITA
26.15.4 PORTFÓLIO DE PRODUTOS
26.15.5 DESENVOLVIMENTOS RECENTES
26.16 GENPACTO
26.16.1 VISÃO GERAL DA EMPRESA
26.16.2 RESUMO DA EMPRESA
26.16.3 ANÁLISE DE RECEITA
26.16.4 PORTFÓLIO DE PRODUTOS
26.16.5 DESENVOLVIMENTOS RECENTES
26.17 CRITÉRIO, INC
26.17.1 VISÃO GERAL DA EMPRESA
26.17.2 RESUMO DA EMPRESA
26.17.3 ANÁLISE DE RECEITA
26.17.4 PORTFÓLIO DE PRODUTOS
26.17.5 DESENVOLVIMENTOS RECENTES
26.18 MEDPACE
26.18.1 VISÃO GERAL DA EMPRESA
26.18.2 RESUMO DA EMPRESA
26.18.3 ANÁLISE DE RECEITA
26.18.4 PORTFÓLIO DE PRODUTOS
26.18.5 DESENVOLVIMENTOS RECENTES
26.19 GRUPO PRODUCTLIFE SA
26.19.1 VISÃO GERAL DA EMPRESA
26.19.2 RESUMO DA EMPRESA
26.19.3 ANÁLISE DE RECEITA
26.19.4 PORTFÓLIO DE PRODUTOS
26.19.5 DESENVOLVIMENTOS RECENTES
26.20 DOR SERVIÇOS FARMACÊUTICOS
26.20.1 VISÃO GERAL DA EMPRESA
26.20.2 RESUMO DA EMPRESA
26.20.3 ANÁLISE DE RECEITA
26.20.4 PORTFÓLIO DE PRODUTOS
26.20.5 DESENVOLVIMENTOS RECENTES
26.21 QSERVE
26.21.1 VISÃO GERAL DA EMPRESA
26.21.2 RESUMO DA EMPRESA
26.21.3 ANÁLISE DE RECEITA
26.21.4 PORTFÓLIO DE PRODUTOS
26.21.5 DESENVOLVIMENTOS RECENTES
26.22 DIAGNÓSTICO ORTOCLÍNICO.
26.22.1 VISÃO GERAL DA EMPRESA
26.22.2 RESUMO DA EMPRESA
26.22.3 ANÁLISE DE RECEITA
26.22.4 PORTFÓLIO DE PRODUTOS
26.22.5 DESENVOLVIMENTOS RECENTES
26.23 ANGSTROM BIOTECH Pvt. Ltda.
26.23.1 VISÃO GERAL DA EMPRESA
26.23.2 RESUMO DA EMPRESA
26.23.3 ANÁLISE DE RECEITA
26.23.4 PORTFÓLIO DE PRODUTOS
26.23.5 DESENVOLVIMENTOS RECENTES
26.24 RQM+
26.24.1 VISÃO GERAL DA EMPRESA
26.24.2 RESUMO DA EMPRESA
26.24.3 ANÁLISE DE RECEITA
26.24.4 PORTFÓLIO DE PRODUTOS
26.24.5 DESENVOLVIMENTOS RECENTES
26.25 ASSOCIADOS DE CONFORMIDADE REGULAMENTAR (SOTERA HEALTH)
26.25.1 VISÃO GERAL DA EMPRESA
26.25.2 RESUMO DA EMPRESA
26.25.3 ANÁLISE DE RECEITA
26.25.4 PORTFÓLIO DE PRODUTOS
26.25.5 DESENVOLVIMENTOS RECENTES
26.26 PESQUISA DX
26.26.1 VISÃO GERAL DA EMPRESA
26.26.2 RESUMO DA EMPRESA
26.26.3 ANÁLISE DE RECEITA
26.26.4 PORTFÓLIO DE PRODUTOS
26.26.5 DESENVOLVIMENTOS RECENTES
26.27 CMIC HOLDINGS CO., LTD.
26.27.1 VISÃO GERAL DA EMPRESA
26.27.2 RESUMO DA EMPRESA
26.27.3 ANÁLISE DE RECEITA
26.27.4 PORTFÓLIO DE PRODUTOS
26.27.5 DESENVOLVIMENTOS RECENTES
26.28 NORTH AMERICAN SCIENCE ASSOCIATES, LLC
26.28.1 VISÃO GERAL DA EMPRESA
26.28.2 RESUMO DA EMPRESA
26.28.3 ANÁLISE DE RECEITA
26.28.4 PORTFÓLIO DE PRODUTOS
26.28.5 DESENVOLVIMENTOS RECENTES
26.29 QARAD BV
26.29.1 VISÃO GERAL DA EMPRESA
26.29.2 RESUMO DA EMPRESA
26.29.3 ANÁLISE DE RECEITA
26.29.4 PORTFÓLIO DE PRODUTOS
26.29.5 DESENVOLVIMENTOS RECENTES
26h30 TRANSCRIÇÃO
26.30.1 VISÃO GERAL DA EMPRESA
26.30.2 RESUMO DA EMPRESA
26.30.3 ANÁLISE DE RECEITA
26.30.4 PORTFÓLIO DE PRODUTOS
26.30.5 DESENVOLVIMENTOS RECENTES
26.31 CLIN-R+
26.31.1 VISÃO GERAL DA EMPRESA
26.31.2 RESUMO DA EMPRESA
26.31.3 ANÁLISE DE RECEITA
26.31.4 PORTFÓLIO DE PRODUTOS
26.31.5 DESENVOLVIMENTOS RECENTES
26,32 VCLS
26.32.1 VISÃO GERAL DA EMPRESA
26.32.2 RESUMO DA EMPRESA
26.32.3 ANÁLISE DE RECEITA
26.32.4 PORTFÓLIO DE PRODUTOS
26.32.5 DESENVOLVIMENTOS RECENTES
26.33 GRUPO PROPHARMA
26.33.1 VISÃO GERAL DA EMPRESA
26.33.2 RESUMO DA EMPRESA
26.33.3 ANÁLISE DE RECEITA
26.33.4 PORTFÓLIO DE PRODUTOS
26.33.5 DESENVOLVIMENTOS RECENTES
26.34 ARRIELLO IRLANDA LIMITADA
26.34.1 VISÃO GERAL DA EMPRESA
26.34.2 RESUMO DA EMPRESA
26.34.3 ANÁLISE DE RECEITA
26.34.4 PORTFÓLIO DE PRODUTOS
26.34.5 DESENVOLVIMENTOS RECENTES
OBSERVAÇÃO: A LISTA DE EMPRESAS APRESENTADA NÃO É EXAUSTIVA E ESTÁ DE ACORDO COM AS NECESSIDADES DE NOSSOS CLIENTES ANTERIORES. APRESENTAMOS O PERFIL DE MAIS DE 100 EMPRESAS EM NOSSO ESTUDO E, PORTANTO, A LISTA DE EMPRESAS PODE SER MODIFICADA OU SUBSTITUÍDA SOB SOLICITAÇÃO.
27. RELATÓRIOS RELACIONADOS
28. QUESTIONÁRIO
29. SOBRE A PESQUISA DE MERCADO DA DATA BRIDGE
Metodologia de Investigação
A recolha de dados e a análise do ano base são feitas através de módulos de recolha de dados com amostras grandes. A etapa inclui a obtenção de informações de mercado ou dados relacionados através de diversas fontes e estratégias. Inclui examinar e planear antecipadamente todos os dados adquiridos no passado. Da mesma forma, envolve o exame de inconsistências de informação observadas em diferentes fontes de informação. Os dados de mercado são analisados e estimados utilizando modelos estatísticos e coerentes de mercado. Além disso, a análise da quota de mercado e a análise das principais tendências são os principais fatores de sucesso no relatório de mercado. Para saber mais, solicite uma chamada de analista ou abra a sua consulta.
A principal metodologia de investigação utilizada pela equipa de investigação do DBMR é a triangulação de dados que envolve a mineração de dados, a análise do impacto das variáveis de dados no mercado e a validação primária (especialista do setor). Os modelos de dados incluem grelha de posicionamento de fornecedores, análise da linha de tempo do mercado, visão geral e guia de mercado, grelha de posicionamento da empresa, análise de patentes, análise de preços, análise da quota de mercado da empresa, normas de medição, análise global versus regional e de participação dos fornecedores. Para saber mais sobre a metodologia de investigação, faça uma consulta para falar com os nossos especialistas do setor.
Personalização disponível
A Data Bridge Market Research é líder em investigação formativa avançada. Orgulhamo-nos de servir os nossos clientes novos e existentes com dados e análises que correspondem e atendem aos seus objetivos. O relatório pode ser personalizado para incluir análise de tendências de preços de marcas-alvo, compreensão do mercado para países adicionais (solicite a lista de países), dados de resultados de ensaios clínicos, revisão de literatura, mercado remodelado e análise de base de produtos . A análise de mercado dos concorrentes-alvo pode ser analisada desde análises baseadas em tecnologia até estratégias de carteira de mercado. Podemos adicionar quantos concorrentes necessitar de dados no formato e estilo de dados que procura. A nossa equipa de analistas também pode fornecer dados em tabelas dinâmicas de ficheiros Excel em bruto (livro de factos) ou pode ajudá-lo a criar apresentações a partir dos conjuntos de dados disponíveis no relatório.