Global Rare Disease Api Orphan Drug Substance Market
Marktgröße in Milliarden USD
CAGR :
% 
 USD
306.90 Million
USD
667.49 Million
2025
2033
USD
306.90 Million
USD
667.49 Million
2025
2033
| 2026 –2033 | |
| USD 306.90 Million | |
| USD 667.49 Million | |
|
|
|
|
Globale Seltene Krankheiten API / Orphan Drug Substance Market Segmentation, Nach API/Drug Substance Type (Biologics APIs, Small-Molecule APIs, Viral Vector APIs, RNA-basierte APIs und Zelltherapie-bezogene Drug Substances), Therapeutic Indication (Oncology, Hematologic Disorders, Neurological & Neuromuscular User Disordocers, Metabolic Industrietrends und Prognosen bis 2033
Seltene Krankheit API / Orphan Drug Subsance Market Size
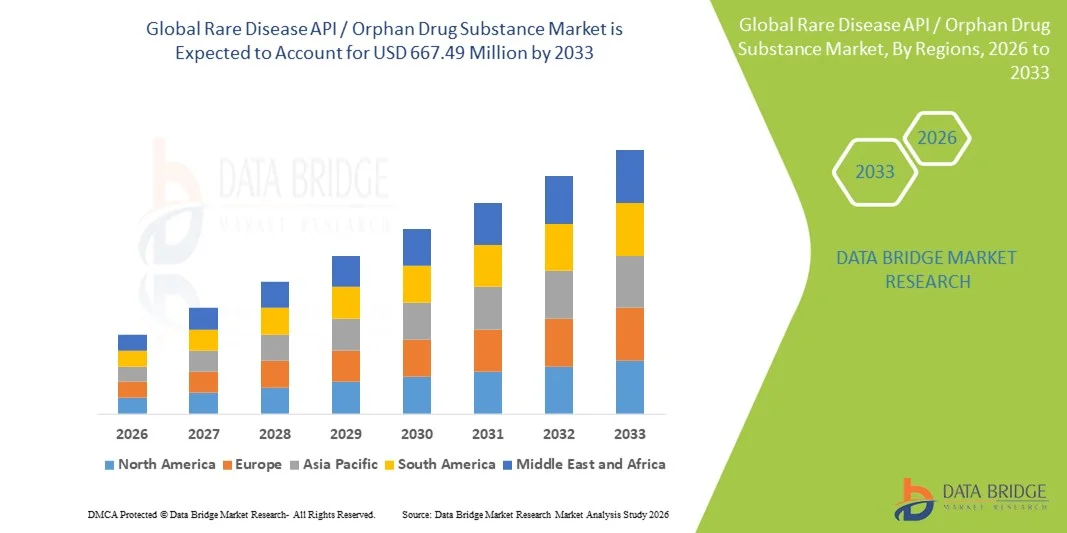
- Die globale Seltenheit API / Waisenstoff Marktgröße wurde bei306,90 Mio. USD im Jahr 2025und wird voraussichtlich erreichen667,49 Mio. USD bis 2033, beiCAGR von 10,20%während des Prognosezeitraums
- Das Marktwachstum wird größtenteils durch die steigende Prävalenz seltener Krankheiten, die Ausweitung von Waisenstoffpipelines und zunehmende regulatorische Anreize, die die Entwicklung und Herstellung von spezialisierten Wirkstoffen für seltene und ultra-rare Bedingungen fördern
- Darüber hinaus wächst Investitionen in Biologik,Gentherapien, und andere fortgeschrittene Modalitäten, zusammen mit der Notwendigkeit von qualitativ hochwertigen, kleinen und hochwirksamen Medikamentensubstanzen, setzen Waisen-APIs als kritischer Bestandteil der modernen pharmazeutischen Entwicklung. Diese konvergierenden Faktoren beschleunigen die Nachfrage nach seltenen Krankheits-APIs, wodurch das Wachstum der Industrie deutlich erhöht
Seltene Krankheit API / Orphan Drug Subsance Market Analysis
- Seltene Krankheits-APIs und Waisensubstanzen, die hochspezialisierte Wirkstoffe zur Behandlung seltener und ultra-rassiger Bedingungen enthalten, werden aufgrund ihrer Rolle bei der gezielten, präzisen und lebenserhaltenden Therapien in mehreren therapeutischen Bereichen immer kritischer für die moderne pharmazeutische Entwicklung.
- Die eskalierende Nachfrage nach seltenen Krankheits-APIs wird in erster Linie durch die wachsende Prävalenz seltener Krankheiten, expandierender Waisen-Drogen-Pipeline, günstige regulatorische Anreize und zunehmende Investitionen in fortgeschrittene Modalitäten wie Biologik, Gentherapien und RNA-basierte Behandlungen angetrieben.
- Nordamerika dominierte den Markt für seltene Krankheiten API / Waisenstoff mit dem größten Umsatzanteil von 41.5% im Jahr 2025, unterstützt durch einen starken regulatorischen Rahmen für Waisenarzneimittel, hohe FuE-Ausgaben und eine robuste PräsenzBiopharmazeutikaUnternehmen und spezialisierte CDMOs, mit den USA ein signifikantes Wachstum in der klinischen und kommerziellen Waisen-API-Produktion
- Asia-Pacific wird erwartet, dass die am schnellsten wachsende Region in der seltenen Krankheit API-Markt während der Prognosezeit durch die Zunahme der Outsourcing von API-Produktion, die Erweiterung von Biotechnologie-Ökosystemen, die Verbesserung der regulatorischen Ausrichtung und steigende Investitionen in seltene Krankheiten Drogenentwicklung in China, Japan, Südkorea und Indien
- Biologics APIs dominierten die seltene Krankheit API / Waisenstoffmarkt mit einem Marktanteil von 58,3% im Jahr 2025, angetrieben durch ihre weit verbreitete Verwendung in Enzymersatztherapien,monoklonale Antikörper, und Gen-basierte Behandlungen, zusammen mit ihrer starken Wirksamkeit bei der Behandlung komplexer genetischer und metabolischer seltener Krankheiten
Report Scope und seltene Krankheiten API / Orphan Drug Substance Market Segmentation
| Attribute | Seltene Krankheit API / Orphan Drug Substance Key Market Insights |
| Verdeckte Segmente |
|
| Überarbeitete Länder | Nordamerika
Europa
Asien-Pazifik
Naher Osten und Afrika
Südamerika
|
| Key Market Players |
|
| Marktmöglichkeiten |
|
| Daten Infos zum Wert hinzugefügt | Neben den Erkenntnissen über Marktszenarien wie Marktwert, Wachstumsrate, Segmentierung, geographische Erfassung und wichtige Akteure umfassen die Marktberichte, die von der Data Bridge Market Research kuratiert werden, auch eingehende Expertenanalysen, Patientenepidemiologie, Pipelineanalyse, Preisanalyse und regulatorische Rahmenbedingungen. |
Seltene Krankheit API / Orphan Drug Subsance Market Trends
Verschiebliche Fortgeschrittene biologische und genetische Wirkstoffe
- Ein signifikanter und beschleunigter Trend im globalen Seltenerkrankung API / Waisenstoffmarkt ist der zunehmende Wandel in Richtung Biologik, Gentherapien und RNA-basierte Medikamentensubstanzen, die durch ihre Fähigkeit, die zugrunde liegenden genetischen Ursachen von seltenen und ultra-rassigen Krankheiten mit hoher Präzision anzustreben
- Die zunehmende Anzahl von regulatorischen Zulassungen für Gen- und Zelltherapien, die auf seltene Erkrankungen abzielen, verstärkt die Nachfrage nach viralen Vektor-APIs, rekombinanten Proteinen und hochspezialisierten biologen Wirkstoffen, die unter strengen Qualitätsstandards hergestellt werden.
- Die Weiterentwicklung der Molekularbiologie, Genomik und Begleitdiagnostik ermöglicht die Entwicklung von hochzielgerichteten Waisendrogensubstanzen und ermöglicht es Herstellern, auf bestimmte Mutationen oder Krankheitswege zugeschnittene APIs zu entwerfen, wodurch die Wirksamkeit der Behandlung und die Patientenergebnisse verbessert werden
- Die zunehmende Einführung von Präzisions-Medikament-Ansätzen ist es, Pharmaunternehmen zu ermutigen, in komplexe, kostengünstige, hochwertige API-Produktion zu investieren, die spezialisierte Einrichtungen, fortschrittliche analytische Fähigkeiten und strenge regulatorische Compliance erfordert
- Der Anstieg der plattformbasierten Fertigungstechnologien unterstützt die flexible und skalierbare Produktion von Waisen-APIs und ermöglicht es Herstellern, mehrere seltene Krankheitsprogramme gleichzeitig effizient zu handhaben
- Dieser Trend zu komplexeren und kundenspezifischen Waisendrogenstoffen ist die Umgestaltung von API-Herstellungsstrategien, mit erhöhtem Schwerpunkt auf Kleinserienproduktion, hohem Potenzhandling und schnellen Umrüstfähigkeiten
- Folglich erweitern Unternehmen wie Lonza und Catalent ihre Biologik und Gentherapie-API-Fähigkeiten, um die steigende Nachfrage nach fortgeschrittenen Waisendrogenstoffen über mehrere seltene Krankheitsanzeigen zu unterstützen
Seltene Krankheit API / Orphan Drug Substance Market Dynamics
Fahrer
Erweitern von Orphan Drug Pipelines und ungünstigen Regulatory Incentives
- Die zunehmende Zahl der Waisendrogenbezeichnungen und Zulassungen, die durch günstige regulatorische Anreize wie Marktausschließlichkeit, Steuergutschriften und beschleunigte Überprüfungswege unterstützt werden, ist ein wichtiger Treiber für die Nachfrage nach seltenen Krankheiten APIs
- So haben beispielsweise regulatorische Rahmenbedingungen in den USA, Europa und Japan die Entwicklungszeiträume für Waisenarzneimittel deutlich reduziert, biopharmazeutische Unternehmen ermutigt, ihre Seltenheitspipeline zu erweitern und in spezialisierte API-Produktion zu investieren
- Da die Bewusstseins-, Screening- und Diagnoseraten von seltenen Krankheiten weltweit verbessern, steigt die Notwendigkeit einer konsequenten und qualitativ hochwertigen Medikamentenstoffversorgung, die das Wachstum auf dem Markt der Waisen-API direkt unterstützt
- Darüber hinaus ermöglichen starke Risikokapital und öffentliche Finanzierungen für die seltene Krankheitsforschung kleinere Biotech-Firmen, klinische Programme zu fördern, die Abhängigkeit von ausgelagerten API-Produktionen und spezialisierten CDMOs zu erhöhen.
- Der zunehmende Fokus auf Präzision und personalisierte Therapien, kombiniert mit langfristigen kommerziellen Potenzialen aufgrund eines begrenzten Wettbewerbs, setzt weiterhin eine anhaltende Nachfrage nach Waisenstoffen fort
- Die Erhöhung der staatlichen und gemeinnützigen Unterstützung für die Entwicklung der seltenen Krankheiten verstärkt die langfristige Rentabilität von Investitionen in die Waisenstoffproduktion
- Die Fähigkeit von Waisendrogen, Premium-Preise zu beherrschen, verbessert die Rendite von Investitionen, die weitere Förderung der Erweiterung der Waisen API Produktionskapazität
Zurückhaltung/Challenge
Fertigungskomplexität und regulierende Compliance-Barriers
- Die Produktion von seltenen Krankheits-APIs beinhaltet oft komplexe Fertigungsprozesse, strenge Qualitätsanforderungen und begrenzte Chargengrößen, die Produktionskosten und technische Risiken deutlich erhöhen können
- So erfordern z.B. biologe und Gentherapie-Medikamente spezialisierte Einrichtungen, hochqualifiziertes Personal und fortgeschrittene Eindämmungssysteme, wodurch die Herstellung technisch anspruchsvoll und kapitalintensiv
- Regulatorische Compliance in mehreren Regionen fügt weitere Komplexität hinzu, da Waisendrogen unterschiedliche und sich entwickelnde Standards in Bezug auf Sicherheit, Rückverfolgbarkeit und Qualitätskontrolle erfüllen müssen
- Diese Herausforderungen können die Zahl der qualifizierten API-Lieferanten begrenzen, die möglicherweise zu Versorgungsengpässe und höheren Kosten führen, wodurch eine breitere Markterweiterung zurückgehalten wird
- Eine begrenzte Verfügbarkeit von spezialisierten Rohstoffen und Reagenzien für fortgeschrittene Waisen APIs kann die Produktionszeiträume weiter stören und die Abhängigkeit von Nischenlieferanten erhöhen
- Die Notwendigkeit einer umfangreichen Validierung, langen Vorlaufzeiten und strengen Kontrollen nach der Genehmigung können die Herstellung Agilität und Verzögerung der kommerziellen Versorgung mit Waisendrogen verlangsamen
Seltene Krankheit API / Orphan Drug Subsance Market Scope
Der Markt wird auf der Grundlage von API / Wirkstofftyp, therapeutische Indikation und Endverbraucher segmentiert.
- Durch API / Drug Subsance Type
Auf Basis des API / Drogentyps wird der globale Seltenheits-API / Waisenstoffmarkt in Biologics APIs, Small-Molecule APIs, virale Vektor-APIs, RNA-basierte APIs und Zelltherapie-bezogene Arzneimittelsubstanzen segmentiert. Das Segment Biologics APIs dominierte den Markt mit dem größten Umsatzanteil von 58,3% im Jahr 2025, angetrieben durch den weit verbreiteten Einsatz von monoklonalen Antikörpern, Enzymersatztherapien und rekombinanten Proteinen bei der Behandlung von seltenen genetischen und metabolischen Störungen. Biologics bieten hohe Spezifität und klinische Wirksamkeit, so dass sie die bevorzugte Wahl für viele Waisen-Droge-Programme. Die starke Präsenz von zugelassenen biologen Waisendrogen und die fortgesetzte Pipeline-Erweiterung unterstützen die Dominanz dieses Segments. Darüber hinaus tragen die Prämienpreise und die langfristigen Behandlungssysteme zu einer höheren Ertragserzeugung bei. Auch die etablierte Fertigungskompetenz und die regulatorische Vertrautheit mit Biologen stärken ihre führende Position.
Das virale Vektor-APIs-Segment wird erwartet, dass das schnellste Wachstum während der Prognoseperiode, die durch die rasche Fortentwicklung von Gentherapien für seltene und ultra-rassige Krankheiten. Die zunehmenden Zulassungen von Adeno-assoziierten Virus (AAV) und lentiviralen vektorbasierten Therapien führen zu einer starken Nachfrage nach spezialisierter Vektorproduktion. Hoher ungenutzter medizinischer Bedarf, kuratives Behandlungspotenzial und wachsende Investitionen in Gentherapie-Plattformen beschleunigen die Expansion dieses Segments. Begrenzte Lieferantenverfügbarkeit und komplexe Fertigungsanforderungen erhöhen die strategische Bedeutung und Wachstumsdynamik von viralen Vektor-APIs weiter.
- Durch Therapeutische Indikation
Auf der Grundlage der therapeutischen Indikation wird der Markt in die Onkologie, hämatologische Störungen, neurologische und neuromuskuläre Erkrankungen, metabolische und endokrine Störungen, immunologische und seltene Infektionskrankheiten und Herz-Kreislauf-, Augen- und andere seltene Erkrankungen segmentiert. Das Onkologie-Segment dominierte den Markt im Jahr 2025, aufgrund der hohen Anzahl an Waisendrogenbezeichnungen für seltene Krebserkrankungen und anhaltende Investitionen in gezielte Krebstherapien. Seltene Onkologie-Medikamente verlassen sich oft auf hochwirksame APIs und Biologik und tragen maßgeblich zur gesamten API-Anforderung bei. Starke klinische Pipelines, beschleunigte regulatorische Zulassungen und höhere Behandlungskosten unterstützen die Umsatzführerschaft dieses Segments weiter. Darüber hinaus priorisieren Pharmaunternehmen seltene Onkologie aufgrund günstiger Erstattungs- und Marktexklusivleistungen.
Das neurologische und neuromuskuläre Unordnungssegment wird während der Prognosezeit mit der schnellsten Rate wachsen, die durch die zunehmende Erforschung genetischer neurologischer Zustände wie Spinalmuskelatrophie, Duchenne Muskeldystrophie und seltene Epilepsien verursacht wird. Fortschritte in der Gentherapie, RNA-basierte Medikamente und Präzisionsmedizin transformieren Therapieansätze in diesem Raum. Steigende Diagnoseraten und starke Advocacy-Unterstützung fördern die Entwicklung. Da viele dieser Therapien komplexe APIs erfordern, wächst die Nachfrage nach spezialisierten Wirkstoffen in diesem Segment rasch.
- Mit dem Endbenutzer
Auf der Grundlage des Endverbrauchers wird der weltweite Markt für seltene Krankheiten API / Waisenstoffe in biopharmazeutische Unternehmen, Vertragsentwicklung & Produktionsorganisationen (CDMOs) und Forschungsinstitute & Spezialhersteller segmentiert. Das Segment Biopharmazeutische Unternehmen entfiel im Jahr 2025 auf den größten Marktanteil, der durch das Eigentum an Waisenstoffpipelines und die direkte Kontrolle über die gewerbliche Fertigung für hochwertige Therapien getrieben wurde. Große und mittlere Biopharma-Unternehmen investieren stark in die Sicherung einer zuverlässigen API-Versorgung, um Exklusivitätszeiten zu schützen und eine gleichbleibende Produktqualität zu gewährleisten. Die hausinterne Herstellung kritischer APIs ist oft aus strategischen und intellektuellen Gründen bevorzugt. Die Dominanz dieses Segments wird durch starke finanzielle Fähigkeiten und regulatorische Expertise weiter gestärkt.
Das Segment CDMOs wird voraussichtlich das schnellste Wachstum über den Prognosezeitraum registrieren, unterstützt durch steigende Outsourcing-Trends bei Biotech- und Pharmaunternehmen. Die Komplexität der Waisen-APIs, kombiniert mit kleinen Chargengrößen und hohen Kapitalanforderungen, ist ermutigen Sponsoren auf spezialisierte CDMOs zu verlassen. CDMOs bieten flexible Herstellungs-, Regulierungs- und fortschrittliche Technologien, die für Arzneimittel mit seltenen Krankheiten geeignet sind. Da kleinere Biotech-Firmen Innovationen in Waisendrogen vorantreiben, beschleunigt sich die Abhängigkeit von CDMOs für skalierbare und konforme API-Produktion schnell.
Seltene Krankheit API / Orphan Drug Subsance Market Regionale Analyse
- Nordamerika dominierte den Markt für seltene Krankheiten API / Waisenstoff mit dem größten Umsatzanteil von 41.5% im Jahr 2025, unterstützt durch einen starken regulatorischen Rahmen für Waisenarzneimittel, hohe FuE-Ausgaben und eine robuste Präsenz von biopharmazeutischen Unternehmen und spezialisierten CDMOs
- Unternehmen in der Region legen hohen Wert auf fortgeschrittene Fertigungsfähigkeiten, strenge Qualität Compliance und zuverlässige Versorgung komplexer Arzneimittel, insbesondere für Biologik, Gentherapien und andere hochwertige Waisen-APIs
- Diese weit verbreitete Marktführerschaft wird durch eine hohe Konzentration an Waisendrogenzulassungen, eine starke Finanzierung für seltene Krankheiten Forschung, und die Präsenz führender biopharmazeutischer Unternehmen und spezialisierter CDMOs unterstützt, die Nordamerika als primärer Knotenpunkt für seltene Krankheiten API Entwicklung und Produktion
US Seltene Krankheit API / Orphan Drug Substance Market Insight
Der US-Markt für seltene Krankheiten API / Waisendrogen eroberte den größten Umsatzanteil in Nordamerika im Jahr 2025, der durch einen starken regulatorischen Rahmen für Waisenarzneimittel, umfangreiche FuE-Investitionen und eine hohe Konzentration an biopharmazeutischen und biotechnologischen Unternehmen getrieben wurde. Hersteller priorisieren zunehmend die Entwicklung und sichere Versorgung komplexer APIs, um expandierende Waisenstoffpipelines zu unterstützen. Das Vorhandensein günstiger Anreize wie Marktausschließlichkeit, Steuergutschriften und beschleunigte Zulassungswege stimuliert weiterhin die Nachfrage nach spezialisierten Arzneimitteln. Darüber hinaus trägt die starke Rolle von CDMOs und fortschrittlicher Fertigungsinfrastruktur maßgeblich zum nachhaltigen Marktwachstum bei.
Europa Seltene Krankheit API / Orphan Drug Substance Market Insight
Der europäische Markt für seltene Krankheiten API / Waisendrogen wird in der Vorausschätzungsperiode auf einem beträchtlichen CAGR ausbauen, vor allem durch eine unterstützende EMA-Politik zur Waisenarzneimittel und steigende Investitionen in die seltene Krankheitsforschung. Das zunehmende Bewusstsein, verbesserte Diagnoseraten und grenzüberschreitende Kooperationen fördern die Entwicklung der Waisendrogen in der gesamten Region. Europäische Hersteller betonen Qualität, Rückverfolgbarkeit und regulatorische Compliance und unterstützen stetige Nachfrage nach hochwertigen APIs. Sowohl innovatorgetriebene als auch ausgelagerte Fertigungsmodelle, insbesondere für Biologik und fortgeschrittene Therapien, werden Wachstum beobachtet.
U.K. Seltene Krankheit API / Orphan Drug Substance Market Insight
Der US Seltene Krankheit API / Waisenstoff-Markt wird erwartet, um bei einem bemerkenswerten CAGR über den Prognosezeitraum zu wachsen, unterstützt durch starke akademische-industrielle Zusammenarbeit und staatliche unterstützte seltene Krankheit Initiativen. Das fortgeschrittene Biowissenschaften-Ökosystem der U.K. fördert die frühe Entwicklung der Waisenmedizin und erhöht die Nachfrage nach klinisch-stufigen APIs. Die anhaltende Investition in die Biologik und Gentherapieforschung verstärkt den Marktausblick. Darüber hinaus verbessert die regulatorische Ausrichtung mit globalen Standards die Attraktivität des Landes für Waisen-API-Produktions- und Entwicklungspartnerschaften.
Deutschland Seltene Krankheit API / Orphan Drug Substance Market Insight
Der deutsche Markt für seltene Krankheiten API / Waisendrogen soll sich während des Prognosezeitraums mit einem beträchtlichen CAGR ausweiten, der durch eine robuste pharmazeutische Fertigungsbasis und starke Betonung auf Innovation und Qualität gefördert wird. Deutschlands führender Anbieter von Biologik-Produktions- und fortschrittlichen Fertigungstechnologien unterstützt die stetige Nachfrage nach komplexen Waisenstoffen. Der Fokus des Landes auf Compliance, Sicherheit und Präzisionsfertigung richtet sich gut an die strengen Anforderungen von seltenen Krankheits-APIs. Die zunehmende Investition in fortgeschrittene Therapien verstärkt die Wachstumsaussichten des Marktes weiter.
Asia-Pacific Rare Disease API / Orphan Drug Subsance Market Insight
Der asiatisch-pazifische Seltenheits-API / Waisenstoffmarkt ist bereit, während der Prognosezeit mit dem schnellsten CAGR zu wachsen, der durch die Ausweitung der Biotechnologie-Fähigkeiten, steigende Gesundheitsinvestitionen und zunehmende Outsourcing aus den westlichen Märkten getrieben wird. Länder wie China, Japan und Indien stärken ihre Regulierungsrahmen für seltene Krankheiten und Produktionsinfrastruktur. Die Kostenvorteile der Region und das wachsende technische Know-how ziehen globale biopharmazeutische Unternehmen an, die eine skalierbare API-Produktion suchen. Dieser Trend beschleunigt die Markterweiterung über APAC deutlich.
Japan Seltene Krankheit API / Orphan Drug Substance Market Insight
Der Japan Seltene Krankheit API / Waisenstoffmarkt gewinnt an Dynamik aufgrund einer starken staatlichen Unterstützung für die Entwicklung von Waisendrogen und fortgeschrittene pharmazeutische Fertigungsmöglichkeiten. Japan legt großen Wert auf Qualität, Sicherheit und Innovation, die Nachfrage nach hochspezialisierten Arzneimitteln. Der Fokus des Landes auf genetische und neurologische seltene Krankheiten erhöht die Notwendigkeit komplexer APIs, darunter Biologik und RNA-basierte Substanzen. Eine alternde Bevölkerung und steigende Prävalenz seltener Störungen unterstützen das Marktwachstum weiter.
Indien Seltene Krankheit API / Orphan Drug Substance Market Insight
Der indische Seltenheits-API / Waisenstoff-Markt entfiel auf einen signifikanten Umsatzanteil am asiatisch-pazifischen im Jahr 2025, der auf ein starkes API-Produktions-Know-how, Kosten-Wettbewerbsfähigkeit und den Ausbau von Biotechnologie-Investitionen zurückzuführen ist. Indien ist ein wichtiger Lieferant von klein-molekulen und zunehmend biologen Waisen-APIs für globale Märkte. Regierungsinitiativen zur Unterstützung der Entwicklung der seltenen Krankheiten und der lokalen Produktion verbessern die Marktaussichten. Die wachsende Präsenz von heimischen CDMOs und Vertragsherstellern verstärkt Indiens Rolle in der globalen Waisenstoffversorgungskette.
Seltene Krankheit API / Orphan Drug Subsance Market Share
Die Seltene Krankheit API / Orphan Drug Substance Industrie wird in erster Linie von etablierten Unternehmen geführt, darunter:
- Lonza Ltd (Schweiz)
- Catalent, Inc. (USA)
- WuXi AppTec Co., Ltd. (China)
- Pfizer Inc. (USA)
- Novartis AG (Schweiz)
- F. Hoffmann-La Roche AG (Schweiz)
- Bristol-Myers Squibb Company (USA)
- Amgen Inc. (USA)
- Sanofi (Frankreich)
- Takeda Pharmaceutical Company Limited (Japan)
- AbbVie Inc. (USA)
- GSK plc (USA)
- Bayer AG (Deutschland)
- Vertex Pharmaceuticals Incorporated (US)
- Biogen Inc. (USA)
- PTC Therapeutics, Inc. (USA)
- Schwedisches Orphan Biovitrum AB (Schweden)
- SOM Innovation Biotech, S.A. (Spain)
- Ultragenyx Pharmaceutical Inc. (USA)
Was sind die jüngsten Entwicklungen in Global Rare Disease API / Orphan Drug Substance Market?
- Im August 2025 erteilte die U.S. FDA Papzimeos (zopapogene imadenovec), die erste Immuntherapie zur rezidivierenden Atem Papillomatose (RRP), eine mit Waisen bezeichnete seltene Erkrankung, die Gen-basierte immuntherapeutische Fortschritte bei seltenen Krankheiten untermauert
- Im April 2025 kündigte der gemeinnützige Orphan Therapeutics Accelerator wichtige Partnerschaften an, die darauf abzielen, Entwicklungs- und Kommerzialisierungswege für ultra-rassige Krankheitstherapien zu fördern, historische Herausforderungen bei der Finanzierung und Bereitstellung von Waisendrogenkandidaten voranzutreiben
- Im Januar 2024 verzeichnete die Waisen-Drogenlandschaft der FDA eine signifikante Expansion mit einer Rekordzahl von Zulassungen (28 neuartige Waisen-Drogen), einschließlich erstklassiger Therapien für Bedingungen wie Friedreichs Ataxie und Rett-Syndrom, was ein rasches Wachstum in der therapeutischen Entwicklung von seltenen Krankheiten hervorruft
- Im August 2023 genehmigte die US FDA Pozelimab (Veopoz) als erste Behandlung für die CHAPLE-Krankheit, eine ultra-rare Komplement-Systemstörung, was eine neue rekombinante monoklonale Antikörpertherapie darstellt, die eine ansonsten tödliche Erkrankung anspricht
- Im Mai 2023 genehmigte die US FDA Adzynma (apadamtase alfa), eine rekombinante ADAMTS13 Enzymersatztherapie für angeborene thrombotische thrombozytopenische Purpura (cTTP), die die erste zugelassene biologische Adressierung dieser ultra-rassigen Blutgerinnungsstörung und Erweiterung von Enzymersatzoptionen für seltene Krankheiten Patienten markiert
SKU-
Erhalten Sie Online-Zugriff auf den Bericht zur weltweit ersten Market Intelligence Cloud
- Interaktives Datenanalyse-Dashboard
- Unternehmensanalyse-Dashboard für Chancen mit hohem Wachstumspotenzial
- Zugriff für Research-Analysten für Anpassungen und Abfragen
- Konkurrenzanalyse mit interaktivem Dashboard
- Aktuelle Nachrichten, Updates und Trendanalyse
- Nutzen Sie die Leistungsfähigkeit der Benchmark-Analyse für eine umfassende Konkurrenzverfolgung
Forschungsmethodik
Die Datenerfassung und Basisjahresanalyse werden mithilfe von Datenerfassungsmodulen mit großen Stichprobengrößen durchgeführt. Die Phase umfasst das Erhalten von Marktinformationen oder verwandten Daten aus verschiedenen Quellen und Strategien. Sie umfasst die Prüfung und Planung aller aus der Vergangenheit im Voraus erfassten Daten. Sie umfasst auch die Prüfung von Informationsinkonsistenzen, die in verschiedenen Informationsquellen auftreten. Die Marktdaten werden mithilfe von marktstatistischen und kohärenten Modellen analysiert und geschätzt. Darüber hinaus sind Marktanteilsanalyse und Schlüsseltrendanalyse die wichtigsten Erfolgsfaktoren im Marktbericht. Um mehr zu erfahren, fordern Sie bitte einen Analystenanruf an oder geben Sie Ihre Anfrage ein.
Die wichtigste Forschungsmethodik, die vom DBMR-Forschungsteam verwendet wird, ist die Datentriangulation, die Data Mining, die Analyse der Auswirkungen von Datenvariablen auf den Markt und die primäre (Branchenexperten-)Validierung umfasst. Zu den Datenmodellen gehören ein Lieferantenpositionierungsraster, eine Marktzeitlinienanalyse, ein Marktüberblick und -leitfaden, ein Firmenpositionierungsraster, eine Patentanalyse, eine Preisanalyse, eine Firmenmarktanteilsanalyse, Messstandards, eine globale versus eine regionale und Lieferantenanteilsanalyse. Um mehr über die Forschungsmethodik zu erfahren, senden Sie eine Anfrage an unsere Branchenexperten.
Anpassung möglich
Data Bridge Market Research ist ein führendes Unternehmen in der fortgeschrittenen formativen Forschung. Wir sind stolz darauf, unseren bestehenden und neuen Kunden Daten und Analysen zu bieten, die zu ihren Zielen passen. Der Bericht kann angepasst werden, um Preistrendanalysen von Zielmarken, Marktverständnis für zusätzliche Länder (fordern Sie die Länderliste an), Daten zu klinischen Studienergebnissen, Literaturübersicht, Analysen des Marktes für aufgearbeitete Produkte und Produktbasis einzuschließen. Marktanalysen von Zielkonkurrenten können von technologiebasierten Analysen bis hin zu Marktportfoliostrategien analysiert werden. Wir können so viele Wettbewerber hinzufügen, wie Sie Daten in dem von Ihnen gewünschten Format und Datenstil benötigen. Unser Analystenteam kann Ihnen auch Daten in groben Excel-Rohdateien und Pivot-Tabellen (Fact Book) bereitstellen oder Sie bei der Erstellung von Präsentationen aus den im Bericht verfügbaren Datensätzen unterstützen.