Global Rare Disease Api Orphan Drug Substance Market
Tamaño del mercado en miles de millones de dólares
Tasa de crecimiento anual compuesta (CAGR) :
% 
 USD
306.90 Million
USD
667.49 Million
2025
2033
USD
306.90 Million
USD
667.49 Million
2025
2033
| 2026 –2033 | |
| USD 306.90 Million | |
| USD 667.49 Million | |
|
|
|
|
Global Rare Disease API / Orphan Drug Substance Market Segmentation, By API/Drug Substance Type (Biologics API, Small-Molecule APIs, Viral Vector APIs, RNA-based APIs, and Cell Therapy-related Drug Substances), Therapeutic Indication (Oncology, Hematologic Disorders, Neuromuscular Disorders Tendencias y pronósticos industriales a 2033
Enfermedades Raras API / Substancia de Medicamentos Huérfanos Tamaño
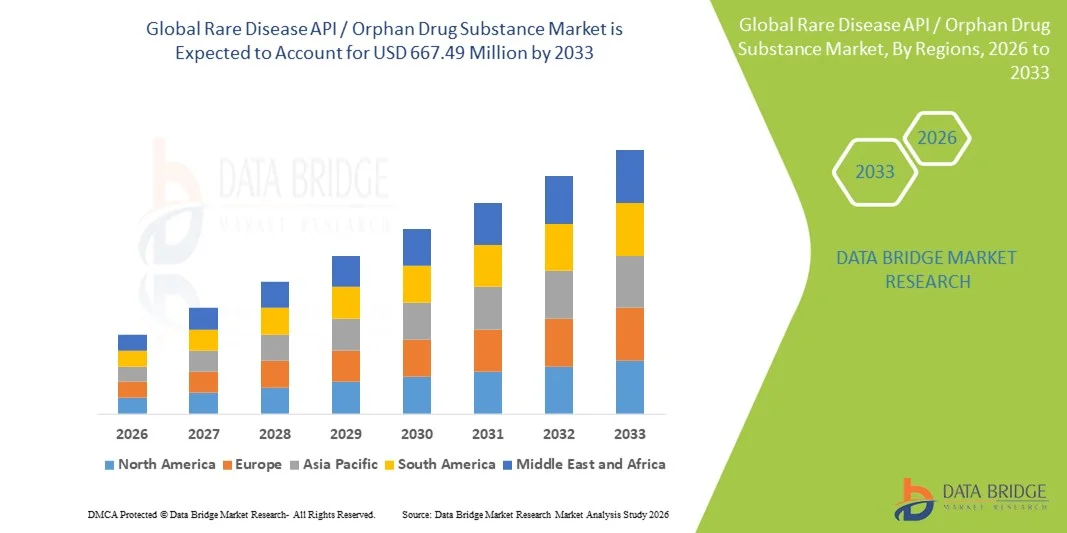
- El tamaño del mercado mundial de la enfermedad rara API / sustancias de origen huérfano se valoró enUSD 306.90 millones en 2025y se espera que alcanceUSD 667.49 million by 2033, aCAGR of 10.20%durante el período previsto
- El crecimiento del mercado está impulsado en gran medida por la creciente prevalencia de enfermedades raras, la expansión de los oleoductos de drogas huérfanos y el aumento de los incentivos reglamentarios que fomentan el desarrollo y la fabricación de ingredientes farmacéuticos activos especializados para las condiciones raras y ultrarres
- Además, la creciente inversión en biologics,terapias genéticas, y otras modalidades avanzadas, junto con la necesidad de sustancias farmacéuticas de alta calidad, pequeñas y muy potentes, están estableciendo API huérfanos como componente crítico del desarrollo farmacéutico moderno. Estos factores convergentes están acelerando la demanda de API de enfermedades raras, lo que aumenta significativamente el crecimiento de la industria
Rare Disease API / Orphan Drug Substance Market Analysis
- Las API de enfermedades raras y las sustancias farmacéuticas huérfanas, que comprenden ingredientes farmacéuticos activos altamente especializados para el tratamiento de las condiciones raras y ultra-raras, se están volviendo cada vez más críticos para el desarrollo farmacéutico moderno debido a su función de permitir terapias específicas, precisas y salvavidas en múltiples áreas terapéuticas
- La creciente demanda de API de enfermedades raras se ve impulsada principalmente por la creciente prevalencia de enfermedades raras, la expansión de los oleoductos de drogas huérfanos, los incentivos regulatorios favorables y el aumento de la inversión en modalidades avanzadas como los biológicos, las terapias génicas y los tratamientos basados en ARN.
- América del Norte dominaba el mercado de sustancias antidrogas raras API / huérfano con la mayor cuota de ingresos del 41,5% en 2025, con el apoyo de un fuerte marco regulador de medicamentos huérfanos, un alto gasto de R plagaD y una presencia robusta debiofarmacéuticaempresas y CDMOs especializados, con Estados Unidos presenciando un crecimiento significativo tanto en la fabricación de API de fase clínica como comercial
- Se espera que Asia-Pacífico sea la región de más rápido crecimiento en el mercado de API de enfermedades raras durante el período de previsión impulsado por el aumento de la externalización de la fabricación de API, la expansión de los ecosistemas biotecnológicos, la mejora de la alineación reglamentaria y el aumento de las inversiones en el desarrollo de drogas raras en China, Japón, Corea del Sur y la India
- Las API de Biologics dominaron el mercado de sustancias farmacéuticas raras API / huérfano con una cuota de mercado de 58,3% en 2025, impulsado por su uso generalizado en terapias de sustitución de enzimas,anticuerpos monoclonales, y tratamientos basados en genes, junto con su fuerte eficacia para abordar enfermedades genéticas complejas y raras metabólicas
Report Scope and Rare Disease API / Orphan Drug Substance Market Segmentation
| Atributos | Rare Disease API / Substancia de Medicamentos Huérfanos |
| Segmentos cubiertos |
|
| Países cubiertos | América del Norte
Europa
Asia y el Pacífico
Oriente Medio y África
América del Sur
|
| Principales jugadores del mercado |
|
| Oportunidades de mercado |
|
| Valor añadido Data Infosets | Además de las ideas sobre escenarios de mercado como el valor de mercado, la tasa de crecimiento, la segmentación, la cobertura geográfica y los principales actores, los informes de mercado comisariados por Data Bridge Market Research también incluyen análisis profundos de expertos, epidemiología de pacientes, análisis de tuberías, análisis de precios y marco regulatorio |
Rare Disease API / Orphan Drug Substance Market Trends
Cambio hacia substancias avanzadas de drogas biológicas y genéticas
- Una tendencia significativa y aceleradora en el mercado mundial de sustancias de la enfermedad rara API / fármaco huérfano es el creciente cambio hacia las biologicas, terapias genéticas y sustancias de la RNA basadas en la droga, impulsado por su capacidad de atacar las causas genéticas subyacentes de las enfermedades raras y ultra-rare con alta precisión
- Por ejemplo, el creciente número de aprobaciones reglamentarias para terapias genéticas y celulares contra trastornos raros está intensificando la demanda de API de vectores virales, proteínas recombinantes y sustancias biológicas altamente especializadas fabricadas bajo estándares de calidad estrictos
- El avance de la biología molecular, la genómica y el diagnóstico de acompañantes está permitiendo el desarrollo de sustancias de medicamentos huérfanos altamente focalizadas, permitiendo a los fabricantes diseñar APIs adaptadas a mutaciones específicas o vías de enfermedad, mejorando así la eficacia del tratamiento y los resultados del paciente
- La creciente adopción de enfoques de medicina de precisión es alentar a las empresas farmacéuticas a invertir en una producción de API compleja, de bajo volumen y de alto valor, que requiere instalaciones especializadas, capacidades analíticas avanzadas y estricto cumplimiento reglamentario
- El aumento de las tecnologías de fabricación basadas en plataformas está apoyando la producción flexible y escalable de API huérfanos, permitiendo a los fabricantes manejar eficientemente múltiples programas de enfermedades raras simultáneamente
- Esta tendencia hacia sustancias farmacéuticas huérfanos más complejas y personalizadas está remodelando las estrategias de fabricación de API, con mayor énfasis en la producción de cubos pequeños, el manejo de alta potencia y las capacidades de cambio rápido
- En consecuencia, empresas como Lonza y Catalent están ampliando sus capacidades de biologica y terapia génica API para apoyar la creciente demanda de sustancias avanzadas de medicamentos huérfanos en múltiples indicios de enfermedades raras
Rare Disease API / Orphan Drug Substance Market Dynamics
Conductor
Ampliación de tuberías orfanosas e incentivos regulatorios favorables
- El creciente número de designaciones y aprobaciones de medicamentos huérfanos, respaldados por incentivos regulatorios favorables como la exclusividad del mercado, los créditos fiscales y las vías de revisión aceleradas, es una demanda clave para impulsar las API de enfermedades raras
- Por ejemplo, los marcos regulatorios en EE.UU., Europa y Japón han reducido significativamente los plazos de desarrollo para los medicamentos huérfanos, alentando a las empresas biofarmacéuticas a ampliar sus oleoductos de enfermedades raras e invertir en la fabricación especializada de API
- A medida que las tasas de sensibilización, detección y diagnóstico de las enfermedades raras mejoran a nivel mundial, aumenta la necesidad de un suministro constante y de alta calidad de las drogas, lo que contribuye directamente al crecimiento del mercado de las API huérfanos
- Además, el capital de riesgo sólido y la financiación pública para la investigación de enfermedades raras están permitiendo que las empresas de biotecnología más pequeñas avancen programas clínicos, aumentando la dependencia de la fabricación externa de API y los CDMOs especializados
- El enfoque cada vez mayor en las terapias de precisión y personalizadas, junto con el potencial comercial a largo plazo debido a la competencia limitada, sigue impulsando la demanda sostenida de sustancias de drogas huérfanos
- Aumentar el apoyo gubernamental y sin fines de lucro para el desarrollo de tratamientos de enfermedades raras está fortaleciendo la viabilidad a largo plazo de las inversiones en la fabricación de medicamentos huérfanos
- La capacidad de los medicamentos huérfanos para ordenar precios de primera calidad está mejorando el rendimiento de la inversión, alentando aún más la ampliación de la capacidad de producción de los API huérfanos
Restraint/Challenge
Manufacturing Complexity and Regulatory Compliance Barriers
- La producción de API de enfermedades raras a menudo implica procesos de fabricación complejos, requisitos de calidad estrictos y tamaños de lotes limitados, que pueden aumentar significativamente los costos de producción y los riesgos técnicos
- Por ejemplo, las sustancias farmacológicas y de terapia génica requieren instalaciones especializadas, personal altamente cualificado y sistemas avanzados de contención, lo que hace que la escala de fabricación sea técnicamente difícil y intensiva al capital
- El cumplimiento reglamentario en múltiples regiones añade mayor complejidad, ya que las sustancias de los medicamentos huérfanos deben cumplir normas diversas y cambiantes relacionadas con la seguridad, la trazabilidad y el control de calidad
- Estos desafíos pueden limitar el número de proveedores calificados de API, lo que podría conducir a limitaciones de oferta y costos más altos, lo que limita la expansión del mercado más amplia
- La disponibilidad limitada de materias primas especializadas y reactivos para las API de huérfanos avanzadas puede perturbar aún más los plazos de producción y aumentar la dependencia de los proveedores de nicho
- La necesidad de una amplia validación, largos plazos y estrictos controles de cambio post-aprobación pueden retrasar la agilidad de la fabricación y retrasar el suministro comercial de sustancias de drogas huérfanos
Rare Disease API / Orphan Drug Substance Market Scope
El mercado se segmenta sobre la base de API / tipo de sustancia de drogas, indicación terapéutica y usuario final.
- Por API / Tipo de Sustancia de Drogas
Sobre la base del tipo de API / sustancia de fármacos, el mercado global de las enfermedades raras API / substancia de medicamentos huérfanos se segmenta en APIs biológicas, API de moléculas pequeñas, API de vectores virales, API basadas en ARN y sustancias farmacéuticas relacionadas con la terapia celular. El segmento de APIs biológicas dominaba el mercado con la mayor cuota de ingresos del 58,3% en 2025, impulsado por el uso generalizado de anticuerpos monoclonales, terapias de sustitución de enzimas y proteínas recombinantes en el tratamiento de trastornos genéticos y metabólicos raros. Los biológicos ofrecen alta especificidad y eficacia clínica, lo que les convierte en la opción preferida para muchos programas de medicamentos huérfanos. La fuerte presencia de medicamentos biológicos aprobados y la expansión continua del oleoducto apoya aún más el dominio de este segmento. Además, los regímenes de precios premium y tratamiento a largo plazo contribuyen a aumentar la generación de ingresos. La experiencia de fabricación establecida y la familiaridad reglamentaria con los biológicos también refuerzan su posición principal.
Se espera que el segmento de API vectorial viral sea testigo del crecimiento más rápido durante el período de pronóstico, alimentado por el rápido avance de las terapias genéticas para enfermedades raras y ultra-raras. Aumentar las aprobaciones del virus asociado adeno (AAV) y las terapias basadas en vectores entivirales están impulsando una fuerte demanda de producción de vectores especializados. La alta necesidad médica sin atención, el potencial de tratamiento curativo y la creciente inversión en plataformas de terapia génica están acelerando la expansión de este segmento. La disponibilidad limitada de proveedores y los complejos requisitos de fabricación aumentan aún más la importancia estratégica y el impulso de crecimiento de las API de vectores virales.
- Por Indicación Terapéutica
Sobre la base de la indicación terapéutica, el mercado se segmenta en oncología, trastornos hematológicos, trastornos neurológicos neuromusculares, trastornos metabólicos " endocrinos, enfermedades infecciosas inmunológicas " raras, y trastornos cardiovasculares, oftálmicos y otros trastornos raros. El segmento de oncología dominó el mercado en 2025, debido al elevado número de designaciones de medicamentos huérfanos para cánceres raros y la inversión sostenida en terapias de cáncer selectivas. Los medicamentos de oncología raras a menudo dependen de API y biologics altamente potentes, contribuyendo significativamente a la demanda global de API. Los oleoductos clínicos fuertes, las aprobaciones regulatorias aceleradas y los costos de tratamiento más altos apoyan aún más el liderazgo de ingresos de este segmento. Además, las empresas farmacéuticas priorizan la oncología rara debido a beneficios favorables de reembolso y exclusividad del mercado.
Se proyecta que el segmento de trastornos neurológicos y neuromusculares crezca a la velocidad más rápida durante el período de pronóstico, impulsado por el aumento de la investigación en condiciones neurológicas genéticas como la atrofia muscular espinal, la distrofia muscular duchena y las epilepsias raras. Los avances en terapia génica, medicamentos basados en ARN y medicamentos de precisión están transformando enfoques de tratamiento en este espacio. El aumento de las tasas de diagnóstico y el firme apoyo a la promoción están impulsando aún más la actividad de desarrollo. Dado que muchas de estas terapias requieren API complejas, la demanda de sustancias especializadas de drogas se está expandiendo rápidamente dentro de este segmento.
- Por Usuario final
Sobre la base del usuario final, el mercado mundial de sustancias farmacéuticas raras API / orfanato se segmenta en empresas biofarmacéuticas, organizaciones de elaboración de contratos (CDMOs), e institutos de investigación y fabricantes de especialidades. El segmento de las empresas biofarmacéuticas representó la mayor cuota de mercado en 2025, impulsada por su propiedad de oleoductos huérfanos y control directo sobre la fabricación comercial para terapias de alto valor. Las grandes y medianas empresas de biofarma invierten fuertemente en asegurar un suministro confiable de API para proteger los períodos de exclusividad y asegurar una calidad de producto consistente. La fabricación interna de APIs críticas suele ser preferida por razones estratégicas e intelectuales. El dominio de este segmento se ve reforzado aún más por una sólida capacidad financiera y una sólida experiencia normativa.
Se espera que en el segmento de los OMD se registre el crecimiento más rápido durante el período previsto, apoyado por el aumento de las tendencias de la contratación externa entre las empresas biotecnológicas y farmacéuticas. La complejidad de las API de huérfanos, combinadas con pequeños tamaños de lotes y altos requisitos de capital, es alentador que los patrocinadores dependan de los CDMO especializados. Los CDMO ofrecen tecnologías flexibles de fabricación, apoyo reglamentario y avanzadas adaptadas para sustancias raras de drogas. A medida que las empresas de biotecnología más pequeñas impulsan la innovación en los medicamentos huérfanos, la dependencia de los CDMOs para la producción de API escalable y compatible se está acelerando rápidamente.
Rare Disease API / Orphan Drug Substance Market Regional Analysis
- América del Norte dominaba el mercado de sustancias farmacéuticas raras API / huérfano con la mayor cuota de ingresos del 41,5% en 2025, con el apoyo de un fuerte marco regulador de drogas huérfanos, un alto gasto de R plagaD y una presencia robusta de empresas biofarmacéuticas y CDMOs especializados
- Las empresas de la región tienen un alto valor en las capacidades de fabricación avanzada, el estricto cumplimiento de la calidad y el suministro fiable de sustancias complejas de drogas, en particular para las biológicas, terapias genéticas y otras API de alto valor
- Esta dirección generalizada del mercado está respaldada además por una alta concentración de aprobaciones de medicamentos huérfanos, una fuerte financiación para la investigación de enfermedades raras, y la presencia de las principales empresas biofarmacéuticas y los CDMO especializados, estableciendo América del Norte como el principal centro para el desarrollo y producción de API de enfermedades raras
U.S. Rare Disease API / Orphan Drug Substance Market Insight
El mercado de sustancias farmacéuticas raras de EE.UU. API / antidrogas huérfanos capturó la mayor cuota de ingresos dentro de América del Norte en 2025, impulsada por un fuerte marco regulador de medicamentos huérfanos, inversiones extensas R plagaD y una alta concentración de empresas biofarmacéuticas y biotecnológicas. Los fabricantes priorizan cada vez más el desarrollo y el suministro seguro de API complejas para apoyar la expansión de los oleoductos de drogas huérfanos. La presencia de incentivos favorables como la exclusividad del mercado, los créditos fiscales y las vías de aprobación aceleradas sigue estimulando la demanda de sustancias farmacéuticas especializadas. Además, la fuerte función de los MDL y la infraestructura de fabricación avanzada contribuye considerablemente al crecimiento sostenido del mercado.
Europe Rare Disease API / Orphan Drug Substance Market Insight
Se prevé que el mercado de sustancias de la enfermedad rara de Europa API / fármacos huérfanos se expanda en un CAGR sustancial durante el período de previsión, impulsado principalmente por políticas de fármacos huérfanos de EMA de apoyo e inversiones crecientes en investigación de enfermedades raras. El aumento de la concienciación, la mejora de las tasas de diagnóstico y las colaboraciones transfronterizas están fomentando el desarrollo de los medicamentos huérfanos en toda la región. Los fabricantes europeos enfatizan la calidad, trazabilidad y cumplimiento regulatorio, apoyando la demanda constante de API de alto valor. El crecimiento se observa en los modelos de fabricación impulsados por innovadores y subcontratados, en particular para las terapias biológicas y avanzadas.
U.K. Rare Disease API / Orphan Drug Substance Market Insight
Se prevé que el mercado de sustancias de drogas de U.K. raras enfermedades API / huérfanos crezca en un CAGR notable durante el período de previsión, apoyado por una fuerte colaboración académica-industria e iniciativas de enfermedades raras respaldadas por el gobierno. El ecosistema avanzado de ciencias de la vida de U.K. fomenta el desarrollo temprano de medicamentos huérfanos, aumentando la demanda de API en estadio clínico. La inversión continua en biologics e investigación de terapia génica está fortaleciendo las perspectivas del mercado. Además, la armonización reglamentaria con las normas mundiales aumenta el atractivo del país para las asociaciones de fabricación y desarrollo de las API huérfanos.
Alemania Enfermedades Raras API / Substancia de Medicamentos Huérfanos Insight
Se espera que el mercado alemán de sustancias farmacéuticas raras se expanda en un CAGR considerable durante el período previsto, alimentado por una sólida base de fabricación farmacéutica y un fuerte énfasis en la innovación y la calidad. El liderazgo de Alemania en la producción de biologics y tecnologías avanzadas de fabricación apoya la demanda constante de sustancias complejas de los huérfanos. El enfoque del país en el cumplimiento, seguridad y fabricación de precisión se ajusta bien a los estrictos requisitos de las API de enfermedades raras. El aumento de la inversión en terapias avanzadas fortalece aún más las perspectivas de crecimiento del mercado.
Asia-Pacific Rare Disease API / Orphan Drug Substance Market Insight
El mercado de sustancias farmacéuticas raras de Asia y el Pacífico está preparado para crecer en la CAGR más rápida durante el período de previsión, impulsado por la ampliación de las capacidades biotecnológicas, el aumento de las inversiones sanitarias y el aumento de la externalización de los mercados occidentales. Países como China, Japón e India están fortaleciendo sus marcos reguladores de enfermedades raras e infraestructuras de fabricación. Las ventajas de coste de la región y la creciente experiencia técnica atraen a las empresas biofarmacéuticas mundiales que buscan una producción de API escalable. Esta tendencia está acelerando significativamente la expansión del mercado en la APAC.
Japan Rare Disease API / Orphan Drug Substance Market Insight
El mercado de sustancias farmacéuticas raras de Japón está cobrando impulso debido al fuerte apoyo gubernamental para el desarrollo de medicamentos huérfanos y las capacidades avanzadas de fabricación farmacéutica. Japón asigna gran importancia a la calidad, la seguridad y la innovación, impulsando la demanda de sustancias de drogas altamente especializadas. El enfoque del país en las enfermedades genéticas y neurológicas raras está aumentando la necesidad de API complejas, incluyendo biológicas y sustancias basadas en el ARN. Un envejecimiento de la población y una creciente prevalencia de trastornos raros apoyan aún más el crecimiento del mercado.
India Rare Disease API / Orphan Drug Substance Market Insight
El mercado de drogas de la India de la rara enfermedad de API y la droga de huérfanos representó una importante cuota de ingresos en Asia-Pacífico en 2025, atribuida a una sólida experiencia de fabricación de API, competitividad de costos y inversiones biotecnológicas en expansión. India está surgiendo como proveedor clave de API de huérfanos pequeños y cada vez más biológicos para mercados globales. Las iniciativas gubernamentales que apoyan el desarrollo del tratamiento de las enfermedades raras y la fabricación local están mejorando las perspectivas de mercado. La creciente presencia de MDL y fabricantes de contratos nacionales está reforzando aún más el papel de la India en la cadena mundial de suministro de estupefacientes huérfanos.
Rare Disease API / Orphan Drug Substance Market Share
La industria de substancias de drogas por enfermedades raras está dirigida principalmente por empresas bien establecidas, incluyendo:
- Lonza Ltd (Suiza)
- Catalent, Inc. (U.S.)
- WuXi AppTec Co., Ltd. (China)
- Pfizer Inc. (U.S.)
- Novartis AG (Suiza)
- F. Hoffmann-La Roche Ltd (Suiza)
- Bristol-Myers Squibb Company (Estados Unidos)
- Amgen Inc. (U.S.)
- Sanofi (Francia)
- Takeda Pharmaceutical Company Limited (Japón)
- AbbVie Inc. (Estados Unidos)
- GSK plc (U.K.)
- Bayer AG (Alemania)
- Incorporated (U.S.)
- Biogen Inc. (Estados Unidos)
- PTC Therapeutics, Inc. (U.S.)
- Suecia Orphan Biovitrum AB (Suecia)
- SOM Innovation Biotech, S.A. (España)
- Ultragenyx Pharmaceutical Inc. (U.S.)
¿Cuáles son los desarrollos recientes en la API de enfermedades raras globales / mercado de sustancias tóxicas?
- En agosto de 2025, la FDA de EE.UU. concedió la aprobación a Papzimeos (zopapogene imadenovec), la primera inmunoterapia para la papilomatosis respiratoria recurrente (RRP), una condición rara designada por huérfano, subrayando los avances inmunoterapéuticos basados en genes para enfermedades raras
- En abril de 2025, el Acelerador de Terapéutica Huérfana sin fines de lucro anunció alianzas clave encaminadas a promover las vías de desarrollo y comercialización de terapias de enfermedades ultrarrestres, abordando retos históricos en la financiación y el avance de los candidatos a medicamentos huérfanos
- En enero de 2024, el paisaje de medicamentos huérfanos de la FDA vio una expansión significativa con un número récord de aprobaciones (28 nuevos medicamentos huérfanos), incluyendo terapias de primera clase para condiciones como la ataxia de Friedreich y el síndrome de Rett, destacando el rápido crecimiento en el desarrollo terapéutico de enfermedades raras
- En agosto de 2023, la FDA de EE.UU. aprobó pozelimab (Veopoz) como el primer tratamiento para la enfermedad de CHAPLE, un trastorno del sistema de complementos ultra-rare, representando una nueva terapia anticuerpo monoclonal recombinante que aborda una afección fatal de otra manera
- En mayo de 2023, la FDA de EE.UU. aprobó Adzynma (apadamtase alfa), una terapia de sustitución de enzimas recombinantes ADAMTS13 para la purpura trombocitopénica trombocótica congénita (cTTP), marcando la primera biológica aprobada abordando este trastorno de coagulación de sangre ultra-rare y ampliando opciones de reemplazo de enzimas para pacientes de enfermedades raras
SKU-
Obtenga acceso en línea al informe sobre la primera nube de inteligencia de mercado del mundo
- Panel de análisis de datos interactivo
- Panel de análisis de empresas para oportunidades con alto potencial de crecimiento
- Acceso de analista de investigación para personalización y consultas
- Análisis de la competencia con panel interactivo
- Últimas noticias, actualizaciones y análisis de tendencias
- Aproveche el poder del análisis de referencia para un seguimiento integral de la competencia
Metodología de investigación
La recopilación de datos y el análisis del año base se realizan utilizando módulos de recopilación de datos con muestras de gran tamaño. La etapa incluye la obtención de información de mercado o datos relacionados a través de varias fuentes y estrategias. Incluye el examen y la planificación de todos los datos adquiridos del pasado con antelación. Asimismo, abarca el examen de las inconsistencias de información observadas en diferentes fuentes de información. Los datos de mercado se analizan y estiman utilizando modelos estadísticos y coherentes de mercado. Además, el análisis de la participación de mercado y el análisis de tendencias clave son los principales factores de éxito en el informe de mercado. Para obtener más información, solicite una llamada de un analista o envíe su consulta.
La metodología de investigación clave utilizada por el equipo de investigación de DBMR es la triangulación de datos, que implica la extracción de datos, el análisis del impacto de las variables de datos en el mercado y la validación primaria (experto en la industria). Los modelos de datos incluyen cuadrícula de posicionamiento de proveedores, análisis de línea de tiempo de mercado, descripción general y guía del mercado, cuadrícula de posicionamiento de la empresa, análisis de patentes, análisis de precios, análisis de participación de mercado de la empresa, estándares de medición, análisis global versus regional y de participación de proveedores. Para obtener más información sobre la metodología de investigación, envíe una consulta para hablar con nuestros expertos de la industria.
Personalización disponible
Data Bridge Market Research es líder en investigación formativa avanzada. Nos enorgullecemos de brindar servicios a nuestros clientes existentes y nuevos con datos y análisis que coinciden y se adaptan a sus objetivos. El informe se puede personalizar para incluir análisis de tendencias de precios de marcas objetivo, comprensión del mercado de países adicionales (solicite la lista de países), datos de resultados de ensayos clínicos, revisión de literatura, análisis de mercado renovado y base de productos. El análisis de mercado de competidores objetivo se puede analizar desde análisis basados en tecnología hasta estrategias de cartera de mercado. Podemos agregar tantos competidores sobre los que necesite datos en el formato y estilo de datos que esté buscando. Nuestro equipo de analistas también puede proporcionarle datos en archivos de Excel sin procesar, tablas dinámicas (libro de datos) o puede ayudarlo a crear presentaciones a partir de los conjuntos de datos disponibles en el informe.