Оценки клинических результатов (COA) — это инструменты и меры, используемые в клинических исследованиях и медицинских учреждениях для оценки влияния медицинских процедур, вмешательств или состояний на здоровье и благополучие пациентов. Они предназначены для сбора информации непосредственно от пациентов об их симптомах, функционировании и качестве жизни. Эти оценки играют решающую роль в понимании эффективности и безопасности медицинских вмешательств и помогают специалистам здравоохранения принимать обоснованные решения.
Общая численность населения и бремя болезней растут во всем мире, что увеличивает спрос на лекарства и заставляет ведущие фармацевтические компании проводить все больше клинических испытаний для увеличения поставок эффективных лекарственных средств на рынок. Кроме того, рост числа клинических испытаний во всем мире и необходимость разработки лекарств в течение более короткого периода времени с высокой точностью приводят к принятию платформ eCOA специалистами по клиническим исследованиям, что увеличивает спрос на решения eCOA на рынке.
Доступ к полному отчету по адресу https://www.databridgemarketresearch.com/reports/global-electronic-clinical-outcome-assessment-ecoa-market
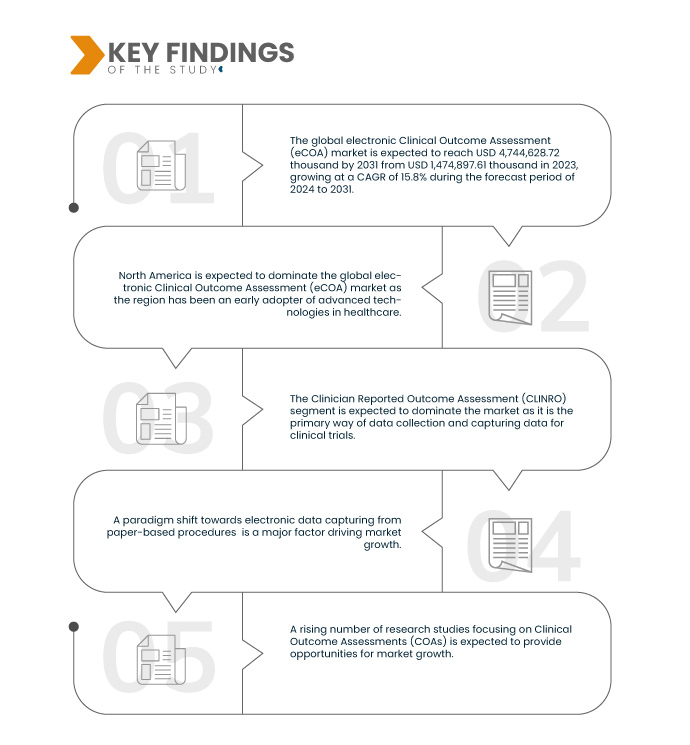
По данным исследования рынка Data Bridge, ожидается, что глобальный рынок электронной оценки клинических результатов (ECOA) к 2031 году достигнет 4 744 628,72 тыс. долларов США по сравнению с 1 474 897,61 тыс. долларов США в 2023 году, при этом среднегодовой темп роста составит 15,8% в прогнозируемый период с 2024 по 2031 год.
Основные выводы исследования
Правительственные инициативы по внедрению электронных клинических платформ
Правительственные инициативы включают стратегические усилия по модернизации и оцифровке процесса клинических исследований, направленные на повышение эффективности, качества данных и соответствия нормативным требованиям. Эти инициативы часто направлены на поощрение использования электронных инструментов и технологий для сбора, управления и анализа данных в клинических испытаниях. Эти усилия признают потенциал электронных инструментов для революционного изменения сбора, управления и анализа данных в клинических испытаниях . Правительства поощряют переход отрасли от трудоемких бумажных методов путем создания нормативных рамок, которые подтверждают целостность и безопасность электронных записей. Финансовые стимулы, такие как финансирование и гранты, еще больше мотивируют исследовательские институты и фармацевтические компании использовать решения eClinical.
Область отчета и сегментация рынка
Отчет Метрика
|
Подробности
|
Прогнозируемый период
|
2024-2031
|
Базовый год
|
2023
|
Исторические годы
|
2022 (Можно настроить на 2016–2021)
|
Количественные единицы
|
Доход в тыс. долл. США
|
Охваченные сегменты
|
Тип (оценка результатов, сообщаемая врачом (Clinician Reporting Outcome Assessment, CLINRO), оценка результатов, сообщаемых пациентом (Patient Reporting Outcome Assessment, PRO), оценка результатов, сообщаемых наблюдателем (Observer Reporting Outcome Assessment, OBSRO) и оценка результатов эффективности (Perfo)), Модальность (решения на основе сайта, веб-решения и портативные устройства), Конечный пользователь (контрактные исследовательские организации (CRO), фармацевтические и биотехнологические фирмы, компании по производству медицинского оборудования, больницы/поставщики медицинских услуг, компании по оказанию консалтинговых услуг, академические и исследовательские институты и другие), Режим доставки (облачный и размещенный в Интернете)
|
Страны, охваченные
|
США, Канада, Мексика, Великобритания, Германия, Испания, Франция, Италия, Швейцария, Нидерланды, Бельгия, Турция, Россия, Швеция, Дания, Финляндия, Норвегия, Польша и остальные страны Европы, Китай, Япония, Австралия, Южная Корея, Индия, Сингапур, Таиланд, Малайзия, Индонезия, Филиппины, Новая Зеландия, Вьетнам, Тайвань и остальные страны Азиатско-Тихоокеанского региона, Бразилия, Аргентина и остальные страны Южной Америки, Южная Африка, ОАЭ, Израиль, Саудовская Аравия, Египет, Кувейт, Оман, Катар, Бахрейн и остальные страны Ближнего Востока и Африки
|
Охваченные участники рынка
|
Medidata (дочерняя компания Dassault Systèmes) (США), Clario (США), IQVIA Inc. (США), Signant Health (США), ArisGlobal (США), TransPerfect Life Sciences (США), WCG Clinical (США), Kayentis (Франция), Castor (Нидерланды), Suvoda LLC (США), Vitalograph (Ирландия), Medable Inc. (США), Cloudbyz (США), YPrime LLC (США), Merative (Австралия), EvidentIQ (США), Climedo Health GmbH (Германия), RAYLYTIC GmbH (Германия), Clinical Ink (США), Assistek (США), Pattern Health Technologies, Inc. (США), clincapture (США), Crucial Data Solutions (США) и другие
|
Данные, отраженные в отчете
|
Помимо аналитических данных о рыночных сценариях, таких как рыночная стоимость, темпы роста, сегментация, географический охват и основные игроки, рыночные отчеты, подготовленные Data Bridge Market Research, также включают в себя углубленный экспертный анализ, эпидемиологию пациентов, анализ воронки продаж, анализ ценообразования и нормативную базу.
|
Анализ сегмента
Глобальный рынок электронной оценки клинических результатов (eCOA) разделен на четыре основных сегмента в зависимости от типа, модальности, конечного пользователя и способа доставки.
- По типу рынок сегментирован на оценку результатов, сообщаемых клиницистами (CLINRO), оценку результатов, сообщаемых пациентами (PRO), оценку результатов, сообщаемых наблюдателями (OBSRO), и оценку результатов эффективности (PERFO).
Ожидается, что в 2024 году сегмент оценки клинических результатов (CLINRO) будет доминировать на мировом рынке электронной оценки клинических результатов (eCOA).
Ожидается, что в 2024 году сегмент оценки результатов клинических исследований (CLINRO) будет доминировать на рынке с долей рынка 45,39%, поскольку это основной способ сбора и фиксации данных для клинических испытаний.
- На основе модальности рынок сегментируется на решения на базе сайта, веб-решения и карманные решения.
Ожидается, что в 2024 году сегмент решений на базе сайта будет доминировать на мировом рынке электронной оценки клинических результатов (eCOA).
Ожидается, что в 2024 году сегмент решений на базе сайта будет доминировать на рынке с долей рынка 54,97%, поскольку они пользуются большим спросом из-за обеспечиваемой ими безопасности и возможности предоставления высоконастраиваемых функций.
- На основе конечного пользователя рынок сегментирован на контрактные исследовательские организации (CRO), фармацевтические и биотехнологические фирмы, компании по производству медицинских приборов, больницы/поставщики медицинских услуг, консалтинговые компании, академические и научно-исследовательские институты и т. д. Ожидается, что в 2024 году сегмент контрактных исследовательских организаций (CRO) будет доминировать на рынке с долей рынка 45,42%.
- На основе способа доставки рынок сегментируется на облачный и веб-хостинг. Ожидается, что в 2024 году облачный сегмент будет доминировать на рынке с долей рынка 73,31%
Основные игроки
Компания Data Bridge Market Research анализирует Medidata (дочернюю компанию Dassault Systèmes) (США), IQVIA Inc (США), Clario (США), Signant Health (США) и ArisGlobal (США) как основных игроков, работающих на мировом рынке электронной оценки клинических результатов (eCOA).
Последние события
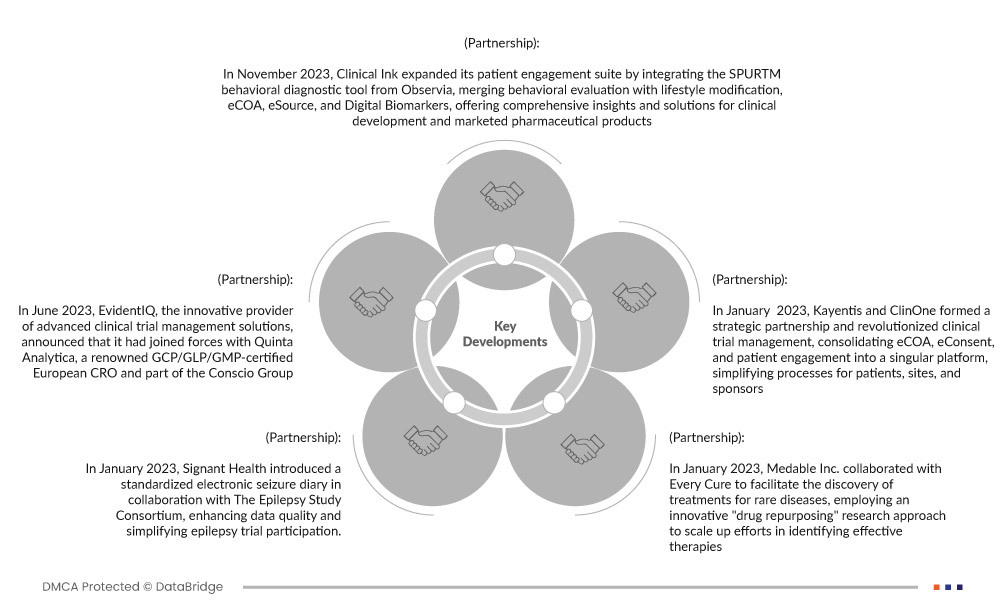
- В ноябре 2023 года Clinical Ink расширила свой набор инструментов для вовлечения пациентов, интегрировав инструмент поведенческой диагностики SPURTM от Observia, объединив поведенческую оценку с модификацией образа жизни, eCOA, eSource и цифровыми биомаркерами, предлагая комплексные идеи и решения для клинической разработки и маркетинга фармацевтических продуктов. Партнерство позволило компании создать надежную платформу, включающую поведенческие данные наряду с клиническими результатами и цифровыми биомаркерами, повышая вовлеченность и приверженность пациентов, а также стандартизируя рекомендации по образу жизни, что приводит к улучшению результатов испытаний и более целостному пониманию поведения пациентов.
- В июне 2023 года EvidentIQ, инновационный поставщик передовых решений для управления клиническими испытаниями, объявил об объединении усилий с Quinta Analytica, известной сертифицированной GCP/GLP/GMP европейской CRO и частью Conscio Group. Это сотрудничество направлено на повышение эффективности и результативности процессов сбора данных для исследований фазы 1 с использованием системы Clindex eClinical от EvidentIQ
- В январе 2023 года Signant Health в сотрудничестве с The Epilepsy Study Consortium представила стандартизированный электронный дневник приступов, что повысило качество данных и упростило участие в испытаниях эпилепсии. Эта инициатива расширила портфолио Signant, предоставив индивидуальное решение, которое усилило их возможности по созданию доказательств для испытаний эпилепсии, укрепив доверие среди спонсоров и CRO. Разработка стандартизированного электронного дневника приступов в сотрудничестве с The Epilepsy Study Consortium расширила экспертные знания и предложения Signant Health, еще больше укрепив компанию как лидера в создании доказательств для клинических испытаний
- В январе 2023 года Medable Inc. сотрудничала с Every Cure, чтобы облегчить открытие методов лечения редких заболеваний, используя инновационный исследовательский подход «перепрофилирования лекарств» для масштабирования усилий по выявлению эффективных методов лечения. Это привело к решению ключевых проблем отрасли
- В январе 2023 года Kayentis и ClinOne сформировали стратегическое партнерство и произвели революцию в управлении клиническими испытаниями, объединив eCOA, eConsent и вовлечение пациентов в единую платформу, упростив процессы для пациентов, центров и спонсоров. Это стратегическое сотрудничество укрепило их позиции как лидеров отрасли, предоставляя интегрированные решения и услуги, улучшая процесс клинических испытаний для всех заинтересованных сторон. Это сотрудничество значительно улучшило опыт клинических испытаний, предложив единую точку входа для различных типов испытаний, снизив сложность, оптимизировав операции и укрепив репутацию ведущих поставщиков в области клинических испытаний.
Региональный анализ
Географически странами, охваченными глобальным рынком электронной оценки клинических результатов (eCOA), являются США, Канада, Мексика, Великобритания, Германия, Испания, Франция, Италия, Швейцария, Нидерланды, Бельгия, Турция, Россия, Швеция, Дания, Финляндия, Норвегия, Польша и остальные страны Европы, Китай, Япония, Австралия, Южная Корея, Индия, Сингапур, Таиланд, Малайзия, Индонезия, Филиппины, Новая Зеландия, Вьетнам, Тайвань и остальные страны Азиатско-Тихоокеанского региона, Бразилия, Аргентина и остальные страны Южной Америки, Южная Африка, ОАЭ, Израиль, Саудовская Аравия, Египет, Кувейт, Оман, Катар, Бахрейн и остальные страны Ближнего Востока и Африки.
Согласно анализу Data Bridge Market Research:
Ожидается, что Северная Америка будет доминировать на мировом рынке электронной оценки клинических результатов (eCOA)
Ожидается, что на рынке будет доминировать Северная Америка, поскольку регион обладает обширной инфраструктурой здравоохранения в сочетании с надежной сетью фармацевтических и биотехнологических предприятий, а также способствует широкому внедрению исследований и технологий.
По оценкам, Азиатско-Тихоокеанский регион является самым быстрорастущим регионом на мировом рынке электронной оценки клинических результатов (eCOA).
Азиатско-Тихоокеанский регион считается самым быстрорастущим регионом на рынке из-за его строгих систем регулирования в различных отраслях. Эти требования часто требуют от организаций наличия комплексных процессов и технологий управления рисками для обеспечения соответствия. В результате растет спрос на решения и услуги по управлению рисками.
Для получения более подробной информации о глобальном отчете о рынке электронной оценки клинических результатов (eCOA) нажмите здесь – https://www.databridgemarketresearch.com/reports/global-electronic-clinical-outcome-assessment-ecoa-market