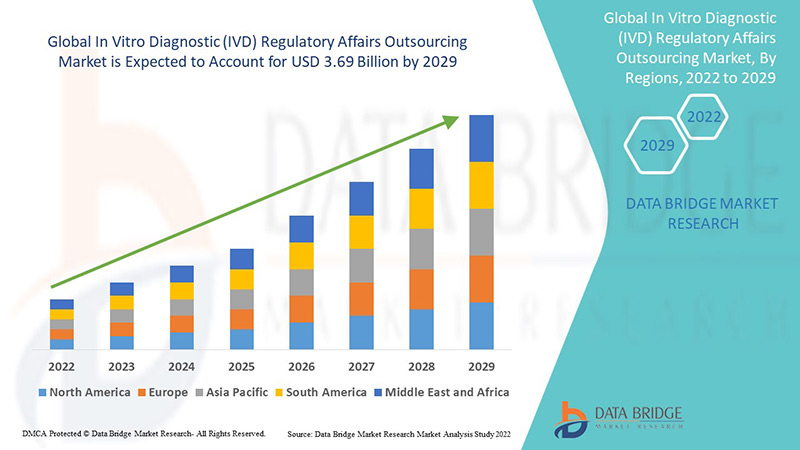
Global In Vitro Diagnostic Ivd Regulatory Affairs Outsourcing Market
Taille du marché en milliards USD
TCAC :
% 
 USD
674,277.97 Thousand
USD
1,830,957.45 Thousand
2021
2029
USD
674,277.97 Thousand
USD
1,830,957.45 Thousand
2021
2029
| 2022 –2029 | |
| USD 674,277.97 Thousand | |
| USD 1,830,957.45 Thousand | |
|
|
|
|
Marché mondial de l'externalisation des affaires réglementaires du diagnostic in vitro (DIV), par service (rédaction et soumissions réglementaires, enregistrement réglementaire et demandes d'essais cliniques , conseil réglementaire, représentation juridique, services de gestion des données, services de fabrication et de contrôle de produits chimiques (CMC) et autres), indication (oncologie, neurologie, cardiologie, chimie clinique et immuno-essais, médecine de précision, maladies infectieuses, diabète, tests génétiques, VIH/SIDA, hématologie, tests de médicaments/pharmacogénomique, transfusion sanguine, point de service et autres), mode de déploiement (cloud et sur site), taille de l'organisation (petites et moyennes entreprises (PME) et grandes entreprises), stade (clinique, préclinique et PMA (autorisation post-commercialisation)), classe (classe I, classe II et classe III), utilisateur final (sociétés pharmaceutiques, sociétés de dispositifs médicaux, sociétés de biotechnologie et autres) - Tendances et prévisions du secteur 2029
Analyse du marché et taille
Les entreprises de santé ont rencontré des difficultés pour se conformer aux normes réglementaires, notamment en raison de la pandémie de COVID-19 (coronavirus). Pour instaurer une culture axée sur la qualité au sein des entreprises de technologies médicales, les cabinets de conseil utilisent des logiciels de gestion de la qualité (SGQ). Les entreprises impliquées dans l' externalisation des affaires réglementaires en matière de diagnostic in vitro (DIV) offrent un accompagnement personnalisé aux établissements de santé.
Le déploiement de l'externalisation se traduit par la conclusion d'accords d'externalisation à long terme. Le marché mondial de l'externalisation des affaires réglementaires en matière de diagnostic in vitro (DIV) était évalué à 1,6 milliard USD en 2021 et devrait atteindre 3,69 milliards USD d'ici 2029, enregistrant un TCAC de 11 % sur la période de prévision 2022-2029. Les sociétés pharmaceutiques devraient connaître une forte croissance grâce à l'augmentation du nombre d'approbations cliniques.
Définition du marché
Les affaires réglementaires jouent un rôle crucial dans le secteur des dispositifs de diagnostic in vitro (DIV). Elles concernent le cycle de vie de divers produits de santé et offrent un soutien et une orientation stratégiques, tactiques et opérationnels aux fabricants pour les aider à respecter le cadre réglementaire.
Portée du rapport et segmentation du marché
|
Rapport métrique |
Détails |
|
Période de prévision |
2022 à 2029 |
|
Année de base |
2021 |
|
Années historiques |
2020 (personnalisable de 2019 à 2014) |
|
Unités quantitatives |
Chiffre d'affaires en millions USD, volumes en unités, prix en USD |
|
Segments couverts |
Service (rédaction et soumissions réglementaires, demandes d'enregistrement réglementaire et d'essais cliniques, conseil réglementaire, représentation juridique, services de gestion des données, services de fabrication et de contrôle de produits chimiques (CMC) et autres), indication (oncologie, neurologie, cardiologie, chimie clinique et immuno-essais, médecine de précision, maladies infectieuses, diabète, tests génétiques, VIH/SIDA, hématologie, tests de médicaments/pharmacogénomique, transfusion sanguine, point de service et autres), mode de déploiement (cloud et sur site), taille de l'organisation (petites et moyennes entreprises [PME] et grandes entreprises), stade (clinique, préclinique et PMA (autorisation post-commercialisation)), classe (classe I, classe II et classe III), utilisateur final (sociétés pharmaceutiques, sociétés de dispositifs médicaux, sociétés de biotechnologie et autres) |
|
Pays couverts |
États-Unis, Canada et Mexique en Amérique du Nord, Allemagne, France, Royaume-Uni, Pays-Bas, Suisse, Belgique, Russie, Italie, Espagne, Turquie, reste de l'Europe en Europe, Chine, Japon, Inde, Corée du Sud, Singapour, Malaisie, Australie, Thaïlande, Indonésie, Philippines, reste de l'Asie-Pacifique (APAC) en Asie-Pacifique (APAC), Arabie saoudite, Émirats arabes unis, Afrique du Sud, Égypte, Israël, reste du Moyen-Orient et de l'Afrique (MEA) en tant que partie du Moyen-Orient et de l'Afrique (MEA), Brésil, Argentine et reste de l'Amérique du Sud en tant que partie de l'Amérique du Sud. |
|
Acteurs du marché couverts |
Freyr Solutions (Inde), PPD Inc. (États-Unis), EMERGO (États-Unis), ICON (Santé), Parexel International Corporation (États-Unis), CRITERIUM, INC. (États-Unis), Groupe ProductLife SA (France), Labcorp Drug Development (États-Unis), WuXi AppTec (Chine), Genpact (États-Unis), Medpace (États-Unis), Dor Pharmaceutical Services (Israël), Qserve (Pays-Bas), entre autres |
|
Opportunités de marché |
|
Dynamique du marché de l'externalisation des affaires réglementaires en matière de diagnostic in vitro (DIV)
Cette section vise à comprendre les moteurs, les avantages, les opportunités, les contraintes et les défis du marché. Tous ces éléments sont détaillés ci-dessous :
- Utilisation intensive dans le secteur de la santé
L'essor des services d'externalisation dans le secteur de la santé est l'un des principaux moteurs de la croissance du marché de l'externalisation des affaires réglementaires en matière de diagnostic in vitro (DIV). L'essor des activités d'expansion géographique visant à accélérer les approbations sur les marchés locaux contribue également à cette croissance.
- Recherche et développement
L’augmentation des activités de recherche et développement, qui augmente le volume des demandes d’essais cliniques et l’enregistrement des produits, accélère la croissance du marché.
- Approbations cliniques
On observe une augmentation de la demande d'externalisation des affaires réglementaires en matière de diagnostic in vitro (DIV), les entreprises étant soumises à une pression constante pour obtenir rapidement les autorisations cliniques des autorités réglementaires. La demande de services d'affaires réglementaires augmente donc en raison de ces mesures.
Opportunités
En outre, le développement de biomarqueurs et de tests spécifiques à la maladie et l'importance des diagnostics compagnons étendent les opportunités rentables aux acteurs du marché au cours de la période de prévision de 2022 à 2029. De plus, l'augmentation des investissements élargira encore le marché.
Contraintes/Défis
D'autre part, l'évolution de la réglementation concernant l'externalisation des affaires réglementaires pour les dispositifs médicaux et les diagnostics in vitro (DIV) devrait freiner la croissance du marché. De plus, le manque d'infrastructures dans les services de santé devrait constituer un défi pour le marché de l'externalisation des affaires réglementaires pour les diagnostics in vitro (DIV) sur la période de prévision 2022-2029.
Ce rapport sur le marché de l'externalisation des affaires réglementaires pour le diagnostic in vitro (DIV) détaille les évolutions récentes, la réglementation commerciale, l'analyse des importations et exportations, l'analyse de la production, l'optimisation de la chaîne de valeur, la part de marché, l'impact des acteurs nationaux et locaux, l'analyse des opportunités de revenus émergents, l'évolution de la réglementation, l'analyse stratégique de la croissance du marché, la taille du marché, la croissance des catégories de marché, les niches d'application et la domination du marché, les homologations et les lancements de produits, les expansions géographiques et les innovations technologiques. Pour plus d'informations sur le marché de l'externalisation des affaires réglementaires pour le diagnostic in vitro (DIV), contactez Data Bridge Market Research pour obtenir un briefing d'analyste. Notre équipe vous aidera à prendre une décision éclairée et à stimuler votre croissance.
Impact du Covid-19 sur le marché des tests de diagnostic
La COVID-19 a eu un impact négatif sur le secteur de la santé. Les principaux acteurs ont adopté des stratégies innovantes face à l'évolution rapide de la situation pendant l'épidémie. Les pays ont adopté des changements cruciaux dans le système de santé jusqu'à ce que la crise passe au second plan. Les réformes du système de santé devraient permettre de maîtriser les coûts, d'améliorer l'accès aux soins et de progresser technologiquement dans les années à venir. Une augmentation de la demande d'externalisation des affaires réglementaires en matière de diagnostic in vitro (DIV) a été constatée en raison de l'importance accordée au diagnostic, aux soins et aux consultations à distance. Ces services allègent la charge des hôpitaux dans le contexte post-pandémique.
Développements récents
- Le magazine technologique USA-9 a classé Freyr parmi les « 10 meilleurs fournisseurs de solutions technologiques de 2021 » en novembre 2021. USA-9.com, un magazine technologique, a classé Freyr Solutions, leader mondial des solutions et services réglementaires, parmi les « 10 meilleurs fournisseurs de solutions technologiques de 2021 ». Fryer continue de concevoir des solutions logicielles innovantes et d'accompagner ses clients dans leurs objectifs de conformité. Cela a contribué à accroître la popularité de l'entreprise.
Portée et taille du marché mondial de l'externalisation des affaires réglementaires en matière de diagnostic in vitro (DIV)
Le marché de l'externalisation des affaires réglementaires pour le diagnostic in vitro (DIV) est segmenté selon les services, l'indication, le mode de déploiement, la taille de l'organisation, le stade d'avancement, la classe et l'utilisateur final. La croissance de ces segments vous permettra d'analyser les segments à faible croissance des industries et de fournir aux utilisateurs une vue d'ensemble et des informations précieuses sur le marché, facilitant ainsi la prise de décisions stratégiques pour identifier les applications clés.
Services
- Rédaction et soumissions réglementaires
- Enregistrement réglementaire et demandes d'essais cliniques
- Conseil réglementaire
- Représentation juridique
- Services de gestion des données
- Services de fabrication et de contrôle de produits chimiques (CMC)
- Autres
Sur la base des services, le marché mondial de l'externalisation des affaires réglementaires en matière de diagnostic in vitro (DIV) est segmenté en rédaction et soumissions réglementaires, enregistrement réglementaire et demandes d'essais cliniques, conseil réglementaire, représentation juridique, services de gestion de données, services de fabrication et de contrôle de produits chimiques (CMC) et autres.
Indication
- Oncologie
- Neurologie
- Cardiologie
- Chimie clinique et immuno-essais
- Médecine de précision
- Maladies infectieuses
- Diabète
- Tests génétiques
- VIH/SIDA
- Hématologie
- Tests de médicaments/Pharmacogénomique
- Transfusion sanguine
- Point de service
- Autres
Sur la base des indications, le marché mondial de l'externalisation des affaires réglementaires en matière de diagnostic in vitro (DIV) est segmenté en oncologie, neurologie, cardiologie, chimie clinique et immuno-essais, médecine de précision, maladies infectieuses, diabète, tests génétiques, VIH/SIDA, hématologie, tests de médicaments/pharmacogénomique, transfusion sanguine, point de service et autres.
Mode de déploiement
- Nuage
- Sur site
Sur la base du mode de déploiement, le marché mondial de l'externalisation des affaires réglementaires en matière de diagnostic in vitro (DIV) est segmenté en cloud et sur site.
Taille de l'organisation
- Petites et moyennes entreprises (PME)
- Grandes entreprises
Sur la base de la taille de l'organisation, le marché mondial de l'externalisation des affaires réglementaires en matière de diagnostic in vitro (DIV) est segmenté en petites et moyennes entreprises (PME) et grandes entreprises.
Scène
- Clinique
- Préclinique
- PMA (Autorisation Post-Mise sur le Marché)
Sur la base du stade, le marché mondial de l'externalisation des affaires réglementaires du diagnostic in vitro (DIV) est segmenté en clinique, préclinique et PMA (autorisation post-commercialisation).
Classe
- Classe I
- Classe II
- Classe III
Sur la base de la classe, le marché mondial de l'externalisation des affaires réglementaires du diagnostic in vitro (DIV) est segmenté en classe I, classe II et classe III.
Utilisateur final
- sociétés pharmaceutiques
- entreprises de dispositifs médicaux
- entreprises de biotechnologie
- Autres
Sur la base de l'utilisateur final, le marché mondial de l'externalisation des affaires réglementaires en matière de diagnostic in vitro (DIV) est segmenté en sociétés pharmaceutiques, sociétés de dispositifs médicaux, sociétés de biotechnologie et autres.
Analyse et perspectives régionales du marché de l'externalisation des affaires réglementaires du diagnostic in vitro (DIV)
Le marché de l'externalisation des affaires réglementaires du diagnostic in vitro (IVD) est analysé et des informations et tendances sur la taille du marché sont fournies par pays, services, indication, mode de déploiement, taille de l'organisation, étape, classe et utilisateur final comme référencé ci-dessus.
Français Les pays couverts dans le rapport sur le marché de l'externalisation des affaires réglementaires du diagnostic in vitro (DIV) sont les États-Unis, le Canada et le Mexique en Amérique du Nord, l'Allemagne, la France, le Royaume-Uni, les Pays-Bas, la Suisse, la Belgique, la Russie, l'Italie, l'Espagne, la Turquie, le reste de l'Europe en Europe, la Chine, le Japon, l'Inde, la Corée du Sud, Singapour, la Malaisie, l'Australie, la Thaïlande, l'Indonésie, les Philippines, le reste de l'Asie-Pacifique (APAC) dans l'Asie-Pacifique (APAC), l'Arabie saoudite, les Émirats arabes unis, l'Afrique du Sud, l'Égypte, Israël, le reste du Moyen-Orient et de l'Afrique (MEA) dans le cadre du Moyen-Orient et de l'Afrique (MEA), le Brésil, l'Argentine et le reste de l'Amérique du Sud dans le cadre de l'Amérique du Sud.
L'Asie-Pacifique (APAC) domine le marché de l'externalisation des affaires réglementaires en matière de diagnostic in vitro (DIV) en raison de l'augmentation du nombre d'essais cliniques et du nombre croissant d'entreprises dans la région.
L’Amérique du Nord devrait connaître une croissance significative au cours de la période de prévision de 2022 à 2029 en raison de la présence de sociétés pharmaceutiques et de dispositifs médicaux clés et de l’augmentation des dépenses de recherche et développement dans la région.
La section nationale du rapport présente également les facteurs d'impact sur les marchés individuels et les évolutions réglementaires nationales qui influencent les tendances actuelles et futures du marché. Des données telles que l'analyse des chaînes de valeur en aval et en amont, les tendances techniques, l'analyse des cinq forces de Porter et les études de cas sont quelques-uns des indicateurs utilisés pour prévoir le scénario de marché pour chaque pays. De plus, la présence et la disponibilité des marques mondiales et les défis auxquels elles sont confrontées en raison de la forte ou de la faible concurrence des marques locales et nationales, l'impact des tarifs douaniers nationaux et les routes commerciales sont pris en compte lors de l'analyse prévisionnelle des données nationales.
Croissance des infrastructures de santé Base installée et pénétration des nouvelles technologies
Le marché de l'externalisation des affaires réglementaires du diagnostic in vitro (DIV) vous propose également une analyse détaillée de chaque pays : croissance des dépenses de santé en biens d'équipement, parc installé de différents types de produits, impact des technologies (courbes de vie), évolution des scénarios réglementaires de santé et impact sur le marché de l'externalisation des affaires réglementaires du diagnostic in vitro (DIV). Les données sont disponibles pour la période 2010-2020.
Analyse du paysage concurrentiel et des parts de marché de l'externalisation des affaires réglementaires en matière de diagnostic in vitro (DIV)
Le paysage concurrentiel du marché de l'externalisation des affaires réglementaires pour le diagnostic in vitro (DIV) est détaillé par concurrent. Il comprend une présentation de l'entreprise, ses données financières, son chiffre d'affaires, son potentiel de marché, ses investissements en recherche et développement, ses nouvelles initiatives, sa présence mondiale, ses sites et installations de production, ses capacités de production, ses forces et faiblesses, le lancement de nouveaux produits, leur ampleur et leur portée, ainsi que la prédominance de ses applications. Les données ci-dessus concernent uniquement les entreprises du marché de l'externalisation des affaires réglementaires pour le diagnostic in vitro (DIV).
Certains des principaux acteurs opérant sur le marché de l'externalisation des affaires réglementaires en matière de diagnostic in vitro (DIV) sont :
- Freyr Solutions (Inde)
- PPD Inc. (États-Unis)
- EMERGO (États-Unis)
- ICÔNE (Santé)
- Parexel International Corporation (États-Unis)
- CRITERIUM, INC. (États-Unis)
- Groupe ProductLife SA (France)
- Labcorp Drug Development (États-Unis)
- WuXi AppTec (Chine)
- Genpact (États-Unis)
- Medpace (États-Unis)
- Dor Pharmaceutical Services (Israël)
- Qserve (Pays-Bas)
SKU-
Accédez en ligne au rapport sur le premier cloud mondial de veille économique
- Tableau de bord d'analyse de données interactif
- Tableau de bord d'analyse d'entreprise pour les opportunités à fort potentiel de croissance
- Accès d'analyste de recherche pour la personnalisation et les requêtes
- Analyse de la concurrence avec tableau de bord interactif
- Dernières actualités, mises à jour et analyse des tendances
- Exploitez la puissance de l'analyse comparative pour un suivi complet de la concurrence
Table des matières
1. INTRODUCTION
1.1 OBJECTIFS DE L'ÉTUDE
1.2 DÉFINITION DU MARCHÉ
1.3 APERÇU DU MARCHÉ MONDIAL DE L'EXTERNALISATION DES AFFAIRES RÉGLEMENTAIRES DU DIAGNOSTIC IN VITRO (DIV)
1.4 MONNAIE ET TARIFS
1.5 LIMITATION
1.6 MARCHÉS COUVERTS
2. SEGMENTATION DU MARCHÉ
2.1 POINTS CLÉS À RETENIR
2.2 ATTEINDRE LA TAILLE DU MARCHÉ MONDIAL DE L'EXTERNALISATION DES AFFAIRES RÉGLEMENTAIRES DU DIAGNOSTIC IN VITRO (DIV)
2.2.1 GRILLE DE POSITIONNEMENT DES FOURNISSEURS
2.2.2 COURBE DE LA LIGNE DE VIE TECHNOLOGIQUE
2.2.3 MODÉLISATION MULTIVARIÉE
2.2.4 ANALYSE DE HAUT EN BAS
2.2.5 NORMES DE MESURE
2.2.6 ANALYSE DE LA PART DES FOURNISSEURS
2.2.7 POINTS DE DONNÉES DES PRINCIPAUX ENTRETIENS
2.2.8 POINTS DE DONNÉES PROVENANT DE BASES DE DONNÉES SECONDAIRES CLÉS
2.3 MARCHÉ MONDIAL DE L'EXTERNALISATION DES AFFAIRES RÉGLEMENTAIRES DU DIAGNOSTIC IN VITRO (DIV) : APERÇU DE LA RECHERCHE
2.4 HYPOTHÈSES
3. APERÇU DU MARCHÉ
3.1 PILOTES
3.2 RESTRICTIONS
3.3 OPPORTUNITÉS
3.4 DÉFIS
4. INFORMATIONS PREMIUM
4.1 ANALYSE PESTEL
4.2 MODÈLE DES CINQ FORCES DE PORTER
5. APERÇU DU SECTEUR
5.1 FACTEURS MICRO ET MACRO ÉCONOMIQUES
5.2 CARTOGRAPHIE DES PERSPECTIVES DE PÉNÉTRATION ET DE CROISSANCE
5.3 STRATÉGIES DE TARIFICATION CLÉS
5.4 ENTRETIENS AVEC UN SPÉCIALISTE
5.5 ANALYSE ET RECOMMANDATION
6. PORTEFEUILLE DE PROPRIÉTÉ INTELLECTUELLE (PI)
6.1 QUALITÉ ET FORCE DU BREVET
6.2 FAMILLES DE BREVETS
6.3 LICENCES ET COLLABORATIONS
6.4 PAYSAGE CONCURRENTIEL
6.5 STRATÉGIE ET GESTION DE LA PI
6.6 AUTRE
7. ANALYSE DES COÛTS
8. FEUILLE DE ROUTE TECHNOLOGIQUE
9. SUIVI DE L'INNOVATION ET ANALYSE STRATÉGIQUE
9.1 ANALYSE DES PRINCIPALES AFFAIRES ET DES ALLIANCES STRATÉGIQUES
9.1.1 COENTREPRISES
9.1.2 FUSIONS ET ACQUISITIONS
9.1.3 LICENCES ET PARTENARIATS
9.1.4 COLLABORATIONS TECHNOLOGIQUES
9.1.5 DÉSINVESTISSEMENTS STRATÉGIQUES
9.2 NOMBRE DE PRODUITS EN DÉVELOPPEMENT
9.3 STADE DE DÉVELOPPEMENT
9.4 ÉCHÉANCIERS ET JALONS
9.5 STRATÉGIES ET MÉTHODOLOGIES D'INNOVATION
9.6 ÉVALUATION ET ATTÉNUATION DES RISQUES
9.7 PERSPECTIVES D'AVENIR
10. CONFORMITÉ RÉGLEMENTAIRE
10.1 AUTORITÉS DE RÉGLEMENTATION
10.2 CLASSIFICATIONS RÉGLEMENTAIRES
10.2.1 CLASSE I
10.2.2 CLASSE II
10.2.3 CLASSE III
10.3 SOUMISSIONS RÉGLEMENTAIRES
10.4 HARMONISATION INTERNATIONALE
10.5 SYSTÈMES DE GESTION DE LA CONFORMITÉ ET DE LA QUALITÉ
10.6 DÉFIS ET STRATÉGIES RÉGLEMENTAIRES
11. CADRE DE REMBOURSEMENT
12. ANALYSE DE LA CARTE DES OPPORTUNITÉS
13. DONNÉES DE BASE INSTALLÉES
14. ANALYSE DE LA CHAÎNE DE VALEUR
15. ÉCONOMIE DE LA SANTÉ
15.1 DÉPENSES DE SANTÉ
15.2 DÉPENSES D'INVESTISSEMENT
15.3 TENDANCES DES DÉPENSES D'INVESTISSEMENT
15.4 ALLOCATION DES DÉPENSES D'INVESTISSEMENT
15.5 SOURCES DE FINANCEMENT
15.6 REPÈRES DE L'INDUSTRIE
15,7 % DU PIB DANS LE PIB GLOBAL
15.8 STRUCTURE DU SYSTÈME DE SANTÉ
15.9 POLITIQUES GOUVERNEMENTALES
15.10 DÉVELOPPEMENT ÉCONOMIQUE
16. MARCHÉ MONDIAL DE L'EXTERNALISATION DES AFFAIRES RÉGLEMENTAIRES DU DIAGNOSTIC IN VITRO (DIV), PAR SERVICE
16.1 APERÇU
16.2 RÉDACTION ET SOUMISSIONS RÉGLEMENTAIRES
16.3 ENREGISTREMENT RÉGLEMENTAIRE ET DEMANDES D'ESSAIS CLINIQUES
16.4 CONSEIL RÉGLEMENTAIRE
16.5 REPRÉSENTATION LÉGALE
16.6 SERVICES DE GESTION DES DONNÉES
16.7 SERVICES DE FABRICATION ET DE CONTRÔLE DE PRODUITS CHIMIQUES (CMC)
16.8 AUTRES
17. MARCHÉ MONDIAL DE L'EXTERNALISATION DES AFFAIRES RÉGLEMENTAIRES EN MATIÈRE DE DIAGNOSTIC IN VITRO (DIV), PAR INDICATION
17.1 APERÇU
17.2 ONCOLOGIE
17.3 NEUROLOGIE
17.4 CARDIOLOGIE
17.5 CHIMIE CLINIQUE ET IMMUNO-ESSAIS
17.6 MÉDECINE DE PRÉCISION
17.7 MALADIES INFECTIEUSES
17.7.1 SEPSIS
17.7.2 VIROLOGIE
17.7.3 BACTÉRIOLOGIE
17.7.4 MICROBIOLOGIE ET MYCOLOGIE
17.7.5 HÉPATITE B
17.7.6 HÉPATITE C
17.7.7 SYPHILIS
17.7.8 TUBERCULOSE
17.7.9 PALUDISME
17.7.10 INFECTION PAR LE VIRUS DU PAPILLOME HUMAIN (VPH)
17.7.11 AUTRES
17.8 DIABÈTE
17.9 TESTS GÉNÉTIQUES
17.10 VIH/SIDA
17.11 HÉMATOLOGIE
17.12 DÉPISTAGE DE DROGUES/PHARMACOGÉNOMIQUE
17.13 TRANSFUSION SANGUINE
17.14 AUTRES
18. MARCHÉ MONDIAL DE L'EXTERNALISATION DES AFFAIRES RÉGLEMENTAIRES DU DIAGNOSTIC IN VITRO (DIV), PAR ÉTAPE
18.1 APERÇU
18.2 PRÉCLINIQUE
18.3 CLINIQUE
18.4 PMA (AUTORISATION POST-MISE SUR LE MARCHÉ)
19. MARCHÉ MONDIAL DE L'EXTERNALISATION DES AFFAIRES RÉGLEMENTAIRES EN MATIÈRE DE DIAGNOSTIC IN VITRO (DIV), PAR CATÉGORIE
19.1 APERÇU
19.2 CLASSE I
19.3 CLASSE II
19.4 CLASSE III
20. MARCHÉ MONDIAL DE L'EXTERNALISATION DES AFFAIRES RÉGLEMENTAIRES EN MATIÈRE DE DIAGNOSTIC IN VITRO (DIV), PAR TYPE
20.1 APERÇU
20.2 PRODUIT DIV AU POINT DE SOINS (POC)
20.3 TESTS DÉVELOPPÉS EN LABORATOIRE (LDTS) PRODUIT DIV
20.4 PRODUIT DE DIAGNOSTIC D'ACCOMPAGNEMENT IVD
20.5 PRODUIT DIV POUR TEST DIRECT AU CONSOMMATEUR (DTC)
20.6 AUTRES PRODUITS DIV
21. MARCHÉ MONDIAL DE L'EXTERNALISATION DES AFFAIRES RÉGLEMENTAIRES DU DIAGNOSTIC IN VITRO (DIV), PAR MODE DE DÉPLOIEMENT
21.1 APERÇU
21.2 CLOUD
21.3 SUR LOCAL
22. MARCHÉ MONDIAL DE L'EXTERNALISATION DES AFFAIRES RÉGLEMENTAIRES DU DIAGNOSTIC IN VITRO (DIV), PAR TAILLE D'ORGANISATION
22.1 APERÇU
22.2 PETITES ET MOYENNES ENTREPRISES (PME)
22.3 GRANDES ENTREPRISES
23. MARCHÉ MONDIAL DE L'EXTERNALISATION DES AFFAIRES RÉGLEMENTAIRES DU DIAGNOSTIC IN VITRO (DIV), PAR UTILISATEUR FINAL
23.1 APERÇU
23.2 SOCIÉTÉS PHARMACEUTIQUES
23.2.1 PAR TAILLE DE L'ORGANISATION
23.2.1.1. PETITES ET MOYENNES ENTREPRISES (PME)
23.2.1.2. GRANDES ENTREPRISES
23.2.2 PAR SERVICE
23.2.2.1. RÉDACTION ET SOUMISSIONS RÉGLEMENTAIRES
23.2.2.2. ENREGISTREMENT RÉGLEMENTAIRE ET DEMANDES D'ESSAIS CLINIQUES
23.2.2.3. CONSEIL RÉGLEMENTAIRE
23.2.2.4. REPRÉSENTATION LÉGALE
23.2.2.5. SERVICES DE GESTION DES DONNÉES
23.2.2.6. SERVICES DE FABRICATION ET DE CONTRÔLE DE PRODUITS CHIMIQUES (CMC)
23.2.2.7. AUTRES
23.3 ENTREPRISES DE DISPOSITIFS MÉDICAUX
23.3.1 PAR TAILLE DE L'ORGANISATION
23.3.1.1. PETITES ET MOYENNES ENTREPRISES (PME)
23.3.1.2. GRANDES ENTREPRISES
23.3.2 PAR SERVICE
23.3.2.1. RÉDACTION ET SOUMISSIONS RÉGLEMENTAIRES
23.3.2.2. ENREGISTREMENT RÉGLEMENTAIRE ET DEMANDES D'ESSAIS CLINIQUES
23.3.2.3. CONSEIL RÉGLEMENTAIRE
23.3.2.4. REPRÉSENTATION LÉGALE
23.3.2.5. SERVICES DE GESTION DES DONNÉES
23.3.2.6. SERVICES DE FABRICATION ET DE CONTRÔLE DE PRODUITS CHIMIQUES (CMC)
23.3.2.7. AUTRES
23.4 ENTREPRISES DE BIOTECHNOLOGIE
23.4.1 PAR TAILLE DE L'ORGANISATION
23.4.1.1. PETITES ET MOYENNES ENTREPRISES (PME)
23.4.1.2. GRANDES ENTREPRISES
23.4.2 PAR SERVICE
23.4.2.1. RÉDACTION ET SOUMISSIONS RÉGLEMENTAIRES
23.4.2.2. ENREGISTREMENT RÉGLEMENTAIRE ET DEMANDES D'ESSAIS CLINIQUES
23.4.2.3. CONSEIL RÉGLEMENTAIRE
23.4.2.4. REPRÉSENTATION LÉGALE
23.4.2.5. SERVICES DE GESTION DES DONNÉES
23.4.2.6. SERVICES DE FABRICATION ET DE CONTRÔLE DE PRODUITS CHIMIQUES (CMC)
23.4.2.7. AUTRES
23,5 AUTRES
24. MARCHÉ MONDIAL DE L'EXTERNALISATION DES AFFAIRES RÉGLEMENTAIRES EN MATIÈRE DE DIAGNOSTIC IN VITRO (DIV), PAR RÉGION
24.1 MARCHÉ MONDIAL DE L'EXTERNALISATION DES AFFAIRES RÉGLEMENTAIRES EN MATIÈRE DE DIAGNOSTIC IN VITRO (DIV) (TOUTES LES SEGMENTATIONS FOURNIES CI-DESSUS SONT REPRÉSENTÉES DANS CE CHAPITRE PAR PAYS)
24.1.1 AMÉRIQUE DU NORD
24.1.1.1. États-Unis
24.1.1.2. CANADA
24.1.1.3. MEXIQUE
24.1.2 EUROPE
24.1.2.1. ALLEMAGNE
24.1.2.2. FRANCE
24.1.2.3. Royaume-Uni
24.1.2.4. ITALIE
24.1.2.5. ESPAGNE
24.1.2.6. RUSSIE
24.1.2.7. TURQUIE
24.1.2.8. BELGIQUE
24.1.2.9. PAYS-BAS
24.1.2.10. SUISSE
24.1.2.11. RESTE DE L'EUROPE
24.1.3 ASIE-PACIFIQUE
24.1.3.1. JAPON
24.1.3.2. CHINE
24.1.3.3. CORÉE DU SUD
24.1.3.4. INDE
24.1.3.5. AUSTRALIE
24.1.3.6. SINGAPOUR
24.1.3.7. THAÏLANDE
24.1.3.8. MALAISIE
24.1.3.9. INDONÉSIE
24.1.3.10. PHILIPPINES
24.1.3.11. RESTE DE L'ASIE-PACIFIQUE
24.1.4 AMÉRIQUE DU SUD
24.1.4.1. BRÉSIL
24.1.4.2. ARGENTINE
24.1.4.3. RESTE DE L'AMÉRIQUE DU SUD
24.1.5 MOYEN-ORIENT ET AFRIQUE
24.1.5.1. AFRIQUE DU SUD
24.1.5.2. ÉGYPTE
24.1.5.3. ISRAËL
24.1.5.4. Émirats arabes unis
24.1.5.5. ARABIE SAOUDITE
24.1.5.6. RESTE DU MOYEN-ORIENT ET DE L'AFRIQUE
24.1.6 PRINCIPALES INFORMATIONS : PAR PRINCIPAUX PAYS
25. MARCHÉ MONDIAL DE L'EXTERNALISATION DES AFFAIRES RÉGLEMENTAIRES DU DIAGNOSTIC IN VITRO (DIV), PAYSAGE DES ENTREPRISES
25.1 ANALYSE DES ACTIONS DE L'ENTREPRISE : MONDIAL
25.2 ANALYSE DES ACTIONS DE L'ENTREPRISE : AMÉRIQUE DU NORD
25.3 ANALYSE DES ACTIONS DE L'ENTREPRISE : EUROPE
25.4 ANALYSE DES ACTIONS DE L'ENTREPRISE : ASIE-PACIFIQUE
25.5 FUSIONS ET ACQUISITIONS
25.6 DÉVELOPPEMENT ET APPROBATIONS DE NOUVEAUX PRODUITS
25.7 EXTENSION
25.8 MODIFICATIONS RÉGLEMENTAIRES
25.9 PARTENARIAT ET AUTRES DÉVELOPPEMENTS STRATÉGIQUES
26. MARCHÉ MONDIAL DE L'EXTERNALISATION DES AFFAIRES RÉGLEMENTAIRES DU DIAGNOSTIC IN VITRO (DIV), PROFIL DE L'ENTREPRISE
26.1 FREYR SOLUTIONS
26.1.1 PRÉSENTATION DE L'ENTREPRISE
26.1.2 INSTANTANÉ DE L'ENTREPRISE
26.1.3 ANALYSE DES REVENUS
26.1.4 PORTEFEUILLE DE PRODUITS
26.1.5 ÉVOLUTIONS RÉCENTES
26.2 AXSOURCE CONSULTING INC.
26.2.1 PRÉSENTATION DE L'ENTREPRISE
26.2.2 INSTANTANÉ DE L'ENTREPRISE
26.2.3 ANALYSE DES REVENUS
26.2.4 PORTEFEUILLE DE PRODUITS
26.2.5 ÉVOLUTIONS RÉCENTES
26.3 GROUPE LORENZ LIFE SCIENCES
26.3.1 PRÉSENTATION DE L'ENTREPRISE
26.3.2 INSTANTANÉ DE L'ENTREPRISE
26.3.3 ANALYSE DES REVENUS
26.3.4 PORTEFEUILLE DE PRODUITS
26.3.5 ÉVOLUTIONS RÉCENTES
26.4 LABORATORY CORPORATION OF AMERICA HOLDINGS
26.4.1 PRÉSENTATION DE L'ENTREPRISE
26.4.2 INSTANTANÉ DE L'ENTREPRISE
26.4.3 ANALYSE DES REVENUS
26.4.4 PORTEFEUILLE DE PRODUITS
26.4.5 ÉVOLUTIONS RÉCENTES
26,5 REG IQ PTY LTD.
26.5.1 PRÉSENTATION DE L'ENTREPRISE
26.5.2 INSTANTANÉ DE L'ENTREPRISE
26.5.3 ANALYSE DES REVENUS
26.5.4 PORTEFEUILLE DE PRODUITS
26.5.5 ÉVOLUTIONS RÉCENTES
26.6 PROMEDICA INTERNATIONAL, UNE SOCIÉTÉ CALIFORNIENNE (IUVO BIOSCIENCES)
26.6.1 PRÉSENTATION DE L'ENTREPRISE
26.6.2 INSTANTANÉ DE L'ENTREPRISE
26.6.3 ANALYSE DES REVENUS
26.6.4 PORTEFEUILLE DE PRODUITS
26.6.5 ÉVOLUTIONS RÉCENTES
26.7 MAKROCARE
26.7.1 PRÉSENTATION DE L'ENTREPRISE
26.7.2 INSTANTANÉ DE L'ENTREPRISE
26.7.3 ANALYSE DES REVENUS
26.7.4 PORTEFEUILLE DE PRODUITS
26.7.5 ÉVOLUTIONS RÉCENTES
26.8 EMERGO PAR UL
26.8.1 PRÉSENTATION DE L'ENTREPRISE
26.8.2 INSTANTANÉ DE L'ENTREPRISE
26.8.3 ANALYSE DES REVENUS
26.8.4 PORTEFEUILLE DE PRODUITS
26.8.5 ÉVOLUTIONS RÉCENTES
26.9 ICON PLC
26.9.1 PRÉSENTATION DE L'ENTREPRISE
26.9.2 INSTANTANÉ DE L'ENTREPRISE
26.9.3 ANALYSE DES REVENUS
26.9.4 PORTEFEUILLE DE PRODUITS
26.9.5 ÉVOLUTIONS RÉCENTES
26.10 WUXI APPTEC
26.10.1 PRÉSENTATION DE L'ENTREPRISE
26.10.2 INSTANTANÉ DE L'ENTREPRISE
26.10.3 ANALYSE DES REVENUS
26.10.4 PORTEFEUILLE DE PRODUITS
26.10.5 ÉVOLUTIONS RÉCENTES
26.11 THERMO FISHER SCIENTIFIC INC.
26.11.1 PRÉSENTATION DE L'ENTREPRISE
26.11.2 INSTANTANÉ DE L'ENTREPRISE
26.11.3 ANALYSE DES REVENUS
26.11.4 PORTEFEUILLE DE PRODUITS
26.11.5 ÉVOLUTIONS RÉCENTES
26.12 LABORATOIRES CHARLES RIVER.
26.12.1 PRÉSENTATION DE L'ENTREPRISE
26.12.2 INSTANTANÉ DE L'ENTREPRISE
26.12.3 ANALYSE DES REVENUS
26.12.4 PORTEFEUILLE DE PRODUITS
26.12.5 ÉVOLUTIONS RÉCENTES
26.13 ACCELL CLINICAL RESEARCH, LLC
26.13.1 PRÉSENTATION DE L'ENTREPRISE
26.13.2 INSTANTANÉ DE L'ENTREPRISE
26.13.3 ANALYSE DES REVENUS
26.13.4 PORTEFEUILLE DE PRODUITS
26.13.5 ÉVOLUTIONS RÉCENTES
26.14 PAREXEL INTERNATIONAL (MA) CORPORATION
26.14.1 PRÉSENTATION DE L'ENTREPRISE
26.14.2 INSTANTANÉ DE L'ENTREPRISE
26.14.3 ANALYSE DES REVENUS
26.14.4 PORTEFEUILLE DE PRODUITS
26.14.5 ÉVOLUTIONS RÉCENTES
26.15 METECON GMBH
26.15.1 PRÉSENTATION DE L'ENTREPRISE
26.15.2 INSTANTANÉ DE L'ENTREPRISE
26.15.3 ANALYSE DES REVENUS
26.15.4 PORTEFEUILLE DE PRODUITS
26.15.5 ÉVOLUTIONS RÉCENTES
26.16 GENPACT
26.16.1 PRÉSENTATION DE L'ENTREPRISE
26.16.2 INSTANTANÉ DE L'ENTREPRISE
26.16.3 ANALYSE DES REVENUS
26.16.4 PORTEFEUILLE DE PRODUITS
26.16.5 ÉVOLUTIONS RÉCENTES
26.17 CRITERIUM, INC
26.17.1 PRÉSENTATION DE L'ENTREPRISE
26.17.2 INSTANTANÉ DE L'ENTREPRISE
26.17.3 ANALYSE DES REVENUS
26.17.4 PORTEFEUILLE DE PRODUITS
26.17.5 ÉVOLUTIONS RÉCENTES
26.18 MEDPACE
26.18.1 PRÉSENTATION DE L'ENTREPRISE
26.18.2 INSTANTANÉ DE L'ENTREPRISE
26.18.3 ANALYSE DES REVENUS
26.18.4 PORTEFEUILLE DE PRODUITS
26.18.5 ÉVOLUTIONS RÉCENTES
26.19 GROUPE PRODUCTLIFE SA
26.19.1 PRÉSENTATION DE L'ENTREPRISE
26.19.2 INSTANTANÉ DE L'ENTREPRISE
26.19.3 ANALYSE DES REVENUS
26.19.4 PORTEFEUILLE DE PRODUITS
26.19.5 ÉVOLUTIONS RÉCENTES
26.20 DOR SERVICES PHARMACEUTIQUES
26.20.1 PRÉSENTATION DE L'ENTREPRISE
26.20.2 INSTANTANÉ DE L'ENTREPRISE
26.20.3 ANALYSE DES REVENUS
26.20.4 PORTEFEUILLE DE PRODUITS
26.20.5 ÉVOLUTIONS RÉCENTES
26.21 QSERVE
26.21.1 PRÉSENTATION DE L'ENTREPRISE
26.21.2 INSTANTANÉ DE L'ENTREPRISE
26.21.3 ANALYSE DES REVENUS
26.21.4 PORTEFEUILLE DE PRODUITS
26.21.5 ÉVOLUTIONS RÉCENTES
26.22 DIAGNOSTIC ORTHO CLINIQUE.
26.22.1 PRÉSENTATION DE L'ENTREPRISE
26.22.2 INSTANTANÉ DE L'ENTREPRISE
26.22.3 ANALYSE DES REVENUS
26.22.4 PORTEFEUILLE DE PRODUITS
26.22.5 ÉVOLUTIONS RÉCENTES
26.23 ANGSTROM BIOTECH PVT. LTD.
26.23.1 PRÉSENTATION DE L'ENTREPRISE
26.23.2 INSTANTANÉ DE L'ENTREPRISE
26.23.3 ANALYSE DES REVENUS
26.23.4 PORTEFEUILLE DE PRODUITS
26.23.5 ÉVOLUTIONS RÉCENTES
26,24 RQM+
26.24.1 PRÉSENTATION DE L'ENTREPRISE
26.24.2 INSTANTANÉ DE L'ENTREPRISE
26.24.3 ANALYSE DES REVENUS
26.24.4 PORTEFEUILLE DE PRODUITS
26.24.5 ÉVOLUTIONS RÉCENTES
26.25 ASSOCIÉS DE CONFORMITÉ RÉGLEMENTAIRE (SOTERA HEALTH)
26.25.1 PRÉSENTATION DE L'ENTREPRISE
26.25.2 INSTANTANÉ DE L'ENTREPRISE
26.25.3 ANALYSE DES REVENUS
26.25.4 PORTEFEUILLE DE PRODUITS
26.25.5 ÉVOLUTIONS RÉCENTES
26.26 RESEARCHDX
26.26.1 PRÉSENTATION DE L'ENTREPRISE
26.26.2 INSTANTANÉ DE L'ENTREPRISE
26.26.3 ANALYSE DES REVENUS
26.26.4 PORTEFEUILLE DE PRODUITS
26.26.5 ÉVOLUTIONS RÉCENTES
26.27 CMIC HOLDINGS CO., LTD.
26.27.1 PRÉSENTATION DE L'ENTREPRISE
26.27.2 INSTANTANÉ DE L'ENTREPRISE
26.27.3 ANALYSE DES REVENUS
26.27.4 PORTEFEUILLE DE PRODUITS
26.27.5 ÉVOLUTIONS RÉCENTES
26.28 NORTH AMERICAN SCIENCE ASSOCIATES, LLC
26.28.1 PRÉSENTATION DE L'ENTREPRISE
26.28.2 INSTANTANÉ DE L'ENTREPRISE
26.28.3 ANALYSE DES REVENUS
26.28.4 PORTEFEUILLE DE PRODUITS
26.28.5 ÉVOLUTIONS RÉCENTES
26.29 QARAD BV
26.29.1 PRÉSENTATION DE L'ENTREPRISE
26.29.2 INSTANTANÉ DE L'ENTREPRISE
26.29.3 ANALYSE DES REVENUS
26.29.4 PORTEFEUILLE DE PRODUITS
26.29.5 ÉVOLUTIONS RÉCENTES
26.30 TRANSCRIP
26.30.1 PRÉSENTATION DE L'ENTREPRISE
26.30.2 INSTANTANÉ DE L'ENTREPRISE
26.30.3 ANALYSE DES REVENUS
26.30.4 PORTEFEUILLE DE PRODUITS
26.30.5 ÉVOLUTIONS RÉCENTES
26.31 CLIN-R+
26.31.1 PRÉSENTATION DE L'ENTREPRISE
26.31.2 INSTANTANÉ DE L'ENTREPRISE
26.31.3 ANALYSE DES REVENUS
26.31.4 PORTEFEUILLE DE PRODUITS
26.31.5 ÉVOLUTIONS RÉCENTES
26,32 VCLS
26.32.1 PRÉSENTATION DE L'ENTREPRISE
26.32.2 INSTANTANÉ DE L'ENTREPRISE
26.32.3 ANALYSE DES REVENUS
26.32.4 PORTEFEUILLE DE PRODUITS
26.32.5 ÉVOLUTIONS RÉCENTES
26.33 GROUPE PROPHARMA
26.33.1 PRÉSENTATION DE L'ENTREPRISE
26.33.2 INSTANTANÉ DE L'ENTREPRISE
26.33.3 ANALYSE DES REVENUS
26.33.4 PORTEFEUILLE DE PRODUITS
26.33.5 ÉVOLUTIONS RÉCENTES
26.34 ARRIELLO IRLANDE LIMITÉE
26.34.1 PRÉSENTATION DE L'ENTREPRISE
26.34.2 INSTANTANÉ DE L'ENTREPRISE
26.34.3 ANALYSE DES REVENUS
26.34.4 PORTEFEUILLE DE PRODUITS
26.34.5 ÉVOLUTIONS RÉCENTES
REMARQUE : LA LISTE DES ENTREPRISES PRÉSENTÉES N'EST PAS EXHAUSTIVE ET EST CONFORME AUX EXIGENCES DE NOS CLIENTS PRÉCÉDENTS. NOTRE ÉTUDE COMPREND PLUS DE 100 ENTREPRISES. LA LISTE PEUT ÊTRE MODIFIÉE OU REMPLACÉE SUR DEMANDE.
27. RAPPORTS CONNEXES
28. QUESTIONNAIRE
29. À PROPOS DE DATA BRIDGE MARKET RESEARCH
Méthodologie de recherche
La collecte de données et l'analyse de l'année de base sont effectuées à l'aide de modules de collecte de données avec des échantillons de grande taille. L'étape consiste à obtenir des informations sur le marché ou des données connexes via diverses sources et stratégies. Elle comprend l'examen et la planification à l'avance de toutes les données acquises dans le passé. Elle englobe également l'examen des incohérences d'informations observées dans différentes sources d'informations. Les données de marché sont analysées et estimées à l'aide de modèles statistiques et cohérents de marché. De plus, l'analyse des parts de marché et l'analyse des tendances clés sont les principaux facteurs de succès du rapport de marché. Pour en savoir plus, veuillez demander un appel d'analyste ou déposer votre demande.
La méthodologie de recherche clé utilisée par l'équipe de recherche DBMR est la triangulation des données qui implique l'exploration de données, l'analyse de l'impact des variables de données sur le marché et la validation primaire (expert du secteur). Les modèles de données incluent la grille de positionnement des fournisseurs, l'analyse de la chronologie du marché, l'aperçu et le guide du marché, la grille de positionnement des entreprises, l'analyse des brevets, l'analyse des prix, l'analyse des parts de marché des entreprises, les normes de mesure, l'analyse globale par rapport à l'analyse régionale et des parts des fournisseurs. Pour en savoir plus sur la méthodologie de recherche, envoyez une demande pour parler à nos experts du secteur.
Personnalisation disponible
Data Bridge Market Research est un leader de la recherche formative avancée. Nous sommes fiers de fournir à nos clients existants et nouveaux des données et des analyses qui correspondent à leurs objectifs. Le rapport peut être personnalisé pour inclure une analyse des tendances des prix des marques cibles, une compréhension du marché pour d'autres pays (demandez la liste des pays), des données sur les résultats des essais cliniques, une revue de la littérature, une analyse du marché des produits remis à neuf et de la base de produits. L'analyse du marché des concurrents cibles peut être analysée à partir d'une analyse basée sur la technologie jusqu'à des stratégies de portefeuille de marché. Nous pouvons ajouter autant de concurrents que vous le souhaitez, dans le format et le style de données que vous recherchez. Notre équipe d'analystes peut également vous fournir des données sous forme de fichiers Excel bruts, de tableaux croisés dynamiques (Fact book) ou peut vous aider à créer des présentations à partir des ensembles de données disponibles dans le rapport.