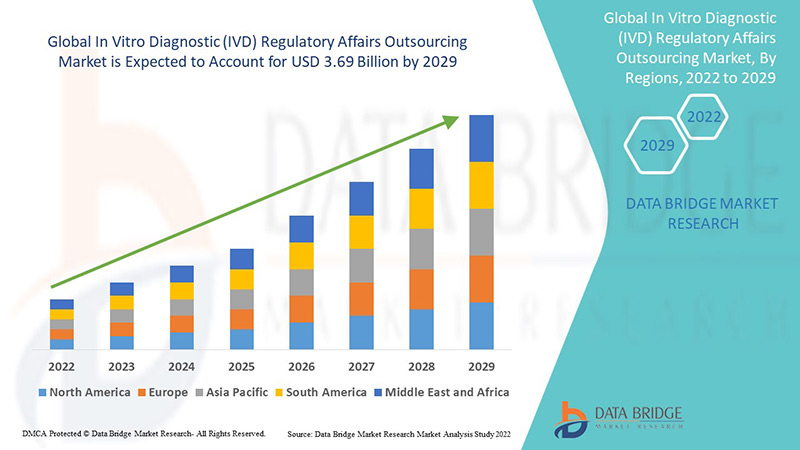
Global In Vitro Diagnostic Ivd Regulatory Affairs Outsourcing Market
Marktgröße in Milliarden USD
CAGR :
% 
 USD
674,277.97 Thousand
USD
1,830,957.45 Thousand
2021
2029
USD
674,277.97 Thousand
USD
1,830,957.45 Thousand
2021
2029
| 2022 –2029 | |
| USD 674,277.97 Thousand | |
| USD 1,830,957.45 Thousand | |
|
|
|
|
Globaler Markt für das Outsourcing von regulatorischen Angelegenheiten im Bereich In-vitro -Diagnostik (IVD), nach Dienstleistung (Erstellung und Einreichung von Zulassungsanträgen, Zulassungsregistrierung und Anträge auf klinische Studien, regulatorische Beratung, Rechtsvertretung, Datenverwaltungsdienste, Dienstleistungen zur Herstellung und Kontrolle chemischer Substanzen (CMC) und andere), Indikation (Onkologie, Neurologie, Kardiologie, Klinische Chemie und Immunoassays, Präzisionsmedizin, Infektionskrankheiten, Diabetes, Gentests, HIV/AIDS, Hämatologie, Arzneimitteltests/Pharmakogenomik, Bluttransfusion, Point of Care und andere), Bereitstellungsmodus (Cloud und vor Ort), Unternehmensgröße (kleine und mittlere Unternehmen (KMU) und große Unternehmen), Phase (klinisch, präklinisch und PMA (Post-Market Authorization)), Klasse (Klasse I, Klasse II und Klasse III), Endbenutzer (Pharmaunternehmen, Medizinprodukteunternehmen, Biotechnologieunternehmen und andere) – Branchentrends und Prognose bis 2029
Marktanalyse und Größe
Gesundheitsunternehmen standen insbesondere aufgrund der COVID-19-Pandemie (Coronavirus) vor der Herausforderung, regulatorische Standards einzuhalten. Um eine qualitätsorientierte Unternehmenskultur in Medizintechnikunternehmen zu fördern, setzen Beratungsfirmen Qualitätsmanagementsystem-Software (QMS) ein. Unternehmen, die im Outsourcing regulatorischer Angelegenheiten im Bereich In- vitro-Diagnostik (IVD) tätig sind, bieten Gesundheitsorganisationen projektbasierte Unterstützung.
Der Einsatz des Outsourcings führt zum Abschluss langfristiger Outsourcing-Vereinbarungen. Der globale Markt für regulatorische Angelegenheiten im Bereich In-vitro-Diagnostik (IVD) wurde 2021 auf 1,6 Milliarden US-Dollar geschätzt und soll bis 2029 3,69 Milliarden US-Dollar erreichen, was einer durchschnittlichen jährlichen Wachstumsrate (CAGR) von 11 % im Prognosezeitraum 2022–2029 entspricht. Für Pharmaunternehmen wird aufgrund der steigenden Anzahl klinischer Zulassungen ein hohes Wachstum erwartet.
Marktdefinition
Regulatorische Angelegenheiten spielen in der IVD -Branche eine entscheidende Rolle . Sie befassen sich mit dem Lebenszyklus verschiedener Gesundheitsprodukte und bieten produzierenden Unternehmen strategische, taktische und operative Unterstützung und Orientierung bei der Einhaltung der regulatorischen Rahmenbedingungen.
Berichtsumfang und Marktsegmentierung
|
Berichtsmetrik |
Details |
|
Prognosezeitraum |
2022 bis 2029 |
|
Basisjahr |
2021 |
|
Historische Jahre |
2020 (Anpassbar auf 2019 – 2014) |
|
Quantitative Einheiten |
Umsatz in Millionen USD, Mengen in Einheiten, Preise in USD |
|
Abgedeckte Segmente |
Service (Erstellung und Einreichung von Zulassungsanträgen, Zulassungsregistrierung und Anträge auf klinische Studien, Zulassungsberatung, Rechtsvertretung, Datenverwaltungsdienste, Dienste zur Herstellung und Kontrolle chemischer Substanzen (CMC) und andere), Indikation (Onkologie, Neurologie, Kardiologie, klinische Chemie und Immunassays, Präzisionsmedizin, Infektionskrankheiten, Diabetes, Gentests, HIV/AIDS, Hämatologie, Arzneimitteltests/Pharmakogenomik, Bluttransfusion, Point of Care und andere), Bereitstellungsmodus (Cloud und vor Ort), Unternehmensgröße (kleine und mittlere Unternehmen (KMU) und große Unternehmen), Phase (klinisch, präklinisch und PMA (Post-Market Authorization)), Klasse (Klasse I, Klasse II und Klasse III), Endbenutzer (Pharmaunternehmen, Hersteller medizinischer Geräte, Biotechnologieunternehmen und andere) |
|
Abgedeckte Länder |
USA, Kanada und Mexiko in Nordamerika, Deutschland, Frankreich, Großbritannien, Niederlande, Schweiz, Belgien, Russland, Italien, Spanien, Türkei, Restliches Europa in Europa, China, Japan, Indien, Südkorea, Singapur, Malaysia, Australien, Thailand, Indonesien, Philippinen, Restlicher Asien-Pazifik-Raum (APAC) im Asien-Pazifik-Raum (APAC), Saudi-Arabien, Vereinigte Arabische Emirate, Südafrika, Ägypten, Israel, Restlicher Naher Osten und Afrika (MEA) als Teil des Nahen Ostens und Afrikas (MEA), Brasilien, Argentinien und Restliches Südamerika als Teil von Südamerika. |
|
Abgedeckte Marktteilnehmer |
Freyr Solutions (Indien), PPD Inc. (USA), EMERGO (USA), ICON (Gesundheitswesen), Parexel International Corporation (USA), CRITERIUM, INC. (USA), Groupe ProductLife SA (Frankreich), Labcorp Drug Development (USA), WuXi AppTec (China), Genpact (USA), Medpace (USA), Dor Pharmaceutical Services (Israel), Qserve (Niederlande) und andere |
|
Marktchancen |
|
Marktdynamik für das Outsourcing regulatorischer Angelegenheiten im Bereich In-vitro-Diagnostik (IVD)
In diesem Abschnitt geht es um das Verständnis der Markttreiber, Vorteile, Chancen, Einschränkungen und Herausforderungen. All dies wird im Folgenden ausführlich erläutert:
- Hoher Einsatz in der Gesundheitsbranche
Der zunehmende Einsatz von Outsourcing-Dienstleistungen im Gesundheitssektor ist einer der Hauptfaktoren für das Wachstum des Outsourcing-Marktes für regulatorische Angelegenheiten im Bereich In-vitro-Diagnostik (IVD). Die verstärkte geografische Expansion mit dem Ziel schneller Zulassungen in lokalen Märkten trägt zusätzlich zum Wachstum bei.
- Forschung und Entwicklung
Der Anstieg der Forschungs- und Entwicklungsaktivitäten sowie die zunehmende Anzahl von Anträgen für klinische Studien und Produktregistrierungen beschleunigen das Marktwachstum.
- Klinische Zulassungen
Die Nachfrage nach Outsourcing regulatorischer Angelegenheiten im Bereich In-vitro-Diagnostik (IVD) steigt, da Unternehmen unter ständigem Druck stehen, rechtzeitig klinische Zulassungen von den Aufsichtsbehörden einzuholen. Die Nachfrage nach regulatorischen Dienstleistungen steigt daher.
Gelegenheiten
Darüber hinaus eröffnen die Entwicklung krankheitsspezifischer Biomarker und Tests sowie die Bedeutung der Begleitdiagnostik den Marktteilnehmern im Prognosezeitraum 2022 bis 2029 lukrative Möglichkeiten. Auch ein Anstieg der Investitionen wird den Markt weiter ausbauen.
Einschränkungen/Herausforderungen
Andererseits dürften sich ändernde Vorschriften für Medizinprodukte und das Outsourcing regulatorischer Angelegenheiten im Bereich In-vitro-Diagnostik (IVD) das Marktwachstum behindern. Auch die mangelnde Infrastruktur im Gesundheitswesen dürfte den Markt für das Outsourcing regulatorischer Angelegenheiten im Bereich In-vitro-Diagnostik (IVD) im Prognosezeitraum 2022–2029 vor Herausforderungen stellen.
Dieser Marktbericht zum Outsourcing von regulatorischen Angelegenheiten im Bereich In-vitro-Diagnostik (IVD) enthält Details zu aktuellen Entwicklungen, Handelsbestimmungen, Import-Export-Analysen, Produktionsanalysen, Wertschöpfungskettenoptimierung, Marktanteilen, dem Einfluss inländischer und lokaler Marktteilnehmer, analysiert Chancen hinsichtlich neuer Umsatzfelder, Änderungen der Marktregulierung, strategische Marktwachstumsanalysen, Marktgröße, Kategoriewachstum, Anwendungsnischen und Marktdominanz, Produktzulassungen, Produkteinführungen, geografischer Expansion und technologischen Innovationen. Für weitere Informationen zum Outsourcing von regulatorischen Angelegenheiten im Bereich In-vitro-Diagnostik (IVD) kontaktieren Sie Data Bridge Market Research für ein Analysten-Briefing. Unser Team unterstützt Sie bei fundierten Marktentscheidungen und unterstützt Sie bei Ihrem Marktwachstum.
Auswirkungen von Covid-19 auf den Markt für Diagnosetests
COVID-19 hatte negative Auswirkungen auf den Gesundheitssektor. Wichtige Akteure passten während des COVID-19-Ausbruchs innovative Strategien an die sich rasch verändernde Situation an. Die Länder führten kritische Veränderungen im Gesundheitswesen durch, bis die Krise in den Hintergrund trat. Es wird erwartet, dass Gesundheitsreformen in den kommenden Jahren zu Kostensenkungen, verbessertem Zugang und technologischem Fortschritt führen werden. Aufgrund der zunehmenden Bedeutung von Ferndiagnose, -versorgung und -beratung stieg die Nachfrage nach Outsourcing von regulatorischen Angelegenheiten im Bereich In-vitro-Diagnostik (IVD). Diese Dienstleistungen entlasten die Krankenhäuser nach der Pandemie.
Jüngste Entwicklungen
- Das Technologiemagazin USA-9 hat Freyr im November 2021 unter die „10 besten Technologielösungsanbieter des Jahres 2021“ gewählt. USA-9.com ist ein Technologiemagazin, das Freyr Solutions, einen führenden globalen Anbieter von regulatorischen Lösungen und Dienstleistungen, unter die „10 besten Technologielösungsanbieter des Jahres 2021“ gewählt hat, da Fryer weiterhin innovative Softwarelösungen entwickelt und Kunden bei ihren Compliance-Zielen unterstützt. Dies hat dem Unternehmen zu einer gesteigerten Popularität verholfen.
Globaler Outsourcing-Markt für In-vitro-Diagnostik (IVD) Regulatory Affairs – Umfang und Marktgröße
Der Markt für das Outsourcing regulatorischer Angelegenheiten im Bereich In-vitro-Diagnostik (IVD) ist nach Dienstleistungen, Indikation, Bereitstellungsmodus, Unternehmensgröße, Entwicklungsstadium, Klasse und Endnutzer segmentiert. Das Wachstum dieser Segmente hilft Ihnen, schwach wachsende Branchensegmente zu analysieren und bietet Ihnen einen wertvollen Marktüberblick und Markteinblicke, die Ihnen helfen, strategische Entscheidungen zur Identifizierung zentraler Marktanwendungen zu treffen.
Leistungen
- Verfassen von behördlichen Anträgen und Einreichungen
- Zulassungs- und klinische Studienanträge
- Regulatorische Beratung
- Rechtsvertretung
- Datenverwaltungsdienste
- Dienstleistungen im Bereich Chemieherstellung und -kontrolle (CMC)
- Sonstiges
Auf der Grundlage der Dienstleistungen ist der globale Outsourcing-Markt für regulatorische Angelegenheiten im Bereich In-vitro-Diagnostik (IVD) in die Bereiche Verfassen und Einreichen von Vorschriften, Registrierung von Vorschriften und Anträge auf klinische Studien, regulatorische Beratung, Rechtsvertretung, Datenverwaltungsdienste, Dienste zur Herstellung und Kontrolle chemischer Stoffe (CMC) und andere unterteilt.
Anzeige
- Onkologie
- Neurologie
- Kardiologie
- Klinische Chemie und Immunassays
- Präzisionsmedizin
- Infektionskrankheiten
- Diabetes
- Genetische Tests
- HIV/AIDS
- Hämatologie
- Arzneimittelprüfung/Pharmakogenomik
- Bluttransfusion
- Behandlungsort
- Sonstiges
Auf der Grundlage der Indikation ist der globale Markt für das Outsourcing regulatorischer Angelegenheiten im Bereich In-vitro-Diagnostik (IVD) in die Bereiche Onkologie, Neurologie, Kardiologie, klinische Chemie und Immunassays, Präzisionsmedizin, Infektionskrankheiten, Diabetes, genetische Tests, HIV/AIDS, Hämatologie, Arzneimitteltests/Pharmakogenomik, Bluttransfusion, Point of Care und andere unterteilt.
Bereitstellungsmodus
- Wolke
- Vor Ort
Auf der Grundlage des Bereitstellungsmodus ist der globale Outsourcing-Markt für regulatorische Angelegenheiten im Bereich der In-vitro-Diagnostik (IVD) in Cloud und On-Premises segmentiert.
Unternehmensgröße
- Kleine und mittlere Unternehmen (KMU)
- Große Unternehmen
Auf der Grundlage der Unternehmensgröße ist der globale Markt für das Outsourcing regulatorischer Angelegenheiten im Bereich der In-vitro-Diagnostik (IVD) in kleine und mittlere Unternehmen (KMU) und große Unternehmen segmentiert.
Bühne
- Klinisch
- Präklinisch
- PMA (Post-Market-Authorization)
Der globale Markt für das Outsourcing regulatorischer Angelegenheiten im Bereich der In-vitro-Diagnostik (IVD) ist auf der Grundlage der Phase in die Bereiche Klinik, Präklinik und PMA (Post-Market Authorization) unterteilt.
Klasse
- Klasse I
- Klasse II
- Klasse III
Auf der Grundlage der Klasse ist der globale Outsourcing-Markt für regulatorische Angelegenheiten im Bereich der In-vitro-Diagnostik (IVD) in Klasse I, Klasse II und Klasse III segmentiert.
Endbenutzer
- Pharmaunternehmen
- Hersteller medizinischer Geräte
- Biotechnologieunternehmen
- Sonstiges
Auf der Grundlage des Endbenutzers ist der globale Markt für das Outsourcing regulatorischer Angelegenheiten im Bereich In-vitro-Diagnostik (IVD) in Pharmaunternehmen, Unternehmen für medizinische Geräte, Biotechnologieunternehmen und andere segmentiert.
Regionale Analyse/Einblicke zum Outsourcing des Marktes für regulatorische Angelegenheiten im Bereich In-vitro-Diagnostik (IVD)
Der Outsourcing-Markt für regulatorische Angelegenheiten im Bereich der In-vitro-Diagnostik (IVD) wird analysiert und es werden Einblicke in die Marktgröße und Trends nach Land, Diensten, Indikation, Bereitstellungsmodus, Organisationsgröße, Phase, Klasse und Endbenutzer wie oben angegeben bereitgestellt.
Die im Marktbericht zum Outsourcing regulatorischer Angelegenheiten im Bereich In-vitro-Diagnostik (IVD) abgedeckten Länder sind die USA, Kanada und Mexiko in Nordamerika, Deutschland, Frankreich, Großbritannien, Niederlande, Schweiz, Belgien, Russland, Italien, Spanien, Türkei, Restliches Europa in Europa, China, Japan, Indien, Südkorea, Singapur, Malaysia, Australien, Thailand, Indonesien, Philippinen, Restlicher Asien-Pazifik-Raum (APAC) in der Asien-Pazifik-Region (APAC), Saudi-Arabien, Vereinigte Arabische Emirate, Südafrika, Ägypten, Israel, Restlicher Naher Osten und Afrika (MEA) als Teil des Nahen Ostens und Afrikas (MEA), Brasilien, Argentinien und Restliches Südamerika als Teil von Südamerika.
Der asiatisch-pazifische Raum (APAC) dominiert den Outsourcing-Markt für regulatorische Angelegenheiten im Bereich der In-vitro-Diagnostik (IVD) aufgrund der steigenden Zahl klinischer Studien und der zunehmenden Anzahl von Unternehmen in der Region.
In Nordamerika wird im Prognosezeitraum von 2022 bis 2029 aufgrund der Präsenz wichtiger Pharmaunternehmen und Medizintechnikunternehmen sowie steigender Ausgaben für Forschung und Entwicklung in der Region ein deutliches Wachstum erwartet.
Der Länderteil des Berichts enthält zudem Informationen zu einzelnen marktbeeinflussenden Faktoren und regulatorischen Veränderungen im Inland, die sich auf die aktuellen und zukünftigen Markttrends auswirken. Datenpunkte wie die Analyse der nachgelagerten und vorgelagerten Wertschöpfungskette, technische Trends, die Fünf-Kräfte-Analyse nach Porter sowie Fallstudien dienen unter anderem der Prognose des Marktszenarios für einzelne Länder. Auch die Präsenz und Verfügbarkeit globaler Marken und ihre Herausforderungen aufgrund starker oder geringer Konkurrenz durch lokale und inländische Marken sowie die Auswirkungen inländischer Zölle und Handelsrouten werden bei der Prognoseanalyse der Länderdaten berücksichtigt.
Wachstum der Gesundheitsinfrastruktur, installierte Basis und Durchdringung neuer Technologien
Der Markt für das Outsourcing von regulatorischen Angelegenheiten im Bereich In-vitro-Diagnostik (IVD) bietet Ihnen außerdem detaillierte Marktanalysen für jedes Land, das Wachstum der Gesundheitsausgaben für Investitionsgüter, die installierte Basis verschiedener Produkte für das Outsourcing von regulatorischen Angelegenheiten im Bereich In-vitro-Diagnostik (IVD), den Einfluss der Technologie anhand von Lebenslinienkurven sowie Änderungen der regulatorischen Szenarien im Gesundheitswesen und deren Auswirkungen auf den Outsourcing-Markt für regulatorische Angelegenheiten im Bereich In-vitro-Diagnostik (IVD). Die Daten sind für den historischen Zeitraum 2010–2020 verfügbar.
Wettbewerbsumfeld und Outsourcing der regulatorischen Angelegenheiten im Bereich In-vitro-Diagnostik (IVD) Analyse der Marktanteile
Die Wettbewerbslandschaft im Markt für das Outsourcing regulatorischer Angelegenheiten im Bereich In-vitro-Diagnostik (IVD) bietet detaillierte Informationen zu den einzelnen Wettbewerbern. Zu den Details gehören Unternehmensübersicht, Unternehmensfinanzen, Umsatz, Marktpotenzial, Investitionen in Forschung und Entwicklung, neue Marktinitiativen, globale Präsenz, Produktionsstandorte und -anlagen, Produktionskapazitäten, Stärken und Schwächen des Unternehmens, Produkteinführung, Produktbreite und -umfang sowie Anwendungsdominanz. Die oben genannten Datenpunkte beziehen sich ausschließlich auf den Fokus der Unternehmen im Markt für das Outsourcing regulatorischer Angelegenheiten im Bereich In-vitro-Diagnostik (IVD).
Zu den wichtigsten Akteuren auf dem Outsourcing-Markt für regulatorische Angelegenheiten im Bereich der In-vitro-Diagnostik (IVD) zählen:
- Freyr Solutions (Indien)
- PPD Inc. (USA)
- EMERGO (USA)
- ICON (Gesundheitswesen)
- Parexel International Corporation (USA)
- CRITERIUM, INC. (USA)
- Groupe ProductLife SA (Frankreich)
- Labcorp Arzneimittelentwicklung (USA)
- WuXi AppTec (China)
- Genpact (USA)
- Medpace (USA)
- Dor Pharmaceutical Services (Israel)
- Qserve (Niederlande)
SKU-
Erhalten Sie Online-Zugriff auf den Bericht zur weltweit ersten Market Intelligence Cloud
- Interaktives Datenanalyse-Dashboard
- Unternehmensanalyse-Dashboard für Chancen mit hohem Wachstumspotenzial
- Zugriff für Research-Analysten für Anpassungen und Abfragen
- Konkurrenzanalyse mit interaktivem Dashboard
- Aktuelle Nachrichten, Updates und Trendanalyse
- Nutzen Sie die Leistungsfähigkeit der Benchmark-Analyse für eine umfassende Konkurrenzverfolgung
Inhaltsverzeichnis
1. EINLEITUNG
1.1 ZIELE DER STUDIE
1.2 MARKTDEFINITION
1.3 Überblick über den globalen Markt für das Outsourcing regulatorischer Angelegenheiten im Bereich der In-vitro-Diagnostik (IVD)
1.4 WÄHRUNG UND PREISE
1.5 EINSCHRÄNKUNG
1.6 ABGEDECKTE MÄRKTE
2. Marktsegmentierung
2.1 WICHTIGSTE ERGEBNISSE
2.2 ERREICHUNG DER GLOBALEN MARKTGRÖSSE FÜR DAS OUTSOURCING VON REGULATORISCHEN ANGELEGENHEITEN IM BEREICH DER IN-VITRO-DIAGNOSTIK (IVD)
2.2.1 LIEFERANTENPOSITIONIERUNGSRASTER
2.2.2 TECHNOLOGIE-LEBENSLINIENKURVE
2.2.3 MULTIVARIATE MODELLIERUNG
2.2.4 TOP-TO-BOTTOM-ANALYSE
2.2.5 MESSSTANDARDS
2.2.6 ANALYSE DES LIEFERANTENANTEILS
2.2.7 DATENPUNKTE AUS WICHTIGEN PRIMÄRINTERVIEWS
2.2.8 DATENPUNKTE AUS WICHTIGEN SEKUNDÄRDATENBANKEN
2.3 GLOBALER MARKT FÜR DAS OUTSOURCING VON REGULATORISCHEN ANGELEGENHEITEN IM BEREICH DER IN-VITRO-DIAGNOSTIK (IVD): FORSCHUNGSÜBERSICHT
2.4 ANNAHMEN
3. MARKTÜBERSICHT
3.1 TREIBER
3.2 EINSCHRÄNKUNGEN
3.3 CHANCEN
3.4 HERAUSFORDERUNGEN
4. PREMIUM-EINBLICKE
4.1 PESTEL-ANALYSE
4.2 PORTERS FÜNF-KRÄFTE-MODELL
5. Brancheneinblicke
5.1 MIKRO- UND MAKROÖKONOMISCHE FAKTOREN
5.2 Marktdurchdringung und Wachstumsperspektiven-Mapping
5.3 WICHTIGE PREISSTRATEGIEN
5.4 INTERVIEWS MIT FACHKRÄFTEN
5.5 ANALYSE UND EMPFEHLUNG
6. PORTFOLIO DES GEISTIGEN EIGENTUMS (IP)
6.1 PATENTQUALITÄT UND STÄRKE
6.2 PATENTFAMILIEN
6.3 LIZENZIERUNG UND KOOPERATIONEN
6.4 WETTBEWERBSLANDSCHAFT
6.5 IP-Strategie und -Management
6.6 SONSTIGES
7. Kostenanalyse
8. TECHNOLOGIE-ROADMAP
9. INNOVATIONSTRACKER UND STRATEGISCHE ANALYSE
9.1 ANALYSE WICHTIGER ABSCHLÜSSE UND STRATEGISCHER ALLIANZEN
9.1.1 Joint Ventures
9.1.2 FUSIONEN UND ÜBERNAHMEN
9.1.3 LIZENZIERUNG UND PARTNERSCHAFT
9.1.4 TECHNOLOGIEKOOPERATIONEN
9.1.5 STRATEGISCHE DESINSTALLATIONEN
9.2 ANZAHL DER IN ENTWICKLUNG BEFINDLICHEN PRODUKTE
9.3 ENTWICKLUNGSSTAND
9.4 ZEITPLAN UND MEILENSTEINE
9.5 INNOVATIONSSTRATEGIEN UND -METHODEN
9.6 RISIKOBEWERTUNG UND -MINDERUNG
9.7 ZUKÜNFTIGE AUSSICHTEN
10. Einhaltung gesetzlicher Vorschriften
10.1 AUFSICHTSBEHÖRDEN
10.2 GESETZLICHE KLASSIFIZIERUNGEN
10.2.1 KLASSE I
10.2.2 KLASSE II
10.2.3 KLASSE III
10.3 REGULATORISCHE EINREICHUNGEN
10.4 INTERNATIONALE HARMONISIERUNG
10.5 COMPLIANCE- UND QUALITÄTSMANAGEMENTSYSTEME
10.6 REGULATORISCHE HERAUSFORDERUNGEN UND STRATEGIEN
11. RAHMENBEDINGUNGEN FÜR DIE RÜCKERSTATTUNG
12. Analyse der Chancenkarte
13. INSTALLIERTE BASISDATEN
14. WERTKETTENANALYSE
15. GESUNDHEITSWIRTSCHAFT
15.1 GESUNDHEITSAUSGABEN
15.2 INVESTITIONSAUSGABEN
15.3 CAPEX-TRENDS
15.4 CAPEX-ZUWEISUNG
15.5 FINANZIERUNGSQUELLEN
15.6 Branchen-Benchmarks
15,7 BIP-Anteil am Gesamt-BIP
15.8 STRUKTUR DES GESUNDHEITSSYSTEMS
15.9 REGIERUNGSPOLITIK
15.10 WIRTSCHAFTLICHE ENTWICKLUNG
16. GLOBALER MARKT FÜR DAS OUTSOURCING VON REGULATORISCHEN ANGELEGENHEITEN IM BEREICH DER IN-VITRO-DIAGNOSTIK (IVD) NACH DIENSTLEISTUNG
16.1 ÜBERSICHT
16.2 REGULATORISCHE SCHRIFTLICHE BESCHREIBUNGEN UND EINREICHUNGEN
16.3 Zulassungs- und klinische Studienanträge
16.4 REGULATORISCHE BERATUNG
16.5 RECHTLICHE VERTRETUNG
16.6 DATENMANAGEMENTDIENSTE
16.7 DIENSTLEISTUNGEN FÜR DIE HERSTELLUNG UND KONTROLLE VON CHEMIKALIEN (CMC)
16.8 SONSTIGES
17. GLOBALER MARKT FÜR DAS OUTSOURCING VON REGULATORISCHEN ANGELEGENHEITEN IM BEREICH DER IN-VITRO-DIAGNOSTIK (IVD) NACH INDIKATION
17.1 ÜBERSICHT
17.2 ONKOLOGIE
17.3 NEUROLOGIE
17.4 KARDIOLOGIE
17.5 KLINISCHE CHEMIE UND IMMUNOASSAYS
17.6 PRÄZISIONSMEDIZIN
17.7 Infektionskrankheiten
17.7.1 SEPSIS
17.7.2 VIROLOGIE
17.7.3 BAKTERIOLOGIE
17.7.4 MIKROBIOLOGIE UND MYKOLOGIE
17.7.5 HEPATITIS B
17.7.6 HEPATITIS C
17.7.7 SYPHILIS
17.7.8 TUBERKULOSE
17.7.9 Malaria
17.7.10 Infektion mit humanen Papillomviren (HPV)
17.7.11 SONSTIGES
17.8 DIABETES
17.9 GENTESTS
17.10 HIV/AIDS
17.11 HÄMATOLOGIE
17.12 Arzneimitteltests/Pharmakogenomik
17.13 Bluttransfusion
17.14 SONSTIGES
18. GLOBALER MARKT FÜR DAS OUTSOURCING VON REGULATORISCHEN ANGELEGENHEITEN IM BEREICH DER IN-VITRO-DIAGNOSTIK (IVD) NACH STUFEN
18.1 ÜBERSICHT
18.2 PRÄKLINISCHE
18.3 KLINISCH
18.4 PMA (Post Market Authorization)
19. GLOBALER MARKT FÜR DAS OUTSOURCING VON REGULATORISCHEN ANGELEGENHEITEN IM BEREICH DER IN-VITRO-DIAGNOSTIK (IVD) NACH KLASSE
19.1 ÜBERSICHT
19.2 KLASSE I
19.3 KLASSE II
19.4 KLASSE III
20. GLOBALER MARKT FÜR DAS OUTSOURCING VON REGULATORISCHEN ANGELEGENHEITEN IM BEREICH DER IN-VITRO-DIAGNOSTIK (IVD) NACH ART
20.1 ÜBERBLICK
20.2 POINT-OF-CARE (POC) IVD-PRODUKT
20.3 Laborentwickelte Tests (LDTS) IVD-Produkt
20.4 Begleitdiagnostika-IVD-Produkt
20.5 DIRECT-TO-CONSUMER (DTC)-TESTS VON IVD-PRODUKTEN
20.6 ANDERE IVD-PRODUKTE
21. GLOBALER MARKT FÜR DAS OUTSOURCING VON REGULATORISCHEN ANGELEGENHEITEN IM BEREICH DER IN-VITRO-DIAGNOSTIK (IVD) NACH EINSATZMODUS
21.1 ÜBERSICHT
21.2 CLOUD
21.3 VOR ORT
22. GLOBALER MARKT FÜR DAS OUTSOURCING VON REGULATORISCHEN ANGELEGENHEITEN IM BEREICH DER IN-VITRO-DIAGNOSTIK (IVD) NACH UNTERNEHMENSGRÖSSE
22.1 ÜBERBLICK
22.2 KLEINE UND MITTLERE UNTERNEHMEN (KMU)
22.3 Große Unternehmen
23. GLOBALER OUTSOURCING-MARKT FÜR IN-VITRO-DIAGNOSTIK (IVD)-REGULATORISCHE ANGELEGENHEITEN, NACH ENDBENUTZER
23.1 ÜBERSICHT
23.2 PHARMAZEUTISCHE UNTERNEHMEN
23.2.1 NACH ORGANISATIONSGRÖSSE
23.2.1.1. KLEINE UND MITTLERE UNTERNEHMEN (KMU)
23.2.1.2. Große Unternehmen
23.2.2 DURCH DIENST
23.2.2.1. SCHRIFTLICHE VORSCHRIFTEN UND EINREICHUNGEN
23.2.2.2. Zulassungs- und Zulassungsanträge für klinische Studien
23.2.2.3. REGULATORISCHE BERATUNG
23.2.2.4. RECHTLICHE VERTRETUNG
23.2.2.5. DATENMANAGEMENTDIENSTE
23.2.2.6. DIENSTLEISTUNGEN FÜR DIE HERSTELLUNG UND KONTROLLE VON CHEMIKALIEN (CMC)
23.2.2.7. SONSTIGES
23.3 MEDIZINPRODUKTEUNTERNEHMEN
23.3.1 NACH ORGANISATIONSGRÖSSE
23.3.1.1. KLEINE UND MITTLERE UNTERNEHMEN (KMU)
23.3.1.2. Große Unternehmen
23.3.2 DURCH DIENST
23.3.2.1. REGULATORISCHE SCHRIFTLICHE ANGABEN UND EINREICHUNGEN
23.3.2.2. Zulassungs- und Zulassungsanträge für klinische Studien
23.3.2.3. REGULATORISCHE BERATUNG
23.3.2.4. RECHTLICHE VERTRETUNG
23.3.2.5. DATENMANAGEMENTDIENSTE
23.3.2.6. DIENSTLEISTUNGEN FÜR DIE HERSTELLUNG UND KONTROLLE VON CHEMIKALIEN (CMC)
23.3.2.7. SONSTIGES
23.4 BIOTECHNOLOGIEUNTERNEHMEN
23.4.1 NACH UNTERNEHMENSGRÖSSE
23.4.1.1. KLEINE UND MITTLERE UNTERNEHMEN (KMU)
23.4.1.2. Große Unternehmen
23.4.2 DURCH DIENST
23.4.2.1. SCHRIFTLICHE VORSCHRIFTEN UND EINREICHUNGEN
23.4.2.2. Zulassungs- und Zulassungsanträge für klinische Studien
23.4.2.3. REGULATORISCHE BERATUNG
23.4.2.4. RECHTLICHE VERTRETUNG
23.4.2.5. DATENMANAGEMENTDIENSTE
23.4.2.6. DIENSTLEISTUNGEN FÜR DIE HERSTELLUNG UND KONTROLLE VON CHEMIKALIEN (CMC)
23.4.2.7. SONSTIGES
23.5 SONSTIGE
24. GLOBALER MARKT FÜR DAS OUTSOURCING VON REGULATORISCHEN ANGELEGENHEITEN IN DER IN-VITRO-DIAGNOSTIK (IVD) NACH REGIONEN
24.1 GLOBALER MARKT FÜR DAS OUTSOURCING VON REGULATORISCHEN ANGELEGENHEITEN IM BEREICH DER IN-VITRO-DIAGNOSTIK (IVD) (ALLE OBEN ANGEGEBENEN SEGMENTIERUNGEN WERDEN IN DIESEM KAPITEL NACH LÄNDERN DARGESTELLT)
24.1.1 NORDAMERIKA
24.1.1.1. USA
24.1.1.2. KANADA
24.1.1.3. MEXIKO
24.1.2 EUROPA
24.1.2.1. DEUTSCHLAND
24.1.2.2. FRANKREICH
24.1.2.3. Vereinigtes Königreich
24.1.2.4. ITALIEN
24.1.2.5. SPANIEN
24.1.2.6. RUSSLAND
24.1.2.7. TÜRKEI
24.1.2.8. BELGIEN
24.1.2.9. NIEDERLANDE
24.1.2.10. SCHWEIZ
24.1.2.11. RESTLICHES EUROPA
24.1.3 ASIEN-PAZIFIK
24.1.3.1. JAPAN
24.1.3.2. CHINA
24.1.3.3. SÜDKOREA
24.1.3.4. INDIEN
24.1.3.5. AUSTRALIEN
24.1.3.6. SINGAPUR
24.1.3.7. THAILAND
24.1.3.8. MALAYSIA
24.1.3.9. INDONESIEN
24.1.3.10. PHILIPPINEN
24.1.3.11. RESTLICHER ASIEN-PAZIFIK-RAUM
24.1.4 SÜDAMERIKA
24.1.4.1. BRASILIEN
24.1.4.2. ARGENTINIEN
24.1.4.3. RESTLICHES SÜDAMERIKA
24.1.5 NAHER OSTEN UND AFRIKA
24.1.5.1. SÜDAFRIKA
24.1.5.2. ÄGYPTEN
24.1.5.3. ISRAEL
24.1.5.4. VAE
24.1.5.5. Saudi-Arabien
24.1.5.6. RESTLICHER NAHER OSTEN UND AFRIKA
24.1.6 WICHTIGE PRIMÄRE ERKENNTNISSE: NACH WICHTIGEN LÄNDERN
25. GLOBALER OUTSOURCING-MARKT FÜR IN-VITRO-DIAGNOSTIK (IVD) REGULATORISCHE ANGELEGENHEITEN, UNTERNEHMENSLANDSCHAFT
25.1 UNTERNEHMENSAKTIENANALYSE: GLOBAL
25.2 UNTERNEHMENSAKTIENANALYSE: NORDAMERIKA
25.3 UNTERNEHMENSAKTIENANALYSE: EUROPA
25.4 UNTERNEHMENSAKTIENANALYSE: ASIEN-PAZIFIK
25.5 FUSIONEN UND ÜBERNAHMEN
25.6 NEUE PRODUKTENTWICKLUNG UND ZULASSUNGEN
25.7 ERWEITERUNGEN
25.8 ÄNDERUNGEN DER VORSCHRIFTEN
25.9 PARTNERSCHAFTEN UND ANDERE STRATEGISCHE ENTWICKLUNGEN
26. GLOBALER OUTSOURCING-MARKT FÜR IN-VITRO-DIAGNOSTIK (IVD)-REGULATORISCHE ANGELEGENHEITEN, FIRMENPROFIL
26.1 FREYR-LÖSUNGEN
26.1.1 UNTERNEHMENSÜBERSICHT
26.1.2 UNTERNEHMENSÜBERSICHT
26.1.3 UMSATZANALYSE
26.1.4 PRODUKTPORTFOLIO
26.1.5 JÜNGSTE ENTWICKLUNGEN
26.2 AXSOURCE CONSULTING INC.
26.2.1 UNTERNEHMENSÜBERSICHT
26.2.2 UNTERNEHMENSÜBERSICHT
26.2.3 Umsatzanalyse
26.2.4 PRODUKTPORTFOLIO
26.2.5 JÜNGSTE ENTWICKLUNGEN
26.3 LORENZ LIFE SCIENCES GROUP
26.3.1 UNTERNEHMENSÜBERSICHT
26.3.2 UNTERNEHMENSÜBERSICHT
26.3.3 Umsatzanalyse
26.3.4 PRODUKTPORTFOLIO
26.3.5 JÜNGSTE ENTWICKLUNGEN
26.4 LABORATORY CORPORATION OF AMERICA HOLDINGS
26.4.1 UNTERNEHMENSÜBERSICHT
26.4.2 UNTERNEHMENSÜBERSICHT
26.4.3 Umsatzanalyse
26.4.4 PRODUKTPORTFOLIO
26.4.5 JÜNGSTE ENTWICKLUNGEN
26.5 REG IQ PTY LTD.
26.5.1 UNTERNEHMENSÜBERSICHT
26.5.2 UNTERNEHMENSÜBERSICHT
26.5.3 UMSATZANALYSE
26.5.4 PRODUKTPORTFOLIO
26.5.5 JÜNGSTE ENTWICKLUNGEN
26.6 PROMEDICA INTERNATIONAL, EIN KALIFORNISCHES UNTERNEHMEN (IUVO BIOSCIENCES)
26.6.1 UNTERNEHMENSÜBERSICHT
26.6.2 UNTERNEHMENSÜBERSICHT
26.6.3 UMSATZANALYSE
26.6.4 PRODUKTPORTFOLIO
26.6.5 JÜNGSTE ENTWICKLUNGEN
26.7 MAKROCARE
26.7.1 UNTERNEHMENSÜBERSICHT
26.7.2 UNTERNEHMENSÜBERSICHT
26.7.3 UMSATZANALYSE
26.7.4 PRODUKTPORTFOLIO
26.7.5 JÜNGSTE ENTWICKLUNGEN
26.8 NOTFALL VON UL
26.8.1 UNTERNEHMENSÜBERSICHT
26.8.2 UNTERNEHMENSÜBERSICHT
26.8.3 UMSATZANALYSE
26.8.4 PRODUKTPORTFOLIO
26.8.5 JÜNGSTE ENTWICKLUNGEN
26.9 ICON PLC
26.9.1 UNTERNEHMENSÜBERSICHT
26.9.2 UNTERNEHMENSÜBERSICHT
26.9.3 UMSATZANALYSE
26.9.4 PRODUKTPORTFOLIO
26.9.5 JÜNGSTE ENTWICKLUNGEN
26.10 WUXI APPTEC
26.10.1 UNTERNEHMENSÜBERSICHT
26.10.2 UNTERNEHMENSÜBERSICHT
26.10.3 UMSATZANALYSE
26.10.4 PRODUKTPORTFOLIO
26.10.5 JÜNGSTE ENTWICKLUNGEN
26.11 THERMO FISHER SCIENTIFIC INC.
26.11.1 UNTERNEHMENSÜBERSICHT
26.11.2 UNTERNEHMENSÜBERSICHT
26.11.3 UMSATZANALYSE
26.11.4 PRODUKTPORTFOLIO
26.11.5 JÜNGSTE ENTWICKLUNGEN
26.12 CHARLES RIVER LABORATORIES.
26.12.1 FIRMENÜBERSICHT
26.12.2 UNTERNEHMENSÜBERSICHT
26.12.3 Umsatzanalyse
26.12.4 PRODUKTPORTFOLIO
26.12.5 NEUESTE ENTWICKLUNGEN
26.13 ACCELL CLINICAL RESEARCH, LLC
26.13.1 UNTERNEHMENSÜBERSICHT
26.13.2 UNTERNEHMENSÜBERSICHT
26.13.3 UMSATZANALYSE
26.13.4 PRODUKTPORTFOLIO
26.13.5 NEUESTE ENTWICKLUNGEN
26.14 PAREXEL INTERNATIONAL (MA) CORPORATION
26.14.1 UNTERNEHMENSÜBERSICHT
26.14.2 UNTERNEHMENSÜBERSICHT
26.14.3 UMSATZANALYSE
26.14.4 PRODUKTPORTFOLIO
26.14.5 NEUESTE ENTWICKLUNGEN
26.15 METECON GMBH
26.15.1 UNTERNEHMENSÜBERSICHT
26.15.2 UNTERNEHMENSÜBERSICHT
26.15.3 UMSATZANALYSE
26.15.4 PRODUKTPORTFOLIO
26.15.5 NEUESTE ENTWICKLUNGEN
26.16 GENPACT
26.16.1 UNTERNEHMENSÜBERSICHT
26.16.2 UNTERNEHMENSÜBERSICHT
26.16.3 UMSATZANALYSE
26.16.4 PRODUKTPORTFOLIO
26.16.5 NEUESTE ENTWICKLUNGEN
26.17 CRITERIUM, INC
26.17.1 UNTERNEHMENSÜBERSICHT
26.17.2 UNTERNEHMENSÜBERSICHT
26.17.3 UMSATZANALYSE
26.17.4 PRODUKTPORTFOLIO
26.17.5 NEUESTE ENTWICKLUNGEN
26.18 MEDPACE
26.18.1 UNTERNEHMENSÜBERSICHT
26.18.2 UNTERNEHMENSÜBERSICHT
26.18.3 UMSATZANALYSE
26.18.4 PRODUKTPORTFOLIO
26.18.5 NEUESTE ENTWICKLUNGEN
26.19 GROUPE PRODUCTLIFE SA
26.19.1 UNTERNEHMENSÜBERSICHT
26.19.2 UNTERNEHMENSÜBERSICHT
26.19.3 UMSATZANALYSE
26.19.4 PRODUKTPORTFOLIO
26.19.5 JÜNGSTE ENTWICKLUNGEN
26.20 DOR PHARMAZEUTISCHE DIENSTLEISTUNGEN
26.20.1 UNTERNEHMENSÜBERSICHT
26.20.2 UNTERNEHMENSÜBERSICHT
26.20.3 UMSATZANALYSE
26.20.4 PRODUKTPORTFOLIO
26.20.5 JÜNGSTE ENTWICKLUNGEN
26.21 QSERVE
26.21.1 UNTERNEHMENSÜBERSICHT
26.21.2 UNTERNEHMENSÜBERSICHT
26.21.3 UMSATZANALYSE
26.21.4 PRODUKTPORTFOLIO
26.21.5 JÜNGSTE ENTWICKLUNGEN
26.22 ORTHO-KLINISCHE DIAGNOSTIK.
26.22.1 UNTERNEHMENSÜBERSICHT
26.22.2 UNTERNEHMENSÜBERSICHT
26.22.3 UMSATZANALYSE
26.22.4 PRODUKTPORTFOLIO
26.22.5 JÜNGSTE ENTWICKLUNGEN
26,23 ANGSTROM BIOTECH PVT. LTD.
26.23.1 UNTERNEHMENSÜBERSICHT
26.23.2 UNTERNEHMENSÜBERSICHT
26.23.3 UMSATZANALYSE
26.23.4 PRODUKTPORTFOLIO
26.23.5 JÜNGSTE ENTWICKLUNGEN
26,24 RQM+
26.24.1 UNTERNEHMENSÜBERSICHT
26.24.2 UNTERNEHMENSÜBERSICHT
26.24.3 UMSATZANALYSE
26.24.4 PRODUKTPORTFOLIO
26.24.5 JÜNGSTE ENTWICKLUNGEN
26.25 Mitarbeiter für die Einhaltung gesetzlicher Vorschriften (SOTERA HEALTH)
26.25.1 UNTERNEHMENSÜBERSICHT
26.25.2 UNTERNEHMENSÜBERSICHT
26.25.3 Umsatzanalyse
26.25.4 PRODUKTPORTFOLIO
26.25.5 NEUESTE ENTWICKLUNGEN
26.26 FORSCHUNGDX
26.26.1 UNTERNEHMENSÜBERSICHT
26.26.2 UNTERNEHMENSÜBERSICHT
26.26.3 UMSATZANALYSE
26.26.4 PRODUKTPORTFOLIO
26.26.5 JÜNGSTE ENTWICKLUNGEN
26,27 CMIC HOLDINGS CO., LTD.
26.27.1 UNTERNEHMENSÜBERSICHT
26.27.2 UNTERNEHMENSÜBERSICHT
26.27.3 UMSATZANALYSE
26.27.4 PRODUKTPORTFOLIO
26.27.5 NEUESTE ENTWICKLUNGEN
26.28 NORTH AMERICAN SCIENCE ASSOCIATES, LLC
26.28.1 UNTERNEHMENSÜBERSICHT
26.28.2 UNTERNEHMENSÜBERSICHT
26.28.3 UMSATZANALYSE
26.28.4 PRODUKTPORTFOLIO
26.28.5 JÜNGSTE ENTWICKLUNGEN
26.29 QARAD BV
26.29.1 UNTERNEHMENSÜBERSICHT
26.29.2 UNTERNEHMENSÜBERSICHT
26.29.3 UMSATZANALYSE
26.29.4 PRODUKTPORTFOLIO
26.29.5 NEUESTE ENTWICKLUNGEN
26.30 TRANSKRIPTION
26.30.1 UNTERNEHMENSÜBERSICHT
26.30.2 UNTERNEHMENSÜBERSICHT
26.30.3 UMSATZANALYSE
26.30.4 PRODUKTPORTFOLIO
26.30.5 NEUESTE ENTWICKLUNGEN
26.31 CLIN-R+
26.31.1 UNTERNEHMENSÜBERSICHT
26.31.2 UNTERNEHMENSÜBERSICHT
26.31.3 UMSATZANALYSE
26.31.4 PRODUKTPORTFOLIO
26.31.5 JÜNGSTE ENTWICKLUNGEN
26,32 VCLS
26.32.1 UNTERNEHMENSÜBERSICHT
26.32.2 UNTERNEHMENSÜBERSICHT
26.32.3 UMSATZANALYSE
26.32.4 PRODUKTPORTFOLIO
26.32.5 JÜNGSTE ENTWICKLUNGEN
26,33 PROPHARMA-GRUPPE
26.33.1 UNTERNEHMENSÜBERSICHT
26.33.2 UNTERNEHMENSÜBERSICHT
26.33.3 UMSATZANALYSE
26.33.4 PRODUKTPORTFOLIO
26.33.5 JÜNGSTE ENTWICKLUNGEN
26.34 ARRIELLO IRELAND LIMITED
26.34.1 UNTERNEHMENSÜBERSICHT
26.34.2 UNTERNEHMENSÜBERSICHT
26.34.3 UMSATZANALYSE
26.34.4 PRODUKTPORTFOLIO
26.34.5 NEUESTE ENTWICKLUNGEN
HINWEIS: DIE PROFILIERTEN UNTERNEHMEN SIND KEINE ERSCHLIESSENDE LISTE UND ENTSPRECHEN DEN ANFORDERUNGEN UNSERER VORHERIGEN KUNDEN. WIR PROFILIEREN MEHR ALS 100 UNTERNEHMEN IN UNSERER STUDIE. DAHER KANN DIE LISTE DER UNTERNEHMEN AUF ANFRAGE GEÄNDERT ODER ERSETZT WERDEN.
27. ZUGEHÖRIGE BERICHTE
28. FRAGEBOGEN
29. ÜBER DATA BRIDGE MARKET RESEARCH
Forschungsmethodik
Die Datenerfassung und Basisjahresanalyse werden mithilfe von Datenerfassungsmodulen mit großen Stichprobengrößen durchgeführt. Die Phase umfasst das Erhalten von Marktinformationen oder verwandten Daten aus verschiedenen Quellen und Strategien. Sie umfasst die Prüfung und Planung aller aus der Vergangenheit im Voraus erfassten Daten. Sie umfasst auch die Prüfung von Informationsinkonsistenzen, die in verschiedenen Informationsquellen auftreten. Die Marktdaten werden mithilfe von marktstatistischen und kohärenten Modellen analysiert und geschätzt. Darüber hinaus sind Marktanteilsanalyse und Schlüsseltrendanalyse die wichtigsten Erfolgsfaktoren im Marktbericht. Um mehr zu erfahren, fordern Sie bitte einen Analystenanruf an oder geben Sie Ihre Anfrage ein.
Die wichtigste Forschungsmethodik, die vom DBMR-Forschungsteam verwendet wird, ist die Datentriangulation, die Data Mining, die Analyse der Auswirkungen von Datenvariablen auf den Markt und die primäre (Branchenexperten-)Validierung umfasst. Zu den Datenmodellen gehören ein Lieferantenpositionierungsraster, eine Marktzeitlinienanalyse, ein Marktüberblick und -leitfaden, ein Firmenpositionierungsraster, eine Patentanalyse, eine Preisanalyse, eine Firmenmarktanteilsanalyse, Messstandards, eine globale versus eine regionale und Lieferantenanteilsanalyse. Um mehr über die Forschungsmethodik zu erfahren, senden Sie eine Anfrage an unsere Branchenexperten.
Anpassung möglich
Data Bridge Market Research ist ein führendes Unternehmen in der fortgeschrittenen formativen Forschung. Wir sind stolz darauf, unseren bestehenden und neuen Kunden Daten und Analysen zu bieten, die zu ihren Zielen passen. Der Bericht kann angepasst werden, um Preistrendanalysen von Zielmarken, Marktverständnis für zusätzliche Länder (fordern Sie die Länderliste an), Daten zu klinischen Studienergebnissen, Literaturübersicht, Analysen des Marktes für aufgearbeitete Produkte und Produktbasis einzuschließen. Marktanalysen von Zielkonkurrenten können von technologiebasierten Analysen bis hin zu Marktportfoliostrategien analysiert werden. Wir können so viele Wettbewerber hinzufügen, wie Sie Daten in dem von Ihnen gewünschten Format und Datenstil benötigen. Unser Analystenteam kann Ihnen auch Daten in groben Excel-Rohdateien und Pivot-Tabellen (Fact Book) bereitstellen oder Sie bei der Erstellung von Präsentationen aus den im Bericht verfügbaren Datensätzen unterstützen.