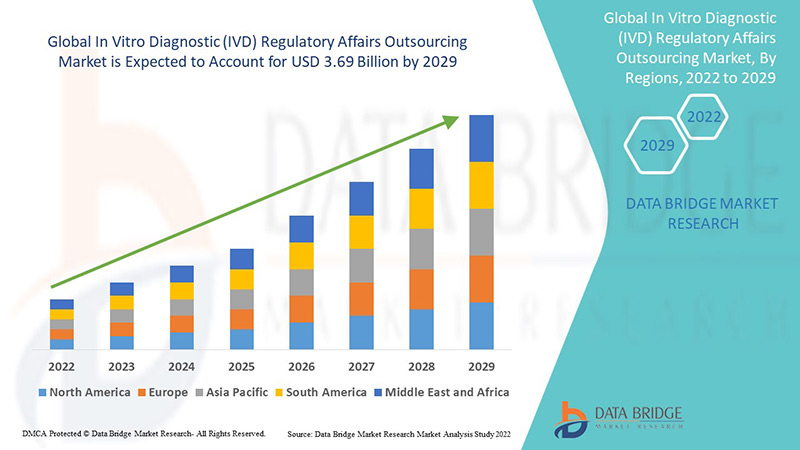
Global In Vitro Diagnostic Ivd Regulatory Affairs Outsourcing Market
Размер рынка в млрд долларов США
CAGR :
% 
 USD
674,277.97 Thousand
USD
1,830,957.45 Thousand
2021
2029
USD
674,277.97 Thousand
USD
1,830,957.45 Thousand
2021
2029
| 2022 –2029 | |
| USD 674,277.97 Thousand | |
| USD 1,830,957.45 Thousand | |
|
|
|
|
Глобальный рынок аутсорсинга нормативно-правовых вопросов диагностики in vitro (IVD), по услугам (нормативное написание и подача документов, нормативная регистрация и заявки на клинические испытания, нормативный консалтинг, юридическое представительство, услуги по управлению данными, услуги по производству и контролю химии (CMC) и другие), показания (онкология, неврология, кардиология, клиническая химия и иммуноанализы, прецизионная медицина, инфекционные заболевания, диабет, генетическое тестирование, ВИЧ/СПИД, гематология, тестирование на наркотики/фармакогеномика, переливание крови, точка оказания медицинской помощи и другие), режим развертывания (облачный и локальный), размер организации (малые и средние предприятия (SMES) и крупные предприятия), стадия (клиническая, доклиническая и PMA (пострегистрационная авторизация)), класс (класс I, класс II и класс III), конечный пользователь (фармацевтические компании, компании по производству медицинских приборов, биотехнологические компании и Другие) – Тенденции отрасли и прогноз до 2029 г.
Анализ и размер рынка
Компании здравоохранения столкнулись с трудностями в соблюдении нормативных стандартов, особенно из-за пандемии COVID-19 (коронавируса). Чтобы обеспечить культуру, ориентированную на качество, для компаний в сфере медицинских технологий консалтинговые фирмы используют программное обеспечение для систем управления качеством (QMS). Компании, занимающиеся аутсорсингом регуляторных вопросов диагностики in vitro (IVD), оказывают организациям здравоохранения поддержку на основе проектов.
Развертывание аутсорсинга приводит к заключению долгосрочных соглашений об аутсорсинге. Глобальный рынок аутсорсинга нормативно-правовых вопросов диагностики in vitro (IVD) оценивался в 1,6 млрд долларов США в 2021 году и, как ожидается, достигнет 3,69 млрд долларов США к 2029 году, зарегистрировав среднегодовой темп роста в 11% в прогнозируемый период 2022-2029 годов. Ожидается, что фармацевтические компании будут свидетелями высокого роста в связи с увеличением числа клинических одобрений.
Определение рынка
Нормативные вопросы играют крайне важную роль в отрасли диагностических устройств для ЭКО (IVD). Эти вопросы касаются жизненного цикла различных медицинских продуктов и предлагают стратегическую, тактическую и операционную поддержку и направление для производственных компаний для работы в рамках нормативной базы.
Область отчета и сегментация рынка
|
Отчет Метрика |
Подробности |
|
Прогнозируемый период |
2022-2029 |
|
Базовый год |
2021 |
|
Исторические годы |
2020 (Можно настроить на 2019 - 2014) |
|
Количественные единицы |
Доход в млн. долл. США, объемы в единицах, цены в долл. США |
|
Охваченные сегменты |
Услуга (написание и подача нормативных документов, нормативная регистрация и заявки на клинические испытания, нормативный консалтинг, юридическое представительство, услуги по управлению данными, услуги по производству и контролю химии (CMC) и другие), Показания (онкология, неврология, кардиология, клиническая химия и иммуноанализы, прецизионная медицина, инфекционные заболевания, диабет, генетическое тестирование, ВИЧ/СПИД, гематология, тестирование лекарств/фармакогеномика, переливание крови, точка оказания медицинской помощи и другие), Режим развертывания (облачный и локальный), Размер организации (малые и средние предприятия (SMES) и крупные предприятия), Стадия (клиническая, доклиническая и PMA (пострегистрационная авторизация)), Класс (класс I, класс II и класс III), Конечный пользователь (фармацевтические компании, компании по производству медицинских приборов, биотехнологические компании и другие) |
|
Страны, охваченные |
США, Канада и Мексика в Северной Америке, Германия, Франция, Великобритания, Нидерланды, Швейцария, Бельгия, Россия, Италия, Испания, Турция, Остальная Европа в Европе, Китай, Япония, Индия, Южная Корея, Сингапур, Малайзия, Австралия, Таиланд, Индонезия, Филиппины, Остальная часть Азиатско-Тихоокеанского региона (APAC) в Азиатско-Тихоокеанском регионе (APAC), Саудовская Аравия, ОАЭ, Южная Африка, Египет, Израиль, Остальной Ближний Восток и Африка (MEA) как часть Ближнего Востока и Африки (MEA), Бразилия, Аргентина и Остальная часть Южной Америки как часть Южной Америки. |
|
Охваченные участники рынка |
Freyr Solutions (Индия), PPD Inc. (США), EMERGO (США), ICON (здравоохранение), Parexel International Corporation (США), CRITERIUM, INC. (США), Groupe ProductLife SA (Франция), Labcorp Drug Development (США), WuXi AppTec (Китай), Genpact (США), Medpace (США), Dor Pharmaceutical Services (Израиль), Qserve (Нидерланды) и другие |
|
Возможности рынка |
|
Динамика рынка аутсорсинга нормативно-правового регулирования диагностики in vitro (IVD)
В этом разделе рассматривается понимание движущих сил рынка, преимуществ, возможностей, ограничений и проблем. Все это подробно обсуждается ниже:
- Широкое применение в сфере здравоохранения
Рост использования аутсорсинговых услуг в секторе здравоохранения является одним из основных факторов, способствующих росту рынка аутсорсинга регуляторных вопросов диагностики in vitro (IVD). Рост активности по географическому расширению, направленной на быстрые одобрения на местных рынках, еще больше способствует росту.
- Исследования и разработки
Рост научно-исследовательской деятельности, увеличение объема заявок на клинические испытания и регистрацию продуктов ускоряют рост рынка.
- Клинические одобрения
Наблюдается рост спроса на аутсорсинг регуляторных вопросов in vitro диагностики (IVD), поскольку компании находятся под постоянным давлением, требующим своевременных клинических одобрений от регулирующих органов. Спрос на услуги регуляторных вопросов растет из-за таких действий.
Возможности
Кроме того, разработка биомаркеров и тестов, специфичных для заболеваний, а также значимость сопутствующей диагностики расширяют прибыльные возможности для участников рынка в прогнозируемый период с 2022 по 2029 год. Кроме того, резкий рост инвестиций будет способствовать дальнейшему расширению рынка.
Ограничения/Проблемы
С другой стороны, ожидается, что изменяющиеся правила, касающиеся медицинских приборов и аутсорсинга вопросов регулирования диагностики in vitro (IVD), будут препятствовать росту рынка. Кроме того, ожидается, что отсутствие инфраструктуры в сфере услуг здравоохранения осложнит рынок аутсорсинга вопросов регулирования диагностики in vitro (IVD) в прогнозируемый период 2022-2029 гг.
В этом отчете по аутсорсингу рынка регуляторных вопросов диагностики in vitro (IVD) содержатся сведения о последних новых разработках, правилах торговли, анализе импорта-экспорта, анализе производства, оптимизации цепочки создания стоимости, доле рынка, влиянии внутренних и локальных игроков рынка, анализируются возможности с точки зрения новых источников дохода, изменений в правилах рынка, анализ стратегического роста рынка, размер рынка, рост рынка категорий, ниши приложений и доминирование, одобрение продуктов, запуск продуктов, географическое расширение, технологические инновации на рынке. Чтобы получить больше информации о рынке аутсорсинга регуляторных вопросов диагностики in vitro (IVD), свяжитесь с Data Bridge Market Research для получения аналитического обзора, наша команда поможет вам принять обоснованное рыночное решение для достижения роста рынка.
Влияние COVID-19 на рынок диагностических тестов
COVID-19 оказал негативное влияние на сектор здравоохранения. Основные ключевые игроки адаптировали инновационные стратегии к быстро меняющейся ситуации во время вспышки COVID-19. Страны принимали критические изменения в здравоохранении, пока кризис не отошел на второй план. Ожидается, что реформы здравоохранения станут свидетелями сдерживания расходов, расширения доступа и технологического прогресса в ближайшие годы. Рост спроса на аутсорсинг регуляторных вопросов диагностики in vitro (IVD) был отмечен из-за акцента на важности удаленной диагностики, ухода и консультаций. Эти услуги снижают нагрузку на больницы в постпандемическом сценарии.
Последние события
- Журнал USA-9 Technology Magazine включил Freyr в список «10 лучших поставщиков технологических решений 2021 года» в ноябре 2021 года. USA-9.com — это технологический журнал, который включил Freyr Solutions, ведущего мирового поставщика решений и услуг в области регулирования, в список «10 лучших поставщиков технологических решений 2021 года», поскольку Fryer продолжает разрабатывать инновационные программные решения и оказывать поддержку клиентам в достижении их соответствующих целей по обеспечению соответствия. Это помогло компании повысить свою популярность.
Масштаб и размер мирового рынка аутсорсинга нормативно-правового регулирования диагностики in vitro (IVD)
Рынок аутсорсинга регуляторных вопросов диагностики in vitro (IVD) сегментирован на основе услуг, показаний, способа развертывания, размера организации, стадии, класса и конечного пользователя. Рост среди этих сегментов поможет вам проанализировать сегменты с незначительным ростом в отраслях и предоставить пользователям ценный обзор рынка и рыночные идеи, которые помогут им принимать стратегические решения для определения основных рыночных приложений.
Услуги
- Нормативные документы и документы
- Регуляторная регистрация и заявки на клинические испытания
- Нормативный консалтинг
- Юридическое представительство
- Услуги по управлению данными
- Услуги по производству и контролю химии (CMC)
- Другие
На основе услуг глобальный рынок аутсорсинга нормативно-правовых вопросов диагностики in vitro (IVD) сегментируется на написание и подачу нормативных документов, нормативную регистрацию и заявки на клинические испытания, нормативный консалтинг, юридическое представительство, услуги по управлению данными, услуги по химическому производству и контролю (CMC) и другие.
Индикация
- Онкология
- Неврология
- Кардиология
- Клиническая химия и иммуноферментный анализ
- Точная медицина
- Инфекционные заболевания
- Диабет
- Генетическое Тестирование
- ВИЧ/СПИД
- Гематология
- Тестирование лекарств/Фармакогеномика
- Переливание крови
- Точка ухода
- Другие
На основе показаний глобальный рынок аутсорсинга нормативно-правового регулирования диагностики in vitro (IVD) сегментирован на онкологию, неврологию, кардиологию, клиническую химию и иммуноанализы, прецизионную медицину, инфекционные заболевания, диабет, генетическое тестирование, ВИЧ/СПИД, гематологию, тестирование на наркотики/фармакогеномику, переливание крови, оказание медицинской помощи на месте и другие.
Режим развертывания
- Облако
- Локально
По способу развертывания глобальный рынок аутсорсинга нормативно-правового регулирования диагностики in vitro (IVD) сегментируется на облачный и локальный.
Размер организации
- Малые и средние предприятия (МСП)
- Крупные предприятия
В зависимости от размера организации глобальный рынок аутсорсинга нормативно-правовых вопросов диагностики in vitro (IVD) сегментируется на малые и средние предприятия (МСП) и крупные предприятия.
Этап
- Клинический
- Доклинические
- PMA (Пострегистрационное разрешение)
В зависимости от стадии глобальный рынок аутсорсинга нормативно-правового регулирования диагностики in vitro (IVD) сегментируется на клинический, доклинический и PMA (пострегистрационный).
Сорт
- Класс I
- Класс II
- Класс III
На основе класса глобальный рынок аутсорсинга нормативно-правового регулирования диагностики in vitro (IVD) сегментируется на класс I, класс II и класс III.
Конечный пользователь
- Фармацевтические компании
- Компании по производству медицинского оборудования
- Биотехнологические компании
- Другие
В зависимости от конечного пользователя глобальный рынок аутсорсинга нормативно-правового регулирования диагностики in vitro (IVD) сегментируется на фармацевтические компании, компании по производству медицинских приборов, биотехнологические компании и другие.
Региональный анализ/информация о рынке аутсорсинга нормативно-правового регулирования диагностики in vitro (IVD)
Проанализирован рынок аутсорсинга нормативно-правового регулирования диагностики in vitro (IVD), а также предоставлены сведения о размерах рынка и тенденциях по странам, услугам, показаниям, режиму развертывания, размеру организации, стадии, классу и конечному пользователю, как указано выше.
Страны, охваченные отчетом о рынке аутсорсинга нормативно-правового регулирования диагностики in vitro (IVD): США, Канада и Мексика в Северной Америке, Германия, Франция, Великобритания, Нидерланды, Швейцария, Бельгия, Россия, Италия, Испания, Турция, остальные страны Европы в Европе, Китай, Япония, Индия, Южная Корея, Сингапур, Малайзия, Австралия, Таиланд, Индонезия, Филиппины, остальные страны Азиатско-Тихоокеанского региона (APAC) в Азиатско-Тихоокеанском регионе (APAC), Саудовская Аравия, ОАЭ, Южная Африка, Египет, Израиль, остальные страны Ближнего Востока и Африки (MEA) как часть Ближнего Востока и Африки (MEA), Бразилия, Аргентина и остальные страны Южной Америки как часть Южной Америки.
Азиатско-Тихоокеанский регион (APAC) доминирует на рынке аутсорсинга нормативно-правовых вопросов в области диагностики in vitro (IVD) из-за роста числа клинических испытаний и увеличения числа компаний в регионе.
Ожидается, что в прогнозируемый период с 2022 по 2029 год в Северной Америке будет наблюдаться значительный рост за счет присутствия ключевых компаний по производству фармацевтических препаратов и медицинских приборов, а также увеличения расходов на исследования и разработки в регионе.
Раздел отчета по странам также содержит отдельные факторы, влияющие на рынок, и изменения в регулировании на внутреннем рынке, которые влияют на текущие и будущие тенденции рынка. Такие данные, как анализ цепочки создания стоимости вверх и вниз по течению, технические тенденции и анализ пяти сил Портера, тематические исследования, являются некоторыми из указателей, используемых для прогнозирования рыночного сценария для отдельных стран. Кроме того, при предоставлении прогнозного анализа данных по странам учитываются наличие и доступность глобальных брендов и их проблемы, связанные с большой или малой конкуренцией со стороны местных и внутренних брендов, влияние внутренних тарифов и торговых путей.
Рост инфраструктуры здравоохранения Установленная база и проникновение новых технологий
Рынок аутсорсинга регуляторных вопросов диагностики in vitro (IVD) также предоставляет вам подробный анализ рынка для каждой страны по росту расходов на здравоохранение на капитальное оборудование, установленной базы различных видов продукции для рынка аутсорсинга регуляторных вопросов диагностики in vitro (IVD), влияния технологий с использованием кривых жизненной линии и изменений в сценариях регулирования здравоохранения и их влияния на рынок аутсорсинга регуляторных вопросов диагностики in vitro (IVD). Данные доступны за исторический период 2010-2020 гг.
Анализ доли рынка аутсорсинга в сфере аутсорсинга в сфере диагностики in vitro (IVD) и конкурентной среды
Конкурентная среда рынка аутсорсинга регуляторных вопросов диагностики in vitro (IVD) содержит сведения по конкурентам. Включены сведения о компании, ее финансах, полученном доходе, рыночном потенциале, инвестициях в исследования и разработки, новых рыночных инициативах, глобальном присутствии, производственных площадках и объектах, производственных мощностях, сильных и слабых сторонах компании, запуске продукта, широте и широте продукта, доминировании приложений. Приведенные выше данные касаются только фокуса компаний, связанного с рынком аутсорсинга регуляторных вопросов диагностики in vitro (IVD).
Некоторые из основных игроков, работающих на рынке аутсорсинга нормативно-правовых вопросов в области диагностики in vitro (IVD):
- Freyr Solutions (Индия)
- PPD Inc. (США)
- ЭМЕРГО (США)
- ЗНАЧОК (Здравоохранение)
- Parexel International Corporation (США)
- CRITERIUM, INC. (США)
- Groupe ProductLife SA (Франция)
- Labcorp Drug Development (США)
- WuXi AppTec (Китай)
- Генпакт (США)
- Медпейс (США)
- Dor Pharmaceutical Services (Израиль)
- Qserve (Нидерланды)
SKU-
Получите онлайн-доступ к отчету на первой в мире облачной платформе рыночной аналитики
- Интерактивная панель анализа данных
- Панель анализа компании для возможностей с высоким потенциалом роста
- Доступ аналитика-исследователя для настройки и запросов
- Анализ конкурентов с помощью интерактивной панели
- Последние новости, обновления и анализ тенденций
- Используйте возможности сравнительного анализа для комплексного отслеживания конкурентов
Содержание
1. ВВЕДЕНИЕ
1.1 ЦЕЛИ ИССЛЕДОВАНИЯ
1.2 ОПРЕДЕЛЕНИЕ РЫНКА
1.3 ОБЗОР МИРОВОГО РЫНКА АУТСОРСИНГА ВОПРОСОВ РЕГУЛИРОВАНИЯ ДИАГНОСТИКИ IN VITRO (IVD)
1.4 ВАЛЮТА И ЦЕНЫ
1.5 ОГРАНИЧЕНИЕ
1.6 ОХВАЧЕННЫЕ РЫНКИ
2. СЕГМЕНТАЦИЯ РЫНКА
2.1 КЛЮЧЕВЫЕ ВЫВОДЫ
2.2 ДОСТИЖЕНИЕ ОБЪЕМА МИРОВОГО РЫНКА АУТСОРСИНГА ВОПРОСОВ РЕГУЛИРОВАНИЯ ДИАГНОСТИКИ IN VITRO (IVD)
2.2.1 СЕТКА ПОЗИЦИОНИРОВАНИЯ ПОСТАВЩИКА
2.2.2 КРИВАЯ ЛИНИИ ЖИЗНИ ТЕХНОЛОГИЙ
2.2.3 МНОГОФАКТОРНОЕ МОДЕЛИРОВАНИЕ
2.2.4 АНАЛИЗ СВЕРХУ ВНИЗ
2.2.5 СТАНДАРТЫ ИЗМЕРЕНИЯ
2.2.6 АНАЛИЗ ДОЛИ ПОСТАВЩИКА
2.2.7 ТОЧКИ ДАННЫХ ИЗ КЛЮЧЕВЫХ ПЕРВИЧНЫХ ИНТЕРВЬЮ
2.2.8 ТОЧКИ ДАННЫХ ИЗ КЛЮЧЕВЫХ ВТОРИЧНЫХ БАЗ ДАННЫХ
2.3 ГЛОБАЛЬНЫЙ РЫНОК АУТСОРСИНГА ВОПРОСОВ РЕГУЛИРОВАНИЯ ДИАГНОСТИКИ IN VITRO (IVD): ОБЗОР ИССЛЕДОВАНИЯ
2.4 ПРЕДПОЛОЖЕНИЯ
3. ОБЗОР РЫНКА
3.1 ВОДИТЕЛИ
3.2 ОГРАНИЧЕНИЯ
3.3 ВОЗМОЖНОСТИ
3.4 ПРОБЛЕМЫ
4. ПРЕМИУМ-ИНФОРМАЦИЯ
4.1 АНАЛИЗ ПЕСТЕЛЯ
4.2 МОДЕЛЬ ПЯТИ СИЛ ПОРТЕРА
5. ОТРАСЛЕВЫЕ ИНСАЙТЫ
5.1 МИКРО- И МАКРОЭКОНОМИЧЕСКИЕ ФАКТОРЫ
5.2 КАРТИРОВАНИЕ ПЕРСПЕКТИВ ПРОНИКНОВЕНИЯ И РОСТА
5.3 КЛЮЧЕВЫЕ СТРАТЕГИИ ЦЕНООБРАЗОВАНИЯ
5.4 ИНТЕРВЬЮ СО СПЕЦИАЛИСТОМ
5.5 АНАЛИЗ И РЕКОМЕНДАЦИИ
6. ПОРТФЕЛЬ ИНТЕЛЛЕКТУАЛЬНОЙ СОБСТВЕННОСТИ (ИС)
6.1 КАЧЕСТВО И ПРОЧНОСТЬ ПАТЕНТА
6.2 ПАТЕНТНЫЕ СЕМЕЙСТВА
6.3 ЛИЦЕНЗИРОВАНИЕ И СОТРУДНИЧЕСТВО
6.4 КОНКУРЕНТНЫЙ ЛАНДШАФТ
6.5 СТРАТЕГИЯ И УПРАВЛЕНИЕ ИС
6.6 ДРУГОЕ
7. РАСПРЕДЕЛЕНИЕ АНАЛИЗА СТОИМОСТИ
8. ТЕХНОЛОГИЧЕСКАЯ ДОРОЖНАЯ КАРТА
9. ИННОВАЦИОННЫЙ ТРЕКЕР И СТРАТЕГИЧЕСКИЙ АНАЛИЗ
9.1 АНАЛИЗ КРУПНЫХ СДЕЛОК И СТРАТЕГИЧЕСКИХ АЛЬЯНСОВ
9.1.1 СОВМЕСТНЫЕ ПРЕДПРИЯТИЯ
9.1.2 СЛИЯНИЯ И ПОГЛОЩЕНИЯ
9.1.3 ЛИЦЕНЗИРОВАНИЕ И ПАРТНЕРСТВО
9.1.4 ТЕХНОЛОГИЧЕСКОЕ СОТРУДНИЧЕСТВО
9.1.5 СТРАТЕГИЧЕСКИЕ ОТЧУЖДЕНИЯ
9.2 КОЛИЧЕСТВО ПРОДУКТОВ В РАЗРАБОТКЕ
9.3 СТАДИЯ РАЗВИТИЯ
9.4 СРОКИ И ВЕХИ
9.5 ИННОВАЦИОННЫЕ СТРАТЕГИИ И МЕТОДОЛОГИИ
9.6 ОЦЕНКА РИСКОВ И ИХ СМЯГЧЕНИЕ
9.7 ПЕРСПЕКТИВЫ БУДУЩЕГО
10. СООТВЕТСТВИЕ НОРМАТИВНЫМ ТРЕБОВАНИЯМ
10.1 РЕГУЛИРУЮЩИЕ ОРГАНЫ
10.2 НОРМАТИВНЫЕ КЛАССИФИКАЦИИ
10.2.1 КЛАСС I
10.2.2 КЛАСС II
10.2.3 КЛАСС III
10.3 НОРМАТИВНЫЕ ПРЕДСТАВЛЕНИЯ
10.4 МЕЖДУНАРОДНАЯ ГАРМОНИЗАЦИЯ
10.5 СИСТЕМЫ УПРАВЛЕНИЯ СООТВЕТСТВИЕМ И КАЧЕСТВОМ
10.6 ПРОБЛЕМЫ И СТРАТЕГИИ РЕГУЛИРОВАНИЯ
11. СТРУКТУРА ВОЗМЕЩЕНИЯ
12. АНАЛИЗ КАРТЫ ВОЗМОЖНОСТЕЙ
13. УСТАНОВЛЕННЫЕ БАЗОВЫЕ ДАННЫЕ
14. АНАЛИЗ ЦЕПОЧКИ СОЗДАНИЯ СТОИМОСТИ
15. ЭКОНОМИКА ЗДРАВООХРАНЕНИЯ
15.1 РАСХОДЫ НА ЗДРАВООХРАНЕНИЕ
15.2 КАПИТАЛЬНЫЕ РАСХОДЫ
15.3 ТЕНДЕНЦИИ КАПИТАЛЬНЫХ ЗАТРАТ
15.4 РАСПРЕДЕЛЕНИЕ КАПИТАЛЬНЫХ ЗАТРАТ
15.5 ИСТОЧНИКИ ФИНАНСИРОВАНИЯ
15.6 ОТРАСЛЕВЫЕ ПОКАЗАТЕЛИ
15.7 ДОЛЯ ВВП В ОБЩЕМ ВВП
15.8 СТРУКТУРА СИСТЕМЫ ЗДРАВООХРАНЕНИЯ
15.9 ПОЛИТИКА ПРАВИТЕЛЬСТВА
15.10 ЭКОНОМИЧЕСКОЕ РАЗВИТИЕ
16. МИРОВОЙ РЫНОК АУТСОРСИНГА ВОПРОСОВ РЕГУЛИРОВАНИЯ ДИАГНОСТИКИ IN VITRO (IVD), ПО УСЛУГАМ
16.1 ОБЗОР
16.2 НОРМАТИВНЫЕ ДОКУМЕНТЫ И ПРЕДСТАВЛЕНИЯ
16.3 ЗАЯВКИ НА РЕГИСТРАЦИЮ В НОРМАТИВНЫХ ОРГАНАХ И КЛИНИЧЕСКИЕ ИСПЫТАНИЯ
16.4 КОНСАЛТИНГ ПО ВОПРОСАМ НОРМАТИВНОГО ПРАВА
16.5 ЮРИДИЧЕСКОЕ ПРЕДСТАВИТЕЛЬСТВО
16.6 УСЛУГИ УПРАВЛЕНИЯ ДАННЫМИ
16.7 УСЛУГИ ПО ПРОИЗВОДСТВУ И КОНТРОЛЮ ХИМИИ (CMC)
16.8 ДРУГИЕ
17. ГЛОБАЛЬНЫЙ РЫНОК АУТСОРСИНГА ВОПРОСОВ РЕГУЛИРОВАНИЯ ДИАГНОСТИКИ IN VITRO (IVD), ПО ПОКАЗАНИЯМ
17.1 ОБЗОР
17.2 ОНКОЛОГИЯ
17.3 НЕВРОЛОГИЯ
17.4 КАРДИОЛОГИЯ
17.5 КЛИНИЧЕСКАЯ ХИМИЯ И ИММУНОАНАЛИЗЫ
17.6 ТОЧНАЯ МЕДИЦИНА
17.7 ИНФЕКЦИОННЫЕ ЗАБОЛЕВАНИЯ
17.7.1 СЕПСИС
17.7.2 ВИРУСОЛОГИЯ
17.7.3 БАКТЕРИОЛОГИЯ
17.7.4 МИКРОБИОЛОГИЯ И МИКОЛОГИЯ
17.7.5 ГЕПАТИТ В
17.7.6 ГЕПАТИТ С
17.7.7 СИФИЛИС
17.7.8 ТУБЕРКУЛЕЗ
17.7.9 МАЛЯРИЯ
17.7.10 ИНФЕКЦИЯ, ВЫЗВАННАЯ ВИРУСОМ ПАПИЛЛОМЫ ЧЕЛОВЕКА (ВПЧ)
17.7.11 ДРУГИЕ
17.8 ДИАБЕТ
17.9 ГЕНЕТИЧЕСКОЕ ТЕСТИРОВАНИЕ
17.10 ВИЧ/СПИД
17.11 ГЕМАТОЛОГИЯ
17.12 ТЕСТИРОВАНИЕ НАРКОТИКОВ/ФАРМАКОГЕНОМИКА
17.13 ПЕРЕЛИВАНИЕ КРОВИ
17.14 ДРУГИЕ
18. МИРОВОЙ РЫНОК АУТСОРСИНГА ВОПРОСОВ РЕГУЛИРОВАНИЯ ДИАГНОСТИКИ IN VITRO (IVD), ПО ЭТАПАМ
18.1 ОБЗОР
18.2 ДОКЛИНИЧЕСКИЙ
18.3 КЛИНИЧЕСКИЙ
18.4 PMA (ПОСТ-РАЗРЕШЕНИЕ НА РЫНОК)
19. МИРОВОЙ РЫНОК АУТСОРСИНГА ВОПРОСОВ РЕГУЛИРОВАНИЯ ДИАГНОСТИКИ IN VITRO (IVD), ПО КЛАССАМ
19.1 ОБЗОР
19.2 КЛАСС I
19.3 КЛАСС II
19.4 КЛАСС III
20. МИРОВОЙ РЫНОК АУТСОРСИНГА ВОПРОСОВ РЕГУЛИРОВАНИЯ ДИАГНОСТИКИ IN VITRO (IVD), ПО ТИПУ
20.1 ОБЗОР
20.2 ПРОДУКТ IVD ДЛЯ МЕДИЦИНСКОЙ ДИАГНОСТИКИ В МЕСТЕ УХОДА (POC)
20.3 ЛАБОРАТОРНО-РАЗРАБОТАННЫЕ ТЕСТЫ (LDTS) ПРОДУКЦИЯ IVD
20.4 СОПУТСТВУЮЩАЯ ДИАГНОСТИКА IVD ПРОДУКТ
20.5 ТЕСТИРОВАНИЕ IVD-ПРОДУКЦИИ ПРЯМО У ПОТРЕБИТЕЛЯ (DTC)
20.6 ДРУГИЕ IVD-ИЗДЕЛИЯ
21. ГЛОБАЛЬНЫЙ РЫНОК АУТСОРСИНГА ВОПРОСОВ РЕГУЛИРОВАНИЯ ДИАГНОСТИКИ IN VITRO (IVD), ПО РЕЖИМУ РАЗВЕРТЫВАНИЯ
21.1 ОБЗОР
21.2 ОБЛАКО
21.3 ЛОКАЛЬНЫЕ
22. МИРОВОЙ РЫНОК АУТСОРСИНГА ВОПРОСОВ РЕГУЛИРОВАНИЯ ДИАГНОСТИКИ IN VITRO (IVD) ПО РАЗМЕРУ ОРГАНИЗАЦИИ
22.1 ОБЗОР
22.2 МАЛЫЕ И СРЕДНИЕ ПРЕДПРИЯТИЯ (МСП)
22.3 КРУПНЫЕ ПРЕДПРИЯТИЯ
23. ГЛОБАЛЬНЫЙ РЫНОК АУТСОРСИНГА ВОПРОСОВ РЕГУЛИРОВАНИЯ ДИАГНОСТИКИ IN VITRO (IVD) ПО КОНЕЧНОМУ ПОЛЬЗОВАТЕЛЮ
23.1 ОБЗОР
23.2 ФАРМАЦЕВТИЧЕСКИЕ КОМПАНИИ
23.2.1 ПО РАЗМЕРУ ОРГАНИЗАЦИИ
23.2.1.1 МАЛЫЕ И СРЕДНИЕ ПРЕДПРИЯТИЯ (МСП)
23.2.1.2 КРУПНЫЕ ПРЕДПРИЯТИЯ
23.2.2 ПО УСЛУГАМ
23.2.2.1. НОРМАТИВНЫЕ ДОКУМЕНТЫ И ПРЕДСТАВЛЕНИЯ
23.2.2.2. ЗАЯВКИ НА РЕГИСТРАЦИЮ В ОРГАНАХ РЕСПУБЛИКИ И КЛИНИЧЕСКИЕ ИСПЫТАНИЯ
23.2.2.3.КОНСАЛТИНГ ПО НОРМАТИВНЫМ ВОПРОСАМ
23.2.2.4. ЮРИДИЧЕСКОЕ ПРЕДСТАВИТЕЛЬСТВО
23.2.2.5.УСЛУГИ ПО УПРАВЛЕНИЮ ДАННЫМИ
23.2.2.6. УСЛУГИ ПО ПРОИЗВОДСТВУ И КОНТРОЛЮ ХИМИИ (CMC)
23.2.2.7 ДРУГИЕ
23.3 КОМПАНИИ-ПРОИЗВОДИТЕЛИ МЕДИЦИНСКОГО ОБОРУДОВАНИЯ
23.3.1 ПО РАЗМЕРУ ОРГАНИЗАЦИИ
23.3.1.1 МАЛЫЕ И СРЕДНИЕ ПРЕДПРИЯТИЯ (МСП)
23.3.1.2 КРУПНЫЕ ПРЕДПРИЯТИЯ
23.3.2 ПО УСЛУГАМ
23.3.2.1. НОРМАТИВНЫЕ ДОКУМЕНТЫ И ПРЕДСТАВЛЕНИЯ
23.3.2.2. ЗАЯВКИ НА РЕГИСТРАЦИЮ В ОРГАНАХ РЕСПУБЛИКИ И КЛИНИЧЕСКИЕ ИСПЫТАНИЯ
23.3.2.3. НОРМАТИВНОЕ КОНСАЛТИНГОВАНИЕ
23.3.2.4. ЮРИДИЧЕСКОЕ ПРЕДСТАВИТЕЛЬСТВО
23.3.2.5.УСЛУГИ УПРАВЛЕНИЯ ДАННЫМИ
23.3.2.6. УСЛУГИ ПО ПРОИЗВОДСТВУ И КОНТРОЛЮ ХИМИИ (CMC)
23.3.2.7 ДРУГИЕ
23.4 БИОТЕХНОЛОГИЧЕСКИЕ КОМПАНИИ
23.4.1 ПО РАЗМЕРУ ОРГАНИЗАЦИИ
23.4.1.1 МАЛЫЕ И СРЕДНИЕ ПРЕДПРИЯТИЯ (МСП)
23.4.1.2 КРУПНЫЕ ПРЕДПРИЯТИЯ
23.4.2 ПО УСЛУГАМ
23.4.2.1. НОРМАТИВНЫЕ ДОКУМЕНТЫ И ПРЕДСТАВЛЕНИЯ
23.4.2.2. ЗАЯВКИ НА РЕГИСТРАЦИЮ В ОРГАНАХ РЕСПУБЛИКИ И КЛИНИЧЕСКИЕ ИСПЫТАНИЯ
23.4.2.3. НОРМАТИВНОЕ КОНСАЛТИНГОВАНИЕ
23.4.2.4. ЮРИДИЧЕСКОЕ ПРЕДСТАВИТЕЛЬСТВО
23.4.2.5.УСЛУГИ УПРАВЛЕНИЯ ДАННЫМИ
23.4.2.6. УСЛУГИ ПО ПРОИЗВОДСТВУ И КОНТРОЛЮ ХИМИИ (CMC)
23.4.2.7 ДРУГИЕ
23.5 ДРУГИЕ
24. МИРОВОЙ РЫНОК АУТСОРСИНГА ВОПРОСОВ РЕГУЛИРОВАНИЯ ДИАГНОСТИКИ IN VITRO (IVD), ПО РЕГИОНАМ
24.1 ГЛОБАЛЬНЫЙ РЫНОК АУТСОРСИНГА ВОПРОСОВ РЕГУЛИРОВАНИЯ ДИАГНОСТИКИ IN VITRO (IVD) (ВСЯ СЕГМЕНТАЦИЯ, ПРЕДСТАВЛЕННАЯ ВЫШЕ, ПРЕДСТАВЛЕНА В ЭТОЙ ГЛАВЕ ПО СТРАНАМ)
24.1.1 СЕВЕРНАЯ АМЕРИКА
24.1.1.1.США
24.1.1.2 КАНАДА
24.1.1.3.МЕКСИКА
24.1.2 ЕВРОПА
24.1.2.1.ГЕРМАНИЯ
24.1.2.2.ФРАНЦИЯ
24.1.2.3 Великобритания
24.1.2.4.ИТАЛИЯ
24.1.2.5 ИСПАНИЯ
24.1.2.6.РОССИЯ
24.1.2.7.ТУРЦИЯ
24.1.2.8.БЕЛЬГИЯ
24.1.2.9. НИДЕРЛАНДЫ
24.1.2.10 ШВЕЙЦАРИЯ
24.1.2.11 ОСТАЛЬНАЯ ЕВРОПА
24.1.3 АЗИАТСКО-ТИХООКЕАНСКИЙ РЕГИОН
24.1.3.1 ЯПОНИЯ
24.1.3.2.КИТАЙ
24.1.3.3 ЮЖНАЯ КОРЕЯ
24.1.3.4 ИНДИЯ
24.1.3.5 АВСТРАЛИЯ
24.1.3.6.СИНГАПУР
24.1.3.7.ТАИЛАНД
24.1.3.8 МАЛАЙЗИЯ
24.1.3.9 ИНДОНЕЗИЯ
24.1.3.10.ФИЛИППИНЫ
24.1.3.11. ОСТАЛЬНЫЕ СТРАНЫ АЗИАТСКО-ТИХООКЕАНСКОГО РЕГИОНА
24.1.4 ЮЖНАЯ АМЕРИКА
24.1.4.1.БРАЗИЛИЯ
24.1.4.2.АРГЕНТИНА
24.1.4.3 ОСТАЛЬНАЯ ЧАСТЬ ЮЖНОЙ АМЕРИКИ
24.1.5 БЛИЖНИЙ ВОСТОК И АФРИКА
24.1.5.1 ЮЖНАЯ АФРИКА
24.1.5.2.ЕГИПЕТ
24.1.5.3 ИЗРАИЛЬ
24.1.5.4.ОАЭ
24.1.5.5 САУДОВСКАЯ АРАВИЯ
24.1.5.6 ОСТАЛЬНЫЕ СТРАНЫ БЛИЖНЕГО ВОСТОКА И АФРИКИ
24.1.6 КЛЮЧЕВЫЕ ПЕРВИЧНЫЕ ИНДЕКСЫ: ПО ОСНОВНЫМ СТРАНАМ
25. ГЛОБАЛЬНЫЙ РЫНОК АУТСОРСИНГА ВОПРОСОВ РЕГУЛИРОВАНИЯ ДИАГНОСТИКИ IN VITRO (IVD), КОМПАНИЯ ЛАНДШАФТ
25.1 АНАЛИЗ АКЦИЙ КОМПАНИИ: ГЛОБАЛЬНЫЙ
25.2 АНАЛИЗ АКЦИЙ КОМПАНИИ: СЕВЕРНАЯ АМЕРИКА
25.3 АНАЛИЗ АКЦИЙ КОМПАНИИ: ЕВРОПА
25.4 АНАЛИЗ АКЦИЙ КОМПАНИИ: АЗИАТСКО-ТИХООКЕАНСКИЙ РЕГИОН
25.5 СЛИЯНИЯ И ПОГЛОЩЕНИЯ
25.6 РАЗРАБОТКА И УТВЕРЖДЕНИЕ НОВЫХ ПРОДУКТОВ
25.7 РАСШИРЕНИЯ
25.8 ИЗМЕНЕНИЯ В НОРМАТИВНОМ ПРАВЕ
25.9 ПАРТНЕРСТВО И ДРУГИЕ СТРАТЕГИЧЕСКИЕ РАЗВИТИЯ
26. ГЛОБАЛЬНЫЙ РЫНОК АУТСОРСИНГА ВОПРОСОВ РЕГУЛИРОВАНИЯ ДИАГНОСТИКИ IN VITRO (IVD), ПРОФИЛЬ КОМПАНИИ
26.1 РЕШЕНИЯ ФРЕЙРА
26.1.1 ОБЗОР КОМПАНИИ
26.1.2 ОБЗОР КОМПАНИИ
26.1.3 АНАЛИЗ ДОХОДОВ
26.1.4 АССОРТИМЕНТ ПРОДУКЦИИ
26.1.5 ПОСЛЕДНИЕ СОБЫТИЯ
26.2 AXSOURCE CONSULTING INC.
26.2.1 ОБЗОР КОМПАНИИ
26.2.2 ОБЗОР КОМПАНИИ
26.2.3 АНАЛИЗ ДОХОДОВ
26.2.4 АССОРТИМЕНТ ПРОДУКЦИИ
26.2.5 ПОСЛЕДНИЕ СОБЫТИЯ
26.3 ГРУППА НАУК О ЖИЗНИ ЛОРЕНЦА
26.3.1 ОБЗОР КОМПАНИИ
26.3.2 ОБЗОР КОМПАНИИ
26.3.3 АНАЛИЗ ДОХОДОВ
26.3.4 АССОРТИМЕНТ ПРОДУКЦИИ
26.3.5 ПОСЛЕДНИЕ СОБЫТИЯ
26.4 ЛАБОРАТОРНАЯ КОРПОРАЦИЯ АМЕРИКИ ХОЛДИНГС
26.4.1 ОБЗОР КОМПАНИИ
26.4.2 ОБЗОР КОМПАНИИ
26.4.3 АНАЛИЗ ДОХОДОВ
26.4.4 АССОРТИМЕНТ ПРОДУКЦИИ
26.4.5 ПОСЛЕДНИЕ СОБЫТИЯ
26.5 РЕГ IQ PTY LTD.
26.5.1 ОБЗОР КОМПАНИИ
26.5.2 ОБЗОР КОМПАНИИ
26.5.3 АНАЛИЗ ДОХОДОВ
26.5.4 ПОРТФЕЛЬ ПРОДУКЦИИ
26.5.5 ПОСЛЕДНИЕ СОБЫТИЯ
26.6 PROMEDICA INTERNATIONAL, КАЛИФОРНИЙСКАЯ КОРПОРАЦИЯ (IUVO BIOSCIENCES)
26.6.1 ОБЗОР КОМПАНИИ
26.6.2 ОБЗОР КОМПАНИИ
26.6.3 АНАЛИЗ ДОХОДОВ
26.6.4 ПОРТФЕЛЬ ПРОДУКЦИИ
26.6.5 ПОСЛЕДНИЕ СОБЫТИЯ
26.7 МАКРОУХОД
26.7.1 ОБЗОР КОМПАНИИ
26.7.2 ОБЗОР КОМПАНИИ
26.7.3 АНАЛИЗ ДОХОДОВ
26.7.4 АССОРТИМЕНТ ПРОДУКЦИИ
26.7.5 ПОСЛЕДНИЕ СОБЫТИЯ
26.8 АВАРИЙНАЯ СИТУАЦИЯ ПО UL
26.8.1 ОБЗОР КОМПАНИИ
26.8.2 ОБЗОР КОМПАНИИ
26.8.3 АНАЛИЗ ДОХОДОВ
26.8.4 ПОРТФЕЛЬ ПРОДУКЦИИ
26.8.5 ПОСЛЕДНИЕ СОБЫТИЯ
26.9 ИКОНА ПЛК
26.9.1 ОБЗОР КОМПАНИИ
26.9.2 ОБЗОР КОМПАНИИ
26.9.3 АНАЛИЗ ДОХОДОВ
26.9.4 ПОРТФЕЛЬ ПРОДУКЦИИ
26.9.5 ПОСЛЕДНИЕ СОБЫТИЯ
26.10 УСИ APPTEC
26.10.1 ОБЗОР КОМПАНИИ
26.10.2 ОБЗОР КОМПАНИИ
26.10.3 АНАЛИЗ ДОХОДОВ
26.10.4 АССОРТИМЕНТ ПРОДУКЦИИ
26.10.5 ПОСЛЕДНИЕ СОБЫТИЯ
26.11 ТЕРМО ФИШЕР САЙЕНТИФИК ИНК.
26.11.1 ОБЗОР КОМПАНИИ
26.11.2 ОБЗОР КОМПАНИИ
26.11.3 АНАЛИЗ ДОХОДОВ
26.11.4 АССОРТИМЕНТ ПРОДУКЦИИ
26.11.5 ПОСЛЕДНИЕ СОБЫТИЯ
26.12 ЛАБОРАТОРИИ ЧАРЛЬЗА РИВЕРА.
26.12.1 ОБЗОР КОМПАНИИ
26.12.2 ОБЗОР КОМПАНИИ
26.12.3 АНАЛИЗ ДОХОДОВ
26.12.4 АССОРТИМЕНТ ПРОДУКЦИИ
26.12.5 ПОСЛЕДНИЕ СОБЫТИЯ
26.13 ACCELL КЛИНИЧЕСКИЕ ИССЛЕДОВАНИЯ, ООО
26.13.1 ОБЗОР КОМПАНИИ
26.13.2 ОБЗОР КОМПАНИИ
26.13.3 АНАЛИЗ ДОХОДОВ
26.13.4 ПОРТФЕЛЬ ПРОДУКЦИИ
26.13.5 ПОСЛЕДНИЕ СОБЫТИЯ
26.14 КОРПОРАЦИЯ PAREXEL INTERNATIONAL (MA)
26.14.1 ОБЗОР КОМПАНИИ
26.14.2 ОБЗОР КОМПАНИИ
26.14.3 АНАЛИЗ ДОХОДОВ
26.14.4 ПОРТФЕЛЬ ПРОДУКЦИИ
26.14.5 ПОСЛЕДНИЕ СОБЫТИЯ
26.15 МЕТЕКОН ГМБХ
26.15.1 ОБЗОР КОМПАНИИ
26.15.2 ОБЗОР КОМПАНИИ
26.15.3 АНАЛИЗ ДОХОДОВ
26.15.4 ПОРТФЕЛЬ ПРОДУКЦИИ
26.15.5 ПОСЛЕДНИЕ СОБЫТИЯ
26.16 ГЕНПАКТ
26.16.1 ОБЗОР КОМПАНИИ
26.16.2 ОБЗОР КОМПАНИИ
26.16.3 АНАЛИЗ ДОХОДОВ
26.16.4 ПОРТФЕЛЬ ПРОДУКЦИИ
26.16.5 ПОСЛЕДНИЕ СОБЫТИЯ
26.17 КРИТЕРИУМ, ИНК.
26.17.1 ОБЗОР КОМПАНИИ
26.17.2 ОБЗОР КОМПАНИИ
26.17.3 АНАЛИЗ ДОХОДОВ
26.17.4 ПОРТФЕЛЬ ПРОДУКЦИИ
26.17.5 ПОСЛЕДНИЕ СОБЫТИЯ
26.18 МЕДПЕЙС
26.18.1 ОБЗОР КОМПАНИИ
26.18.2 ОБЗОР КОМПАНИИ
26.18.3 АНАЛИЗ ДОХОДОВ
26.18.4 ПОРТФЕЛЬ ПРОДУКЦИИ
26.18.5 ПОСЛЕДНИЕ СОБЫТИЯ
26.19 ГРУППА PRODUCTLIFE SA
26.19.1 ОБЗОР КОМПАНИИ
26.19.2 ОБЗОР КОМПАНИИ
26.19.3 АНАЛИЗ ДОХОДОВ
26.19.4 ПОРТФЕЛЬ ПРОДУКЦИИ
26.19.5 ПОСЛЕДНИЕ СОБЫТИЯ
26.20 ДОР ФАРМАЦЕВТИЧЕСКИЕ УСЛУГИ
26.20.1 ОБЗОР КОМПАНИИ
26.20.2 ОБЗОР КОМПАНИИ
26.20.3 АНАЛИЗ ДОХОДОВ
26.20.4 ПОРТФЕЛЬ ПРОДУКЦИИ
26.20.5 ПОСЛЕДНИЕ СОБЫТИЯ
26.21 QSERVE
26.21.1 ОБЗОР КОМПАНИИ
26.21.2 ОБЗОР КОМПАНИИ
26.21.3 АНАЛИЗ ДОХОДОВ
26.21.4 ПОРТФЕЛЬ ПРОДУКЦИИ
26.21.5 ПОСЛЕДНИЕ СОБЫТИЯ
26.22 ОРТОКЛИНИЧЕСКАЯ ДИАГНОСТИКА.
26.22.1 ОБЗОР КОМПАНИИ
26.22.2 ОБЗОР КОМПАНИИ
26.22.3 АНАЛИЗ ДОХОДОВ
26.22.4 АССОРТИМЕНТ ПРОДУКЦИИ
26.22.5 ПОСЛЕДНИЕ СОБЫТИЯ
26.23 АНГСТРОМ БИОТЕХ ПВТ. ЛТД.
26.23.1 ОБЗОР КОМПАНИИ
26.23.2 ОБЗОР КОМПАНИИ
26.23.3 АНАЛИЗ ДОХОДОВ
26.23.4 АССОРТИМЕНТ ПРОДУКЦИИ
26.23.5 ПОСЛЕДНИЕ СОБЫТИЯ
26.24 РМК+
26.24.1 ОБЗОР КОМПАНИИ
26.24.2 ОБЗОР КОМПАНИИ
26.24.3 АНАЛИЗ ДОХОДОВ
26.24.4 АССОРТИМЕНТ ПРОДУКЦИИ
26.24.5 ПОСЛЕДНИЕ СОБЫТИЯ
26.25 АССОЦИАЦИИ ПО СОБЛЮДЕНИЮ НОРМАТИВНЫХ ТРЕБОВАНИЙ (SOTERA HEALTH)
26.25.1 ОБЗОР КОМПАНИИ
26.25.2 ОБЗОР КОМПАНИИ
26.25.3 АНАЛИЗ ДОХОДОВ
26.25.4 ПОРТФЕЛЬ ПРОДУКЦИИ
26.25.5 ПОСЛЕДНИЕ СОБЫТИЯ
26.26 ИССЛЕДОВАНИЯDX
26.26.1 ОБЗОР КОМПАНИИ
26.26.2 ОБЗОР КОМПАНИИ
26.26.3 АНАЛИЗ ДОХОДОВ
26.26.4 АССОРТИМЕНТ ПРОДУКЦИИ
26.26.5 ПОСЛЕДНИЕ СОБЫТИЯ
26.27 CMIC HOLDINGS CO., LTD.
26.27.1 ОБЗОР КОМПАНИИ
26.27.2 ОБЗОР КОМПАНИИ
26.27.3 АНАЛИЗ ДОХОДОВ
26.27.4 АССОРТИМЕНТ ПРОДУКЦИИ
26.27.5 ПОСЛЕДНИЕ СОБЫТИЯ
26.28 СЕВЕРОАМЕРИКАНСКИЕ НАУЧНЫЕ АССОЦИАЦИИ, ООО
26.28.1 ОБЗОР КОМПАНИИ
26.28.2 ОБЗОР КОМПАНИИ
26.28.3 АНАЛИЗ ДОХОДОВ
26.28.4 ПОРТФЕЛЬ ПРОДУКЦИИ
26.28.5 ПОСЛЕДНИЕ СОБЫТИЯ
26.29 КАРАД БВ
26.29.1 ОБЗОР КОМПАНИИ
26.29.2 ОБЗОР КОМПАНИИ
26.29.3 АНАЛИЗ ДОХОДОВ
26.29.4 ПОРТФЕЛЬ ПРОДУКЦИИ
26.29.5 ПОСЛЕДНИЕ СОБЫТИЯ
26.30 РАСШИФРОВКА
26.30.1 ОБЗОР КОМПАНИИ
26.30.2 ОБЗОР КОМПАНИИ
26.30.3 АНАЛИЗ ДОХОДОВ
26.30.4 ПОРТФЕЛЬ ПРОДУКЦИИ
26.30.5 ПОСЛЕДНИЕ СОБЫТИЯ
26.31 КЛИН-Р+
26.31.1 ОБЗОР КОМПАНИИ
26.31.2 ОБЗОР КОМПАНИИ
26.31.3 АНАЛИЗ ДОХОДОВ
26.31.4 ПОРТФЕЛЬ ПРОДУКЦИИ
26.31.5 ПОСЛЕДНИЕ СОБЫТИЯ
26.32 ВКЛС
26.32.1 ОБЗОР КОМПАНИИ
26.32.2 ОБЗОР КОМПАНИИ
26.32.3 АНАЛИЗ ДОХОДОВ
26.32.4 ПОРТФЕЛЬ ПРОДУКЦИИ
26.32.5 ПОСЛЕДНИЕ СОБЫТИЯ
26.33 ГРУППА ПРОФАРМА
26.33.1 ОБЗОР КОМПАНИИ
26.33.2 ОБЗОР КОМПАНИИ
26.33.3 АНАЛИЗ ДОХОДОВ
26.33.4 ПОРТФЕЛЬ ПРОДУКЦИИ
26.33.5 ПОСЛЕДНИЕ СОБЫТИЯ
26.34 АРРИЕЛЛО АЙРЛЕНД ЛИМИТЕД
26.34.1 ОБЗОР КОМПАНИИ
26.34.2 ОБЗОР КОМПАНИИ
26.34.3 АНАЛИЗ ДОХОДОВ
26.34.4 ПОРТФЕЛЬ ПРОДУКЦИИ
26.34.5 ПОСЛЕДНИЕ СОБЫТИЯ
ПРИМЕЧАНИЕ: СПИСОК КОМПАНИЙ, ОПРЕДЕЛЕННЫХ В ПРОФИЛЕ, НЕ ИСЧЕРПЫВАЕТСЯ И СООТВЕТСТВУЕТ ТРЕБОВАНИЯМ НАШИХ ПРЕДЫДУЩИХ КЛИЕНТОВ. МЫ ОПРЕДЕЛЯЕМ БОЛЕЕ 100 КОМПАНИЙ В НАШЕМ ИССЛЕДОВАНИИ, И ПОЭТОМУ СПИСОК КОМПАНИЙ МОЖЕТ БЫТЬ ИЗМЕНЕН ИЛИ ЗАМЕНЕН ПО ЗАПРОСУ
27. СВЯЗАННЫЕ ОТЧЕТЫ
28. АНКЕТА
29. О РЫНОЧНЫХ ИССЛЕДОВАНИЯХ DATA BRIDGE
Методология исследования
Сбор данных и анализ базового года выполняются с использованием модулей сбора данных с большими размерами выборки. Этап включает получение рыночной информации или связанных данных из различных источников и стратегий. Он включает изучение и планирование всех данных, полученных из прошлого заранее. Он также охватывает изучение несоответствий информации, наблюдаемых в различных источниках информации. Рыночные данные анализируются и оцениваются с использованием статистических и последовательных моделей рынка. Кроме того, анализ доли рынка и анализ ключевых тенденций являются основными факторами успеха в отчете о рынке. Чтобы узнать больше, пожалуйста, запросите звонок аналитика или оставьте свой запрос.
Ключевой методологией исследования, используемой исследовательской группой DBMR, является триангуляция данных, которая включает в себя интеллектуальный анализ данных, анализ влияния переменных данных на рынок и первичную (отраслевую экспертную) проверку. Модели данных включают сетку позиционирования поставщиков, анализ временной линии рынка, обзор рынка и руководство, сетку позиционирования компании, патентный анализ, анализ цен, анализ доли рынка компании, стандарты измерения, глобальный и региональный анализ и анализ доли поставщика. Чтобы узнать больше о методологии исследования, отправьте запрос, чтобы поговорить с нашими отраслевыми экспертами.
Доступна настройка
Data Bridge Market Research является лидером в области передовых формативных исследований. Мы гордимся тем, что предоставляем нашим существующим и новым клиентам данные и анализ, которые соответствуют и подходят их целям. Отчет можно настроить, включив в него анализ ценовых тенденций целевых брендов, понимание рынка для дополнительных стран (запросите список стран), данные о результатах клинических испытаний, обзор литературы, обновленный анализ рынка и продуктовой базы. Анализ рынка целевых конкурентов можно проанализировать от анализа на основе технологий до стратегий портфеля рынка. Мы можем добавить столько конкурентов, о которых вам нужны данные в нужном вам формате и стиле данных. Наша команда аналитиков также может предоставить вам данные в сырых файлах Excel, сводных таблицах (книга фактов) или помочь вам в создании презентаций из наборов данных, доступных в отчете.